副溶血性弧菌(Vibrio parahaemolyticus)是海洋环境和海产品中广泛存在的食源性致病菌,能引起人类急性肠胃炎、伤口感染和败血症[1]。在世界范围内,尤其是亚洲和美国,经常有副溶血性弧菌感染疾病爆发的报道[2]。在我国,副溶血性弧菌是每年引起食物中毒发生率最高的微生物病原[3-5]。食源性致病菌控制技术一直以来都是研究热点,副溶血性弧菌作为海产品特有的食源性致病菌,其控制技术也受到广泛关注。传统的食源性致病菌控制技术主要基于抗菌药物、化学保鲜剂等化学制剂,随着社会的发展,食品的安全性以及抗菌药物引起的耐药性问题引发人们对化学制剂的担忧,因此,开发安全性高、高效、低廉的生物抑菌剂具有重要意义。噬菌体是细菌的病毒,在自然界中广泛存在,裂解性噬菌体能专一地引起宿主细胞的裂解而导致细菌死亡,为食源性致病菌的控制提供了一种新的手段[6]。噬菌体裂解宿主特异性强、生产成本低,对人和动物安全,不易产生耐受性,在致病菌的控制方面具有优于化学制剂的特点[7-8]。许多食源性致病菌的噬菌体陆续被分离,并显示出显著的杀菌作用,其在食品安全领域的应用也越来越多[9-12]。目前,己报道的副溶血性弧菌裂解性噬菌体数量有限,为了丰富该致病菌的噬菌体库,从中筛选具有潜在应用价值的菌株,本实验对从贝类样品中分离到的1 株裂解性副溶血性弧菌噬菌体进行生物学特性分析,并探讨该噬菌体对生三文鱼片中副溶血性弧菌的控制作用,旨在为其进一步的应用研究提供一定参考。
1 材料与方法
1.1 材料与试剂
1.1.1 菌株
宿主菌为副溶血性弧菌,购自美国典型微生物保藏中心,编号为ATCC17802。
噬菌体VpJYP2,由本实验室从贝类样品中分离得到,能裂解副溶血性弧菌ATCC17802。
1.1.2 样品
冻生三文鱼购自青岛当地超市,实验前采用GB 4789.7—2013《食品微生物学检验 副溶血性弧菌检验》[13]方法测定样品中副溶血性弧菌的污染情况,无副溶血性弧菌检出即可用于实验。将样品解冻,在低温条件下无菌操作将样品切成约3 cm×5 cm的片状(约10 g),备用。
1.1.3 培养基及试剂
营养肉汤、营养琼脂 北京陆桥生物技术有限公司;营养琼脂半固体培养基为营养肉汤中添加0.75%琼脂配制而成;弧菌显色培养基 法国科玛嘉公司;聚乙二醇(polyethyleneglycol,PEG)8000、平衡酚 北京索莱宝科技有限公司;DNase I、RNase A、蛋白酶K、DNA分子质量标准 宝生物工程(大连)有限公司;乙二胺四乙酸(ethylene diamine tetraacetic acid,EDTA)、十二烷基硫酸钠(sodium dodecyl sulfate,SDS)、氯化铯(CsCl) 生工生物工程(上海)有限公司;SM缓冲液(每升溶液含5.8 g NaCl、2 g MgSO4·7H2O、50 mL 1 mol/L pH 7.5 Tris-HCl、5 mL 2%明胶溶液,121 ℃高压灭菌20 min,4 ℃保存)。
1.2 仪器与设备
高压蒸汽灭菌器、生化培养箱 日本Sanyo公司;恒温培养振荡箱 上海智城分析仪器制造有限公司;生物安全柜 美国Nuaire公司;JEM-1200EX型透射电镜 日本Jeol公司。
1.3 方法
1.3.1 噬菌体的分离纯化和效价测定
采用双层平板法进行噬菌体的分离纯化和效价测定[14]。将宿主菌接种于3% NaCl营养肉汤中活化,36 ℃培养至约108~109 CFU/mL。将采集的贝类样品匀浆,取10 g样品加入90 mL 3% NaCl营养肉汤中,同时加入5 mL上述宿主菌悬液,36 ℃培养过夜,将培养液8 500 r/min离心10 min,收集上清液,用0.22 µm的滤膜过滤除菌,收集到的滤液即为噬菌体悬液。用SM缓冲液对噬菌体悬液进行适当稀释,取适宜稀释度各100 µL与200 µL培养过夜的宿主菌悬液混合,加入5 mL 3% NaCl营养琼脂半固体培养基(溶解后在46~50 ℃保温),充分混匀后倒于预先制备好的3% NaCl营养琼脂固体平板上,待其凝固后于36 ℃培养24 h,观察平板上噬菌斑情况,挑取直径大、生长均匀的单斑于SM缓冲液中,适当稀释后按以上分离操作进行纯化,重复3~4 次后即得到纯化的噬菌体,命名为VpJYP2。采用相同的操作,对适宜稀释度的噬菌斑进行计数,经计算后获得噬菌体效价。
1.3.2 噬菌体颗粒的浓缩和纯化
参考文献[15]方法。将宿主菌培养至浓度约109 CFU/mL,以最佳感染复数(multiplicity of infection,MOI)加入噬菌体悬液,培养至细菌完全裂解。在裂解液中加入DNase I和RNase A至终质量浓度为l mg/L,室温放置30 min。加入NaCl至终浓度为1 mol/L,搅拌使其溶解,冰浴1 h。4 ℃、8 500 r/min离心15 min去除其中的细菌碎片,收集上清液,加入终质量浓度为10 g/100 mL的PEG 8000,缓慢搅拌溶解,冰浴1 h以上,使噬菌体颗粒沉淀。4 ℃、8 500 r/min离心30 min,弃尽上清液,将沉淀悬于适量SM溶液中。加入等体积的氯仿抽提,温和振荡30 s,4 ℃、5 000 r/min离心15 min,回收含噬菌体颗粒的水相。采用CsCl平衡梯度等密度离心,收集纯化的噬菌体颗粒,透析,4 ℃保存备用。
1.3.3 噬菌体的生物学特性分析
1.3.3.1 噬菌体的形态学鉴定
取铜网浸入纯化的噬菌体悬液中,待其作用5 min,用滤纸吸去多余的液体,用2%的磷钨酸染色5 min,自然干燥后采用透射电镜进行观察。
1.3.3.2 噬菌体核酸的提取和全基因组测序
参考文献[15]方法。在纯化的噬菌体悬液中加入DNase I至终质量浓度为10 µg/mL、RNase A至终质量浓度为5 µg/mL,37 ℃温育1 h。加入pH 8.0 EDTA至终浓度为20 mmol/mL,灭活DNase I。加蛋白酶K至终质量浓度为50 µg/mL、SDS至终质量分数为0.5%,混匀,56 ℃温育1 h,然后冷却至室温。用等量平衡酚抽提,12 000 r/min离心5 min,收集水相,用等量平衡酚-氯仿-异戊醇(25∶24∶1,V/V)抽提,12 000 r/min离心5 min,收集水相,再用氯仿-异戊醇(24∶1,V/V)抽提,12 000 r/min离心5 min,取上层水相2 倍体积的无水乙醇沉淀噬菌体核酸,12 000 r/min离心5 min,再用70%乙醇溶液洗涤沉淀2 次,用TE缓冲液溶解沉淀核酸。依托生工生物工程(上海)股份有限公司的MiSeq测序平台进行全基因组测序,采用SPAdes软件(http://cab.spbu.ru/software/spades)对序列进行拼接,全基因组使用RAST(http://rast.nmpdr.org)进行在线注释,使用在线BLASTp工具(http://www.ncbi.nlm.nih.gov/BLAST)对注释蛋白进行功能预测。
1.3.3.3 热稳定性实验
按文献[16]的方法,取效价约108 PFU/mL的噬菌体悬液1.0 mL于无菌EP管中,分别于40、50、60、70 ℃的水浴中作用10、20、30、40、50、60 min,待作用时间结束后取出并立即置于冰浴中冷却,测定噬菌体效价。
1.3.3.4 pH值稳定性实验
按文献[16]的方法,取效价约109 PFU/mL的噬菌体悬液0.1 mL于无菌EP管中,分别加入0.9 mL pH值不同的3% NaCl营养肉汤,36 ℃水浴作用1 h,取出后测定噬菌体效价。
1.3.3.5 最佳MOI的测定
按文献[16]的方法,将宿主菌培养至对数生长早期,调麦氏浓度为0.5,即相当于约1×108 CFU/mL。按照MOI分别为10、1、0.1、0.01、0.001、0.000 1的比例加入噬菌体和宿主菌,36 ℃、150 r/min培养3.5 h后,12 000 r/min离心10 min,收集上清液测定噬菌体效价。以产生最高噬菌体效价的MOI为最佳MOI。
1.3.3.6 一步生长曲线的测定
按文献[16]的方法稍作改动,将宿主菌培养至对数生长早期,调菌液麦氏浓度为0.5,然后以最佳MOI的比例加入噬菌体液,与宿主菌液混合后36 ℃孵育15 min,然后12 000 r/min离心30 s,弃上清液,用3% NaCl营养肉汤洗涤菌体沉淀2 次。加入5 mL 36 ℃预热的3% NaCl营养肉汤悬浮沉淀并充分混匀,迅速置于36 ℃振荡培养,同时开始计时,在0、5 min和之后每隔10 min取样一次,12 000 r/min离心30 s,取上清液测定噬菌体在每一时间段的效价。以感染时间为横坐标、噬菌体效价为纵坐标,绘制一步生长曲线。
1.3.4 噬菌体对生三文鱼片中副溶血性弧菌的减菌作用
1.3.4.1 样品处理
按1.3.2节方法获得高浓度噬菌体悬液(约1011 PFU/mL),然后稀释成适宜的使用浓度。每片生三文鱼表面接种100 μL 1×106 CFU/mL的副溶血性弧菌悬液(终浓度为104 CFU/g),低温放置2 h让其充分吸附到样品上。取200 μL不同浓度噬菌体悬液(MOI分别为0、1、10、100、1 000、10 000)添加至人工污染了副溶血性弧菌的三文鱼片表面。将处理好样品置于无菌封口袋中,于4、15 ℃和25 ℃贮藏2 h,测定副溶血性弧菌数,确定噬菌体最佳添加量。另取样品,按以上方法人工污染副溶血性弧菌,然后添加最佳浓度的噬菌体,将处理好样品置于无菌封口袋中,分别在4、15 ℃和25 ℃贮藏一定时间,测定副溶血性弧菌数。
1.3.4.2 副溶血性弧菌的计数
将10 g样品加入90 mL磷酸盐缓冲液中,均质,制成1∶10样品匀液。为避免噬菌体对副溶血性弧菌的干扰,取10 mL样品匀液,8 000 r/min离心10 min,沉淀重悬于10 mL磷酸盐缓冲液中,取100 μL涂布弧菌显色培养基平板;对于菌浓度极低样品,将10 mL匀液沉淀重悬于1 mL磷酸盐缓冲液中,涂布3 块平板(检出限为1 CFU/g)。在36 ℃培养18~24 h,计数平板上典型副溶血性弧菌菌落数,从而计算样品中副溶血性弧菌含量[17]。
1.4 数据分析
结果以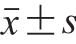 表示。采用t检验对数据的差异性进行统计分析,P<0.05,差异显著。
表示。采用t检验对数据的差异性进行统计分析,P<0.05,差异显著。
2 结果与分析
2.1 噬菌体的生物学特性
2.1.1 噬菌体的形态鉴定
噬菌体VpJYP2在双层平板上形成圆形、透明、边缘整齐的噬菌斑,直径约为1~2 mm,周围有晕圈,呈现出裂解性噬菌体的噬菌斑特征(图1)。纯化的噬菌体VpJYP2经透射电镜观察,头部呈二十面体立体结构,直径约64 nm,噬菌体的尾部长约70 nm,带收缩性尾鞘,宽约20 nm(图2)。根据《国际病毒分类委员会第9次报告》提出的噬菌体分类与命名标准,噬菌体VpJYP2属于有尾噬菌体目(Caudovirales)肌尾病毒科(Myoviridae)[18]。
图1 噬菌体VpJYP2的噬菌斑
Fig. 1 Plaques of phage VpJYP2

图2 噬菌体VpJYP2的透射电镜图
Fig. 2 Transmittance electron micrograph of phage VpJYP2
2.1.2 噬菌体的基因组特性
表1 噬菌体VpJYP2部分ORF功能预测
Table 1 Functional prediction of some ORF of phage VpJYP2
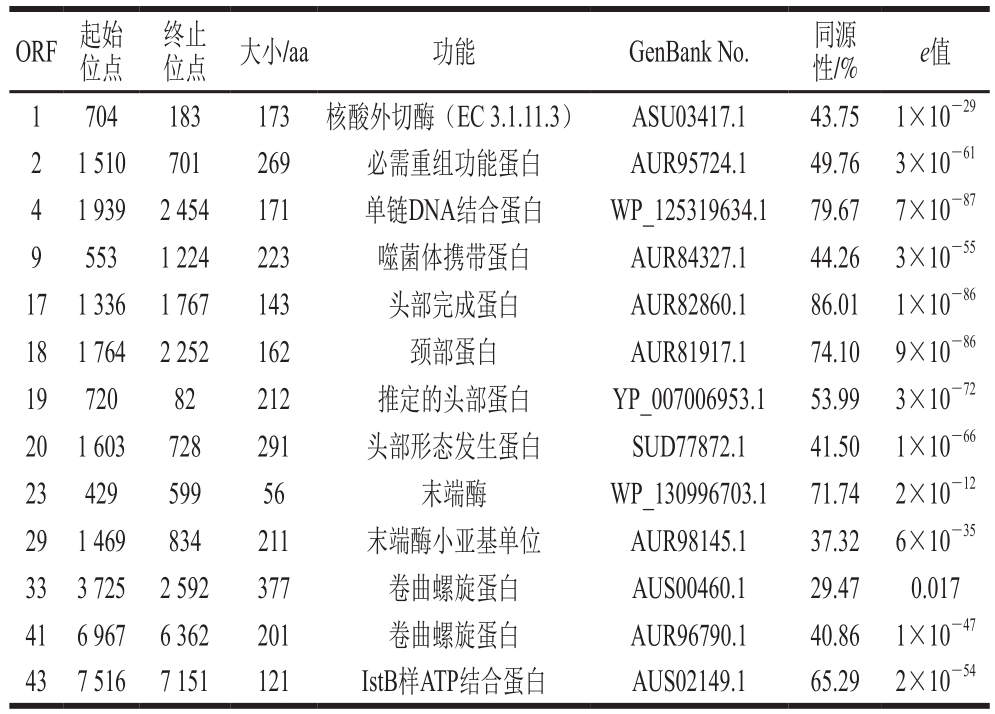
ORF起始位点终止位点 大小/aa 功能 GenBank No. 同源性/% e值1 704 183 173 核酸外切酶(EC 3.1.11.3) ASU03417.1 43.75 1×10-29 2 1 510 701 269 必需重组功能蛋白 AUR95724.1 49.76 3×10-61 4 1 939 2 454 171 单链DNA结合蛋白 WP_125319634.1 79.67 7×10-87 9 553 1 224 223 噬菌体携带蛋白 AUR84327.1 44.26 3×10-55 17 1 336 1 767 143 头部完成蛋白 AUR82860.1 86.01 1×10-86 18 1 764 2 252 162 颈部蛋白 AUR81917.1 74.10 9×10-86 19 720 82 212 推定的头部蛋白 YP_007006953.1 53.99 3×10-72 20 1 603 728 291 头部形态发生蛋白 SUD77872.1 41.50 1×10-66 23 429 599 56 末端酶 WP_130996703.1 71.74 2×10-12 29 1 469 834 211 末端酶小亚基单位 AUR98145.1 37.32 6×10-35 33 3 725 2 592 377 卷曲螺旋蛋白 AUS00460.1 29.47 0.017 41 6 967 6 362 201 卷曲螺旋蛋白 AUR96790.1 40.86 1×10-47 43 7 516 7 151 121 IstB样ATP结合蛋白 AUS02149.1 65.29 2×10-54
噬菌体VpJYP2的核酸为双链DNA,基因组全长为25 363 bp,G+C含量为39.56%。通过全基因组RAST在线注释和BLASTp分析,预测到该基因组含有45 个开放阅读框(open reading frames,ORF),核酸序列长度在114~1 134 bp之间,对应的蛋白质序列在37~377 aa之间。其中推定为己知功能的仅有13 个序列,其余为未知功能的假定蛋白序列,其中16 个序列未找到具有同源性的序列。表1列出了13 个预测的功能蛋白序列,主要包含DNA复制和调控相关蛋白、噬菌体包装蛋白、噬菌体头部和颈部相关的结构蛋白等。ORF1编码噬菌体核酸外切酶,ORF2编码噬菌体必需重组功能蛋白,ORF4编码单链DNA结合蛋白,ORF43编码ATP结合蛋白,为DNA复制和调控的相关基因。ORF23和ORF29编码噬菌体末端酶,在噬菌体包装时起重要作用。ORF17~20编码噬菌体结构蛋白,其中ORF17、ORF19和ORF20编码噬菌体头部蛋白,ORF18编码噬菌体颈部蛋白。ORF33和ORF41编码卷曲螺旋蛋白,通常为结构蛋白或转录因子的低聚结构域。未预测到与己知序列同源的裂解酶和穿孔蛋白基因。
2.1.3 噬菌体的热稳定性

图3 噬菌体VpJYP2的热稳定性
Fig. 3 Thermal stability of phage VpJYP2
如图3所示,噬菌体VpJYP2在40 ℃和50 ℃作用1 h后,效价基本不变,表明其活性不受温度影响;当温度为60 ℃时,VpJYP2效价下降缓慢,60 min后降低了1.5(lg(PFU/mL)),VpJYP2保持了较高的活性;当温度高于70 ℃,VpJYP2效价迅速下降,作用10 min效价下降了4.5(lg(PFU/mL)),作用20 min后下降了5.6(lg(PFU/mL)),作用30 min后降至检测水平以下。结果表明,高温会破坏噬菌体VpJYP2的活性。
2.1.4 噬菌体的pH值稳定性

图4 噬菌体VpJYP2的最适pH值
Fig. 4 pH stability of phage VpJYP2
如图4所示,噬菌体VpJYP2在pH 4~11时,效价与初始效价无显著性差异,维持良好的裂解活性,说明该噬菌体对pH值的适应范围较广;当pH值为3时,效价降低4.2(lg(PFU/mL));当pH≤2和pH≥12时,噬菌体基本丧失活性。
2.1.5 噬菌体的最佳MOI
如表2所示,当MOI为0.01时,噬菌体VpJYP2感染宿主产生子代噬菌体效价为3.9×109 PFU/mL,在6 个MOI中最高。因此,该噬菌体的最佳MOI为0.01。
表2 噬菌体VpJYP2的最佳MOI
Table 2 Optimal multiplicity of infection of phage VpJYP2
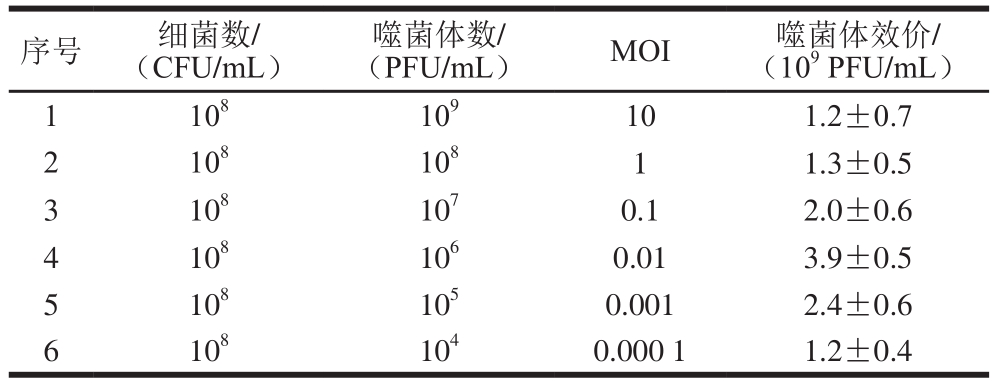
序号 细菌数/(CFU/mL)噬菌体数/(PFU/mL) MOI 噬菌体效价/(109 PFU/mL)1 108 109 10 1.2±0.7 2 108 108 1 1.3±0.5 3 108 107 0.1 2.0±0.6 4 108 106 0.01 3.9±0.5 5 108 105 0.001 2.4±0.6 6 108 104 0.000 1 1.2±0.4
2.1.6 噬菌体的一步生长曲线
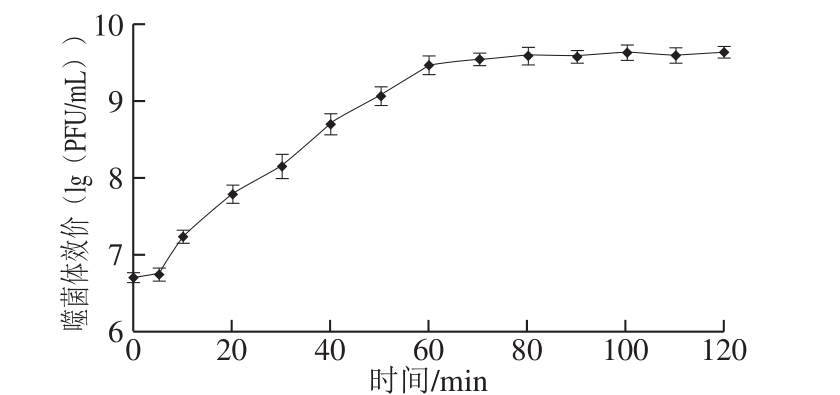
图5 噬菌体VpJYP2的一步生长曲线
Fig. 5 One-step growth curve of VpJYP2
如图5所示,噬菌体VpJYP2感染宿主菌后的5 min内效价没有明显变化,表明其潜伏期约为5 min,从5 min后效价开始上升,一直持续到60 min,之后效价趋于稳定,说明噬菌体裂解期约为55 min。根据裂解量=裂解末期噬菌体效价/感染初期宿主菌浓度计算得到,噬菌体VpJYP2裂解量=4.5×109/1.0×108=45。
2.2 噬菌体对生三文鱼片中副溶血性弧菌的减菌作用
2.2.1 噬菌体的最佳添加量
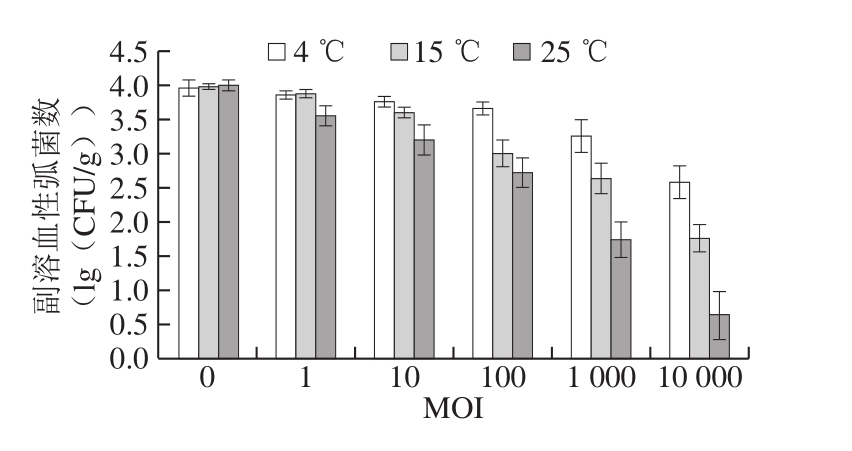
图6 不同浓度噬菌体VpJYP2对生三文鱼片中副溶血性弧菌的减菌作用
Fig. 6 Effect of different concentrations of phage VpJYP2 on reduction of V. parahaemolyticus counts on raw salmon fillets
由图6可以看出,在4、15 ℃和25 ℃条件下,随着MOI的增加,样品中副溶血性弧菌数逐渐降低。当MOI为10 000,即噬菌体添加量为108 PFU/g时,在4、15 ℃和25 ℃贮藏2 h后副溶血性弧菌数降低最多,分别降低了1.4、2.2(lg(CFU/g))和3.4(lg(CFU/g))。表明噬菌体添加量越高,减菌效果越好。考虑到制备更高浓度的噬菌体会增加实验操作的难度和成本,选择噬菌体的最佳添加量为108 PFU/g。
2.2.2 不同贮藏温度下噬菌体的减菌作用
在生三文鱼样品中添加108 PFU/g的噬菌体,在不同温度下贮藏时,副溶血性弧菌的变化结果如图7所示。在4 ℃条件下,未添加噬菌体样品中副溶血性弧菌数随着时间的延长逐渐降低,到7 d降至约1.2(lg(CFU/g));而添加噬菌体样品中副溶血性弧菌在8 h即可降至检测限以下,此后一直未检出。在15 ℃条件下,未添加噬菌体样品中副溶血性弧菌数随着时间的延长缓慢增加,添加噬菌体样品中副溶血性弧菌数先降低后增加,在8 h时降至最低,与初始菌数相比降低了3.4(lg(CFU/g))。在25 ℃条件下,未添加噬菌体样品中副溶血性弧菌数随着时间的延长迅速增加,添加噬菌体样品中副溶血性弧菌数迅速降低,在4 h降至检测限以下,而后逐渐升高。3 个温度下,所有添加噬菌体的实验组副溶血性弧菌数均显著低于未添加噬菌体的对照组(P<0.05)。
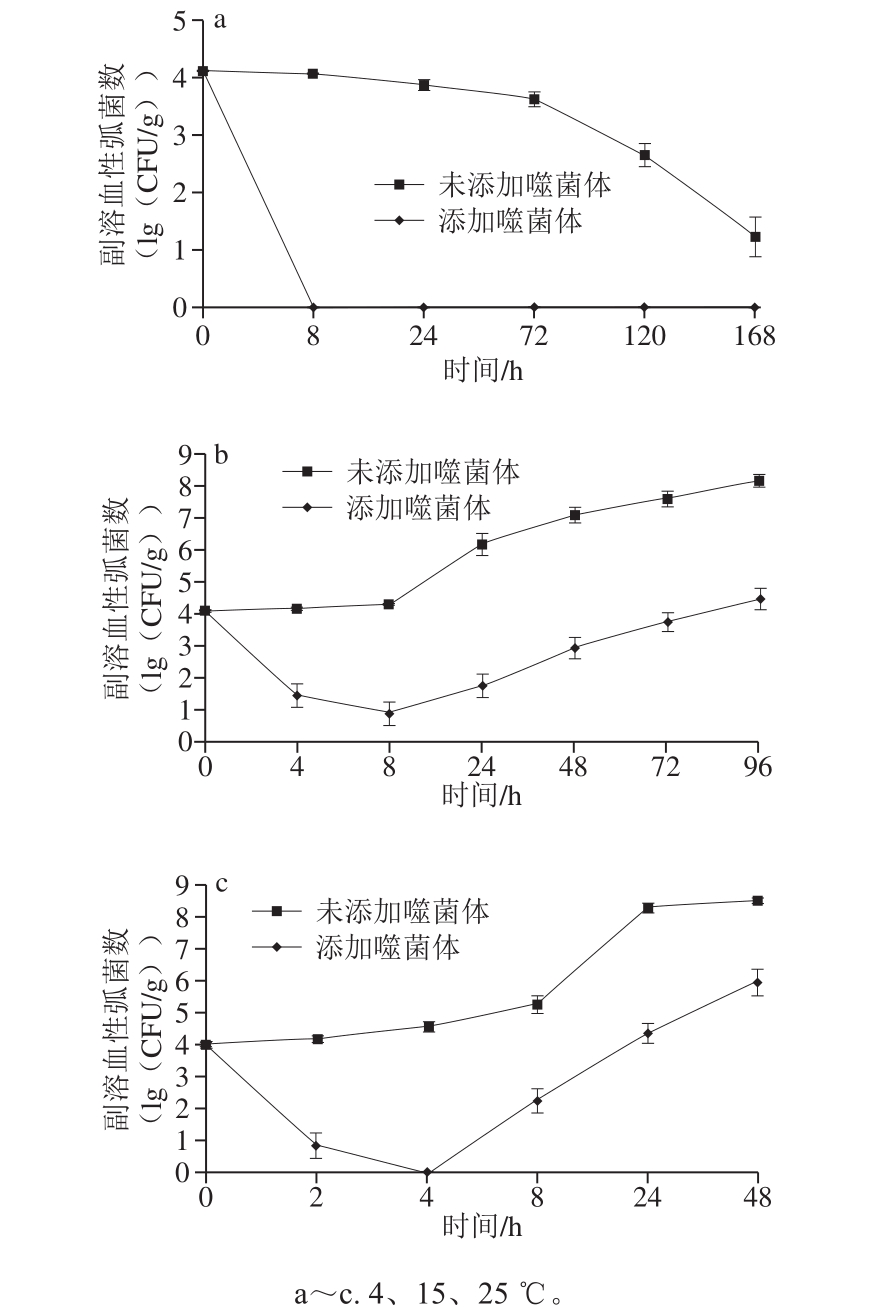
图7 不同温度贮藏条件下噬菌体VpJYP2对生三文鱼片中副溶血性弧菌的减菌作用
Fig. 7 Effect of phage VpJYP2 on reduction of V. parahaemolyticus counts on raw salmon fillets during storage at different temperatures
3 讨 论
噬菌体在环境中分布极广,凡是有细菌的场所,就可能有相应噬菌体的存在。据估计,噬菌体丰度是原核生物的5~10 倍左右,是自然界最丰富的生物体[19],因此,自然界提供了丰富的噬菌体库。然而,现阶段分离到的噬菌体还较少,对噬菌体的基因信息和应用的挖掘也极其有限。副溶血性弧菌作为一种重要的食源性致病菌,对其噬菌体的研究和该病原菌的重要性很不匹配。
目前分离的副溶血性弧菌噬菌体主要分属于长尾病毒科(Siphoviridae)[20-22]、短尾病毒科(Podoviridae)[16,23-25]、肌尾病毒科[21,26-28]和盖病毒科(Tectiviridae)[22,29],均为二十面体结构,但大小不同,生物学特性、基因组大小也不同。其中以副溶血性弧菌ATCC17802为宿主菌的噬菌体有qdvp001、VPMS1、VPp1、VPp2和VPp3。噬菌体VPMS1属于短尾病毒科,头部直径60 nm,尾部长10 nm,基因组大小为42.3 kb[23];噬菌体qdvp001属于肌尾病毒科,头部直径79 nm,尾长118 nm,基因组大小为35 kb,耐受温度40~60 ℃,最适pH值为4~10,最佳MOI为0.001[26];VPp2属于肌尾病毒科,头部直径64 nm,尾部长114 nm,基因组大小为2 kb,最佳MOI为0.000 01,潜伏期为5 min,裂解量为11.1[28];VPp3属于肌尾病毒科,头部直径89 nm,尾部长106 nm,基因组大小为2 kb,最佳MOI为0.001,潜伏期为25 min,裂解量为45.3[28];VPp1属于盖噬菌体科,头部直径为44 nm,无尾,基因组大小为15 kb,最佳MOI为0.000 1,潜伏期为10 min,裂解量为90.3[29]。可以看出,本实验分离到的噬菌体VpJYP2和这几株菌在形态、基因组大小和生物学特性方面均不同。从VpJYP2的生物学特性看,该菌株耐受60 ℃以下的温度,最适pH值范围较宽,在pH 4~11都能保持很高的活性,最佳MOI低,潜伏期短,裂解量较高,这些特性都赋予该菌株较高的裂解效率和应用潜力。本实验利用高通量测序仪对噬菌体VpJYP2进行了全基因组测序,利用BLASTp进行分析,结果发现该噬菌体有16 个ORF未找到相似序列,而其他ORF与相似序列的同源性也很低。在ORF分析中,未找到裂解酶基因序列和穿孔蛋白基因序列,这增加了挖掘该噬菌体功能基因的难度。后期希望通过其他方式找到相关裂解基因,挖掘基因的功能与应用。
利用噬菌体控制副溶血性弧菌有少量报道,这些研究显示噬菌体可降低海产食品或养殖海产品中副溶血性弧菌的含量。噬菌体SHOU24在常温条件下对即食对虾中副溶血性弧菌的生长具有良好抑制作用,能使副溶血性弧菌数下降1(lg(CFU/g))[21];此外,采用不同剂量的混合噬菌体VppMIX处理污染的黄鱼片,在25 ℃保藏12 h后,能使样品中副溶血性弧菌数比对照组低1.41~4.98(lg(CFU/g))[22]。噬菌体qdvp001能使养殖牡蛎体内副溶血性弧菌数下降3 个数量级[26];噬菌体VPp1能使实验室养殖规模下的牡蛎体内副溶血性弧菌数降低2.35~2.76(lg(CFU/g)),能使工厂化养殖规模下的牡蛎体内副溶血性弧菌降低1.11(lg(CFU/g))[30-31];噬菌体pVp-1采用浸浴的方式作用72 h后能使牡蛎食品中副溶血性弧菌由8.9×106 CFU/g降低至14 CFU/g,采用喷淋的方式处理12 h后能使副溶血性弧菌由1.44×106 CFU/g降低至1.94 CFU/g[32]。这些报道表明,噬菌体在副溶血性弧菌的控制方面效果显著。本实验探讨了噬菌体VpJYP2对生三文鱼片中副溶血性弧菌的减菌作用,结果显示,该噬菌体能显著杀灭生三文鱼片中的副溶血性弧菌,温度越低,对样品中副溶血性弧菌的控制效果越明显。推测可能是低温抑制副溶血性弧菌的生长,并使菌量逐渐减少,噬菌体作用于副溶血性弧菌表面的相对数量则会增加,从而裂解效率升高,导致样品中残留的菌数降低;当温度较高时,副溶血性弧菌生长速度较快,如果噬菌体作用不到样品中的副溶血性弧菌,残余菌会快速增殖,在样品中含量升高,同时噬菌体作用于副溶血性弧菌表面的相对数量则会减少,从而导致裂解效率降低。然而,使用噬菌体处理样品后,在所有测试时间点副溶血性弧菌的含量都显著低于未用噬菌体处理的对照组,因此,噬菌体VpJYP2具有一定的应用潜力。
4 结 论
本研究对1 株副溶血性弧菌裂解性噬菌体VpJYP2进行生物学特性分析和在水产品中应用。结果表明:1)噬菌体VpJYP2的噬菌斑清晰,为裂解性噬菌体,其头部呈二十面体立体结构,直径约64 nm,尾部长约70 nm,尾鞘带宽约20 nm,属于肌尾病毒科(Myoviridae);2)VpJYP2基因组全长25 363 bp,含有45 个ORF,推定为己知功能的有13 个,未找到相似序列的有16 个,未发现裂解酶基因和穿孔蛋白基因序列;3)VpJYP2在40~50 ℃稳定,在pH 4~11稳定,最佳MOI为0.01,感染宿主菌的潜伏期约为5 min,裂解期约为55 min,裂解量约为45;4)VpJYP2能显著降低生三文鱼片中副溶血性弧菌的含量,噬菌体浓度越高,杀菌效果越明显,结合低温处理,VpJYP2对样品中副溶血性弧菌的控制效果更好。结果表明,VpJYP2具有作为副溶血性弧菌生物杀菌剂的应用潜力。
[1] FUJINO T, OKUNO Y, NAKADA D, et al. On the bacteriological examination of shirasu food poisoning[J]. Medical Journal of Osaka University, 1953, 4: 299-304.
[2] FAO/WHO. Risk assessment of Vibrio parahaemolyticus in seafood:Interpretative summary and technical report[M]//Microbiological rish assessment series No. 16. Rome: FAO/WHO, 2011: 5-6.
[3] 李薇薇, 王三桃, 梁进军, 等. 2013年中国大陆食源性疾病暴发监测资料分析[J]. 中国食品卫生杂志, 2018, 30(3): 293-298.DOI:10.13590/j.cjfh.2018.03.015.
[4] 付萍, 刘志涛, 梁骏华, 等. 2014年中国大陆食源性疾病暴发事件监测资料分析[J]. 中国食品卫生杂志, 2018, 30(6): 628-634.DOI:10.13590/j.cjfh.2018.06.015.
[5] 付萍, 王连森, 陈江, 等. 2015年中国大陆食源性疾病暴发事件监测资料分析[J]. 中国食品卫生杂志, 2019, 31(1): 64-70. DOI:10.13590/j.cjfh.2019.01.014.
[6] KEEN E C, ADHAY S L. Phage therapy: current research and application[J]. Clinical Infectious Diseases, 2015, 61(1): 141-142.DOI:10.3390/ph10020043.
[7] HWANG J Y, KIM J E, SONG Y J, et al. Safety of using Escherichia coli bacteriophages as a sanitizing agent based on inflammatory responses in rats[J]. Food Science and Biotechnology, 2016, 25(1):355-360. DOI:10.1007/s10068-016-0050-6.
[8] BRUTTIN A, BRÜSSOW H. Human volunteers receiving Escherichia coli phage T4 orally: a safety test of phage therapy[J]. Antimicrobial Agents and Chemotherapy, 2005, 49(7): 2874-2878. DOI:10.1128/aac.49.7.2874-2878.2005.
[9] BAO H D, ZHANG P Y, ZHANG H, et al. Bio-control of Salmonella enteritidis in foods using bacteriophages[J]. Viruses, 2015, 7(8): 4836-4853. DOI:10.1002/jobm.201400257.
[10] 龙门, 詹歌, 金双潮, 等. JS25噬菌体生物特性及对食品中致病菌的生物防治[J]. 农业工程学报, 2016, 32(22): 303-308. DOI:10.11975/j.issn.1002-6819.2016.22.042.
[11] XU D, JIANG Y, WANG L, et al. Biocontrol of Salmonella typhimurium in raw salmon fillets and scallop adductors using bacteriophage SLMP1[J]. Journal of Food Protection, 2018, 81(8):1304-1312. DOI:10.4315/0362-028X.JFP-17-525.
[12] 胡颖, 李洪军, 贺稚非. 噬菌体防控食源性致病菌的研究进展[J].食品与发酵工业, 2019, 45(1): 246-251. DOI:10.13995/j.cnki.11-1802/ts.01752.
[13] 国家卫生和计划生育委员会. 食品微生物学检验 副溶血性弧菌检验: GB 4789.7—2013[S]. 北京: 中国标准出版社, 2013.
[14] CAREY-SMITH G V, BILLINGTON C, CORNELIUS A J. et al.Isolation and characterization of bacteriophages infecting Salmonella spp.[J]. FEMS Microbiology Letters, 2006, 258: 182-186.DOI:10.1111/j.1574-6968.2006.00217.x.
[15] 萨姆布鲁克 J, 拉塞尔 D W. 分子克隆实验指南[M]. 3版. 黄培堂等译. 北京: 科学出版社, 2002: 185-197.
[16] 江艳华, 王联珠, 李风铃, 等. 一株副溶血性弧菌裂解性噬菌体的分离、鉴定及其生物学特性[J]. 中国生物制品学杂志, 2015, 28(11):1147-1156.
[17] BIGWOOD T, HUDSON J A, BILLINGTON C, et al. Phage inactivation of foodborne pathogens on cooked and raw meat[J]. Food Microbiology, 2008, 25: 400-406. DOI:10.1016/j.fm.2007.11.003.
[18] 冯烨, 刘军, 孙洋, 等. 噬菌体最新分类与命名[J]. 中国兽医学报,2013, 33(12): 1954-1958.
[19] WOMMACK K E, COLWELL R R. Virioplankton: viruses in aquatic ecosystems[J]. Microbiology and Molecular Biology Reviews, 2000,64(1): 69-114. DOI:10.1128/MMBR.64.1.69-114.2000.
[20] YUAN L, CUI Z, WANG Y, et al. Complete genome sequence of virulent bacteriophage SHOU24, which infects foodborne pathogenic Vibrio parahaemolyticus[J]. Archives Virology, 2014, 159(11): 3089-3093. DOI:10.1007/s00705-014-2160-x.
[21] 袁琳, 张昭寰, 崔泽林, 等. 副溶血性弧菌噬菌体的分离及其在即食虾中的应用[J]. 食品工业科技, 2014, 35(21): 175-178.DOI:10.13386/j.issn1002-0306.2014.21.030.
[22] 郑小双, 高璐, 张辉, 等. 副溶血性弧菌光谱裂解性噬菌体的筛选及其在海产品安全控制中的应用[J]. 食品科学, 2019, 40(10): 141-148.DOI:10.7506/spkx1002-6630-20180621-405.
[23] RAMIREZ-OROZCO M, SERRANO-PINTO V, OCHOA-ALVAREZ N,et al. Genome sequence analysis of Vibrio parahaemolyticus lytic bacteriophage VPMS1[J]. Archives Virology, 2013, 158(5): 195-199.DOI:10.1007/s00705-013-1726-3.
[24] CHANG H J, HONG J, LEE N, et al. Growth inhibitory effect of bacteriophage isolated from western and southern coastal areas of Korea against Vibrio parahaemolyticus in Manila clams[J]. Applied Biological Chemistry, 2016, 59(3): 359-365. DOI:10.1007/s13765-016-0162-y.
[25] HARDIES S C, COMEAU A M, SERWER P, et al. The complete sequence of marine bacteriophage VpV262 infecting Vibrio parahaemolyticus indicates that an ancestral component of a T7 viral supergroup is widespread in the marine environment[J]. Virology,2003, 310(2): 359-371. DOI:10.1016/S0042-6822(03)00172-7.
[26] 丁云娟. 副溶血性弧菌噬菌体qdvp001的分离鉴定及其在牡蛎净化中的初步应用[D]. 青岛: 中国海洋大学, 2012.
[27] MATSUZAKI S, INOUE T, TANAKA S, et al. Characterization of a novel Vibrio parahaemolyticus phage, KVP241, and its relatives frequently isolated from seawater[J]. Microbiology and Immunology,2000, 44(11): 953-956. DOI:10.1111/j.1348-0421.2000.tb02589.x.
[28] 彭勇, 王静雪, 丁云娟, 等. 两株副溶血性弧菌裂噬菌体的分离鉴定及裂解性能[J]. 水产科学, 2012, 31(11): 645-650.
[29] 彭勇, 丁云娟, 林洪, 等. 一株副溶血性弧菌噬菌体VPp1的分离鉴定及裂解性能[J]. 海洋科学, 2013, 37(1): 96-101. DOI:10.3969/j.issn.1003-1111.2012.11.003.
[30] RONG R, LIN H, WANG J, et al. Reductions of Vibrio parahaemolyticus in oysters after bacteriophage application during depuration[J]. Aquaculture, 2014, 418/419: 171-176. DOI:10.1016/j.aquaculture.2013.09.028.
[31] 荣蓉. 副溶血性弧菌噬菌体VPp1在牡蛎净化中的应用及其规模化制备和保存[D]. 青岛: 中国海洋大学, 2014.
[32] JUN J W, KIM H J, YUN S K, et al. Eating oysters without risk of vibriosis: application of a bacteriophage against Vibrio parahaemolyticus in oysters[J]. International Journal of Food Microbiology, 2014, 188: 31-35. DOI:10.1016/j.ijfoodmicro.2014.07.007.