纳米材料应用于食品包装中[1-4],除了能改善包装的机械性能[5]、阻隔性[6]外,还能使包装具有良好的抗菌效果[7-10],从而使食品货架期延长。在纳米金属复合包装材料中,纳米铜具有广谱抗菌性,对抑制革兰氏阳性和阴性菌及酵母菌都有效果[11]。因此,纳米铜在食品包装中具有一定应用前景[12]。
己有研究表明,纳米材料应用于食品包装中,会通过扩散、表面解吸附或溶解等方式释放到食品中[13-14],进而对人体健康产生潜在危害[15]。所以,在纳米材料应用之前,需要对其进行充分的安全性评估。纳米材料的迁移研究是安全性评估的重要环节[16] ,目前,纳米铜复合包装材料的迁移研究主要注重纳米铜在食品模拟物中的迁移研究[17-19],关于纳米铜在真实食品中的迁移研究较少[20]。虽然使用食品模拟物能使迁移实验更加方便,但是,常规的迁移方法中使用的食品模拟液是否适用于有着特殊性能的纳米复合包装材料还值得商榷[21]。
为了研究纳米铜在真实食品中的迁移行为,本实验选择乳制品为实验对象,而市场上乳制品的包装大部分为利乐包,利乐包的内层由低密度聚乙烯(low density polyethylene,LDPE)制成。本实验选择LDPE为基材,主要研究纳米铜/LDPE复合膜中铜在纯乳和酸乳中的迁移,对比复合膜中铜在乳制品及其对应食品模拟物的迁移,重点考察现行标准中关于食品模拟液的选择在纳米铜迁移研究中的适用性。
1 材料与方法
1.1 材料与试剂
纯牛乳、风味发酵乳 市购;LDPE母粒 陶氏杜邦有限责任公司;纳米铜粉(平均粒径50 nm,纯度99%) 阿拉丁试剂(上海)有限公司;浓硝酸(色谱纯)、调谐液 赛默飞世尔科技(中国)有限公司;过氧化氢(30%、优级纯) 广州化学试剂厂;一级水(18.2 MΩ/cm)由Millipore纯水系统制得;铜标准溶液(1 000 μg/mL) 国家有色金属及电子材料分析测试中心;Ge、Y标准溶液(1 000 μg/mL) 美国O2si公司;无水乙醇(分析纯) 广州化学试剂厂;冰乙酸(分析纯) 天津市科密欧化学试剂有限公司。
1.2 仪器与设备
MEDU-22/40型双螺杆挤出造粒机 广州市普同实验分析仪器有限公司;小型流延膜实验机 佛山市金中河机械有限公司;ETHOS UP微波消解系统 意大利Milestone有限公司;ICP RQ电感耦合等离子体质谱(inductive coupled plasma-mass spectrometry,ICP-MS)仪美国Thermo Fisher Scientific公司;Optima 8000电感耦合等离子体发射光谱(inductively coupled plasma optical emission spectrometry,ICP-OES)仪 美国PerkinElmer公司;SHA-B水浴恒温振荡器 金坛市医疗仪器厂;V5平面袋真空保鲜机 深圳瑞朗克斯科技有限公司;ST5000实验室pH计 奥豪斯仪器(常州)有限公司。
1.3 方法
1.3.1 膜的制备
将LDPE母粒和纳米粉末充分混匀后通过造粒机进行造粒,重复造粒3 次[22],得到纳米铜/LDPE复合母粒,料筒1~9 区的温度分别为155、155、165、165、165、165、165、165、165 ℃;模头温度为165 ℃。造粒完成后将复合母粒用小型流延膜实验机进行流延成膜,得到纳米铜/LDPE复合膜,流延机1~3 区的温度分别为180、185、185 ℃,合流区温度为190 ℃,模具区温度为195 ℃。纳米铜和LDPE母粒的比例见表1。CF-0.5的厚度为(74.80±6.272)μm,密度为(0.827 2±0.017 98)g/cm3。C F-1的厚度为(7 3.6 8±7.5 3 5)μ m,密度为(0.878 5±0.012 37)g/cm3。
表1 复合膜中各组分的配比
Table 1 Formulation of composite films%
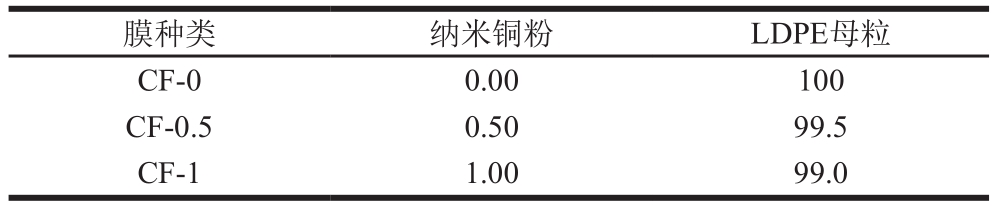
膜种类 纳米铜粉 LDPE母粒CF-0 0.00 100 CF-0.5 0.50 99.5 CF-1 1.00 99.0
1.3.2 标准溶液配制
使用体积分数为1%的硝酸溶液将Cu标准溶液(1 000 μg/mL)和Ge、Y标准溶液(1 000 μg/mL)进行逐级稀释,配制Cu标准溶液质量浓度为0.1、1、5、10、20、50 μg/L的微波消解-ICP-MS标准工作液;Ge、Y内标使用液质量浓度为20 μg/L。内标使用液由三通管在线加入ICP-MS。
分别使用体积分数为3%和4%的乙酸溶液将Cu(1 000 μg/mL)标准溶液逐级稀释为0.5、1、2、5、10、20 μg/mL的ICP-OES标准工作液。
1.3.3 迁移实验
常用于牛乳包装的利乐包里层通常为LDPE,本实验为了模拟牛乳包装内层与牛乳的实际接触情况,并保持牛乳在迁移过程中的完整性,选择制袋法进行迁移实验。GB 23296.1—2009《食品接触材料及制品迁移试验通则》[23]中规定迁移实验中,采用袋装实验的表面积-体积比一般为2 dm2食品接触面积比100 mL食品模拟物。用封口机将纳米铜/LDPE复合膜制成6 cm×10 cm的食品包装袋,装入30 mL的食品或者食品模拟液,再将包装袋密封严实,根据后续实验需求,在一定的迁移温度和迁移时间条件下进行迁移实验。迁移实验完成后,待样品冷却至室温后,将样品取出装好存放在4 ℃的冰箱中待测。每组3 个平行,同时做空白对照。
1.3.4 样品前处理
1.3.4.1 乳制品的前处理
称取乳制品2 g左右(精确到0.000 1 g)放入聚四氟乙烯消解罐内,加入5 mL浓硝酸,加盖静置1 h以上,再加入2 mL H2O2,旋紧外盖后放入微波消解仪中进行消解,微波消解程序[24]见表2。微波消解程序完成后,取出聚四氟乙烯罐,缓慢旋开外盖后用少量的一级水冲洗内盖,将消解罐在超声水浴箱中超声脱气10 min,用一级水将溶液转移并定容到100 mL容量瓶中,再用0.45 μm针式过滤器过滤后进行测定。
表2 微波消解程序
Table 2 Microwave digestion program
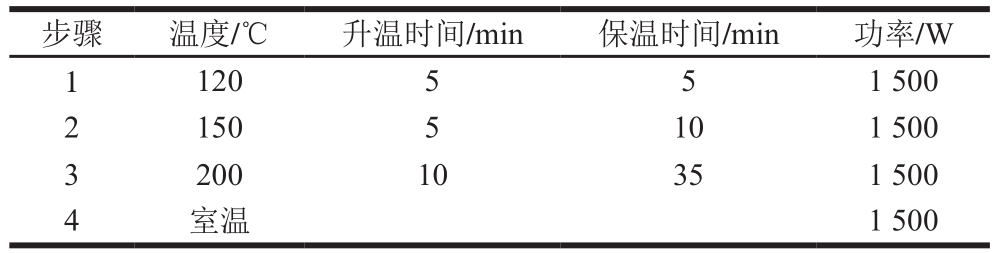
步骤 温度/℃ 升温时间/min 保温时间/min 功率/W 1 120 5 5 1 500 2 150 5 10 1 500 3 200 10 35 1 500 4 室温 1 500
1.3.4.2 食品模拟液的前处理
由于50%乙醇溶液无法直接用ICP-MS进行检测,需进行一定的前处理。准确量取10 mL的50%乙醇模拟液于25 mL具塞试管中,将试管放置在氮吹仪中进行氮吹处理,当溶液体积低于5 mL时取出试管,用1%的硝酸溶液将样品溶液定容到25 mL容量瓶中,用0.45 μm针式过滤器过滤后进行测定。铜向乙酸中的迁移检测方法己由课题组刘芳等[19]建立,因此3%和4%乙酸模拟液无需前处理,可直接用ICP-OES进行检测。
1.3.5 仪器工作条件
用调谐液对ICP-MS进行优化,确保仪器灵敏度、背景强度、双离子强度等在制定范围内。优化后ICP-MS和ICP-OES的工作参数见表3。
表3 ICP-MS和ICP-OES操作条件
Table 3Operating conditions of ICP-MS and ICP-OES
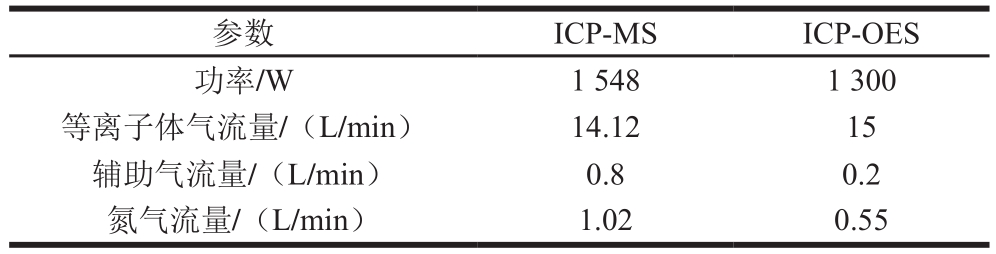
参数 ICP-MS ICP-OES功率/W 1 548 1 300等离子体气流量/(L/min) 14.12 15辅助气流量/(L/min) 0.8 0.2氮气流量/(L/min) 1.02 0.55
1.3.6 方法的线性相关性、曲线稳定性检出限和定量限
以标准工作溶液各元素的质量浓度为横坐标,各元素与内标计数值的比值为纵坐标,绘制标准曲线。对曲线的高、中、低质量浓度点进行重复6 次测定,观察曲线的稳定性。对11 份样品空白进行测定,以测量结果3 倍标准偏差作为方法的检出限,以测量结果10 倍标准偏差作为方法的定量限。
1.3.7 加标回收率和精密度测定
在空白膜制成的包装袋中加入30 mL纯乳,再分别加入15 μL的100 mg/L的铜标准溶液、15 μL的1 000 mg/L的铜标准溶液、75 μL的1 000 mg/L的铜标准溶液分别使加标质量浓度为0.05、0.5、2.5 mg/L。按照1.3.3节进行迁移实验之后按1.3.4.1节进行前处理,每个添加水平进行6 次测定,同时做空白实验。
1.3.8 迁移量的计算
乳制品中及不同溶液中铜迁移量的计算如式(1)~(4)所示:
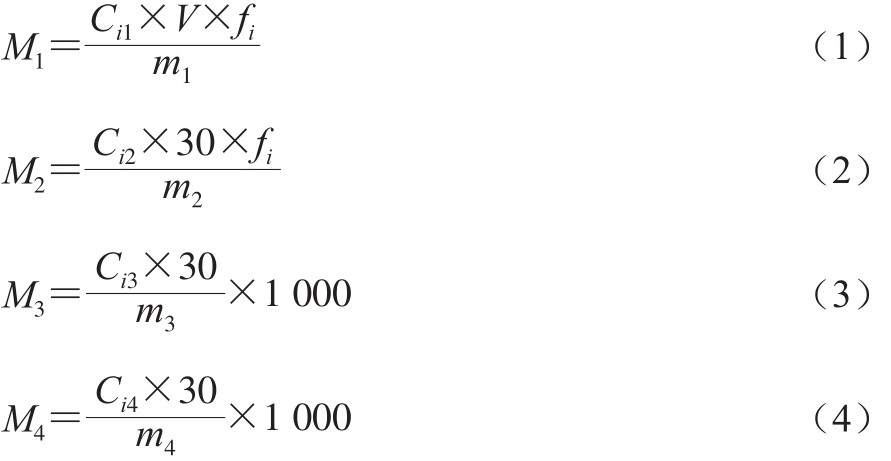
式中:M1、M2、M3、M4分别为乳制品、50%乙醇、3%乙酸、4%乙酸模拟液中铜的迁移量/(μg/kg);Ci1和Ci2分别为ICP-MS测得的乳制品、50%乙醇经前处理后的铜的质量浓度/(μg/L);Ci3和Ci4分别为ICP-OES测得的3%、4%乙酸中铜的质量浓度/(μg/L);V为试样消化液定容的体积/mL;fi为试样稀释倍数;m1为称取乳制品的质量/g;m2为30 mL 50%乙醇的质量/g;m3和m4分别为30 mL 3%和4%乙酸的质量/g。
1.3.9 迁移实验
1.3.9.1 纳米铜/LDPE复合膜中铜在乳制品中的迁移
实验探究纳米铜/LDPE复合膜中铜在纯乳和酸乳中的迁移。按照1.3.3节方法进行迁移实验后按1.3.4.1节进行样品前处理,同时做空白实验。迁移量为迁移后乳制品中的铜含量与乳制品本身含有的铜含量之差。
1.3.9.2 纳米铜/LDPE复合膜中铜在乳制品及其对应的食品模拟物中的迁移对比
GB 31604.1—2015《食品接触材料及制品迁移试验通则》[25]以及欧盟标准EU 10/2011[26]中规定,纯乳对应的食品模拟物均为50%乙醇溶液,而对于酸乳的食品模拟物的规定则不一样,国标规定体积分数4%乙酸为酸乳的食品模拟物,而欧盟规定质量分数3%乙酸为酸乳的食品模拟物。实验分别选择了50%乙醇、3%乙酸及4%乙酸3 种食品模拟液进行迁移实验,并且对比纳米铜在真实食品中的迁移,以考察现行标准中关于食品模拟液的选择在纳米成分迁移研究中的适用性。按照1.3.3节方法进行迁移实验,3%乙酸和4%乙酸溶液中铜质量浓度用ICPOES进行定量测定,50%乙醇溶液需按照方法1.3.4.2节进行前处理后用ICP-MS进行定量分析。
1.3.9.3 紫外照射处理后的复合膜中铜在乳制品中的迁移
紫外光常用于食品接触材料的消毒,为研究紫外照射对迁移的影响,在迁移实验开始前用紫外照射处理纳米铜/LDPE复合膜。将裁剪好的纳米铜/LDPE复合膜均匀放置在紫外波长为254 nm的环境中处理30 min,按照1.3.3节方法进行迁移实验后按1.3.4.1节进行样品前处理。
1.3.9.4 蒸煮条件下复合膜中铜在纯乳中的迁移
纯乳包装在实际使用过程中可能会涉及蒸煮条件,为了研究纳米铜在蒸煮状态下在纯乳迁移的情况,因此将灌装好牛乳的包装袋在蒸煮条件下进行迁移实验。取1 000 mL烧杯装入适量纯水,置于电热板上加热到水沸腾,沸腾后将灌装好样品的纳米铜/LDPE复合包装袋浸没在沸水中15 min。按照1.3.3节方法进行迁移实验后按1.3.4.1节进行样品前处理,同时做空白实验。
1.4 数据处理
用Office软件Excel对数据结果进行统计分析并作图,用Minitab 17对结果进行差异显著性分析,采用t检验,取95%置信度,差异显著,P<0.05。
2 结果与分析
2.1 方法的建立
ICP-MS检测铜元素的方法的标准曲线方程为y=5 600.077 2x+189.734 1,仪器检出限为0.016 μg/L,方法检出限为8.42 μg/kg,方法定量限为28.06 μg/kg。相关系数r>0.999 9,这说明用ICP-MS法检测铜在0.10~50.00 μg/L范围内的线性关系较好,相对标准偏差均小于5%,说明曲线比较稳定。用微波消解结合ICP-MS法检测铜在乳制品中的迁移,方法的加标回收率在97.46%~107.30%之间,精密度在1.98%~6.06%之间,说明此方法满足分析测定的要求。
2.2 迁移结果
2.2.1 纳米铜/LDPE复合膜中铜在乳制品中的迁移
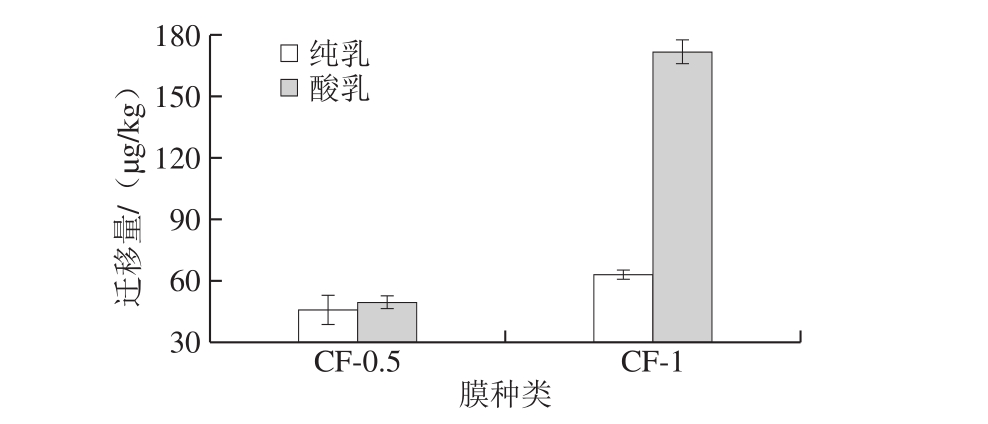
图1 纳米铜/LDPE复合膜中铜在乳制品中的迁移(n=3)
Fig. 1 Migration of nano-copper from nano-copper/LDPE composite film to milk products (n = 3)
图1 显示,铜在纯乳中的迁移量为46.32~64.21 μg/kg,在酸乳中的迁移量为49.91~171.57 μg/kg。不论是在纯乳中还是酸乳中,CF-1比CF-0.5中铜的迁移量大(P<0.05),这说明,复合膜中纳米铜的添加量对纳米铜的迁移量有影响,这与其在食品模拟液中迁移的规律一致[27]。同时,从图1还可以看出,纳米铜在酸乳中的迁移量比纯乳中高出3.59~107.37 μg/kg。在CF-1中,当纳米铜初始添加量为1%时,差异更为明显(P<0.05)。用pH计测得纯乳的pH 6.64,酸乳的pH 4.18,推测可能是因为酸乳的pH值比纯乳小,符合纳米铜在酸性大的溶液中更容易发生迁移行为的规律[27]。
2.2.2 纳米铜/LDPE复合膜中铜在乳制品和食品模拟液中的迁移对比
食品模拟液是能够接近真实地反映食品接触材料及制品中组分向与之接触的食品中的迁移,具有某类食品的典型共性,用于模拟食品进行迁移实验的测试介质[25]。从图2可以看出,纳米铜/LDPE复合膜中铜在纯乳中的迁移量比向50%乙醇溶液中的迁移量高出39.19~48.94 μg/kg,且存在显著性差异(P<0.05);但从图3发现,纳米铜在酸乳中的迁移量远小于在3%和4%乙酸溶液中的迁移量(P<0.05),差值分别在1 598.66~1 760.92 μg/kg和1 868.97~2 159.58 μg/kg之间。这说明,用50%乙醇溶液模拟牛乳,以及用3%和4%乙酸模拟酸乳进行纳米复合膜中纳米金属的迁移实验并不合适,需要选择更为合适的食品模拟液代替真实食品进行迁移研究。
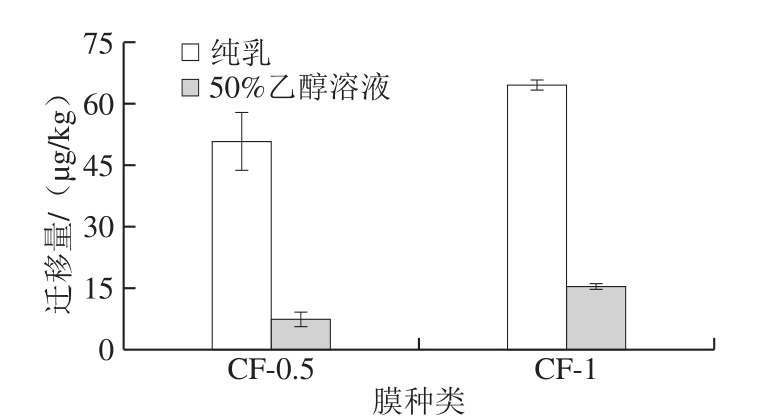
图2 纳米铜/LDPE复合膜中铜在纯乳和50%乙醇溶液中的迁移(n=3)
Fig. 2 Migration of nano-copper from nano-copper/LDPE composite film to pure milk and 50% ethanol solution (n = 3)
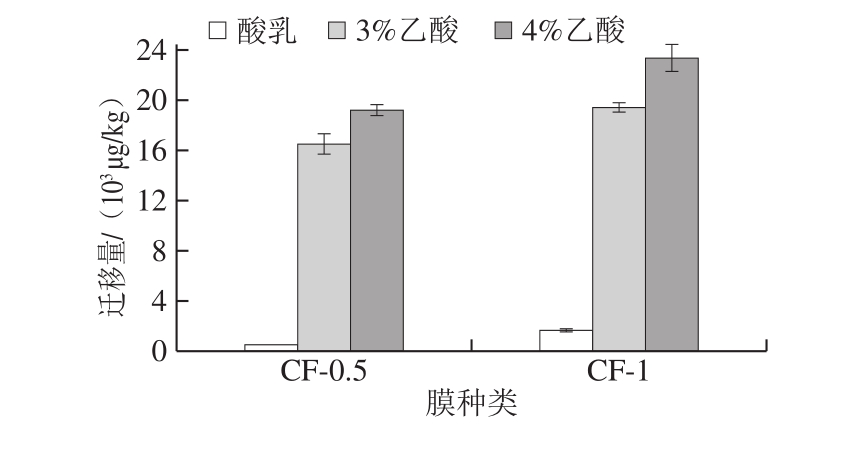
图3 纳米铜/LDPE复合膜中铜在酸乳和乙酸溶液中的迁移(n=3)
Fig. 3 Migration of nano-copper from nano-copper/LDPE composite film to yogurt and acetic acid solution (n = 3)
2.2.3 紫外照射处理的纳米铜/LDPE复合膜中铜在乳制品中的迁移
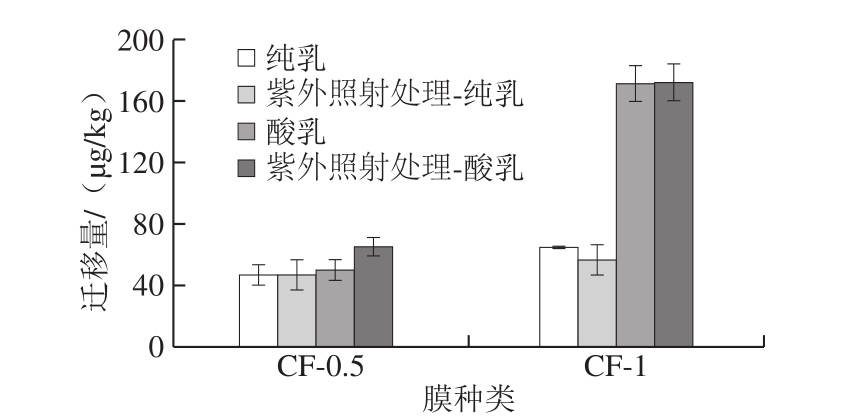
图4 紫外照射处理的纳米铜/LDPE复合膜中铜在乳制品中的迁移(n=3)
Fig. 4 Migration of nano-copper in UV-treated nano-copper/LDPE composite film to milk products (n = 3)
如图4所示,紫外照射处理复合膜后,复合膜中铜在纯乳和在酸乳中的迁移规律与2.2.1节一致,即当纳米铜添加量为1%时,纳米铜在酸乳中的迁移量显著高于在纯乳中的迁移量。但经过紫外照射处理后的复合膜与未经紫外照射处理的复合膜中铜在纯乳和酸乳中的迁移无显著差异(P>0.05),说明紫外照射对纳米铜的迁移没有影响。
2.2.4 蒸煮处理的纳米铜/LDPE复合膜中铜向乳制品中的迁移
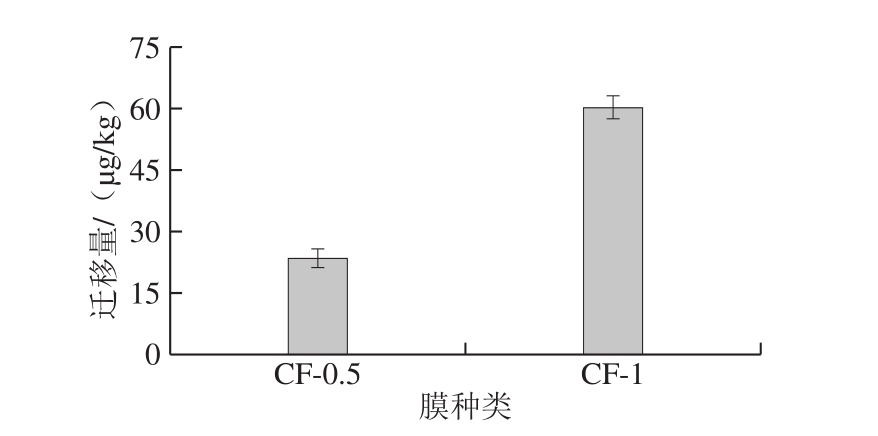
图5 100 ℃、15 min条件下纳米铜/LDPE复合膜中铜在纯乳中的迁移(n=3)
Fig. 5 Migration of nano-copper from nano-copper/LDPE composite film to pure milk after 15 min cooking at 100 ℃ (n = 3)
如图5所示,经蒸煮处理的复合膜中铜的迁移量在23.63~60.35 μg/kg之间,说明,在模拟蒸煮这种恶劣条件下,即使如本实验选用较大添加量的纳米铜(一般不超过质量分数0.5%),纳米铜在纯乳中的迁移量也远小于GB 9685—2016《食品接触材料及制品用添加剂使用标准》[28]及EU 2016/1416[29]规定中的特定迁移量为5 mg/kg。但尽管如此,复合膜中迁移出的纳米铜在溶液中可能以离子形态或纳米粒子形态存在,当以纳米粒子形态迁移时,其毒理机制复杂,有待进一步的毒理学研究[30],而纳米铜的迁移形态和毒理也正是课题组后期的研究重点。
3 结 论
纳米材料作为一种非常有应用前景的材料,在其应用于市场前应该进行充分的安全性评估。本实验建立纳米铜/LDPE复合膜中铜向牛乳中的迁移检测方法,方法检出限为8.42 μg/L,方法定量限为28.06 μg/L,方法回收率和精密度均满足分析方法建立的要求。实验发现,食品基质的pH值可能会对纳米铜的迁移产生影响,当纳米铜添加量为1%时,复合膜中铜在酸乳中的迁移量显著大于在纯乳中的迁移量。但总体来说,纳米铜向乳制品中的迁移量比较小,在迁移实验中,纳米铜在纯乳中的最大迁移量不超过65 μg/kg,在酸乳中的迁移量也不超过190 μg/kg,远低于法规中的限量。同时,在纳米铜的迁移实验中,用50%乙醇作为纯乳的食品模拟物、3%和4%乙酸作为酸乳的食品模拟物都不能很好地和相应的乳制品吻合,说明现行标准中对纯乳和酸乳模拟物的设定不适用于纳米铜,应寻找更合适的食品模拟物模拟纳米铜在乳制品中的迁移实验。
[1] MARILENA C, DOMENIA T D, GIANFRANCO S, et al. Silver nanoparticles in polymeric matrices for fresh food packaging[J].Journal of King Saud University-Science, 2016, 28(4): 273-279.DOI:10.1016/j.jksus.2016.05.004.
[2] JOKAR M, ABDUL R R. Study of silver ion migration from meltblended and layered-deposited silver polyethylene nanocomposite into food simulants and apple juice[J]. Food Additives and Contaminants Part A Chemistry Analysis Control Exposure & Risk Assessment,2014, 31(4): 734-742. DOI:10.1080/19440049.2013.878812.
[3] GARCIA C V, SHIN G H, KIM J T. Metal oxide-based nanocomposites in food packaging: applications, migration, and regulations[J]. Trends in Food Science & Technology, 2018, 82: 21-31. DOI:10.1016/j.tifs.2018.09.021.
[4] BUMBUDSANPHAROKE N, KO S. Nano-food packaging: an overview of market, migration research, and safety regulations[J].Journal of Food Science, 2015, 80(5): 910-923. DOI:10.1111/1750-3841.12861.
[5] 孙新, 黄俊彦, 吴双岭, 等. 纳米复合包装材料的研究与应用进展[J].塑料科技, 2012, 40(12): 100-103.
[6] CARDENAS G, DIAZ V J, MELENDREZ M, et al. Colloidal Cu nanoparticles/chitosan composite film obtained by microwave heating for food packaging applications[J]. Polymer Bulletin, 2009, 62(4):511-524. DOI:10.1007/s00289-008-0031-x.
[7] YUMI J, GARCIA C V, SEONGHYUK K, et al. Characterization and antibacterial properties of nanosilver-applied polyethylene and polypropylene composite films for food packaging applications[J].Food Bioscience, 2018, 23:83-90. DOI:10.1016/j.fbio.2018.03.008.
[8] CHU Z Z, ZHAO T R, LI L, et al. Characterization of antimicrobial poly (lactic acid)/nano-composite films with silver and zinc oxide nanoparticles[J]. Materials (Basel), 2017, 10(6): 659. DOI:10.3390/ma10060659.
[9] NILOOFAR B B, ABDOLREZA A, AHMADREZA R, et al. Surface coating of silver nanoparticles on polyethylene for fabrication of antimicrobial milk packaging films[J]. International Journal of Dairy Technology, 2017, 70(2): 204-211. DOI:10.1111/1471-0307.12320.
[10] AMIRSOLEIMANI M, KHALILZADEH M A, SADEGHIFAR F, et al.Surface modification of nanosatrch using nano silver: a potential antibacterial for food package coating[J]. Journal of Food Science and Technology, 2018, 55(3): 899-904. DOI:10.1007/s13197-017-2996-7.
[11] USMAN M S, EI ZOWALATY ME, SHAMELI K, et al.Synthesis, characterization, and antimicrobial properties of copper nanoparticles[J]. International Journal of Nanomedicine, 2013, 8(1):4467-4479. DOI:10.2147/IJN.S50837.
[12] BERGIN I L, WITZMANN F A. Nanoparticle toxicity by the gastrointestinal route: evidence and knowledge gaps[J]. International Journal of Biomedical Nanoscience and Nanotechnology, 2013, 3(2):1-44. DOI:10.1504/IJBNN.2013.054515.
[13] DUNCAN T V, PILLAI K. Release of engineered nanomaterials from polymer nanocomposite: diffusion, dissolution, and desorption[J].ACS Applied Materials & Interfaces, 2015, 7(1): 2-19. DOI:10.1021/am5062745.
[14] ECHEGOYEN Y, NERIN C. Nanoparticle release from nano-silver antimicrobial food containers[J]. Food and Chemical Toxicology,2013, 62: 16-22. DOI:10.1016/j.fct.2013.08.014.
[15] HUANG Y, CHEN S, BING X, et al. Nanosilver migrated into food-simulating solutions from commercially available food fresh containers[J]. Packaging Technology & Science, 2011, 24(5): 291-297. DOI:10.1002/pts.938.
[16] BUMBUDSANPHAROKE N, KO S. Nano-food packaging: an overview of market, migration research, and safety regulations[J].Journal of Food Science, 2015, 80(5): 910-923. DOI:10.1111/1750-3841.12861.
[17] LIN Q B, LI B, SONG H, et al. Determination of silver in nano-plastic food packaging by microwave digestion coupled with inductively coupled plasma atomic emission spectrometry or inductively coupled plasma mass spectrometry[J]. Food Additives and Contaminants Part A Chemistry Analysis Control Exposure & Risk Assessment, 2011,28(4): 1123-1128. DOI:10.1080/19440049.2011.580013.
[18] 石玉杰, 胡长鹰, 姜紫薇, 等. 不同结构纳米铜/PP复合膜中铜向食品模拟物的迁移[J]. 食品与发酵工业, 2018, 41(1): 92-97.DOI:10.13995/j.cnki.11-1802/ts.014440.
[19] 刘芳, 胡长鹰, 石玉杰, 等. 纳米铜/低密度聚乙烯复合膜中铜向食品模拟物迁移量的测定[J]. 食品与发酵工业, 2017, 40(1): 199-203.
[20] CUSHEN M, KERRY J, MORRIS M, et al. Evaluation and simulation of silver and copper nanoparticle migration from polyethylene nanocomposites to food and an associated exposure assessment[J].Journal of Agriculture and Food Chemistry, 2014, 62(6): 1403-1411.DOI:10.1021/jf404038y.
[21] 苏启枝, 林勤保, 钟怀宁, 等. 纳米塑料复合食品包装中的纳米成分及其迁移研究进展[J]. 食品科学, 2018, 39(15): 283-289.DOI:10.7506/spkx1002-6630-201815041.
[22] 史迎春, 胡长鹰, 黄金宇. 纳米ZnO/LDPE食品包装膜及食品模拟物中ZnO含量的测定[J]. 食品与发酵工业, 2017, 43(3): 229-233.DOI:10.13995/j.cnki.11-1802/ts.201703040.
[23] 国家质量监督检验检疫总局. 食品接触材料塑料中受限物质 塑料中物质向食品及食品模拟物特定迁移试验和含量测定方法以及食品模拟物暴露条件选择的指南: GB/T 23296.1—2009[S]. 北京:中国标准出版社, 2009.
[24] 张越. 婴幼儿配方奶粉中多元素的同时快速分析方法研究[D].杭州: 浙江大学, 2017.
[25] 国家卫生和计划生育委员会. 食品接触材料及制品迁移试验通则:GB 31604.1—2015[S]. 北京: 中国标准出版社, 2015.
[26] Commision Regulation. Commission Regulation (EU) No 10/2011 on plastic materials and articles intended to come into contact with food[S]. Brussels: Official Journal of the European Union, 2011.
[27] 姜紫薇, 胡长鹰, 石玉杰, 等. 纳米铜/聚丙烯复合膜中铜向食品模拟物的迁移及其对膜性能的影响[J]. 食品与发酵工业, 2019, 45(5):68-74. DOI:10.13995/j.cnki.11-1802/ts.017551.
[28] 国家卫生和计划生育委员会. 食品接触材料及制品用添加剂使用标准: GB 9685—2016[S] 北京: 中国标准出版社, 2016.
[29] Commision regulation. Commission regulation (EU) 2016/1416 of 24 August 2016 amending and correcting regulation (EU) No 10/2011 on plastic materials and articles intended to come into contact with food[S]. Brussels: Official Journal of the European Union, 2016.
[30] JOSEPH C H, JOSEPH K, MALCO C R, et al. Advances and challenges for the use of engineered nanoparticles in food contact materials[J]. Trends in Food Science & Technology, 2015, 43(1):43-62. DOI:10.1016/j.tifs.2015.01.008.