鱿鱼品种繁多,营养丰富,并且价格低廉,是一种低脂肪、低胆固醇、高蛋白质的水产品[1]。但是由于捕捞过度和海洋生态环境的不断恶化,海洋生物资源结构已经发生了巨大变化,北太鱿鱼和阿根廷鱿鱼等经济型鱿鱼资源呈不断下降趋势,因此寻找能够替代北太鱿鱼和阿根廷鱿鱼的低值型鱿鱼已经越来越急迫。鸢乌贼(Symplectoteuthis oualaniensis)属于鞘亚纲,枪形目,柔鱼科,莺乌贼属,广泛分布在印度洋、太平洋的赤道和亚热带等海域,其资源量大,繁殖速度快,已经越来越受到人们的关注。
印度洋鸢乌贼肉质硬,氨味重,且有令人不愉快的酸涩味,国内外对其研究较少。目前国内对于印度洋鸢乌贼的研究主要包括资源分布[2]和生物学特性[3],曲映红等[4]对印度洋西北海域鸢乌贼的理化特性进行测定;王进勉等[5]对印度洋鸢乌贼的加工特性进行研究,分析鸢乌贼各个部分的基本成分及重金属Pb、Cd含量,并主要研究了肌肉蛋白质在不同温度下随时间变化的情况;冯慧等[6]对印度洋鸢乌贼肌肉中的氧化三甲胺脱甲基酶进行分离纯化,发现纯化后该酶的最适温度和pH值分别为55 ℃和7.0,并且在50 ℃和pH 7.0~9.0条件下具有很好的稳定性。国内对秘鲁鱿鱼脱酸的工艺研究较多,泮 凤[1]研究了不同磷酸盐对秘鲁鱿鱼脱酸的效果,优选出复合除酸剂及除酸后鱿鱼品质的变化;王雅楠[7]研究了不同钠盐对冷冻秘鲁鱿鱼片的脱酸和保水性质的影响并确定了最佳的脱酸时间,但均未对鱿鱼酸味产生的原因进行研究。鉴于文献对印度洋鸢乌贼酸味产生的原因鲜有报道,本实验拟对印度洋鸢乌贼酸味相关的化学物质进行分析,并通过感官减除实验发现鸢乌贼肌肉的特征酸味物质,揭示酸味相关物质变化与酸味生成的关系,阐明印度洋鸢乌贼酸涩味形成的原因,以期为印度洋鸢乌贼加工利用提供理论依据。
1 材料与方法
1.1 材料与试剂
印度洋鸢乌贼体质量(6.14±0.23)kg,体长(52.31±0.18)cm,由海之星(福建)远洋渔业有限公司于2019年5月在印度洋西北海域(近霍尔木兹海峡)捕捞获得,-38 ℃快速冻结后在船上-18 ℃贮藏15 d后经运输船运至陆上实验室。
奥品类物质(meso-丙氨奥品、β-丙氨奥品、牛磺奥品、β-甘氨奥品)为实验室自制;5-磺基水杨酸、磷酸、磷酸二氢钾、磷酸氢二钾(均为分析纯) 上海凌峰化学试剂有限公司;腺嘌呤核苷三磷酸(adenosine triphosphate,ATP)及其关联物标准品、甘氨酸甜菜碱等标准品 美国Sigma公司;乙腈(色谱纯) 德国Merck公司。
1.2 仪器与设备
S-433D型氨基酸自动分析仪 德国Sykam公司;HR2860型高速匀浆机 荷兰飞利浦公司;e2695型高效液相色谱仪 美国Waters公司;IRIS Intrepid II型电感耦合等离子体质谱 美国Thermo Elemental公司;752N紫外-可见分光光度计、PHS-3C型数显酸度计 上海精科仪器有限公司;TGL-16M高速台式冷冻离心机长沙湘仪离心机仪器有限公司。
1.3 方法
1.3.1 样品前处理
选取体型相近、体态完好的鸢乌贼样品,流水解冻后去除皮、骨和内脏等废弃物,将胴体肉表层和内层切去薄薄一层后切成5 cm×5 cm小块用于分析测定。
1.3.2 pH值的测定
参照GB 5009.237—2016《食品pH值的测定》,称取5.00 g鱿鱼加入到50 mL蒸馏水中,高速匀浆机匀浆后用pH计测定pH值(温度(20±2)℃)。
1.3.3 滋味成分分析
1.3.3.1 游离氨基酸含量的测定
准确称量5.00 g鱿鱼胴体肉,加入15 mL 0.02 mol/L稀盐酸,均质后超声波清洗5 min,然后用冷冻离心机4 ℃、5 000×g离心10 min,收取上清液。将剩余残渣加入10 mL 0.02 mol/L稀盐酸后搅拌,4 ℃、5 000×g再次离心5 min,合并2 次离心上清液,定容至50 mL。定容后移取2 mL,加入2 mL体积分数5% 5-磺基水杨酸溶液,4 ℃、10 000×g离心10 min,然后经0.22 μm水相过滤膜过滤,用氨基酸自动分析仪测定。
1.3.3.2 奥品含量的测定
meso-丙氨奥品、β-丙氨奥品、牛磺奥品、β-甘氨奥品的制备和测定参照Haque等[8]的方法并加以改进。
奥品的提取:精确称取5.0 0 g胴体肉,加入50 mL 1.2 mol/L于4 ℃预冷的HClO4溶液,用高速匀浆机匀浆2 min后于4 ℃静置30 min,然后4 ℃、10 000×g离心20 min,收集上清液并于残渣中加入30 mL 0.6 mol/L HClO4溶液,按上述方法离心,合并上清液。上清液用1.0 mol/L KOH溶液中和后过滤,滤液用蒸馏水定容至100 mL。将上述100 mL滤液经过D201(OH-型)离子 交换树脂柱,经1 L超纯水冲洗后用1 L 1 mol/L乙酸溶液 洗脱,洗脱液经真空旋转蒸发后浓缩至25 mL。
奥品的衍生:从上述浓缩液中移取100 μL加入2 mL Eppendorf离心管中,于40 ℃条件下真空干燥4 h后加入20 μL乙醇-三乙胺-水(2∶2∶1,V/V)溶液,再次于40 ℃真空干燥1 h,然后溶于50 μL乙醇-三乙胺-水(7∶1∶1,V/V)溶液中并加入5 μL异硫氰酸苯酯,充分振荡,于室温下反应20 min后30 ℃真空干燥1 h。最后加入1 mL乙腈-水(2∶7,V/V)溶液,经孔径为0.45 μm的有机滤膜过滤后进液相色谱分析。
高效液相色谱条件:X b r i d g e C1 8色谱柱(4.6 mm×250 mm,5 μm);柱温35 ℃,检测波长254 nm;流速1 mL/min;进样量10 μL;流动相A为60%乙腈溶液,流动相B为100 mmol/L乙酸-乙酸钠缓冲液(pH 3.43),梯度洗脱条件见表1。
表1 高效液相色谱测定奥品的梯度洗脱程序
Table 1 Gradient elution conditions for opines separation by HPLC
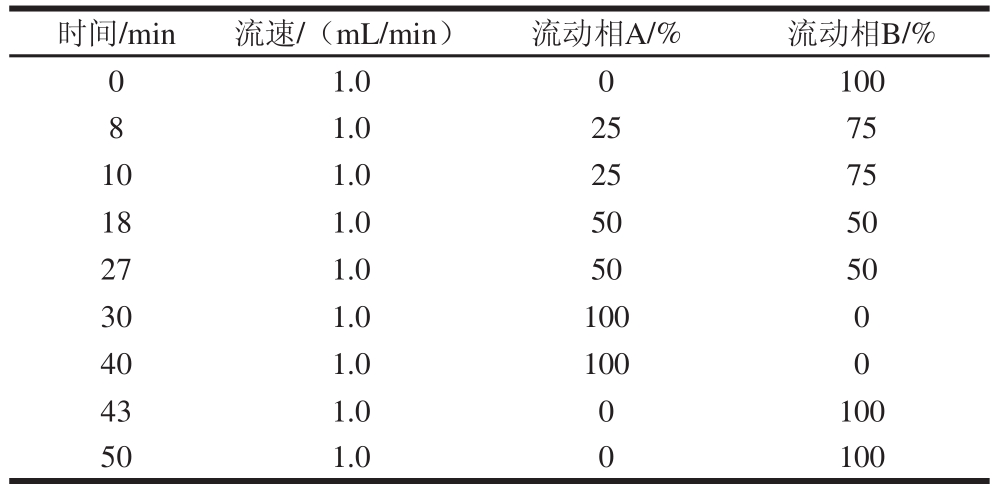
时间/min 流速/(mL/min) 流动相A/% 流动相B/%0 1.0 0 100 8 1.0 25 75 10 1.0 25 75 18 1.0 50 50 27 1.0 50 50 30 1.0 100 0 40 1.0 100 0 43 1.0 0 100 50 1.0 0 100
1.3.3.3 核苷酸含量的测定
精确称取5.00 g鱿鱼胴体肉,溶于50 mL 1.2 mol/L 4 ℃预冷的HClO4溶液中,用高速匀浆机匀浆2 min后于4 ℃静置30 min,然后4 ℃、3 000×g离心20 mi n,收集上清液。沉淀重复提取1 次,合并上清液,用10 mol/L KOH溶液中和至pH 6.5±0.05。过滤沉淀物并定容至100 mL,过膜(0.45 μm)后进液相色谱分析。
液相色谱条件:X0bridgeC1 8色谱柱(4.6 mm×250 mm,5 μm);流动相为0.1 mol/L磷酸盐缓冲液溶液(pH 7.0,0.04 mol/L KH2PO4+0.06 mol/L K2HPO4),流速0.75 mL/min,检测波长254 nm,柱温30 ℃,进样量10 μL。
1.3.3.4 有机酸含量的测定
采用刘书来等[9]的方法,并适当修改。精确称取10.00 g鱿鱼胴体肉,加入50 mL 1.2 mol/L 4 ℃预冷的HClO4溶液,高速匀浆2 min后于4 ℃静置30 min,4 ℃、5 000×g离心20 min,收集上清液并于残渣中加入30 mL 0.6 mol/L HClO4溶液,按上述方法离心,合并2 次上清液,上清液用1.0 mol/L KOH溶液中和后定容至100 mL,经0.45 μm滤膜过滤后用于高效液相色谱分析。有机酸标准品分别为酒石酸、苹果酸、柠檬酸、丁二酸、乳酸、丙酸和乙酸,配制成初始质量浓度10 mg/mL,梯度稀释后采用高效液相色谱分析。
高效液相色谱条件:AtlantisT 3色谱柱(4.6 mm×150 mm,5 μm);流动相为KH2PO4溶液(0.08 mol/L,用磷酸调至pH 3.00);流速0.5 mL/min,波长210 nm;柱温30 ℃,进样量10 μL。
1.3.3.5 无机离子含量测定
K+、Na+、Ca2+、Mg2+的测定采用电感耦合等离子体质谱法[10]。精确称取2.00 g鱿鱼胴体肉搅碎后置于消解罐中,加10 mL硝酸放入微波消解仪中消解,消解后待样品完全冷却,于130 ℃赶酸1 h后转移至50 mL容量瓶中定容,同时做空白实验。
电感耦合等离子体质谱法测定条件:等离子气流量15 L/min,蠕动泵转速0.2 r/s,雾化室温度2 ℃,辅助气流量0.8 L/min,载气流量0.8 L/min,He气流量5 mL/min,射频功率1 500 W,数据采集模式为跳峰采集模式,采样深度为10 mm,重复3 次,扫描100 次。
C l-的测定采用硝酸银直接滴定法[1 1]。精确称取5.00 g鱿鱼胴体肉加入100 mL纯水中,沸水浴加热15 min并不断搅拌,冷却至室温后依次加入2 mL 106 g/L K4Fe(CN)6·3H2O和2 mL 220 g/L Zn(CH3COO)2·2H2O,彻底混匀后于室温下静置30 min,转移到200 mL容量瓶后用蒸馏水稀释至刻度后过滤。取20 mL上述滤液,依次加入5 mL稀硝酸、1 mL NH4Fe(SO4)2、20 mL硝酸银溶液和3 mL硝基苯,剧烈振荡后用硫氰化钾滴定,同时做空白实验。
PO4 3-的测定参照GB 5009.87—2016《食品中磷的测定》[12]。精确称取2.00 g鱿鱼胴体肉于坩埚中,在火上灼烧成炭分后于马弗炉550 ℃条件下灼烧成灰分,直至白色,加1.4 mol/L稀盐酸10 mL及硝酸2 滴,水浴蒸干后再次加入2 mL 1.4 mol/L稀盐酸,多次加蒸馏水将残渣洗入100 mL容量瓶中并加水定容。取上述溶液0.5 mL于25 mL比色管中,依次加入2 mL 50 g/L的钼酸铵溶液、1 mL 200 g/L的亚硫酸钠溶液、1 mL 5 g/L的对苯二酚溶液后加水至刻度,摇匀后静置30 min,以不加溶液为空白对照,于波长660 nm处测其吸光度。
 含量的测定参照Márquez-Ríos等[13]的方法,并稍作改进。准确称取5.00 g鱿鱼样品,匀浆后加入45 mL 2.5%的磷钨酸溶液,振荡2 min,然后于3 000×g离心15 min。过滤上清液,移取2 mL滤液加入8 mL蒸馏水稀释,然后依次加入1 mL 12.5%的NaOH溶液、2 mL正丁醇(含10%百里酚溶液)、5 mL 2.5% NaOH溶液(含0.5%溴水),加入后摇匀,同时做2.5%磷钨酸的空白对照实验。混合液静置20 min后加入20 mL正丁醇振荡1 min,静置20 min,于波长680 nm处测定吸光度。
含量的测定参照Márquez-Ríos等[13]的方法,并稍作改进。准确称取5.00 g鱿鱼样品,匀浆后加入45 mL 2.5%的磷钨酸溶液,振荡2 min,然后于3 000×g离心15 min。过滤上清液,移取2 mL滤液加入8 mL蒸馏水稀释,然后依次加入1 mL 12.5%的NaOH溶液、2 mL正丁醇(含10%百里酚溶液)、5 mL 2.5% NaOH溶液(含0.5%溴水),加入后摇匀,同时做2.5%磷钨酸的空白对照实验。混合液静置20 min后加入20 mL正丁醇振荡1 min,静置20 min,于波长680 nm处测定吸光度。
1.3.3.6 氧化三甲胺与甜菜碱的测定
氧化三甲胺(trimetlylamine oxide,TMAO)含量的测定采用黄国霞等[14]的方法,用20 mmol/L Fe2+-EDTA二钠溶液将鸢乌贼中的TMAO还原成三甲胺,采用GB 5009.179—2016《食品中三甲胺的测定》测定三甲胺,通过测定还原前后三甲胺的含量计算鸢乌贼中TMAO的含量。甜菜碱的测定采用分光光度法[15],对雷氏盐离子进行比色,测OD525 nm。
1.3.4 感官实验
1.3.4.1 样品准备
将鸢乌贼除去皮和内脏等废弃物,取相同部位胴体肉捣 碎,用小袋分装后于-20 ℃贮藏待用。取相同部位胴体肉流水解冻后备用。
1.3.4.2 鸢乌贼天然提取液的制备
采用热水-乙醇法[16-17]提取鸢乌贼肉中的滋味物质。
1.3.4.3 鸢乌贼合成提取液的制备
将滋味物质准确称量后溶于纯水中,然后用0.01 mol/L稀硫酸将溶液pH值调为5.82(鸢乌贼肌肉天然pH值),平衡10 min后,将其与天然提取液进行比较,进行感官评价。
1.3.4.4 感官评定
参照GB/T 22210—2008《肉与肉制品感官评定规范》[18]要求选取富有感官评定经验的10 名评价员并进行训练,组成感官评定小组。感官评定过程在食品感官实验室内进行,控制实验室内温度为19~22 ℃。在感官评定过程中,用感官鼻夹将评定员鼻子夹住,避免气味对评定员形成干扰;每次评定样品不超过5 个;评定过程中不得相互交流;样品在评定员口腔中进行短暂的旋转后以去离子水漱口,间隔2 min后再进行下一个样品的品评。每次品评的样品组由3 位随机编号的3 个样品构成,其中2 个样品为相同溶液,另外一个是要求被区分的样品溶液,要求感官评定员识别出不同于其他2 个的样品,评定重复2 次,得到20 个结果,然后采用3 点检验,挑选出3 个样品中不同于另外2 个的样品,记录其编号。
1.3.4.5 感 官减除实验
为研究单个酸味物质对整体酸味的贡献,将鸢乌贼酸味相关物质分成游离氨基酸、核苷酸关联化合物、奥品、有机酸、无机离子和季铵盐类6 个味觉重组体,忽略单独的味觉重组体或重组体中单一的酸味物质(其中将游离氨基酸味觉重组体按其含量高低分为3 个亚组,忽略单独的某一亚组或亚组中单一的酸味相关物质),然后通过感官评定员的评定确定减除后的整体酸味与天然提取液的酸味是否相同。正确发现酸味差异的评定员被要求判断样品的差异强度,以0、1、2表示差异程度(数字越大,则差异越显著)。
1.4 数据处理
实验平行测定3 次,利用软件SPSS 21.0进行数据处理分析,数据以 表示,P<0.05,显著性差异。
表示,P<0.05,显著性差异。
2 结果与分析
2.1 印度洋鸢乌贼肉中的酸味相关物质分析
游离氨基酸、核苷酸关联化合物、奥品、有机酸、无机离子和季铵盐类物质是鸢乌贼中主要的酸味相关物质。游离氨基酸对水产品的滋味有重要影响,通常呈现鲜味、甜味、酸味和苦味[19-20]。苦味氨基酸为精氨酸(Arg)、组氨酸(His)、赖氨酸(Lys)、脯氨酸(Pro);酸味氨基酸为谷氨酸(Glu)和天冬氨酸(Asp);甜味氨基酸为丝氨酸(Ser)、甘氨酸(Gly)、丙氨酸(Ala)、苏氨酸(Thr)。有机酸赋予了鱿鱼特有的酸味,准确测定鸢乌贼肉中有机酸的组成及含量对研究鸢乌贼肉中的怪酸味具有重要意义[9]。游离氨基酸和核苷酸关联化合物赋予了水产品特有的鲜味,并且二者的协同作用可以显著增强水产品的鲜味[21]。海洋软体动物在无氧代谢时体内氨基酸在相应的奥品脱氢酶催化下与糖酵解产生的丙酮酸缩合生成的奥品类物质[22],主要有章鱼肉碱、甘氨奥品、牛磺奥品和丙氨奥品,奥品类物质对维持细胞质pH值、渗透压恒定具有重要作用[23]。奥品具有类似乳酸的口感,在头足类动物中拥有与乳酸相似的厌氧代谢途径[24],是鸢乌贼肌肉酸味组成的重要物质之一,奥品含量的高低与动物体内游离氨基酸的改变量和体内细胞所处的有氧/无氧环境相关[25]。无机盐离子是水产品重要的辅助呈味成分,对水产品滋味具有重要作用[26];阳离子一般呈咸味,而阴离子对咸味有抑制作用[27]。TMAO和甜菜碱是头足类海产品中常见的含氮碱类物质,TMAO具有鲜味,对水产品鲜腥风味有重要贡献[28];甜菜碱类物质可赋予海产品鲜味、甜味并且增强其浓厚感[29-30],鲜味对酸味有抑制作用[31]。
表2 印度洋鸢乌贼肌肉中酸味相关物质的组成及含量
Table 2 Composition and contents of sour substances in the muscles of S. oualaniensis
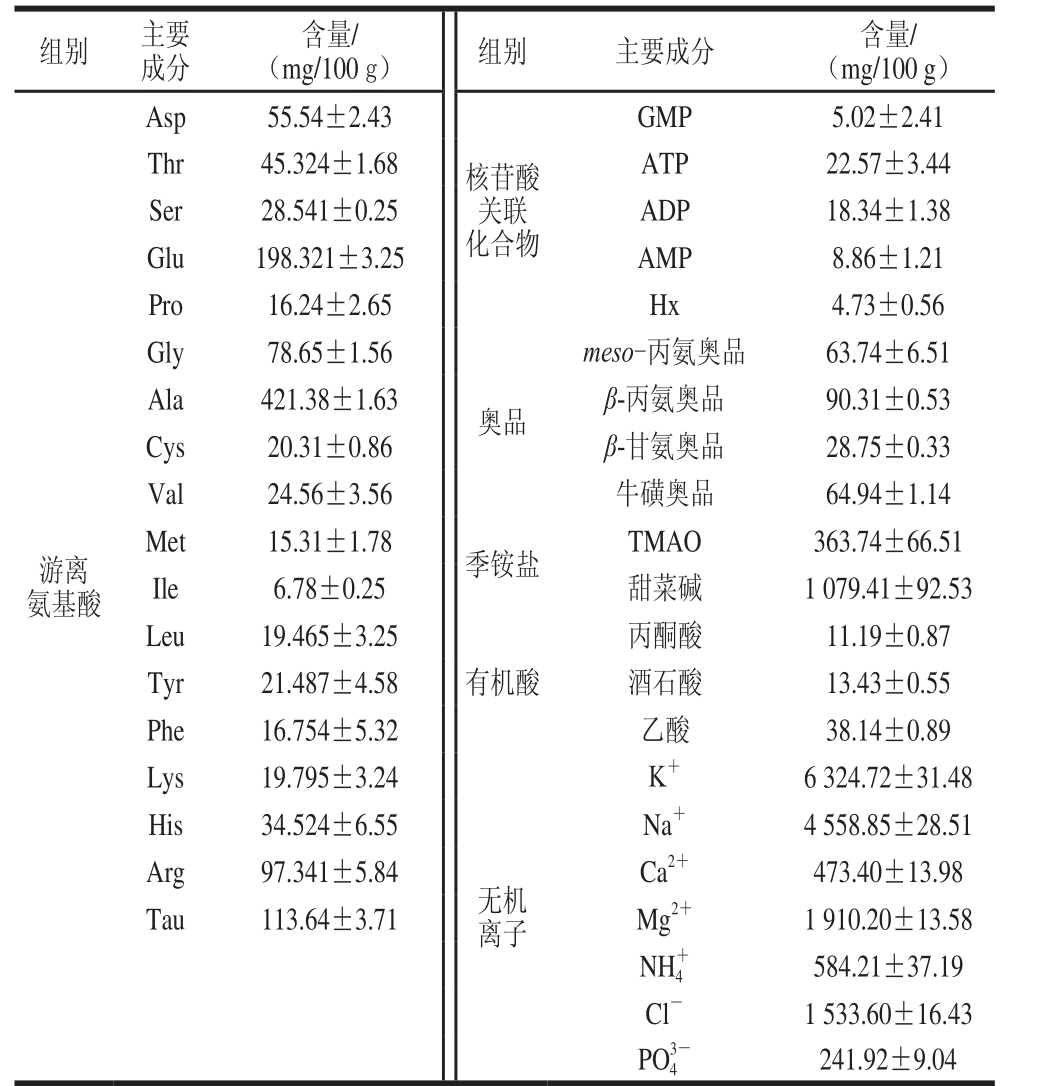
注:鸟嘌呤核苷酸(guanylate,GMP);二磷酸腺苷(adenosine diphosphate,ADP);腺嘌呤核苷酸(adenine nucleotide,AMP);次黄嘌呤(hypoxanthine,Hx)。
组别 主要成分 (mg/100 g) 组别 主要成分 含量/(mg/100 g)含量 /Asp 55.54±2.43 meso-丙氨奥品 63.74±6.51 Ala 421.38±1.63 β-丙氨奥品 90.31±0.53 Cys 20.31±0.86 β-甘氨奥品 28.75±0.33 Val 24.56±3.56 牛磺奥品 64.94±1.14 Met 15.31±1.78 季铵盐 TMAO 363.74±66.51 Ile 6.78±0.25 甜菜碱 1 079.41±92.53 Leu 19.465±3.25有机酸GMP 5.02±2.41 Thr 45.324±1.68 ATP 22.57±3.44 Ser 28.541±0.25 ADP 18.34±1.38 Glu 198.321±3.25 AMP 8.86±1.21 Pro 16.24±2.65 Hx 4.73±0.56 Gly 78.65±1.56奥品核苷酸关联化合物游离氨基酸丙酮酸 11.19±0.87 Tyr 21.487±4.58 酒石酸 13.43±0.55 Phe 16.754±5.32 乙酸 38.14±0.89 Lys 19.795±3.24 3- 241.92±9.04 K+ 6 324.72±31.48 His 34.524±6.55 Na+ 4 558.85±28.51 Arg 97.341±5.84 Ca2+ 473.40±13.98 Tau 113.64±3.71 Mg2+ 1 910.20±13.58 NH4+ 584.21±37.19 Cl- 1 533.60±16.43 PO4无机离子
从表2可以看出,印度洋鸢乌贼肌肉中游离氨基酸总含量为1 233.96 mg/100 g,少于Kagawa等[32]报道的日本乌贼中总游离氨基酸含量(3 147 mg/100 g),但接近Yamanaka[33]报道的秘鲁鱿鱼(Dosidicus gigas)中总游离氨基酸含量。鸢乌贼肌肉中含量较高的游离氨基酸为Ala、牛磺酸(Tau)、Glu、Arg、Gly和Asp,其中Glu和Asp为酸味氨基酸,Arg为苦味氨基酸,Ala和Gly为甜味氨基酸,较高含量的酸味氨基酸也可能是鸢乌贼肌肉呈酸味的原因之一。根据实验结果将所测得的游离氨基酸按含量分为3 组:高含量组(Ala、Tau、Glu、Arg、Gly、Asp)、中含量组(Thr、His、Ser、Val、Tyr、Cys)、低含量组(Lys、Leu、Phe、Pro、Met、Ile)。在核苷酸检测中,ATP和ADP含量较高,可能与鸢乌贼贮藏时间有关。在奥品的检测中,β-丙氨奥品的含量最高,为90.31 mg/10 0 g,占到整个奥品含量的36.45%,高于秘鲁鱿鱼的63.82 mg/100 g[34],β-丙氨奥品的高含量可能与鸢乌贼体内含量较高的Ala含量有关;meso-丙氨奥品和牛磺奥品的含量也较高,含量最低的奥品为β-甘氨奥品,但均高于秘鲁鱿鱼中奥品的含量,其原因可能是鸢乌贼肌肉中相应的游离氨基酸含量均高于秘鲁鱿鱼[34],并且催化丙酮酸与氨基酸缩合形成相应奥品的奥品脱氢酶的催化活性要高于秘鲁鱿鱼,较高的奥品含量可能直接影响了鸢乌贼肌肉的酸味感。季铵盐的测定中鸢乌贼TMAO含量与太平洋丛鱿鱼(Tradodes pacificus)中TMAO含量相似(198~1 134 mg/100 g)[32-33],但甜菜碱的含量低于赵巧灵等[27]测得阿根廷鱿鱼和秘鲁鱿鱼中甜菜碱的含量,这也说明了印度洋鸢乌贼酸味强于阿根廷鱿鱼,且味道不及阿根廷鱿鱼鲜美的原因。有机酸的检测中分别检出了酒石酸、丙酮酸和乙酸,其中酒石酸和乙酸的含量较高,且二者带有刺激性酸味,可能与鸢乌贼怪异的酸味有关,影响了鸢乌贼肉质的鲜美。鸢乌贼体内的有机酸不同于其他种类的鱿鱼[35],其原因尚不明确。无机离子中,阳 离子的含量远高于阴 离子,其中含量 最高为K+,占离子总量的40%以上。较高的NH4+含量也说明了鸢乌贼肌肉中 涩味和脱酸过程中强烈的氨味。
2.2 天然提取液与合成提取液的比较
与天然提取液相比,合成提取液能够较好地模拟天然提取液的滋味,合成提取液的酸味没有天然提取液重,苦涩味也没有天然提取液强。将合成提取液分成6 个组分,即游离氨基酸、核苷酸关联化合物、奥品、有机酸、无机离子和季铵盐类物质,并对这6 个组分进行感官评价,分析结果见表3。
表3 单个组别的感官实验
Table 3 Sensory descriptions of six individual sour compounds

组别 描述游离氨基酸 有较轻微甜味和酸味,多数人认为酸味不明显核苷酸关联化合物 有鲜味,稍有涩味奥品 有明显酸味,稍有涩味有机酸 有酸味和涩味无机离子 无酸味,有较重咸味季铵盐类 无酸味,有甜味和鲜味
2.3 组别减除实验
表4 感官组别减除实验
Table 4 Results of sensory omission experiments on six individual sour compounds

被减除组别 正确区分度(n=20)差异显著性差异程度0 1 2游离氨基酸 18 P<0.05 1 6 3核苷酸关联化合物 16 P<0.05 2 6 1奥品 20 P<0.05 0 1 9有机酸 18 P<0.05 0 8 2无机离子 17 P<0.05 1 8 1季铵盐类 15 P<0.05 1 9 0
将减除了任意一组的合成提取液进行感官评价实验,结果见表4。当减除游离氨基酸组时,合成液甜味稍有下降,酸味和鲜味降低,但酸味降低的程度不及奥品组和有机酸组的减除;当减除核苷酸组和季铵盐类组时,酸味和涩味变化不明显,甜味稍有下降,鲜味明显下降;当减除奥品组时,酸味基本消失,涩味降低,鲜味和咸味增加;当减除有机酸组时,酸味降低,鲜味和咸味加重;当减除无机离子组时,咸味消失,鲜味和酸涩味增加。感官评定结果表明:奥品和有机酸的酸味掩盖了鸢乌贼肌肉的鲜味,导致了令人不愉快的酸味,可能是使鸢乌贼肌肉呈酸味的主要物质;较高含量的甜味和苦味氨基酸一定程度上抑制了酸味;核苷酸关联化合物和季铵盐类物质与氨基酸起协同作用,对鲜味有较大影响;无机离子中较高含量的阳离子本身的咸味可以掩盖鸢乌贼肌肉的酸味和鲜味。通过上述实验可以看出,6 个组别对鸢乌贼肌肉酸味的形成都有一定影响,其中奥品和有机酸是构成鸢乌贼肌肉酸味的最主要物质;游离氨基酸和无机离子对酸味有一定抑制作用;核苷酸及其关联物和季铵盐类物质对酸味影响不大,可增加鲜味。
2.4 单个组别的减除实验
2.4.1 氨基酸对酸味的 贡献
根据游离氨基酸的含量,将18 种游离氨基酸按其含量分为3 组,分组结果见表5。当减除组A(Ala、Tau、Glu、Arg、Gly、Asp)时,鲜味和酸味稍有增加,苦味增加,甜味降低;当减除组B(Thr、His、Ser、Val、Tyr、Cys)时,甜味和苦味降低,酸味和鲜味无明显变化;当减除组C(Lys、Leu、Phe、Pro、Met、Ile)时,基本感知不到味觉变化,有甜味和苦味,稍有鲜味和酸味。在引起酸味明显变化的组A中,当减除Ala时,甜味下降明显,苦味和鲜味增加,酸味稍有增加;当减除Tau时,鲜味增加,有酸味且变化不明显;当减除Glu时,酸味和鲜味下降,苦味增加;当减除Arg时,苦味减少,酸味增加但不明显;当减除Gly时,整体味觉基本无变化;当减除Asp时,酸味增加,苦味减弱。在组B中,当减除Thr时,甜味稍减弱,酸味基本无变化;当减除His时,苦味降低,酸味稍有增加;当减除Ser时,甜味稍有加强,鲜味增加,酸味无明显变化;当减除Val、Tyr、Cys时,整体味觉无明显变化。结果表明:Glu、Asp等酸性氨基酸会影响鸢乌贼肌肉酸味,是构成酸味的物质;Arg等苦味氨基酸一定程度上抑制了酸味,对酸味强弱有一定影响;其他氨基酸如Ala、Tau等仅对酸味的呈现起协同作用。
表5 氨基酸减除实验
Table 5 Results of sensory omission experiments on amino acids
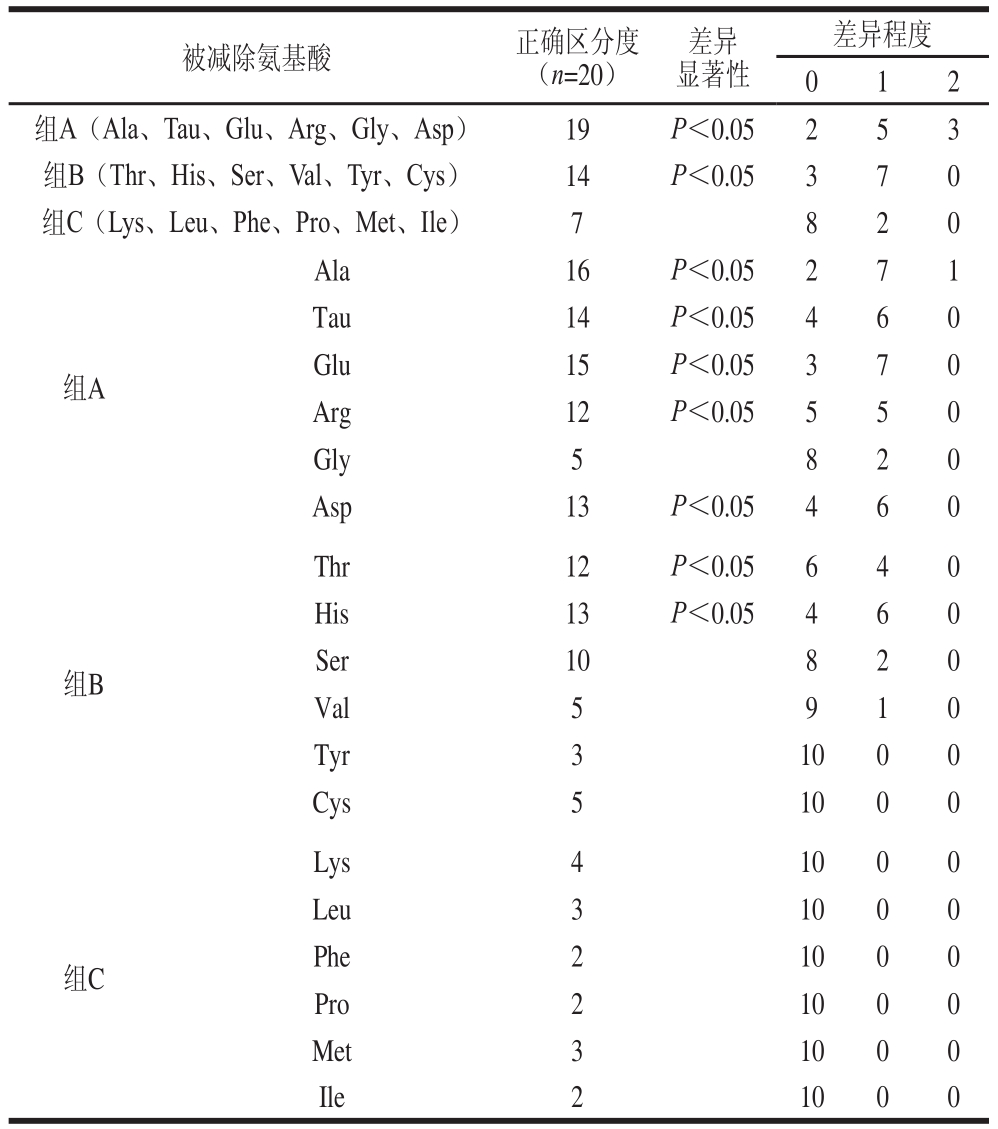
差异显著性被减除氨基酸 正确区分度(n=20)差异程度0 1 2组A(Al a、Tau 、Glu、Arg、Gly、As p) 19 P<0.05 2 5 3组B(Th r、His 、Ser、Val、Tyr、Cy s) 14 P<0.05 3 7 0组C(Ly s、Leu 、Phe、Pro、M et、Ile) 7 8 2 0组A Ala 16 P<0.05 2 7 1 Tau 14 P<0.05 4 6 0 Glu 15 P<0.05 3 7 0 Arg 12 P<0.05 5 5 0 Gly 5 8 2 0 Asp 13 P<0.05 4 6 0组B Thr 12 P<0.05 6 4 0 His 13 P<0.05 4 6 0 Ser 10 8 2 0 Val 5 9 1 0 Tyr 3 10 0 0 Cys 5 10 0 0组C Lys 4 10 0 0 Leu 3 10 0 0 Phe 2 10 0 0 Pro 2 10 0 0 Met 3 10 0 0 Ile 2 10 0 0
2.4.2 核苷酸关联化合物对酸味的贡献
表6 核苷酸关联化合物减除实验
Table 6 Results of sensory omission experiments on nucleotide-related compounds

被减除成分 正确区分度(n=20)差异显著性差异程度0 1 2 ATP 16 P<0.05 3 5 2 ADP 15 P<0.05 6 3 1 AMP 14 P<0.05 7 3 0 GMP 7 9 1 0 Hx 6 10 0 0
如表6所示,核苷酸关联化合物中,当减除ATP和ADP时,鲜味和咸味明显减弱,酸味稍微 增加,但增加不明显;当减除AMP时,鲜味略微降低,但变化不明显,酸味基本无变化;当减除Hx和GMP时,溶液口感基本无变化。结果表明:ATP和ADP、AMP是鸢乌贼体内的主要呈鲜物质,一定程度上抑制了酸味,核苷酸关联化合物也仅对酸味起到抑 制的作用。
2.4.3 奥品对酸味的贡献
表7 奥品类物质减除实验
Table 7 Re sults of s ensory omission experiments on opines

差异显著性被减除成分 正确区分度(n=20)差异程度0 1 2 β-丙氨奥品 19 P<0.05 0 4 6牛磺奥品 18 P<0.05 0 7 3 meso-丙氨奥品 16 P<0.05 1 8 1 β-甘氨奥品 14 P<0.05 7 3 0
如表7所示,在奥品类物质中,当 减除含量最 高的β-丙氨奥品时,绝大多数人认为酸味大幅降低,涩味减弱,鲜味有较明显增 加;当减除含量第二 高的牛磺奥品时,酸味下降仍很明显,涩味稍有减弱,鲜味增加,涩味减弱,鲜味明显增加;当减除meso-丙氨奥品时,酸味略微下降,鲜味增加,涩味稍微增 加;当减除含量最少的β-甘氨奥品时,酸味变化不明显,其他味道基本不变。 结果表明:β-丙氨奥品、牛磺奥品和meso-丙氨奥品对印度洋鸢乌贼的酸味影响最大,且奥品含量的高低直接影响了酸味的强弱,奥品含量越高,酸味越强;奥品含量越低,酸味和涩味越弱。奥品是鸢乌贼肌肉呈酸味最重要的物质。
2.4.4 季铵盐类 物质对酸味的影响
表8 季铵盐类物质减除实验
Table 8 Results of sensory omission experiments on quaternary ammonium saallttss
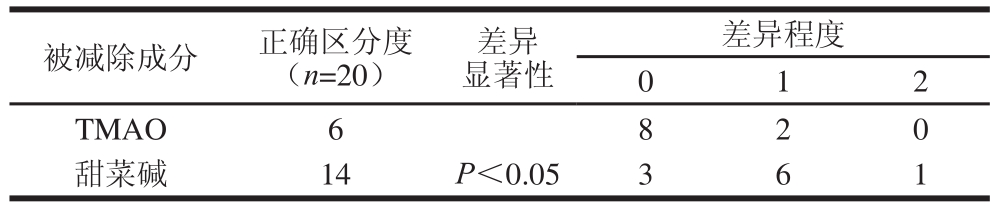
被减除成分 正确区分度(n=20)差异显著性差异程度0 1 2 TMAO 6 8 2 0甜菜碱 14 P<0.05 3 6 1
如表8所示,在季铵盐类物质中,当减除TMAO时,溶液整体口味无明显变化,可能是TMAO含量降低的原因;当减除甜菜碱时,鲜甜味基本消失,酸味稍微增加。结果表明:季铵盐类物质对鸢乌贼鲜甜的口感有一定影响,对酸味影响不大,但在一定程度上会抑制酸味。
2.4.5 有机酸对酸味的影响
表9 有机酸减除实验
Table 9 Results of sensory omission experiments on organic acids

被减除成分 正确区分度(n=20)差异显著性差异程度0 1 2丙酮酸 7 9 1 0酒石酸 14 P<0.05 4 6 0乙酸 15 P<0.05 4 5 1
如表9所示,在有机酸中,当减除丙酮酸时,酸味变化不明显,溶液整体口感变化不大,可能与其含量较低有关;当减除酒石酸和乙酸时,溶液酸味降低,但影响不及奥品类物质减除时大,鲜味稍微增加。结果表明:酒石酸和乙酸增加了鸢乌贼酸味,且对鲜味有抑制作用。
2.4.6 无机离子对酸味的影响
表10 无机离子减除实验
Table 10 Results of sensory omission experiments on inorganic ions
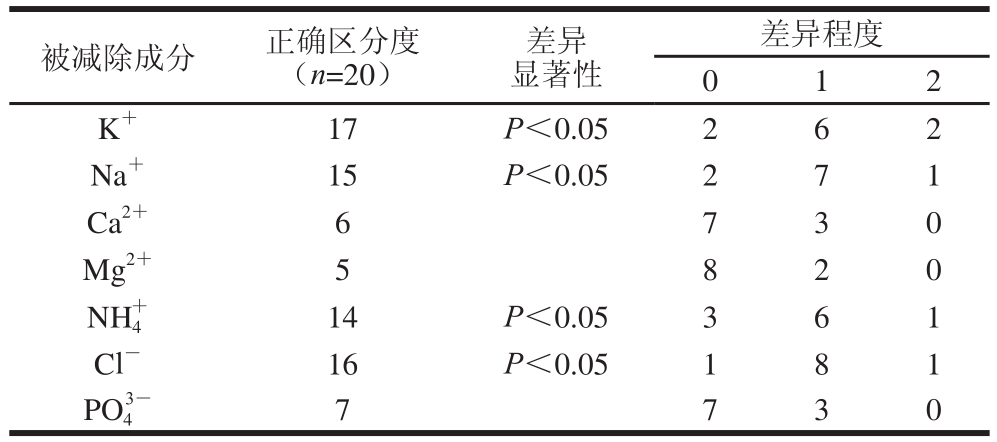
被减除成分 正确区分度(n=20)差异显著性差异程度0 1 2 K+ 17 P<0.05 2 6 2 Na+ 15 P<0.05 2 7 1 Ca2+ 6 7 3 0 Mg2+ 5 8 2 0 NH4+ 14 P<0.05 3 6 1 Cl- 16 P<0.05 1 8 1 PO43- 7 7 3 0
如表10所示,在无机离子组中,当减除K+、Na+时,溶液酸涩感增加,咸味明显减弱;当减除Ca2+、Mg2+时,溶液整体滋味无明显变化;当减除 时,苦味明显降低,酸味和鲜味有一定程度增加;当减除Cl-时,酸味增加,咸味也有一定程度增加但不明显;当减除
时,苦味明显降低,酸味和鲜味有一定程度增加;当减除Cl-时,酸味增加,咸味也有一定程度增加但不明显;当减除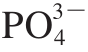 时,鲜味有所减弱,其他滋味变化不明显。实验结果表明:K+、Na+、NH+4、Cl-是鸢乌贼酸味的重要影响物质,对酸味有抑制作用,其中K+、Na+影响较明显。
时,鲜味有所减弱,其他滋味变化不明显。实验结果表明:K+、Na+、NH+4、Cl-是鸢乌贼酸味的重要影响物质,对酸味有抑制作用,其中K+、Na+影响较明显。
3 结 论
对印度洋鸢乌贼酸味相关成分的分析结果表明,游离氨基酸、核苷酸关联化合物、奥品、有机酸、无机离子和季铵盐类物质是鸢乌贼肌肉中主要的酸味相关物质。Ala、Tau、Glu、Arg、ATP、ADP、β-丙氨奥品、meso-丙氨奥品、牛磺奥品、甜菜碱、乙酸、K+、Na+、NH4+含量较大,其中奥品中β-丙氨奥品的含量最高,为90.31 mg/100 g,占奥品含量的36.45%,含量最低的为β-甘氨奥品。通过感官减除实验对鸢乌贼肌肉呈酸味的原因分析结果表明,Glu、Asp、Arg、奥品类物质、酒石酸、乙酸、K+、Na+、NH4+、Cl-是鸢乌贼酸味的重要影响物质。Arg、K+、Na+、NH4+、Cl-对酸味有抑制作用,其中K+、Na+影响较明显;Glu、Asp、酒石酸、乙酸、β-丙氨奥品、牛磺奥品和meso-丙氨奥品对鸢乌贼酸味有增强作用。其中β-丙氨奥品、牛磺奥品和meso-丙氨奥品是印度洋鸢乌贼的特征酸味物质,且它们的含量越高,酸味越强,是印度洋鸢乌贼肌肉呈酸味的主要原因。
[1] 泮凤. 除酸剂对秘鲁鱿鱼的除酸效果 及对其品质的影响[D]. 舟山:浙江海洋学院, 2014.
[2] 邵锋, 陈新军. 印度洋西北海域鸢乌贼渔场分布与海面高度的关系[J].海洋科学, 2008, 32(11): 88-92.
[3] 范江涛, 张俊, 冯雪, 等. 南沙海域鸢乌贼渔场与海洋环境因子的关系[J]. 上海海洋大学学报, 2019, 28(3): 103-110. DOI:10.12024/jsou.20190102505.
[4] 曲映红, 陈新军, 陈舜胜. 印度洋西北海域鸢乌贼理化特性的初步分析[J]. 上海海洋大学学报, 2004, 13(4): 335-338. DOI:10.3969/j.issn.1004-7271.2004.04.009.
[5] 王进勉, 薛长湖, 刘鑫, 等. 印度洋鸢乌贼加工特性的初步研究[J]. 食品工业科技, 2007, 28(6): 128-130. DOI:10.3969/j.issn.1002-0306.2007.06.037.
[6] 冯慧, 付雪艳, 薛长湖, 等. 印度洋鸢乌贼氧化三甲胺脱甲基酶的分离纯化及生化特性的研究[J]. 食品与发酵工业, 2008, 34(9): 27-32.DOI:10.13995/j.cnki.11-1802/ts.2008.09.040.
[7] 王雅楠. 钠盐对冷冻秘鲁鱿鱼片脱酸和保水性质的影响[D]. 大连:大连海洋大学, 2014.
[8] HAQUE M E, FUJISAWA T, YAMAMOTO M, et al. Improved HPLC determination of acidic opines by phenylisothiocyanate derivatization and its application to marine animals[J]. Acta Medica Okayama, 2000, 54(1): 1-8. DOI:10.1016/S0024-3205(99)00670-0.
[9] 刘书来, 郭元帅, 许凯希, 等. 高效液相色谱法测定秘鲁鱿鱼肌肉中的有机酸[J]. 食品与发酵工业, 2015, 41(10): 135-139.DOI:10.13995/j.cnki.11-1802/ts.201510025.
[10] 颜敏, 刘园园, 贺瑞玲, 等. ICP-MS 法测定药用玻璃容器中13 种金属元素的浸出量[J]. 药物分析杂志, 2016, 36(1): 133-137.DOI:10.16155/j.0254-1793.2016.01.21.
[11] WEI X, ZHANG X, ZHENG X, et al. Determination of chloride ion and nitrate nitrogen in cellar water of Huan County Qingyang[J].Advances in Analytical Chemistry, 2018, 8(3): 129-136.DOI:10.12677/AAC.2018.83016.
[12] 国家卫生和计划生育委员会, 国家食品药品监督管理总局. 食品中磷的测定: GB 5009.87—2016[S]. 北京: 中国标准出版社, 2016.
[13] MÁRQUEZ-RÍOS E, MORÁN-PALACIO E F, LUGO-SÁNCHE Z M E,et al. Postmortem biochemical behavior of giant squid (Dosidicus gigas) mantle muscle stored in ice and its relation with quality parameters[J]. Journal of Food Science, 2010, 72(7): C356-C362.
[14] 黄国霞, 赖春华, 李军生, 等. 6 种水产动物中氧化三甲胺的提取与含量测定[J]. 食品科技, 2012, 37(7): 305-307. DOI:10.13684/j.cnki.spkj.2012.07.010.
[15] 黄丽贞. 海产品中呈味成份甜菜碱的测定[J]. 上海海洋大学学报,1994, 3(3): 160-163.
[16] 翁丽萍. 养殖大黄鱼和野生大黄鱼风味的研究[D]. 杭州: 浙江工商大学, 2012.
[17] 石建高, 钟文珠. 太平洋柔鱼中呈味物质的抽提方法比较[J].大连海洋大学学报, 2002, 17(4): 291-296. DOI:10.3969/j.issn.1000-9957.2002.04.005.
[18] 国家质量监督检验检疫总局. 肉与肉制品感官评定规范: GB/T 22210—2008[S]. 北京: 中国标准出版社, 2008.
[19] PRATAMA R I, ROSTINI I, ROCHIMA E. Amino acid profile and volatile flavour compounds of raw and steamed Patin catfish(Pangasius hypophthalmus) and narrow-barred Spanish mackerel(Scomberomorus commerson)[C]//Proceedings of the IOP Conference Series: Earth and Environmental Science, F, 2018. DOI:10.1088/1755-1315/116/1/012056.
[20] 付娜, 王锡昌. 电子舌分析和感官评价在游离氨基酸对中华绒螯蟹整体滋味贡献评价中的研究[J]. 食品工业科技, 2014, 35(20): 91-96.DOI:10.13386/j.issn1002-0306.2014.20.011.
[21] 尹涛, 刘敬科, 赵思明, 等. 冷藏和热加工对鲢肌肉主要滋味活性物质的影响[J]. 华中农业大学学报, 2015, 34(1): 108-114.DOI:10.13300/j.cnki.hnlkxb.2015.01.018.
[22] 郑尧, 田元勇, 刘洋, 等. 海洋经济贝类中Opine脱氢酶研究进展[J].大连海洋大学学报, 2019, 34(2): 296-302. DOI:10.16535/j.cnki.dlhyxb.2019.02.021.
[23] JIMÉNEZ-RUIZ E, OCAO-HIGUERA V M, MAEDA-MARTÍNEZ A N, et al. Effect of seasonality and storage temperature on rigor mortis in the adductor muscle of lion's paw scallop Nodipecten subnodosus[J]. Aquaculture, 2013, 388/389/390/391(1): 35-41.DOI:10.1016/j.aquaculture.2013.01.006.
[24] LEE A C, LEE K T. The enzyme activities of opine and lactate dehydrogenases in the gills, mantle, foot, and adductor of the hard clam Meretrix lusoria[J]. Journal of Marine Science and Technology,2011, 19(4): 361-367.
[25] HARCET M, PERINA D, PLEŠE B. Opine dehydrogenases in marine invertebrates[J]. Biochemical Genetics, 2013, 51(9/10): 666-676.DOI:10.1007/s10528-013-9596-7.
[26] UEDA Y, FUKAMI K. Flavor constituents in savory seafood:dried kelp (kombu), scallop, and dried bonito (Katsuobushi)[J].Aqua-BioScience Monographs, 2017, 10(1): 1-22. DOI:10.5047/absm.2017.01001.0001.
[27] 赵巧灵, 吴佳佳, 李春萍, 等. 3 种鱿鱼的特征滋味成分分析与比较[J].中国食品学报, 2014, 14(6): 244-250. DOI:10.16429/j.1009-7848.2014.06.005.
[28] 翁丽萍, 赵芸, 陈飞东, 等. 养殖大黄鱼滋味成分及其呈味贡献的研[J]. 食品工业科技, 2015, 36(3): 82-90. DOI:10.13386/j.issn1002-0306.2015.03.008.
[29] 祝亚辉, 曹文红, 章超桦. 华贵栉孔扇贝干贝呈味特性评价[J]. 食品与发酵工业, 2016, 42(12): 183-188. DOI:10.13995/j.cnki.11-1802/ts.201612032.
[30] 曲广新. 甜菜碱的营养功能及应用[J]. 畜牧与饲料科学, 2014,35(12): 36. DOI:10.3969/j.issn.1672-5190.2014.12.014.
[31] 宋兰兰. 筛选乳酸菌与KCl部分替代NaCl改善低钠盐干酪品质[D].哈尔滨: 东北农业大学, 2017.
[32] KAGAWA M, MATSUMOTO M, HATAE K. Taste differences among three kinds of squid and the effect of cold storage on the taste[J]. Journal of Home Economics of Japan, 1999, 50(12): 1245-1254.
[33] YAMANAKA H. Studies on components of off- flavor in the muscle of American jumbo squid[J]. Nippon Suisan Gakkaishi, 1995, 61(4):612-618. DOI:10.2331/suisan.61.612.
[34] 郭元帅. 秘鲁鱿鱼特征酸味物质分析及酸味产生机制研究[D].杭州: 浙江工业大学, 2016.
[35] GARCÍA-SÁNCHEZ G, SOTELO-ROMERO C R, PACHECOAGUILAR R, et al. Effect of freezing on protein denaturation and gelling capacity of jumbo squid (Dosidicus gigas) mantle muscle[J].LWT-Food Science and Technology, 2015, 60(2): 737-742.DOI:10.1016/j.lwt.2014.10.051.