烟熏液具有赋予食品烟熏风味的作用[1],且在应用到食品之前,已经定向除去了多环芳烃等化学危害物,因而被消费者 所喜爱。一直以来,烟熏调味料作为商业调味添加剂被广泛运用于各种食品,如鱼类、肉类、乳制品、坚果和零食等,其化学成分与感官特性之间的关系是食品风味科学家们一直关注的问题,尤其在烟熏调味料的化学成分研究方面,取得了很大发展[2]。姜绍通[3]、吴靖娜[4]等采用顶空固相微萃取-气相色谱-质谱(gas chromatography-mass spectrometry,GC-MS)联用技术测定烟熏液中挥发性成分,发现酚类化合物对烟熏风味的贡献最大,这与Guillen[5]和Giri[6]等的研究结果相似。有学者汇总了近年来有关烟熏液风味成分文献,发现烟熏液中的主要成分有酚类、羰基类、有机酸类、醇类及酯类等化合物[7],这些成分相互作用,在一定程度上改变了食品的感官特性包括味道、质地和颜色以及保质期[8]。基于烟熏液在食物中形成某些特性的能力取决于其所含成分的性质和浓度[9],而商业烟熏液的化合物种类复杂多样,且含量各不相同。因此,充分了解烟熏液中的化学成分对食品开发人员在特殊的食品基质中选择合适的烟熏液具有重要的意义和价值。
目前关于烟熏液风味分析报道中,GC-MS技术为分析烟熏液风味成分的主要手段,但该技术只能检测单一物质挥发性组分,具有一定的局限性[10]。电子鼻技术具有模仿人类嗅觉系统的功能,可以对复杂气味进行检测和识别[11]。电子舌作为一种模拟人体味觉系统对食品进行评价和检测技术,现已广泛用于食品、医药等领域[12]。目前将GC-MS结合电子鼻、电子舌技术分析烟熏液的研究鲜见报道,因此,为使研究人员更好地了解烟熏液的复杂成分,本研究以9 种不同商业烟熏液为研究对象,采用GC-MS联用技术结合电子鼻和电子舌技术对其风味物质系统比较和分析,旨在探究不同类型烟熏液中风味物质的种类及浓度,寻找不同烟熏液风味物质的差异,为商业烟熏液在实际食品加工运用中提供一定的参考。
1 材料与方法
1.1 材料与试剂
山楂核烟熏液I号、II号、II-2002、II-2003 济南华鲁食品有限公司;红箭烟熏液Smokez poly C-10-03(C-10-03)、Smokez poly C-10-05(C-10-05)、Smokez poly C-10-10(C-10-10)、Smokez poly C-10-11(C-10-11)、Smokez poly C-10-22(C-10-22) 美国红箭公司;2-辛醇(99%)、二氯甲烷(色谱纯) 上海阿拉丁生化科技股份有限公司;C7~C40正构烷烃标准品 美国o2si公司。
1.2 仪器与设备
7890B GC仪 美国Agilent公司;LECO Pegasus HT MS仪 美国LECO公司;α-Gemini型电子鼻 法国Alpha MOS公司;HS-100型自动进样器 瑞士CTC公司;Avanti JXN-26高速冷冻离心机 贝克曼库尔特商贸有限公司;SA-402B味觉分析系统 日本Insent公司。
1.3 方法
1.3.1 电子鼻传感器性能
电子鼻传感器的性能描述如表1所示。
表1 电子鼻传感器性能描述
Table 1 Performance of 6 electronic nose sensors

序号 传感器名称 性能描述 敏感物质类型1 T30/1 对有机化合物灵敏 极性化合物、氯化氢2 T70/2 对芳香族化合物灵敏 甲苯3 PA/2 对有机化合物以及有毒挥发性物质灵敏 乙醇、氨水、胺类化合物4 P30/2 对有机化合物灵敏 氯化氢、酮5 LY2/AA 对有机化合物灵敏 乙醇、丙酮、氨6 LY2/gCT 对易燃气体灵敏 丙烷、丁烷
1.3.2 电子鼻检测条件
参考王琼等[13]的方法,取2.5 mL烟熏液样品于10 mL顶空瓶中,在室温下平衡10 min进样分析。顶空加热温度65 ℃;加热时间180 s;延滞采集时间600 s;数据采集时间120 s;采集周期1.0 s;流速150 mL/min;每个样品做3 次重复。
1.3.3 电子舌检测条件
采用2 步清洗法。清洗溶剂90 s,清洗溶剂120 s,清洗溶剂120 s,调节溶剂30 s,样品液30 s,清洗溶剂3 s,清洗溶剂3 s,标准溶液30 s。
1.3.4 烟熏液风味物质的测定
1.3.4.1 样品前处理
参考李琦等[14]的方法,稍作修改。吸取烟熏液3 mL置于离心管,加入二氯甲烷、再加入一定浓度的内标2-辛醇,2 000 r/min旋涡混合10 min、直立放入冰箱进行萃取,取出解冻,3 500 r/min离心10 min,吸取下层有机相过无水硫酸钠后,过0.22 μm有机滤膜进仪器分析,每个样品重复3 次,将得到的数据取平均值。
1.3.4.2 GC-MS条件
GC条件:DB-WAX色谱柱(30 m×0.250 mm,0.25 μm);进样口温度250 ℃;进样量1 μL;分流比20∶1;载气(He)流速1.0 mL/min;程序升温:50 ℃保持0.5 min,以3 ℃/min升温至100 ℃,以6 ℃/min升温至230 ℃,保持20 min。
MS条件:电子电离源;电子能量70 eV;离子源温度200 ℃;四极杆温度180 ℃;传输线温度250 ℃;溶剂延迟6 min;质量扫描范围m/z 35~500。
1.3.4.3 定性分析
将C7~C40正构烷烃标准品在与样品相同的进样条件下进行分析,获得保留时间,按式(1)计算保留指数[15]:
式中:n为碳原子数;tx为待测组分的保留时间/min;tn为碳原子数为n的正构烷烃保留时间/min;tn+1为碳原子数为n+1的正构烷烃保留时间/min;tn-1为碳原子数为n-1的正构烷烃保留时间/min。
1.3.4.4 定量分析
根据己知的内标化合物浓度对挥发性风味组分进行半定量分析,依据化合物的峰面积比值与含量呈正比的原理,按式(2)计算每一种挥发性风味组分相对于内标化合物的含量[16]:
式中:Cx为未知挥发性风味组分质量浓度/(mg/L);C0为烟熏液中内标化合物质量浓度/(mg/L);Sx为未知挥发性风味组分峰面积;S0为添加的内标化合物峰面积。
1.4 数据处理
电子鼻数据利用Alpha Soft V12.0软件进行分析;GC-MS采用工作站自带数据处理软件进行处理,实验数据经过Microsoft Excel 2013进行整理;电子舌结果采用SPSS 24.0软件进行主成分分析(principal component analysis,PCA),采用Origin 2018进行相应绘图。
2 结果与分析
2.1 电子鼻测定结果
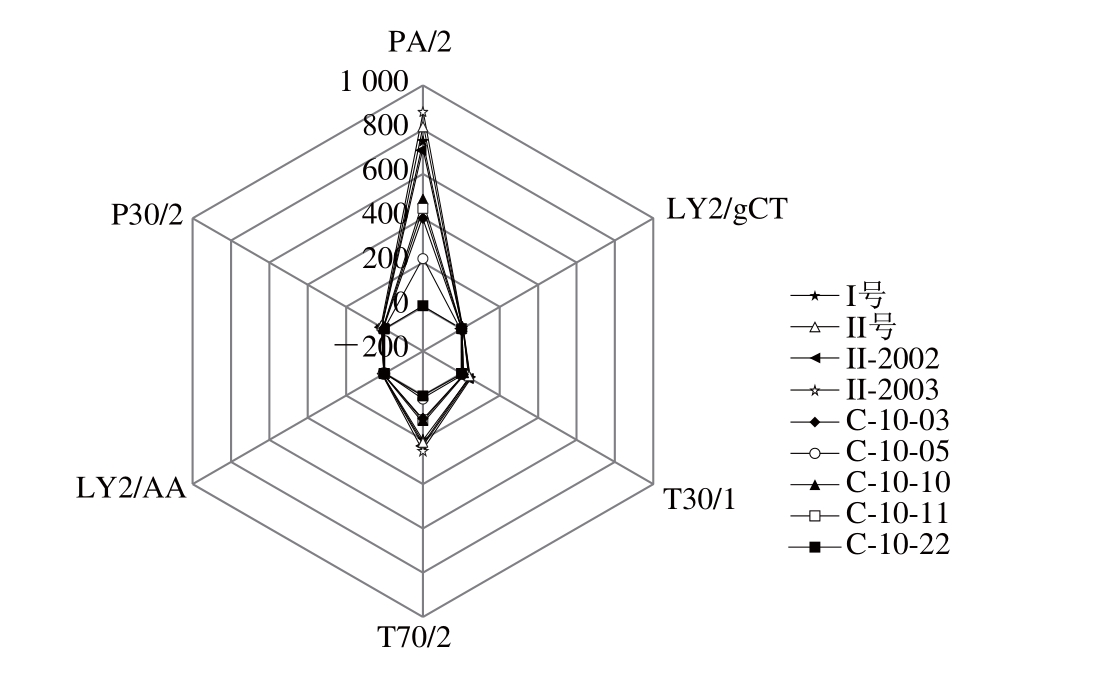
图1 传感器的感应强度雷达图
Fig. 1 Radar graph for odor intensity of nine liquid smokes measured by electronic nose
从图1可以看出,9 种不同烟熏液样品的风味轮廓相似,但每个传感器对香气的响应强度都有所不同[17],且各样品的香气成分有一定的差别,其中传感器PA/2和T70/2响应峰值较大,说明不同类型烟熏液中的有机化合物和芳香族化合物风味较为明显,而PA/2又远高于T70/2,且II-2003>II号>I号>II-2002>C-10-10>C-10-11>C-10-03>C-10-05>C-10-22,前4 种烟熏液在PA/2的响应值几乎聚集在一起,说明这4 种山楂核烟熏液在风味上具有一定的相似性。而后面5 种红箭烟熏液响应值较为分散,原因可能是烟熏液中风味物质不同而引起香气的差异。2 组不同类型烟熏液的香气响应值存在的异同,可能是由于红箭烟熏液在提取风味物质时,由于提取方法的不同,从而引起烟熏液中有机化合物和芳香族化合物的数量在某种程度上的变化。
2.2 电子舌测定结果
表2 电子舌对不同类型烟熏液的响应分析
Table 2 Electronic tongue responses to different liquid smokes

注:同列不同小写字母表示差异显著(P<0.05)。
样品名 咸味 酸味 苦味 涩味 鲜味 丰富度I号 -22.65±0.53cd4.38±4.88a 2.15±0.58e -6.78±0.58c 2.06±0.82b 2.06±0.82a II号 -23.68±0d 5.45±4.84a 1.88±0.48de -5.91±0.35c 1.68±0.77b 1.68±0.77a II-2002 -22.32±0c -0.38±4.54a 2.71±0.38cde -6.36±0.25c 3.01±0.77b 3.01±0.77a II-2003 -21.94±0c -4.72±4.35a 3.39±0.27c -6.46±0.3c 4.1±0.76b 4.1±0.76a C-10-03 -18.42±0.3a-27.81±3.33b10.49±0.13b -2.11±0.08b 8.96±0.73a 8.96±0.73a C-10-05 -20.64±0.72b-4.39±4.24a 3.03±0.19cd -5.72±0.47c 3.75±0.94b 3.75±0.94a C-10-10 -20.58±0.23b-27.88±2.47b13.06±0.14a 0.03±0.11a 6.83±0.5a 6.83±0.5a
由表2可知,6 种滋味传感器对7 种不同类型的烟熏液滋味均有响应,但敏感程度各有不同,其中2 组烟熏液在咸味上存在明显差异(P<0.05),且红箭烟熏液强于山楂核烟熏液;而对于酸味、涩味和鲜味,C-10-03和C-10-10两种烟熏液与其余5 种烟熏液差异明显,且这2 种烟熏液酸味稍弱于其他5 种烟熏液,而涩味和鲜味则高于其他5 种;对于苦味,这7 种类型的烟熏液存在较大差异,而丰富度则差异不明显。

图2 电子舌PPCCAA
Fig. 2 Principal component analysis based on electronic tongue data
如图2A所示,PC1和PC2的总贡献率接近100%,说明电子舌PCA法适用于烟熏液的滋味评价。从图2B可以看出,7 个烟熏液样品分布较散乱,其中C-10-03和C-10-10位于PC1左侧,而I号、II号、II-2002、II-2003、C-10-05烟熏液位于PC2右侧,说明PC1对其具有较好的区分效果;I号烟熏液在PC2上距离II号、II-2002、II-2003、C-10-05烟熏液较远,所以PC2对其也具有一定的区分效果。结合图2A,C-10-03和C-10-10两种类型的烟熏液主要受咸味影响,剩余5 种烟熏液主要是受鲜味、苦味和涩味及丰富度的影响,其中I号烟熏液同时受到酸味的影响。
2.3 GC-MS测定结果
表3 不同类型烟熏风味化合物的GC-MS鉴定结果
Table 3 Results of GC-MS Identification of different smoke liquid compounds

编号 化合物 保留指数质量浓度/(mg/L)I号 II号 II-2002 II-2003 C-10-03 C-10-05 C-10-10 C-10-11 C-10-22 1苯基丙酮 1 710 0.98 — — — — — — — —2环己酮 1 286 — — — 1.23 — — — — —3 2,5-己二酮 1 498 — — — — 2.84 4.58 2.90 — —4 2-甲基环戊酮 1 178 4.42 8.90 8.91 4.53 — 25.85 — — —5 甲基环戊烯醇酮 1 366 66.21 59.64 58.92 26.42 222.75 108.58 459.99 317.10 —6 2,3-二甲基-2-环戊烯酮 1 539 444.39 132.52 30.33 15.67 225.79 282.94 268.62 127.71 —
续表3
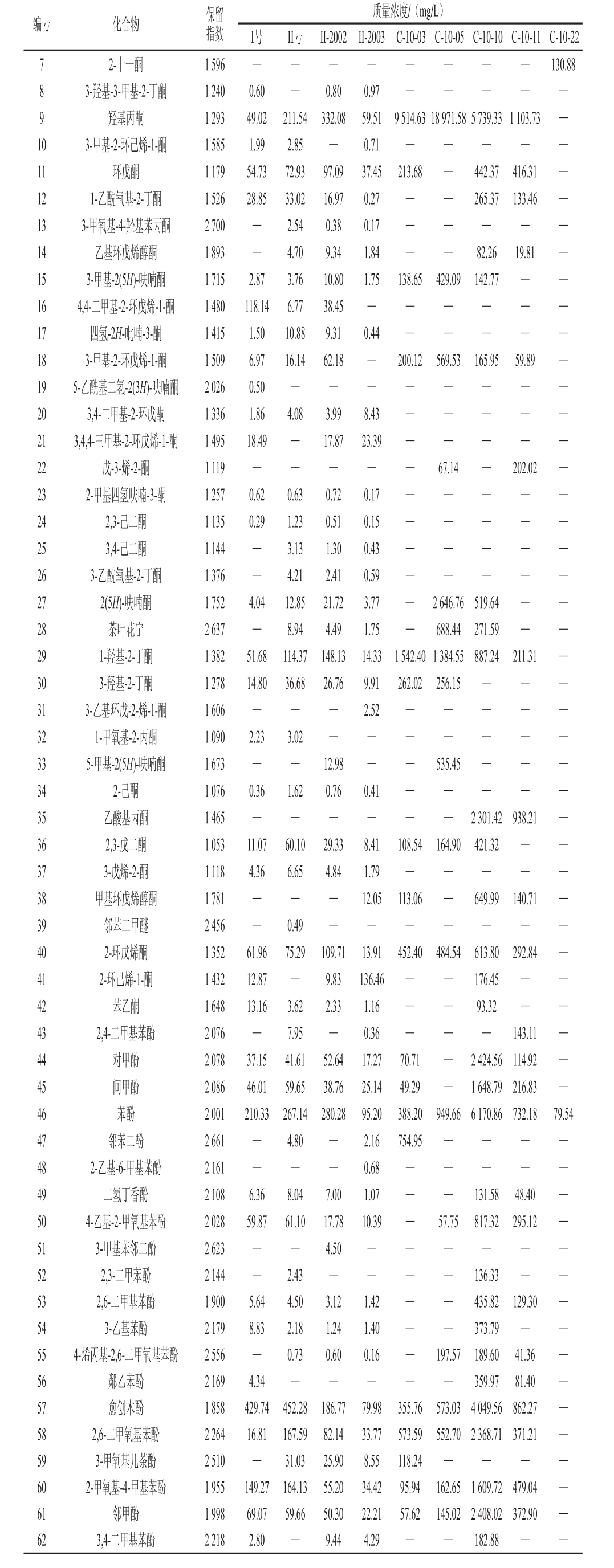
编号 化合物 保留指数质量浓度/(mg/L)I号 II号 II-2002II-2003 C-10-03 C-10-05 C-10-10 C-10-11 C-10-22 7 2-十一酮 1 596 — — — — — — — —130.88 8 3-羟基-3-甲基-2-丁酮 1 240 0.60 — 0.80 0.97 — — — — —9羟基丙酮 1 293 49.02 211.54 332.08 59.51 9 514.63 18 971.58 5 739.33 1 103.73 —10 3-甲基-2-环己烯-1-酮 1 585 1.99 2.85 — 0.71 — — — — —11 环戊酮 1 179 54.73 72.93 97.09 37.45 213.68 — 442.37 416.31 —12 1-乙酰氧基-2-丁酮 1 526 28.85 33.02 16.97 0.27 — — 265.37 133.46 —13 3-甲氧基-4-羟基苯丙酮 2 700 — 2.54 0.38 0.17 — — — — —14 乙基环戊烯醇酮 1 893 — 4.70 9.34 1.84 — — 82.26 19.81 —15 3-甲基-2(5H)-呋喃酮 1 715 2.87 3.76 10.80 1.75 138.65 429.09 142.77 — —16 4,4-二甲基-2-环戊烯-1-酮 1 480 118.14 6.77 38.45 — — — — — —17 四氢-2H-吡喃-3-酮 1 415 1.50 10.88 9.31 0.44 — — — — —18 3-甲基-2-环戊烯-1-酮 1 509 6.97 16.14 62.18 — 200.12 569.53 165.95 59.89 —19 5-乙酰基二氢-2(3H)-呋喃酮 2 026 0.50 — — — — — — — —20 3,4-二甲基-2-环戊酮 1 336 1.86 4.08 3.99 8.43 — — — — —21 3,4,4-三甲基-2-环戊烯-1-酮 1 495 18.49 — 17.87 23.39 — — — — —22 戊-3-烯-2-酮 1 119 — — — — — 67.14 — 202.02 —23 2-甲基四氢呋喃-3-酮 1 257 0.62 0.63 0.72 0.17 — — — — —24 2,3-己二酮 1 135 0.29 1.23 0.51 0.15 — — — — —25 3,4-己二酮 1 144 — 3.13 1.30 0.43 — — — — —26 3-乙酰氧基-2-丁酮 1 376 — 4.21 2.41 0.59 — — — — —27 2(5H)-呋喃酮 1 752 4.04 12.85 21.72 3.77 — 2 646.76 519.64 — —28 茶叶花宁 2 637 — 8.94 4.49 1.75 — 688.44 271.59 — —29 1-羟基-2-丁酮 1 382 51.68 114.37 148.13 14.33 1 542.40 1 384.55 887.24 211.31 —30 3-羟基-2-丁酮 1 278 14.80 36.68 26.76 9.91 262.02 256.15 — — —31 3-乙基环戊-2-烯-1-酮 1 606 — — — 2.52 — — — — —32 1-甲氧基-2-丙酮 1 090 2.23 3.02 — — — — — — —33 5-甲基-2(5H)-呋喃酮 1 673 — — 12.98 — — 535.45 — — —34 2-己酮 1 076 0.36 1.62 0.76 0.41 — — — — —35 乙酸基丙酮 1 465 — — — — — — 2 301.42 938.21 —36 2,3-戊二酮 1 053 11.07 60.10 29.33 8.41 108.54 164.90 421.32 — —37 3-戊烯-2-酮 1 118 4.36 6.65 4.84 1.79 — — — — —38 甲基环戊烯醇酮 1 781 — — — 12.05 113.06 — 649.99 140.71 —39 邻苯二甲醚 2 456 — 0.49 — — — — — — —40 2-环戊烯酮 1 352 61.96 75.29 109.71 13.91 452.40 484.54 613.80 292.84 —41 2-环己烯-1-酮 1 432 12.87 — 9.83 136.46 — — 176.45 — —42 苯乙酮 1 648 13.16 3.62 2.33 1.16 — — 93.32 — —43 2,4-二甲基苯酚 2 076 — 7.95 — 0.36 — — — 143.11 —44 对甲酚 2 078 37.15 41.61 52.64 17.27 70.71 — 2 424.56 114.92 —45 间甲酚 2 086 46.01 59.65 38.76 25.14 49.29 — 1 648.79 216.83 —46 苯酚 2 001 210.33 267.14 280.28 95.20 388.20 949.66 6 170.86 732.18 79.54 47 邻苯二酚 2 661 — 4.80 — 2.16 754.95 — — — —48 2-乙基-6-甲基苯酚 2 161 — — — 0.68 — — — — —49 二氢丁香酚 2 108 6.36 8.04 7.00 1.07 — — 131.58 48.40 —50 4-乙基-2-甲氧基苯酚 2 028 59.87 61.10 17.78 10.39 — 57.75 817.32 295.12 —51 3-甲基苯邻二酚 2 623 — — 4.50 — — — — — —52 2,3-二甲苯酚 2 144 — 2.43 — — — — 136.33 — —53 2,6-二甲基苯酚 1 900 5.64 4.50 3.12 1.42 — — 435.82 129.30 —54 3-乙基苯酚 2 179 8.83 2.18 1.24 1.40 — — 373.79 — —55 4-烯丙基-2,6-二甲氧基苯酚 2 556 — 0.73 0.60 0.16 — 197.57 189.60 41.36 —56 鄰乙苯酚 2 169 4.34 — — — — — 359.97 81.40 —57 愈创木酚 1 858 429.74 452.28 186.77 79.98 355.76 573.03 4 049.56 862.27 —58 2,6-二甲氧基苯酚 2 264 16.81 167.59 82.14 33.77 573.59 552.70 2 368.71 371.21 —59 3-甲氧基儿茶酚 2 510 — 31.03 25.90 8.55 118.24 — — — —60 2-甲氧基-4-甲基苯酚 1 955 149.27 164.13 55.20 34.42 95.94 162.65 1 609.72 479.04 —61 邻甲酚 1 998 69.07 59.66 50.30 22.21 57.62 145.02 2 408.02 372.90 —62 3,4-二甲基苯酚 2 218 2.80 — 9.44 4.29 — — 182.88 — —
续表3
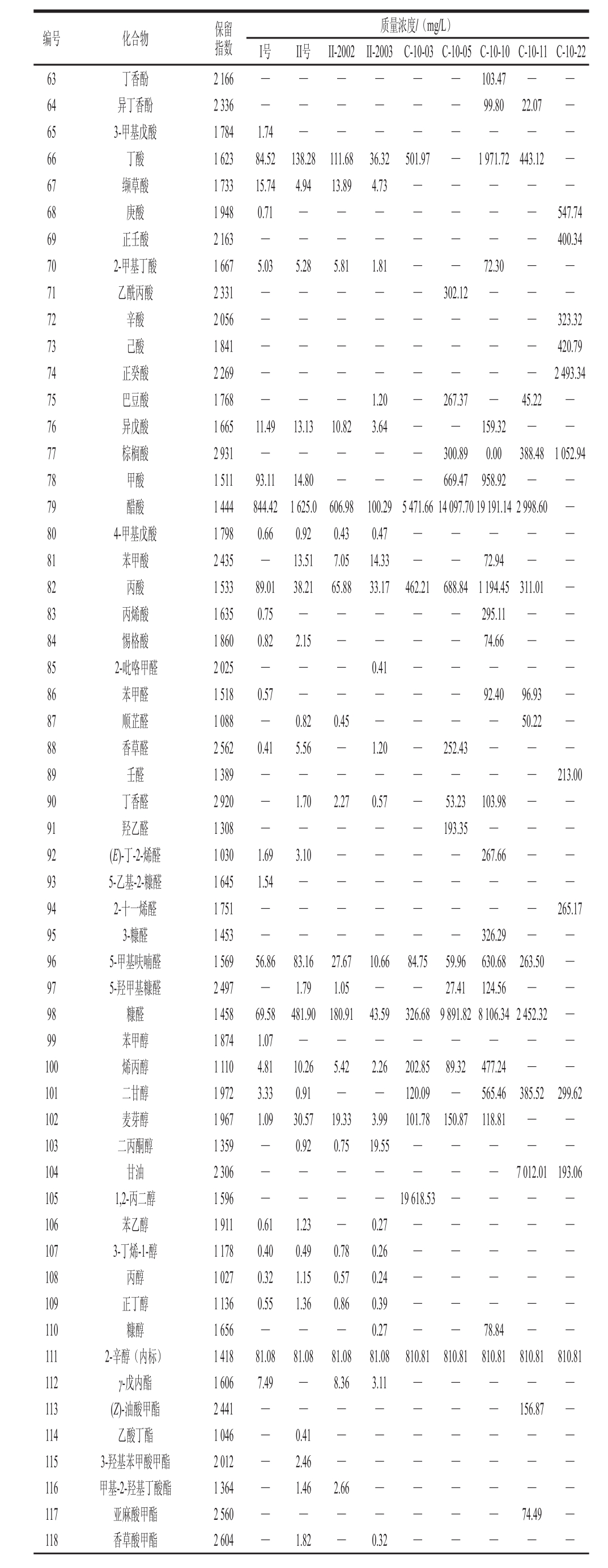
编号 化合物 保留指数质量浓度/(mg/L)I号 II号 II-2002 II-2003 C-10-03 C-10-05 C-10-10 C-10-11 C-10-22 63 丁香酚 2 166 — — — — — —103.47 — —64 异丁香酚 2 336 — — — — — — 99.80 22.07 —65 3-甲基戊酸 1 784 1.74 — — — — — — — —66 丁酸 1 623 84.52 138.28 111.68 36.32 501.97 — 1 971.72 443.12 —67 缬草酸 1 733 15.74 4.94 13.89 4.73 — — — — —68 庚酸 1 948 0.71 — — — — — — —547.74 69 正壬酸 2 163 — — — — — — — —400.34 70 2-甲基丁酸 1 667 5.03 5.28 5.81 1.81 — — 72.30 — —71 乙酰丙酸 2 331 — — — — — 302.12 — — —72 辛酸 2 056 — — — — — — — —323.32 73 己酸 1 841 — — — — — — — —420.79 74 正癸酸 2 269 — — — — — — — —2 493.34 75 巴豆酸 1 768 — — — 1.20 — 267.37 — 45.22 —76 异戊酸 1 665 11.49 13.13 10.82 3.64 — — 159.32 — —77 棕榈酸 2 931 — — — — —300.89 0.00 388.48 1 052.94 78 甲酸 1 511 93.11 14.80 — — —669.47 958.92 — —79 醋酸 1 444 844.42 1 625.0 606.98 100.29 5 471.66 14 097.70 19 191.14 2 998.60 —80 4-甲基戊酸 1 798 0.66 0.92 0.43 0.47 — — — — —81 苯甲酸 2 435 — 13.51 7.05 14.33 — — 72.94 — —82 丙酸 1 533 89.01 38.21 65.88 33.17 462.21 688.84 1 194.45 311.01 —83 丙烯酸 1 635 0.75 — — — — —295.11 — —84 惕格酸 1 860 0.82 2.15 — — — — 74.66 — —85 2-吡咯甲醛 2 025 — — — 0.41 — — — — —86 苯甲醛 1 518 0.57 — — — — — 92.40 96.93 —87 顺芷醛 1 088 — 0.82 0.45 — — — — 50.22 —88 香草醛 2 562 0.41 5.56 — 1.20 — 252.43 — — —89 壬醛 1 389 — — — — — — — —213.00 90 丁香醛 2 920 — 1.70 2.27 0.57 — 53.23 103.98 — —91 羟乙醛 1 308 — — — — —193.35 — — —92 (E)-丁-2-烯醛 1 030 1.69 3.10 — — — — 267.66 — —93 5-乙基-2-糠醛 1 645 1.54 — — — — — — — —94 2-十一烯醛 1 751 — — — — — — — — 265.17 95 3-糠醛 1 453 — — — — — —326.29 — —96 5-甲基呋喃醛 1 569 56.86 83.16 27.67 10.66 84.75 59.96 630.68 263.50 —97 5-羟甲基糠醛 2 497 — 1.79 1.05 — — 27.41 124.56 — —98 糠醛 1 458 69.58 481.90 180.91 43.59 326.68 9 891.82 8 106.34 2 452.32 —99 苯甲醇 1 874 1.07 — — — — — — — —100 烯丙醇 1 110 4.81 10.26 5.42 2.26 202.85 89.32 477.24 — —101 二甘醇 1 972 3.33 0.91 — — 120.09 — 565.46 385.52 299.62 102 麦芽醇 1 967 1.09 30.57 19.33 3.99 101.78 150.87 118.81 — —103 二丙酮醇 1 359 — 0.92 0.75 19.55 — — — — —104 甘油 2 306 — — — — — — —7 012.01 193.06 105 1,2-丙二醇 1 596 — — — — 19 618.53 — — — —106 苯乙醇 1 911 0.61 1.23 — 0.27 — — — — —107 3-丁烯-1-醇 1 178 0.40 0.49 0.78 0.26 — — — — —108 丙醇 1 027 0.32 1.15 0.57 0.24 — — — — —109 正丁醇 1 136 0.55 1.36 0.86 0.39 — — — — —110 糠醇 1 656 — — — 0.27 — —78.84 — —111 2-辛醇(内标) 1 418 81.08 81.08 81.08 81.08 810.81 810.81 810.81 810.81 810.81 112 γ-戊内酯 1 606 7.49 — 8.36 3.11 — — — — —113 (Z)-油酸甲酯 2 441 — — — — — — — 156.87 —114 乙酸丁酯 1 046 — 0.41 — — — — — — —115 3-羟基苯甲酸甲酯 2 012 — 2.46 — — — — — — —116 甲基-2-羟基丁酸酯 1 364 — 1.46 2.66 — — — — — —117 亚麻酸甲酯 2 560 — — — — — — — 74.49 —118 香草酸甲酯 2 604 — 1.82 — 0.32 — — — — —
续表3

注:—.未检出。
编号 化合物 保留指数质量浓度/(mg/L)I号 II号 II-2002 II-2003 C-10-03 C-10-05 C-10-10 C-10-11 C-10-22 119 戊内酯 1 783 — 1.05 — 0.31 — — — — —120 1,2-乙二醇单乙酸酯 1 629 — 1.18 — — — 1 525.31 — — —121 异戊酸甲酯 1 015 0.65 — — — — — — — —122 当归内酯 1 427 — — 1.38 — — 74.25 — — —123 乙酸烯丙酯 1 018 3.65 8.84 2.83 0.45 — — 191.71 222.59 —124 丙酮酸甲酯 1 217 — — 1.51 — — — — — —125 2-糠酸甲酯 1 569 27.01 87.84 17.49 13.85 — — — — —126 戊酸甲酯 1 082 0.98 1.75 1.01 0.47 — — — — —127 乙酰丙酸甲酯 1 560 — 4.90 12.89 1.26 — — — — —128 1,2-丙二醇-1-醋酸酯 1 579 — 112.59 — — — — — — —129 磷酸三乙酯 1 657 — 2.31 — — — — — — —130 2-甲基丁酸甲酯 1 005 — 0.37 0.18 0.09 — — — — —131 苯酸甲酯 1 619 19.87 3.22 — 1.16 — — — — —132 γ-丁内酯 1 625 48.44 29.05 32.85 10.62 704.50 930.79 — — —133 2-乙酰基呋喃 1 499 45.79 77.56 61.17 18.98 280.00 458.07 — 320.79 —134 5-甲基-2-乙酰基呋喃 1 611 — 12.29 5.49 2.21 — — — — —135 2-乙基吡啶 1 282 — — — 0.24 — — — — —136 2-甲基吡啶 1 216 — — 0.32 0.48 — — — — —137 吡啶 1 179 — — —2.21 — — — — —138 3-乙基吡啶 1 382 — — — 0.22 — — — — —139 2-乙酰基吡咯 1 970 — 2.64 — — — — — — —140 2-甲基吡嗪 1 261 2.00 — 1.57 1.22 — — — — —141 2-乙基吡嗪 1 331 0.89 — 0.42 0.38 — — — — —142 2-乙基-6-甲基吡嗪 1 384 — — — 0.39 — — — — —143 吡嗪 1 206 2.06 3.52 2.78 1.88 — — — — —144 甲基糠基醚 1 251 — 0.46 — — — — — — —145 邻苯二甲醚 1 719 1.62 — — 0.75 — — — — —146 N-甲基丁二酰胺 1 906 — 4.30 — 1.52 — — — — —147 N,N-二甲基乙酰胺 1 410 — — — 17.27 — — — — —148 2,4,5-三甲基恶唑 1 194 — — — 0.30 — — — — —149 2,3-二甲基马来酸酐 1 725 1.94 4.19 — — — — — — —150 3-(2-甲基丙基)-1-环己烯 1 628 — — — — — — — — 129.38 151 1-十四烯 1 444 — — — — — — — — 187.00 152 苯甲腈 1 593 2.58 — — — — — — — —153 丙腈 1 020 0.72 3.70 2.05 1.52 — — — — —154 丁腈 1 091 — 2.30 1.27 0.87 — — — — —155 3,4-二羟基甲苯 2 748 — 2.57 0.91 3.76 — 321.06 — — —156 3,4-二甲氧基甲苯 1 805 1.35 — 0.37 0.21 — — — — —
酚类化合物是烟熏肉制品典型的特征风味物质,是重要的调味和芳香化合物,同时也被认为具有抗氧化和抗菌活性[18]。食品熏制过程中所吸附的酚类化合物,是造成烟熏产品独特香气主要原因[19]。它们可以由木质素热降解产生,也可以通过纤维素和半纤维素的热降解得到[20]。有研究表明,酚类阈值较低,对烟熏干腌火腿的风味影响较大[21]。从表3可以看出,含量较高的苯酚(79.54~6 170.86 mg/L),愈创木酚(79.98~4 049.56 mg/L)、2,6-二甲氧基苯酚(16.81~2 368.71 mg/L)、邻甲酚(22.21~2 408.02 mg/L)、对甲酚(1 7.2 7~2 4 2 4.5 6 m g/L)、间甲酚(25.14~1 648.79 mg/L)等存在于多种烟熏液中(C-10-22烟熏液除外),这与Montazeri等[22]研究结果相似,它们是典型的烟熏液风味化合物。还有研究报道,愈创木酚及其衍生物的总含量与苯酚、甲酚和二甲苯酚的总含量的相对比率可能对木烟中的香气产生相当大的影响,而对甲酚、邻甲酚是典型烟熏液风味的重要贡献者[23]。Kostyra等[24]研究发现,2,6-二甲氧基苯酚及其衍生物通常与新鲜烟熏食品中检测到的异味没有太大关联。值得注意的是烟熏液C-10-22,其酚类物质仅检测到苯酚,其质量浓度为79.54 mg/L,均低于其余8 种烟熏液中的苯酚化合物含量。而丁香酚仅存在于C-10-10中,质量浓度为103.47 mg/L。从图3可知,酚类化合物含量由高到低为C-10-05>C-10-10>C-10-11>II号>C-10-22>C-10-03>II-2002>I号>II-2003,其中C-10-05总含量高出II-2003约187 倍。总体上看,红箭烟熏液中酚类化合物含量,明显优于山楂核烟熏液。
羰基化合物有助于形成木材烟雾的整体感官特性,它们是通过纤维素和半纤维素的热分解和重新排列而成[25]。含羰基的化合物散发出焦甜的香气,可软化与酚类化合物相关的浓烟熏味,并带有典型的烟熏香气和风味[26]。如1-羟基-2-丁酮的形成发生在木材半纤维素的低温热解过程中[27],其香气感带有甜味、类似咖啡和谷物的气味[28];2-环戊烯酮及其衍生物通常存在于木材或烟雾中,其感官特征为难闻苦味,带有草味,对烟味有影响[29]。羰基化合物是醛、酮、羧酸类化合物的合称,其中醛酮类化合物被认为在结构、颜色和香气的发育过程中具有重要的影响,在质地和颜色的形成中所起的作用与食物蛋白质的胺类反应有关,类似于美拉德反应[30],如具有脂肪香味的糠醛可作为美拉德反应的特征产物,其具有苦杏仁气味[31]。从表3可以看出,在测定的烟熏液样品中(C-10-22除外),酮类化合物的数量较丰富,质量浓度较高的有羟基丙酮(49.02~18 971.58 mg/L)、2,3-二甲基-2-环戊烯酮(15.67~444.39 mg/L)、甲基环戊烯醇酮(26.42~459.99 mg/L)、1-羟基-2-丁酮(14.33~1 542.40 mg/L)、2-环戊烯酮(13.91~613.80 mg/L);而醛类化合物中,5-甲基呋喃醛(10.66~630.68 mg/L)、糠醛(43.59~9 891.82 mg/L)质量浓度较高;在其含量相对较低的风味化合物中,苯基丙酮、环己酮仅在I号和II号烟熏液中检测到,3-糠醛仅存在于C-10-10中,质量浓度为326.29 mg/L。而对于C-10-22烟熏液,酮类化合物仅检测到2-十一酮,质量浓度为130.88 mg/L,醛类化合物检测到壬醛(213.0 mg/L)和2-十一烯醛(265.17 mg/L)。从图3可知,醛酮类化合物总含量由高到低为C-10-05>C-10-10>C-10-03>C-10-11>II号>II-2002>I号>C-10-22>II-2003,其中C-10-05总含量高出II-2003约83 倍。总体上看,红箭烟熏液中醛酮类化合物总含量,明显优于山楂核烟熏液。
有机酸是木质纤维素和半纤维素的部分热解产物[32]。在熏制过程中,一系列有机酸可能会沉积在产品表面,因其对食品的风味(酸味)、颜色、质地和微生物的影响而闻名[33]。对于烟熏液来说,酸类主要是作为防腐剂和pH值控制剂存在,因为其挥发性较小,呈香性相对较差且对香气的贡献较低,但其含量的高低也可在一定程度上影响食品的保存。从表3可以看出,在测定的烟熏液样品中,质量浓度较高的有丁酸(36.32~1 971.72 mg/L)、醋酸(1 0 0.2 9~1 9 1 9 1.1 4 m g/L)和丙酸(33.17~1 194.45 mg/L)等。而庚酸(547.74 mg/L)、正壬酸(400.34 mg/L)、辛酸(323.32 mg/L)、己酸(420.79 mg/L)、正癸酸(2 493.34 mg/L)这几种酸类化合物质量浓度较高仅存于烟熏液C-10-22中,且均为强香气载体。而醋酸和丙酸的气味带刺激性,均可引起烟熏液整体气味的变化。从图3可以看出,酸类化合物总含量由高到低为C-10-10>C-10-05>C-10-03>C-10-22>C-10-11>II号>I号>II-2002>II-2003。
烟熏食品的感官属性与熏制过程中酚类、醛类、和酮类有关。除此之外,还有很多次要成分也有着至关重要的作用,如醇类化合物对肉制品风味的影响不如醛类化合物显著,但对整体气味有协同作用;酯类化合物主要赋予食品果味和甜味[34]。它们是广泛使用的香料,常作为主香剂和辅助剂使用,但由于两者在烟熏液中的含量较低,阈值高且容易挥发,因此在一定程度上是作为烟熏液中重要的风味调和物的存在。由表3可以看出,红箭烟熏液C-10-03中含1,2-丙二醇质量浓度较高(19 618.53 mg/L),在其他8 种烟熏液中没有检测出该化合物;同样地,1,2-乙二醇单乙酸酯(1 525.31 mg/L)大量存在于C-10-05中;对于油溶性烟熏液C-10-11和C-10-22,测定出质量浓度较高的甘油,分别为7 012.01 mg/L和193.06 mg/L,且在其他几种烟熏液中未检测出;另外,在山楂核烟熏液中检测出吡啶、吡嗪、吡咯及其衍生物,它们均属于杂环含氮化合物,主要是由于木材含有氮源,其中吡嗪类化合物主要提供烤香、坚果香等风味,可对肉制品的烟熏风味起修饰作用[35],5 种红箭烟熏液中均未检测该类化合物的存在,由于烟熏液中的化合物成分很大程度上取决于烟熏原料的成分以及其制备工艺,因此推测烟熏液在熏材选择和制备工艺上存在差异。还有其他类化合物,它们相互补充共同组成了整个烟熏液风味的轮廓,在烟熏液中扮演着不可或缺的角色。
为了可视化4 种山楂核烟熏液风味物质的组成,根据表3的测定结果进行维恩图分析,如图4所示。4 种山楂核烟熏液样品成分中共检测到88 种风味物质,其中52 种为共有化合物,主要包含酮类20 种以及酚类11 种,酸类7 种,醛类2 种,醇类5 种,酯类5 种其他类2 种化合物。在I号、II号、II-2002、II-2003中分别鉴定出11、8、4 种和13 种不同的风味化合物,II-2003烟熏液中异于其他3 种烟熏液的化合物最多,推测这些化合物的分布差异可能与烟熏液的形成过程有关。

图3 不同类型烟熏液各种类化合物含量
Fig. 3 Contents of different classes of flavor components in liquid smokes

图4 4 种烟熏液不同化合物维恩图
Fig. 4 Venn diagram showing unique and shared flavor compounds in four hawthorn kernel liquid smokes
2.4 烟熏液风味物质PCA
表4 主成分的特征值及其方差贡献率
Table 4 Eigenvalues, contributions and cumulative contributions to total variance of principal components

主成分 初始特征值特征值 方差贡献率/% 累计方差贡献率/%1 5.097 63.712 63.712 2 1.452 18.156 81.868 3 0.995 12.443 94.311
主成分的数目可以根据相关系数矩阵的特征值判定[36],对9 种烟熏液中的风味物质种类进行PCA。从表4可以看出,前3 个主成分包含了94.311%的信息。因此取前3 个主成分能够很好地说明9 种烟熏液风味物质的变化趋势。各主成分在各因子变量上的载荷值代表该主成分对该因子所能反映的程度[37]。
表5 9 种烟熏液风味物质主成分特征向量及其载荷矩阵
Table 5 Principal component eigenvectors and loading matrix

化合物种类PC1 PC2 PC3特征向量 载荷值 特征向量 载荷值 特征向量 载荷值酮类 0.42 0.949 0.096 0.116 0.067 0.067酚类 0.409 0.924 -0.296 -0.357 -0.093 -0.093酸类 0.377 0.852 -0.243 -0.293 -0.422 -0.421醛类 0.409 0.924 -0.296 -0.357 -0.093 -0.093醇类 0.048 0.108 0.728 0.877 -0.38 -0.379酯类 0.37 0.836 0.144 0.174 0.497 0.496含氮类 -0.322 -0.727 0.323 -0.389 0.382 0.381其他 0.32 0.722 0.318 0.383 0.513 0.512
如表5所示,酮类、酚类、醛类与PC1高度正相关;PC2中载荷值最高的正相关风味物质为醇类化合物;PC3中载荷值影响最高的为其他类化合物,上述结果说明酮类、酚类、醛类、醇类和酯类化合物为这9 种烟熏液中含量发生显著变化的风味物质。
2.5 烟熏液样品中风味物质品质评价模型的建立
将得到的特征向量与标准化后的数据相乘得出9 种红箭烟熏液化合物主成分的线性关系式如下:

其中X1~X8为原始变量标准化后的值,Z1、Z2、Z3表示3 个主成分的得分值,得分值相对越大,品质越好。
表6 标准化后主成分综合得分
Table 6 Synthetic scores of principal components after standardization

烟熏液 Z1 Z2 Z3 Z 排名I号 -1.693 -0.414 0.248 -1.123 8 II号 -1.562 -0.525 0.542 -1.023 6 II-2002 -1.693 -0.411 0.297 -1.116 7 II-2003 -2.034 -0.616 0.485 -1.347 9 C-10-03 0.395 2.599 -0.848 0.618 3 C-10-05 4.758 -0.138 1.587 3.204 1 C-10-10 2.259 -1.707 -2.001 0.88 2 C-10-11 0.24 0.921 -0.169 0.299 4 C-10-22 -0.67 0.29 -0.142 -0.392 5
根据特征向量与标准化后的数据相乘求和,再与对应的3 个主成分方差贡献率做内积,得到综合风味品质的评价函数Z,其表达式Z=0.637 12Z1+0.181 56Z2+0.124 43Z3。从表6可以看出,PC1得分最高的是C-10-05烟熏液,其次是C-10-10烟熏液,这2 种烟熏液主要是受PC1的影响,结合表5可知,酮类、酚类以及醛类物质对这2 种烟熏液的影响较高,因此它们可能共同决定了这2 种烟熏液的风味特征。PC2得分最高的是C-10-03烟熏液,因此醇类化合物可能决定了该烟熏液的风味特征;PC3得分最高的是C-10-05烟熏液,受到其他类化合物的影响。在风味品质综合排名中可以更加直观地看出,9 种不同类型烟熏液中风味物质强度综合得分从高到低顺序依次为C-10-05、C-10-10、C-10-03、C-10-11、C-10-22、II号、II-2002、I号、II-2003烟熏液,从该模型排序得出5 种红箭牌烟熏液的风味优于4 种山楂核烟熏液的风味。
3 结 论
采用电子鼻技术发现4 种山楂核烟熏液在风味上有一定的相似性,这与维恩图分析的结果相映证;而5 种红箭烟熏液的风味存在差异,推测是烟熏液提取方法的不同而引起其中某些化合物的变化。电子舌结合PCA发现7 种类型烟熏液(油溶性烟熏液除外)的滋味品质整体结构存在差异,C-10-03和C-10-10主要受咸味影响,剩余5 种烟熏液主要是受咸味、苦味和涩味及丰富度的影响,其中I号烟熏液同时受到酸味的影响。GC-MS结果共检测出156 种风味物质,仅苯酚为共有风味物质,说明烟熏液在风味组成上存在较大差异,其中酮类、酚类、醛类、酸类化合物在含量上具有较大优势,如羟基丙酮、2,3-二甲基-2-环戊烯酮、甲基环戊烯醇酮、1-羟基-2-丁酮、2-环戊烯酮、5-甲基呋喃醛、糠醛、苯酚、愈创木酚、2,6-二甲氧基苯酚、邻甲酚、对甲酚、间甲酚、丁酸、醋酸和丙酸等含量较高且存在于多种烟熏液中(C-10-22烟熏液除外);值得注意的是含氮类化合物如吡嗪、吡咯、吡啶等化合物及其衍生物在红箭烟熏液中未检测出,推测是由于熏材原料不同而导致的差异;还有质量浓度较高的1,2-丙二醇、1,2-乙二醇单乙酸酯分别存在于C-10-03、C-10-05中,对于油溶性烟熏液C-10-11和C-10-22,测定出质量浓度较大的甘油,且在其他几种烟熏液中未检测出,推测是提取过程的添加物。最后从烟熏液风味物质品质综合评价模型可知,山楂核烟熏液的风味物质相较于红箭烟熏液弱。
综上所述,电子鼻可以从香气上感知不同类型烟熏液的差异,而GC-MS结果可在一定程度上解释该差异来源,电子舌则作为滋味补充,三者从整体上相互映证、相互补充,为分析不同类型烟熏液提供了理论依据和技术参考。
[1] 赵冰, 任琳, 陈文华, 等. 烟熏工艺对熏肉挥发性风味物质的影响[J].食品科学, 2013, 34(6): 180-187. DOI:10.7506/spkx1002-6630-201306040.
[2] VITT S M, HIMELBLOOM B H, CRAPO C A. Inhibition of Listeria innocua and L. monocytogenes in a laboratory medium and cold-smoked salmon containing liquid smoke[J]. Journal of Food Safety, 2001,21(2): 111-125. DOI:10.1111/j.1745-4565.2001.tb00311.x.
[3] 姜绍通, 王旗, 蔡克周, 等. 顶空固相微萃取-气质联用法测定山楂核烟熏液的挥发性风味物质[J]. 食品科学, 2013, 34(18): 206-211.DOI:10.7506/spkx1002-6630-201318042.
[4] 吴靖娜, 路海霞, 蔡水淋, 等. 基于电子鼻和SPME-GC-MS评价烟熏液对熏鲍挥发性风味物质的影响[J]. 现代食品科技, 2016, 32(7):220-230. DOI:10.13982/j.mfst.1673-9078.2016.7.034.
[5] GUILLEN M D, MANZANOS M J, ZABALA L. Study of a commercial liquid smoke flavoring by means of gas chromatography/mass spectrometry and Fourier transform infrared spectroscopy[J].Journal of Agricultural and Food Chemistry, 1995, 43(2): 463-468.DOI:10.1021/jf00050a039.
[6] GIRI A, ZELINKOVA Z, WENZL T. Experimental design-based isotope-dilution SPME-GC/MS method development for the analysis of smoke flavouring products[J]. Food Additives & Contaminants: Part A,2017, 34(12): 2069-2084. DOI:10.1080/19440049.2017.1374564.
[7] 高宁宁, 胡萍, 朱秋劲, 等. 烟熏液及其在肉制品中的应用研究进展[J].肉类研究, 2019, 33(1): 66-70. DOI:10.7506/rlyj1001-8123-20181112-214.
[8] LINGBECK J M, CORDERO P, O'BRYAN C A, et al.Functionality of liquid smoke as an all-natural antimicrobial in food preservation[J]. Meat Science, 2014, 97(2): 197-206. DOI:10.1016/j.meatsci.2014.02.003.
[9] GUILLEN M D, MANZANOS M J, IBARGOITIA M L. Carbohydrate and nitrogenated compounds in liquid smoke flavorings[J]. Journal of Agricultural and Food Chemistry, 2001, 49(5): 2395-2403.DOI:10.1021/jf000760t.
[10] 邝格灵, 王新宇, 李树, 等. 基于电子鼻与气相色谱-质谱联用区分不同陈酿期恒顺香醋风味物质的差异性[J]. 食品科学, 2020, 41(12):228-233. DOI:10.7506/spkx1002-6630-20190508-071.
[11] SHI H, ZHANG M, ADHIKARI B. Advances of electronic nose and its application in fresh foods: a review[J]. Critical Reviews in Food Science and Nutrition, 2018, 58(16): 2700-2710. DOI:10.1080/104083 98.2017.1327419.
[12] 牛海霞. 电子舌在现代食品科学技术中的应用[J]. 食品科技, 2007,32(8): 26-30. DOI:10.3969/j.issn.1005-9989.2007.08.008.
[13] 王琼, 徐宝才, 于海, 等. 电子鼻和电子舌结合模糊数学感官评价优化培根烟熏工艺[J]. 中国农业科学, 2017, 50(1): 161-170.DOI:10.3864/j.issn.0578-1752.2017.01.014.
[14] 李琦, 李春艳, 徐畅, 等. 低温冷冻液液萃取/GC-MS结合保留指数分析香蕉中的挥发性成分[J]. 分析测试学报, 2017, 36(4): 457-463.DOI:10.3969/j.issn.1004-4957.2017.04.003.
[15] 吕玉, 臧明伍, 史智佳, 等. 气相色谱-嗅闻-质谱联用分析烟熏液中的挥发性风味物质[J]. 肉类研究, 2012, 26(12): 5-7. DOI:10.7506/spkx1002-6630-201318042.
[16] 孟军, 张建才, 邹静, 等. 不同品种樱桃利口酒香气成分分析[J].酿酒科技, 2018(3): 93-97. DOI:10.13746/j.njkj.2017301.
[17] 何余勤, 胡荣锁, 张海德, 等. 基于电子鼻技术检测不同焙烤程度咖啡的特征性香气[J]. 农业工程学报, 2015, 31(18): 247-255.DOI:10.11975/j.issn.1002-6819.2015.18.034.
[18] FAISAL M, GANI A. The effectiveness of liquid smoke produced from palm kernel shells pyrolysis as a natural preservative in fish balls[J]. International Journal, 2018, 15(47): 145-150.DOI:10.21660/2018.47.06109.
[19] SOARES J M, SILVA P F, PUTON B M S, et al. Antimicrobial and antioxidant activity of liquid smoke and its potential application to bacon[J]. Innovative Food Science & Emerging Technologies, 2016,38: 189-197. DOI:10.1016/j.ifset.2016.10.007.
[20] ŠIMKO P. Factors affecting elimination of polycyclic aromatic hydrocarbons from smoked meat foods and liquid smoke flavorings[J].Molecular Nutrition & Food Research, 2005, 49(7): 637-647.DOI:10.1002/mnfr.200400091.
[21] RADOVCIC N M, VIDACEK S, JANCI T, et al. Characterization of volatile compounds, physico-chemical and sensory characteristics of smoked dry-cured ham[J]. Journal of Food Science and Technology,2016, 53(11): 4093-4105. DOI:10.1007/sl13197-016-248-2.
[22] MONTAZERI N, OLIVEIRA A C M, HIMELBLOOM B H, et al.Chemical characterization of commercial liquid smoke products[J].Food Science & Nutrition, 2013, 1(1): 102-115. DOI:10.1002/fsn3.9.
[23] FUJIMAKI M, KIM K, KURATA T. Analysis and comparison of flavor constituents in aqueous smoke condensates from various woods[J]. Agricultural and Biological Chemistry, 1974, 38(1): 45-52.DOI:10.1271/bbb1961.38.45.
[24] KOSTYRA E, BARYLKO-PIKIELNA N. Volatiles composition and flavour profile identity of smoke flavourings[J]. Food Quality and Preference, 2006, 17(1/2): 85-95. DOI:10.1016/j.foodqual.2005.06.008.
[25] PINO J A. Characterisation of volatile compounds in a smoke flavouring from rice husk[J]. Food Chemistry, 2014, 153: 81-86.DOI:10.1016/ j.foodchem.2013.12.041.
[26] YE N, XIAO Z, LIU Q, et al. Determination of furfural in tobacco smoke based on GC/MS combined with selected ion scan[J].Science and Technology of Food Industry, 2012, 33(9): 366-368.DOI:10.13386/j.issn1002-0306.2012.09.021.
[27] WU Y, ZHAO Z, LI H, et al. Low temperature pyrolysis characteristics of major components of biomass[J]. Journal of Fuel Chemistry and Technology, 2009, 37(4): 427-432. DOI:10.1016/s1872-5813(10)60002-3.
[28] KASELEHT K, LEITNER E, PAALME T. Determining aromaactive compounds in Kama flour using SPME-GC/MS and GC-olfactometry[J]. Flavour and Fragrance Journal, 2011, 26(2): 122-128.DOI:10.1002/ffj.2032.
[29] KIM K, KURATA T, FUJIMAKI M. Identification of flavor constituents in carbonyl, non-carbonyl neutral and basic fractions of aqueous smoke condensates[J]. Agricultural and Biological Chemistry,1974, 38(1): 53-63. DOI:10.1271/bbb1961.38.53.
[30] VARLET V, PROST C, SEROT T. Volatile aldehydes in smoked fish:analysis methods, occurence and mechanisms of formation[J]. Food Chemistry, 2007, 105(4): 1536-1556. DOI:10.1271/bbb1961.38.53.
[31] 鲍杰, 李莹灿, 刘雅冉, 等. 笃斯越橘果酱特征香气成分分析[J].食品与发酵工业, 2017, 43(6): 255-262. DOI:10.13995/j.cnki.11-1802/ts.201706044.
[32] GILBERT J, KNOWLES M E. The chemistry of smoked foods: a review[J]. International Journal of Food Science & Technology, 1975,10(3): 245-261. DOI:10. 1111/j.1365-2621.1975.tb00028.x.
[33] SALDANA E, SALDARRIAGA L, CABRERA J, et al. Relationship between volatile compounds and consumer-based sensory characteristics of bacon smoked with different Brazilian woods[J].Food Research International, 2019, 119: 839-849. DOI:10.1016/j.foodres.2018.10.067.
[34] 马建荣, 潘腾, 王振宇, 等. 传统炭烤羊腿特征挥发性风味物质分析[J]. 肉类研究, 2019, 33(1): 50-54. DOI:10.7506/rlyj1001-8123-20181211-228.
[35] 刘登勇, 王逍, 吴金城, 等. 肉制品烟熏风味物质研究进展[J]. 肉类研究, 2018, 32(10): 53-60. DOI:10.7506/rlyj1001-8123-201810010.
[36] 刘秀明, 李源栋, 王家俊, 等. 基于UPLC-PDA技术的主成分分析在香精质量稳定性评价中的应用[J]. 中国食品添加剂, 2015(6): 145-149. DOI:10.3969/j.issn.1006-2513.2015.06.017.
[37] 沈静, 杜若曦, 魏婷, 等. 干制方式对鲜食枣脆片香气品质的影响[J].食品科学, 2017, 38(18): 131-137. DOI:10.7506/spkx1002-6630-201718021.