刘俊山,李清华,朱丹实,王 勃,何余堂,马 涛,刘 贺 *
(渤海大学化学化工与食品安全学院,食品科学研究院,辽宁省食品安全重点实验室,辽宁省食品贮藏加工及质量安全控制工程技术研究中心,辽宁 锦州 121013)
摘 要:主要考察葡萄糖、果糖、山梨醇等单糖、柠檬酸与钾离子对大豆种皮多糖凝胶的透明度、持水性及凝胶强度的影响。通过Design-Expert软件的分析结果表明:大豆种皮多糖质量浓度对凝胶的持水能力、透明度以及凝胶强度均产生显著影响;柠檬酸对凝胶透明度的影响显著;葡萄糖质量浓度对持水性和凝胶强度影响显著,对透明度的作用不显著;果糖的添加对透明度有改善作用;山梨醇的添加促使大豆多糖的凝胶强度与持水能力较好,但凝胶透明度较差,大豆种皮多糖质量浓度为3.00 g/100 mL,钾离子浓度为0.20 mol/L和柠檬酸质量浓度为0.75 g/100 mL时,山梨醇质量浓度为2.50 g/100 mL条件下的凝胶持水力、强度均达到最大,分别为98%、37.74 g。
关键词:大豆多糖;葡萄糖;果糖;山梨醇;持水性;透明度;凝胶强度
果胶因其凝胶特性在食品、医药、纺织、化妆品工业及其他领域中都有广泛的应用 [1-3]。周艳红 [4]、郑建仙 [5]、孙元琳 [6]、刘贺 [7-10]和Gnanasambandam [11]等对大豆种皮多糖尤其是对大豆种皮的提取和性质进行了相关考察,对凝胶性质也做了初步分析。国外学者研究了单价阳离子Na +与K +对果胶凝胶性质的影响,结果表明添加K +的凝胶强度要好于Na +的凝胶强度 [12-13]。近几年国内外对食用胶的复配也倍加关注 [2,14-15],但主要集中于蔗糖与其他食用胶之间的复配 [16-17],对大豆多糖与果糖、葡萄糖及山梨醇单糖物质的复配效果却鲜有报道。本实验主要研究酸及单糖复合钾离子对大豆种皮多糖持水能力、透明度及凝胶强度特性的影响,为开发这种新型的复合胶、拓宽大豆种皮多糖的应用领域提供有益的参考,从而为工业化应用大豆种皮多糖提供有力的支持。
1.1 材料与试剂
大豆皮,采购自锦州大豆皮经销公司。
葡萄糖(分析纯) 天津市天力化学试剂有限公司;D-果糖(分析纯) 天津市化学试剂厂;山梨醇(分析纯) 连云港罗盖特精细化工有限公司;99%乙醇、草酸铵(分析纯) 天津市致远化学试剂有限公司;KCl(分析纯) 天津市大茂化学试剂厂;柠檬酸(分析纯) 天津市风船化学试剂科技有限公司。
1.2 仪器与设备
RRH-100万能高速粉碎机 欧凯莱英(香港)公司;JJ-1精密增力电动搅拌器 金坛市鑫鑫实验仪器厂;电热恒温鼓风干燥箱 上海一恒科技有限公司;L-535R离心机 上海五久自动化设备有限公司;RE-3000旋转蒸发仪 上海亚荣生化仪器厂;PHS-3CW pH计 上海般特有限公司;HHS-2S电子恒温不锈钢水浴锅 上海市南阳仪器有限公司;SZ-1快速混匀器江苏金坛江南仪器厂;SH-3双显恒温加热磁力搅拌器北京金紫光科技发展有限公司;循环水式多用真空泵郑州长城科工贸有限公司;RS-232精密电子天平 上海舜宇恒平科学仪器有限公司;AR224CN电子天平 奥豪斯仪器(上海)有限公司;TA-XTPluS质构仪 北京超技仪器有限公司。
1.3 方法
1.3.1 大豆多糖的制备
参考刘贺等 [18]的大豆种皮果胶类凝胶多糖的制备方法。
1.3.2 大豆多糖溶液的制备
分别配制质量分数为4%的大豆多糖储备液、1.20 mol/L的氯化钾储备液、质量分数为12%的柠檬酸储备液,根据具体实验条件在使用前稀释。分别向稀释好的大豆多糖溶液中加入氯化钾使其浓度达到0.2 mol/L、柠檬酸以及不同的单糖溶液(葡萄糖、果糖、山梨醇),在高温下充分混匀。
1.3.3 大豆多糖凝胶持水能力测定 [7]
将制备的凝胶溶液1.00 mL左右加入到2.00 mL塑料离心管中,待其凝胶后,于4 000 r/min离心30 min,吸去上层水,测量质量差,持水力(water holding capacity,WHC)计算公式如下。
式中:m 0为空离心管质量/g;m 1为离心前装有凝胶的离心管质量/g;m 2为吸去水分后离心管质量/g。
1.3.4 大豆多糖凝胶透明度实验
将制备的凝胶溶液取2.00 mL加入到比色皿中,待其静置一夜后,用721分光光度计进行测试,透明度以490 nm波长处吸光度表示。
1.3.5 大豆多糖凝胶强度实验
将不同浓度的大豆多糖凝胶溶液倒入10.00 mL烧杯中冷却,室温放置观察大豆多糖凝胶情况。质构仪参数:选择P/0.5探头,设置触发力为5.00 g,探头下降速率为1.50 mm/s,下压距离为10.00 mm。
1.4 数据处理
利用Design-Expert 8.0软件(试用版)对实验数据进行方差分析。
2.1 柠檬酸与葡萄糖及复合钾离子对大豆多糖凝胶性质的影响
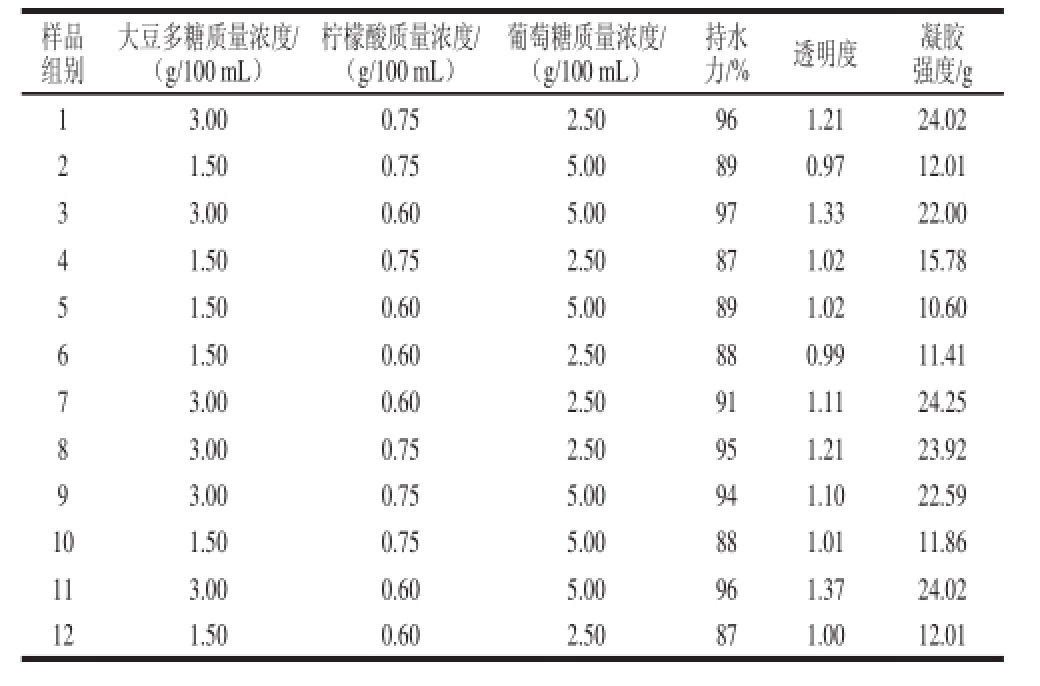
表1 柠檬酸与葡萄糖对大豆多糖凝胶性质的配制组别及结果
Table 1 Effect of citric acid combined with glucose at different concentrations on properties of soybean pectin gel
样品组别力/%透明度凝胶强度/g 1 3.000.752.50961.2124.02 2 1.500.755.00890.9712.01 3 3.000.605.00971.3322.00 4 1.500.752.50871.0215.7 8 5 1.500.605.00891.0210.60 6 1.500.602.50880.9911.41 7 3.000.602.50911.1124.25 8 3.000.752.50951.2123.92 9 3.000.755.00941.1022.59 101.500.755.00881.0111.86 113.000.60 5.00961.3724.02 121.500.602.50871.0012.01大豆多糖质量浓度/(g/10 0 mL)柠檬酸质量浓度/(g/100 mL)葡萄糖质量浓度/(g/100 mL)持水
表2 方差分析及参数估计表Table 2 Analysis of variance for combinations of citric acid with glucose
Table 2 Analysis of var
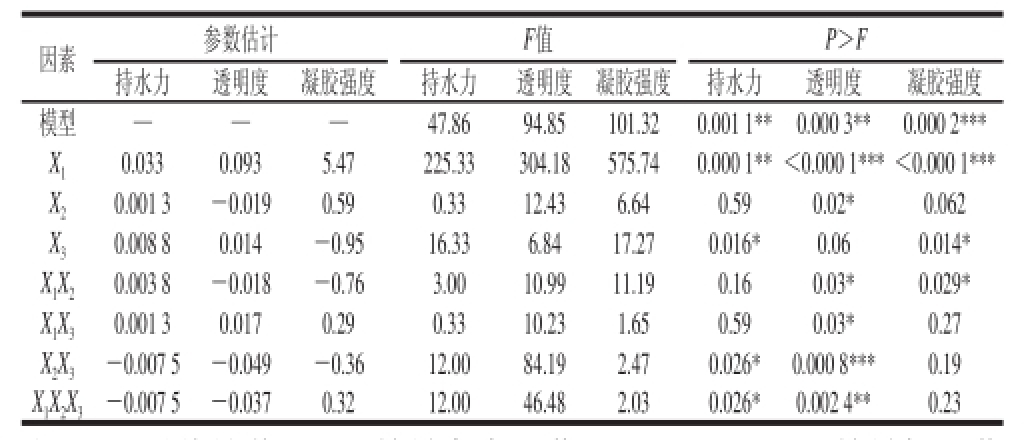
注:—. 无估计值。***. 差异高度显著(P<0.001);**. 差异极显著(P<0.01);*. 差异显著(P<0.05)。下同。X 1为大豆多糖质量浓度;X 2为柠檬酸质量浓度;X 3为葡萄糖质量浓度。
因素参数估计F值P >F持水力透明度凝胶强度持水力透明度凝胶强度持水力透明度凝胶强度模型——47.8694.85101.320.001 1**0.000 3**0.000 2*** X 10.0 330.0935.47225.33304.18575.740.000 1**<0.000 1***<0.000 1*** X 20.001 3-0.0190.590.3312.436. 640.590.02*0.062 X 30.008 80.014-0.9516.336.8417.270.016*0.060.014* X 1X 20.003 8-0.018-0.763.0010.9911.190.160.03*0.029* X 1X 30.001 30.0170.290.3310.231.650.59 0.03*0.27 X 2X 3-0.007 5-0.049-0.3612.0084.192.470.026*0.000 8***0.19 X 1X 2X 3-0.007 5-0.0370.3212.0046.482.030.026*0.002 4**0.23
多糖凝胶的持水力是指凝胶体系网状结构束缚水分能力的特性,持水力会影响产品的质构特性和加工损失 [19]。食品的质构特性同样对消费者的感官接受性有较大影响,本实验研究了添加不同物质对所形成凝胶力学性质的影响,主要考察凝胶强度。由表1可知,当大豆多糖质量浓度为3.00 g/100 mL,柠檬酸质量浓度为0.75 g/100 mL,葡萄糖质量浓度为2.50 g/100 mL时,持水力与凝胶强度值都偏高,但同时透明度也偏高。由表2可知,模型持水力、透明度与凝胶强度的F值分别为47.86、94.85、101.32>F 0.05,表明实验初始阶段的方案设计是具备可行性的。大豆多糖质量浓度与持水性、透明度与凝胶强度均呈高度显著正相关(P<0.001),可能是因为当大豆多糖质量浓度逐渐增加时,体系中的多糖分子逐渐增多,网状结构在增加,对束缚水分子的能力在增强,此时主要是靠氢键与疏水相互作用产生的凝胶体系。澄清度是影响感官评定的一个非常重要的指标 [7]。柠檬酸质量浓度只对凝胶透明度有显著影响(P<0.05),其原因可能在于,柠檬酸在体系中只是起到了辅助性的作用,如降低pH值和提供溶液中的氢键,当柠檬酸增加时,增加的氢键数目不足以影响持水性和凝胶强度。葡萄糖质量浓度对持水性和凝胶强度影响显著(P<0.05),而对透明度的影响作用不显著。原因可能是由于葡萄糖、果糖与山梨醇具有多羟基的结构对水分子产生了很好的吸附力,从而增强了凝胶的持水能力。考察两两因素相互作用时发现,柠檬酸与葡萄糖的结合对增强体系的凝胶效果有一定提升,尤其是对透明度方面起到了高度显著的影响(P<0.001)。
2.2 柠檬酸与果糖及复合钾离子对大豆多糖凝胶性质的影响
表3 柠檬酸与果糖对大豆多糖凝胶性质的配制组别及结果
Table 3 Effect of citric acid combined with fructose at different concentrations on properties of soybean pectin gel

样品组别力/%透明度凝胶强度/g 13.000.752.50961.6132.02 21.500.755.00881.3714.90 33.000.605.00951.7127.78 41.500.752.50891.3616.87 51.500.605.00931.3211.67 61.500.602.50871.3015.61 73.000.602.50941.3922.49 83.000.752.50951.6331.53 93.000.755.00941.6331.74 101.500.755.00891.3314.12 113.000.605.00941.6928.01 121.500.602.50881.2714.83大豆多糖质量浓度/(g/100 mL)柠檬酸质量浓度/(g/100 mL)果糖质量浓度/(g/100 mL)持水
由表3可知,当大豆多糖质量浓度为3.00 g/100 mL,柠檬酸为0.75 g/100 mL,果糖为2.50 g/100 mL时,与葡萄糖的凝胶性质相同,持水力与凝胶强度都偏高,但是其透明度也偏高。由表4方差分析可知,持水力、透明度与凝胶强度的F值分别为34.19、89.69、537.50>F 0.05,表明实验初始阶段的设计方案同样是具备可行性的。由表4参数分析可知,大豆多糖和果糖质量浓度对凝胶持水力均体现正相关作用;而大豆多糖和果糖质量浓度的交互作用对凝胶的持水性却起到了负相关作用,对其他指标的影响也各有特点,其原因较复杂,需要进一步研究其相关机制。
表4 方差分析及参数估计表
Table 4 Analysis of variance for combinations of citric acid with fructose

注:X 1为大豆多糖质量浓度;X 2为柠檬酸质量浓度;X 3为果糖质量浓度。
因素参数估计F值P>F持水力透明度凝胶强度持水力透明度凝胶强度持水力透明度凝胶强度模型——34.1989.69537.500.002 1**0.000 3***0.000 1*** X 10.0250.136.95133.33347.792 803.480.000 3**0.000 1***0.000 1*** X 2-0.002 50.0332.201.3322.43281.660.310.009 1**0.000 1*** X 30.0050.043-0.0685.3337.450.250.0820.003 6**0.65 X 1X 20.0050.006 91.085.330.8367.190.0820.410.001 2** X 1X 3-0.007 50.0371.4112.0027.13114.730.026*0.006 5**0.000 4*** X 2X 3-0.01-0.043-0.5321.3342.5116.250.009 9**0.002 9**0.016* X 1X 2X 30.005-0.032-0.835.3321.4040.120.0820.009 8**0.003 2**
2.3 柠檬酸与山梨醇及复合钾离子对大豆多糖凝胶性质的影响
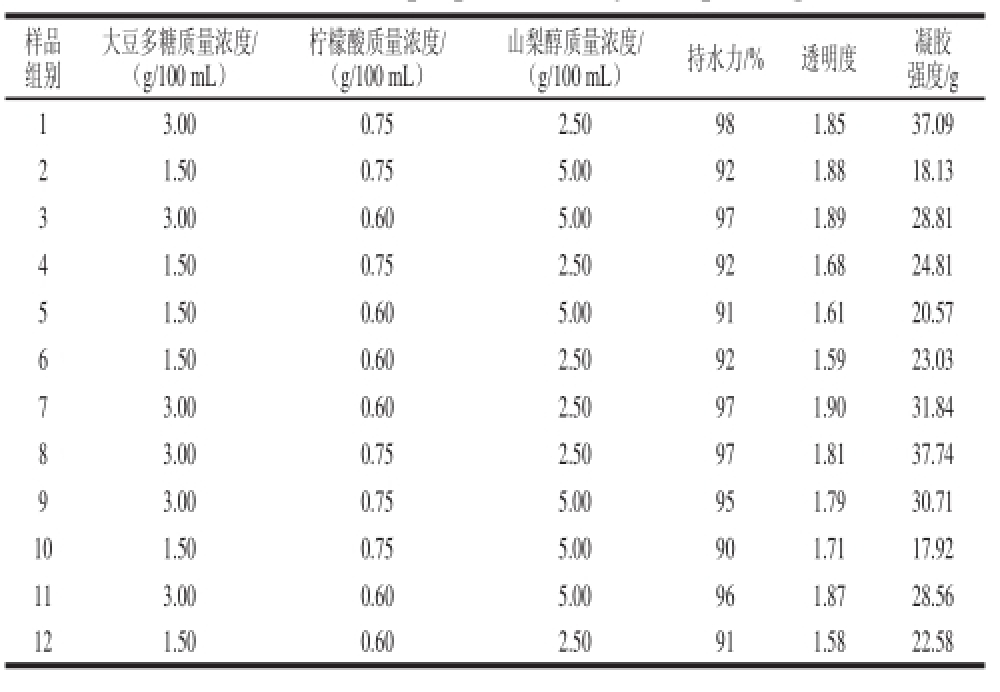
表5 柠檬酸与山梨醇对大豆多糖凝胶性质的配制组别及结果
Table 5 Effect of citric acid combined with sorbitol at different concentrations on properties of soybean pectin gel
样品组别(g/100 mL)持水力/%透明度凝胶强度/g 1 3.000.752.50981.8537.09 2 1.500.755.00921.8818.13 3 3.000.605.00971.8928.81 4 1.500.752.50921.6824.81 5 1.500.605.00911.6120.57 6 1.500.602.50921.5923.03 7 3.000.602.50971.9031.84 8 3.000.752.50971.8137.74 9 3.000.755.00951.7930.71 101.500.755.00901.7117.92 113.000.605.00961.8728.56 121.500.602.50911.5822.58大豆多糖质量浓度/(g/100 mL)柠檬酸质量浓度/(g/100 mL)山梨醇质量浓度/
表6 方差分析及参数估计表Table 6 Analysis of variance for combinations of citric acid with sorbitol
Table 6 Analysis of vari

注:X 1为大豆多糖质量浓度;X 2为柠檬酸质量浓度;X 3为山梨醇质量浓度。
因素参数估计F值P>F持水力透明度凝胶强度持水力 透明度凝胶强度持水力 透明度凝胶强度模型——14.785.45786.120.010*0.0600.000 1*** X 10.0260.0925.3080.0522.463 290.020.001***0.009 0**0.000 1*** X 2-0.000 620.0140.880.050.5191.270.840.510.000 7** X 3-0.005 60.011-2.363.860.32652.150.120.600.000 1*** X 1X 2-0.001 9-0.0551.010.437.93121.060.550.048*0.000 4** X 1X 3-0.001 9-0.026-0.100.431.811.280.550.250.32 X 2X 3-0.003 190.009-1.0141.190.22120.230.340.660.000 4** X 1X 2X 3-0.001 9-0.0130.120.430.461.810.550.530.25
由表5可知,当大豆多糖质量浓度为3.00 g/100 mL,柠檬酸为0.75 g/100 mL,山梨醇为2.50 g/100 mL时,大豆多糖的凝胶持水力与凝胶强度最大。可能是因为山梨醇的亲水性很强,山梨醇与多糖争夺水溶剂的趋势愈加剧烈,多糖与水溶剂水合的程度大大降低,迫使多糖链彼此间的距离拉近,从而造成多糖溶液稠度和黏度指标的上升,流动性减弱,再加上金属离子的作用,使得凝胶强度大大提高 [20]。由表6可知,模型透明度的F值为5.45<F 0.05,说明实验条件对透明度的影响是不显著的。而在持水力与凝胶强度中,F值分别为14.78、786.12>F 0.05,因此持水力与凝胶强度的模型是显著的,从参数分析方面来看,山梨醇的添加对透明度有改善作用,而随着山梨醇的增加持水力和凝胶强度有下降趋势,原因可能是过多的山梨醇,影响到大豆多糖之间的交联作用,但适当的添加量可以起到积极的作用。
酸及单糖复合钾离子的协同作用赋予大豆多糖凝胶体系较好的持水能力、透明度与凝胶强度。山梨醇促使大豆多糖的凝胶强度与持水能力较好,但凝胶透明度较差。葡萄糖则使大豆多糖凝胶的透明度较好。随着葡萄糖与果糖质量浓度的增加,大豆多糖凝胶强度和持水能力都逐渐增强。随着山梨醇质量浓度的增加,凝胶强度逐渐减小。柠檬酸在大豆多糖凝胶体系中具有重要作用,随着柠檬酸质量浓度的增加,凝胶体系逐渐趋于稳定,当柠檬酸质量浓度为0.75 g/100 mL时,山梨醇作用下的多糖凝胶强度及持水力都最大。
参考文献:
[1] 高建华, 戴思齐, 刘家明. 六种果皮原料果胶的理化及凝胶特性比较[J]. 农业工程学报, 2012, 28(16): 288-292.
[2] 张亦澜. 可溶性大豆多糖在酸性蛋白饮料中的应用研究[D]. 上海:华东师范大学, 2013.
[3] 杨晓泉, 齐军茹, 司华静. 大豆多糖的研究进展及在含乳饮料、米面等食品上的应用[J]. 中国食品添加剂, 2008(3): 135-139.
[4] 周艳红, 金征宇. 大豆皮果胶多糖的提取工艺研究[J]. 食品工业科技, 2004, 25(3): 76-78.
[5] 郑建仙, 丁霄霖. 大豆膳食纤维化学与工艺学的研究(Ⅱ)化学结构鉴定(上)[J]. 中国粮油学报, 1995, 10(3): 16-22.
[6] 孙元琳, 汤坚. 果胶类多糖的研究进展[J]. 食品与机械, 2004, 20(6): 60-63.
[7] 刘贺, 刘昊东, 郭晓飞. 大豆皮低酯-高酯复合果胶凝胶的持水能力及力学、光学特性[J]. 食品科学, 2010, 31(19): 111-114.
[8] 刘贺, 郭晓飞, 胡洋. 利用大豆皮果胶凝胶包埋保加利亚乳杆菌的初步研究[J]. 乳业科学与技术, 2011, 34(2): 51-54.
[9] 刘贺, 郭晓飞, 刘俊山. 大豆果胶类多糖组成特性及空间结 构的初步解析[J]. 中国粮油学报, 2012, 27(12): 12-16.
[10] LIU He, LI Qinghua, ZHU Danshi. Effects of sucrose and urea o n soy hull pectic polysaccharide gel induced by D-glucono-1,5-lactone[J]. Carbohydra te Polymers, 2013, 98(1): 542-545.
[11] GNANASAMBANDAM R, PROCTOR A.Preparation of soy hull pectin[J]. Food Chemistry, 1999, 65(4): 461-467.
[12] YOO S H, LEE B H, SAVARY B J. Characteristics of enzymatic allydeesterifi ed pectin gels produced in the presence of monovalent ionic salts[J]. Food Hydrocolloids, 2009, 23(7): 1926-1929.
[13] YOO S H, FISHMAN M L, SAVARY B J. Monovalent salt- induced gelation of enzymatically deesterifi ed pectin[J]. Journal of Agricultural and Food Chemistry, 2003, 51(25): 7 410-7417.
[14] KHOTIMCHENKO M, KOVALEV V, KHOTIMCHENKO Y. Equilibrium studies of sorption of lead (ii) ions by different pectin compounds[J]. Journal of Hazardous Materials, 2007, 149(3): 693-699.
[15] BOLAND A B, BUHR K, GIANNOULI P. Infl uence of gelatin, starch, pectin and artifi cial saliva on the release of 11 fl avour compounds from model gel systems[J]. Food Chemistry, 2004, 86(3): 401-411.
[16] 何 东保, 詹东风. 黄原胶与槐豆胶协同相互作用及其凝胶化的研究[J].林产化学与工业, 1998, 18(1): 12-16.
[17] 毛成达, 雷激, 赵丽杰. 低甲氧基果胶凝胶影响因素研究[J]. 食品科技, 2009, 34(4): 100-104.
[18] 刘贺, 朱丹实, 何余堂. 一种大豆种皮果胶类凝胶多糖的制备方法:中国, 201110400583.3[P]. 2012-06-13. .
[19] HUANG Y Q, TANG J M, SWANSON B G. Effect of calcium concentration on textural properti es of high and low acyl mixed gellan gels[J]. Carbohydrate Polymers, 2003, 54(4): 517-522.
[20] 刘刚, 雷激, 芮光伟. 低甲氧基果胶流体质构特性研究[J]. 食品工业科技, 2011, 32(1): 253-255.
Combined Infl uence of Citric Acid, Monosaccharide and Potassium Ion on Properties of Soybean Pectin Gel
LIU Junshan, LI Qinghua, ZHU Danshi, WANG Bo, HE Yutang, MA Tao, LIU He*
(Engineering and Technology Research Center of Food Preservation, Processing and Safety Control of Liaoning Province, Food Safety Key Laboratory of Liaoning Province, Food Science Research Institute, College of Chemistry, Chemical Engineering and Food Safety, Bohai University, Jinzhou 121013, China)
Abstract:In this manuscript, the combined effects of one of three monosaccharides (glucose, fructose or sorbitol), citric acid and potassium ion (at a fi xed concentration of 0.2 mol/L) on the transparency, water-holding capacity and gel strength of soybean hull pectin were studied. Statistical analysis with Design-Expert software showed that polysaccharide concentration had a signifi cant infl uence on water-holding capacity, transparency and gel strength. The highest water-holding capacity and gel strength (98% and 37.74 g, respectively) were observed for 3.00 g/100 mL soybean hull pectin gel with 0.20 mol/L potassium ion, 0.75 g/100 mL citric acid and 2.50 g/100 mL sorbitol. Citric acid and soluble solids also had signifi cant effects on the transparency. Pectin concentration was correlated negatively with the transparency but positively with the gel strength. Citric acid concentration only affected signifi cantly the gel transparency, while glucose concentration exerted signifi cant effects on both water-holding capacity and gel strength (P < 0.05) but not on the transparency.
Key words:soybean pectin; glucose; fructose; sorbitol; water-holding capacity; transparency; gel strength
中图分类号:TS201.7
文献标志码:A
文章编号:1002-6630(2015)01-0027-04
doi:10.7506/spkx1002-6630-201501005
收稿日期:2014-03-04
基金项目:国家自然科学基金面上项目(31471621);国家自然科学基金青年科学基金项目(31201385);辽宁省高等学校优秀人才支持计划项目(LR2014034)
作者简介:刘俊山(1988—),男,硕士研究生,研究方向为粮食油脂与植物蛋白工程。E-mail:1804411203@qq.com
*通信作者:刘贺(1979—),男,副教授,博士,研究方向为食品大分子的结构与功能及其修饰。E-mail:liuhe2069@163.com