
图1 Eaq4的化学结构
Fig.1 Chemical structure of 3,7,3',4'-O-tetraethyl acetate quercetin
何 翊,秦 燕,范亚苇,邓泽元,胡蒋宁 *
(南昌大学 食品科学与技术国家重点实验室,江西 南昌 330047)
摘 要:通过测定槲皮素及其酯化物的平衡溶解度和油水分配系数,检测酯化后的槲皮素衍生物脂溶性是否提高。采用高效液相色谱法测定槲皮素及3,7,3',4'-O-四乙酸乙酯槲皮素在水、不同缓冲盐溶液中的质量浓度;采用摇瓶-液相色谱法,测定二者在正辛醇-水、缓冲液体系中的油水分配系数。37 ℃时,槲皮素在水中的平衡溶解度为23.02 μg/mL,而3,7,3',4'-O-四乙酸乙酯槲皮素在水中的平衡溶解度更小,为10.23 μg/mL。随着溶剂pH值的增大,槲皮素的平衡溶解度增大,3,7,3',4'-O-四乙酸乙酯槲皮素变化并不显著。槲皮素、3,7,3',4'-O-四乙酸乙酯槲皮素在正辛醇-水体系条件下的油水分配系数分别为1.819、3.696。酯化修饰后的3,7,3',4'-O-四乙酸乙酯槲皮素脂溶性高于槲皮素。
关键词:槲皮素;3,7,3',4'-O-四乙酸乙酯槲皮素;平衡溶解度;油水分配系数
槲皮素,3,3',4',5,7-五羟基黄酮,是膳食中最常见的类黄酮之一,广泛存在于水果和蔬菜中,如洋葱、茶叶、苹果和莓类等植物性食品中,同时也是一些中草药如槐米花、三七、银杏叶等的有效成分,在机体内能发挥有益的健康保护作用。这种保护作用包括抗氧化 [1]、抗炎症 [2-3]、血管舒张 [4-6]、抗肿瘤 [7-8]等。但由于槲皮素的分子结构中含有多个极性羟基基团,亲脂性较弱,并且由于其分子结构中的羟基结构造成的分子间作用,形成氢键,造成晶格能较高,其水溶性也较弱,在水中的溶解度只有7μg/mL [9]。槲皮素进入体内后,吸收并代谢,以甲基化、硫酸化和葡萄糖醛酸化的简单代谢为主,存在强烈的首过效应,生物利用度低,一直以来在临床上作为药物而使用有很大的局限性 [10]。本实验室通过酯化修饰合成了3,7,3',4'-O-四乙酸乙酯槲皮素(3,7,3',4'-O-tetraethyl acetate quercetin,Eaq4) [11],如图1所示,以期提高槲皮素的脂溶性以及在体内的稳定性,从而提高其生物利用度 [12]。
本实验通过对槲皮素及其乙酸乙酯衍生物Eaq4的平衡溶解度、表观油水分配系数进行研究和测定,初步考察槲皮素及其酯化衍生物的溶解性和渗透性,以期为槲皮素及其衍生物的体内吸收代谢及其他相关药学研究提供参考。

图1 Eaq4的化学结构
Fig.1 Chemical structure of 3,7,3',4'-O-tetraethyl acetate quercetin
1.1 材料与试剂
槲皮素 上海晶纯生化科技股份有限公司;Eaq4,本实验室通过以槲皮素为原料的烷基化合成,利用柱层析、制备色谱技术纯化,高效液相色谱纯度为95.5%;甲醇(色谱纯) 德国Meker公司;其他有机试剂均为国产分析纯。
1.2 仪器与设备
FA1604电子天平 上海精密科学仪器有限公司;1100型高效液相色谱仪 美国安捷伦公司;5810R离心机 德国艾本德公司;ZD-88 PK恒温摇床 苏州威尔实验用品有限公司。
1.3 方法
1.3.1 色谱条件
色谱柱:C 18(2.1 mm×100 mm,3.5 μm);流动相:甲醇-水(73∶27,V/V);流速1 mL/min;检测波长365 nm;柱温30 ℃。
1.3.2 标准曲线的绘制
精密称取槲皮素,Eaq4对照品10 mg,置于10 mL容量瓶中,加适量甲醇溶解并稀释,配成质量浓度1 mg/mL储备液,采用逐级稀释法配成0.5、0.05、0.025、0.01 mg/mL标准溶液,精密吸取10 μL,注入液相色谱仪,依法测定,记录峰面积。
1.3.3 精密度的测定 [13]
取槲皮素和Eaq4对照品0.5、0.25、0.1 mg/mL 3 个质量浓度,按1.3.1节色谱条件连续进样6 次,以峰面积来考察其日内精密度。同样,取槲皮素和Eaq4对照品0.5、0.25、0.1 mg/mL 3 个质量浓度,每日进样测定1 次,记录峰面积,连续测试6 d,考察日间精密度。
1.3.4 回收率的测定
分别称取含量已知的槲皮素和Eaq4对照品5 mg,分别置于10 mL量瓶中,再分别加入0.6、0.5、0.5 mg/mL对照品溶液适量,甲醇定容至刻度,进样测定,计算平均回收率。
1.3.5 不同pH值缓冲溶液条件下平衡溶解度的考察 [14]
按药典方法配制pH值为7.4的磷酸缓冲液,分别以NaOH溶液和磷酸溶液调节一系列pH值分别为2.5、4.5、5.8、6.8、7.0、7.4、8.0的磷酸缓冲液。取过量的槲皮素及Eaq4,分别加入1 mL纯水、0.1 mol/L盐酸,pH值为2.5、4.5、5.8、6.8、7.0、7.4、8.0的磷酸缓冲液于2 mL试管中。37 ℃条件下放入恒温摇床中避光振荡24 h,静置,离心(13 000 r/min、5 min),各吸取上清饱和液,经适当稀释后,精密吸取10 μL,注入液相色谱仪,记录峰面积,以标准曲线法计算槲皮素及Eaq4在不同pH值溶液中的溶解度。
1.3.6 油水分配系数的测定 [15]
采用经典的摇瓶法,以正辛醇-水为系统测定槲皮素及Eaq4的油水分配系数。取适量槲皮素及Eaq4溶解于被水饱和的正辛醇中,制成药物的正辛醇溶液,精密量取该溶液0.5 mL置于10 mL具塞试管中,再分别加入被正辛醇饱和的水、pH 5.8、6.5,7.4的磷酸缓冲液4.5 mL,放入恒温摇床中,于37 ℃避光振摇24 h平衡,离心,取上层正辛醇溶液400 μL,冷冻干燥12 h,加入1 mL甲醇溶液,10 μL注入高效液相色谱仪检测;取1.0 mg/mL对照品溶液10 μL注入液相色谱仪,记录峰面积。以外标法以峰面积计算槲皮素和Eaq4的质量浓度,按公式(1)、(2)计算水相质量浓度和油水分配系数。
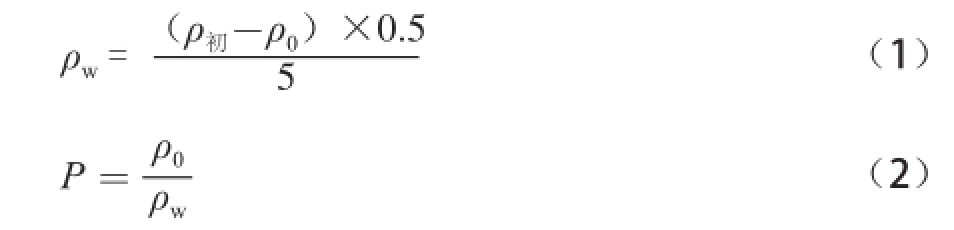
式中:ρ 初为初始药物质量浓度/(mg/mL);ρ o为油相药物质量浓度/(mg/mL);ρ w为水相质量浓度/(mg/mL);P为油水分配系数。
2.1 标准曲线
取槲皮素和Eaq4储备液稀释至0.5、0.05、0.025、0.01 mg/mL,按1.3.1节色谱条件进行液相色谱测定,槲皮素的保留时间为3.308 min,Eaq4保留时间为15.472 min,记录峰面积。以槲皮素和Eaq4的质量浓度为横坐标,峰面积为纵坐标,建立标准曲线,得其线性回归方程:Y=10.8x-2.323 9(R 2=0.999 8);Y=2.598 8x+4.402 6(R 2=0.995)。结果表明,槲皮素和Eaq4在0.01~0.5 mg/mL范围内线性关系良好。

图2 槲皮素及Eaq4的HPLLCC图
Fig.2 HPLC chromatograms of quercetin and Eaq4
2.2 精密度的测定
表1 槲皮素及其酯化物的精密度
Table1 Between-day and within-day assay precision (RSDs) for quercetin and its ethyl acetate derivative
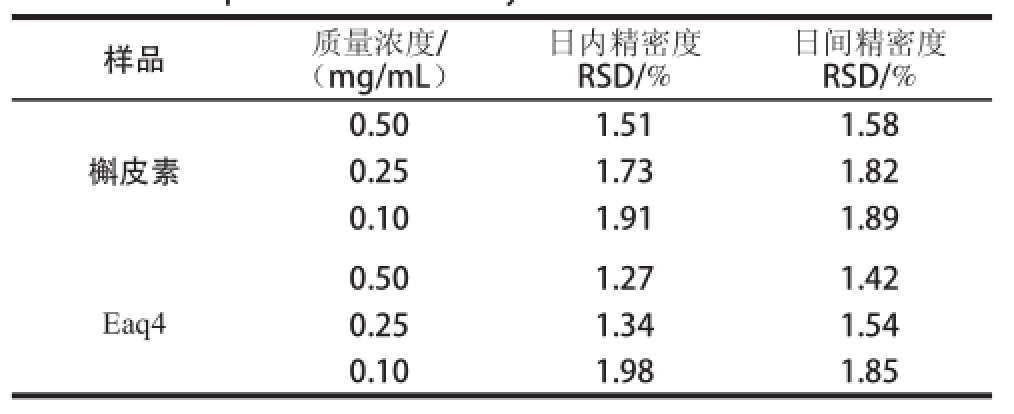
样品质量浓度/(mg/mL)日内精密度RSD/%日间精密度RSD/%槲皮素0.501.511.58 0.251.731.82 0.101.911.89 Eaq4 0.501.271.42 0.251.341.54 0.101.981.8 5
如表1所示,日间、日内精密度的相对标准偏差(relative standard deviation,RSD)均小于2%,表明检测方法可靠,稳定性好。
2.3 回收率的测定
表2 槲皮素及其酯化物的回收率
Table2 Recoveries of quercetin and its ethyl acetate derivative

样品加入对照品质量浓度/(mg/mL) 平均回收率/%RSD/%槲皮素0.4099.121.75 0.5099.331.98 0.6099.122.32 Eaq4 0.4099.891.37 0.50100.741.22 0.6099.191.89
回收率结果如表2所示。平均回收率为99.19%、99.94%。结果表明:该法回收率高,可用于槲皮素和Eaq4的平衡溶解度及油水分配系数的测定。
2.4 不同溶剂条件下的平衡溶解度
如表3所示,槲皮素的溶解度随着溶剂pH值的增加而逐渐增大,在1 mol/L盐酸溶液中的溶解度大于在pH值为2.5的磷酸盐缓冲液(phosphate buffered saline,PBS)中的溶解度,而Eaq4随溶剂pH值的增加,没有明显变化。
表3 槲皮素及其酯化物在不同介质中的平衡溶解度(37 ℃)
Table3 Equilibrium solubility of quercetin and its ethyl acetate derivative in different media (37 ℃)
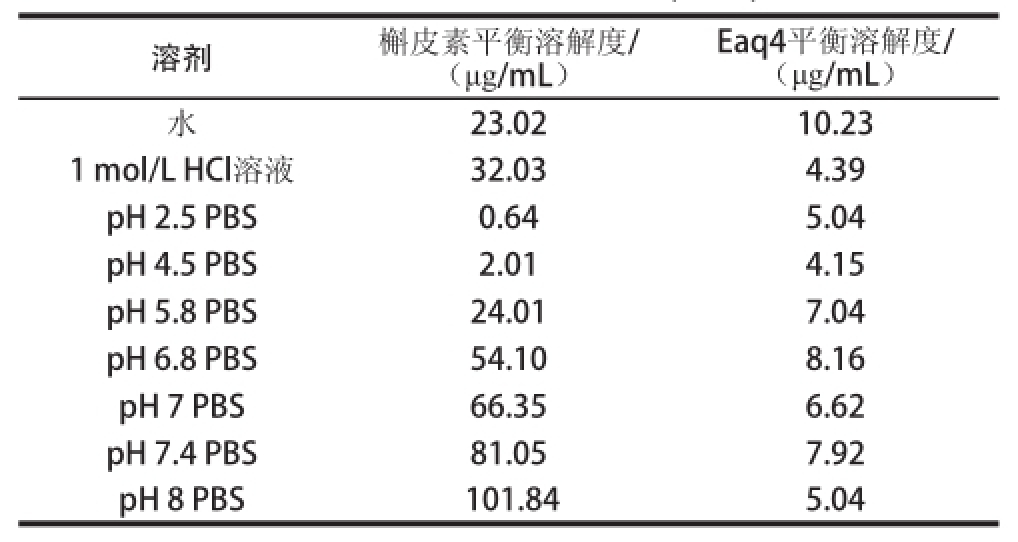
Eaq4平衡溶解度/(μg/mL)水23.0210.23 1 mol/L HCl溶液32.034.39 pH 2.5 PBS0.645.04 pH 4.5 PBS2.014.15 pH 5.8 PBS24.017.04 pH 6.8 PBS54.108.16 pH 7 PBS66.356.62 pH 7.4 PBS81.057.92 pH 8 PBS 101.845.04溶剂槲皮素平衡溶解度/(μg/mL)
2.5 油水分配系数
表4 槲皮素及其酯化物在不同溶液体系中的表观油水分配系数(37 ℃)37
Table4 Apparent oil-water partition coefficients of quercetin and its ethyl acetate derivative in different solution systems (37 ℃)
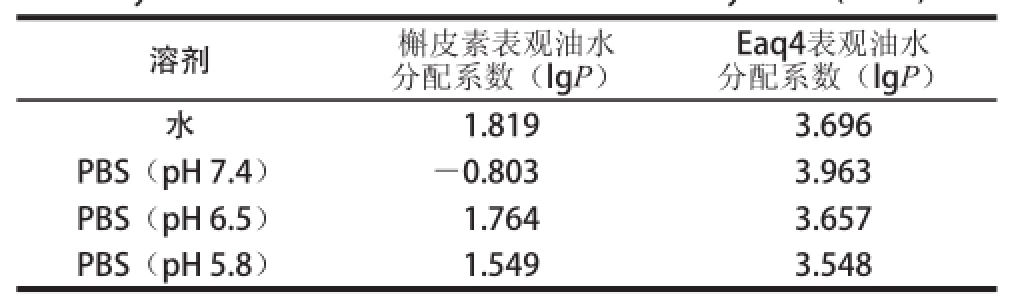
Eaq4表观油水分配系数(lgP)水1.8193.696 PBS(pH 7.4)-0.8033.963 PBS(pH 6.5)1.7643.657 PBS(pH 5.8)1.5493.548溶剂槲皮素表观油水分配系数(lgP)
如表4所示,槲皮素的表观油水分配系数小于Eaq4,表明其脂溶性小于Eaq4。槲皮素在pH值偏碱性时,lgP小于0,亲水性更强,而Eaq4在不同pH值条件下的lgP值变化不大,故pH值对槲皮素的影响较显著,对Eaq4的影响不大。
在37 ℃条件下不同pH值溶液中药物溶解度的变化是由其化学结构所决定的。通常药物以分子型通过生物膜,进入细胞后,在膜内水介质中解离成离子型,以离子型起作用。槲皮素是一个弱酸性药物,其pK a约为6.5,当溶液的pH值大于药物的pK a时,药物解离度高,药物在溶液中大部分以离子形式存在,即药物的溶解度大;当溶液的pH值小于药物的pK a时,药物的解离受到抑制,药物在溶液中主要以分子形式存在,即溶解度小 [16]。从槲皮素溶解度的测定结果表明,槲皮素的溶解度受介质的pH值影响较大,随着pH值增大,槲皮素的溶解度也增大;当pH值大于6.8时,槲皮素的溶解度增加明显,在pH值为8时,达到101.84 μg/mL,测得与钟玲等 [14]测定芦丁在不同pH值条件下溶解度的变化规律相似,这与槲皮素分子中的酸性羟基碱化成盐有关。而Eaq4的溶解度受pH值的影响并不显著,说明其在实验pH值范围内主要以分子形式存在。而人体肠道吸收主要段的pH值在6~8,主要吸收亲脂性药物 [17],槲皮素易解离,难被吸收,分子型的药物更易吸收,所以Eaq4在肠道内可能比槲皮素有更好地吸收。该实验结果为研究2种药物在体内吸收过程中的转运方式提供了参考依据。
药物在体内的溶解、吸收、分布、转运与药物的水溶性和脂溶性有关,亦即和油水分配系数有关。药物要有适当的脂溶性,才能扩散并透过生物膜,而具有水溶性才有利于药物在体液内转运,达到作用部位与受体结合,从而产生药物效应,所以药物需要有适当的油水分配系数 [18-19]。
本实验采用经典的摇瓶法测定样品的油水分配系数,以正辛醇-水为系统,液相法进行测定,操作简便,准确性好 [20-21]。以正辛醇-水系统测出的油水分配系数对预测药物的定量结构-吸收等有重要意义。一般将药物分为3类:lgP小于-0.3的水溶性药物为第1类,lgP在0.3~4.5的为第2类,lgP大于4.5的脂溶性药物为第3类 [22-23]。槲皮素lgP为-0.803,Eaq4 的lgP为3.696,可以推断Eaq4的脂溶性较槲皮素更好,可能有较高的吸收率及组织分布。Eaq4是槲皮素与溴乙酸乙酯发生烷基化反应生成的具有酯类基团的醚类化合物,醚类化合物由于醚中的氧原子有孤对电子,能吸引质子 [24],具有亲水性,碳原子具有亲油性,使醚类化合物在脂-水交界处定向排布,易于通过生物膜;乙酸乙酯基提高了化合物的脂溶性,进入细胞内后,又易于在体内酶的作用下发生水解反应生成羧酸,从而提高其水溶性,提高其生物利用度。以上只是通过分析槲皮素及其酯化物的理化性质来推测其在体内的吸收代谢,更进一步的研究其在体内的吸收转运机制,则需要在Caco-2细胞模型条件下加以验证 [25]。
参考文献:
[1] LEOPOLDINI M, RUSSO N, TOSCANO M, et al. The molecular basis of working mechanism of natural polyphenolic antioxidants[J]. Food Chemistry, 2011, 125(2): 288-306.
[2] CH IRUMBOLO S. The role of quercetin, flavonols and flavones in modulating inflammatory cell function[J]. Inflammation and Allergy Drug Targets, 2010, 9(4): 263-285.
[3] MUELLER M, HOBIGER S, JUNGBAUER A. Antiinflammatory activity of extracts from fruits, herbs and spices[J]. Food Chemistry, 2010, 122(4): 987-996.
[4] GALINDO P, GONZALEZ-MANZANO S, ZARZUELO M J, et al. Different cardiovascular protective effects of quercetin administered orally or intraperitoneally in spontaneously hypertensive rats[J]. Food and Function, 2012, 3(6): 643-650.
[5] NISHIDA S, SATOH H. Role of gap junction involved with endothelium-derived hyperpolarizing factor for the quercetin-induced vasodilatation in rat mesenteric artery[J]. Life Sciences, 2013, 92(13):752-756.
[6] MONORI-KISS A, MONOS E, NADASY G L. Quantitative analysis of vasodilatory action of quercetin on intramural coronary resistance arteries of the rat in vitro[J]. Plos One, 2014, 7(8): 2-6
[7] GACCHE R N, SHEGOKAR H D, GOND D S, et al. Evaluation of selected flavonoids as antiangiogenic, anticancer, and radical scavenging agents: an experimental and in silico analysis[J]. Cell Biochemistry and Biophysics, 2011, 61(3): 651-663.
[8] WEI Yuquan, ZHAO Xia, KARIYA Y, et al. Induction of apoptosis by quercetin: involvement of heat shock protein[J]. Cancer Reasearch,1994, 54: 4952-4957.
[9] 彭游. 植物黄酮的微波辅助提取, 苯磺酸酯修饰与药物动力学研究[D].南昌: 南昌大学, 2009: 17-20.
[10] 叶慧. 槲皮素衍生物的合成及其对氧化损伤保护作用的研究[D]. 南昌: 南昌大学, 2013: 16-18.
[11] 胡蒋宁, 叶慧, 邓泽元. 槲皮素衍生物及其合成方法: 中国,201310745899.5[P]. 2014-04-09. http://www2.drugfuture.com/cnpat/ search.aSpx.
[12] CHEN Chen, ZHOU J, JI Chunyan. Quercetin: a potential drug to reverse multidrug resistance[J]. Life Sciences, 2010, 87: 333-338.
[13] 钱一鑫, 康冀川, 文庭池, 等. 银杏黄酮苷元的平衡溶解度和表观油水分配系数的测定[J]. 时珍国医国药, 2011, 22(7): 1643-1644.
[14] 钟玲, 臧志和, 鲁朝江. 芦丁的溶解度及油水分配系数研究[J]. 中国药业, 2009, 18(19): 10-12.
[15] 杨秀丽, 孙进, 何仲贵. 格列吡嗪油水分配系数和平衡溶解度的测定[J]. 中国药剂学杂志, 2009, 7(3): 121-126.
[16] 樊志顺, 李勤朗. 用pH分配原理pK a值对临床用药问题的讨论分析[J].实用医技杂志, 1996, 2(3): 6-8.
[17] 孙洁胤, 周芝芳, 刘放. 苦参素油水分配系数及pH值对其的影响[J].浙江省医学科学院学报, 2006, 64(3): 19-21.
[18] 王春雷, 芦柏震, 侯桂兰. 药物转运体与药物体内过程[J]. 安徽医药,2005, 9(10): 721-723.
[19] 徐文, 孙进, 张婷婷. HPLC法测定冬凌草甲素的平衡溶解度和表观油水分配系数[J]. 沈阳药科大学学报, 2007, 24(4): 220-222.
[20] 张立军, 潘岳峰, 张多婷. 高效液相色谱法测定去氧氟尿苷在不同介质中的平衡溶解度和表观油水分配系数[J]. 中南药学, 2009,7(12): 923-926.
[21] 刘强, 万新祥, 黄小平. 药物的油水分配系数及透皮吸收速率常数的相关性研究[J]. 第一军医大学分校学报, 2000, 23(1): 5-6.
[22] 张给智. 头孢噻肟钠油水分配系数的测定研究[J]. 黑龙江科技信息,2013, 12(2): 87.
[23] 李东芬, 尹蓉莉, 吕懿平, 等. 芍药苷油水分配系数的测定及pH对其的影响中药与临床[J]. 中药与临床, 2011, 2(4): 21-23.
[24] 陈国庆, 吴亚敏. 乙醚的荧光光谱及其特性[J]. 原子与分子物理学报, 2007, 4(1): 101-105.
[25] ARTURSSON P, PALM K, LUTHMA N. Ca co-2 monolayers in experimental and theoretical predictions of drug transport[J]. Advanced Drug Delivery Reviews, 2012, 64: 280-289.
Determination of Equilibrium Solubility and Apparent Oil/Water Partition Coefficients of Quercetin and Its Ethyl Acetate Derivatives
HE Yi, QIN Yan, FAN Yawei, DENG Zeyuan, HU Jiangning
*
(State Key Laboratory of Food Science and Technology, Nanchang University, Nanchang 330047, China)
Abstract:This study aimed to determine the equilibrium solubility and oil/water partition coefficients of quercetin and its ester derivative. The equilibrium solutions of quercetin and its ethyl acetate derivative in various media were detected by high performance liquid chromatogram (HPLC); and the shake flask-HPLC method was applied to determine the partition coefficients of quercetin and its ethyl acetate derivative in n-octanol-water-buffer solutions of different pH values. The equilibrium solubility of querctin and its ethyl acetate derivative was 23.02 and 10.23 μg/mL in water at 37 ℃, and the equilibrium solubility of querctin increased with increasing pH of the buffer solution, but no remarkable change was observed for its ethyl acetate derivative. The partition coefficients of quercetin and its ethyl acetate derivative in n-octanolwater-buffer solutions of different pH were 1.819 and 3.696, respectively. The esterification modification of quercetin improved its lipid solubility.
Key words:querctin; ethyl acetate derivative of quercetin; equilibrium solubility; apparent oil/water partition coefficient
中图分类号:TS201.2
文献标志码:A
文章编号:1002-6630(2015)14-0055-04
doi:10.7506/spkx1002-6630-201514011
收稿日期:2014-11-05
基金项目:国家自然科学基金地区科学基金项目(31360370);2014年江西省科学技术研究项目(GJJ14092)
作者简介:何翊(1990—),女,硕士研究生,研究方向为天然活性物质开发与利用。E-mail:heyi615@hotmail.com
*通信作者:胡蒋宁(1981—),男,副教授,博士,研究方向为天然活性物质开发与利用。E-mail:hujiangning@ncu.edu.cn