表1 仪器工作参数设定表
Table 1 Working parameters of the instrument

注:扣背景(氘灯)均为BGC-D2。
?
徐 皓,刘水英
(陕西理工学院生物科学与工程学院,陕西 汉中 723000)
摘 要:以福建省武平县和云南省红河州紫山药块根为实验材料,采用湿法消解-原子吸收光谱法对其中12 种矿质元素含质进行分析检测。结果表明:湿法消解-原子吸收光谱法能准确测定紫山药中矿质元素的含质,回收率在92.00%~106.00%之间,相对标准偏差在10%以下,且方法简单、快捷;供试的紫山药中矿质元素含质丰富,不仅富含 Mg、Fe、Zn,还含有对人体有益的Se元素。重金属中除了Ni元素,其他重金属(Cr、Pb、As、Cd、Hg)的含质均符合GB 2762—2012《食品中污染物限质》。
关键词:紫山药;湿法消解;原子吸收光谱法;矿质元素
紫山药(Dioscorea alata L.)属薯蓣科(Dioscorea)山药属(Dioscorea)多年生草本蔓生植物 [1],俗称“紫淮山、紫人参”,又名薯蓣和长芋,以其肥大的块根或圆柱状根供食用。因其富含蛋白质、维生素、多原、胆碱、薯蓣皂苷 [2-3]、酚类黄酮物质等 [4]多种营养及生物活性成分而具有很高的药用价值 [5],并被誉为“蔬菜之王” [6]。与普通山药相比,紫山药中含有更多的维生素、花青苷类天然色素 [7-8]和微质元素 [9]。因此,紫山药不仅是药食兼用的绿色食品,而且极具市场潜力 [10-11]。
目前,有关紫山药的研究主要集中在引种、种植、品种改良及部分营养成分分析方面,而对紫山药中的矿质元素的相关研究及文献报道很少 [12-13]。有关矿质元素、重金属和非金属的检测方法很多,常见的有原子吸收光谱(atomic absorption spectrometry,AAS)法、原子荧光光谱法、电化学法等 [14],AAS法是目前供试样中待测元素检测最常用的一种方法 [15-17]。为了更加科学地分析研究紫山药以及更好地利用紫山药资源,本实验采用湿法消解-AAS法对福建和云南两地供试紫山药中12 种矿质元素的含质进行了对比分析,旨在为紫山药资源的综合开发利用、提供矿质元素检测方法及矿质元素含质方面的实验指导和数据参考。
1.1 材料与试剂
新鲜的紫山药样品分别采购于福建省武平县和云南省红河州屏边苗族自治县。
Mn、Fe、Zn、Cu、Ni、Cr、Mg、Cd、Hg、Pb、As、Se标准溶液 中国医药集团上海化学试剂公司;浓硝酸、氢氟酸等(均为优级纯) 上海国药集团;实验用水均为超纯水(电阻率18.25 MΩ·cm,25 ℃)。
1.2 仪器与设备
101-3A电热鼓风恒温干燥箱 炉南电炉烘箱厂;
FW-177高速万能粉碎机 北京泰亚赛福科技发展有限责任公司;AUY220万分之一电子天平 日本岛津公司;ECH-1型电子控温加热板 上海新仪微波化学科技有限公司;M6型AAS仪(配有火焰原子化系统和石墨炉原子化系统) 美国Thermo Electron公司;Mn、Fe、Zn、Cu、Ni、Cr、Mg、Cd、Hg、Pb、As、Se空心阴极灯 北京市朝阳路天宫电器厂;VE-AS系列超纯水机深圳沃尔奇科技有限公司。
1.3 方法
1.3.1 仪器参数设置及分析条件
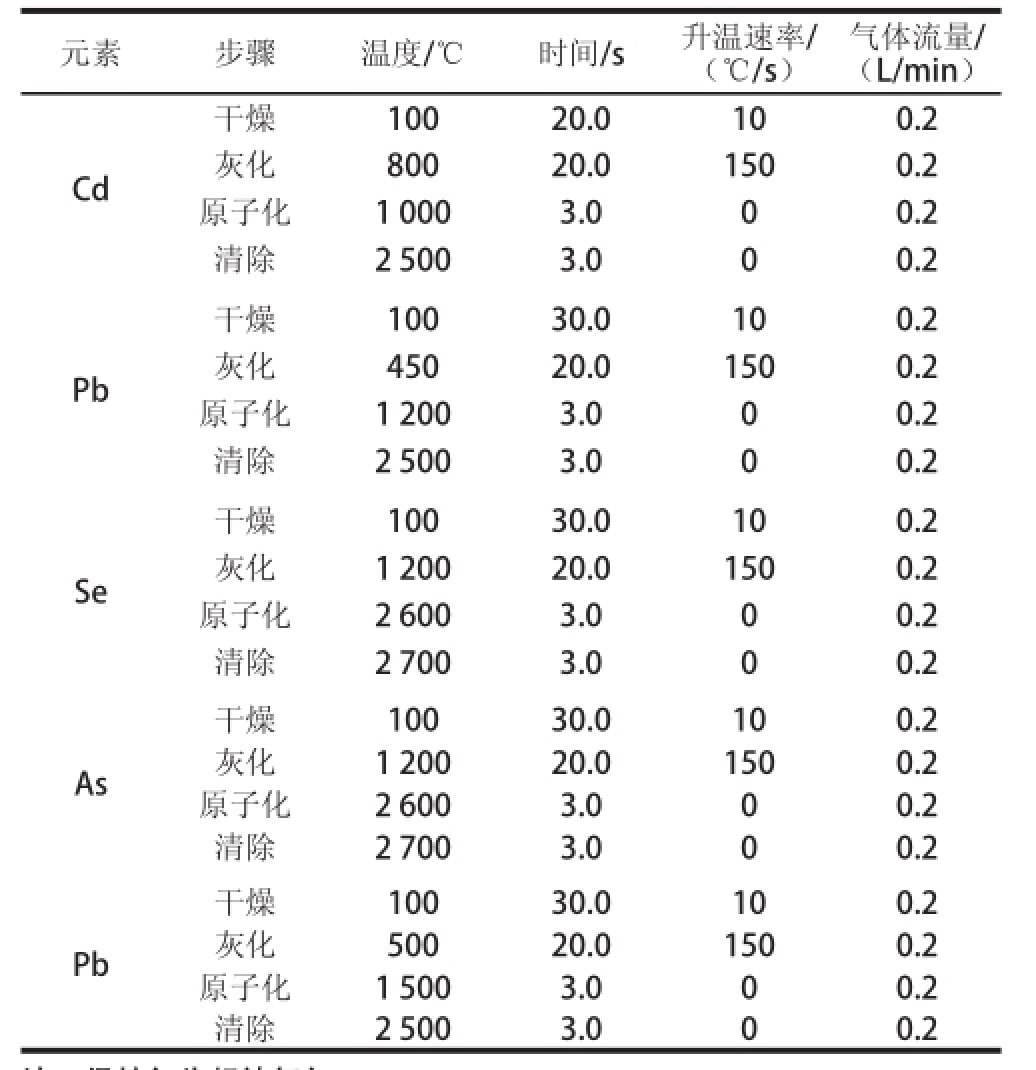
表1 仪器工作参数设定表
Table 1 Working parameters of the instrument

注:扣背景(氘灯)均为BGC-D2。
?
表2 光谱仪工作条件
Table 2 Spectrometer working conditions

注:塞曼扣背景。
?
表3 石墨炉工作条件Table 3 Working conditions of graphite furnace
注:保护气为超纯氩气。
?
火焰AAS法测定Cu、Ni、Zn、Fe、Mn、Mg、Cr含质,石墨炉AAS法测定Pb、Se、As、Hg、Cd含质,保护气为超纯氩气。仪器参数设置见表1,光谱仪工作条件见表2,石墨炉工作条件见表3,背景校正方式均采用Zeeman偏振效应背景校正。
1.3.2 标准溶液的制备
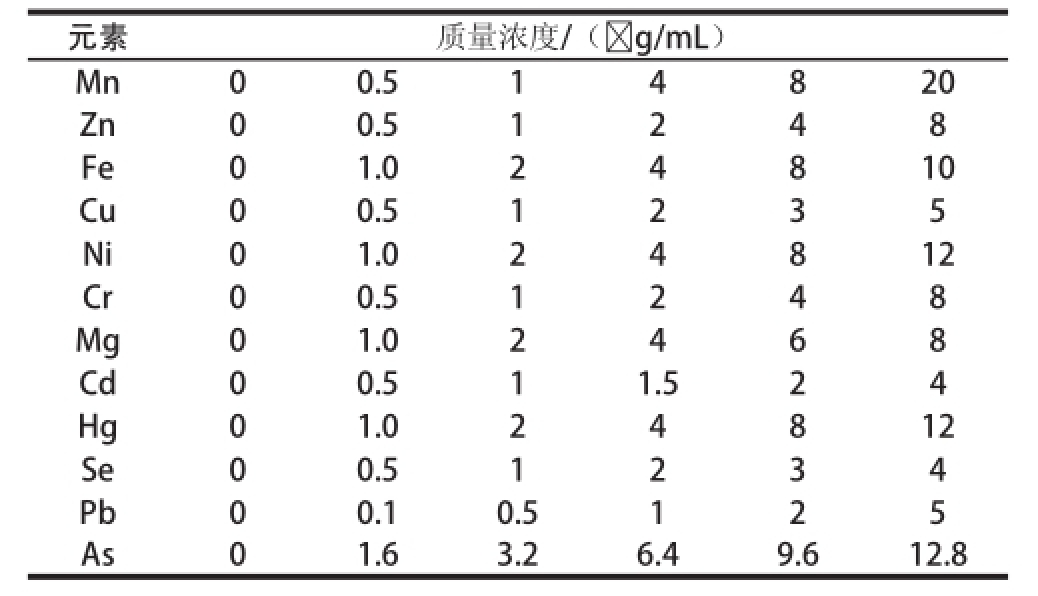
取Mn、Zn、Cu、Ni、Cr、Mg、Cd、Hg、Pb、As、Se、Fe元素的标准液配制成相应质质浓度的系列溶液,各元素的标准溶液质质浓度梯度见表4。
表4 12 种矿质元素标准溶液的质量浓度
Table 4 The concentrations of 12 mineral elements in mixed standard solutions
?
1.3.3 消化条件的优化
本研究比较了HNO 3、HF-HNO 3、HNO 3-H 2O 2(2∶1,V/V)、HNO 3-HClO 4(4∶1,V/V)消化体系在相同体积、相同消化时间下的消化效果;以HF-HNO 3(3∶5,V/V)混酸作为消化体系,固定混酸体积为8 mL,研究不同消化时间(0.5、1.0、1.5、2.0、2.5、3.0的消化效果。
1.3.4 样品前处处及消化液制备
分别将紫山药用超纯水清洗净,切成3~5 mm的薄片,平铺在非金属制品的盘子中,于45 ℃在鼓风干燥箱中烘干24 h,再在高速万能粉碎机中粉碎,过80 目筛、编号(福建样、云南样),保存于二氧化硅干燥器中、备用。
分别精密称取2 种样品0.500 0 g,每种样品做6 个平行样。置于消化管中,用移液管加入3 mL浓HF静置1 h,用移液管加入5 mL浓HNO 3静置30 min后再放入电热鼓风干燥箱中,在130 ℃消化3 h,取出冷却至室温后倒入挥酸管中,用少质1%稀HNO 3清洗消化管,洗液倒入挥酸管中,将挥酸管置于电子恒温加热板上,在170 ℃条件下挥发至液体质在0.5~1 mL之间,再将其倒入50 mL小烧杯中,用少质1%稀HNO 3溶液清洗挥酸管,洗液倒入烧杯中,再将烧杯中的样品用1%稀HNO 3溶液定容于50 mL容质瓶中,置于阴凉处备用。
1.3.5 标准曲线的绘制及样品的测定
按表1的仪器工作条件来测定标准系列吸光度、紫山药消化液的吸光度。所有元素的测定用氘灯扣除背景。仪器自动处处数据,并显示标准曲线。确认后在同一条件下按顺序进行空白溶液和样品溶液吸光度的测定,必要时将样品溶液适当稀释到线性范围。以超纯水作为空白参比溶液,依次对标准系列溶液、紫山药消化液测定吸光度,根据所绘制的标准工作曲线可以得到样品中各元素的质质浓度。根据工作曲线、测定质质浓度、定容体积、样品称样质和稀释倍数,计算各元素含质。
1.3.6 方法学实验
1.3.6.1 检出限实验
取所测元素的稀释标准溶液(Mn 1.0 μg/mL、Zn 2.0 μg/mL、Cu 3.0 μg/mL、Ni 2.0 μg/mL、Cr 1.0 μg/mL、Mg 2.0 μg/mL、Cd 1.0 μg/mL、Hg 2.0 μg/mL、Pb 10.0 μg/mL、As 3.2 μg/mL、Se 2.0 μg/mL、Fe 1.0 μg/mL)连续测定10 次,计算检出限。
1.3.6.2 精密度实验
取福建样和云南样均做6 个平行,每个平行样重复测定3 次,根据测定结果的相对标准偏差(relative standard deviation,RSD)值来判断实验的精密度。
1.3.6.3 加标回收实验
福建样、云南样进行加标回收实验,在已知含质的3 种样品中加入一定已知含质的Mn、Fe、Zn、Cu、Ni、Cr、Mg、Cd、Hg、Pb、As、Se的标准溶液,测定各检测波长处对应的吸光度,将吸光度带入相应的标准曲线计算出各矿质元素的含质。在此基础上计算各矿质元素的回收率,见式(1)。
1.3.7 紫山药中矿质元素的含质
材料中每个元素含质测定6 个平行样,每个样测定3次。元素含质计算见式(2) [19]。
式中:m为样品质质/g;V为样品第一次定容体积/mL;V 1为从V中吸出质/mL;V 2为测定时定容得体积/mL;ρ为测试溶液中某元素质质浓度/(μg/mL)。
2.1 消化条件选择
消化后,所得到的消化液液体澄清、透亮,消解液中无固体、沉淀及悬浮微粒。说明:样品消解彻底;采用HF-HNO 3混酸体系作消化液是合适的;消解温度选择130 ℃并恒温3 h,再于170 ℃条件下挥酸2 h消解效果较佳。
2.2 标准曲线方程的建立
表5 标准曲线的线性方程和相关系数Table 5 Standard curve regression equations with correlation coefficients

元素线性方程相关系数(r)FeA=0.038 64ρ+0.004 60.999 5 MnA=0.079 27ρ+0.002 10.999 8 ZnA=0.287 94ρ+0.015 40.999 2 NiA=17.544 4ρ+0.111 90.999 8 MgA=1.101 1ρ-0.437 50.994 9 CuA=0.647 9ρ-0.014 00.998 7 CrA=0.026 2ρ+0.001 10.999 5 PbA=0.013 4ρ+0.014 20.999 4 HgA=4.050 8ρ+0.220 00.999 7 AsA=0.010 8ρ+0.018 30.999 7 SeA=44.341 4ρ-6.600 30.999 2 CdA=0.069 6ρ+0.014 60.999 5
标准曲线的回归方程及相关系数见表5。由各元素的相关系数(r)可知,各元素在其线性范围内相关程度高、线性关系良好。其中除Mg、Cu以外,其他元素的相关系数均达到0.999 0以上,各元素的吸光度和质质浓度之间线性拟合较好。
2.3 检出限
根据1.3.6.1节的方法,各所测标准溶液分析方法的检出限依次为:Mn 1.213 μg/mL、Zn 0.134 μg/mL、Cu 0.125 μg/mL、Ni 0.341 μg/mL、Cr 1.205 μg/mL、Mg 0.179 μg/mL、Cd 0.293 μg/mL、Hg 0.258 μg/mL、Pb 1.401 μg/mL、As 0.373 μg/mL、Se 2.135 μg/mL、Fe 1.251 μg/mL。
2.4 精密度
表6 精密度实验结果
Table 6 Results of precision experiments
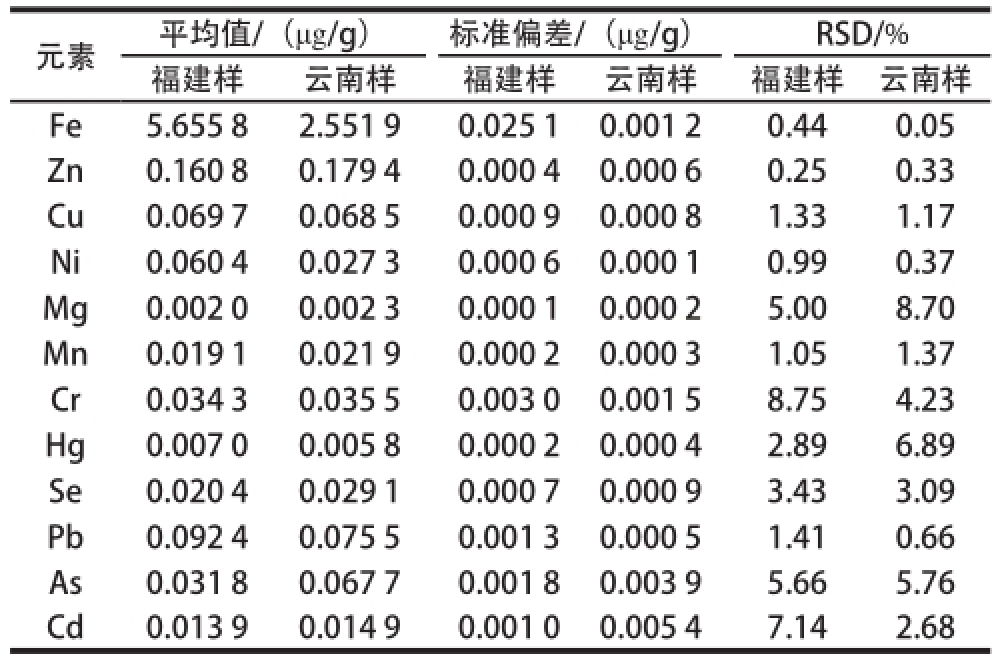
由表6可知,福建样12 种元素的RSD(n=6)的范围在0.25%~8.75%之间,云南样12 种元素的RSD(n=6)的范围在0.05%~8.70%之间,表明实验的精密度良好。
2.5 回收率
表7 加标回收实验结果
Table 7 Results of spiked recovery experiments
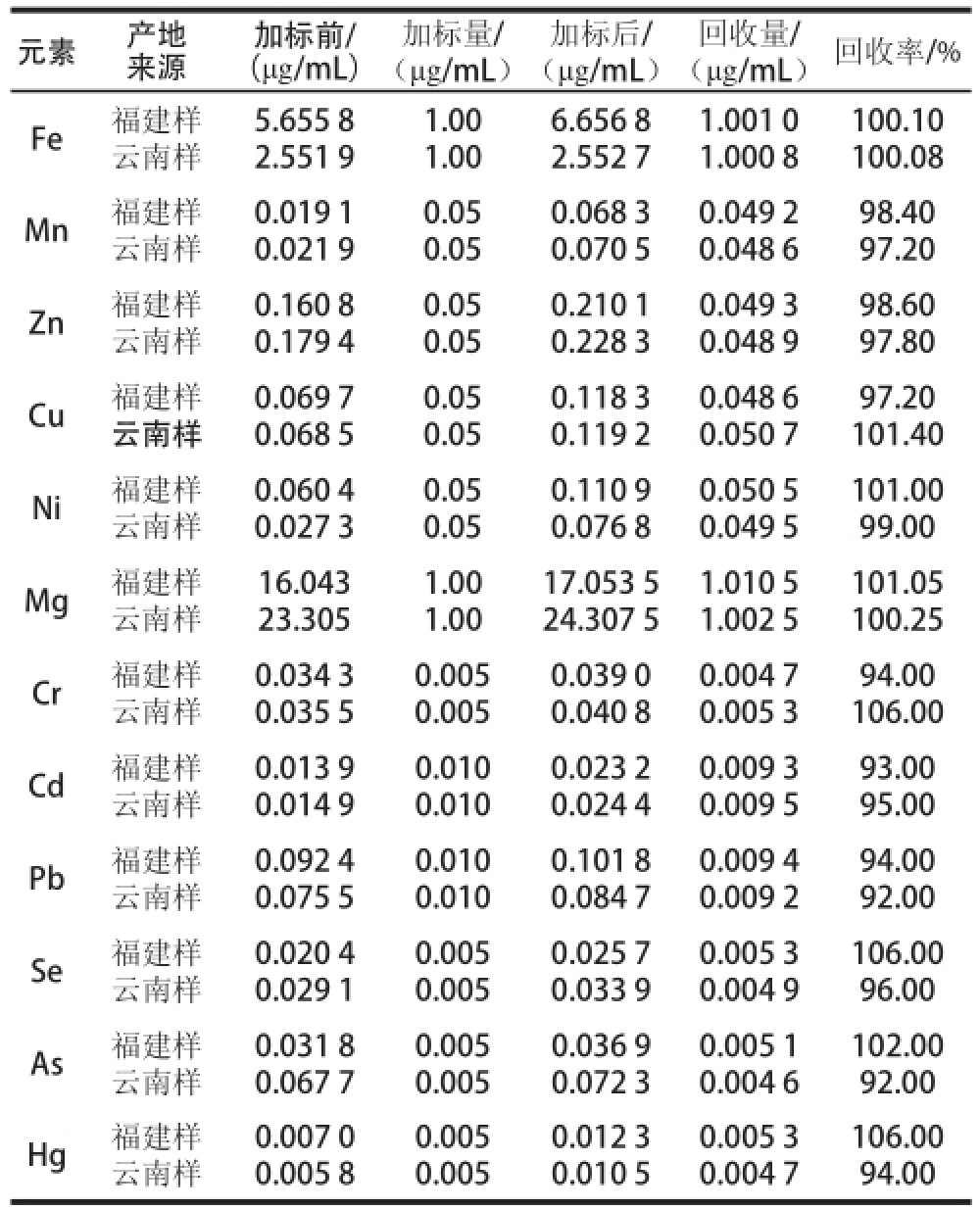
由表7可知,方法回收率在92%~106%之间,可见实验方法的可靠性较高。
由以上结果可以看出,2 种紫山药中12 种元素的回收率在92.00%~106.00%之间,12 种元素的RSD在10%以下,由此可见仪器的精密度良好,分析结果可靠准确性高。
2.6 紫山药中矿质元素的含质
表8 紫山药中Mg、Fe、Zn、Mn、Cu、Ni的含量
Tab Dioscorea allaattaa L. tubers
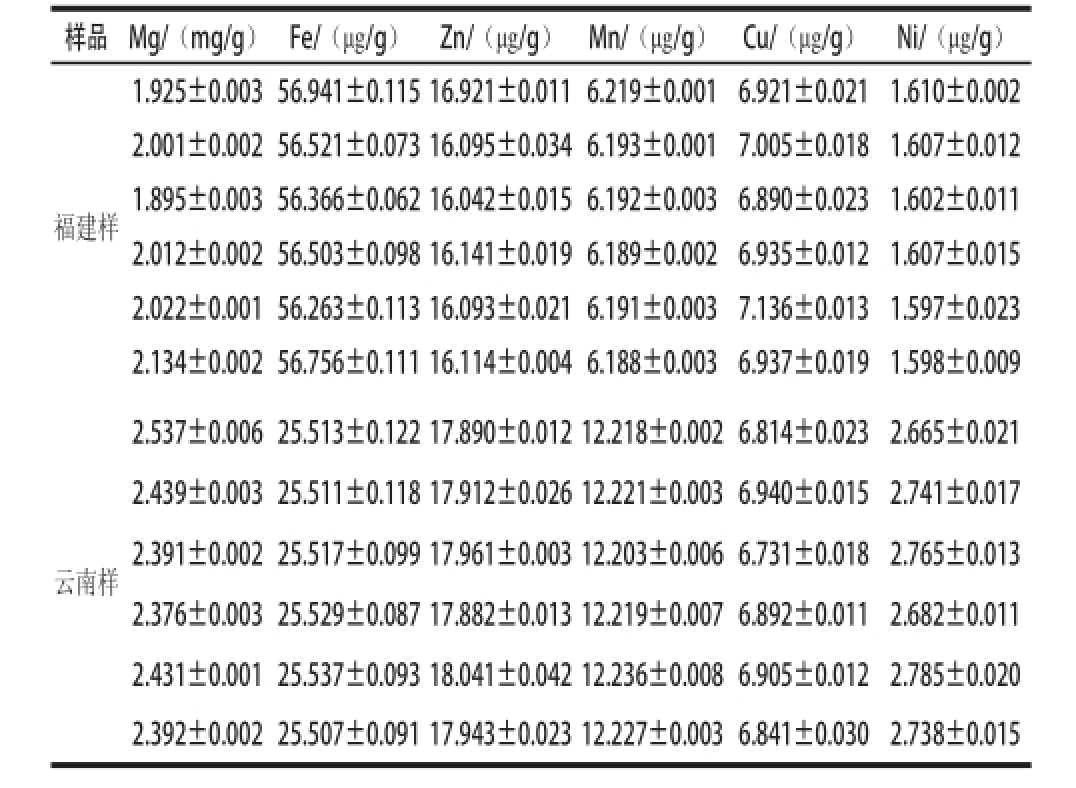
样品Mg/(mg/g)Fe/(μg/g)Zn/(μg/g)Mn/(μg/g)Cu/(μg/g)Ni/(μg/g)福建样1.925±0.00356.941±0.11516.921±0.0116.219±0.0016.921±0.0211.610±0.002 2.001±0.00256.521±0.07316.095±0.0346.193±0.0017.005±0.0181.607±0.012 1.895±0.00356.366±0.06216.042±0.0156.192±0.0036.890±0.0231.602±0.011 2.012±0.00256.503±0.09816.141±0.0196.189±0.0026.935±0.0121.607±0.015 2.022±0.00156.263±0.11316.093±0.0216.191±0.0037.136±0.0131.597±0.023 2.134±0.00256.756±0.11116.114±0.0046.188±0.0036.937±0.0191.598±0.009云南样2.537±0.00625.513±0.12217.890±0.01212.218±0.0026.814±0.0232.665±0.021 2.439±0.00325.511±0.11817.912±0.02612.221±0.0036.940±0.0152.741±0.017 2.391±0.00225.517±0.09917.961±0.00312.203±0.0066.731±0.0182.765±0.013 2.376±0.00325.529±0.08717.882±0.01312.219±0.0076.892±0.0112.682±0.011 2.431±0.00125.537±0.09318.041±0.04212.236±0.0086.905±0.0122.785±0.020 2.392±0.00225.507±0.09117.943±0.02312.227±0.0036.841±0.0302.738±0.015
表9 紫山 药中Cr、Hg、Pb、As、Cd、 Se的含量
Table 9 The contents of Cr, Hg, Pb, As, Cd and Se in Dioscorea allaattaa L. tubeerrssμg/g
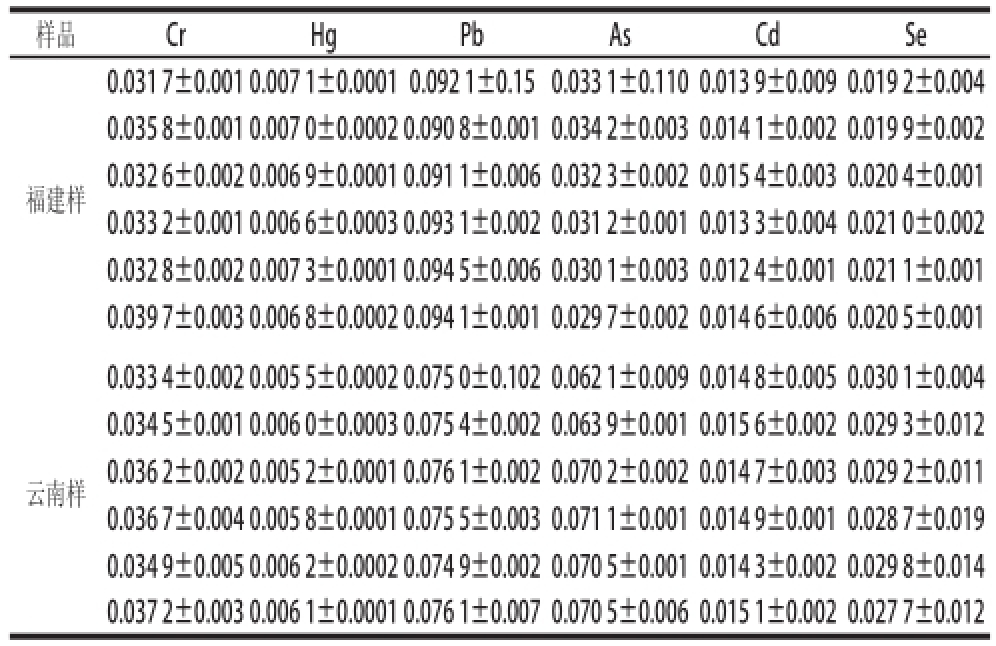
样品CrHgPbAsCdSe福建样0.031 7±0.0010.007 1±0.00010.092 1±0.150.033 1±0.1100.013 9±0.0090.019 2±0.004 0.035 8±0.0010.007 0±0.00020.090 8±0.0010.034 2±0.0030.014 1±0.0020.019 9±0.002 0.032 6±0.0020.006 9±0.00010.091 1±0.0060.032 3±0.0020.015 4±0.0030.020 4±0.001 0.033 2±0.0010.006 6±0.00030.093 1±0.0020.031 2±0.0010.013 3±0.0040.021 0±0.002 0.032 8±0.0020.007 3±0.00010.094 5±0.0060.030 1±0.0030.012 4±0.0010.021 1±0.001 0.039 7±0.0030.006 8±0.00020.094 1±0.0010.029 7±0.0020.014 6±0.0060.020 5±0.001云南样0.033 4±0.0020.005 5±0.00020.075 0±0.1020.062 1±0.0090.014 8±0.0050.030 1±0.004 0.034 5±0.0010.006 0±0.00030.075 4±0.0020.063 9±0.0010.015 6±0.0020.029 3±0.012 0.036 2±0.0020.005 2±0.00010.076 1±0.0020.070 2±0.0020.014 7±0.0030.029 2±0.011 0.036 7±0.0040.005 8±0.00010.075 5±0.0030.071 1±0.0010.014 9±0.0010.028 7±0.019 0.034 9±0.0050.006 2±0.00020.074 9±0.0020.070 5±0.0010.014 3±0.0020.029 8±0.014 0.037 2±0.0030.006 1±0.00010.076 1±0.0070.070 5±0.0060.015 1±0.0020.027 7±0.012
由表8、9可看出,供试的2 种紫山药中矿质元素含质丰富。福建样中矿质元素含质高低比较是:Mg>Fe>Zn>Cu>Mn>Ni>Cr,重金属元素含质高低比较为:Pb>Cr>As>Se>Cd>Hg;云南样中矿质元素含质高低比较:Mg>Fe>Zn>Mn>Cu>Ni>Cr,重金属元素含质高低比较:Pb>As>Cr>Se>Cd>Hg;福建样中Fe元素含质明显高于云南样,Mn含质约是云南样中Mn含质的1/2,Mg、Zn、Ni、Cr含质低于云南样,Cu含质与云南样基本相同;福建样中Pb、Hg含质稍高于云南样,Cd和Se含质略低于云南样,福建样中的As含质为云南样1/2,福建样和云南样中的Cr含质相近;供试的2 种紫山药中矿质元素种类多,含质丰富。不仅富含Mg、Fe、Zn之外,还含有对人体有益的Se元素,重金属中除了Ni元素,其他重金属(Cr、Pb、As、Cd、Hg)的含质均符合食品安全国家标准食品中污染物限质 [18]。
本实验通过采用HF-HNO 3(3∶5,V/V)混酸作为消化体系,普通酸电热板湿法消解样品,用火焰AAS法测定紫山药块根中7 种微质元素的含质,方法快速简便、试剂用质少、环境污染少、方法精密度高、重复性好,准确度好,适用于同类物质中微质元素的测定 [19-20]。用石墨炉AAS法测定紫山药中5 种重金属元素含质,优点在于只要样品均匀,不管是溶液、乳浊液还是悬浮液均可直接进样测定 [21-23]。
据报道 [24-29],Fe、Mn、Zn、Cu是人体及植物生长必需的矿质元素,这些矿质元素对生物免疫功能的维护、新陈代谢等生命活动起着重要作用。实验所测2 种紫山药的4 种矿质元素含质普遍较高,都是人体所必需的,可知经常食用紫山药,可补充机体中这几类矿质元素。从紫山药中的微质元素的含质可以看出,所检的2 种紫山药的品质整体较好,福建武平紫山药中Fe、Ni、Cd的含量相对较高,云南红河州紫山药样Zn、Se含量较高。从安全性方面来分析,重金属在人体内能和蛋白质及各种酶发生强烈的相互作用,使它们失去活性,也可能在人体的某些器官中富集,如果超过人体所能耐受的限度,会造成人体急性中毒、亚急性中毒、慢性中毒等,对人体会造成很大的危害。2 种紫山药中重金属元素除了Ni元素之外,其他重金属(Cr、Pb、As、Cd、Hg)的含质均符合食品安全国家标准食品中污染物限质和无公害蔬菜国家标准中的限质标准 [30]。
参考文献:
[1] 徐成基. 中国薯蓣资源[M]. 成都: 四川科技出版社, 2000: 135-138.
[2] 李婷婷. 紫山药的营养价值及开发前景[J]. 现代农村科技,2013(22): 77-78.
[3] 于东, 林跃伟, 陈桂星, 等. 紫山药营养成分分析研究[J]. 营养学报,2010, 32(2): 84-86.
[4] 曾哲灵, 傅婧, 彭超. 紫山药色素提取工艺研究[J]. 食品工业科技,2011, 32(3): 229-231.
[5] 王哲, 徐皓. 不同产地紫山药中花色苷含量分析[J]. 北方园艺,2013(3): 49-51.
[6] 刘庞源, 宋曙辉, 张宝海. 紫山药种质资源及其利用研究[J]. 北方园艺, 2011(23): 55-56.
[7] 王蕊. 山药的营养保健功能与贮藏加工技术[J]. 江苏食品与发酵,2006(3): 4-36.
[8] 蔡金辉, 严渐子, 黄晓辉, 等. 山药品种资源的分类研究[J]. 江西农业大学学报, 1999(21): 44-45.
[9] 赵冬兰, 唐君, 刘靖, 等. 紫山药的引种与标准化栽培技术初探[J].江西农业学报, 2009(2): 45-48; 51.
[10] 杨永庆. 红紫山药[J]. 农村百事通, 2006(18): 31.
[11] 周燕琼, 赵昶灵, 李云, 等. 云南紫薯蓣块根紫色素化学本质和含量的初步研究[J]. 江苏农业科学, 2010(4): 183-185.
[12] 徐恒戬, 李翠香, 巩旭东. 不同细毛山药品种矿质元素含量的研究[J].作物杂志, 2011(6): 63-67.
[13] 张虹, 白红丽, 王宝森, 等. 云南红河紫山药与白山药中微量元素的比较分析[J]. 江苏农业科学, 2009(4): 164-165.
[14] 姜洪波. 原子吸收光谱法测定微量元素的发展及展望[J]. 绥化师专学报, 2003, 23(3): 96-97.
[15] 黄志伟, 黎中良, 韦庆敏. 微波消解-火焰原子吸收光谱法测定紫菜中八种微量元素[J]. 广东微量元素科学, 2007, 14(1): 40-44.
[16] 肖谷清. 微波消解-原子吸收光谱法测定茶叶和栽培土壤中的微量元素[J]. 光谱实验室, 2006, 23(3): 493-496.
[17] 王宝森, 刘贵阳, 刘卫, 等. 不同消解方法对原子吸收光谱法测定三七中铅含量的影响[J]. 江苏农业科学, 2012, 40(5): 273-275.
[18] GB 2762—2012 食品中污染物限量[S].
[19] 成娟, 胡久梅, 李婧, 等. 火焰原子吸收光谱法测定山药中微量元素含量[J]. 中国实验方剂学杂志, 2012, 18(24): 154-156.
[20] 何志鹏, 吴琦, 韩婷. 温县铁棍山药中微量元素的测定[J]. 微量元素与健康研究, 2013(4): 22-23.
[21] 刘凤娇. 原子吸收光谱法在农产品重金属检测中的应用[J]. 现代农业科技, 2014(17): 318-319.
[22] 曹珺, 赵丽娇, 钟儒刚. 原子吸收光谱法测定食品中重金属含量的研究进展[J]. 食品科学, 2012, 33(7): 304-309.
[23] 张峰, 仇农学. 原子吸收光谱法测定苹果中重金属元素[J]. 食品工业科技, 2008, 29(12): 230-233.
[24] 牛芸民, 杨天林. 若干重要微量金属元素的生物化学功能及其与人体健康的关系[J]. 微量元素与健康研究, 2014, 31(2): 78-80.
[25] 姚蕾, 王晓平. 关注保健食品中的微量元素[J]. 食品研究与开发,2014, 35(5): 124-127.
[26] 党娅, 刘水英. 汉中绿茶中6 种矿质元素含量及其溶出特性[J]. 食品科学, 2014, 35(16): 170-174. doi: 10.7506/spkx1002-6630-201416033.[27] 胡丽娜. 微量元素对植物的作用[J]. 现代农业, 2014(7): 25.
[28] 秦俊法. 试谈中国特色的现代微量元素研究[J]. 广东微量元素科学,2014, 21(10): 30-35.
[29] 董国力. 微量元素铁、锌、碘、硒、氟与人体健康的相关性探究[J].中国当代医药, 2013(6): 65-67.
[30] GB/T 18407.1—2001 农产品安全质量无公害蔬菜产地环境要求[S].北京: 中国标准出版社, 2001: 137-140.
Determination of Mineral Elements in Dioscorea alata L. Tubers by Atomic Absorption Spectrometry with Wet Digestion
XU Hao, LIU Shuiying
(School of Biological Science and Engineering, Shaanxi University of Technology, Hanzhong 723000, China)
Abstract:The contents of 12 mineral elements in Dioscorea alata L. tubers from Wuping county of Fujian province and Honghe prefecture of Yunnan province were analyzed by atomic absorption spectrometry (AAS) after wet digestion. The results showed that the AAS method was a simple and f ast method that provided accurate measurement of mineral elements in Dioscorea alata L. tubers with recoveries ranging from 92.00% to 106.00% and relative standard deviation below 10%. The tested samples were found to be rich y in Mg, Fe and Zn as well as Se, which is beneficial to the human body. Except for Ni, the contents of all heavy metals includ ing Cr, Pb, As, Cd, and Hg are in line with the national food safety standards for the maximum limits of contaminants in foods.
Key words:Dioscorea alata L.; wet digestion; atomic absorption spectrometry; mineral elements
中图分类号:TS207.3
文献标志码:A
文章编号:1002-6630(2015)16-0192-05
doi:10.7506/spkx1002-6630-201516035
收稿日期:2014-12-03
基金项目:陕西省教育厅省级重点实验室项目(14JS018)
作者简介:徐皓(1972—),女,副教授,硕士,研究方向为植物资源开发与利用。E-mail:xhxbdx@126.com