肖 雄,彭 梅,杨 娟*
(贵州省、中国科学院天然产物化学重点实验室,贵州 贵阳 550002)
摘 要:以土党参多糖( Campanumoea javanica polysaccharide, CJP)和氯化铁( FeCl 3)为底物合成土党参多糖铁配合物( CJP-Fe 3+)。采用邻菲罗啉分光光度法测定配合物中铁含量,分析配合物的理化性质、稳定性和还原性,通过红外光谱法对其结构进行表征。结果表明:实验制备的 CJP-Fe 3+为红棕色无定型粉末,铁含量达到 22.81%;定性鉴定结果表明 CJP-Fe 3+中不存在游离的 Fe 3+,稳定性实验结果显示 CJP与 Fe 3+形成了稳定的配合物,在空气中不易分解。 CJP-Fe 3+在 pH 3~ 12范围内可以稳定存在,在此酸碱度范围内配合物结构不会被破坏。 CJP-Fe 3+有望被开发为新型的补铁剂。
关键词:土党参多糖铁配合物;理化性质;补铁剂
土党参为桔梗科金钱豹属植物金钱豹(Campanumoea javanica Bl. subsp. japonica( Makino) Hong),民间以其根入药,常用来炖鸡、炖瘦肉等,具有补气、止血、通乳等作用 [1]。土党参多糖(Campanumoea javanica polysaccharide, CJP)由本课题组从土党参根中提取得到,在土党参中含量丰富且具有多种生物活性 [2-5]。近年来不少学者利用生物多糖与铁配合生成多糖铁复合物,作为补铁剂来治疗缺铁性贫血症。许多以中药或食品所含多糖作为配体的多糖铁复合物如当归多糖铁 [6]、香菇多糖铁 [7]、玉竹多糖铁 [8]、茶叶多糖铁 [9]、孔石莼多糖铁 [10]等见于报道。与传统的补铁剂相比,多糖铁配合物具有稳定的高水溶性,能以分子形式被吸收,吸收率与硫酸亚铁相当。无铁离子存在,对胃肠黏膜无损害,补铁剂在十二指肠被吸收且呈稳定的可溶状态。多糖铁具有很强的还原性,可被体内还原性物质(如 VC等)还原成 Fe 2+吸收利用,符合理想补铁剂的特点 [11-16]。多糖铁复合物具有很好的临床疗效 ,且不良反应少 [17-20]。本实验用土党参多糖与氯化铁( FeCl 3)合成了土党参多糖铁配合物,分析了其含铁量、稳定性、理化性质,用红外光谱初步分析了土党参多糖铁配合物的结构特点,为土党参多糖铁配合物作为新型补铁剂的开发奠定基础。
1.1材料与试剂
土党参多糖( CJP)由本课题组从桔梗科金钱豹属植物金钱豹(Campanumoea javanica) Bl.的根中提取得到。糖含量≥ 95%,分子质量 2 900 D,为β -(2→1)-果聚糖。
透析袋(截留分子质量 1 000 D) 上海绿鸟科技发展有限公司; FeCl 3、 K 4 [Fe(CN) 6 ]、 (NH 4 ) 2 Fe(SO 4 ) 2· 6H 2 O、柠檬酸钠、 NaOH、无水乙醇、邻菲罗啉、抗坏血酸、盐酸羟胺等为国产分析纯。
1.2仪器与设备
BUCHI-R220旋转蒸发仪 美国 GE公司; DZF-6021真空干燥箱 上海精宏实验设备有限公司; C-MAG HS7磁力加热搅拌器 德国 IKA公司; AG285电子分析天平 瑞士 Mettler-Toledo公司; TDL-40C低速台式离心机 上海安亭科学仪器厂; 8453型紫外 -可见分光光度计 美国惠普公司; FT-IR Vector-22傅里叶红外光谱仪 德国 Bruker公司。
1.3方法
1.3.1土党参多糖铁配合物的制备 [21]
取 100 mg干燥土党参多糖( CJP)、 500 mg柠檬酸钠,混合加入到 100 mL反应瓶中,加 60 mL蒸馏水溶解,在 70℃水浴中持续搅拌,同时缓缓滴加质量分数 20%的 NaOH溶液和 2 mol/L的 FeCl 3溶液,控制二者的滴速并不断检测反应体系的 pH值,使 pH值始终维持在 8.0~ 9.0左右。当反应液中刚好有不溶的红棕色沉淀生成,立即停止滴加 FeCl 3和 NaOH溶液,继续搅拌反应 1 h后趁热 4 000 r/min离心 15 min,收集红棕色的上清液,加 3倍体积的无水乙醇搅拌均匀后,静置 24 h。离心收集沉淀并用蒸馏水溶解,加入到截留分子质量为 1 000 D的透析袋中,流水透析 24 h后再用蒸馏水透析 24 h,减压浓缩, 60℃真空干燥后得红褐色的土党参多糖铁配合物( CJP-Fe 3+)。
1.3.2 CJP-Fe 3+中铁含量的测定
采用邻菲罗啉比色法对 CJP-Fe 3+中铁含量进行测定 [22]。精密称取 0.702 3 g (NH 4 ) 2 Fe(SO 4 ) 2· 6H 2 O用少量纯水溶解,加 3.0 mL HCl,蒸馏水定容至 1.0 L,得 100 mg/L的 Fe 2+溶液,冷藏备用。取 10 mL该溶液定容至 100 mL,配制成 10 mg/L的标准 Fe 2+溶液(现配现用)。
铁含量标准曲线的绘制:精密量取 0.4、 0.8、 1.2、 1.6、 2.0、 2.5、 3.0 mL Fe 2+标准溶液,加入 2.0 mL 10%抗坏血酸溶液和 2.5 mL 0.1%的邻菲罗啉溶液,用蒸馏水稀释至 10 mL,混合均匀后在 37℃反应 10 min,以蒸馏水加试剂溶液为空白,在 510 nm波长处测定吸光度,以吸光度为纵坐标, Fe 2+的质量浓度为横坐标,在软件上做出标准曲线。
CJP-Fe 3+中铁含量的测定:精密称取 3份 CJP-Fe 3+样品 20.0 mg置于 25 mL(V 1)容量瓶中,用蒸馏水溶解,定容至刻度,量取样品溶液 1.0 mL(V)至带刻度试管中,加入 10%抗坏血酸溶液 2.0 mL和 0.1%的邻菲罗啉溶液 2.5 mL,用蒸馏水定容至 10 mL(V 2),混合均匀后 37℃静置 1.0 h,然后在 510 nm波长处测定样品溶液吸光度,将结果代入铁含量标准曲线,计算出 CJP-Fe 2+中 Fe 2+的质量浓度ρ( mg/mL),按照下式计算 CJP-Fe 3+中铁含量(S)。
式中:m为 CJP-Fe 3+样品的质量 /mg。
1.3.3 CJP-Fe 3+的结构分析
红外光谱分析:采用 KBr压片法,将完全干燥的 CJP-Fe 3+样品与 KBr按照 1∶100(m /m)的比例混合,研磨成粉末状后压片,于红外光谱仪上对样品进行扫描,以空气为空白吸收,扫描范围为 4 000~ 400 cm -1。
1.3.4 CJP-Fe 3+的定性鉴定
CJP-Fe 3+是在碱性条件下由土党参多糖和 FeCl 3合成制备的,在此条件下, Fe(OH) 3的生成是难以避免的,为了进一步确定生成的红棕色粉末是多糖铁配合物而非 Fe(OH) 3沉淀,参考 2010版《中华人民共和国药典(二部)》 [23]中高价铁盐的鉴别方法,将合成得到的 CJP-Fe 3+和 Fe(OH) 3进行定性比较。
CJP-Fe 3+溶液的配制:称取干燥的红棕色样品粉末适量,加 50 mL蒸馏水充分溶解,即得到 CJP-Fe 3+溶液。
Fe(OH) 3溶胶的制备:将饱和 FeCl 3溶液滴加到 50 mL沸水中,直至溶液变为红褐色,得到 Fe(OH) 3溶胶。
分别量取 CJP-Fe 3+溶液和 Fe(OH) 3溶胶 2 mL于试管中,观察两种溶液是否有丁达尔现象;加入 3倍体积 95%乙醇,观察是否有醇沉现象;分别在两支试管中加入 NaOH、 K 4 [Fe(CN) 6 ]、 KSCN溶液,观察是否有沉淀产生。
1.3.5 CJP-Fe 3+的稳定性实验
将透析除盐后的 CJP-Fe 3+溶于水,观察加入 K 4 [Fe(CN) 6 ]后,水浴加热至沸腾过程中, CJP-Fe 3+溶液的颜色变化。
1.3.6 CJP-Fe 3+的水解实验
配制 0.01 mg/mL的 CJP-Fe 3+溶液,用 NaOH和 HCl调节溶液的 pH值,观察 CJP-Fe 3+溶液变化情况。
1.3.7 CJP-Fe 3+的还原性实验
采用邻菲罗啉比色法对 CJP-Fe 3+进行还原性实验。配制 Fe 3+浓度为 1.0 mmol/L的 CJP-Fe 3+溶液 50 mL,分别量取 CJP-Fe 3+溶液 5.0 mL于 8个 50 mL的容量瓶里,分别加 NaOH溶液和 HCl溶液,使溶液的 pH值分别为 1、 2、 3、 4、 5、 6、 7、 8,然后分别依次加入 10%抗坏血酸 2.0 mL、 0.1%邻菲罗啉 3.0 mL,定容至刻度,恒温 37℃水浴还原,然后每隔 0.5 h取不同 pH值条件下的反应液 5.0 mL,在 510 nm波长处测定吸光度,以不加 CJP-Fe 3+溶液为空白组。
2.1 CJP-Fe 3+中的铁含量
以 Fe 2+的质量浓度( mg/mL)为横坐标,吸光度(A 510 nm)为纵坐标,得到标准曲线的回归方程y= 197.93x- 0.003 8(R 2= 0.999 6)。在实验所设定的 Fe 2+质量浓度范围内线性关系良好,根据铁含量计算公式,平行 3次实验,得到样品的平均铁含量为 22.81%。结果表明邻菲罗啉比色法测定 CJP-Fe 3+中的铁含量具有操作简单、结果稳定、误差小的优点。
2.2 CJP-Fe 3+结构分析结果
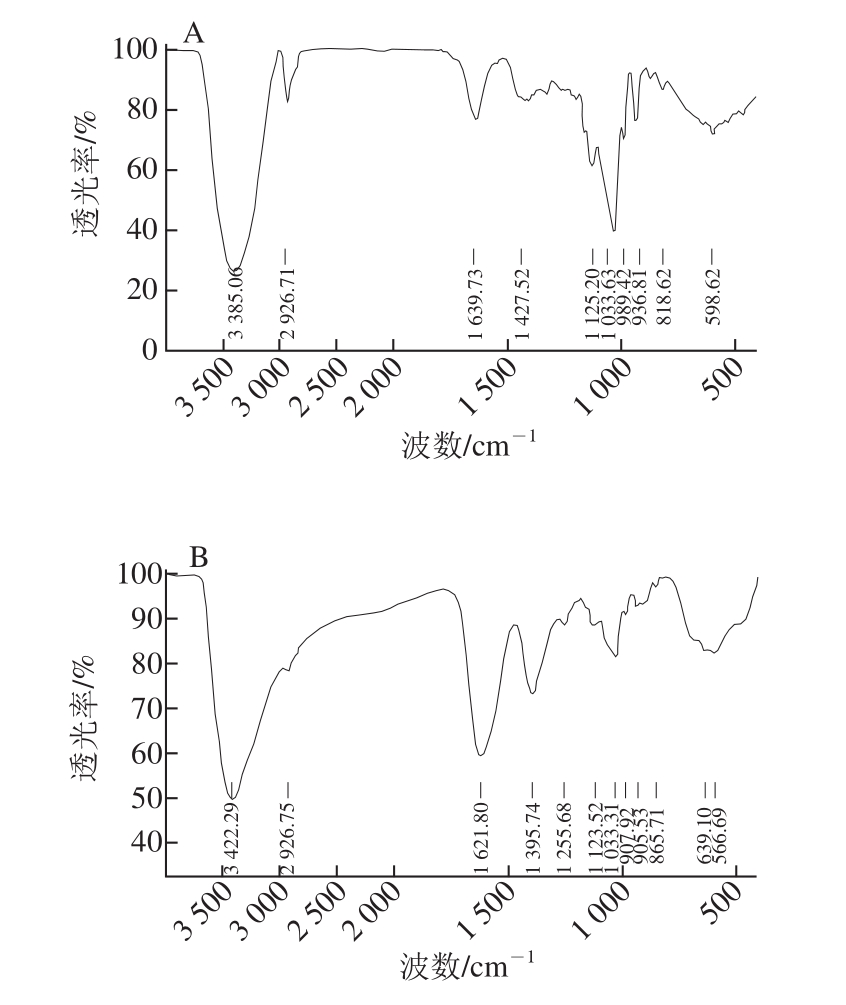
图1 CJP(A)和CJP--ee
3+(B)红外光谱图
Fig.1 IR spectra of CJP (A) and CJP-Fe
3+(B)
对 CJP与 CJP-Fe 3+的红外光谱进行比较。如图 1所示, CJP-Fe 3+在 865 cm -1和 639 cm -1处的特征吸收峰与文献 [24]报道的β -FeOOH的特征吸收峰数据一致,说明 CJP-Fe 3+中铁核是聚合的β -FeOOH结构。 1 622 cm -1处为多糖内 H— OH的吸收峰,此处的吸收峰明显增强,说明多糖的— OH参与了络合反应。在 1 033 cm -1处的 C— O— C伸缩振动及指纹区 900~ 600 cm -1范围内的峰形发生了变化,是多糖与铁形成配合物所引起的。土党参多糖与金属离子络合并没有使多糖的结构发生改变,保留了多糖原来的特征吸收峰, 3 422 cm -1处是多糖分子中 O— H的伸缩振动吸收峰, 2 926 cm -1处是多糖分子中 C— H键 [25]。红外光谱图显示,土党参多糖与 FeCl 3反应,形成了 CJP-Fe 3+。
2.3 CJP-Fe 3+的定性鉴定结果
观察结果显示,合成所得产物是一种土党参多糖与铁的络合物,而非 Fe(OH) 3沉淀,定性鉴定结果见表 1。 CJP-Fe 3+溶液与 Fe(OH) 3溶胶的定性鉴定实验现象有很大的区别, CJP-Fe 3+溶液中没有检测到游离的 Fe 3+,而是生成了稳定的配合物,说明 CJP-Fe 3+的结构修饰是成功的。定性鉴定实验结果充分说明了 CJP-Fe 3+和 Fe(OH) 3是完全不同的两种物质。
表1 CJP--Fe
3+定性鉴定实验结果
Table1 Qualitative identification of CJP-Fe
3+

项目CJP-Fe 3+溶液Fe(OH) 3溶胶外观颜色红棕色暗黄色丁达尔现象有有加入3 倍体积95%乙醇有醇沉现象无醇沉现象加入NaOH溶液无变化红棕色沉淀加入KSCN溶液无变化溶液变为血红色加入K 4[Fe(CN) 6]溶液无变化蓝色沉淀
2.4 CJP-Fe 3+的稳定性
CJP-Fe 3+为红棕色无定形粉末,易在水中溶解,而不溶于一般有机溶剂。透析除盐后的 CJP-Fe 3+样品溶于蒸馏水中,用 K 4 [Fe(CN) 6 ]对其水溶液进行检测,结果未出现 Fe 3+的特殊反应现象,说明 CJP-Fe 3+形成了稳定的多糖铁配合物,没有游离的 Fe 3+存在,并且将 CJP-Fe 3+粉末长期(> 48 h)放置空气中,用 K 4 [Fe(CN) 6 ]对其水溶液进行检测,也未出现 Fe 3+的特殊反应现象,说明 CJP-Fe 3+形成了稳定的多糖铁配合物。
2.5 CJP-Fe 3+的水解性
配制 0.01 mg/mL的 CJP-Fe 3+溶液,用 NaOH溶液和 HCl溶液调节溶液的 pH值。在 CJP-Fe 3+溶液中滴加 NaOH溶液,当溶液 pH值达到 12时,没有混浊现象发生,继续缓缓滴加 NaOH溶液,有红棕色沉淀生成,随着 pH值的不断增大,沉淀增多。向 CJP-Fe 3+溶液中滴加 HCl溶液,当溶液 pH值降到 3时,没有混浊现象发生,继续缓缓滴加 HCl溶液,溶液中就会有少量的沉淀生成,随着 pH值的不断减小,沉淀增多。结果表明, CJP-Fe 3+在 pH 3~ 12范围内可以稳定存在。在 pH≥ 12或者 pH≤ 3时, CJP-Fe 3+的结构被破坏,生成沉淀。
2.6 CJP-Fe 3+的还原性

图2 CJP--FFee
3+被抗坏血酸还原的反应曲线
Fig.2 Reduction curves of CJP-Fe
3+by ascorbic acid
采用邻菲罗啉比色法对 CJP-Fe 3+进行还原性实验,测得不同 pH值条件下各个时间点溶液的吸光度。由图 2可知, CJP-Fe 3+中的铁可以被抗坏血酸还原,而且A 510 nm在反应 0.5 h时即趋于稳定,说明 CJP-Fe 3+中的 Fe 3+在 0.5 h左右可以全部被还原成 Fe 2+。
以土党参多糖和 FeCl 3为底物合成土党参多糖铁配合物,铁含量可达到 22.81%。评价补铁剂生物利用度高低的主要指标之一是补铁剂在机体中铁的主要吸收部位——十二指肠(生理 pH 6~ 7)中是否可溶 [13]。 CJP-Fe 3+在 pH 3~ 12范围内均可溶且能够稳定存在,配合物结构不会被破坏,说明其具有较高的生物利用度。定性鉴定结果表明 CJP-Fe 3+中不存在游离的 Fe 3+。稳定性实验结果显示 CJP与 Fe 3+形成了稳定的配合物,在空气中不易分解,因而土党参多糖铁应有较好的生物利用度,有望成为具有开发前景的生物活性补铁剂。
参考文献:
[1] 何顺志, 徐文芬. 贵州中草药资源研究[M]. 贵阳∶ 贵州科技出版社, 2007∶ 653.
[2] 吴兰芳, 景永帅, 张振东, 等. 土党参多糖不同提取方法的比较研究[J].食品科学, 2012, 33(18)∶ 45-48.
[3] 杨小生, 张占军, 杨再昌, 等. 土党参多糖、衍生物及其制备方法和应用∶ 中国, 1648136[P]. 2005-08-03.
[4] 张振东, 杨娟, 吴兰芳, 等. 土党参多糖对小鼠脑缺血再灌注损伤的保护作用[J]. 中国药理学通报, 2011, 27(4)∶ 508-510.
[5] 彭梅, 张振东, 杨娟. 土党参多糖对小鼠耐缺氧能力的影响[J]. 中国老年学杂志, 2012, 32(6)∶ 1183-1185.
[6] 王凯平, 张玉, 戴立泉. 当归多糖铁理化性质的初步研究[J]. 中国中药杂志, 2006, 31(9)∶ 747-750.
[7] 任广明, 郭兴, 陈志新. 响应曲面分析法优化香菇多糖铁(Ⅲ)配合工艺研究[J]. 食品工业科技, 2014, 35(4)∶ 251-255.
[8] 许丽丽, 展晓日, 曾昭武, 等. 玉竹多糖铁的制备及其理化性质研究中[J]. 中国药学杂志, 2012, 47(5)∶ 331-334.
[9] TANG Minmin, WANG Dongfeng, HOU Yangfeng, et al. Preparation, characterization, bioavailability in vitro and in vivo of tea polysaccharides-iron complex[J]. European Food Research and Technology, 2013, 236(2)∶ 341-350.
[10] SHI Jinming, CHENG Cuilin, ZHAO Haitian, et al. In vivo antiradiation activities of the Ulva pertusa polysaccharides and polysaccharide-iron (III) complex[J]. International Journal of Biological Macromolecules, 2013, 60∶ 341-346.
[11] EICHBAUM Q, FORAN S, DZIK S. Is iron gluconate really safer than iron dextran?[J]. Blood, 2003, 101(9)∶ 3756-3757.
[12] ZHANG Zhongshan, WANG Xiaomei, HAN Zhiping, et al. Physicochemical properties and inhibition effect on iron deficiency anemia of a novel polysaccharide-iron complex (LPPC)[J]. Bioorganic Medicinal Chemistry Letters, 2012, 22(1)∶ 489-492.
[13] 张惠中. 口服补铁剂多糖铁复合物[J]. 中国药师, 2006, 9(8)∶756-757.
[14] 王耀莉, 史锁洪, 朱霖, 等. 多糖铁复合物治疗儿童缺铁性贫血[J].新药与临床, 1994, 13(4)∶ 251-252.
[15] 杨真, 岁海古. 缺铁性贫血及补铁剂研究进展[J]. 国外医学∶ 卫生学分册, 2006, 33(2)∶ 90-93.
[16] 孙丙政, 王云峰, 黄聪, 等. 口服补铁剂及多糖铁络合物的研究进展[J].微量元素与健康研究, 2009, 26(5)∶ 64-67.
[17] 甄学慧, 王义, 洪梅, 等. 多糖铁复合物(PIC)用于妊娠缺铁性贫血的疗效观察[J]. 中国妇幼保健, 2006, 20(21)∶ 2833-2834.
[18] 刘军, 廖敏. 老年人缺铁性贫血[J]. 应用预防医学, 2006, 12(4)∶252-253.
[19] 吴晓亮. 多糖铁复合物治疗成人缺铁性贫血的临床观察[J]. 中国实用医药, 2008, 3(12)∶ 72-74.
[20] 王关煜, 林善铁, 叶朝阳. 多糖铁复合物对肾性贫血肾功能衰竭液血液透析患者的补铁疗效与安全性观察[J]. 中华内科杂志, 2000, 39(4)∶ 380-383.
[21] 王花, 樊君, 汤春妮, 等. 大枣多糖铁复合物的制备及表征[J]. 中成药, 2009, 31(10)∶ 1584-1587.
[22] 戴立泉, 王凯平, 张玉, 等. 当归多糖铁的定性鉴别及其铁含量的初步研究[J]. 中国药师, 2005, 8(7)∶ 608-610.
[23] 国家药典委员会. 中华人民共和国药典(二部)[M]. 北京∶ 中国医药科技出版社, 2010∶ 附录57.
[24] MARSHALL P R, RUTHERFORD D. Physical investigations on colloidal iron-dextran complexes[J]. Journal of Colloid and Interface Science, 1971, 37(2)∶ 390-402.
[25] 张惟杰. 糖复合物生化研究技术[M]. 2版. 杭州∶ 浙江大学出版社, 1999∶ 194-198.
Preparation and Physicochemical Characterization of Campanumoea javanica Polysaccharides-Iron (Ⅲ) Complex
XIAO Xiong, PENG Mei, YANG Juan* (Key Laboratory of Chemistry for Natural Products of Guizhou Province and Chinese Academy of Sciences, Guiyang 550002, China)
Abstract: In this experiment, Campanumoea javanica polysaccharide-iron (Ⅲ ) complexes (CJP-Fe 3+ ) were synthesized with Campanumoea javanica polysaccharide and ferric chloride as substrates. The iron content of the complex was measuredby phenanthroline spectrophotometry and physiochemical properties, stability and reducing power were also investigated.Its structural characteristics were analyzed by infrared (IR) spectroscopy. The CJP-Fe 3+ complexes were obtained as a redbrown amorphous powder with an iron content of 22.81% . Qualitative identification experiments showed that there was nofree Fe 3+ detectedin CJP-Fe 3+ complexes. The complex was stable in the air and within a broad pH range from 3 to 12; thestructure of this complex in this pH range was not destroyed. Thus, CJP-Fe 3+ can be developed as a new iron supplementary.
Key words: Campanumoea javanica polysaccharides-Fe 3+ complex; physicochemical properties; iron supplementary
中图分类号: R284. 3
文献标志码: A 文章编号:1002-6630(2015)17-0013-04
文章编号:1002-6630(2015)17-0013-04
doi:10.7506/spkx1002-6630-201517003
收稿日期:2014-10-29
基金项目:国家自然科学基金地区科学基金项目(81160513)
作者简介:肖雄(1988—),男,硕士研究生,主要从事天然产物提取分离与活性研究。E-mail:382310002@qq.com
*通信作者:杨娟(1971—),女,研究员,博士,主要从事天然活性成分研究。E-mail:yangxz2002@126.com