罗春丽,王 林,李 杏,张子程,张久亮*
(华中农业大学食品科学技术学院,环境食品学教育部重点实验室,湖北 武汉 430070)
摘 要:目的:研究紫薯花青素的体外抗氧化作用,建立 H 2 O 2诱导 HepG2细胞氧化损伤模型,初步评 价紫薯花青素的抗氧化应激作用。方法:紫薯干粉经过提取、纯化制得紫薯花青素干粉,分别测定紫薯花青素的总还原力、对羟自由基(· OH)、超氧阴离子自由基( O 2 -·)的清除能力以及对大鼠红细胞溶血的保护作用。建立 H 2 O 2诱导 HepG2细胞氧化损伤模型,采用四甲基偶氮唑蓝( methyl thiazolyl tetrazolium, MTT)法检测不同质量浓度紫薯花青素对 HepG2细胞氧化损伤的保护作用。结果:紫薯花青素的还原力和 VC基本相当;紫薯花青素对· OH有很好的清除效果,在实验浓度范围内有明显的剂量 -效应关系;随紫薯花青素浓度的升高,对 O 2 -·的清除作用增强,呈现良好的量 -效关系,单位浓度的紫薯花青素对 O 2 -·的清除作 用比2,6-二叔丁基-4-甲基苯酚(butylated hydroxytoluene,BHT)效果好。不同质量浓度的紫薯花青素均可抑制 H 2 O 2诱导的大鼠红细胞溶血,且随着紫薯花青素质量浓度的升高,大鼠红细胞的溶血度降低,呈现良好的量 -效关系。 H 2 O 2诱导的 HepG2细胞氧化损伤模型中, 50~ 1 600μg /mL的紫薯花青素 均能够抑制 H 2 O 2引起的 HepG2细胞凋亡,当紫薯花青素质量浓度达到 800μg /mL时, HepG2细胞存活率为( 88.03± 7.48)%。结论:紫薯花青素具有良好的体外抗氧化作用,并对 H 2 O 2诱导 HepG2细胞氧化损伤具有明显的保护作用,研究初步揭示了紫薯花青素具有体外抗氧化作用。
关键词:紫薯花青素;抗氧化;自由基;氧化应激损伤; HepG2细胞
自由基是一类瞬时形成的含不成对电子的原子或功能基因。人体内的自由基既可以帮助传递维持生命的能量,也可被用来杀灭病菌和寄生虫,还能参与毒素排出,受控的自由基对人体是有益的。但当自由基在体内超过一定量时,则会给人体健康带来伤害,导致正常细胞和组织的损坏,从而引起多种慢性疾病,如心脏病、老年痴呆、恶性肿瘤等 [1]。
花青素是目前发现的安全、有效的自由基清除剂 [2],在自然界,花青素是一类广泛存在于植物中的水溶性天然色素,属类黄酮化合物 [3]。花青素是一种强效抗氧化剂,是药用价值很高的天然强效自由基清除剂,且具有良好的抗肿瘤、预防和治疗心血管疾病、抑菌等多种药用功能。因而,在医药、保健食品和化妆品等领域被广泛应用,是极具发展前景的天然植物色素 [4-5]。本实验采用鄂薯 8号为材料 [6],通过 AB-8大孔吸附树脂法富集紫薯花青素,体外测定紫薯花青素的还原力和对羟自由基(· OH)、超氧阴离子自由基( O 2 -·)两种自由基的清除作用,测定其对 H 2 O 2诱导大鼠红细胞氧化溶血的影响,并初步研究紫薯花青素对 H 2 O 2诱导 HepG2细胞损伤的保护作用,为将其开发成抗氧化、降血脂功能性食品奠定实验基础。
1.1材料、动物与试剂
鄂薯 8号干粉,由武汉普泽天食品有限公司提供。
SPF级雄性老年 Sprague-Dawley( SD)大鼠,体质量( 240± 20) g,购自湖北省实验动物研究中心(合格证号: SCXK(鄂) 2008-0005)。饲养条件:室温 25℃、相对湿度 50%~ 60%,以大鼠标准饲料适应性喂养 1周后,眼球取血,取血前 12 h断食。
HepG2人肝癌细胞 华中科技大学同济医学院药学院;四甲基偶氮唑蓝( methyl thiazolyl tetrazolium, MTT) 上海 Genview公司;胎牛血清 美国 Sigma公司; RPMI-1640培养基 美国 HyClone公司。
1.2仪器与设备
UV-102-02WF紫外 -可见分光光度计 日本 Shimadzu公司; ALPHA 1-4LD真空冷冻干燥机 德国 Marin Christ公司; TDL-5A台式离心机 上海菲恰尔公司; RE-52AA旋转蒸发器 上海亚荣生化仪器厂; TS100倒置显微镜 日本 Nikon公司; HF90 CO 2培养箱力康生物科技医疗集团。
1.3方法
1.3.1紫薯花青素的制备
1.3.1.1紫薯花青素的提取
紫薯花青素的提取流程如下:鄂薯 8号干粉→无水乙醇 -0.1 mol/L盐酸( 60∶40,V /V)提取→ 4 000 r/min离心 10 min→减压浓缩。
其中料液比为 1∶10(m /V), 60℃提取 30 min,经减压浓缩后得到紫薯花青素粗提物,备用 [4]。
1.3.1.2紫薯花青素的纯化
紫薯花青素的纯化流程如下:紫薯花青素粗提物→乙酸乙酯萃取→ AB-8大孔吸附树脂纯化 →减压浓缩→真空冷冻干燥。
先用 0.1% HCl冲洗大孔树脂柱 2~ 3个柱体积,将 1.3.1.1节所得紫薯花青素粗提物上柱纯化,洗脱液为无水乙醇 -缓冲液( 70∶30,V /V),洗脱过程中保持柱内 pH值为 3(以柠檬酸 -Na 2 HPO 4缓冲液保持 pH值),流速为 4 mL/min [1-2]。将冻干后紫薯花青素(紫薯花青素冻干粉)于- 20℃条件下保存备用。
1.3.1.3紫薯花青素含量的测定
参照 Hosseinian等 [7]的方法,取纯化后的紫薯花青素冻干粉 0.22 g两份,加入 pH 4.5的醋酸钠缓冲溶液或 pH 1.0的 KCl缓冲液 4 mL,摇匀,用紫外 -可见分光光度计分别在 520、 700 nm波长处测定吸光度 [8],以矢车菊素 -3-葡萄糖苷为当量,按照公式( 1)、( 2)计算紫薯花青素冻干粉中的花青素含量。
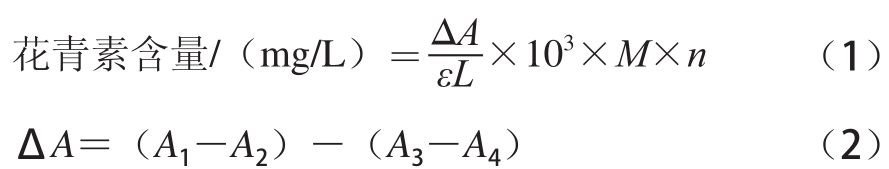
式中:A 1为 pH 1.0缓冲液中的样品在 520 nm波长处的吸光度;A 2为 pH 1.0缓冲液中的样品在 700 nm波长处的吸光度;A 3为 pH 4.5缓冲液中的样品在 520 nm波长处的吸光度;A 4为 pH 4.5缓冲液中的样品在 700 nm波长处的吸光度;L表示比色皿光路长度 /cm;ε为矢车菊素 -3-葡萄糖苷的摩尔吸光系数, 26 900 L/( mol· cm);M为矢车菊素 -3-葡萄糖苷的摩尔质量, 449.2 g/mol [9];n为稀释倍数。
最终结果换算为 1 g紫薯花青素冻干粉中含有花青素的量。
1.3.2紫薯花青素还原力的测定
取一定量的紫薯花青素冻干粉,以甲醇为溶剂配制质量浓度分别为 0.1、 0.3、 0.5、 0.7、 0.9 mg/mL的系列溶液(以矢车菊素 -3-葡萄糖苷计算当量计算得到浓度分别为 0.22、 0.67、 1.11、 1.56、 2.00 mmol/L);以 VC为对照品,同样以甲醇为溶剂配制质量浓度分别为 0.01、 0.03、 0.05、 0.07、 0.09 mg/mL的系列溶液(浓度分别为 0.57、 1.70、 2.84、 3.97、 5.11 mmol/L)。
分别移取上述不同质量浓度的 VC溶液 1 mL于 5个不同的离心管中,依次加入 2.5 mL 0.2 mol/L磷酸盐缓冲溶液( pH 6.6)、 2.5 mL质量分数 1%的 K 3 Fe(CN) 6溶液, 50℃水浴保温 20 min后,再加入 2.5 mL质量分数 10%的三氯乙酸溶液, 3 000 r/min离心 10 min,取 2.5 mL上清液,加入 2.5 mL蒸馏水和 0.5 mL质量分数 0.1%的 FeCl 3溶液,于 700 nm波长处测定反应体系的吸光度(以蒸馏水调零)。
分别移取上述各浓度的紫薯花青素样品 1 mL代替 VC,按照相同的步骤进行操作,在 700 nm波长处测定反应体系的吸光度 [10]。
1.3.3紫薯花青素对· OH的清除作用
根据 Smirnoff等 [11]的方法进行改进:取一定量的紫薯花青素冻干粉和 VC,以甲醇为溶剂配制质量浓度分别为 0.1、 0.5、 1.0、 1.5、 2.0、 3.0 mg/mL的紫薯花青素溶液和 VC溶液,以矢车菊素 -3-葡萄糖苷为当量计算得到紫薯花青素溶液的浓度分别为 0.22、 1.11、 2.22、 3.34、 4.45、 6.68 mmol/L; VC溶液的浓度分别为 0.57、 2.84、 5.68、 8.52、 11.36、 17.03 mmol/L。
取6 支试管,均加入20 mmol/L H 2 O 2 0.5 mL、8 mmol/L FeSO 4 0.6 mL、3 mmol/L水杨酸-乙醇溶液2 mL,以及不同质量浓度的紫薯花青素溶液2 mL,再加入0.5 mL 20 mmol/L H 2 O 2 启动整个反应。37 ℃反应30 min后流水冷却,加入0.9 mL蒸馏水,使体系总体积为6 mL,3 000 r/min离心10 min,在510 nm波长处测定吸光度(A 1 ) [2] 。对照组以VC替代紫薯花青素,操作同上。以浓度为横坐标,吸光度为纵坐标绘制曲线,按照式(3)计算样品的· OH清除率。
式中:A 0为以 2 mL蒸馏水代替紫薯花青素溶液的空白组吸光度;A 2为对照组的吸光度。
1.3.4 紫薯花青素对O 2 - ·的清除作用
取一定量的紫薯花青素冻干粉和 2,6-二叔丁基 -4-甲基苯酚( butylated hydroxytoluene, BHT),以甲醇为溶剂配制质量浓度分别为 0.1、 0.5、 1.0、 1.5、 2.0、 3.0 mg/mL的紫薯花青素溶液和 BHT溶液,以矢车菊素 -3-葡萄糖苷为当量计算得到紫薯花青素浓度分别为 0.22、 1.11、 2.22、 3.34、 4.45、 6.68 mmol/L; BHT溶液的浓度为 0.45、 2.27、 4.54、 6.81、 9.08、 13.61 mmol/L。
取 pH 8.2的 0.05 mol/L Tris-HCl缓冲溶液 4.5 mL,置于 25℃水浴中预热 20 min,分别加入 1 mL不同浓度的紫薯花青素溶液、 0.4 mL 25 mmol/L邻苯三酚溶液,混匀后将混合液放入 25℃水浴中反应 5 min,再加入 1 mL 8 mol/L HCl终止反应,用蒸馏水稀释 10倍。在 299 nm波长处测定吸光度(A 1),以等量的 BHT溶液代替紫薯花青素溶液作为对照品 [3,10,12],按照式( 4)计算样品的 O 2 -·清除率 [13]。
式中:A 0为以 1 mL蒸馏水代替不同浓度的紫薯花青素的空白组吸光度。
1.3.5紫薯花青素对 H 2 O 2诱导大鼠红细胞氧化溶血的影响
从 SD大鼠眼眶静脉丛取血,肝素抗凝, 3 000 r/min离心 10 min分离得红细胞,冷生理盐水洗涤红细胞 3次,制成质量分数 0.5%的大鼠红细胞悬浮液, 4℃条件下保存备用。
取 1 mL大鼠红细胞悬浮液,加入 0.2 mL不同质量浓度的紫薯花青素溶液、 0.1 mL 100 mmol/L H 2 O 2溶液混匀。在 37℃条件下温育 1 h,以生理盐水稀释 6倍, 3 000 r/min离心 10 min,取上清液,于 415 nm波长处比色测定吸光度 (A 1 )(以生理盐水调零) [14],按照式( 5)计算大鼠红细胞的溶血度。

式中:A 0为以等体积生理盐水代替样品溶液和 H 2 O 2溶液的正常对照组吸光度;A 2为以等体积生理盐水代替样品溶液的 H 2 O 2诱导对照组吸光度。
1.3.6紫薯花青素对 H 2 O 2诱导 HepG2细胞氧化损伤的保护作用
1.3.6.1 H 2 O 2诱导 HepG2细胞氧化损伤模型的建立
体外建立 H 2 O 2诱导 HepG2细胞氧化损伤模型,采用不同浓度的 H 2 O 2作用于 HepG2细胞相同时间,和同一浓度的 H 2 O 2作用于 HepG2细胞不同时间,四甲基偶氮唑蓝( methyl thiazolyl tetrazolium, MTT)法测定 H 2 O 2对 HepG2细胞的抑制率 [15-16]。
1.3.6.2紫薯花青素对 H 2 O 2诱导 HepG2细胞氧化损伤的保护作用
取处于对数生长期的 HepG2细胞稀释至细胞密度为 10 5个 /mL,接种于 96孔板中,每孔 100μL;细胞培养至贴壁后,吸出全部原培养液。实验组分别加入 100μL紫薯花青素质量浓度为 50、 100、 200、 400、 800、 1 600μg /mL的培养基,置于培养箱中培养 24 h,吸弃上清液,每孔加入 400μmol /L的 H 2 O 2 100μL,置于培养箱中孵育 2.5 h。培养 2.5 h后尽可能吸弃上清液,加入 200μL质量浓度为 0.5 mg/mL的 MTT, 37℃孵育 4 h后停止培养 [17],吸出上清液,每孔加入 150μL二甲基亚砜酶标仪振荡 10 min后于 490 nm波长处测定吸光度,每组做 5个复孔,重复 3次 [18-19]。另设:空白组不接种细胞但添加培养液;阴性对照组接种细胞但不加 H 2 O 2和其他药物处理;模型组接种细胞并加 H 2 O 2处理,但不加紫薯花青素溶液处理。其余操作步骤相同。按照公式( 6)、( 7)计算细胞存活率和细胞损伤率。

式中:A 0为空白组的吸光度;A 1为样品组的吸光度;A 2为阴性对照组的吸光度。
1.4数据处理
实验结果用
 表示,用
SAS统计软件进行t检验和方差分析。
表示,用
SAS统计软件进行t检验和方差分析。
2.1紫薯花青素含量
紫薯干粉经过含盐酸的乙醇溶液提取后得到紫薯花青素粗提物,利用乙酸乙酯萃取去除脂溶性成分,采用 AB-8大孔吸附树脂对紫薯花青素进行纯化和富集,浓缩冻干后制得紫薯花青素冻干粉。根据双波长法 [20]测定结果计算得到:紫薯花青素冻干粉中,总花青素的含量约为 312 mg/g(以矢车菊素 -3-葡萄糖苷为当量计算)。
2.2紫薯花青素的还原力

图1 紫薯花青素和VC的还原力
Fig.1 Reducing power of anthocyanins from purple sweet potato and vitamin C
众所周知, VC具有很好的抗氧化活性。如图 1所示,紫薯花青素具有一定的还原力,且随着浓度的增加,反应体系的吸光度增大,即紫薯花青素的还原能力增强,表现出良好的量 -效关系;此外,浓度相同的紫薯花青素和 VC吸光度大致相同,说明紫薯花青素的还原力和 VC基本一致。
2.3紫薯花青素清除· OH的效果
正常情况下,机体自身的抗氧化系统可以抵御氧化应激带来的损伤,以避免自由基攻击细胞,引起细胞死亡。但是若机体正常的抗氧化系统被破坏,失去了对自由基损伤和细胞氧化损伤的控制能力,将带来严重的后果。· OH被认为是毒性很强的自由基,可通过 Fe 2++ VC、 Fe 2++ H 2 O 2等反应产生,能诱导膜系统氧化损伤,对细胞有很强的毒害作用 [7]。紫薯花青素可以提供 H, H与· OH结合,形成稳定性较强的自由基或惰性化合物,进而清除体内过多的有害自由基。
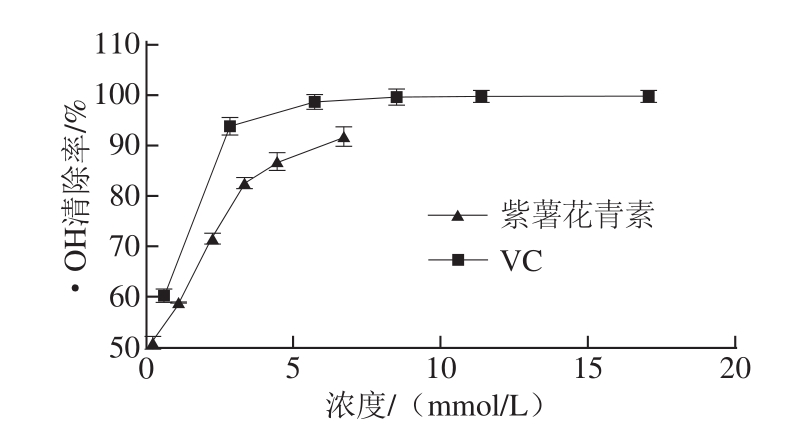
图2 不同浓度紫薯花青素对·OH的清除作用

Fig.2 Hydroxyl radical scavenging effect of different concentrations of anthocyanins from purple sweet potato
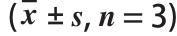
由图 2可知,以 VC为参照物,紫薯花青素对· OH有很好的清除效果,且随着浓度的增大,紫薯花青素对· OH的清除率逐渐增大,有明显的剂量 -效应关系。当反应体系对· OH的清除率为 90%时,对应的 VC的浓度为 2.61 mmol/L,而紫薯花青素的浓度为 5.67 mmol/L,且随着紫薯花青素浓度的增加,其对· OH的清除率逐渐增大。以上结果表明,紫薯花青素与 VC一样,都可以清除· OH,在实验设定的浓度范围内表现出剂量依赖性。
2.4紫薯花青素清除 O 2 - ·的效果
花青素强大的自由基清除能力来源于其分子中大量的酚羟基。研究表明,原花青素分子 B环的邻位酚羟基为主要的还原部位,在抗氧化反应过程中,邻位酚羟基作为 H供体可以捕获氧化过程中产生的 O 2 - ·,自身形成的自由基可以通过形成分子内氢键、半醌式自由基甚至邻苯醌等形式得以稳定,从而中断自由基链式反应。
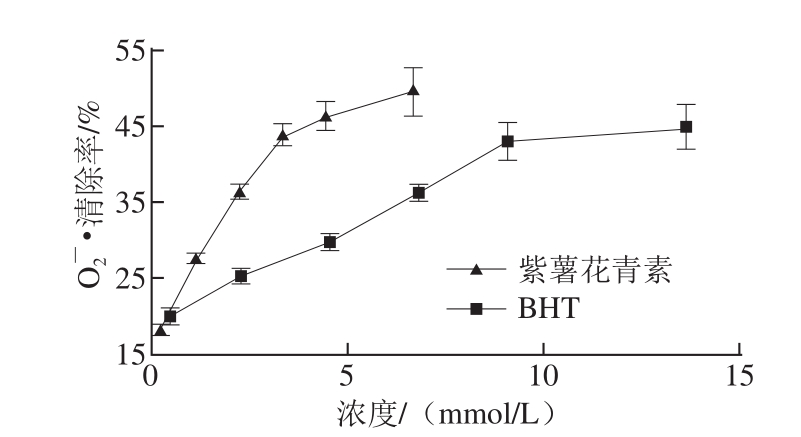
图3 不同浓度紫薯花青素对
 的清除作用(
的清除作用(
Fig.3 Superoxide anion radical scavenging effect of different concentrations of anthocyanins from purple sweet potato

BHT是公认的对 O 2 - ·具有良好清除作用的化合物。由图 3可知,在相同浓度下,紫薯花青素对 O 2 - ·的清除作用比 BHT更好,且随着紫薯花青素浓度的升高,对 O 2 - ·的清除作用增强,呈现良好的量 -效关系,当反应体系对 O 2 - ·的清除率为 45%时,对应的 BHT浓度为 13.61 mmol/L,而紫薯花青素的浓度为 4.45 mmol/L,由此可见,单位浓度的紫薯花青素对 O 2 - ·的清除作用比 BHT效果好。
2.5紫薯花青素对 H 2 O 2诱导大鼠红细胞氧化溶血的抑制作用
H 2 O 2可以氧化红细胞膜,导致血红蛋白逸出,从而导致其吸光度的增加。紫薯花青素上的羟基可以与 H 2 O 2结合,起到保护红细胞的作用,进而降低红细胞的溶血现象 [21-22]。
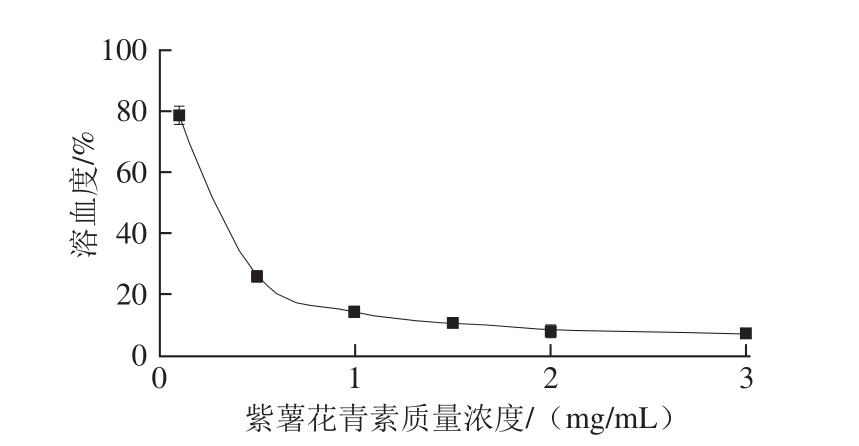
图4 紫薯花青素对H
2O
2诱导大鼠红细胞氧化溶血的影响
Fig.4 Protective effect of anthocyanins from purple sweet potato on red blood cell hemolysis induced by H
2O
2
由图 4可知,不同质量浓度的紫薯花青素均可抑制 H 2 O 2诱导的大鼠红细胞溶血,且随着紫薯花青素质量浓度的升高,大鼠红细胞的溶血度降低。当紫薯花青素的质量浓度为 3 mg/mL时, H 2 O 2诱导的大鼠红细胞溶血度降低到 7.41%,与 0.1 mg/mL质量浓度下大鼠红细胞溶血度 80.07%相比,有更好的抗溶血效果,呈现良好的量 -效关系。
2.6紫薯花青素对 H 2 O 2诱导的 HepG2细胞损伤的保护作用
2.6.1紫薯花青素对 HepG2细胞无毒剂量的确定
表1 紫薯花青素对HepG2细胞的毒性作用
TTaabbllee 11 EEffffeect of anthocyanins from purple sweet potato on the survival rate of HepG2 cells
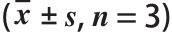

组别紫薯花青素质量浓度/(μg/mL)HepG2细胞存活率/%阴性对照组 94.17±7.78紫薯花青素组5092.80±4.22 10089.68±7.60 200100.01±3.32 400100.01±3.56 80099.68±4.61 1 60096.76±4.78
由表 1可知,各质量浓度的紫薯花青素对 HepG2细胞均无明显的毒性作用,相反有一定的增殖作用,当紫薯花青素质量浓度达到 200~ 400μg /mL时,其对 HepG2细胞的增殖效果最明显。
2.6.2 H 2 O 2诱导 HepG2细胞损伤的模型建立
由表 2可知, 50、 100、 200、 400、 800μmol /L的 H 2 O 2对 HepG2细胞的生长均有一定抑制作用,且细胞抑制率随 H 2 O 2浓度的增加而增大, 400μmol /L的 H 2 O 2对 HepG2细胞的抑制率达到 53.36%,因此建模时 H 2 O 2的最佳浓度选取为 400μmol /L。其余各 H 2 O 2处理组与 50μmol /L H 2 O 2处理组相比均有极显著差异(P< 0.01)。
表2 相同作用时间不同浓度的H
2O
2对HepG2细胞的损伤作用
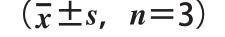
Table2 Efects of incubation with different concentrations of H
2O
2oonn HepG2 cell damage


注:Δ Δ. 与50 μmol/L H 2O 2处理组相比,差异极显著(P<0.01)。
组别H 2O 2浓度/(μmol/L)HepG2细胞抑制率/%阴性对照组0 H 2O 2处理组5021.56±5.82 10035.96±5.21 Δ Δ20037.39±46.15 Δ Δ40053.36±5.82 Δ Δ80056.02±7.75 Δ Δ
2.6.3 400μmol /L H 2 O 2处理不同时间对 HepG2细胞的氧化损伤作用
表3 400 μmolmol/L H/L H
2O
2处理不同时间对HepG2细胞的损伤作用x ±s,n=3)3
Table3 Oxidative stress injury induced by 400μmolmol/L H/L H
2O
2for for different durations in HepG2 cells(x ± s, n = 3)

注:Δ Δ. 与0.5 h H 2O 2处理组相比,差异极显著(P<0.01)。
组别H 2O 2处理时间/hHepG2细胞抑制率/%阴性对照组0 H 2O 2处理组0.552.08±14.50 1.566.07±1.18 Δ3.083.93±0.46 Δ Δ6.097.70±0.48 Δ Δ
由表 3可知, 400μmol /L的 H 2 O 2在不同作用时间内均可引起 HepG2细胞发生氧化损伤(P< 0.01),处理时间越长,对 HepG2细胞的抑制作用也越强, H 2 O 2处理 6 h时, HepG2细胞损伤率已达到 97.70%,不适宜造模,故建模时选取 H 2 O 2的最佳处理时间为 2 h。
2.6.4不同质量浓度紫薯花青素对 H 2 O 2诱导 HepG2细胞氧化损伤的保护作用
表4 紫薯花青素对H
2O
2诱导HepG2细胞损伤的保护作用
Table4 Protective effects of anthocyanins from purple sweet potato Table4 Protectiv against Hnst H
2O
2-induced injury in HepG2 cells

注:Δ. 与模型组相比,差异显著(P<0.05);Δ Δ. 与模型组相比,差异极显著(P<0.01)。
组别紫薯花青素质量浓度/(μg/mL)HepG2细胞存活率/%阴性对照组99.14±4.36模型组60.60±4.37紫薯花青素5066.40±5.11 Δ10067.50±0.59 Δ20075.90±3.47 Δ Δ40076.83±1.78 Δ Δ80088.03±7.48 Δ Δ1 60086.74±3.39 Δ Δ
由表 4可知,模型组的 HepG2细胞存活率只有( 60.60± 4.37)%,而加入不同质量浓度紫薯花青素的 HepG2细胞存活率均高于( 60.60± 4.37)%,即紫薯花青素可显著或极显著提高 HepG2细胞存活率(P< 0.05或P< 0.01)。以上结果说明紫薯花青素可以有效降低 H 2 O 2诱导 HepG2细胞的氧化损伤作用,且随着紫薯花青素质量浓度的升高,其对 HepG2细胞的保护作用愈加明显。
本实验结果表明,紫薯花青素的还原力、对·
OH和
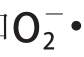 ·的清除能力随其浓度的增大而增强,在本实验所设定的浓度范围内,紫薯花青素·
OH的清除率可达到
91.93%,对
·的清除能力随其浓度的增大而增强,在本实验所设定的浓度范围内,紫薯花青素·
OH的清除率可达到
91.93%,对
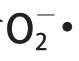 的清除率可达到
47.25%,能够有效清除
Fenton反应产生的·
OH。研究结果还显示,紫薯花青素能显著抑制
H
2
O
2诱导的大鼠红细胞溶血,随着紫薯花青素质量浓度的增大,大鼠红细胞溶血度不断降低。以上结果均表明紫薯花青素具有良好的体外抗氧化功效。
的清除率可达到
47.25%,能够有效清除
Fenton反应产生的·
OH。研究结果还显示,紫薯花青素能显著抑制
H
2
O
2诱导的大鼠红细胞溶血,随着紫薯花青素质量浓度的增大,大鼠红细胞溶血度不断降低。以上结果均表明紫薯花青素具有良好的体外抗氧化功效。
经 H 2 O 2处理的 HepG2细胞会发生显著的氧化损伤,本实验确定 HepG2细胞氧化损伤最佳造模条件为 400μmol /L的 H 2 O 2处理 2 h;使用单一紫薯花青素处理 HepG2细胞发现其对细胞无明显毒性作用;当不同质量浓度紫薯花青素和 H 2 O 2共同作用于 HepG2细胞时,结果显示紫薯花青素对 H 2 O 2诱导 HepG2细胞氧化损伤具有较为明显的保护作用。
本实验发现紫薯花青素对 H 2 O 2诱导 HepG2细胞氧化损伤具有保护作用,进一步的研究需要采取动物模型结合细胞实验深入探究紫薯花青素对超氧化物歧化酶、谷胱甘肽过氧化物酶等体内抗氧化酶活性的影响,以及如何通过调控细胞凋亡蛋白酶 Caspases家族蛋白、氨基端激酶 JNK等关键蛋白的表 达而发挥保护作用,进而阐明紫薯花青素抗氧化损伤的作用机制 [23]。
参考文献:
[1] 吕昱, 严敏. 紫薯花色苷的生理功能及分离纯化研究进展[J]. 食品与机械, 2013, 29(4)∶ 250-253.
[2] 周玮婧, 孙智达, 谢笔钧, 等. 荔枝皮原花青素提取, 纯化及抗氧化活性研究[J]. 食品科学, 2009, 30(8)∶ 68-71.
[3] 程琤, 刘超, 王征, 等. 紫甘薯花青素的稳定性及抗氧化性研究[J].营养学报, 2011, 33(3)∶ 291-296.
[4] 田丽君, 刘志伟. 紫薯花青素分离纯化及理化性质研究[D]. 武汉∶ 武汉工业学院, 2012∶ 1-2.
[5] 杨旸, 文利新. 花青素的生理活性及作用[J]. 湖南农业科学, 2011(10)∶ 27-28.
[6] 杨新笋, 雷剑, 苏文瑾, 等. 紫心甘薯新品种鄂薯8号的选育与高产栽培技术[J]. 湖北农业科学, 2012, 50(22)∶ 4553-4555.
[7] HOSSEINIAN F S, LI W, BETA T. Measurement of anthocyanins and other phytochemicals in purple wheat[J]. Food Chemistry, 2008, 109(4)∶ 916-924.
[8] STEED L E, TRUONG V D. Anthocyanin content, antioxidant activity, and selected physical properties of flowable purple-fleshed sweetpotato purees[J]. Journ al of Food Science, 2008, 73(5)∶ 215-221.
[9] ZHAO Jinge, YAN Qianqian, ZHANG Yuqing. Isolation and identification of colourless caffeoyl compounds in purple sweet potato by HPLC-DAD-ESI/MS and their antioxidant activities[J]. Food Ch emistry, 2014, 161∶ 22-26.
[10] 徐晓云, 潘思轶, 谢笔钧, 等. 沙棘籽原花青素体外抗氧化活性研究[J].食品科学, 200 5, 26(2)∶ 216-220.
[11] SMIRNOFF N, CUMBES Q J. Hydroxyl radical scavenging activity of compatible solutes[J]. Phytochemistry, 1989, 28(4)∶ 1057-1060.
[12] 田喜强, 董艳萍, 马松艳, 等. 紫薯花青素的稳定性及其抗氧化性研究[J]. 食品工业, 2014, 35(18)∶ 49-51.
[13] 孙芸, 徐宝才, 熊晓辉, 等. 葡萄籽原花青素聚合度与自由基清除能力关系的研究[J]. 食品科学, 2007, 28(12)∶ 423-428.
[14] 卢彩鹏, 喻凯. 紫甘薯花青素抗衰老及抗酒精性肝损伤作用的研究[D].成都∶ 西南交通大学, 2011∶ 12-18.
[15] 韩飞, 周孟良. 过氧化氢诱导HepG2细胞产生氧化应激细胞模型的建立[J]. 食品科学, 2011, 32(5)∶ 55-57.
[16] MARTINDALE J L, HOLBROOK N J. Cellular resp onse to oxidative stress∶ signaling for suicide and survival[J]. Journal of Cellular Physiology, 2002, 192(1)∶ 1-15.
[17] HWANG Y P, CHOI J H, JEONG H G. Purple sweet potato anthocyanins attenuate hepatic lipid accumulation through activating adenosine monophosphate-activated protein kinase in human HepG2 cells and obese mice[J]. Nutrition Research, 2011, 31(12)∶ 896-906.
[18] 刘春彦, 金吉淑. 漏芦对H 2O 2诱导的HepG2细胞损伤的保护作用[D].延吉∶ 延边大学, 2012∶ 4-6.
[19] MOORADIAN A D, HAAS M J, WADUD K. Ascorbic acid α-tocopherol down-regulate apolipoprotein A-I gene expression in HepG2 and Caco-2 cell lines[J]. Metabolism, 2006, 55(2)∶ 159-167.
[20] HOU Fangli, ZHANG Ruifen, ZHANG Mingwei, et al. Hepatoprotective and antioxidant activity of anthocyanins in black rice bran on carbon tetrachloride-induced liver injury in mice[J]. Journal of Functional Foods, 2013, 5(4)∶ 1705-1713.
[21] HAN K H, SEKIKAWA M, FUKUSHIMA M, et al. Anthocyaninrich purple potato flake extract has antioxidant capacity and improves antioxidant potential in rats[J]. British Journal of Nutrition, 2006, 96(6)∶ 1125-1133.
[22] WANG Wencheng, LI Jinlian, HAN Yantao, et al. Oral hepatoprotective ability evaluation of purple sweet potato anthocyanins on acute and chronic chemical liver injuries[J]. Cell Biochemistry and Biophysics, 2014, 69(3)∶ 539-548.
[23] 屠迪, 薛立群, 文利新. 矢车菊素在体外对肝细胞脂代谢的影响[D].长沙∶ 湖南农业大学, 2012∶ 22-28.
Antioxidant Activities and Protective Effect of Anthocyanins from Purple Sweet Potato on HepG2 Cell Injury Induced by H 2O 2
LUO Chunli, WANG Lin, LI Xing, ZHANG Zicheng, ZHANG Jiuliang*
(Key Laboratory of Environment Correlative Dietology, Ministry of Education, College of Food Science and Technology, Huazhong Agricultural University, Wuhan 430070, China)
Abstract: Objective∶ To evaluate the in vitro antioxidant activities of anthocyanins extracted from purple sweet potato and investigate the protective effect of the anthocyanins on H 2 O 2 -induced oxidative stress in HepG2 cells. Methods∶ The anthocyanins were extracted and purified from the dried powder of purple sweet potato. The total reducing power, free radical scavenging effect and red blood cell hemolysis-protecting effect of the anthocyanins were measured. Moreover, an in vitro HepG2 cell damage model induced by H 2 O 2 was established, and the MTT (3-(4,5-dimethylthiazol-2-yl)-2,5-diphenyltetrazolium bromide) method was used to detect the protective effect on HepG2 cell injury of different concentrations of the anthocyanins. Results∶ The anthocyanins had good in vitro antioxidant effects, possessing reducing power similar to that of VC and potent scavenging activities hydroxyl and superoxide anion radicals in a dose-dependent manner. The superoxide anion radical scavenging activity was higher than that of BHT at the same concentration. The anthocyanin extract at 50-1 600μg /mL could restrain the HepG2 cells from apoptosis caused by H 2 O 2 and it at 800μg /mL yielded a survival rate of HepG2 cells of (88.03± 7.48)% . Conclusion∶ The anthocyanins from purple sweet potato possess good in vitro antioxidant ability and obvious protective effects on HepG2 cells from oxidative stress injury induced by H 2 O 2 .
Key words: anthocyanins from purple sweet potato; antioxidant; free radicals; oxidative stress injury; HepG2 cells
中图分类号: O629.12; R979.1
文献标志码: A 文章编号:1002-6630(2015)17-0225-06
文章编号:1002-6630(2015)17-0225-06
doi:10.7506/spkx1002-6630-201517042
收稿日期:2014-11-07
基金项目:中央高校基本科研业务费专项资金项目(2013PY095);华中农业大学“国家级大学生创新创业训练计划”项目(201310504034)
作者简介:罗春丽(1992—),女,硕士研究生,研究方向为天然产物化学。E-mail:956526251@qq.com
*通信作者:张久亮(1982—),男,副教授,博士,研究方向为天然活性成分研究与开发。E-mail:zjl_ljz@mail.hzau.edu.cn