马永强,魏 婧,王 鑫,李秀娟
(哈尔滨商业大学 黑龙江省高校食品科学与工程重点实验室,黑龙江 哈尔滨 150076)
摘 要:通过构建蓝莓汁抗坏血酸非酶褐变体系,测定蓝莓汁在贮藏(4、25 ℃和37 ℃)过程中的相关指标,并相应分别用零级、一级和复合动力学模型拟合。结果表明:褐变指数(A 420 nm)符合复合动力学模型;贮藏过程中抗坏血酸不断降解,符合一级动力学模型;5-羟甲基糠醛含量的变化符合零级动力学模型。根据Arrhenius方程进行线性拟合,反映各指标随温度变化情况,在各贮藏温度下5-羟甲基糠醛的产生与褐变指数的变化呈现良好线性关系(R 2≥0.949)。
关键词:蓝莓汁;抗坏血酸;非酶褐变;贮藏;动力学
蓝莓(blueberry)为杜鹃花科(Ericaceae)越橘属(Vaccinium spp.)常绿灌木,是原产于北美洲的一种具有较高经济价值的越橘类浆果,其果皮呈蓝色或蓝黑色故称蓝莓 [1]。蓝莓果实为浆果,果肉细腻,酸甜适度,既可鲜食,也可以加工成果汁饮料、果酒饮品等 [2]。目前世界在制作果汁方面不同程度地存在四大技术难题:果汁褐变、后混浊和二次混浊、营养损耗和芳香物质逸散 [3],其中以果汁褐变最为普遍。果汁褐变分为酶促褐变(enzymatic browning)和非酶促褐变(non-enzymatic browning)。而非酶促褐变主要有以下几种机制:美拉德反应、焦糖化反应、抗坏血酸氧化分解、多元酚氧化缩合反应 [4]。其中抗坏血酸的分解方式分为有氧性及厌氧性分解反应。在厌氧性分解反应方面,抗坏血酸分解的主要产物为糠醛(furfural) [5],因此可用5-羟甲基糠醛含量来衡量果汁的褐变程度 [6-7]。关于果汁非酶褐变动力学,国内外做了较多的研究。Selen Burburlu等 [8]认为浓缩苹果汁在贮藏过程中的非酶褐变都符合零级动力学,Kambo等 [9]研究了抗坏血酸/果糖体系的褐变动力学。而有关蓝莓汁的抗坏血酸非酶褐变反应以及动力学研究均未见报道。本实验以蓝莓为原料,主要对蓝莓果汁贮藏过程中抗坏血酸褐变进行研究,通过反应物消耗、中间产物生成以及褐变指数建立动力学模型,从而为控制褐变的工艺、提高蓝莓果汁品质提供理论依据。
1.1 材料与试剂
蓝莓 大兴安岭百盛蓝莓科技开发有限公司。
抗坏血酸 天津博迪化工股份有限公司;2,6-二氯靛酚 国药集团化学试剂有限公司;亚硫酸氢钠、无水乙醇 天津基准化学试剂有限公司;乙酸锌 天津市巴斯夫化工有限公司;草酸 哈尔滨市新达化工厂;D001强酸大孔苯乙烯系阳离子交换树脂 上海维塔化学试剂有限公司。
1.2 仪器与设备
BS 224S型分析天平 德国赛多利斯科学仪器有限公司;LG10-2.4A型高速离心机 北京京立离心机有限公司;V-5000可见分光光度计 上海元析仪器有限公司;恒温摇床培养箱 上海智诚分析仪器制造有限公司;ZD-2型自动电位滴定仪 上海仪田精密仪器有限公司;UV1000单光束紫外-可见分光光度计 上海天美科学仪器有限公司。
1.3 方法
1.3.1 蓝莓汁抗坏血酸非酶褐变体系样液的制备
蓝莓果→解冻→打浆→加一定量三氯乙酸(trichloroacetic acid,TCA)灭酶→离心→用D001阳离子交换树脂处理上清液(用以去除氨基酸)→即得样液
所得样液分别于4、25 ℃和37 ℃条件下贮藏,定期测定相关指标。
1.3.2 褐变指数的测定
果汁的褐变度用420 nm波长处的吸光度(A 420 nm)表示。取适量待测果汁样品,于9 000 r/min离心20 min,取上清液,测定A 420 nm值,以水为空白 [10-11]。
1.3.3 VC含量测定
采用电位法测定 [12-13]。
1.3.3.1 试剂配制
2,6-二氯靛酚溶液:称取2,6-二氯靛酚钠盐50 mg,溶于50 mL热水中,冷却后定容至250 mL,过滤后置于棕色瓶中;标准VC液:精确称取抗坏血酸50 mg,用5 g/100 mL草酸溶解,小心移至250 mL容量瓶中,并加草酸稀释至刻度,最终质量浓度为200 μg/mL。
1.3.3.2 标定
精确吸取200 μg/mL的抗坏血酸标准溶液5 mL于小锥形瓶中,加5 mL 1 g/100 mL草酸溶液,用2,6-二氯靛酚溶液滴定至淡红色于15 s不褪色为止,即为终点。由此计算2,6-二氯靛酚溶液滴定度T。
式中:T为1.0 mL 2,6-二氯靛酚相当于抗坏血酸的毫克数/mg;ρ为VC标准液质量浓度/(mg/mL);V 1为吸取VC标准液体积/mL;V 2为滴定消耗2,6-二氯靛酚的体积/mL。
1.3.3.3 测定并计算含量
称取样液5.0~10.0 g,加入5 g/100 mL草酸溶液定容至50 mL,过滤,得待测液。吸取5~20 mL待测液于烧杯中,将烧杯放在电磁搅拌器上,杯内放入小磁棒,记录仪与电极的插头相连接,并将电极插入烧杯内,打开记录仪和搅拌器,然后用2,6-二氯靛酚溶液进行滴入,观察记录仪上电位的变化。随着2,6-二氯靛酚的滴入,电位会逐渐上升,当达到终点时,电位突然升高,然后很快下降,最高值即为终点,此时记录滴定2,6-二氯靛酚溶液消耗毫升数。
式中:V 1为滴定样品所用2,6-二氯靛酚液的体积/mL;V 2为滴定时吸取样液体积/mL;V为样品提取液总体积/mL;T为1 mL 2,6-二氯靛酚相当于抗坏血酸毫克数/mg;m为样品质量/g。
1.3.4 5-羟甲基糠醛(5-hydroxymethylfurfural,5-HMF)含量测定
1.3.4.1 溶液的配制
澄清剂Ⅰ,称取15 g亚铁氰化钾溶解后,用蒸馏水定容至100 mL容量瓶。澄清剂Ⅱ,称取30 g乙酸锌溶解后,用蒸馏水定容至100 mL容量瓶。
1.3.4.2 样品测定
取蓝莓汁样品5 g,用25 mL蒸馏水稀释溶解后,移入50 mL容量瓶,加入0.5 mL澄清剂Ⅰ、摇匀;再加入0.5 mL澄清剂Ⅱ,摇匀,用蒸馏水定容至刻度。于9 000 r/min离心10 min,吸取上层清夜各5 mL于2 个10 mL比色管中。在一个比色管中加入5 mL 0.20 g/100 mL NaHSO 3溶液,混匀,为参比液;另一个比色管中5 mL蒸馏水,混匀,为待测液。用石英比色皿于284 nm和336 nm波长处测定待测样液的吸光度 [14]。
式中:X为蓝莓汁样品中5-HMF的含量/(mg/100 g);m为样品质量/g;14.97为换算系数。
1.3.5 动力学模型分析
对贮藏过程中蓝莓汁的褐变指数、抗坏血酸、5-HMF的变化用零级、一级和复合反应动力学模型进行拟合分析。
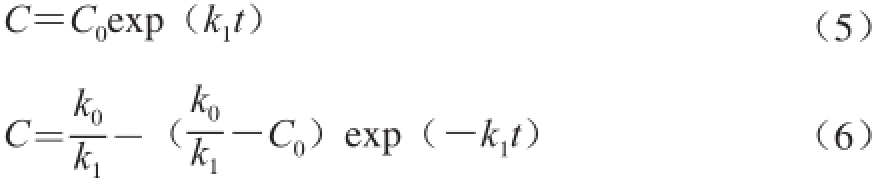
式中:C为任意时间指标测定值;C 0为该指标的起始值;t为时间/min;k 0为零级动力学反应常数;k 1为一级动力学反应常数。
温度对各指标的影响符合Arrhenius等式:
式中:k为平衡常数;k 0为指数系数;E a为活化能/(kJ/mol);R为气体常数,8.314 kJ/(mol·K);T为绝对温度/K。
对Arrhenius等式两边同时取对数可得:
取353、363、373 K时模型的反应常数k值,以-lnk为纵坐标,1/T为横坐标,则斜率为E a/R,可计算出E a值。
2.1 褐变指数的变化
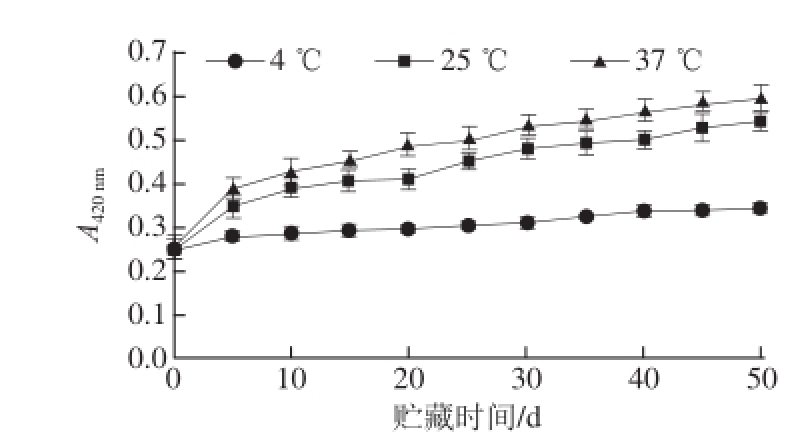
图1 贮藏过程中蓝莓汁褐变指数(A
42200
nnmm)的变化
Fig.1 Changes in browning index (A
420
nm) in blueberry juice during storage
由图1可知,在不同贮藏温度下,蓝莓汁的褐变指数A 420 nm有明显变化。4 ℃条件下贮藏50 d后的蓝莓汁A 420 nm由0.253增加至0.345,仅为起始值的1.36 倍;25 ℃条件下贮藏50 d后的蓝莓汁A 420 nm由0.253增加至0.544,为起始值的2.1 倍;37 ℃条件下贮藏50 d后的蓝莓汁A 420 nm由0.253增加至0.595,为起始值的2.53 倍。这说明,贮藏温度越高,抗坏血酸非酶褐变越严重。将蓝莓汁褐变指数与贮藏时间的关系进行动力学模型拟合,其变化规律更加符合联合动力学模型(表1),在3 个温度梯度贮藏下,相关系数R 2>0.95,同时根据Arrhenius方程对-lnk-1/T进行线性拟合,如图2所示,得出拟合方程为y=3 985x-10.011(R 2=0.974 8),进而计算出蓝莓汁抗坏血酸非酶褐变(以褐变指数计)的活化能为33.13 kJ/mol,小于刘静 [14]研究红枣浓缩汁(活化能为60.40 kJ/mol)在贮藏过程中的活化能,但与Selen Burdurlu等 [8]研究苹果浓缩汁(活化能为33.7 kJ/mol)相似,通常认为反应活化能在40~400 kJ/mol范围内,而小于40 kJ/mol时则认为反应速率非常大 [15]。这说明蓝莓汁在贮藏过程中抗坏血酸非酶褐变反应活性高,很容易发生。
表1 蓝莓汁褐变指数变化的动力学参数
Table 1 Kinetic parameters for browning index change of blueberry juice
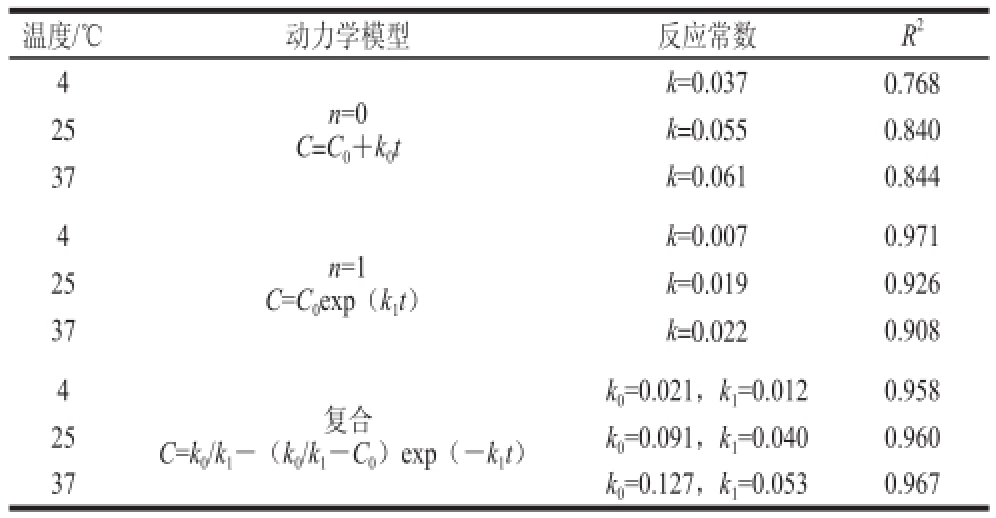
温度/℃动力学模型反应常数R 24 n=0 C=C 0+k 0t k=0.0370.768 25k=0.0550.840 37k=0.0610.844 4 n=1 C=C 0exp(k 1t)k=0.0070.971 25k=0.0190.926 37k=0.0220.908 4复合C=k 0/k 1-(k 0/k 1-C 0)exp(-k 1t)k 0=0.021,k 1=0.0120.958 25k 0=0.091,k 1=0.0400.960 37k 0=0.127,k 1=0.0530.967
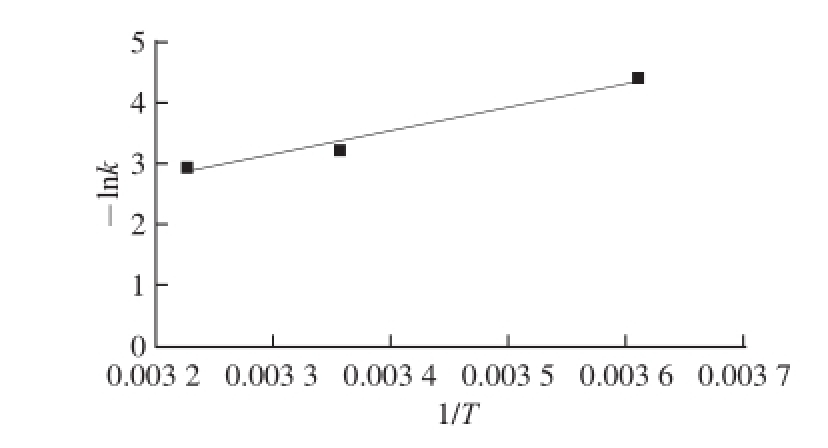
图2 褐变指数--llnnk对11//T线性拟合曲线
Fig.2 Linear fitting curve for -lnk of BI versus 1/T
2.2 抗坏血酸含量的变化

图3 贮藏过程中蓝莓汁抗坏血酸含量的变化
Fig.3 Changes in ascorbic acid content of blueberry juice during storage
VC是果汁的主要营养成分之一,因其兼具酸性和还原性,故极易氧化分解。抗坏血酸氧化有2 种途径:有氧分解和无氧分解。由图3可知,在贮藏过程中,4、25、37 ℃条件下VC含量在开始的5 d内下降较快,后来则缓慢减低,这是由于果汁中含有溶氧或贮藏瓶的顶隙中含氧,这主要遵循有氧降解途径 [16],当氧气消耗到一定程度,且VC降解主要遵循无氧降解,该结果符合果汁中抗坏血酸的有氧降解反应速率高于无氧降解 [17]。
由抗坏血酸的动力学参数(表2)可知,在25、37 ℃条件下,反应速率相对明显加快,这与Klinczak等 [18]研究橙汁中抗坏血酸受温度和贮藏时间其含量变化的结果是一致的。同时可以表明蓝莓果汁在贮藏过程中VC的变化符合一级动力学模型,它能更好地拟合VC变化趋势。根据Arrhenius方程对-lnk-1/T进行线性拟合(图4),得出拟合方程为y=1 866.9x-2.054 6(R 2=0.968 2)。并计算得出E a为15.5 kJ/mol,活化能反映了VC降解速率k随温度变化的程度,即温度越高,蓝莓汁中VC降解速率越快。
表2 蓝莓汁抗坏血酸含量(C/C
0)变化的动力学参数
Table 2 Kinetic parameters for ascorbic acid content(C/C0)change of blueberry juice

温度/℃动力学模型反应常数R 24 n=0 C=C 0+k 0t k=-0.0070.838 25k=-0.0100.875 37k=-0.0100.860 4 n=1 C=C 0exp(k 1t)k=-0.0090.856 25k=-0.0160.949 37k=-0.0180.950 4复合C=k 0/k 1-(k 0/k 1-C 0)exp(-k 1t)k 0=0.038,k 1=0.0630.961 25k 0=0.018,k 1=0.0470.957 37k 0=0.015,k 1=0.0460.926
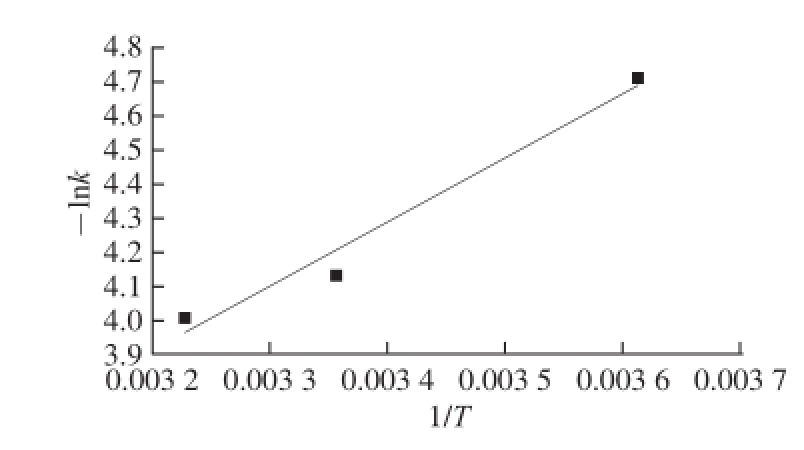
图4 蓝莓汁中抗坏血酸-llnnk对11//T的线性拟合曲线
Fig.4 Linear fitting curve for -lnk of ascorbic acid content of blueberry juice against 1/T
2.3 5-HMF含量的变化

图5 贮藏过程中蓝莓汁5-HMF含量的变化
Fig.5 Changes in 5-HMF content of blueberry juice during storage
5-HMF是美拉德反应、焦糖化反应和抗坏血酸降解的重要中间产物,它是衡量果汁褐变的重要指标 [19-20]。本实验构建的抗坏血酸非酶体系所测得的5-HMF主要是由VC厌氧降解产生的。如图5所示,在整个贮藏过程中,4 ℃条件下5-HMF产生很少,这说明低温不易生成5-HMF。25 ℃和37 ℃条件下5-HMF的形成在前10 d有明显增长,这是由于VC前期有氧快速分解所导致的,同时蓝莓汁在后期贮藏中大致经历了两个时期:迟滞期和增长期,可以看出在4 ℃条件下贮藏15~30 d、25 ℃条件下贮藏10~20 d以及37 ℃条件下贮藏15~20 d增长缓慢,其后5-HMF含量逐渐增加进入增长期。当贮藏50 d时,4、25 ℃和37 ℃条件下产生的5-HMF含量分别为初始值的2.5、5.5 倍和6.3 倍,这说明温度越高,5-HMF生成速率越快。
表3 蓝莓汁5-HMF含量(C/C
0)变化的动力学参数
Table 3 Kinetic parameters for 5-HMF content(C/C0)change of blueberry juice

温度/℃动力学模型反应常数R 24 n=0 C=C0+k0t k=0.0270.934 25k=0.0790.946 37k=0.0990.946 4 n=1 C=C 0exp(k 1t)k=0.0160.858 25k=0.0260.763 37k=0.0290.757 4复合C=k 0/k 1-(k 0/k 1-C 0)exp(-k 1t)k 0=0.088,k 1=0.0310.974 25k 0=0.139,k 1=0.0160.952 37k 0=0.225,k 1=0.0280.983
根据蓝莓汁5-HMF(C/C 0)变化的动力学参数(表3)可知,零级动力学模型更适于5-HMF在贮藏过程中的变化,这一结果与菠萝汁在贮藏过程中5-HMF含量变化符合一级动力学模型的结果不一致 [21],与Trevor等 [22]报道苹果汁5-HMF的变化符合零级动力学模型一致。这些差异可能是由于不同果汁构建不同体系而引起的。图6则反映的是蓝莓汁贮藏过程中5-HMF变化速率的对数值与温度之间的关系,其拟合方程为y=3 496.8x-9.058 5(R 2=0.969 5)。计算可得活化能E a=29.07 kJ/mol,远比Resnik等 [23]发现苹果汁贮藏中非酶褐变的活化能低。因此,温度越高,越容易发生抗坏血酸非酶褐变反应。
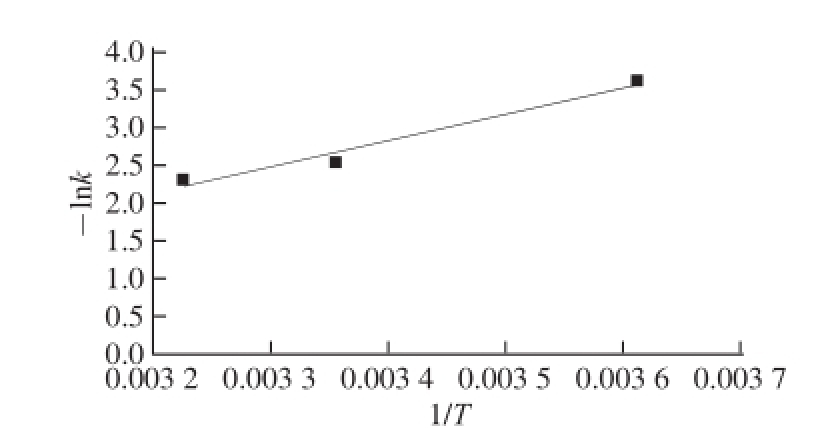
图6 蓝莓汁中5-HMF-llnnk对11//T的线性拟合曲线
Fig.6 Linear fitting curve of -lnk against 1/T for 5-HMF content of blueberry juice
2.4 5-HMF含量与褐变指数(A 420 nm)的关系
5-HMF和褐变指数是两项重要品质指标,同时5-HMF含量可反映果蔬加工和贮藏过程中的褐变程度 [24]。由表4可见,在贮藏过程中,蓝莓汁中的5-HMF含量(y,mg/100 g)和褐变指数(x)的变化呈良好线性关系,相关系数R 2均在0.9以上,这说明根据5-HMF含量的变化可预测在其对应温度下褐变程度,也可看出随着5-HMF的积累,对蓝莓汁的抗坏血酸非酶褐变有着显著的影响。
表4 蓝莓汁贮藏过程中5-HMF含量与褐变指数的相关性
Table 4 Correlation between 5-HMF and BI during storage
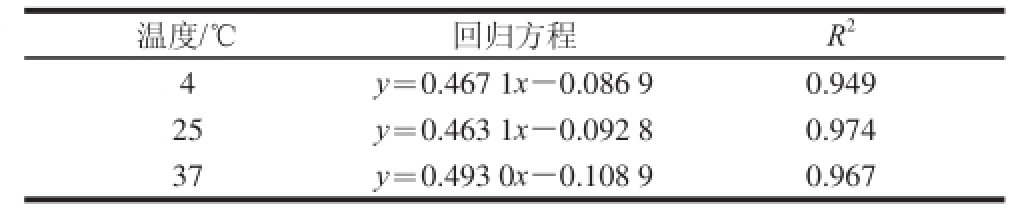
温度/℃回归方程R 24 y=0.467 1x-0.086 90.949 25y=0.463 1x-0.092 80.974 37y=0.493 0x-0.108 90.967
本实验通过构建蓝莓汁抗坏血酸非酶褐变体系,测定褐变指数、VC和5-HMF含量,之后通过不同温度下其含量与时间的关系,建立动力学模型并计算其反应速率,其中抗坏血酸降解反应符合一级动力学模型,褐变指数(A 420 nm)符合复合动力学模型,5-HMF含量的变化符合零级动力学模型,并分别根据Arrhenius方程k=k 0exp(-E a/RT)进行线性拟合,得出拟合方程并计算出相应活化能E a,来反映各个指标反应速率随温度的变化情况。计算得到的各指标活化能相对较小,这就表明贮藏温度越高,蓝莓汁发生抗坏血酸非酶褐变的反应活性越高,且容易发生。与此同时,对5-HMF和褐变指数(A 420 nm)这两项重要品质指标进行回归分析,二者呈现良好的线性关系。贮藏温度越高,抗坏血酸非酶褐变速率越快,因此从某种程度上抑制5-HMF的生成来提高蓝莓汁在贮藏过程中的品质有着重要的意义。
参考文献:
[1] 梁海英, 李亚东. 越橘(蓝莓)生产技术[M]. 长春: 吉林科学技术出版社, 2010: 1-9.
[2] 胡雅馨, 李京, 惠伯棣. 蓝莓果实中主要营养及花青素成分的研究[J].食品科学, 2006, 27(10): 600-603.
[3] 葛毅强, 蔡同一, 胡小松. 果汁二次混浊研究的新进展[J]. 食品与发酵工业, 2002, 28(9): 46-50.
[4] 舒念辉. 果汁褐变及控制研究[J]. 食品与发酵科技, 2011, 47(5): 59-61. DOI:10.3969/j.issn.1674-506X.2011.05.016.
[5] 任述荣, 赵晋府. 果汁风味劣变因素的研究[J]. 食品与发酵工业, 2002, 28(5): 70-73. DOI:10.3321/j.issn:0253-990X.2002.05.017.
[6] 天津轻工业学院, 无锡轻工业学院. 食品生物化学[M]. 北京: 中国轻工业出版社, 2001: 369-376.
[7] BOLIVAR A, WILLIAM R, DAVID B, et al. Selecting new peach and plum genotypes rich in phenolic compounds and enhanced functional properties[J]. Food Chemistry, 2006, 96(2): 273-280. DOI:10.1016/ j.foodchem.2005.02.032.
[8] SELEN BURDURLU H, KARADENIZ F. Effect of storage on nonenzymatic browning of apple juice concentrates[J]. Food Chemistry, 2003, 80(1): 91-97. DOI:10.1016/S0308-8146(02)00245-5.
[9] KAMBO N, UPADHYAY S K. Kinetic behaviour of ascorbic acidfructose browning reaction in alkaline medium[J]. Indian Journal of Chemical Technology, 2010, 19(2): 128-133.
[10] MEYDAV S, SAGUY I, KOPELMAN I J. Browning determination in citrus products[J]. Journal of Agricultural and Food Chemistry, 1977, 25(3): 602-604. DOI:10.1021/jf60211a030.
[11] 赵光远, 李娜, 张培旗, 等. 储藏对苹果混浊汁色泽稳定性的影响[J].江苏农业科学, 2007(2): 170-174.
[12] 孙义. 水果和蔬菜中维生素C含量的测定方法综述[J]. 天津化工, 2008, 22(3): 58-59. DOI:10.3969/j.issn.1008-1267.2008.03.022.
[13] 宁正祥. 食品成分分析手册[M]. 北京: 中国轻工业出版社, 1998: 316-317.
[14] 刘静. 红枣浓缩汁加工和贮藏过程中非酶褐变的研究[D]. 西安: 西北大学, 2011.
[15] 阮卫红, 邓放明, 毕金峰, 等. 桃汁热处理过程中非酶褐变动力学研究[J]. 食品科学, 2014, 35(1): 50-55. DOI:10.7506/spkx1002-6630-201401010.
[16] 万鹏, 刘亮, 潘思轶, 等. 热处理对荔枝果汁品质的影响[J]. 食品科学, 2010, 31(7): 22-27.
[17] 张静, 曹炜, 曹艳萍, 等. 红枣汁中维生素C热降解的动力学[J]. 农业工程学报, 2008, 24(6): 295-298. DOI:10.3321/ j.issn:1002-6819.2008.06.063.
[18] KLIMCZAK I, MALECKA M, SZLACHTA M, et al. Effect of storage on the content of polyphenols, vitamin C and the antioxidant activity of orange juices[J]. Journal of Food Composition and Analysis, 2007, 20: 313-322. DOI:10.1016/j.jfca.2006.02.012.
[19] DAMASCENO L F, FERNANDES F A N, MAGALHÃES M, et al. Non-enzymatic browning in clarified cashew apple juice during thermal treatment: kinetics and process control[J]. Food Chemistry, 2008, 106(1): 172-179. DOI:10.1016/j.foodchem.2007.05.063.
[20] ELEZ-MARTINEZ P, SOLIVA-FORTUNY R C, MARTINBELLOSO O. Comparative study on shelf life of orange juice processed by high intensity pulsed electric fields or heat treatment[J]. European Food Research and Technology, 2006, 222(34): 321-329. DOI:10.1007/s00217-005-0073-3.
[21] 李欣. 菠萝浓缩汁储藏过程中非酶褐变的研究[D]. 南宁: 广西大学, 2007.
[22] TREVOR S, GENTRYA, JOHN S, et al. Kinetics and application of 5-HMF as a time-temperature indicator of lethality for continuous pasteurization of apple cider[J]. Innovative Food Science and Emerging Technologies, 2004, 30: 327-333.
[23] RESNIK S, CHIRIFE J. Effect of moisture content and temperature on some aspects of nonenzymatic browning in dehydrated apple[J]. Food Science, 1979, 44(2): 601-605.
[24] 刘凤霞, 张燕, 汪厚银, 等. 热破碎番茄浆贮藏期间非酶褐变动力学分析[J]. 食品科学, 2011, 32(10): 260-265.
Kinetics of Non-Enzymatic Browning Reaction from Ascorbic Acid Model System of Blueberry Juice
MA Yongqiang, WEI Jing, WANG Xin, LI Xiujuan
(Key Laboratory of Food Science and Engineering, Harbin University of Commerce, Harbin 150076, China)
Abstract:By building a non-enzymatic browning system containing ascorbic acid from blueberry juice, the relevant indicators of blueberry juice during storage (4, 25 and 37 ℃) were determined and tentatively fitted to zero-order, first-order and composite kinetic models. Browning index (BI; absorbance at 420 nm) complied with a composite kinetic model. The ascorbic acid was constantly degraded during storage, which could be described by a first-order kinetic model, while the 5-HMF content variation followed a composite kinetic model. Linear fitting was conducted using the Arrhenius equation to describe each indicator as a function of storage temperature. The generation of 5-HMF and BI showed good linear relationship (R 20.949) at three different storage temperatures.
Key words:blueberry juice; ascorbic acid; non-enzymatic browning; storage; kinetics
DOI:10.7506/spkx1002-6630-201601020
中图分类号:TS255.3
文献标志码:A
文章编号:1002-6630(2016)01-0109-05
引文格式:
马永强, 魏婧, 王鑫, 等. 蓝莓汁抗坏血酸体系非酶褐变反应动力学[J]. 食品科学, 2016, 37(1): 109-113. DOI:10.7506/ spkx1002-6630-201601020. http://www.spkx.net.cn
MA Yongqiang, WEI Jing, WANG Xin, et al. Kinetics of non-enzymatic browning reaction from ascorbic acid model system of blueberry juice[J]. Food Science, 2016, 37(1): 109-113. (in Chinese with English abstract) DOI:10.7506/spkx1002-6630-201601020. http://www.spkx.net.cn
收稿日期:2015-06-05
基金项目:黑龙江省应用技术研究与开发计划项目(2013G0200)
作者简介:马永强(1963—),男,教授,硕士,研究方向为食品化学。E-mail:qyma163@126.com