戴宏杰 1,2,孙玉林 1,2,杨梅语 2,辛欣欣 2,冯梓欣 2,文 菁 1,2,陈道海 1,*
(1.岭南师范学院环北部湾海洋药用动物保护与利用研究所,广东 湛江 524048;2.岭南师范学院生命科学与技术学院,广东 湛江 524048)
摘 要:以拟目乌贼生殖腺为材料,采用碱法提取多糖,并对其抗氧化活性和吸湿保湿性进行研究。结果表明:拟目乌贼生殖腺碱提多糖最佳工艺为NaOH溶液浓度0.3 mol/L、料液比1∶40(g/mL)、提取时间3 h、提取温度80 ℃,此条件下多糖得率为7.697%。拟目乌贼生殖腺碱提多糖具有良好的抗氧化活性,对羟自由基和1,1-二苯基-2-三硝基苯肼自由基具有较好的清除效果,清除率与多糖质量浓度呈正相关。拟目乌贼生殖腺碱提多糖的吸湿性能高于壳聚糖、聚乙二醇6000等常规保湿剂,保湿性能和壳聚糖、聚乙二醇6000、丙三醇接近;吸湿保湿能力均高于翡翠贻贝多糖、近江牡蛎多糖等海洋动物多糖。综上表明,拟目乌贼生殖腺碱提多糖作为天然的抗氧化剂和保湿剂具有一定的应用前景。
关键词:拟目乌贼生殖腺;多糖;抗氧化;吸湿性;保湿性
拟目乌贼(S e p i a l y c i d a s)属软体动物门(Mollusca)、头足类(Cephalopoda)、鞘亚纲(Coleoidea)、乌贼目(Sepiida)、乌贼科(Sepiidae)、乌贼属(Sepia),主要分布于我国东海、南海,菲律宾海,越南和婆罗洲海域 [1]。目前国内外对拟目乌贼的研究主要集中在胚胎发育 [2-3]、幼体培育 [4]、养殖技术 [5-6]和营养分析 [7]方面,但对拟目乌贼生物活性物质研究较少。多糖具有广泛的生物活性,如抗肿瘤和免疫促进、抗炎、抗病毒、抗凝血、降血糖血脂、抗肿瘤、抗疲劳、抗氧化及抗衰老等 [8]。研究表明,从蛤蜊 [9]、鲍鱼 [10]、贻贝 [11]、扇贝 [12]、海参 [13]等海洋动物中提取得到的多糖均表现出良好的生物活性。同时多糖分子中存在大量的羟基、羧基等亲水性基团,使多糖具有一些优良的理化性质,如强吸水性、乳化性和良好的成膜性等 [14]。越来越多的文献研究表明,从海洋动物中提取得到的多糖具有一定的吸湿保湿性能,如马氏珠母贝、企鹅珍珠贝、翡翠贻贝、近江牡蛎 [15]、鲍鱼 [16]、蛤蜊 [9]、贻贝 [17]等。而来自于海洋生物中多糖种类,如壳聚糖、透明质酸等,已在美容食品和化妆品开发方面显示出良好的市场前景 [18]。因此,多糖作为功效型化妆品保湿剂有着十分广阔的应用前景。
近年来,从扇贝性腺 [12,19]、鲍鱼性腺 [20-22]、马粪海胆生殖腺 [23]中获得的多糖显示出良好的生物活性,是一种新型的海洋天然药物和功能性保健食品资源。本实验以拟目乌贼生殖腺为材料,采用碱法制备拟目乌贼生殖腺多糖,并对其抗氧化活性和吸湿保湿性能进行研究,考察其作为天然抗氧化剂和保湿剂的应用前景,以期为拟目乌贼生殖腺在功能性食品、医药制品和化妆品方面的综合开发利用提供理论依据。
1.1 材料与试剂
拟目乌贼于2014年4月在广东省湛江市霞山水产批发市场采集,经鉴定为雌性成体;1,1-二苯基-2-三硝基苯肼(1,1-diphenyl-2-picrylhydrazyl,DPPH) 美国Sigma公司;馥佩貂油润手霜为广州中医药大学研制,购于广东省湛江市赤坎区沃尔玛购物广场。
1.2 仪器与设备
DS-1高速组织捣碎机 上海标本模型厂;DFY-200手提式高速中药粉碎机 青州市三宝中药机械厂;LGJ-18A冷冻干燥机 北京四环科学仪器厂;AUX320电子天平 日本岛津公司;DHG-9123A电热恒温鼓风干燥箱 上海齐欣科学仪器有限公司;HH-4智能数显恒温水浴锅 巩义市予华仪器有限责任公司;N-1100旋转蒸发仪 上海爱朗仪器有限公司;TG16MW台式高速离心机 湖南赫西仪器有限公司;UV3000紫外-可见分光光度计 上海美谱达仪器有限公司。
1.3 方法
1.3.1 拟目乌贼生殖腺基本成分分析
水分含量的测定参照GB 5009.3—2010《食品中水分的测定》,采用105 ℃烘干恒质量法;灰分含量的测定参照GB 5009.4—2010《食品中灰分的测定》,采用炉550 ℃灼烧法;粗蛋白质含量的测定参照GB 5009.5—2010《食品中蛋白质的测定》,采用凯氏定氮法;粗脂肪含量的测定参照GB/T 5009.6—2003《食品中脂肪的测定》,采用索氏抽提法;多糖含量的测定参照GB/T 9695.31—2008《肉制品总糖含量的测定》,采用苯酚-硫酸法。
1.3.2 拟目乌贼生殖腺多糖碱法提取工艺优化
1.3.2.1 多糖提取工艺流程
参照文献[24],采用碱法提取拟目乌贼生殖腺多糖。
材料预处理:拟目乌贼解剖后取出生殖腺,放置于高速组织捣碎机中匀浆,采用丙酮脱脂3 次,-70 ℃条件下预冻3 h后放置于冷冻干燥机中冻干24 h,粉碎后得到拟目乌贼生殖腺冻干粉,-20 ℃条件下保存备用。
拟目乌贼生殖腺冻干粉→NaOH溶液浸提→离心(4 000 r/min,20 min)→取上清液→用4 mol/L盐酸调pH值至中性→旋蒸浓缩至原体积的1/5→95%乙醇沉淀(3 倍体积,4 ℃静置12 h)→离心(4 000 r/min,15 min)→透析脱盐(4 ℃,48 h)→冷冻干燥→拟目乌贼生殖腺碱提多糖。
1.3.2.2 多糖含量的测定
采用苯酚-硫酸法测定样品中多糖含量 [25]。精密称取105 ℃条件下干燥至质量恒定的葡萄糖配制成100 μg/mL葡萄糖标准溶液,分别吸取0、0.2、0.4、0.6、0.8、1.0、1.2、1.4 mL葡萄糖标准溶液于试管中,补水至2 mL,加入1 mL 6%苯酚溶液,混匀后迅速加入5 mL浓硫酸,室温条件下放置30 min,在波长490 nm处测定吸光度,得到标准曲线回归方程为:Y=12.576X-0.002 7,R 2=0.996 2;Y为吸光度,X为葡萄糖含量/(mg/mL),按式(1)计算拟目乌贼生殖腺碱提多糖得率:
式中:Y为多糖得率/%;C为待测液中多糖质量浓度/(mg/mL);V为待测液体积/mL;N为稀释倍数;M为拟目乌贼生殖腺样品质量/g。
1.3.2.3 单因素试验
对NaOH溶液浓度(0.1、0.3、0.5、0.7、0.9 mol/L)、料液比(1∶10、1∶20、1∶30、1∶40、1∶50(g/mL))、提取时间(1、2、3、4、5 h)及提取温度(50、60、70、80、90 ℃)4个影响碱法提取多糖得率的因素分别进行单因素试验,确定其中3 个因素不变的情况下,分析单个因素对拟目乌贼生殖腺多糖得率的影响。
1.3.2.4 正交试验设计
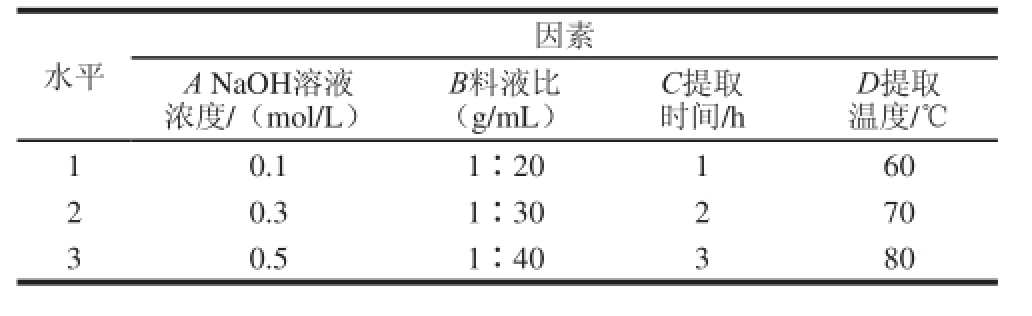
在单因素试验的基础上,选取NaOH溶液浓度(A)、料液比(B)、提取时间(C)、提取温度(D)为考察因素,采用L 9(3 4)正交试验设计进行提取工艺的优化,确定碱法提取拟目乌贼生殖腺多糖的最佳工艺。正交试验设计方案见表1。
表1 正交试验设计因素水平
Table 1 Design for factors and levels of orthogonal array experiments
水平D提取温度/℃1 0.11∶20160 2 0.31∶30270 3 0.51∶40380因素A NaOH溶液浓度/(mol/L)B料液比(g/mL)C提取时间/h
1.3.2.5 拟目乌贼生殖腺多糖成分测定
多糖含量的测定采用苯酚硫酸法 [25];蛋白含量的测定采用考马斯亮蓝法 [25]。
1.3.3 拟目乌贼生殖腺碱提多糖抗氧化活性
1.3.3.1 还原能力的测定
参考文献:[26]的方法。取2 mL不同质量浓度的多糖溶液,加入0.2 mol/L pH 6.6磷酸盐缓冲液2 mL、1%铁氰化钾溶液2 mL,混匀后置于50 ℃水浴20 min,然后加入2 mL 10%三氯乙酸溶液,振荡混匀后,离心(3 000 r/min,10 min),取2 mL上清液、2 mL双蒸水和0.4 mL 0.1% FeCl 3溶液混匀,静置10 min,测定其在波长700 nm处的吸光度;空白对照以双蒸水代替多糖溶液,以VC作阳性对照。
1.3.3.2 对羟自由基清除能力的测定
参考文献[27]的方法。取1 mL不同质量浓度的多糖溶液,加入9 mmol/L FeSO 4溶液1 mL,9 mmol/L的水杨酸-乙醇溶液1 mL,最后加入8.8 mmol/L H 2O 2溶液1 mL,混匀后37 ℃水浴条件下反应30 min,3 000 r/min离心10 min,取上清液测定其在波长510 nm处的吸光度。以VC为阳性对照,空白对照组以双蒸水代替多糖溶液,按式(2)计算清除率:
式中:A 0为空白对照的吸光度;A x为加入多糖溶液的吸光度;A 1为以双蒸水代替H 2O 2溶液的吸光度。
1.3.3.3 对DPPH自由基清除能力的测定
按照文献[28]的方法,取2 mL不同质量浓度的多糖溶液,加入含0.2 mmol/L DPPH的无水乙醇溶液2 mL后混匀,在黑暗环境中常温反应30 min,在波长517 nm处测定吸光度。以VC为阳性对照,按式(3)计算清除率:
式中:A 1为2 mL多糖溶液加2 mL DPPH溶液的吸光度;A 2为2 mL多糖溶液加2 mL无水乙醇的吸光度;A 0为2 mL双蒸水加2 mL DPPH溶液的吸光度。
1.3.4 拟目乌贼生殖腺碱提多糖吸湿保湿性
1.3.4.1 吸湿性的测定
参考文献[17]的方法进行吸湿性的测定。拟目乌贼生殖腺碱提多糖的吸湿性测定在恒温恒湿条件下进行,将碳酸钾饱和溶液和硫酸铵饱和溶液分别置于干燥器内,环境温度为20 ℃,制成相对湿度分别为43%和81%的环境。
将多糖、对照品及数个规格为25 mm×25 mm的称量瓶置于干燥箱中,50 ℃干燥至质量恒定。精确称取样品及对照品各0.1 g放置于在已干燥至质量恒定的称量瓶中,将称量瓶敞口放置于相对湿度分别为43%和81%的干燥器中,密封干燥器。每隔8 h分别称质量,按式(4)计算吸湿率:
式中:m 0为吸湿前各样品的质量/g;m t为吸湿不同时间后各样品的质量/g。
1.3.4.2 保湿性的测定
参考文献[29]的方法并稍作改进后进行保湿性的测定。拟目乌贼生殖腺多糖的保湿性测定选定在恒温干燥环境下进行。控制环境温度为20 ℃,在干燥器底部加入200 g变色硅胶。将多糖、对照品及数个规格为20 mL的小烧杯置于干燥箱中,50 ℃干燥至质量恒定。称取多糖及对照品各0.1 g,分别加水10 mL配制成质量浓度为1 mg/mL的溶液。配制完成的溶液均敞口置于恒温密闭硅胶干燥器中。每隔8 h分别称质量,按式(5)计算保湿率:
式中:m 0为各样品放置前的质量/g;m t为各样品放置不同时间后的质量/g。
2.1 拟目乌贼生殖腺基本成分分析
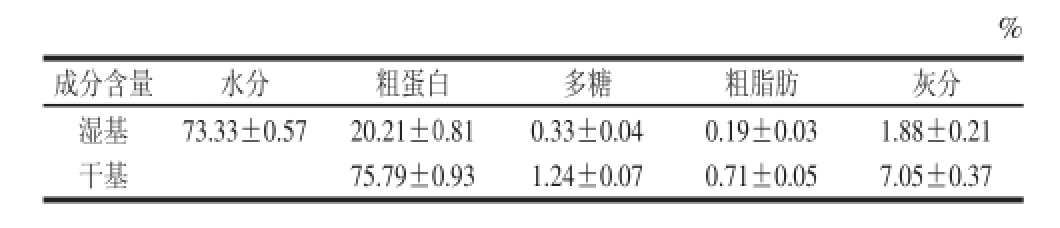
表2 拟目乌贼生殖腺基本成分组成
Table 2 General composition of Sepia lyciiddaass goonnaadd
%成分含量水分粗蛋白多糖粗脂肪灰分湿基73.33±0.5720.21±0.810.33±0.040.19±0.031.88±0.21干基75.79±0.931.24±0.070.71±0.057.05±0.37
由表2可知,拟目乌贼生殖腺的水分含量约为73.33%,粗蛋白含量较高,湿基和干基状态下分别可达到20.21%和75.79%。多糖含量方面,拟目乌贼生殖腺材料参照GB/T 9695.31—2008沸水提取30 min后测得的多糖含量在湿基和干基状态下分别为0.33%和1.24%。粗脂肪的含量较低,湿基状态下为0.19%。灰分含量在干基状态下为7.05%。综上所述,拟目乌贼生殖腺具有高蛋白低脂肪的特点,同时含有一定量的多糖成分,具有较好的研究价值。
2.2 单因素试验结果
2.2.1 NaOH溶液浓度对拟目乌贼生殖腺多糖得率的影响
固定拟目乌贼生殖腺多糖提取时的料液比1∶20(g/mL)、提取时间2 h、提取温度60 ℃,考察NaOH溶液浓度对多糖得率的影响,结果见图1。

图1 NaOH溶液浓度对拟目乌贼生殖腺多糖得率的影响
Fig.1 Effect of NaOH concentration on the yield of polysaccharides from Sepia lycidas gonad
由图1可知,NaOH溶液浓度范围在0.1~0.3 mol/L时,拟目乌贼生殖腺多糖得率有显著增加;当NaOH溶液浓度大于0.3 mo/L时,继续增加NaOH溶液浓度,多糖得率基本保持不变;同时过高的碱液浓度会对多糖结构造成破坏,综合分析选择NaOH溶液浓度0.3 mol/L为最佳。
2.2.2 料液比对拟目乌贼生殖腺多糖得率的影响
固定拟目乌贼生殖腺多糖提取时的NaOH溶液浓度0.3 mol/L、提取时间2 h、提取温度60 ℃,考察料液比对多糖得率的影响,结果见图2。
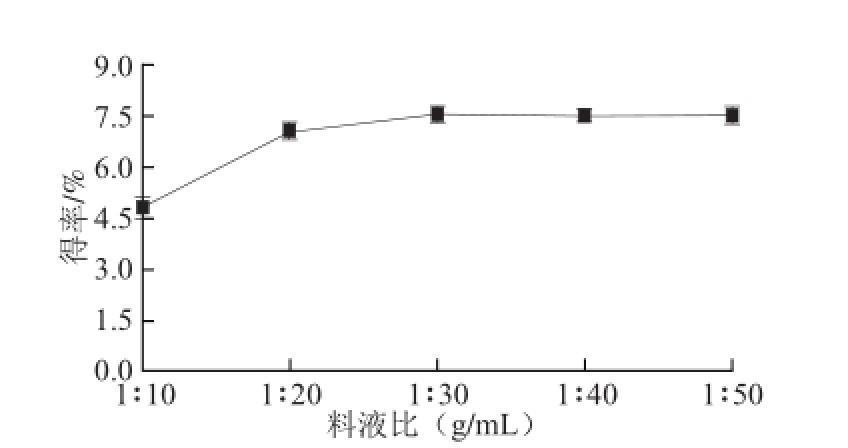
图2 料液比对拟目乌贼生殖腺多糖得率的影响
Fig.2 Effect of material/liquid ratios on the yield of polysaccharides from Sepia lycidas gonad
由图2可知,随着溶剂用量的增加,拟目乌贼生殖腺多糖得率也逐渐增加。料液比在1∶10~1∶30时,多糖得率随溶剂用量的增加显著上升;料液比在1∶30之后,多糖得率变化缓慢。提取溶剂越多,溶剂与样品材料的接触越充分,相同条件下的多糖得率也就越高。当提取溶剂达到一定量时,样品中的多糖已最大化地提取出来,多糖得率不再增加。考虑到后续需浓缩、醇沉等工作,综合分析选择料液比为1∶30为最佳。
2.2.3 提取时间对拟目乌贼生殖腺多糖得率的影响
固定拟目乌贼生殖腺多糖提取时的NaOH溶液浓度0.3 mol/L、料液比1∶20、提取温度60 ℃,考察提取时间对多糖得率的影响,结果见图3。
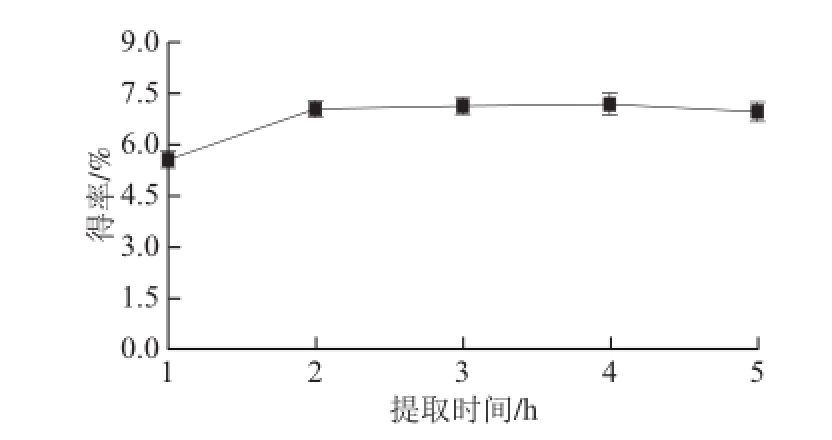
图3 提取时间对拟目乌贼生殖腺多糖得率的影响
Fig.3 Effect of extraction time on the yield of polysaccharides from Sepia lycidas gonad
由图3可知,提取时间在1~2 h范围内,拟目乌贼生殖腺多糖得率增加显著。当提取时间超过2 h后,多糖得率变化趋于平坦,继续延长提取时间对多糖得率影响较小。当提取时间超过4 h时,多糖得率反而出现一定程度的下降。综合分析选定提取时间2 h为最佳。
2.2.4 提取温度对拟目乌贼生殖腺多糖得率的影响
固定拟目乌贼生殖腺多糖提取时的NaOH溶液浓度0.3 mol/L、料液比1∶20、提取时间2 h,考察提取温度对多糖得率的影响,结果见图4。
由图4可知,当提取温度在50~70 ℃时,多糖得率随着提取温度的上升而增加,70 ℃时多糖得率达到最大值。提取温度从70 ℃开始,继续升高提取温度导致多糖得率显著降低。一定程度上的升高提取温度会增加样品材料的多糖溶出,提高多糖得率,但是过高的提取温度也会导致多糖降解。在提取过程中,提取温度为80、90 ℃时,提取液颜色较深,呈褐色,其他温度条件下的多糖提取液颜色较浅。综合分析选择提取温度70 ℃为最佳。
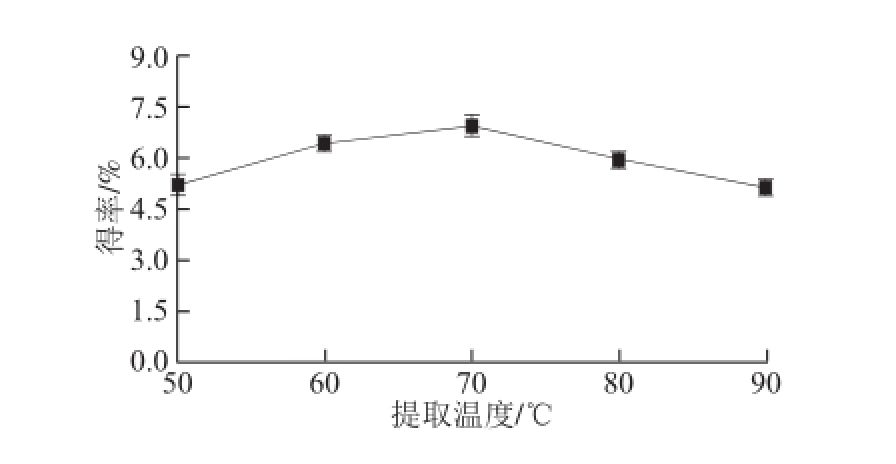
图4 提取温度对拟目乌贼生殖腺多糖得率的影响
Fig.4 Effect of extraction temperature on the yield of polysaccharides from Sepia lycidas gonad
2.3 正交试验结果
在单因素试验的基础上,选取NaOH溶液浓度(A)、料液比(B)、提取时间(C)和提取温度(D)为考察因素,进行L 9(3 4)正交试验,结果见表3、4。
表3 正交试验设计及结果
Table 3 Results of orthogonal array experiments
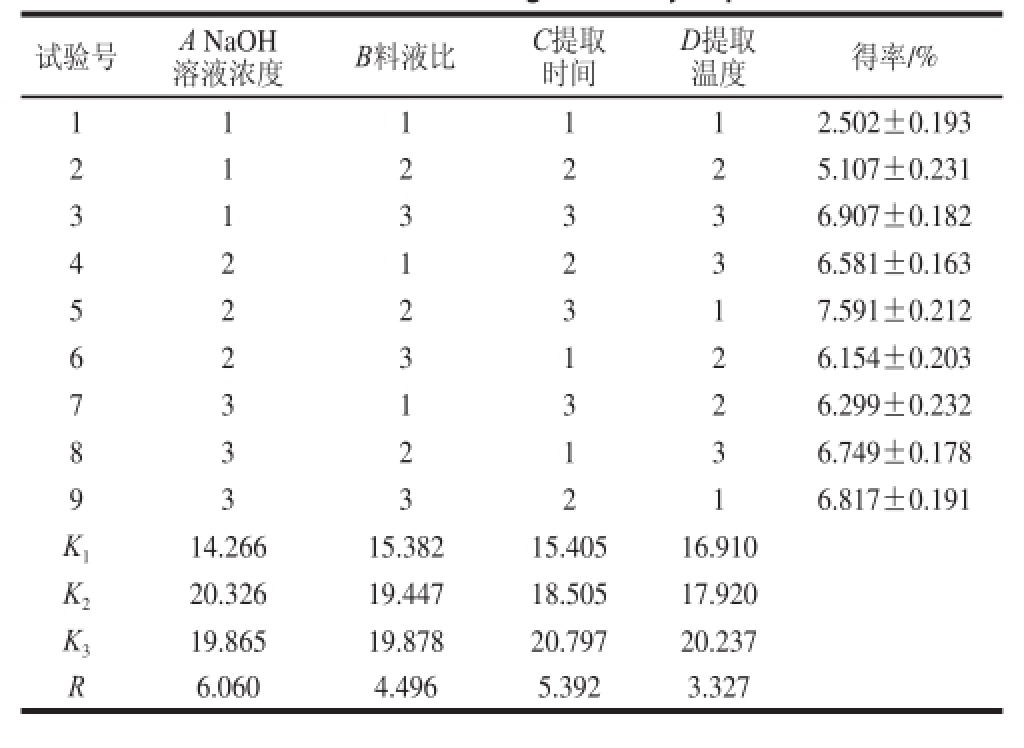
试验号A NaOH溶液浓度B料液比C提取时间D提取温度得率/% 1 112.502±0.193 2 1 2 225.107±0.231 1 1 3 336.907±0.182 4 2 1 2 36.581±0.163 1 3 5 317.591±0.212 6 2 3 126.154±0.203 2 2 7 326.299±0.232 8 3 2 136.749±0.178 3 1 216.817±0.191 K 114.26615.38215.40516.910 K 220.32619.44718.50517.920 K 319.86519.87820.79720.237 R6.0604.4965.3923.327 9 3 3
表4 方差分析
Table 4 Analysis of variance of orthogonal array experiments

注:**.P<0.01,差异极显著。
方差来源平方和自由度均方F值显著性A NaOH溶液浓度13.91226.956959.245** B料液比8.20624.103565.832** C提取时间9.76424.882673.246** D提取温度4.14722.074285.950**误差0.06590.007
根据表3、4可知,4 个因素极差值大小顺序为A>C>B>D,即影响拟目乌贼生殖腺多糖得率的主次因素为NaOH溶液浓度>提取时间>料液比>提取温度,4个因素都对拟目乌贼生殖腺多糖得率影响极显著。根据直观分析结果,拟目乌贼生殖腺多糖碱法提取最优工艺为A 2B 3C 3D 3,即NaOH溶液浓度0.3 mol/L、料液比1∶40、提取时间3 h、提取温度80 ℃。根据优选的最佳工艺,进行验证实验,拟目乌贼生殖腺多糖的得率为(7.697±0.191)%,显著高于扇贝 [30]、蛤蜊 [31]、牡蛎 [32]等海洋动物中提取多糖的得率。
2.4 拟目乌贼生殖腺粗多糖成分分析
采用苯酚-硫酸法和考马斯亮蓝法分别对拟目乌贼生殖腺粗多糖进行多糖和蛋白含量的测定,结果显示其多糖和蛋白含量分别为78.91%和14.86%,表明采用碱法提取得到的拟目乌贼生殖腺粗多糖中其主要成分是多糖,具有较高的纯度。
2.5 拟目乌贼生殖腺碱提多糖的抗氧化活性分析
2.5.1 还原力的测定结果
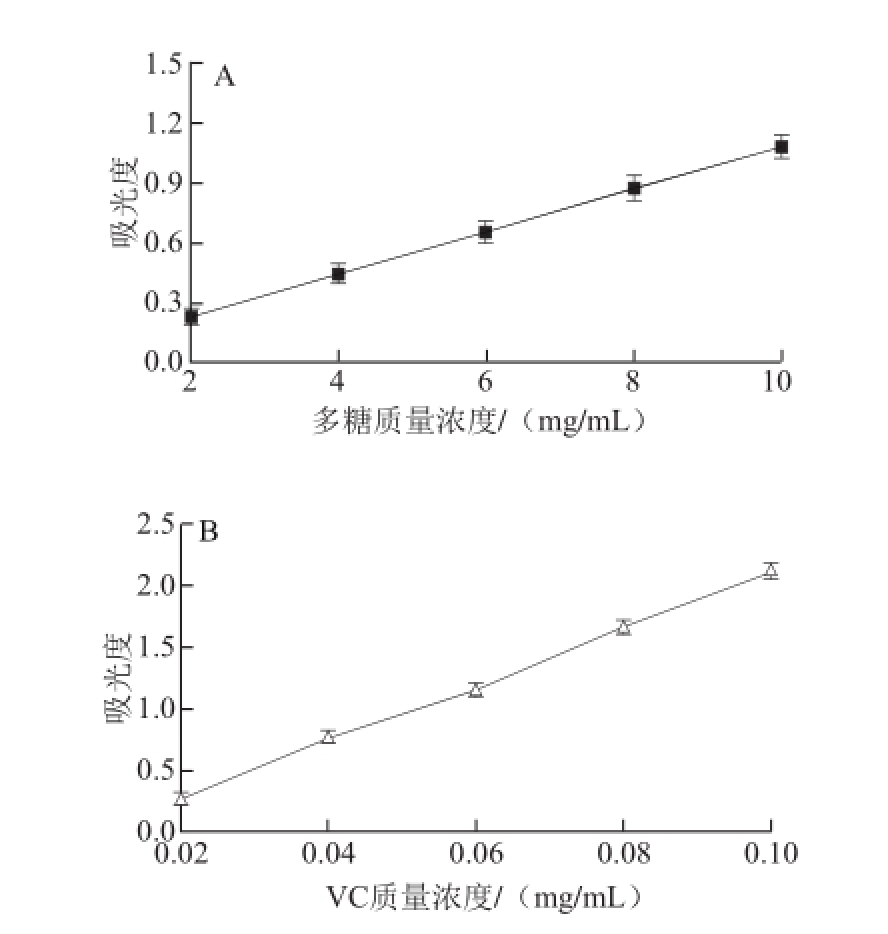
图5 多糖(A)和VC(B)对FFee
33+的还原能力
Fig.5 Ferric reducing power of Sepia lycidas gonad polysaccharides
在反应体系环境下,Fe 3+获得待测物质所提供的电子而被还原为Fe 2+,从而使得反应体系的颜色发生改变,使体系的吸光度增大,在波长700 nm处有最大吸收。吸光度越大,说明被测物质的还原力越强,抗氧化能力越强。由图5可知,拟目乌贼生殖腺碱提多糖具有一定的还原能力,但和VC相比还原力较小。随着多糖质量浓度的增加,其还原力逐渐增强,呈现良好的线性关系。当多糖质量浓度为10 mg/mL时,吸光度为1.08,高于同质量浓度条件下的乌贼墨汁多糖 [33]、四角蛤蜊多糖 [9]、厚壳贻贝多糖 [11]和扇贝性腺多糖 [12]吸光度。Zhu Beiwei等 [10]从鲍鱼脏器中提取多糖,当吸光度为0.2时,其多糖质量浓度约为9.25 mg/mL,而拟目乌贼生殖腺多糖质量浓度小于2 mg/mL。以上分析表明拟目乌贼生殖腺碱提多糖相对其他海洋动物多糖具有更高的还原力。
2.5.2 清除羟自由基能力的测定结果
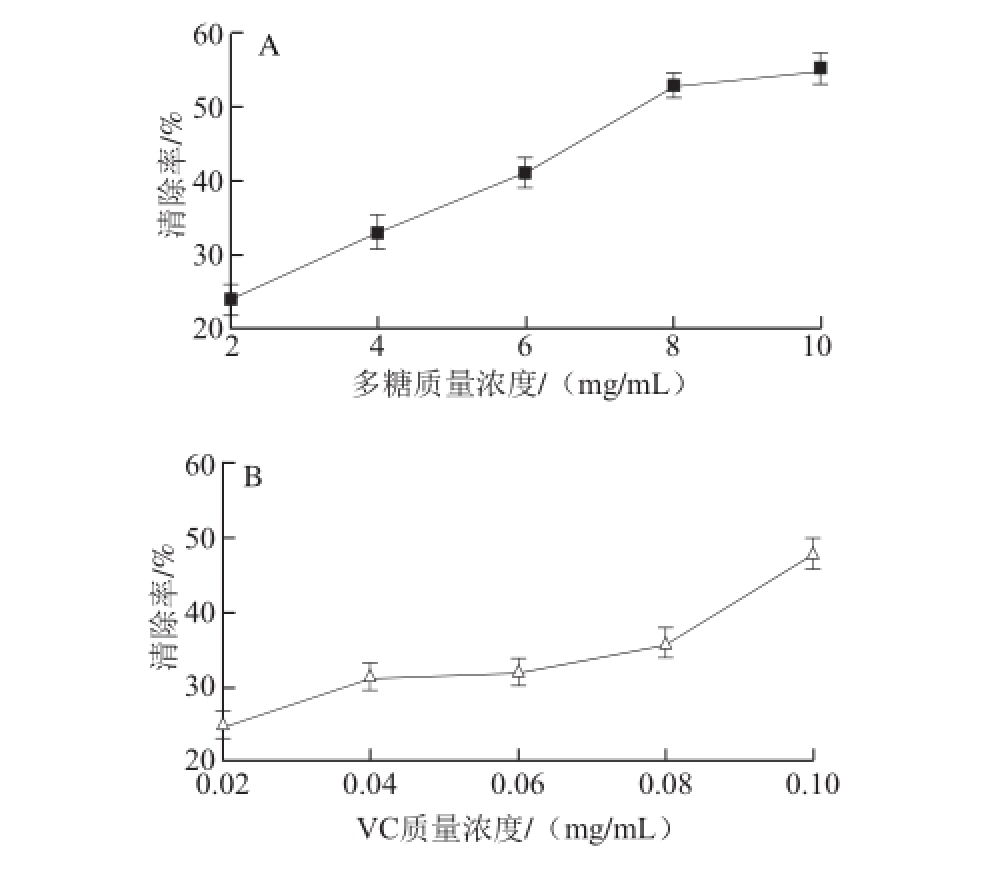
图6 多糖(A)和VC(B)对羟自由基的清除能力
Fig.6 Hydroxyl free radical scavenging abilities of Sepia lycidas gonad polysaccharides and VC
羟自由基是一类化学性质非常活泼的自由基,能夺取糖类、蛋白质、脂肪等生物分子中的氧原子,尤其是对脂质过氧化的作用最强,最终引发机体受损和基因突变,导致衰老和癌症的发生。本实验利用H 2O 2与Fe 2+混合产生羟自由基,在体系内加入水杨酸捕捉自由基并产生有色物质,在510 nm波长条件下具有最大吸收。由图6可知,拟目乌贼生殖腺碱提多糖对羟自由基具有一定的清除作用,随着多糖质量浓度的增加,清除率也逐渐增加,呈现良好的正量效关系。拟目乌贼生殖腺碱提多糖质量浓度为2 mg/mL时,对羟自由基的清除率为23.95%,高于同质量浓度条件下的翡翠贻贝多糖和牡蛎多糖 [34];多糖质量浓度为10 mg/mL时,清除率达到54.93%,高于同质量浓度条件下的乌贼墨多糖 [35]和鲍鱼脏器多糖 [36],与扇贝性腺多糖对羟自由基的清除能力相当 [12]。与植物类多糖相比,Tseng等 [37]从灵芝中提取多糖,当多糖质量浓度达到20 mg/mL时,对羟自由基清除率仅为22.4%。而拟目乌贼生殖腺碱提多糖质量浓度2 mg/mL时,其清除率为23.95%。以上分析表明拟目乌贼生殖腺碱提多糖具有良好的清除羟自由基能力。
2.5.3 清除DPPH自由基能力的测定结果
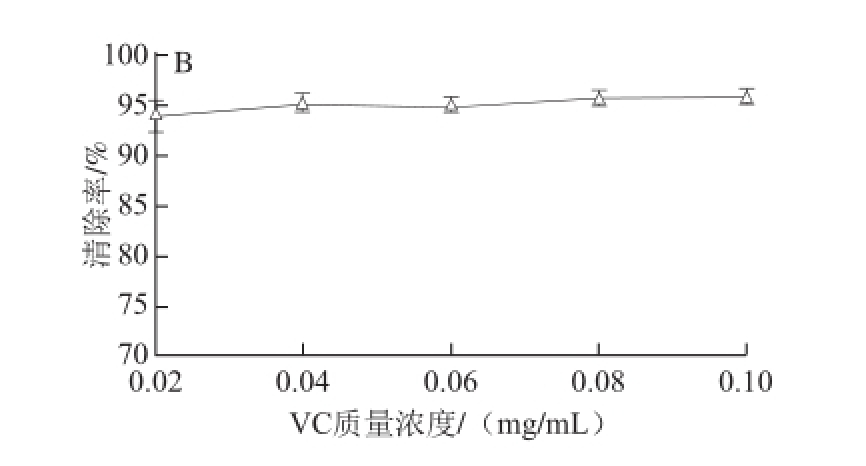
图7 多糖(A)和VC(B)对DPPH自由基的清除能力
Fig.7 DPPH free radical scavenging abilities of Sepia lycidas gonad polysaccharides and VC
由图7可知,随着拟目乌贼生殖腺碱提多糖质量浓度的增加,对DPPH自由基的清除率也逐渐增加,呈现出明显剂量正依赖关系。拟目乌贼生殖腺碱提多糖质量浓度为10 mg/mL时,对DPPH自由基清除率为76.06%,和同质量浓度条件下的厚壳贻贝酶提多糖 [11]的清除率接近。宋荪阳等 [12]从扇贝性腺中提取多糖,其质量浓度为10 mg/mL时,对DPPH自由基的清除率为51.9%。罗萍等 [35]对乌贼墨多糖抗氧化活性进行研究,质量浓度为14.25 mg/mL时,其清除率不足30%,与2 mg/mL的拟目乌贼生殖腺碱提多糖对DPPH自由基的清除率相当。综上表明拟目乌贼生殖腺碱提多糖是一种良好的DPPH自由基清除剂。
2.6 拟目乌贼生殖腺碱提多糖的吸湿性和保湿性
2.6.1 吸湿性分析
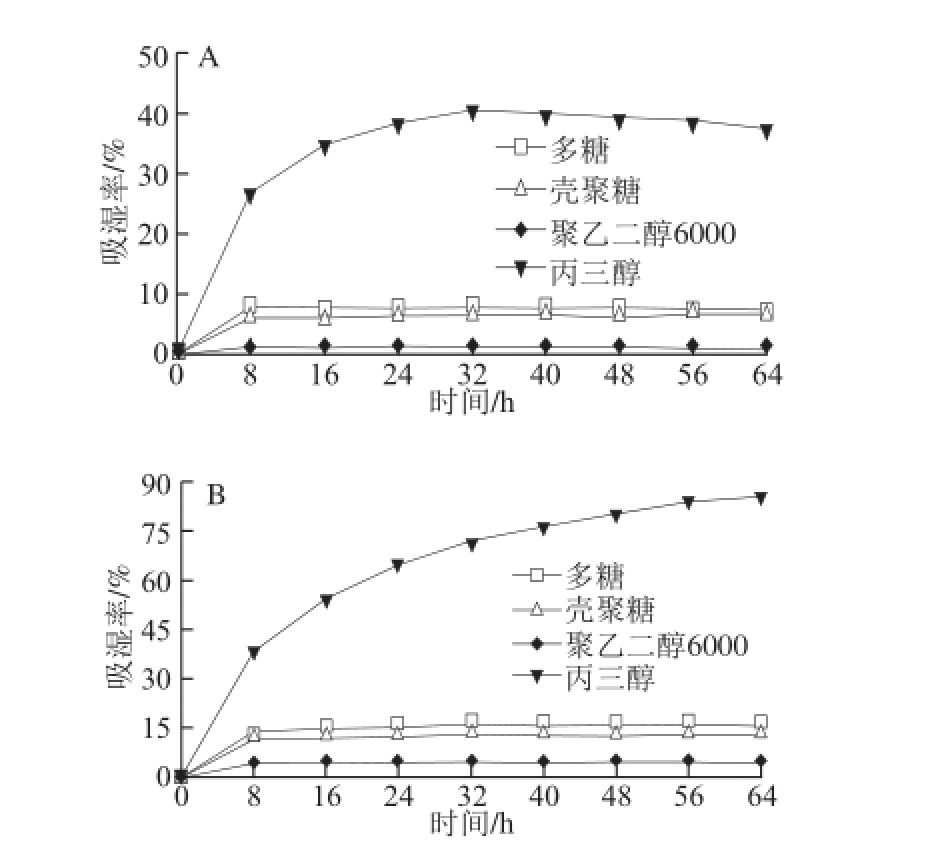
图8 相对湿度43%(AA)和81%(B)条件下多糖和常规保湿剂的吸湿率比较
Fig.8 Hygroscopicity of Sepia lycidas gonad polysaccharides compared with traditional humectants at RHs of 43% (A) and 81% (B)
如图8A所示,在低湿度(43%)条件下,拟目乌贼生殖腺碱提多糖的吸湿率高于壳聚糖和聚乙二醇6000,低于丙三醇。多糖、壳聚糖、聚乙二醇6000和丙三醇的吸湿率在0~8 h内增长较快,8 h后多糖、壳聚糖和聚乙二醇6000的吸湿基本饱和,此时多糖的吸湿率为7.9%,壳聚糖和聚乙二醇6000的吸湿率分别为6.1%和1.3%。丙三醇在吸湿32 h后达到最大吸湿率40.5%,然后吸湿率开始缓慢降低,其他样品吸湿率基本稳定不变。邓一清等 [15]对近江牡蛎、翡翠贻贝、马氏贝和企鹅珍珠贝多糖在相对湿度43%条件下进行吸湿性研究,结果表明在吸湿12 h后达到最大吸湿率,均只有3%左右,显著低于拟目乌贼生殖腺碱提多糖。如图8B所示,在高湿度(81%)条件下,拟目乌贼生殖腺碱提多糖、壳聚糖和聚乙二醇6000在吸湿8 h后吸湿率变化缓慢,32 h后吸湿率达到最大值,分别为16.3%、13.2%、4.8%,其中多糖吸湿率高于壳聚糖和聚乙二醇。丙三醇具有较高的吸湿性,在吸湿56 h后吸湿率基本达到饱和,吸湿率为84.1%,高于拟目乌贼生殖腺碱提多糖。曲敏等 [17]对贻贝多糖的吸湿性能进行研究,在81%条件下吸湿12 h后达到最大吸湿率11.29%,低于拟目乌贼生殖腺碱提多糖的最大吸湿率16.3%。高瑞英等 [38]对几种生物活性多糖吸湿保湿性能进行研究,结果显示透明质酸、鲨鱼软骨素在81%条件下的最大吸湿率和拟目乌贼生殖腺碱提多糖相当;而在43%条件下透明质酸、鲨鱼软骨素、海藻酸钠、卡拉胶寡糖的吸湿率均小于拟目乌贼生殖腺碱提多糖。综上分析表明拟目乌贼生殖腺碱提多糖具有良好的吸湿性能,可作为吸湿剂开发利用。
2.6.2 保湿性分析
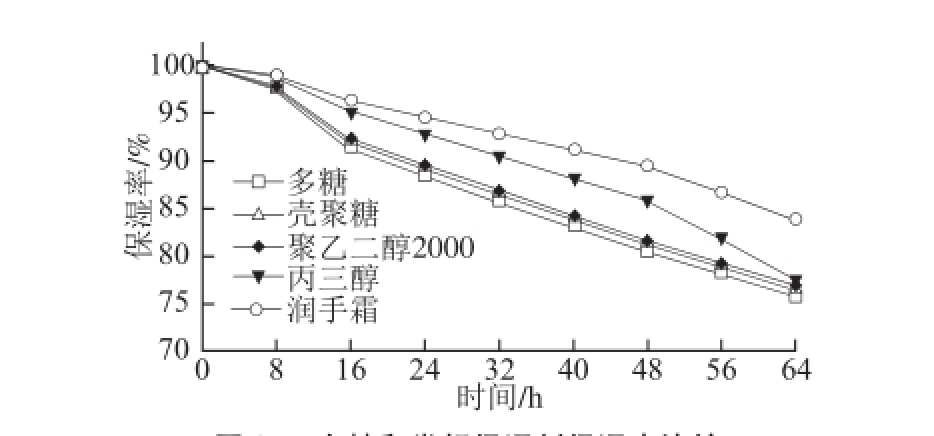
图9 多糖和常规保湿剂保湿率比较
Fig.9 Moisture retention ability of Sepia lycidas gonad polysaccharides compared with traditional humectants
拟目乌贼生殖腺碱提多糖、常规保湿剂(壳聚糖、聚乙二醇6000、丙三醇)和馥佩貂油润手霜在硅胶干燥环境中的保湿性能如图9所示。随着时间的延长,各样品的保湿率均逐渐降低。拟目乌贼生殖腺碱提多糖在硅胶干燥环境中放置64 h后保湿率为75.7%,与壳聚糖、聚乙二醇6000、丙三醇的保湿率相当。保湿时间在0~56 h时,多糖、壳聚糖和聚乙二醇6000的变化曲线类似,保湿率均较接近。多糖在0~56 h时的保湿率低于丙三醇,但64 h后和丙三醇保湿率接近。馥佩貂油润手霜的保湿性相对其他几种样品较好,在64 h后其保湿率为83.7%。拟目乌贼生殖腺碱提多糖在硅胶干燥环境中放置48 h后的保湿率高于同条件下的近江牡蛎多糖、翡翠贻贝多糖、马氏珠母贝多糖、企鹅珍珠贝多糖 [15]和四角蛤蜊多糖 [9]。与植物多糖保湿性能相比,拟目乌贼生殖腺碱提多糖在放置48 h后的保湿率高于绿色巴夫藻多糖 [39]、金荞麦多糖 [40]以及银耳多糖、燕麦多糖和麦冬多糖 [41]。综上分析表明,拟目乌贼生殖腺碱提多糖具有良好的保湿性能。
采用正交试验优化拟目乌贼生殖腺多糖碱法提取工艺,得到拟目乌贼生殖腺多糖碱提最佳工艺:NaOH溶液浓度0.3 mol/L、料液比1∶40、提取时间3 h、提取温度80 ℃。此条件下多糖得率为7.697%,显著高于拟目乌贼生殖腺水提法多糖得率 [42],同时也高于其他海洋软体动物多糖得率 [30-32],表明该优化工艺参数能够较好地提取拟目乌贼生殖腺多糖,指导其生产和综合开发利用。
目前,市场上许多人工合成的抗氧化剂如叔丁基羟基茴香醚、2,6-二叔丁基对甲酚和特丁基对苯二酚等被广泛用作食品添加剂,然而这些抗氧化剂可能有诱导癌症发生的潜在危险 [43],因此开发具有无危害的新型天然抗氧化剂具有重要意义。本实验中拟目乌贼生殖腺多具有一定的还原能力,对DPPH自由基和羟自由基的清除效果较好,表现出良好的抗氧化活性,优于扇贝多糖 [12]、乌贼墨多糖 [35]等海洋动物多糖。采用邻苯三酚法对拟目乌贼生殖腺碱提多糖清除超氧阴离子自由基的能力进行测定时,呈现负清除率,与刘俊等 [44]对三角帆蚌多糖的研究结果类似。分析原因可能是该多糖分子中含有大量的羟基,超氧阴离子自由基在加速邻苯三酚的自氧化的同时,也加速这些物质的自氧化,产生更多的超氧阴离子自由基,从而呈现负清除作用 [44]。
传统的保湿剂,如甘油、丙二醇等,由于吸湿性太强,当空气干燥时,会从皮肤中吸收一定量的水分,对皮肤造成伤害 [15]。目前在化妆品开发领域,具有天然活性的多糖等物质正在逐步取代甘油等常规保湿剂,因此研究海洋贝类多糖的吸湿保湿性具有重要意义。拟目乌贼生殖腺碱提多糖具有良好的吸湿保湿效果,在相对湿度43%和相对湿度81%条件下的最大吸湿率分别为7.9%和16.3%,高于常规保湿剂壳聚糖、聚乙二醇6000;在相对湿度43%条件下的吸湿率高于透明质酸、鲨鱼软骨素、海藻酸钠、卡拉胶寡糖等海洋生物多糖 [38];在相对湿度81%条件下的吸湿率高于贻贝多糖 [17],与透明质酸、鲨鱼软骨素的吸湿率接近。拟目乌贼生殖腺碱提多糖的保湿效果与壳聚糖、聚乙二醇6000接近,硅胶环境中放置64 h后和丙三醇的保湿率相当,高于四角蛤蜊多糖 [9]和其他植物多糖 [39-41]的保湿率。拟目乌贼生殖腺碱提多糖的吸湿保湿性均高于近江牡蛎多糖、翡翠贻贝多糖、马氏珠母贝多糖和企鹅珍珠贝多糖 [15]。综上分析表明,拟目乌贼生殖腺碱提多糖具有良好的吸湿保湿性能,可作为一种优良的天然保湿剂开发利用。
参考文献:
[1] 陈新军, 刘必林, 王尧耕. 世界头足类[M]. 北京: 海洋出版社, 2009: 440-441.
[2] 彭瑞冰, 蒋霞敏, 于曙光, 等. 几种生态因子对拟目乌贼胚胎发育的影响[J]. 生态学报, 2013, 33(20): 6560-6568. DOI:10.5846/ stxb201301260167.
[3] 陈道海, 郭永平, 文菁, 等. 不同盐度下拟目乌贼(Sepia lycidas)胚胎发育过程研究[J]. 海洋与湖沼, 2013, 44(5): 1283-1287.
[4] 陈道海, 徐海洪, 蔡文飞, 等. 拟目乌贼幼体日摄食量及其对体重影响[J]. 氨基酸和生物资源, 2012, 34(4): 67-70. DOI:10.3969/ j.issn.1006-8376.2012.04.016.
[5] 蔡文飞, 徐海洪, 陈道海. 温度对拟目乌贼幼体日生长率和存活率的影响[J]. 氨基酸和生物资源, 2012, 34(4): 63-66. DOI:10.3969/ j.issn.1006-8376.2012.04.015.
[6] 陈道海, 颜蓉, 文菁, 等. 盐度对拟目乌贼受精卵卵径、重量和孵化率的影响[J]. 氨基酸和生物资源, 2013, 35(3): 8-12.
[7] 蒋霞敏, 彭瑞冰, 罗江, 等. 野生拟目乌贼不同组织营养成分分析及评价[J]. 动物营养学报, 2012, 24(12): 2393-2410. DOI:10.3969/ j.issn.1006-267x.2012.12.014.
[8] 丁保金, 金丽琴, 吕建新. 多糖的生物活性研究进展[J]. 中国药学杂志, 2004, 39(8): 561-564. DOI:10.3321/j.issn:1001-2494.2004.08.001.
[9] 刘新, 王令充, 吴皓, 等. 四角蛤蜊多糖的吸湿保湿性及体外抗氧化性研究[J]. 食品工业科技, 2012, 33(24): 85-88. DOI:10.13386/ j.issn1002-0306.2012.24.080.
[10] ZHU B W, WANG L S, ZHOU D Y, et al. Antioxidant activity of sulphated polysaccharide conjugates from abalone[J]. European Food Research and Technology, 2008, 227(6): 1663-1668. DOI:10.1007/ s00217-008-0890-2.
[11] 钟城城, 曲有乐, 陈荫. 厚壳贻贝多糖的提取工艺优化及体外生物活性研究[J]. 食品科学, 2014, 35(10): 107-114. DOI:10.7506/ spkx1002-6630-201410020.
[12] 宋荪阳, 孙黎明, 朱蓓薇, 等. 扇贝性腺多糖提取物的抗氧化及免疫调节活性[J]. 食品科学, 2012, 33(5): 248-251.
[13] ZIERER M S, MOURAO P S. A wide diversity of sulfated polysaccharides are synthesized by different species of marine sponges[J]. Carbohydrate Research, 2000, 328(2): 209-216. DOI:10.1016/S0008-6215(00)00076-8.
[14] 李江滨, 黄迪南. 贻贝的药用价值研究进展[J]. 水产科学, 2004, 23(11): 43-44. DOI:10.3969/j.issn.1003-1111.2004.11.015.
[15] 邓一清, 童银洪, 陈小丽, 等. 4 种海洋贝类多糖提取和保湿性研究[J]. 广东海洋大学学报, 2012, 32(3): 86-89. DOI:10.3969/ j.issn.1673-9159.2012.03.017.
[16] 曲敏, 黄万成, 李伟, 等. 鲍鱼内脏多糖水洗面膜的制备及性能评价[J]. 河北渔业, 2013(1): 10-12. DOI:10.3969/ j.issn.1004-6755.2013.01.003.
[17] 曲敏, 王丽云, 李伟, 等. 贻贝多糖润肤霜的制备及性能评价[J]. 河北渔业, 2013(2): 5-7. DOI:10.3969/j.issn.1004-6755.2013.02.002.
[18] 刘新, 王令充, 吴皓. 与护肤功能相关的海洋多糖研究进展[J]. 食品工业科技, 2013, 34(5): 372-375. DOI:10.13386/ j.issn1002-0306.2013.05.041.
[19] 赵芙钗. 栉孔扇贝和海湾扇贝的生殖腺的基本营养成分分析及其多糖的免疫活性测定[D]. 青岛: 中国海洋大学, 2012.
[20] 王志聪, 王竹清, 倪鑫, 等. 皱纹盘鲍性腺多糖的抗疲劳作用[J]. 中国海洋药物, 2011(5): 34-38.
[21] 李韬, 周大勇, 杨静峰, 等. 皱纹盘鲍性腺多糖抗氧化活性研究[J]. 水产科学, 2009, 28(4): 179-182. DOI:10.3969/ j.issn.1003-1111.2009.04.001.
[22] 徐美玲, 孙黎明, 周大勇, 等. 皱纹盘鲍性腺多糖体外免疫活性和抗凝血活性的研究[J]. 水产科学, 2009, 28(9): 498-500. DOI:10.3969/ j.issn.1003-1111.2009.09.003.
[23] 王少华, 张慧, 郭承华. 马粪海胆生殖腺多糖的抑菌和抗氧化活性研究[J]. 食品研究与开发, 2012, 33(12): 16-18.
[24] 沈鸿, 窦昌贵. 河蚌多糖提取工艺的优化[J]. 时珍国医国药, 2006, 17(3): 380-381. DOI:10.3969/j.issn.1008-0805.2006.03.037.
[25] 宁正祥. 食品成分分析手册[M]. 北京: 中国轻工业出版社, 1998: 9-10.
[26] YUAN J F, ZHANG Z Q, FAN Z C, et al. Antioxidant effects and cytotoxicity of three purified polysaccharides from Ligusticum chuanxiong Hort[J]. Carbohydrate Polymers, 2008, 74(4): 822-827. DOI:10.1016/j.carbpol.2008.04.040.
[27] LIU X, SUN Z L, ZHANG M S, et al. Antioxidant and antihyperlipidemic activities of polysaccharides from sea cucumber Apostichopus japonicus[J]. Carbohydrate Polymers, 2012, 90(4): 1664-1670. DOI:10.1016/j.carbpol.2012.07.047.
[28] YEN G C, HSIEH P P. Antioxidative activity and scavenging effects on active oxygen of xyiose-lysine Maillard reaction products[J]. Journal of the Science of Food and Agriculture, 1995, 67(3): 415-420. DOI:10.1002/jsfa.2740670320.
[29] 祝士惠, 孙培冬, 李海洋. 画眉草多糖提取及其保湿性能研究[J].天然产物研究与开发, 2013, 25(1): 83-86. DOI:10.3969/ j.issn.1001-6880.2013.01.020.
[30] 李雪梅, 苏运聪, 王颉. 响应面法优化水溶性扇贝多糖的提取工艺[J].中国食品学报, 2014, 14(2): 127-131.
[31] 舒留泉, 姚晶, 杨苏梅, 等. 四角蛤蜊多糖分离提取工艺优化[J]. 食品研究与开发, 2012, 33(6): 71-74. DOI:10.3969/ j.issn.1005-6521.2012.06.020.
[32] 田振华, 李永斌, 李颖, 等. 牡蛎多糖制备工艺优化及体外抑菌活性的探讨[J]. 食品研究与开发, 2013, 34(17): 23-26. DOI:10.3969/ j.issn.1005-6521.2013.17.007.
[33] 孙楠楠, 李和生, 张丽媛, 等. 乌贼墨汁多糖的提取及抗氧化作用研究[J]. 食品科学, 2011, 32(22): 95-99.
[34] 卢卫红, 陈忻, 朱峰. 两种海洋贝类多糖的提取及其生物活性评价[J]. 南方农业学报, 2014, 45(10): 1846-1850. DOI:10.3969/ j:issn.2095-1191.2014.10.1846.
[35] 罗萍, 师莉莎, 刘华忠. 乌贼墨多糖的体外抗氧化作用[J]. 食品研究与开发, 2013, 34(8): 1-4.
[36] 罗晓航. PEF结合酶法提取鲍鱼脏器粗多糖及其抗氧化活性研究[D].福州: 福建农林大学, 2012.
[37] TSENG Y H, YANG J H, MAU J L. Antioxidant properties of polysaccharides from Ganoderma tsugae[J]. Food Chemistry, 2008, 107(2): 732-738. DOI:10.1016/j.foodchem.2007.08.073.
[38] 高瑞英, 张秀宇, 慕丹, 等. 透明质酸等化妆品用生物活性多糖吸湿保湿性能测定[J]. 广东化工, 2009, 36(10): 230-232. DOI:10.3969/ j.issn.1007-1865.2009.10.105.
[39] 王凌, 孙利芹. 绿色巴夫藻多糖及降解产品的抗氧化和保湿性能[J].食品科学, 2012, 33(21): 87-90.
[40] 黄仁术, 谷仿丽, 何晓梅. 金荞麦多糖的吸湿保湿性能研究[J]. 化工新型材料, 2014, 42(6): 141-142.
[41] 陈刚, 郭晓蕾, 宝丽. 银耳、麦冬、燕麦多糖的抗氧化活性及吸湿保湿性能研究[J]. 中华中医药学刊, 2013, 31(1): 212-214.
[42] 戴宏杰, 孙玉林, 陈道海, 等. 拟目乌贼生殖腺多糖提取工艺优化及自由基清除能力研究[J]. 食品工业科技, 2015, 36(5): 197-203.
[43] BOTTERWECK A A M, VERHAGEN H, GOLDBOHM R A, et al. Intake of butylated hydroxyanisole and butylated hydroxytoluene and stomach cancer riskresults from analyses in the Netherlands cohort study[J]. Food and Chemical Toxicology, 2000, 38: 599-605. DOI:10.1016/S0278-6915(00)00042-9.
[44] 刘俊, 张燕平, 戴志远, 等. 三角帆蚌多糖的提取及其抗氧化功能研究[J]. 食品科技, 2008, 33(12): 40-44. DOI:10.3969/ j.issn.1005-9989.2008.12.011.
Antioxidant Activity, Moisture Absorption and Retention Capacities of Alkali-Soluble Polysaccharides Extracted from Gonad of Sepia lycidas
DAI Hongjie
1,2, SUN Yulin
1,2, YANG Meiyu
2, XIN Xinxin
2, FENG Zixin
2, WEN Jing
1,2, CHEN Daohai
1,*
(1. Round Beibu Gulf Institute for the Protection and Utilization of Marine Animals in Medicine, Lingnan Normal University, Zhanjiang 524048, China; 2. College of Life Science and Technology, Lingnan Normal University, Zhanjiang 524048, China)
Abstract:The extraction of alkali-soluble polysaccharides from the gonad of Sepia lycidas was investigated, and the antioxidant activity, moisture absorption and retention capacities of the extracted polysaccharides were evaluated. The optimal extraction conditions were determined as follows: NaOH concentration, 0.3 mol/L; solid/liquid ratio, 1:40; extraction time, 3 h; and extraction temperature, 80 ℃, respectively. Under these conditions, the extraction yield of polysaccharides was 7.697%. Antioxidant assays showed that the polysaccharides possessed good radical scavenging activity against hydroxyl and DPPH radicals in a marked dose-dependent manner. Moisture absorption capacity of Sepia lycidas gonad polysaccharides was better than that of chitosan, polyethylene glycol 6000 and other conventional humectants, and moisture retention capacity was close to that of chitosan, polyethylene glycol 6000 and glycerol. The moisture absorption and retention capacity of Sepia lycidas gonad polysaccharides were better than those of the polysaccharides from Perna viridis, Crassostrea rivularis and other marine animals. These results clearly established the possibility that Sepia lycidas gonad polysaccharides could be effectively employed as a natural antioxidant and moisturizer.
Key words:Sepia lycidas gonad; polysaccharides; antioxidant activity; moisture absorption; moisture retention
DOI:10.7506/spkx1002-6630-201602006
中图分类号:TS202.3
文献标志码:A
文章编号:1002-6630(2016)02-0031-08
引文格式:
戴宏杰, 孙玉林, 杨梅语, 等. 拟目乌贼生殖腺碱提多糖的抗氧化及吸湿保湿特性[J]. 食品科学, 2016, 37(2): 31-38.DOI:10.7506/spkx1002-6630-201602006. http://www.spkx.net.cn
DAI Hongjie, SUN Yulin, YANG Meiyu, et al. Antioxidant activity, moisture absorption and retention capacities of alkali-soluble polysaccharides extracted from gonad of Sepia lycidas[J]. Food Science, 2016, 37(2): 31-38. (in Chinese with English abstract) DOI:10.7506/spkx1002-6630-201602006. http://www.spkx.net.cn
收稿日期:2015-04-27
基金项目:中央财政支持地方高校发展专项(0003015119);广东省自然科学基金项目(2015A030310406);广东省科技厅项目(2014B040404071);广东“特支计划”项目(2014TQ01N621);广东省省部产学研合作专项(2013B090500036);湛江市财政资金科技专项竞争性分配项目(2013A05004);湛江市科技攻关计划项目(2014A03011);岭南师范学院博士启动项目(ZL1313);中国科学院热带海洋生物资源与生态重点实验室开放基金项目(LMB131006)
作者简介:戴宏杰(1990—),男,硕士研究生,研究方向为农产品加工与贮藏。E-mail:daihjdemo@163.com
*通信作者:陈道海(1963—),男,教授,博士,研究方向为海洋生物学。E-mail:dhchen11@21cn.com