
图1 CdTe量子点的紫外吸收光谱(1)和荧光发射光谱(2)
Fig.1 UV-vis absorption (1) and fluorescence spectra (2) of CdTe QDs
王蓓蓓 1,2,商 欢 1,王 琪 1,马美湖 1,蔡朝霞 1,*
(1.国家蛋品加工技术研发分中心,华中农业大学食品科学技术学院,湖北 武汉 430070;2.安徽科技学院食品药品学院,安徽 凤阳 233100)
摘 要:基于CdTe量子点作为荧光探针建立了一种定量检测皮蛋中微量铜(Cu 2+)的荧光分析法。采用巯基乙酸和1-硫丙三醇作为稳定剂,水相中快速制得荧光性好、稳定性好的水溶性CdTe量子点,并运用紫外-可见分光光度和荧光光谱法研究CdTe量子点的发光特性。实验探究了Cu 2+对CdTe量子点荧光猝灭的机理,并根据Cu 2+浓度和荧光强度下降量之间的关系,在Cu 2+浓度范围为10~200 nmol/L时建立定量检测微量Cu 2+的线性方程,相关系数高达0.997,检出限低至0.96 nmol/L。本实验方法已经初步应用于皮蛋样品中Cu 2+的检测,结果显示相对标准偏差在1.47%~3.01%之间,回收率为104%~108%,说明了此方法的准确性、可靠性和适用性。
关键词:量子点;荧光猝灭;铜离子;皮蛋
皮蛋是我国传统生食蛋制品,凭借其独特风味和较高的营养价值深受广大消费者喜爱 [1]。目前,国内皮蛋生产工艺虽由传统的氧化铅法改革为“铜浸法”和“铜锌混合法”,但是铜作为微量元素,一旦摄入超标,会对人体健康造成危害。对于铜添加量以及在皮蛋中的残留量,国家尚无明确规定,但是可参考国家标准中对肉制品中铜含量的限量规定(不大于10 mg/kg) [2-3]。有研究 [4-5]报道,铜清料法加工皮蛋的时,鸭蛋在料液中长时间浸泡,铜离子可能由壳外渗进壳内,致使蛋内铜离子含量升高。因此,准确快速检测新型无铅皮蛋中铜的残留,对保障消费者安全健康以及促进皮蛋行业发展都具有重要的现实意义。
传统铜离子的检测多依赖于原子吸收光谱法 [6]、电感耦合等离子体-质谱法 [7]、电感耦合等离子体-原子发射光谱法 [8]、分光光度测定法 [9]、循环伏安法 [10]等。这些方法灵敏度高和精确度好,但是操作繁琐、复杂、耗时长,所需的仪器昂贵,不利于推广使用。
量子点作为新型的纳米材料,化学稳定性和抗光漂白性强,量子产率高,激发谱带宽,发射光谱窄,而且制备方法简便、成本低廉,因此可作为荧光探针应用于分析检测领域 [11-13]。尤其在痕量金属离子分析检测中,由于不同金属离子会猝灭或增强量子点荧光,因此可用于简便快速的检测金属离子 [14-15]。Chen Yongfen等 [16]分别运用硫代甘油和半胱氨酸包被的CdS量子点作为荧光探针检测铜离子和锌离子,并由此提出了以量子点为荧光探针选择性检测金属阳离子的新方法。王柯敏等 [17]则选用以巯基乙酸为稳定剂合成的水溶性CdTe量子点检测Cu 2+。早期已经有研究表明,锌离子、锰离子和镉离子能增强CdS和ZnS量子点的荧光性 [18-19],相反,某些重金属如铜离子、汞离子,能够有效猝灭量子点荧光 [20]。
本实验借鉴前人的研究基础,采用巯基乙酸和1-硫丙三醇作为混合稳定剂,水相合成CdTe量子点,基于铜离子对CdTe量子点的猝灭效应建立定量检测铜离子的分析方法,并对量子点的猝灭机理进行了探讨。实验建立的方法初步应用于皮蛋中微量铜的测定,操作简单、灵敏度好、结果准确。
1.1 材料与试剂
无铅皮蛋 湖北神丹健康食品有限公司;甘氨酸、L-谷氨酸、牛血清蛋白(均为为分析纯) 上海伯奥生物科技有限公司;碲粉、硼氢化钠、巯基乙酸、1-硫丙三醇、氯化镉、氢氧化钠、高氯酸、硝酸、葡萄糖、乳糖和各种无机盐试剂均为国产分析纯;实验用水均为超纯水。
Cu 2+离子标准储备液:精确称CuSO 4·5H 2O,超纯水溶解后转移至容量瓶,定容,备用。
1.2 仪器与设备
RF-5301PC型荧光分光光度计、AA600型原子吸收光谱仪、AA800型自动进样器 日本岛津公司;Nanodrop 2000c型紫外分光光度计 美国热电公司;3-30N型台式低温冷冻离心机 美国Sigma公司;AR2140型分析天平梅特勒-托利多仪器有限公司;PHS-3型pH计 上海精密科学仪器有限公司;SZCL-2A型磁力搅拌器 上海东玺制冷设备有限公司。
1.3 方法
1.3.1 水溶性CdTe量子点的制备
CdTe量子点的水相合成法参考文献[21]。在20 mL的小玻璃瓶中加入26.70 mg Te粉、43.60 mg NaBH 4、1.50 mL双蒸水,迅速用带有针头的橡胶塞密闭玻璃瓶口,以排出反应产生的氢气。置于避光处进行反应。待黑色Te粉完全溶解,溶液变为澄清的淡紫红色液体,得到NaHTe溶液。
将一定量巯基乙酸和1-硫丙三醇作为混合稳定剂加入到160 mL CdCl 2溶液中,其中Cd 2+∶稳定剂∶HTe -的物质的量比例为1.00∶2.40∶0.25。溶液用1 mol/L的NaOH溶液调节pH值到11.2。将所配制的CdCl 2前驱液倒入四颈磨口烧瓶中,采用磁力控温搅拌加热30 min,在N 2保护条件下迅速用注射器抽取新制的NaHTe溶液注入CdCl 2溶液,于95~97 ℃条件下回流加热1 h,得到黄色透明CdTe量子点溶液。向上述制备好的CdTe量子点溶液中加入3 倍体积的冰乙醇溶液,搅拌均匀后离心,离心机转速为8 000 r/min,时间10 min,弃去上层清液,将底部沉淀用等体积的二次蒸馏水溶解。重复上述操作2 次,即可得到提纯后的水溶性CdTe量子点溶液。
采用紫外分光光度计于室温条件下测定制备的CdTe量子点溶液的紫外吸收光谱,采用荧光分光光度计获得其荧光发射图谱,其中荧光光谱扫描时设定激发波长为330 nm,激发光和发射光狭缝宽度为5 nm。扫描范围为400~700 nm。
1.3.2 荧光猝灭法检测铜离子
在5 mL离心管中注入2 mL 0.01 mol/L pH值为7.4的磷酸盐缓冲溶液和50 μL CdTe量子点溶液和一定量的Cu 2+溶液。室温条件下静置反应30 min,反应后的溶液用荧光分光光度计在常温条件下进行荧光扫描,测定反应体系的荧光发射图谱,激发波长设定为330 nm,激发光和发射光狭缝宽度均为5 nm。观察反应后荧光发射光谱图的荧光强度变化,根据荧光强度的变化规律建立定量检测方法。
1.3.3 实际样品分析
称取2.5 g左右皮蛋,置于消化管中,加入50 mL混酸(高氯酸∶硝酸= 1∶4,V/V,以浓酸为基准),置于电炉上采取180 ℃高温消化40 min至溶液澄清。之后调整温度至400 ℃高温消化50 min至冒白烟。取下消化管冷却后添加15 mL蒸馏水继续于400 ℃高温加热进行赶酸约15 min,当溶液剩余3 mL左右时取出定容至50 mL,并采用0.22 μm超滤膜进行过滤。实验重复3 次。

图1 CdTe量子点的紫外吸收光谱(1)和荧光发射光谱(2)
Fig.1 UV-vis absorption (1) and fluorescence spectra (2) of CdTe QDs
由图1可见(线1),CdTe量子点在波长463 nm处具有明显的激子吸收峰。由激子最大吸收峰的波长,按照拟合公式 [20],可计算出量子点的粒径为2.0 nm左右,证明成功合成了半导体纳米材料CdTe量子点。而且本实验合成的量子点比一般实验中合成的粒径略小,根据已有的研究可知,粒径较小的量子点与金属离子反应的灵敏度和选择性更高,这是本实验制备的CdTe量子点作为纳米荧光探针进行快速灵敏定量检测Cu 2+的基础。由图1可见(线2),合成的CdTe量子点发射光谱位于波长501 nm处,半峰宽为34 nm,峰形窄且十分对称,说明所得纳米粒子尺寸分布比较窄,粒径均一。且斯托克斯位移大,能够避免发射谱与激发谱重叠,从而允许在低信号强度的情况下进行光谱学检测。
2.2 Cu 2+猝灭CdTe量子点荧光的反应机理探讨
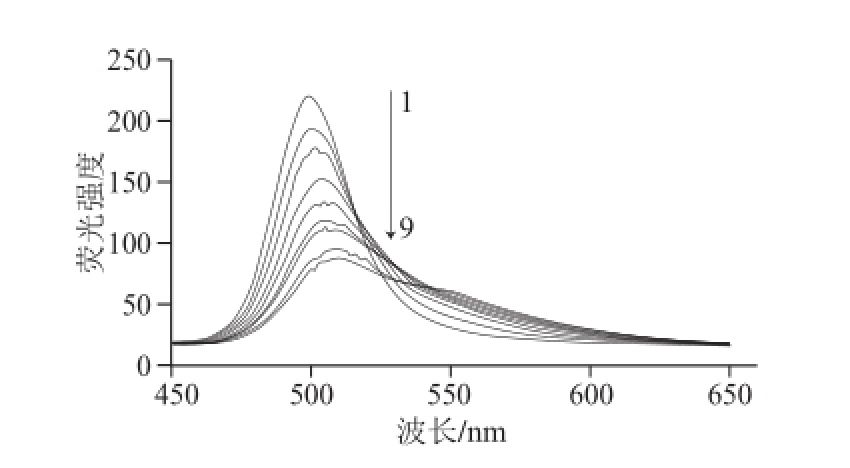
图2 优化条件下CdTe量子点的荧光强度在不同浓度铜离子溶液中的变化
Fig.2 Changes in fluorescence spectra of CdTe QDs due to the presence of different concentrations of Cu
2+under optimal experimental conditions
1.空白;2~9.铜离子浓度分别为25、50、75、100、120、140、180、200 nmol/L。
由图2可知,随着Cu 2+浓度的增加,体系最大发射波长处的荧光强度呈现规律性下降,这是建立出定量检测Cu 2+的荧光分析法的基础。由图2还可观察到,荧光峰的最大发射波长发生了红移和半峰宽的宽化。Cu 2+浓度增长了10 倍,最大发射波长大约红移了10 nm。
金属离子猝灭量子点荧光的机理十分复杂,不同的金属离子猝灭不同的量子点原理不尽相同,而且猝灭并非单一作用促成,之前已经有文献[22-23]对此进行了研究。量子点在受到外界刺激,尤其是光照刺激时,电子会由价带跃迁至导带,于是在价带生成了带正电荷的空穴,在导带生成了电子,之后导带电子跃迁回价带重组时会以光的形式释放能量,这就是量子点发光的基本原理。由于量子点电化学发光时对尺寸和修饰类型不敏感,对表面化学和表面存在状态敏感,未钝化的量子点表面原子可形成电子陷阱和空穴,会导致表面缺陷态间接复合发光,会对电子-空穴对的直接重组发光产生竞争干扰,于是常采用配合物修饰量子点表面缺陷,使复活点子和空穴的能量下降而易于俘获,增强直接复合的几率,提高发光效率。
本实验中采用巯基化合物作为配体合成CdTe量子点,巯基与Cu 2+形成复合物的结合能力远强于与量子点的结合力,于是当向CdTe量子点中加入Cu 2+时,Cu 2+会与量子点表面的Cd 2+发生离子交换,生成CuTe复合物,导致量子点荧光猝灭,而且由于CuTe复合物的能量隙比CdTe量子点低,阳离子交换后会造成荧光光谱红移和半峰宽宽化。原本这种化学交换是受到原子扩散所需的高活化能限制的,但是由于纳米材料较大的比表面积有利于外来金属离子的扩散分布,所以才得以发生。且本实验合成的量子点粒径比普通的量子点略小,具有更大的比表面积,能更充分地与金属离子发生反应,所以灵敏度更高。
此外,与一般金属离子不同,Cu 2+由于其较为特殊的电子轨道排布,与CdTe量子点的反应中会由于Te 2-空位的作用而转变成反磁性的产物CdTe +-Cu +,CdTe +-Cu +相较于单纯的CdTe量子点能量水平较低,再加上Cu +与激发的导带电子和价带空穴均发生非辐射重组,由此导致荧光猝灭和波谱的红移。有学者基于这种红移效应制成铜离子检测的荧光探针 [24],本实验则利用Cu 2+对CdTe量子点猝灭效应进行Cu 2+检测。
2.3 检测条件优化
2.3.1 CdTe量子点浓度的选择
实验固定Cu 2+浓度为100 mol/L,考察不同浓度的CdTe量子点对体系荧光强度变化(ΔF)的影响,以优化出最佳的浓度。
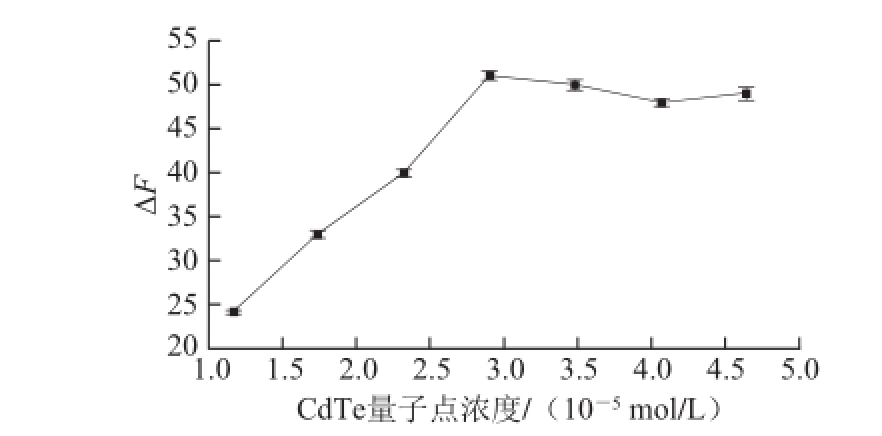
图3 CdTe量子点浓度对荧光变化量的影响
Fig.3 Effect of CdTe QDs concentration of on Δ F
由图3所示,CdTe量子点浓度在1.16×10 -5~2.9×10 -5mol/L范围内增加时,ΔF会随之增大。推测是因为在此浓度范围内,铜离子数量超过了量子点所能提供的结合点位,所以CdTe量子点浓度越高,被猝灭的量子点就越多,ΔF也就越大,即猝灭作用越明显。而当CdTe量子点浓度继续升高,量子点过量时,量子点所能提供的结合位点从理论上说,已经与铜离子全部反应,所以继续添加量子点,猝灭作用也会减弱,在光谱图上表现为,量子点浓度大于2.9×10 -5mol/L时,荧光强度变化趋于平稳,甚至保持不变。
实验还考察了不同CdTe量子点浓度对Cu 2+的响应灵敏度。结果表明,低浓度CdTe量子点(1.16×10 -5~2×10 -8mol/L),其荧光强度会随Cu 2+的浓度增加而增大,而非发生猝灭效应,且对Cu 2+响应范围为5~20 mol/L。当CdTe量子点浓度增加到2.9×10 -5mol/L时,Cu 2+的加入才会对量子点产生明显的猝灭作用,且能响应的范围为20~2 000 nmol/L。分析原因在于小粒径的量子点表面会存在较多的缺陷,容易引发激子非辐射重组。此时少量Cu 2+的加入钝化量子点表面,使其荧光得以增强。当量子点本身的表面缺陷都被填补达到饱和后,继续加入Cu 2+,过量的Cu 2+则会与量子点争夺巯基,使量子点表面配体脱落造成其表面状态改变,导致荧光猝灭。对于粒径较大的量子点,因表面鲜有缺陷,则不会产生这种效应,只会随金属离子的浓度升高而荧光降低。
本实验出现的现象正好与2.1节计算出的CdTe量子点的粒径为2.0 nm相符合。结合上述分析结果来看,CdTe量子点的浓度直接决定了该检测方法的灵敏度和线性范围。低浓度的量子点能够降低检测限,提高灵敏度,但是线性范围过窄;量子点浓度过高,Cu 2+对量子点的猝灭程度小,势必会降低反应的灵敏度。兼顾两方面的考虑,将CdTe量子点的最适浓度定为2.9×10 -5mol/L。
2.3.2 反应体系pH值的优化
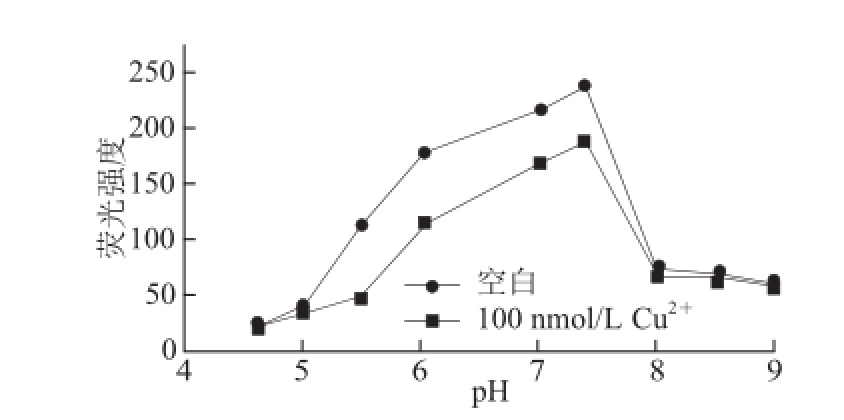
图4 pH值对CdTe量子点荧光猝灭的影响
Fig.4 Effect of pH on fluorescence quenching of CdTe QDs
由图4可知,pH值从4.63增加到7.40时,CdTe量子点荧光强度随之升高,体系荧光强度的改变值Δ F增大;当pH值大于7.40时,随着pH值的增大,CdTe量子点荧光强度和ΔF不断降低。分析原因,当pH值低到一定程度后量子点配体会被质子化,发生解离甚至聚沉,导致荧光下降,因此pH值一定范围内的增强能够使量子点稳定。但是当pH值过高(大于7.40),CdTe量子点会由于表面羧基所带负电荷的增多而引起水化物形成,从而致使荧光减弱 [25]。除此之外,在碱性环境中,Cu 2+易生成氢氧化物沉淀,导致与量子点反应的Cu 2+减少,由反应引发的ΔF也降低。综上所述,pH 7.40作为检测体系的最佳条件。
2.3.3 反应时间的优化
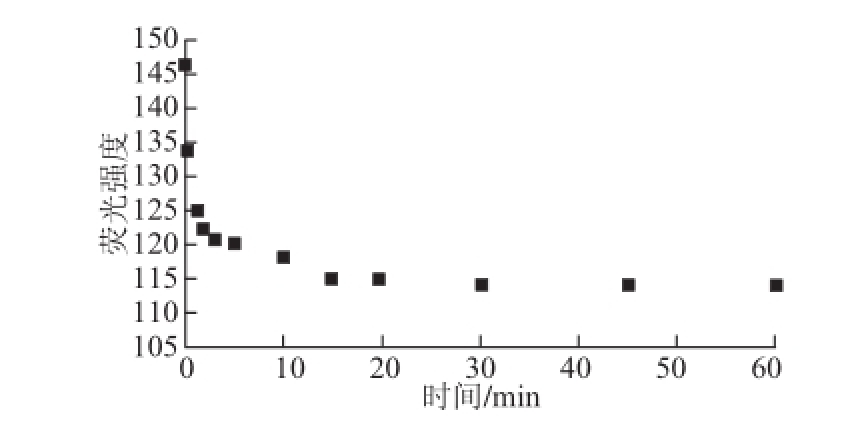
图5 反应时间对CdTe量子点荧光猝灭的影响
Fig.5 Effect of reaction time on fluorescence quenching of CdTe QDs
由图5可知,当加入Cu 2+离子后,刚开始的1 min反应十分剧烈,荧光强度下降幅度大,说明此时反应速率快。之后随着反应时间的延长,CdTe量子点的荧光强度下降幅度减小,速率变慢,30 min后达到最小值,之后的荧光强度基本不变,说明在30 min时反应基本达到平衡。而且在此后的2 h内荧光强度不再变化,说明反应后的体系比较稳定。综合考虑检测方法的准确性和快捷性,在接下来的测定实验中,选取30 min为最佳的反应时间。
2.3.4 共存物质的影响
表1 干扰物质的影响
Table 1 Interference of coexisting substances
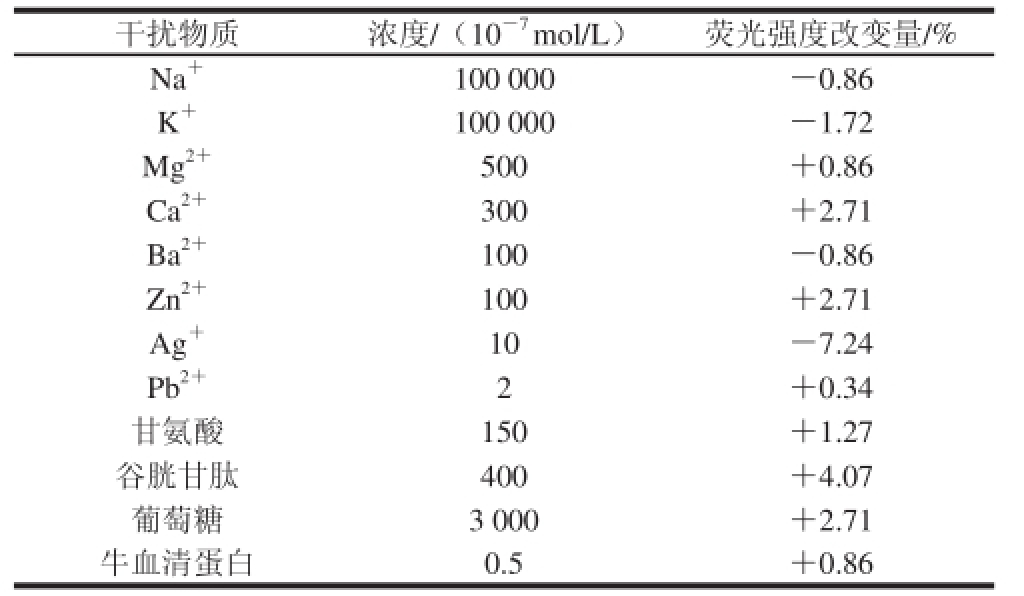
注:Cu 2+浓度为10 -7mol/L。
?
考察了几种常见金属离子及其他干扰物质对CdTe量子点检测Cu 2+离子时的荧光干扰情况,结果如表1所示。在Cu 2+浓度为100 nmol/L的情况下,与食品成分相关的金属离子如K +、Na +、Mg 2+和Ca 2+及葡萄糖、乳糖、谷氨酸、甘氨酸等在很大浓度范围内对CdTe量子点纳米粒子检测Cu 2+的荧光强度基本没有影响;Ag +对CdTe量子点荧光强度比较明显的猝灭效应,故应加入相应的掩蔽剂。在实际检测皮蛋过程,可通过对样品进行一定的前处理如去除蛋白、加大样品稀释梯度,以减少这些共存物质的干扰和影响。
2.4 标准曲线和检出限
在上述优化过的检测条件下,进一步考察了CdTe量子点在检测Cu 2+离子时的线性范围以及最低检出限,并绘制了标准曲线如图6所示。实验结果表明,当Cu 2+离子浓度在10~200 nmol/L内增加时,量子点荧光强度呈现规律性下降。以量子点荧光变化量(ΔF=F 0-F)为Y,Cu 2+浓度为X(mol/L),建立线性回归方程为Y=0.558 6×10 9X+0.746 9,线性相关系数R 2为0.997。由连续11 次测定不含Cu 2+和含Cu 2+的CdTe量子点体系的荧光强度差的3 倍除以标曲斜率,得到最终的检出限为0.96 nmol/L。
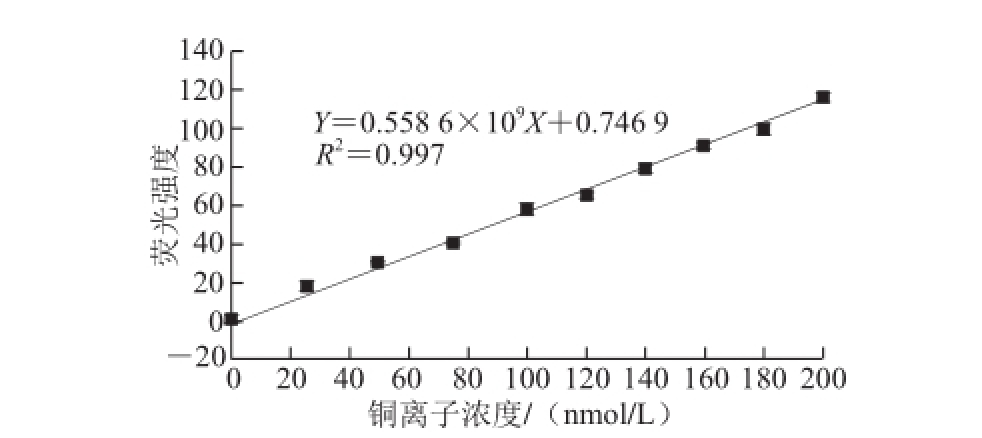
图6 荧光强度变化与铜离子浓度之间的线性关系
Fig.6 Linear relationships between changes in fluorescence intensity and Cu
2+concentration
2.5 合成样品
为了验证CdTe量子点荧光探针检测Cu 2+的准确性与适用性,实验对合成水样中的Cu 2+含量进行检测。表2给出了6 种混合样品的测试结果。对于影响较大的共存物质,在浓度较低时,其对检测结果的干扰也会进一步降低到误差可接受范围内。因此,利用CdTe量子点荧光猝灭法定量测定水溶液中的Cu 2+,具有较好的选择性、回收率与重复性。
表2 合成样本中检测铜离子结果(n=6)
Table 2 Results for the determination of Cu
2+in synthetic samples (n=6)
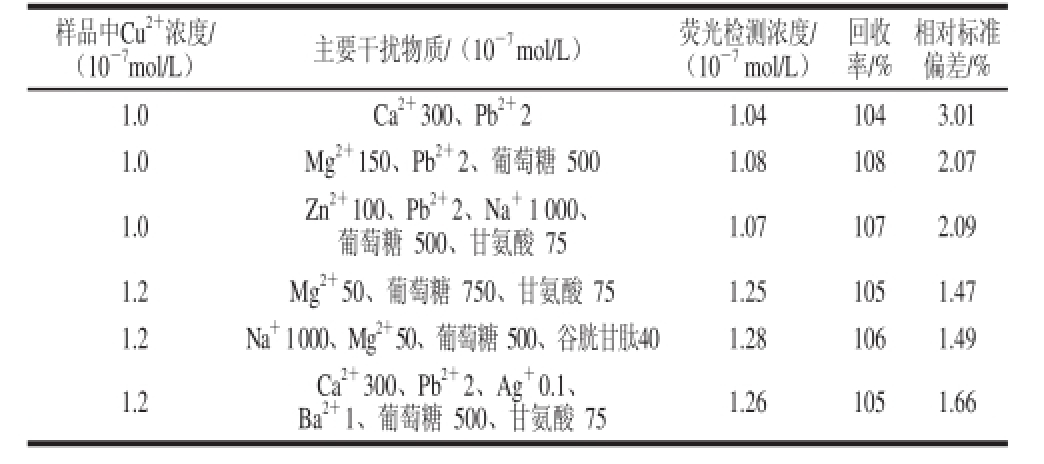
样品中Cu 2+浓度/(10 -7mol/L)主要干扰物质/(10 -7mol/L)荧光检测浓度/相对标准偏差/% 1.0Ca 2+300、Pb 2+21.041043.01 1.0Mg 2+150、Pb 2+2、葡萄糖 5001.081082.07 1.0Zn 2+100、Pb 2+2、Na +1 000、葡萄糖 500、甘氨酸 751.071072.09 1.2Mg 2+50、葡萄糖 750、甘氨酸 751.251051.47 1.2Na +1 000、Mg 2+50、葡萄糖 500、谷胱甘肽401.281061.49 1.2Ca 2+300、Pb 2+2、Ag +0.1、Ba 2+1、葡萄糖 500、甘氨酸 751.261051.66(10 -7mol/L)回收率/%
2.6 无铅皮蛋中铜含量测定
表3 皮蛋中检测铜离子的结果(n=3)
Table 3 Measurement results of copper in preserved egg (n=3)
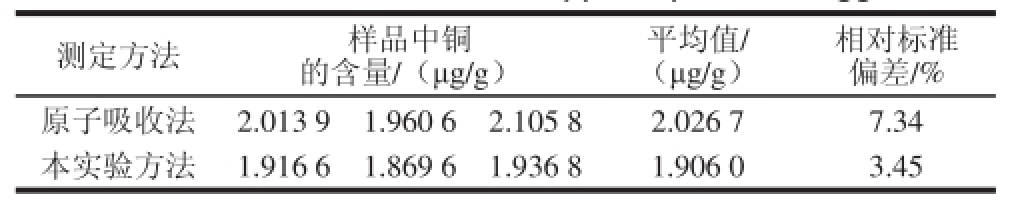
相对标准偏差/%原子吸收法2.013 91.960 62.105 82.026 77.34本实验方法1.916 61.869 61.936 81.906 03.45测定方法样品中铜的含量/(μg/g)平均值/(μg/g)
将该方法应用于无铅皮蛋中铜含量的测定,实验结果见表3。皮蛋为神丹无铅皮蛋,由于是清料法制成,无铅工艺,没有Pb 2+干扰,铜含量较其他金属元素高,适用于此测定实验。采用原子吸收法作为对照实验,结果显示2 种测定结果不存在显著性差异,说明该方法准确性好,可以应用于实际样品检测中。
本实验基于Cu 2+对CdTe量子点的荧光猝灭效应建立了快速灵敏检测皮蛋中铜含量的荧光分析方法,考察了CdTe量子点浓度、反应介质pH值、反应温度和反应时间等多种因素对检测体系的影响,并从机理上探讨Cu 2+选择性猝灭量子点的原因。
本检测方法线性范围宽,检测限低。相比于常规的方法,实验操作简便、检测速度快、灵敏度高。初步应用于无铅皮蛋样品中检测证明其具有较高的准确度,较好的选择性和灵敏度。
参考文献:
[1] 赵燕, 徐明生, 涂勇刚. 皮蛋加工相关机理研究进展[J]. 食品科学, 2010, 31(7): 472-475.
[2] 周艳明, 蔺翠翠. 畜产品中铜残留的风险性评价[J]. 食品科学, 2010, 31(11): 258-262.
[3] 段有刚, 施杏芬, 朱五文, 等. 猪饲料中添加高铜的危害及控制对策[J].畜牧兽医科技信息, 2006(8): 91-92. DOI:10.3969/ j.issn.1671-6027.2006.08.084.
[4] 阎华, 朱瑞卫, 周文兵. 铜、锌、铁清料法加工溏心皮蛋的比较研究[J]. 食品工业科技, 2004, 25(6): 64-66. DOI:10.3969/ j.issn.1002-0306.2004.06.019.
[5] 汤钦林. 锌法皮蛋加工技术的研究[J]. 食品研究与开发, 2007(7): 93-96. DOI:10.3969/j.issn.1005-6521.2007.07.029.
[6] POURREZA N, HOVEIZAVI R. Simultaneous preconcentration of Cu, Fe and Pb as methylthymol blue complexes on naphthalene adsorbent and flame atomic absorption determination[J]. Analytica Chimica Acta, 2005, 549(1): 124-128. DOI:10.1016/j.aca.2005.06.037.
[7] BECKER J S, ZORIY M V, PICKHARDT C, et al. Imaging of copper, zinc, and other elements in thin section of human brain samples (Hippocampus) by laser ablation inductively coupled plasma mass spectrometry[J]. Analytical Chemistry, 2005, 77(10): 3208-3216. DOI:10.1021/ac040184q.
[8] WANG B B, WANG Q, CAI Z X, et al. Simultaneous, rapid and sensitive detection of three food-borne pathogenic bacteria using multicolor quantum dot probes based on multiplex fluoroimmunoassay in food samples[J]. LWT-Food Science and Technology, 2015, 61: 368-376. DOI:10.1016/j.lwt.2014.12.016.
[9] PINTO J J, MORENO C, GARCIA-VARGAS M. A very sensitive flow system for the direct determination of copper in natural waters based on spectrophotometric detection[J]. Talanta, 2004, 64(2): 562-565. DOI:10.1016/j.talanta.2004.03.009.
[10] BENI V, OGURTSOV V I, BAKUNIN N V, et al. Development of a portable electroanalytical system for the stripping voltammetry of metals: determination of copper in acetic acid soil extracts[J]. Analytica Chimica Acta, 2005, 552(1): 190-200. DOI:10.1016/ j.aca.2005.07.058.
[11] 王蓓蓓, 阮晓娟, 马美湖, 等. 新型量子点在食品分析检测领域中的应用[J]. 食品科学, 2013, 34(11): 311-315. DOI:10.7506/spkx1002-6630-201311066.
[12] 文学芳, 杨安树, 陈红兵. 量子点标记技术在食品安全检测中的应用[J]. 食品科学, 2009, 30(21): 399-402.
[13] LOU Y B, ZHAO Y X, CHEN J X, et al. Metal ions optical sensing by semiconductor quantum dots[J]. Journal of Material Chemistry C, 2014, 2(4): 595-613. DOI:10.1039/c3tc31937g.
[14] FRANCESC A E T, ANTONIO A F. Applications of quantum dots as probes in immunosensing of small-sized analytes[J]. Biosensors and Bioelectronics, 2013, 41(15): 12-29. DOI:10.1016/j.bios.2012.09.025.
[15] ISABEL C M, VANESA R, ISELA L, et al. An overview of recent advances in the application of quantum dots as luminescent probes to inorganic-trace analysis[J]. Trend in Analytical Chemistry, 2014, 57: 64-72. DOI:10.1016/j.trac.2014.02.004.
[16] CHEN Y F, ROSENZWEIG Z. Luminescent CdS quantum dots as selective ion probes[J]. Analytical Chemistry, 2002, 74(19): 5132-5138. DOI:10.1021/ac0258251.
[17] 王柯敏, 王益林, 李朝辉, 等. CdTe量子点荧光猝灭法测定铜离子的研究[J]. 湖南大学学报(自然科学版), 2005, 32(3): 1-5.
[18] KELLY S, CULLUM B S, MICHAEL A S, et al. Photophysical properties of ZnS nanoclusters with spatially localized Mn 2+[J]. The Journal of Physical Chemical, 1996, 100(11): 4551-4555. DOI:10.1021/jp952377a.
[19] DALE E, KAUSHIK P. Q-CdS photoluminescence activation on Zn 2+and Cd 2+salt introduction[J]. Langmuir, 2001, 17(8): 2541-2544. DOI:10.1021/la001416t.
[20] XIA Y S, ZHU C Q. Use of surface-modified CdTe quantum dots as fluorescent probes in sensing mercury (Ⅱ)[J]. Talanta, 2008, 75: 215-221. DOI:10.1016/j.talanta.2007.11.008.
[21] WANG B B, SHANG H, NIE C P, et al. A novel two-step controlled basic water phase method for synthesizing size-tunable CdTe/ Cd(OH) 2core/shell quantum dots with high quantum yield and excellent stability[J]. Journal of Luminescence, 2013, 143: 262-270. DOI:10.1016/j.jlumin.2013.05.007.
[22] XIA Y S, CAO C, ZHU C Q. Two distinct photoluminescence responses of CdTe quantum dots to Ag (Ⅰ)[J]. Journal of Luminescence, 2008, 128: 166-172. DOI:10.1016/ j.jlumin.2007.07.007.
[23] WU P, ZHAO T, WANG S L, et al. Semiconductor quantum dotsbased metal ion probes[J]. Nanoscale, 2014(6): 43-64. DOI:10.1039/ c3nr04628a.
[24] HAO Y Q, LIU L, LONG Y F, et al. Sensitive photoluminescent detection of Cu 2+in real samples using CdS quantum dots in combination with a Cu 2+-reducing reaction[J]. Biosensors and Bioelectronics, 2013, 41: 723-729. DOI:10.1016/j.bios.2012.09.064.
[25] KONESWARAN M, NARAYANASWAMY R. Mercaptoacetic acid capped CdS quantum dots as fluorescence single shot probe for mercury(Ⅱ)[J]. Sensors Actuators B, 2009, 139(1): 91-96. DOI:10.1016/j.snb.2008.09.011.
Ultrasensitive and Rapid Detection of Copper in Preserved Eggs Using CdTe Quantum Dot as a Nano-Fluorescence Probe
WANG Beibei
1,2, SHANG Huan
1, WANG Qi
1, MA Meihu
1, CAI Zhaoxia
1,*
(1. National Research and Development Center for Egg Processing, College of Food Science and Technology, Huazhong Agricultural University, Wuhan 430070, China; 2. College of Food and Drug, Anhui Science and Technology University, Fengyang 233100, China)
Abstract:In this study, highly-fluorescent and water-soluble CdTe quantum dots (QDs) were used as fluorescence probe to quantitatively detect Cu 2+in preserved egg samples. Using thioglycollic acid (TGA) and thioglycerol (TGOL) as the stabilizers, the CdTe QDs were synthesized in water phase. The luminescent characteristics of CdTe QDs were studied using UV-visible spectrophotometry and fluorescence spectroscopy. This experiment investigated the mechanism of the fluorescence quenching effect of Cu 2+on CdTe QDs and based on the quenching effect, a method for detecting trace Cu 2+using QDs as a probe was established. The results showed the relationship between Cu 2+concentration in the range from 10 to 200 nmol/L and the quenching intensity of CdTe QDs (F) was fairly linear with high correlation coefficient (R 2= 0.997). The limit of detection was 0.96 nmol/L, and the developed method presented relatively high selectivity and sensitivity. This method was successfully applied to the analysis of preserved egg samples. The precision, expressed as relative standard deviation (RSD), was 1.47%–3.01%, and the recovery rate was between 104% and 108%.
Key words:quantum dots; fluorescence quenching; Cu 2+; preserved egg
DOI:10.7506/spkx1002-6630-201602030
中图分类号:TS201.6
文献标志码:A
文章编号:1002-6630(2016)02-0172-06
引文格式:
王蓓蓓, 商欢, 王琪, 等. CdTe量子点作为荧光探针检测皮蛋中微量铜[J]. 食品科学, 2016, 37(2): 172-177. DOI:10.7506/ spkx1002-6630-201602030. http://www.spkx.net.cn
WANG Beibei, SHANG Huan, WANG Qi, et al. Ultrasensitive and rapid detection of copper in preserved eggs using CdTe quantum dot as a nano-fluorescence probe[J]. Food Science, 2016, 37(2): 172-177. (in Chinese with English abstract) DOI:10.7506/spkx1002-6630-201602030. http://www.spkx.net.cn
收稿日期:2015-04-25
基金项目:公益性行业(农业)科研专项(201303084);安徽科技学院校人才引进项目(ZRC2014445)
作者简介:王蓓蓓(1988—),女,助教,硕士,研究方向为农产品贮藏与加工、食品安全与分析。E-mail:w-beibei@foxmail.com
*通信作者:蔡朝霞(1979—),女,副教授,博士,研究方向为农产品贮藏与加工、食品安全与分析。
E-mail:caizhaoxia@mail.hzau.edu.cn