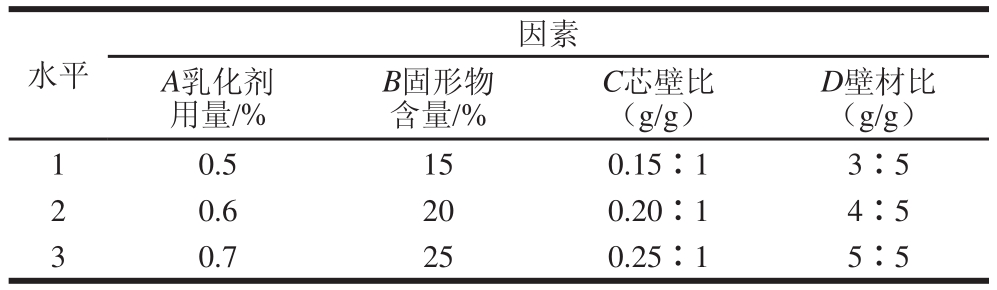
表1 L9(34)正交试验因素与水平
Table 1 Factors and levels used in orthogonal array experiments L9(34) for optimization of microcapsule formulationn
罗程印,程远渡,易有金*,夏 菠,周红丽*,曹 熙
(湖南农业大学食品科学技术学院,食品科学与生物技术湖南省重点实验室,湖南 长沙 410128)
摘 要:以植物甾醇酯和葛根素为芯材,阿拉伯胶和β-环状糊精为壁材,采用喷雾干燥法制备植物甾醇酯葛根素复合微胶囊。考察了乳化剂配比、乳化剂用量、固形物含量、芯壁比、壁材比对乳化液稳定性的影响,以及进风温度、出风温度、均质压力对微胶囊化效率的影响,通过单因素试验和正交试验,确定复合微胶囊的最佳工艺参数。结果显示,复合微胶囊的最佳工艺条件为:乳化剂(蔗糖酯-单甘酯)配比6∶4(g/g)、乳化剂用量0.7%(质量分数)、固形物含量20%(质量分数)、芯壁比0.25∶1(g/g)、壁材(阿拉伯胶和β-环状糊精)比5∶5(g/g)、进风温度180 ℃、出风温度75 ℃、均质压力25 MPa。在此工艺条件下复合微胶囊中植物甾醇酯的包埋率为89.04%,葛根素包埋率为80.15%,产品为乳白色、细小均匀的粉末,气味纯正,密度0.568 g/mL,溶解率95.11%,水分含量3.57%,贮藏稳定性提高。
关键词:植物甾醇酯;葛根素;微胶囊;喷雾干燥
周红丽(1972—),女,副教授,博士,研究方向为微生物活性物质、功能性食品。E-mail:xuanxuan310@126.com
罗程印, 程远渡, 易有金, 等. 植物甾醇酯和葛根素复合微胶囊的制备工艺优化[J]. 食品科学, 2016, 37(6): 26-33. DOI:10.7506/spkx1002-6630-201606005. http://www.spkx.net.cn
LUO Chengyin, CHENG Yuandu, YI Youjin, et al. Optimization of preparation process for blend microcapsules of phytosterol esters and puerarin[J]. Food Science, 2016, 37(6): 26-33. (in Chinese with English abstract) DOI:10.7506/ spkx1002-6630-201606005. http://www.spkx.net.cn
葛根素是从葛根中提取的一种异黄酮类化合物,安全性强,具有扩张冠状动脉、降血脂、降血压、降血糖、治疗非酒精性脂肪肝、减肥等功效[1-2]。植物甾醇酯(phytosterol ester,PSE)是植物油脂中普遍存在的一种微量成分,可通过植物甾醇与脂肪酸进行酯化反应制得,其生理活性与植物甾醇相同甚至比之更优[3],研究表明其具有降低胆固醇、抗炎、抗癌、抗衰老、调节免疫的作用[4-8]。葛根素和PSE联合作用时具有降脂协同作用[9],且其长期使用副作用不明显,安全性高,符合人们保健食品选择的观点。
葛根素难溶于水和油脂,PSE虽可以部分溶于油脂,但难以与其他食品原料混溶,而且PSE长时间暴露于空气中,会氧化酸败,影响风味[10];鉴于两者不易与食品的其他成分均匀混合,难以起到相应功效,因此有必要将两者进行复合微胶囊化处理。
微胶囊不仅可改善芯材的分散性、水中的溶解性以及乳化分散性等能力,而且可以强化对芯材中易氧化成分的保护作用,增强芯材的稳定性,延长产品的货架期,提高其营养价值,也便于运输[11]。本研究以PSE和葛根素为芯材,以阿拉伯胶和β-环状糊精作为壁材,主要原因为PSE和葛根素都是疏水性物质,其中PSE为黏稠状,遇水表现出油脂壮性质难以分散,因此加入乳化剂制配成“油/水”乳化液,进行包埋。阿拉伯胶具有很好的乳化性和成模性,高质量浓度时仍具有低黏度,此外其水溶液无色透明、无异味,阿拉伯胶起到乳化作用,同时作为壁材高成膜性可以提高微胶囊化效率,以及低黏度性成为制备PSE和葛根素复合微胶囊壁材的首选。阿拉伯胶在植物水溶胶中应用最为广泛,具有突出的乳化性能和较好的成膜性能,高质量浓度时仍具有低黏度性,此外其水溶液无色透明,无异味,满足多数壁材要求,但价格偏贵。β-环状糊精价格低廉,性质稳定,十分适合包埋大分子和油性物质,减缓芯材在光、热、氧条件下的反应,提高物质稳定性,同时可以掩蔽异味,可与阿拉伯胶复配作为壁材填充物。采用喷雾干燥法制作复合微胶囊,探讨复合微胶囊的最佳制作工艺,从而为开发PSE和葛根素复合微胶囊提供技术参考。
1.1 材料与试剂
PSE(纯度95%) 湖北兴银河化工有限公司;葛根素(纯度99%) 西安天本生物工程有限公司;阿拉伯树胶粉(食品级) 泰安凯通贸易有限公司;β-环状糊精(食品级) 曲阜市天利药用辅料有限公司;蔗糖脂肪酸酯(食品级,亲水亲油平衡值(hydrophilic lipophilic balance,HLB)=15) 河北百味生物科技有限公司;分子蒸馏单甘酯(食品级,HLB=3.8) 上海试皿赫维化工有限公司;石油醚、氯仿、甲醇、盐酸、氯化亚铁、硫氰酸钾、还原铁粉(均为分析纯) 国药集团化学试剂有限公司;实验用水为蒸馏水。
1.2 仪器与设备
CP114型电子天平 奥豪斯仪器(上海)有限公司;DK-S28型恒温水浴锅 上海精宏实验设备有限公司;JB50-D型电动搅拌机 上海标准模型厂;FA25型高速剪切乳化机 上海弗鲁克流体机械制造有限公司;SPH (60-70)型高压均质机 上海申鹿均质机有限公司;WPG-220型实验室喷雾干燥机 山东奥诺能源科技有限公司;SCIENTZ-ⅡD型超声波粉碎机 宁波新芝股份有限公司;电热鼓风干燥箱 天津泰斯特仪器有限公司;紫外分光光度计 北京莱柏泰科仪器有限公司。
1.3 方法
1.3.1 复合微胶囊制作工艺流程及要点
一定量的阿拉伯树胶粉溶解在50 ℃的蒸馏水中,恒温30 min同时不停搅拌,随后添加β-环状糊精和蔗糖酯,恒温20 min不停搅拌,此为“水相”[12];PSE和葛根素(两者以质量比2∶3组合)中添加单甘酯,搅拌混合,此为“油相”;将水相加入油相中搅拌混合,高速剪切5 min,得到乳状液,将乳状液3 次高压均质后,进行喷雾干燥制得微胶囊粉末。
1.3.2 微胶囊乳化工艺单因素试验
1.3.2.1 复合乳化剂配比的确定
根据PSE和葛根素的性质,采用亲水乳化剂蔗糖酯(HLB=15)和亲油乳化剂单甘酯(HLB=3.8),常温条件下,选取芯壁比0.2∶1(g/g)、固形物含量15%(质量分数)、壁材比5∶5(g/g)、乳化剂用量0.2%(质量分数),以乳化液稳定性为指标,确定两者最佳比例。
1.3.2.2 乳化剂用量的确定
在芯壁比0.2∶1、固形物含量15%、壁材比5∶5的条件下,考察乳化剂用量为0、0.2%、0.4%、0.6%、0.8%、1.0%、1.2%、1.4%时对微胶囊乳化液稳定性的影响。
1.3.2.3 壁材比的确定
在芯壁比0.2∶1、固形物含量15%、乳化剂用量0.2%的条件下,分别考察壁材比(阿拉伯胶和β-环状糊精)为1∶5、2∶5、3∶5、4∶5、5∶5、6∶5时对微胶囊乳化液稳定性的影响。
1.3.2.4 芯壁比的确定
在固形物含量15%、壁材比5∶5、乳化剂用量0.2%的条件下,考察芯壁比为0.05∶1、0.10∶1、0.15∶1、0.2∶1、0.25∶1、0.3∶1时对微胶囊乳化液稳定性的影响。
1.3.2.5 固形物含量的确定
在芯壁比0.2∶1、壁材比5∶5、乳化剂用量0.2%的条件下,考察固形物含量为5%、10%、15%、20%、25%、30%时对微胶囊乳化液稳定性的影响。
1.3.3 微胶囊乳化工艺正交试验
根据上述单因素试验,选定合适的水平,选用相应的正交表,见表1,以乳化液稳定性为指标进行正交试验,确定最佳的乳化液配方。
表1 L9(34)正交试验因素与水平
Table 1 Factors and levels used in orthogonal array experiments L9(34) for optimization of microcapsule formulationn

1.3.4 微胶囊喷雾干燥单因素试验
1.3.4.1 进风温度的确定
利用最佳配方制作乳化液,进行喷雾干燥。选取出风温度60 ℃、均质压力25 MPa,研究分析进风温度为150、160、170、180、190、200 ℃时对微胶囊化效率的影响。
1.3.4.2 出风温度的确定
利用最佳配方制作乳化液,进行喷雾干燥。选取进风温度190 ℃、均质压力25 MPa,研究分析出风温度为40、50、60、70、80、90 ℃时对微胶囊化效率的影响。
1.3.4.3 均质压力的确定
利用最佳配方制作乳化液,进行喷雾干燥。选取进风温度190 ℃、出风温度60 ℃,研究分析均质压力为10、15、20、25、30、35 MPa时对微胶囊化效率的影响。
1.3.5 微胶囊喷雾干燥正交试验
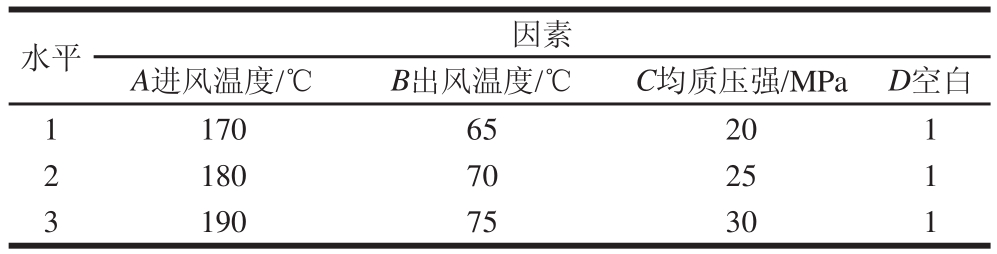
根据上述单因素试验,选定合适的水平,选用相应的正交表,以微胶囊化效率(包埋率)为指标,进行正交试验,确定最佳的喷雾干燥工艺参数,见表2。
表2 L9(34)正交试验因素与水平
Table 2 Factors and levels used orthogonal array experiments L9(34) for optimization of spray drying conditions
1.3.6 复合乳化剂HLB的计算
多种乳化剂混合使用时,复合乳化剂的HLB为某种乳化剂的质量分数与原HLB积的加和性[13]。按式(1)计算HLB。
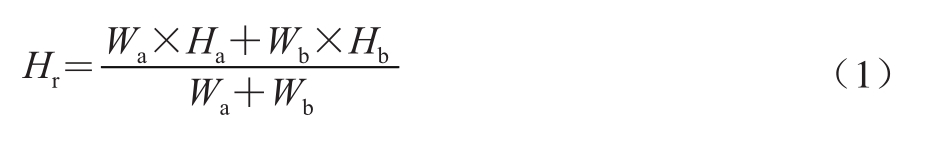
式中:Hr为复合乳化剂HLB;Wa、Wb分别为乳化剂a(蔗糖酯)、b(单甘酯)的质量分数/%;Ha、Hb分别为乳化剂a、b的HLB。
1.3.7 微胶囊乳化液稳定性的测定
将混合液于高速组织剪切机中高速剪切5 min后得到乳化液。用50 mL具塞量筒量取50 mL剪切后的乳化液,随后在30 ℃恒温水浴中静置5 h,记录游离水层的体积。按式(2)计算乳化液稳定性[14]。
1.3.8 微胶囊化效率的测定
1.3.8.1 包埋率计算
微胶囊芯材为PSE和葛根素,两种物质性质有差别,测定微胶囊包埋率时需测定两种物质的包埋率,按式(3)计算包埋率[15]。
1.3.8.2 微胶囊表面PSE含量的测定
准确称取5 g样品于三角瓶中,加入20 mL石油醚,振荡2 min,过滤,重复3 次操作,合并滤液于已称质量小烧杯中,小烧杯放于通风橱中,加速挥发石油醚,再放入50 ℃烘箱中烘至质量恒定,计算表面PSE的质量[16]。
1.3.8.3 微胶囊总PSE含量的测定
准确称取5 g样品置于三角瓶中,加20 mL热水使之完全溶解,再加入20 mL石油醚,振荡萃取2 min,用分液漏斗将萃取液移入已称质量小烧杯,随后重复再萃取两次合并萃取液,小烧杯放于通风厨中,加速挥发石油醚,再放入50 ℃烘箱中烘至质量恒定,计算总PSE的质量[17]。
1.3.8.4 微胶囊表面葛根素含量的测定
准确称取5 g样品于三角瓶中,加入20 mL甲醇,振荡2 min,过滤,重复3 次,合并滤液于已称质量小烧杯中,小烧杯放于通风厨中,加速挥发甲醇,再放入50 ℃烘箱中烘至质量恒定,计算表面葛根素的质量。
1.3.8.5 微胶囊总葛根素含量的测定
准确称取5 g样品于三角瓶中,以100 mL甲醇作为溶剂,连接到超声波粉碎机上,恒定功率500 W,工作5 s,间隔5 s,连续工作4 min,然后过滤到已称质量的小烧杯中,于通风厨中,加速挥发甲醇,再放入50 ℃烘箱中烘至质量恒定,计算总葛根素的质量。
1.3.9 复合微胶囊的质量评价
1.3.9.1 复合微胶囊的感官评价
将复合微胶囊放在自然光线处及白色背景下,对微胶囊的色泽、气味、组织状态进行评价。
1.3.9.2 复合微胶囊含水量的测定
微胶囊产品水分过多会使产品结块、霉变,因此微胶囊产品的水分含量一般保持在2%~5%之间。微胶囊水分含量的测定参照GB/T 5009.3—2010《食品中水分的测定》。
1.3.9.3 复合微胶囊密度的测定
将复合微胶囊成品通过漏斗倒入已知质量、体积的容器中,当容器顶部成锥形后,用平板将锥形粉料轻轻推平,铺满顶部,随后称量容器和微胶囊的总质量,按式(4)计算单位体积复合微胶囊的质量[18]。
式中:ρ为微胶囊密度/(g/mL);m1为容器质量/g;m2为容器和微胶囊总质量/g;V为容器体积/mL。
1.3.9.4 复合微胶囊流动性的测定
休止角的大小可以用来评判微胶囊产品的流动性。将微胶囊粉末倒入固定在铁架台的漏斗内,使样品自由落到玻璃板上,微胶囊粉末堆积成圆锥形,直至不能继续堆高为止,测定堆高和半径,按式(5)计算微胶囊的休止角(θ)[19]。
式中:h为堆高/cm;r为堆半径/cm。休止角θ≤30°表示微胶囊粉末流动性好,30°<θ≤45°表示微胶囊粉末流动性较好,45°<θ≤60°表示粉末颗粒流动性一般,60°<θ表示颗粒流动性差[20]。
1.3.9.5 复合微胶囊溶解率的测定
准确称取5 g样品,置于5 0 m L烧杯中,用38 mL 30 ℃蒸馏水将样品溶解,随后移入50 mL具塞离心管中,以4 000 r/min转速离心10 min,倒去上清液。再加入38 mL 30 ℃蒸馏水,振荡使沉淀悬浮,再次以4 000 r/min转速离心10 min,倒去上清液。用一定量的水将沉淀洗入已称质量的蒸发皿中,移入105 ℃干燥箱中烘至恒定质量[20]。按式(6)计算溶解率。
式中:M为样品质量/g;M1为蒸发皿质量/g;M2为蒸发皿和不溶物质量/g;A为样品含水量/%。
1.3.9.6 复合微胶囊氧化稳定性的测定
将微胶囊粉末和原料于60 ℃烘箱中进行加速氧化,每隔24 h取样测定微胶囊和原料的过氧化值。称6 g左右的微胶囊粉末于50 mL三角瓶中加入20 mL三氯甲烷,用超声波粉碎机粉碎4 min,过滤并洗涤,将过滤液定溶于25 mL容量瓶中,吸取7 mL溶液于10 mL容量瓶,并加3 mL甲醇定容,混匀,采用GB/T 5009.37—2003《食用植物油卫生标准的分析方法》中比色法,测定微胶囊的过氧化值[21]。
2.1 复合微胶囊乳化工艺优化结果
2.1.1 乳化剂HLB对乳化液稳定性的影响
根据芯材的性质采用蔗糖酯和单甘酯作为复合乳化剂,进行乳化作用。以不同质量分数的蔗糖酯和单甘酯进行复配,通过单因素试验确定适合复合微胶囊的HLB值,进而确定两种乳化剂的不同配比,试验结果见表3。
表3 复合乳化剂HLB值的确定
Table 3 Selection of optimal emulsifier composition based on HLB

注:表中数值以 ±s表示,n=3;同列上标字母不同表示差异显著,P<0.05。
±s表示,n=3;同列上标字母不同表示差异显著,P<0.05。
由表3可知,在单因素条件下,随着蔗糖酯和单甘酯配比的不同,HLB值发生变化,乳化液的稳定性也随之发生变化。当HLB值为10.52时,此时乳化液稳定性最好,达到90.92%。因此选择HLB值为10.52时的复合乳化剂的配比,即蔗糖酯-单甘酯质量比6∶4。
2.1.2 乳化剂用量对乳化液稳定性的影响
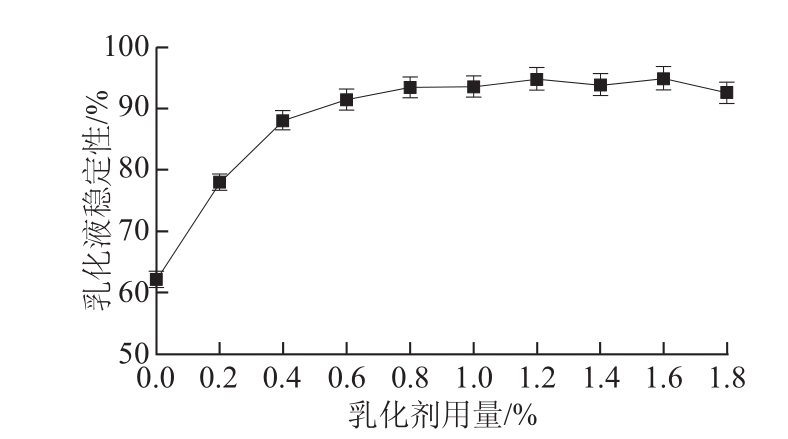
图1 乳化剂用量对乳化液稳定性的影响
Fig.1 Effect of emulsifier dosage on emulsion stability
由图1可知,在一定范围内乳化剂添加量的增加使乳化液的稳定性逐步提高,当用量大于0.6%以后,再继续添加乳化剂,对乳化液稳定性的提高不是很明显。实验表明,乳化剂用量过高,会使乳化液的黏度增大,此外乳化液还会产生微量的絮凝现象,在进行后续喷雾干燥时,固形物分布不均匀且易堵塞喷头,影响喷雾干燥的进行。综合考虑,在不影响乳化液稳定性前提下,减少对乳化剂的用量,因此认为0.5%~0.7%的乳化剂(蔗糖酯-单甘酯质量比6∶4)用量为佳。
2.1.3 固形物含量对乳化液稳定性的影响

图2 固形物含量对乳化液稳定性的影响
Fig.2 Effect of solid content on emulsion stability
在制备微胶囊时,首先应使乳化液稳定性达到最好,以便于喷雾干燥时不会出现凝聚、沉淀或分层现象。由图2可知,固形物含量不同,乳化液的稳定性差别很大,固形物的含量过多或过少,都会造成乳化稳定性的不理想。因此,从芯材含量和乳化液稳定性方面考虑,复合微胶囊的固形物含量可选择15%、20%、25%。
2.1.4 芯壁比对乳化液稳定性的影响

图3 芯壁比对乳化液稳定性的影响
Fig.3 Effect of core/wall material ratio on emulsion stability
由图3可知,刚开始随着芯材-壁材的比例提高,乳化液的稳定性有所升高。但当芯材含量过高,则乳化液的稳定性会有所下降。随着芯材的比例增加,壁材(阿拉伯胶与β-环状糊精)的含量会相对减少,出现壁材不能够完全包埋芯材的现象,会使芯材即PSE和葛根素分别上浮和下沉,影响到乳化液的稳定性。同时芯材的比例过小,则包埋同样数量的芯材所需要的壁材越多,会增加生产成本。在考虑到乳化液的稳定性和实际生产需要的前提下,芯壁比可以选择0.15∶1、0.20∶1、0.25∶1。
2.1.5 壁材比对乳化液稳定性影响
为了获得稳定的微胶囊乳化液,阿拉伯胶和β-环状糊精的质量比例需要适宜,过高或过低均不能形成稳定性高的乳化液。由图4可知,当阿拉伯胶和β-环状糊精质量比为1∶5时,乳化液的稳定性较低为68.42%,由于乳化液中阿拉伯胶过少,不足以包埋芯材,因而乳化液稳定性不高。随着阿拉伯胶所占比例的增加,乳化液的稳定性增强,阿拉伯胶和β-环状糊精质量比为4∶5时,乳化液的稳定性最佳。
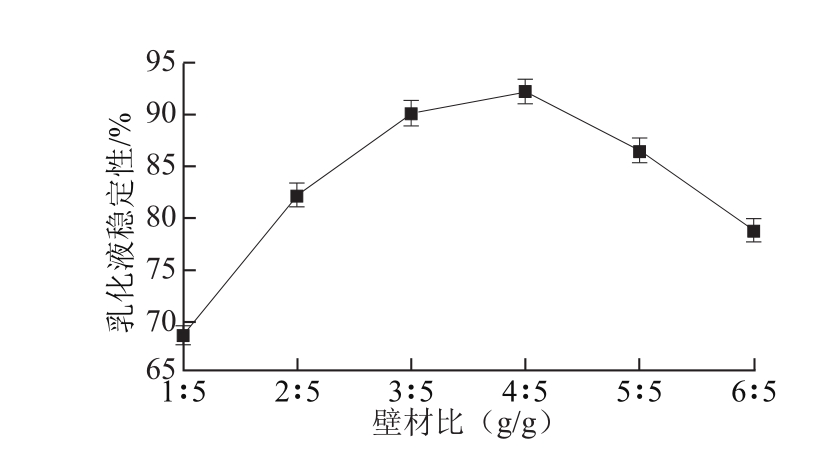
图4 壁材比对乳化液稳定性影响
Fig.4 Effect of wall material composition on emulsion stability
2.1.6 复合微胶囊乳化液最佳配方的确定
在单因素试验的基础上,选取复合乳化剂用量、固形物含量、芯壁比、壁材比4 个因素,每因素取3 个水平,选用L9(34)正交试验表,以乳化液的稳定性为指标,确定乳化液最佳的配方,同时试验中乳化剂的HLB值为10.52(蔗糖酯-单甘酯质量比6∶4)。
表4 复合微胶囊乳化液正交试验设计及结果
Table 4 Orthogonal array design with experimental results for microcapsule formulation
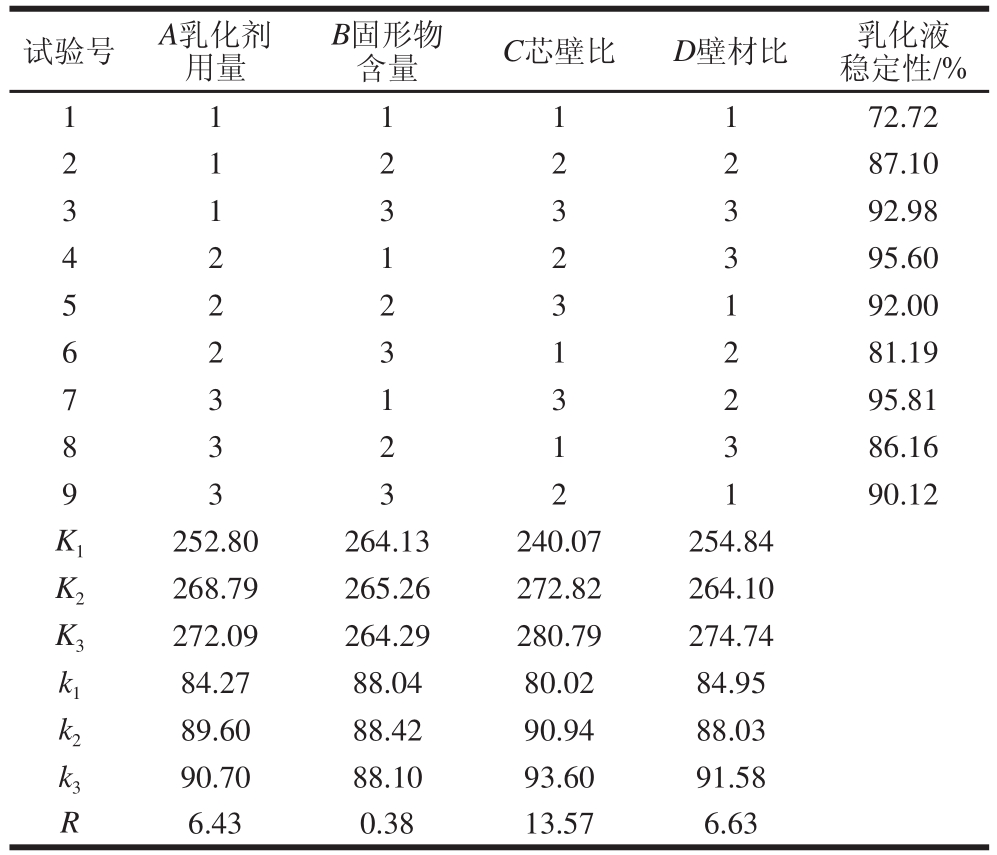
表5 复合微胶囊乳化液正交试验数据方差分析
Table 5 Analysis of variance of the orthogonal array design for microcapsule formulation

由表4得知,B项R值最小,故将其作为空白项进行数据方差分析得表5,4 种因素影响大小顺序为:C>A>D>B,即影响微胶囊乳化液稳定性的主要因素依次为:芯壁比、乳化剂用量、壁材比、固形物含量。从正交试验的9 组结果来看,7号试验组的稳定性最好,其配方组合为:乳化剂用量0.7%、固形物含量15%、芯壁比0.25∶1、壁材比4∶5;从正交试验结果分析来看,最佳配方组合应为A3B2C3D3,即乳化剂用量0.7%、固形物含量20%、芯壁比0.25∶1、壁材比5∶5。由于正交9组试验中没有最佳组合试验,因此需要进行最佳组合的验证实验,经过验证实验测得乳化液稳定性为98.62%,表明正交试验结果的正确,此配方为乳化液最佳配方。
2.2 复合微胶囊喷雾干燥工艺优化结果
利用上述最佳配方制作稳定乳化液进行喷雾干燥,在进料温度为50 ℃条件下,对影响喷雾干燥的进风温度、出风温度、均质压力因素进行试验。
2.2.1 进风温度对微胶囊化效率(包埋率)的影响

图5 进风温度对微胶囊包埋率的影响
Fig.5 Effect of inlet air temperature on microencapsulation efficiency
进风温度过低时,微胶囊成膜时间长,干燥速率慢,使其水分含量明显增加,流动性不好,且喷雾干燥时易出现黏壁现象,不易收集,微胶囊化产率效率都会降低。如图5所示,随着进风温度的升高,两种芯材的微胶囊化效率会逐渐提高,但温度过高后两者的微胶囊化效率都会降低[22],这是因为进风温度的逐渐提高,会不断缩短产品颗粒的恒速干燥阶段,促进微胶囊玻璃体的快速形成,进而有效提高微胶囊化效率,但温度超过两者最佳温度(PSE 180 ℃、葛根素190 ℃)后,会使水分蒸发速率加快,囊壁表面出现凹凸,对已成型的微胶囊造成破裂,同时使微胶囊壁材变性出现小孔,加速芯材变质,降低溶解率,从而使微胶囊质量降低。因此为提高两者微胶囊化效率,可选择进风温度为170、180、190 ℃。
2.2.2 出风温度对微胶囊化效率的影响
升高出风温度,可缩短微胶囊粉末的干燥时间,使产品快速形成完整致密的囊状结构,减少芯材渗出,提高微胶囊化效率,同时避免干燥粉末吸水回潮,降低水分含量,改善干燥效果。出风温度过高也可使微胶囊粉末受热开裂,芯材溢出,降低微胶囊化效率。如图6所示,随着出风温度升高,两种芯材微胶囊化效率都逐步提高,当超过最佳温度(PSE 50 ℃、葛根素80 ℃)时,两者微胶囊化效率都逐渐降低。综合考虑,为使两者包埋率都比较理想,出风温度可选择70 ℃左右。
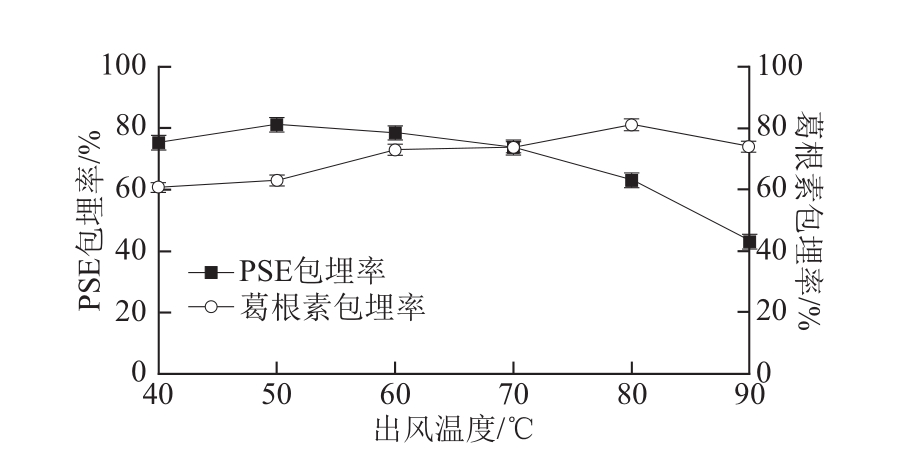
图6 出风温度对微胶囊包埋率的影响
Fig.6 Effect of outlet air temperature on microencapsulation efficiency
2.2.3 均质压力对微胶囊化效率的影响

图7 均质压力对微胶囊包埋率的影响
Fig.7 Effect of homogenization pressure on microencapsulation efficiency
均质压力越高,形成的液滴体积越小,大小越均匀,体系越不容易发生聚集絮凝、上浮、破乳等现象,使乳化液越稳定,从而可提高微胶囊化效率;然而均质压力过高,液滴过小,表面能过大,促使乳化液稳定性降低,反而不利于微胶囊化效率的提高[23-24],同时对设备的要求也过高。如图7所示,随着均质压力的增加,两种芯材的包埋率逐渐提高,但超过其最佳均质压力时,液滴过小,表面能增大,乳化液不稳定,促使两者的包埋率开始下降。为了使两种芯材的包埋率都比较理想,则均质压力可选择在25 MPa左右。
2.2.4 复合微胶囊喷雾干燥正交试验结果
影响喷雾干燥的因素有进风温度、出风温度、均质压力、流速、喷雾压力等因素,正交试验选择进风温度、出风温度、均质压力3 个因素进行讨论。在单因素试验的基础上,每因素取3 个适合水平,选用L9(34)正交表,以微胶囊包埋率为指标,确定微胶囊喷雾干燥的最佳工艺参数。
表6 复合微胶囊喷雾干燥正交试验设计与结果
Table 6 Orthogonal array design with experimental results for spray drying process
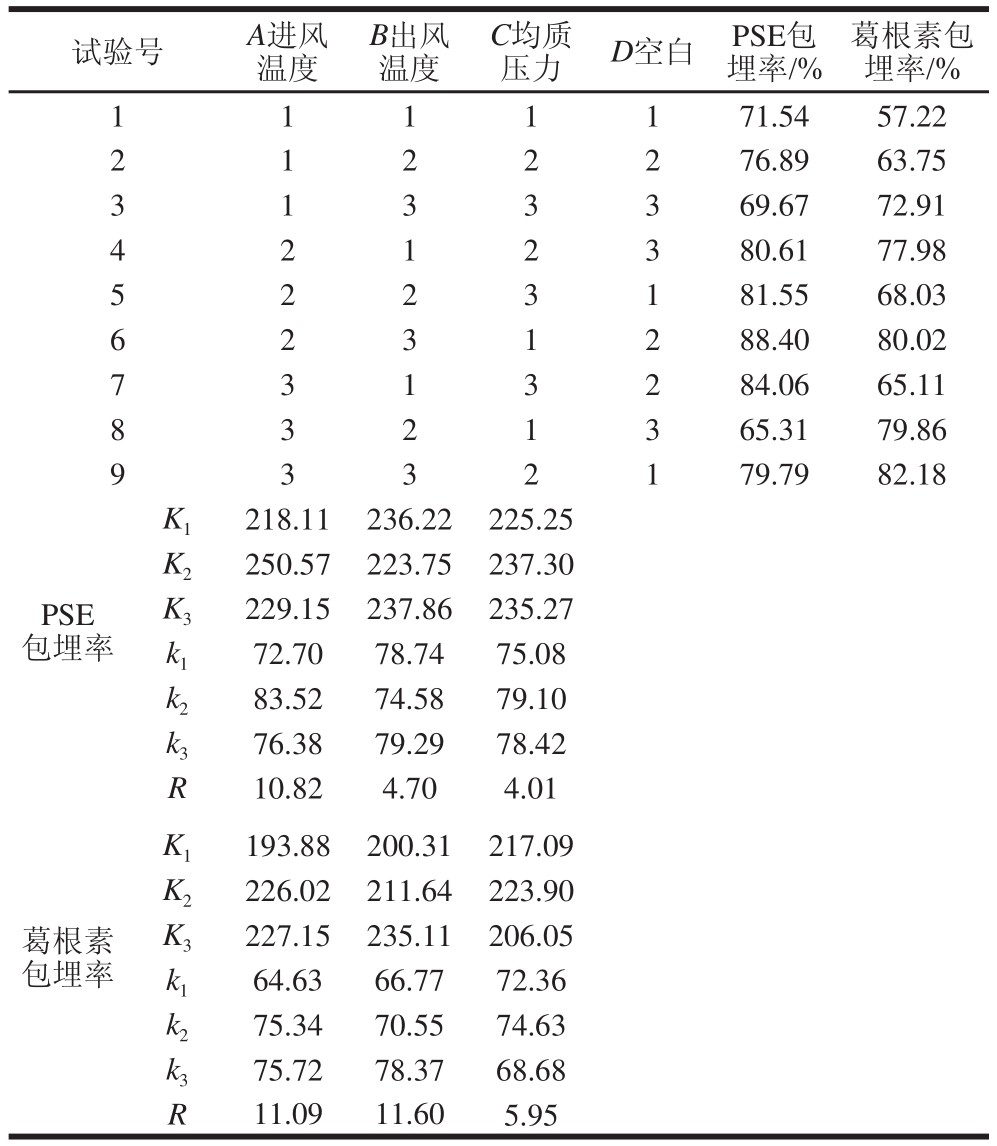
表7 复合微胶囊喷雾干燥正交试验数据方差分析
Table 7 Analysis of variance of the orthogonal array design for spray drying process

由表6、7可知,极差R和方差分析得出各因素影响PSE包埋率大小顺序均为:A>B>C,即影响PSE微胶囊化效率的主次因素依次为:进风温度、出风温度、均质压力;葛根素包埋率R大小顺序为:B>A>C,方差分析得出各因素影响葛根素包埋率大小顺序:A>B>C,以方差分析为准,影响葛根素微胶囊化效率的主次因素依次为:进风温度、出风温度、均质压力。从正交9 组试验结果来看,第6组试验结果比较理想,可保证两者较高的包埋率(PSE包埋率为88.40%,葛根素包埋率为80.02%),其工艺组合为A2B3C1;从正交结果分析来看,PSE包埋率为指标的最佳工艺组合为A2B3C2,葛根素包埋率为指标的最佳工艺组合为A3B3C2,两者条件不一致,需进行综合评价。由于因素A在PSE包埋率中是主要因素,在葛根素包埋率中是次要因素,因此按PSE包埋率要求A2为优水平。这样综合平衡因素水平的较优组合为A2B3C2,该组合工艺未在9组正交试验中,需进行验证实验,验证实验表明在A2B3C2工艺条件下,即进风温度180 ℃、出风温度75 ℃、均质压力25 MPa时,PSE包埋率为89.04%,葛根素包埋率为80.15%。
2.3 复合微胶囊制品质量评价
2.3.1 复合微胶囊感官质量
微胶囊气味纯正,在自然光下为乳白色,粉末状颗粒且细小均匀,休止角为43.3°,流动性较好。
2.3.2 复合微胶囊物理指标
复合微胶囊的水分含量为3.57%,密度为0.568 g/mL,溶解率为95.11%。
2.3.3 复合微胶囊贮藏稳定性
采用Schaal烘箱法对原料和微胶囊粉末进行强制氧化,对比包埋前后产品的抗氧化效果。对微胶囊粉末和原料进行连续7 d氧化,每24 h测定两者的过氧化值,结果见表8。
表8 复合微胶囊氧化稳定性测定
Table 8 Oxidation stability of composite microcapsules meq/kg
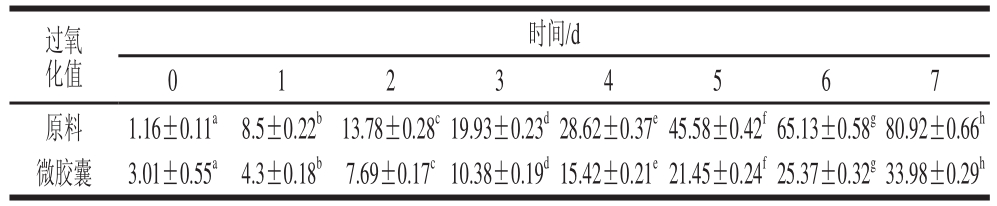
注:同行上标字母不同表示差异显著,P<0.05。
从表8可知,0 d微胶囊粉末的过氧化值略高于原料的过氧化值,这可能是因为在进行喷雾干燥时,部分原料即芯材没有被包埋进去,在进风温度180 ℃高温条件下出现氧化所导致。随后开始进行连续7 d加速氧化(60 ℃,1 d相当于常温条件下16 d ),原料在第5天过氧化值升高,观测感官品质变坏,同时有异味;微胶囊粉末连续7 d加速氧化,过氧化值逐步升高,感官无明显变化,无异味,原料进行微胶囊化后,明显提高抗氧化稳定性,延长微胶囊产品货架期。
影响乳化液稳定性的因素包括壁材选择和配比、乳化剂用量、芯壁比、固形物含量等因素,其中壁材的选择是制作稳定乳化液和获得高微胶囊效率的重要前提[25]。阿拉伯胶在植物水溶胶中应用最为广泛,其由L-鼠李糖、阿拉伯糖、D-葡萄糖醛酸、D-半乳糖以及约2%的蛋白糖构成,具有突出的乳化性能和较好的成膜性能,高质量浓度时仍具有低黏度性,此外其水溶液无色透明,无异味,满足多数壁材要求,但价格偏贵。β-环状糊精价格低廉,性质稳定,其空腔内径达7.0~8.0 nm,十分适合包埋大分子和油性物质,减缓芯材在光、热、氧条件下的反应,提高物质稳定性,同时可以掩蔽异味,可与阿拉伯胶复配作为壁材填充物。以阿拉伯胶作为壁材,β-环状糊精作为壁材填充物分别对乳化剂的配比、乳化剂用量、壁材比、芯壁比、固形物含量等影响乳化液稳定性的重要因素进行了单因素试验和正交试验,得出在乳化条件为复合乳化剂(蔗糖酯-单甘酯)质量比6∶4、乳化剂用量0.7%、壁材(阿拉伯胶和β-环状糊精)比5∶5、芯壁比0.25∶1、固形物含量20%时,乳化液稳定性最高。
乳化液喷雾干燥制作微胶囊粉末。影响喷雾干燥的因素包括乳化液的均质压力、进料温度、进风温度、出风温度、蠕动泵转速、喷雾压力等,本研究从进风温度、出风温度、均质压力3 个方面,考察对微胶囊形成的影响。用最佳配方制备的乳化液进行喷雾干燥,在进行单因素试验和正交试验后发现,在进风温度180 ℃、出风温度75 ℃、均质压力25 MPa条件下,PSE包埋率为89.04%,葛根素的包埋率为80.15%,制得的复合微胶囊产品为乳白色、细小均匀的粉末,其气味纯正,稳定性强,溶解率较高,水分含量较低,便于贮存,达到实验要求。
参考文献:
[1] CHEN Wangchuang, HAYAKAWA S, YAMAMTO T, et al. Mediation of β-endorphin by the isoflavone puerarin to lower plasma glucose in streptozotocin-induced diabetic rats[J]. Planta Medica, 2004, 70(2): 113-116. DOI:10.1055/s-2004-835851.
[2] 张利夫, 陈少伟. 葛根素对高脂血症患者ET、NO及血脂的影响[J].医学临床研究, 2008, 25(8): 1417-1419.
[3] VILLENEVE P, TURON F, CARO Y, et al. Lipase-catalyzed synthesis of canola phytosterols oleate esters as cheolesterol lowering agents[J]. Enzyme and Microbial Technology, 2005, 37: 150-155. DOI:10.1016/j.enzmictec.2005.02.002.
[4] YANKAH V V, JONES P J H. Phytosterols and health implicationscommercial products and their regulation[J]. Inform-International News on Fats Oils and Related Materials, 2001, 12(10): 1011-1017.
[5] BLAIR S N, CAPUZZI D M, GOTTLIEB S O, et al. Incremental reduction of serum total cholesterol and low-density lipoprotein cholesterol with the addition of plant stanol ester-containing spread to statin therapy[J]. American Journal of Cardiology, 2000, 86(1): 46-52.
[6] GABAY O, SANCHEZ C, SALVAT C, et al. Stigmasterol: a phytosterol with potential anti-osteoarthritic properties[J]. Osteoarthritis Cartilage, 2010, 18(1): 106-116.
[7] STEFANI E D, BOFFETTA P, RONCO A L, et al. Plant sterols and risk of stomach cancer: a case-control study in Uruguay[J]. Nutr Cancer, 2000, 37(2): 140-144. DOI:10.1207/S15327914NC3724.
[8] 刘虹蕾, 缪铭, 江波等. 植物甾醇酯的研究与分析[J]. 食品工业科技, 2012, 33(4): 434-437.
[9] 程远渡, 易有金, 易传祝, 等. 植物甾醇酯和葛根素联合使用对高脂血症小鼠降血脂作用研究[J]. 中国油脂, 2015, 40(4): 64-68.
[10] 崔炳群, 王三永, 李晓光, 等. 植物甾醇酯微胶囊化研究[J]. 食品工业科技, 2002, 23(7): 25-29.
[11] 刘福斌, 张根生, 刘广, 等. 微胶囊化玉米胚芽油粉的研制[J]. 现代食品科技, 2011, 27(2): 173-177. DOI:10.3969/ j.issn.1673-9078.2011.02.014.
[12] 徐文秀, 吴彩娥, 李强, 等. 丁香油喷雾干燥微胶囊技术研究[J]. 食品科学, 2006, 27(1): 278-281. DOI:10.3321/ j.issn:1002-6630.2006.01.066.
[13] 刘全亮, 马传国, 季敏, 等. 棕榈油微胶囊化制备工艺研究[J]. 粮食与油脂, 2014, 27(1): 32-35.
[14] 赵巍, 王军, 段长青, 等. 喷雾干燥法制备微胶囊化山葡萄籽油粉末油脂[J]. 中国粮油学报, 2009, 24(12): 77-83.
[15] 郭立华. 玉米醇溶蛋白微胶囊的制备及性质研究[D]. 天津: 天津科技大学, 2012.
[16] 夏辉, 刘欣荣. 甾醇酯微胶囊制备工艺研究[J]. 粮油食品科技, 2012, 20(1): 30-33. DOI:10.3969/j.issn.1007-7561.2012.01.009.
[17] 王丽娟, 李志芬, 闫新丽, 等. 芝麻油微胶囊化复合壁材的选择及工艺条件的研究[J]. 油脂工程, 2007(3): 56-58.
[18] 陈琳, 李荣, 姜子涛, 等. 微胶囊化方法对紫苏油包埋性能的比较研究[J]. 食品工业科技, 2013, 34(20): 176-180.
[19] 冯岩. 复合凝聚法制备维生素E微胶囊的研究[D]. 无锡: 江南大学, 2008.
[20] 康吟, 陶宁萍, 王锡昌. 喷雾干燥法制取宝石鱼油微胶囊技术的研究[J]. 现代食品科技, 2007, 23(7): 59-62.
[21] 吴姣, 郑为完, 周德红, 等. 粉末油脂过氧化值测定方法的研究[J]. 中国油脂, 2006, 31(7): 54-55. DOI:10.3321/ j.issn:1003:7969.2006.07.016.
[22] 魏巍, 李敏, 李纯, 等. 1,3-二油酸-2-棕榈酸结构油脂微胶囊的研制[J].食品工业科技, 2013, 34(20): 294-301.
[23] 冯卫华, 刘邻渭, 许克勇. 猕猴桃籽油微胶囊化技术研究[J]. 农业工程学报, 2004, 20(1): 234-237. DOI:10.3321/j.issn:1002-6819.2004.01.056.
[24] LIU Xiangdong, ATARASHI T, FURUTA T, et al. Microencapsulation of emulsified hydrophobic flavors by spray dying[J]. Drying Technology, 2001, 19(7): 1361-1374. DOI:10.1081/DRT-100105293.
[25] 张旭. 五味子木脂素微胶囊的研制及其抗疲劳功效研究[D]. 长春:吉林农业大学, 2008.
LUO Chengyin, CHENG Yuandu, YI Youjin*, XIA Bo, ZHOU Hongli*, CAO Xi
(Hunan Provincial Key Laboratory of Food Science and Biotechnology, College of Food Science and Technology, Hunan Agricultural University, Changsha 410128, China)
Abstract: Using gum arabic and β-cyclodextrin as wall materials, blend microcapsules of phytosterol esters and puerarin were prepared by a spray drying method. The influences of emulsifier composition, emulsifier dosage, solids content, core material-to-wall material ratio, and gum Arabic-to-β-cyclodextrin ratio on emulsion stability were investigated as well as the influences of inlet temperature, outlet temperature and homogenization pressure on microencapsulation efficiency. The optimum processing parameters for the preparation of composite microcapsules were determined by combined use of single factor and orthogonal array experiments as follows: emulsifier dosage (sucrose ester : monoglyceride = 6:4, g/g), 0.7%; solid content, 20%; core material/wall material ratio, 0.25:1; wall material composition, acacia senegal:β-cyclodextrin = 5:5; inlet temperature, 180 ℃; outlet temperature, 75 ℃; and homogenization pressure, 25 MPa. Under the optimum conditions, the microencapsulation efficiency of phytostetol esters and puerarin were 89.04% and 80.15%, respectively. The composite microcapsule was a milky white, uniform fine powder that smells pure. It had a moisture of 3.57%, density of 0.568 g/mL and solubility of 95.11%, and exhibited high storage stability.
Key words: phytosterol ester; puerarin; microcapsules; spray drying
中图分类号:TS202.3
文献标志码:A
文章编号:1002-6630(2016)06-0026-08引文格式:
DOI:10.7506/spkx1002-6630-201606005
*通信作者:易有金(1968—),女,教授,博士,研究方向为微生物活性物质、功能性食品。E-mail:yiyoujin@163.com
作者简介:罗程印(1992—),男,硕士研究生,研究方向为功能性食品。E-mail:luochengyin503@163.com
基金项目:“十二五”国家科技支撑计划项目(2015BAD16B00;2015BAD16B01);国家自然科学基金面上项目(31071738;31000827);湖南省教育厅重点项目(10A051)
收稿日期:2015-07-30