表1 外观评价表
Table 1 Criteria for appearance evaluation

色泽形态光滑度得分黄褐色、色泽均匀形态完整表面光滑4~5黄褐色、色泽较均匀形态较完整表面较光滑3~4黄褐色、色泽不均匀形态不完整表面粗糙1~2
郑丹丹,王京龙 *,张立华,王 飞,王洪凤
(枣庄学院生命科学学院,山东 枣庄 277160)
摘 要:目的:制备竹叶提取物泡腾片并对其进行质量分析。方法:以崩解时限、pH值、硬度为指标,采用正交试验设计筛选竹叶提取物泡腾片中泡腾剂(柠檬酸、碳酸氢钠)的最佳组成和润滑剂(聚乙二醇6000)的使用方法,并考察泡腾产品的总黄酮含量、崩解时限、pH值、硬度和发泡量。结果:泡腾剂的最佳组成为柠檬酸质量分数20%、碳酸氢钠质量分数20%,制备工艺采用聚乙二醇6000包裹碳酸氢钠后实施粉末直接压片。最优工艺所得泡腾片呈弱酸性,可迅速崩解,发泡量为13.7 mL/g,总黄酮含量为52 mg/g。结论:该工艺所制备的竹叶提取物泡腾片外观良好,崩解迅速,溶解后溶液澄清透明、呈弱酸性。
关键词:竹叶提取物;泡腾片;制备工艺;质量分析
郑丹丹, 王京龙, 张立华, 等. 竹叶提取物泡腾片的制备工艺优化及其质量分析[J]. 食品科学, 2016, 37(8): 39-44.
ZHENG Dandan, WANG Jinglong, ZHANG Lihua, et al. Optimized preparation and quality analysis of bamboo leaf extract effervescent tablets[J]. Food Science, 2016, 37(8): 39-44. (in Chinese with English abstract) DOI:10.7506/spkx1002-6630-201608007. http://www.spkx.net.cn
竹子是禾本科(Gramineae)竹亚科(Bambusoideae Nees)多年生常绿植物 [1]。竹叶提取物是一种以黄酮类物质为主要成分的植物制剂,同时还有生物活性多糖、多种氨基酸、芳香化合物等,具有优良的抗肿瘤 [2]、抗氧化 [3]、抗菌及保护心血管、防治老年退行性疾病 [4-5]等功效。
本研究将泡腾片的制剂技术应用于制备竹叶提取物泡腾片,可提高竹叶中黄酮类物质的生物利用度 [6],有望开发成为一种新的植物源保健品。泡腾片加水后在泡腾剂作用下产生气泡使其溶解,而泡腾剂多为有机酸和含碳弱碱组成,有机酸一般用枸橼酸、酒石酸、苹果酸等 [7]。泡腾片在制备过程中常常面临溶解性差、黏冲,泡腾效果、硬度及口感不佳等问题,为获得合格片剂,在处方及工艺筛选过程中需以崩解时限、pH值、硬度和发泡量 [8]等为指标来评价所得泡腾片。
目前,已有竹叶饮料、竹叶啤酒和竹叶黄酮保健药物等产品的研发 [9],但是鲜有将竹叶提取物制成崩解迅速、吸收好的泡腾片剂型的报道。因此,本研究将竹叶提取物制备成泡腾片,并通过正交试验优化主要辅料的最佳配比及最佳制备工艺,制得口感良好、食用方便、起效迅速、具有调节免疫力、抗疲劳、降血脂、清热解毒 [10-11]等保健功效的竹叶提取物泡腾片。
1.1 材料与试剂
竹叶提取物 陕西恒德堂植物原料有限公司;柠檬酸 国药集团化学试剂有限公司;聚乙二醇6000、甘露醇、乳糖 天津市风船化学试剂科技有限公司;95%乙醇溶液(分析纯) 天津四友精细化学品有限公司;碳酸氢钠、亚硝酸钠等均为分析纯。
1.2 仪器与设备
UV-2000紫外-可见分光光度计 上海尤尼柯仪器有限公司;98-I-C数显控温电热套 苏州江东精密仪器有限公司;PHS-2F数字pH计、FA1104电子分析天平上海仪电科学仪器股份有限公司;XT5118-OV70电热鼓风干燥箱 杭州雪中炭恒温技术有限公司;2P-5A旋转式压片机 青州市精诚医药装备制造有限公司;片剂四用测定仪 上海黄海药检仪器有限公司。
1.3 方法
1.3.1 竹叶提取物泡腾片的制备工艺
预实验中采用湿法制粒,效果不好,颗粒与粉末不能均匀混合,且有黏冲现象。因此选用简单方便的粉末直接混合压片技术,所得泡腾片产品质量较稳定。
1.3.1.1 润滑剂加入方式一
将润滑剂与泡腾剂碱相混合均匀,加热熔融后冷却,粉碎,过80 目筛。另将泡腾剂酸源、甘露醇、乳糖过80目筛,与适量竹叶提取物、上述细粉混匀,直接压片即得 [12-14]。
1.3.1.2 润滑剂加入方式二
将润滑剂、泡腾剂、甘露醇、乳糖分别粉碎,过80 目筛,与竹叶提取物混合均匀,直接压片即得 [15-16]。
1.3.2 竹叶提取物泡腾片配方优化单因素试验
1.3.2.1 泡腾剂种类的选择
泡腾剂中酸源和碱源的选择会影响泡腾片的口感、产气效果等,为控制泡腾片的产品质量,首先通过预实验筛选出适宜的泡腾剂种类。其中碱源通常为碳酸钙、碳酸氢钠或碳酸钠等,经实验发现碳酸钙产气效果不佳且有沉淀现象,而碳酸钠口感较差,因此选择碳酸氢钠为泡腾剂的碱源。然后固定酸碱比为1∶1(质量比,下同),分别以苹果酸、柠檬酸、酒石酸为酸源,采用粉末直接压片,以外观、溶解效果、口感为评价指标,按优(5)、良(4)、中(3)、差(2)、劣(1)进行评分 [17],从而选择最优酸源。感官评审员(30人)均接受过感官实验训练,评审员对每一处方组合所制得的泡腾片进行品尝,根据感官评定标准进行评分,具体评分标准见表1~3,结果取3次评分的平均值。
表1 外观评价表
Table 1 Criteria for appearance evaluation

色泽形态光滑度得分黄褐色、色泽均匀形态完整表面光滑4~5黄褐色、色泽较均匀形态较完整表面较光滑3~4黄褐色、色泽不均匀形态不完整表面粗糙1~2
表2 溶解效果评价表
Table 2 Criteria for dissolubility evaluation

溶液不溶物崩解时限产气效果得分未见不溶物崩解迅速(<3 min)发泡量适中(10~15 mg/L)4~5可见不溶物崩解稍慢(3~5 min)发泡量偏少(5~10 mg/L)3~4有明显可见不溶物崩解迟缓(>5 min)发泡量过少(0~5 mg/L)1~2
表3 口感评价表
Table 3 Criteria for taste evaluation

爽口程度酸甜程度细腻程度得分清爽可口酸甜可口细腻、入口柔顺4~5爽口度较好较酸或较甜细腻、柔顺度较好3~4爽口度差过酸或过甜细腻、柔顺度差1~2
1.3.2.2 泡腾剂酸碱比的选择
固定竹叶提取物质量分数25%、润滑剂质量分数10%、甘露醇质量分数15%,乳糖作填充剂,选择泡腾剂酸碱比为4∶1、3∶1、3∶2、4∶3、1∶1、2∶3、1∶3,按粉末直接混合压片法制备竹叶泡腾片,测定其发泡量及溶解后溶液的pH值。各组试验平行进行3次。
1.3.2.3 润滑剂种类的选择
分别以聚乙二醇6000、硬脂酸镁、滑石粉为润滑剂 [18],按1.3.1.2节方法制备竹叶泡腾片,每组制备3批,通过观察片剂外观性状判断润滑剂的最佳种类。结果发现,当硬脂酸镁或滑石粉质量分数超过1%时,片剂溶解后可见明显不溶物,而用聚乙二醇6000所得颗粒较均匀,压片后溶解,未见不溶物。因此,虽然硬脂酸镁或滑石粉压片后的外观更好,但考虑到溶解效果,仍选择聚乙二醇6000作为润滑剂。
1.3.2.4 润滑剂质量分数的选择
固定竹叶提取物质量分数15%、甘露醇质量分数15%、泡腾剂酸碱比1∶1,选择润滑剂聚乙二醇6000质量分数分别为5%、7.5%、10%、12.5%、15%,乳糖作填充剂,按1.3.1.2节方法制备竹叶泡腾片,每组制备3 批,观察压片情况及产品外观。
1.3.2.5 竹叶提取物质量分数的选择
固定润滑剂质量分数10%、甘露醇质量分数15%、泡腾剂酸碱比1∶1,选择竹叶提取物质量分数分别为15%、30%、45%,乳糖作填充剂,按1.3.1.2节方法制备竹叶泡腾片,每组制备3 批,观察外观及溶解效果。
1.3.3 正交试验优化竹叶提取物泡腾片配方
固定竹叶提取物质量分数25%、润滑剂质量分数10%、甘露醇质量分数15%,乳糖作填充剂,照1.3.1.1或
1.3.1.2 节方法制备竹叶提取物泡腾片,每组制备3 批,分别以崩解时限、pH值、硬度为考察指标,设计L 9(3 4)正交试验表,因素水平设计见表4,优选处方中润滑剂的使用方法、泡腾剂酸源及碱源的最佳质量分数 [19-20]。
表4 正交试验因素与水平
Table 4 Factors and their coded levels used in orthogonal array design
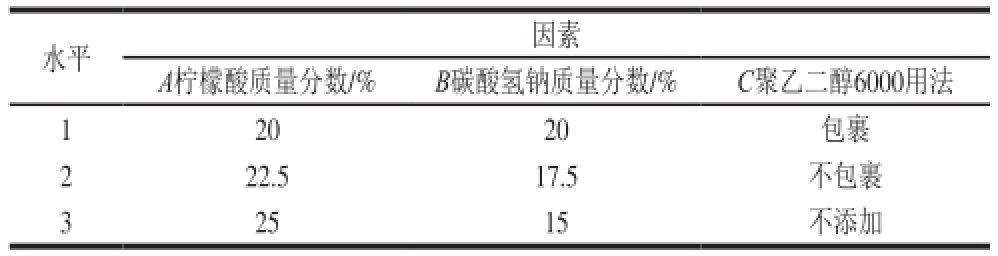
水平因素A柠檬酸质量分数/%B碳酸氢钠质量分数/%C聚乙二醇6000用法1 2020包裹2 22.517.5不包裹3 2515不添加
1.3.4 工艺验证
按1.3.3节所得优化工艺条件制备泡腾片3批,以崩解时限、pH值、硬度为指标进行工艺验证 [21]。
1.3.5 竹叶泡腾片的质量考察
1.3.5.1 pH值测定
取泡腾片3 片,分别分散于100 mL 20 ℃蒸馏水中,测定各溶液的pH值 [22],计算3 次结果平均值。
1.3.5.2 崩解时限的测定
取本品1 片,置于盛有200 mL温水(约20 ℃)的烧杯中,待片剂周围气体停止逸出时,片剂应溶散完全无残留。同法检查6 片,均应在5 min内崩解。
1.3.5.3 硬度考察
以片剂四用测定仪检查泡腾片硬度,应符合2010版《中国药典》 [7]规定。
1.3.5.4 发泡量检查
采用质量损失法,取泡腾片1 片,研磨,精密称取片粉适量(1 g左右),置于已精密称质量的含水烧杯中,待其发泡完全,再精密称量烧杯及溶液总质量 [23]。该操作平行进行6 次,分别计算单位质量CO 2的体积取平均值。CO 2气体生成越多,此配方泡腾效果就越好。
1.3.6 总黄酮含量的测定
1.3.6.1 对照品溶液的制备
精密称定芦丁对照品适量,加乙醇制成0.20 mg/mL的芦丁乙醇溶液,即得。
1.3.6.2 泡腾片溶液的制备
精密称取竹叶泡腾片粉0.15 g,置具塞锥形瓶中,加稀乙醇25.00 mL,摇匀,超声5 min,放置3 h后过滤。精密量取续滤液2 mL,置25 mL量瓶中,加水稀释至刻度,摇匀,作为供试品溶液 [24]。精密量取上述供试品溶液2 mL,置25 mL量瓶中,加水至刻度,摇匀,作为空白溶液。
1.3.6.3 线性关系的考察
精密量取1.3.6.1节对照品溶液1、2、3、4、5、6 mL,分别置于25 mL量瓶中,加水至6 mL,加1 mL 5%亚硝酸钠溶液,混匀,静置6 min后加1 mL 10%硝酸铝溶液,摇匀,再静置6 min后加10 mL氢氧化钠溶液,最后加水定容至刻度,摇匀,静置15 min。在500 nm波长处测定所配系列溶液的吸光度,以吸光度为纵坐标,质量浓度为横坐标,绘制标准曲线,得出标准曲线方程。
1.3.6.4 精密度考察
精密量取1.3.6.1节对照品溶液2.0 mL,按1.3.6.3节方法,连续测定5 次,计算得相对标准偏差(relative standard deviation,RSD)为0.469%,表明方法精密度良好。
1.3.6.5 稳定性考察
精密量取1.3.6.1节对照品溶液2.0 mL,按1.3.6.3节方法,分别于0、2、4、6、8、12 h连续测定6次,计算得RSD为0.981%,证明显色生成的络合物稳定性良好。
1.3.6.6 重复性考察
称取竹叶提取物0.15 g,按1.3.6.2节方法制备供试品溶液,精密量取2.0 mL,置25 mL量瓶中,照1.3.6.3节方法,自“加水至6 mL”起,依法测定吸光度。重复考察6次,计算得RSD为1.138%,证明方法重复性良好。
1.3.6.7 回收率考察
精密称取竹叶提取物0.15 g,与适量芦丁对照品混合均匀,按1.3.6.2节方法,制备供试品溶液,平行制备6 份,按1.3.6.3节方法测定,计算回收率,平均回收率为105.1%,RSD为1.28%,满足测定要求。
1.3.6.8 总黄酮含量计算
测定1.3.6.2节所得供试品溶液的吸光度,代入1.3.6.3节所得标准曲线方程,计算其质量浓度,进而求得竹叶泡腾片中总黄酮含量,实验结果取3 次测量平均值。
1.4 统计分析
使用SPSS v18.0数据统计软件对结果进行分析(n=3)。
2.1 泡腾剂种类的确定
以碳酸氢钠作为泡腾剂碱源,以同比例酒石酸、苹果酸、柠檬酸为酸源,制备竹叶泡腾片并进行感官评价,结果见表5。
表5 不同酸源所得泡腾片的感官评价结果
Table 5 Sensory evaluation scores of tablets with different acidities
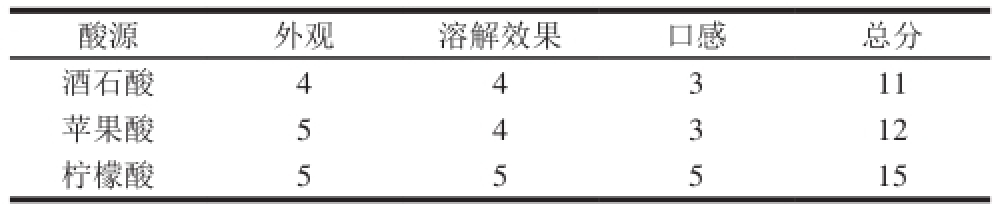
酸源外观溶解效果口感总分酒石酸44311苹果酸54312柠檬酸55515
表5显示,由柠檬酸作为泡腾剂酸源所制片剂的感官评分较高,片剂外观良好,崩解迅速,溶液无可见异物,且口感较好。因此,选择柠檬酸作为酸源。
2.2 泡腾剂酸碱比的确定
以柠檬酸作为泡腾剂的酸源,碳酸氢钠为碱源,选用不同配比的泡腾剂制备泡腾片,测定其发泡量(CO 2体积)和溶解后溶液的pH值,结果见表6。
表6 泡腾剂配比对片剂发泡量和pH值的影响
Table 6 Effect of acid-to-alkaline ratio on gas production and pH
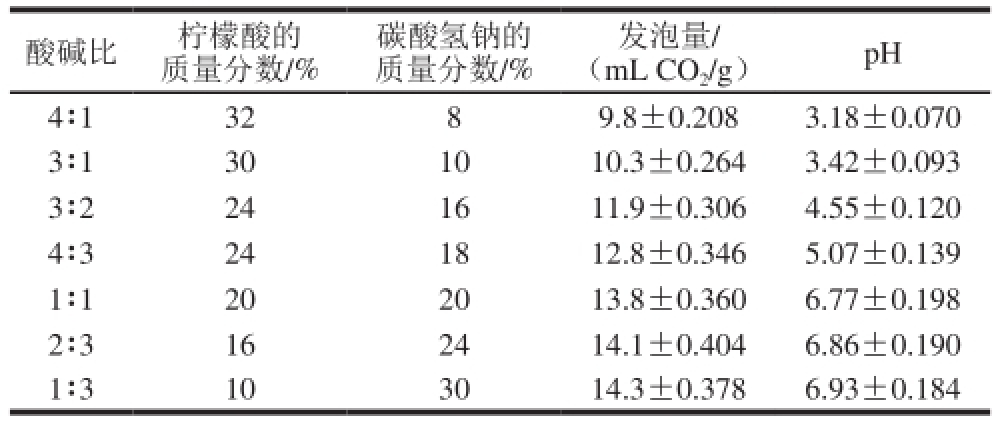
酸碱比柠檬酸的质量分数/%碳酸氢钠的质量分数/%发泡量/(mL CO 2/g)pH 4∶13289.8±0.2083.18±0.070 3∶1301010.3±0.2643.42±0.093 3∶2241611.9±0.3064.55±0.120 4∶3241812.8±0.3465.07±0.139 1∶1202013.8±0.3606.77±0.198 2∶3162414.1±0.4046.86±0.190 1∶3103014.3±0.3786.93±0.184
研究过程中发现,在一定范围内随着碱相添加比例的增加,溶液pH值逐渐升高,接近中性。但考虑到产品口味的因素,不宜添加太多碳酸氢钠 [25],因此选定柠檬酸与碳酸氢钠的质量比在5∶3~1∶1范围内进行正交试验设计。
2.3 润滑剂质量分数的确定
泡腾片剂中润滑剂质量分数对压片过程、崩解速率会有不同程度的影响,同时还会影响片剂的口味、色泽等。考察润滑剂质量分数分别为5%、7.5%、10%、12.5%、15%。结果显示,润滑剂加入量过少会出现黏冲现象,但加入过多时,又会阻碍水分进入片剂中心造成崩解迟缓。当润滑剂质量分数为10%时,所得片剂的外观及崩解时限最好,且无黏冲现象。
2.4 竹叶提取物质量分数的确定
将含有不同质量分数竹叶提取物的泡腾片,分别加入400 mL水中冲服。结果显示,竹叶提取物质量分数为15%时,溶液澄清透明,色泽微黄,口感偏淡,气微香;提取物质量分数为35%时,溶液澄清透明,色泽偏黄褐色,口感微涩,略有焦味;当提取物质量分数为25%时,溶液澄清透明,色泽黄,口感适中,气微香。故泡腾片处方中竹叶提取物质量分数选定为25%。
2.5 正交试验结果
以柠檬酸质量分数、碳酸氢钠质量分数、聚乙二醇6000用法为考察因素,以pH值、崩解时限、硬度为评价指标,选择L 9(3 4)正交试验表,结果见表7。
表7 正交试验设计及结果
Table 7 Orthogonal array design with experimental results

试验号A柠檬酸质量分数/% B碳酸氢钠质量分数/% C聚乙二醇6000用法误差pH崩解时限/s硬度/N 1 116.8812759.0 2 1 2 226.8113846.0 1 1 3 326.8914043.5 4 2 1 215.6913944.0 1 3 5 336.0214133.5 6 2 3 136.8312958.0 2 2 7 315.1415337.0 8 3 2 135.2516456.5 3 1 9 3 3 225.1515545.5 pH K 120.5817.7118.9617.71 K 218.5418.0817.6518.85 K 315.5418.8718.0518.10 R5.041.161.311.14崩解时限K 1’405419420419 K 2’409443432433 K 3’472424434434 R’67241415硬度K 1’’148.5140173.5140 K 2’’135.5136135.5135 K 3’’139147114148 R’’131159.513
按照表7数据对试验结果进行方差分析,结果见表8~10。
表8 pH值方差分析结果
Table 8 Analysis of variance for pH

注:F 0.05(2,2)=19,F 0.01(2,2)=99。下同。
来源偏差平方和自由度均方F值P值A柠檬酸质量分数4.28522.14219.15<0.05 B碳酸氢钠质量分数0.23420.1171.05>0.05 C聚乙二醇6000用法0.30020.1501.34>0.05误差0.22420.112
表9 崩解时限方差分析结果
Table 9 Analysis of variance for disintegration time
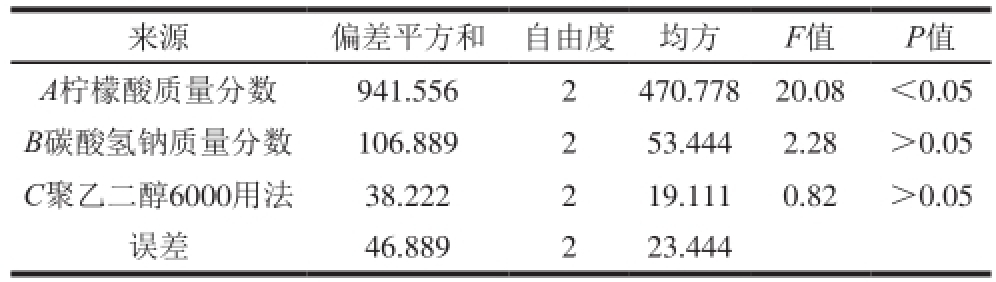
来源偏差平方和自由度均方F值P值A柠檬酸质量分数941.5562470.77820.08<0.05 B碳酸氢钠质量分数106.889253.4442.28>0.05 C聚乙二醇6000用法38.222219.1110.82>0.05误差46.889223.444
表10 硬度方差分析结果
Table 10 Analysis of variance for hardness

来源偏差平方和自由度均方F值P值A柠檬酸质量分数30.167215.0831.05>0.05 B碳酸氢钠质量分数20.667210.3330.72>0.05 C聚乙二醇6000用法605.1672302.58321.11<0.05误差28.667214.333
由正交试验结果可以看出:所考察的3 个因素中,对pH值影响大小的顺序为:A>C>B,柠檬酸质量分数对pH值影响最大(P<0.05),各水平的优劣次序为:A 1>A 2>A 3,B 3>B 2>B 1,C 1>C 3>C 2,所以优水平为A 1(柠檬酸质量分数20%);对崩解时限影响大小的顺序为:A>B>C,柠檬酸质量分数对崩解时限的影响也是最大(P<0.05),其次为碳酸氢钠质量分数,各水平的的优劣次序为:A 1>A 2>A 3,B 1>B 3>B 2,C 1>C 2>C 3,优水平为A 1(柠檬酸质量分数20%);而聚乙二醇是否包裹部分泡腾剂主要影响泡腾片的硬度(P<0.05),其次是柠檬酸质量分数,各水平的优劣次序为:C 1>C 2>C 3,A 1>A 3>A 2,B 3>B 1>B 2,优水平为C 1(包裹);从方差分析的结果看,B因素对pH值、崩解时限、硬度的影响不显著。综合考虑多因素作用,最终确定最佳配比为A 1B 1C 1,即柠檬酸质量分数20%、碳酸氢钠质量分数20%、采用聚乙二醇6000包裹碳酸氢钠,可避免药物直接接触泡腾剂而发生反应,同时制备过程中未见黏冲现象,所得泡腾片崩解迅速,其硬度符合2010版《中国药典》 [7]规定。
2.6 工艺验证实验结果
按所得最佳工艺条件制备竹叶提取物泡腾片3 批,进行工艺验证,结果见表11。
表11 工艺验证实验结果
Table 11 Validation of the optimized formulation

实验号pH崩解时限/s硬度/N 1 6.7313446 2 6.6213751 3 6.7512850平均6.70±0.07133±4.5849±2.65
结果表明,所确定的较优工艺比较稳定,符合2010版《中国药典》 [7]附录ⅠA泡腾片节的规定。
2.7 竹叶泡腾片的质量分析
2.7.1 芦丁标准曲线
按1.3.6.3节方法求得,芦丁标准曲线的回归方程为A=10.609C-0.005 9,R 2=0.999 6,线性关系良好,满足测定要求。
2.7.2 制剂中总黄酮的含量
实验测得竹叶提取物泡腾片中总黄酮的含量为(52.0±0.6)mg/g(RSD为1.216%)。
2.7.3 pH值
按1.3.6.1节pH值测定法,随机选取竹叶提取物泡腾片6 片测定,所得溶液均呈弱酸性,符合2010版《中国药典》 [7]要求。实验以pH值为评价指标的原因在于,泡腾片中使用泡腾剂产气后,过酸或过碱均可能破坏竹叶提取物中黄酮类成分的结构,从而影响泡腾制剂的作用效果,需对产品pH值进行严格控制。
2.7.4 崩解时限
取最优处方所制得泡腾片6 片,按1.3.6.2节方法分别测定其崩解时限,全部在5 min内崩解,符合2010版《中国药典》 [7]泡腾片的质量要求。
2.7.5 制剂发泡量
制剂发泡量测定结果显示,1 g泡腾片粉平均可产生CO 2气体(13.7±0.3)mL(RSD为2.235%)。为消除泡腾片崩解过程对发泡量测定产生的误差,本实验所选用的测定方法是先将泡腾片研磨成粉,再以片粉为对象测定其发泡量,此法可加速CO 2气体的释放,提高实验效率。发泡量的实测值略低于理论值,分析原因可能是由于研磨和称量过程中药物粉暴露在空气中略有吸潮,致使碳酸氢钠有所损失,从而引入误差。
本研究采用工艺简单、操作方便、成本要求较低的粉末直接压片法制备竹叶提取物泡腾片,制得片剂外观整洁、冲调后所得溶液澄清透明。
研究选定聚乙二醇6000作为本品的润滑剂,在单因素试验基础上进行正交试验设计,对泡腾片配方进行优化,结果为:柠檬酸质量分数20%、碳酸氢钠质量分数20%、聚乙二醇6000包裹碳酸氢钠(碱源)。此法可避免主成分与柠檬酸直接接触而发生变质,且制备过程也未见黏冲现象。所得竹叶提取物泡腾片酸碱适宜、崩解时限短、口感好,故选择粉末直接压片与聚乙二醇包裹法制备本品。
本研究制备泡腾片的崩解时限、硬度等质量指标符合2010版《中国药典》 [7]对泡腾片剂的质量要求。而且竹叶提取物具有抗氧化、抗衰老、降血脂等药理活性,开发成目前鲜有报道的泡腾片,兼顾口感好和生物利用度高的优点,市场前景广阔。
参考文献:
[1] 何跃君, 岳永德. 竹叶提取物的有效成分及其应用研究进展[J]. 生物质化学工程, 2008, 42(3): 32-36. DOI:10.3969/ j.issn.1673-5854.2008.03.008.
[2] SANTOS B L, OLIVEIRA M N, COELHO P C, et al. Flavonoids suppress human glioblastoma cell growth by inhibiting cell metabolism, migration, and by regulating extracellular matrix proteins and metalloproteinases expression[J]. Chemico-Biological Interactions,2015, 242: 123-138. DOI:10.1016/j.cbi.2015.07.014.
[3] LU Baiyi, WU Xiaoqin, SHI Jiayi, et al. Toxicology and safety of antioxidant of bamboo leaves. Part 2: developmental toxicity test in rats with antioxidant of bamboo leaves[J]. Food and Chemical Toxicology, 2006, 44(10): 1739-1743. DOI:10.1016/j.fct.2006.05.012.
[4] 夏玉红, 董晋文, 钟耕. 竹叶提取物的研究开发现状[J]. 中国食品添加剂, 2009(2): 77-81. DOI:10.3969/j.issn.1006-2513.2009.02.013.
[5] 金绍黑. 竹叶提取物的制备技术[J]. 技术与市场, 2009, 12(16): 143-145. DOI:10.3969/j.issn.1006-8554.2009.12.116.
[6] ELAD S, ZEEVI I, FINKE J, et al. Improvement in oral chronic graftversus-host disease with the administration of effervescent tablets of topical budesonide-an open, randomized, multicenter study[J]. Biology of Blood and Marrow Transplantation, 2012, 18(1): 134-140. DOI:10.1016/j.bbmt.2011.06.001.
[7] 药典委员会. 中国药典: 二部[M]. 北京: 化学工业出版社, 2010.
[8] 赵存梅, 朱世斌. 药物泡腾剂技术[M]. 北京: 化学工业出版社, 2007: 5-13.
[9] 尹利端, 王桐, 石丽花, 等. 竹叶提取物的工业制备与功效研究进展[J].食品工业科技, 2012, 33(16): 383-386.
[10] 张英. 天然功能性添加剂: 竹叶提取物[J]. 精细与专用化学品,2002(7): 20-22. DOI:10.3969/j.issn.1008-1100.2002.07.008.
[11] 杨抚林, 邓放明, 黄群, 等. 竹叶提取物中功能性成分及效用[J]. 中国食物与营养, 2004(5): 53-55. DOI:10.3969/ j.issn.1006-9577.2004.05.020.
[12] 许宣林. 绿茶泡腾片的制备及质量评价[J]. 中国药业, 2014, 23(3): 42-44.
[13] 田秀峰, 边宝林. 中药泡腾片及工艺研究进展[J]. 中国中药杂志,2004, 29(7): 624-627. DOI:10.3321/j.issn:1001-5302.2004.07.004.
[14] 孙俊杰, 朱友兰. 中药泡腾片的工艺研究概况[J]. 传统医药, 2008,17(10): 72.
[15] 王淑华, 林永强. 泡腾片的常用辅料及制备方法[J]. 食品与药品,2006, 8(3): 70-72. DOI:10.3969/j.issn.1672-979X.2006.03.025.
[16] 郭晓青, 吴金鸿, 刘畅, 等. 明日叶黄酮类物质泡腾饮片的研制[J].食品科学, 2013, 34(12): 346-350. DOI:10.7506/spkx1002-6630-201312072.
[17] 王宁, 陈雪峰, 王锐平. 茶饮料泡腾片的加工工艺[J]. 食品与发酵工业, 2007, 33(3): 151-154. DOI:10.3321/j.issn:0253-990X.2007.03.039.
[18] 崔福德. 药剂学[M]. 北京: 人民卫生出版社, 2006: 111-140.
[19] 肖焕, 张嘉乐, 崔升淼. 山楂叶提取物泡腾片成型工艺的研究[J]. 中南药学, 2010, 8(3): 202-204.
[20] 胡林水, 邵胜荣. 银杏叶提取物泡腾片的研制及质量考察[J]. 中药材, 2005, 28(1): 52-54. DOI:10.3321/j.issn:1001-4454.2005.01.029.
[21] 宋良斌, 陈三宝. 银黄泡腾片的制备工艺研究[J]. 齐鲁药事, 2011,30(1): 8-9. DOI:10.3969/j.issn.1672-7738.2011.01.004.
[22] 王文宝, 南极星. 法莫替丁泡腾片的制备与质量控制[J]. 海峡药学,2011, 23(8): 36-37. DOI:10.3969/j.issn.1006-3765.2011.08.012.
[23] 范宝庆. 黑莓泡腾片的研制[J]. 现代食品科技, 2008, 24(8): 822-824. DOI:10.3969/j.issn.1673-9078.2008.08.023.
[24] 刘江雏, 周荣琪. 竹叶提取物总黄酮含量测定方法的改进[J]. 食品科技, 2005, 30(7): 76-79. DOI:10.3969/j.issn.1005-9989.2005.07.023.
[25] 柴军红, 杨春文, 马怀良, 等. 普洱茶泡腾片的生产工艺优化[J]. 食品科学, 2010, 31(18): 428-432.
Optimized Preparation and Quality Analysis of Bamboo Leaf Extract Effervescent Tablets
ZHENG Dandan, WANG Jinglong
*, ZHANG Lihua, WANG Fei, WANG Hongfeng
(College of Life Sciences, Zaozhuang University, Zaozhuang 277160, China)
Abstract:Objective: To optimize the preparation process of bamboo leaf extract effervescent tablets and to evaluate their quality attributes. Methods: An orthogonal array design was used to optimize the formulation of effervescent tablets including the usage of lubricant (polyethylene glycol 6000) and effervescent agent composition (i.e. ratio of sodium bicarbonate to citric acid) based on pH, disintegration time and hardness. Total flavonoids content and foaming capacity of the optimized effervescent tablets were also analyzed. Results: The optimum combination of effervescent agents was citric acid 20% and sodium bicarbonate 20%. Sodium bicarbonate was wrapped with polyethylene glycol 6000 before direct powder compression. The obtained tablets were slightly acidic and rapidly disintegrated. Foam volume of the tablets was 13.7 mL/g and the content of total flavonoids was 52 mg/g. Conclusion: The obtained effervescent tablets displayed good appearance, rapid disintegration, and clear solution without precipitation after dissolution.
Key words:bamboo leaf extracts; effervescent tablets; preparation; quality analysis
DOI:10.7506/spkx1002-6630-201608007
中图分类号:TS218;R944.4
文献标志码:A
文章编号:1002-6630(2016)08-0039-06
DOI:10.7506/spkx1002-6630-201608007. http://www.spkx.net.cn
收稿日期:2015-08-12
基金项目:山东省自然科学基金项目(ZR2013BL018)
作者简介:郑丹丹(1989—),女,助教,硕士,研究方向为中药制剂新剂型与新技术。E-mail:zddsdu@163.com
*通信作者:王京龙(1988—),男,讲师,博士,研究方向为中药新药研发与中药炮制原理。E-mail:jlwang8121@163.com
引文格式: