张 慧,尹训兰,侯汉学,董海洲 *
(山东农业大学食品科学与工程学院,山东 泰安 271018)
摘 要:为了改善阳离子淀粉的性质,采用微波辐射与半干法结合工艺制备阳离子淀粉,比较微波半干法及半干法两种工艺制备的阳离子淀粉的分子结构及糊液性质的差异。结果显示:相比半干法工艺,微波半干法对阳离子支链淀粉的降解作用更明显。电子显微镜图片显示,半干法阳离子淀粉颗粒形态未发生明显变化,仅表面变得粗糙、破裂,而微波半干法阳离子淀粉颗粒出现了变形和凹坑。微波半干法阳离子淀粉较半干法样品的溶解度、透光率和冻融稳定性提高,峰值黏度及终黏度降低。
关键词:阳离子淀粉;微波;分子质量分布;黏度;淀粉性质
张慧, 侯汉学, 尹训兰, 等. 微波辐射对阳离子淀粉性质的影响[J]. 食品科 学, 2016, 37(15): 118-123. DOI:10.7506/ spkx1002-6630-201615020. http://www.spkx.net.cn
ZHANG Hui, HOU Hanxue, YIN Xunlan, et al. Effect of microwave treatment on the properties of cationic starch[J]. Food Science,2016, 37(15): 118-123. (in Chinese with English abstract) DOI:10.7506/spkx1002-6630-201615020. http://www.spkx.net.cn
阳离子淀粉是一类重要的变性淀粉,广泛应用于食品、造纸、纺织、医药等众多工业领域 [1],其制备方法分为湿法、干法、半干法及溶剂法。半干法工艺以水作为反应介质,体系含水量介于湿法和干法之间,具有工艺简单、反应条件缓和、耗能低、无污染等优点,适合制备高取代度的阳离子淀粉 [1]。在我国能源紧张、水资源短缺、环境污染治理压力大的情况下,半干法成为一种极具优势的制备方法。但半干法工艺存在加热不均匀、加热速率慢等缺点,影响了产品质量的均一性和生产效率,限制了半干法工艺的工业普及 [1-3]。
近年来,微波作为一种新型加热方式,逐渐应用于淀粉工业。微波辐射对淀粉变性反应的影响主要体现在两个方面:1)微波是介质内部无温度梯度的加热方式,在极性高频变换的微波场中,介质分子做有序高频振动,相互碰撞、挤压和摩擦,分子具有的动能转变成热能,快速升温,利于提高淀粉反应活性 [4-6];2)微波辐射使淀粉非结晶区的氢键破坏,致密程度降低,更有利于淀粉分子中羟基与变性试剂反应 [7-9]。赵海波等 [10]采用微波辐射技术合成醋酸淀粉酯,微波加热5 min所得醋酸淀粉酯的取代度为0.14;而常规反应条件下反应时间长达60 min,所得产品取代度一般低于0.1。丁筑红等 [11]采用微波辐射技术制备淀粉磷酸酯,微波加热功率为900 W,微波辐射时间为9 min,所得产品取代度等同于干法工艺140 ℃加热120 min的产品。兰冬梅等 [12]发现一定的微波输出功率和时间能显著提高锥栗抗性淀粉得率。在制备油酸淀粉酯 [13]与马来酸淀粉酯 [14]等变性淀粉的研究中也发现微波能显著提高反应效率。与传统的依靠热对流、热传导的加热方式相比,微波具有低能耗、快速高效、环保等优点,因而在变性淀粉生产应用上具有较大的发展潜力。
目前,国内外对微波在变性淀粉领域的研究集中在工艺参数探讨方面 [10-15],有关微波对变性淀粉的性质影响特别是对分子结构的影响研究报道较少,关于微波法半干法与半干法阳离子淀粉性质的比较研究还未见报道。本研究针对以上问题,将微波辐射技术与半干法工艺相结合制备阳离子淀粉,对相同取代度的微波半干法与半干法阳离子淀粉的理化性质进行比较分析,研究微波辐射对阳离子淀粉分子结构及糊液性质的影响,旨在为阳离子淀粉的高效生产提供一定的数据参考和理论依据。
1.1 材料与试剂
玉米淀粉 山东诸城兴贸有限公司;Shodex Standard P-82普鲁兰多糖 昭和电工株式会社;3氯-2羟丙基三甲基氯化铵((3-chloro-2-hydroxypropyl)trimethylammonium chloride,CHPTMA)、硝酸钠、氢氧化钠、冰醋酸、盐酸、硫酸铜、硫酸钾、硼酸、硫酸、无水乙醇等均为分析纯。
1.2 仪器与设备
高效混合器、干法变性淀粉反应器 山东农业大学粮油食品加工实验室自制;D8023CSL-K4微波炉 格兰仕电器实业有限公司;PHS-25型酸度计 上海伟业仪器厂;101A-1型电热鼓风干燥箱 黄骅市凯丰仪器厂;KDN-04A凯氏定氮仪 上海新嘉电子有限公司;LC-20A液相色谱仪、UV-2450紫外分光光度计 日本岛津有限公司;SUPER-3RVA型快速黏度分析仪 澳大利亚Newport科学仪器公司;S-2500型扫描电子显微镜 日本日立公司;D8 ADVANCE型X射线衍射仪、TENSOR 27型红外光谱仪 德国Bruker公司。
1.3 方法
1.3.1 阳离子淀粉的制备
将1 500 g含水量为14%的玉米淀粉与30.3 g氢氧化钠粉末于高效混合器中混匀,并喷洒一定量质量分数为55%的CHPTMA水溶液,使其反应体系含水量在25%,混匀后采用干法变性淀粉反应器55 ℃条件下加热3~4 h或640 W微波加热4~6 min,反应完毕后,取出样品,用醋酸调pH值至7左右,然后用70%乙醇洗涤样品。样品室温下自然干燥后粉碎过筛,备用。
1.3.2 阳离子淀粉取代度(degree of substitution,DS)的计算 [1]
淀粉含氮量的测定采用凯氏定氮法。取代度按以下公式计算。
式中:W为阳离子淀粉的含氮量与原淀粉的含氮量差值/%;162为脱水葡萄糖残基的相对分子质量;1 400为氮的相对原子质量×100;152.5为阳离子取代基的摩尔质量/(g/mol)。
1.3.3 红外光谱的测定 [3]
将样品置于烘箱中,130 ℃条件下烘至恒质量,放在干燥器中待用。称取2.00 mg样品,200.00 mg溴化钾,磨碎后用压片机压成薄片,采用傅里叶红外光谱仪进行全波段扫描(400~4 000 cm -1),扫描128 次,分辨率为4 cm -1。
1.3.4 凝胶渗透高效液相色谱法测定分子质量
色谱条件:色谱柱:TSK gel columns系列G5000、G3000(Tosohaas);流动相:0.01 mol/L硝酸钠溶液;柱温:30 ℃;流速:0.4 mL/min;检测器:RID-10A示差折光检测器。样品测定:将100 mg淀粉溶解于二甲基亚砜中,在沸水浴中加热0.5 h。加入无水乙醇,在3 000×g离心10 min。沉淀物加10 mL水,100 ℃水浴加热30 min,注入液相色谱进样器,测定阳离子淀粉的分子质量。采用Shodex Standard P-82 Pullulan作为分子质量标准品。使用凝胶渗透色谱(gel permeation chromatography,GPC)软件绘制流出曲线。
1.3.5 淀粉颗粒形态的测定
阳离子淀粉在烘箱内烘至恒质量,加速电压10 kV喷金处理后,采用扫描电子显微镜(scanning electron microscope,SEM)观察阳离子淀粉的颗粒形态。
1.3.6 溶解度的测定 [11]
将2 g/100 mL淀粉溶液85 ℃搅拌30 min,8 000 r/min条件下离心l0 min,取上清液,将其置于培养皿中,105 ℃烘干至恒质量,得到溶解的淀粉质量,按下式计算溶解度。
式中:m 1为上清液烘干后的恒质量/g;m为样品干基质量/g。
1.3.7 透光率的测定 [11]
将20 mL、2 g/100 mL的淀粉溶液置于20 mL具塞刻度试管中,混匀后,沸水浴中加热30 min,每隔5 min振荡试管,使其充分溶解。冷却3 h至室温,以蒸馏水为对照,650 nm波长处测定透光率。
1.3.8 凝沉性的测定 [4]
将20 mL、2 g/100 mL的淀粉溶液置于20 mL具塞刻度试管中,混匀后,沸水浴中加热30 min,每隔5 min振荡试管,使其充分加热。冷却后,8 000 r/min条件下离心l0 min,取上清液,以蒸馏水为对照,650 nm波长处测定其透光率(T 0);取部分上清液于4 ℃保存5 d后取出,自然升温至室温,8 000 r/min条件下离心l0 min,650 nm波长处测其透光率(T),按下式计算凝沉值(以透光率差值表征)。
1.3.9 冻融稳定性的测定 [6]
配制6 g/100 mL的淀粉溶液,取25 mL置于预先称质量的50 mL离心管中,称质量,并计算出淀粉糊的净质量,离心管密封,置于-18 ℃冷却贮藏24 h后取出,自然解冻,3 000 r/min条件下离心20 min,弃去上清液,称取沉淀物质量,按如下公式计算析水率,共进行7次冻融循环。
1.3.10 糊化性质的测定
参照AACC7621 General Pasting Method for Wheat or Rye Flour or Starch Using the Rapid Visco Analyser标准方法1 [16]使用快速黏度分析仪(rapid viscosity analyzer,RVA) 测定样品的糊化性质。分别称取3.0 g已备好的样品,分别与25.0 g蒸馏水混合于RVA样品钵中,搅拌均匀,上机测试。测试过程:50 ℃维持1 min,于3.7 min内升温至95 ℃,保持2.5 min,然后在3.7 min内冷却到50 ℃,保持2 min。样品放入黏度计中的前10 s内以960 r/min的转速搅拌,以后的整个过程转速为160 r/min。RVA测得峰黏度、谷黏度、破损值、终黏度、峰值时间、糊化温度等参数使用Thermocline软件进行分析。
1.4 数据分析
用SPSS 18.0软件中的邓肯氏新多变域测定法(Duncan’s new multiple range test)比较平均值之间的差异(P<0.05)。
2.1 阳离子淀粉样品
通过半干法和微波半干法工艺制备了取代度不同的6种阳离子淀粉样品,样品编号及取代度见表1,通过两种工艺各3个取代度样品的性质分析,研究微波半干法工艺阳离子淀粉与半干法阳离子淀粉性质的差异。
表1 用于性质研究的淀粉样品
Table 1 Starch samples tested in this study

样品样品编号取代度天然玉米淀粉S0半干法阳离子淀粉DS-0.010.01 DS-0.050.05 DS-0.100.10微波半干法阳离子淀粉MDS-0.010.01 MDS-0.050.05 MDS-0.100.10
2.2 阳离子淀粉红外光谱
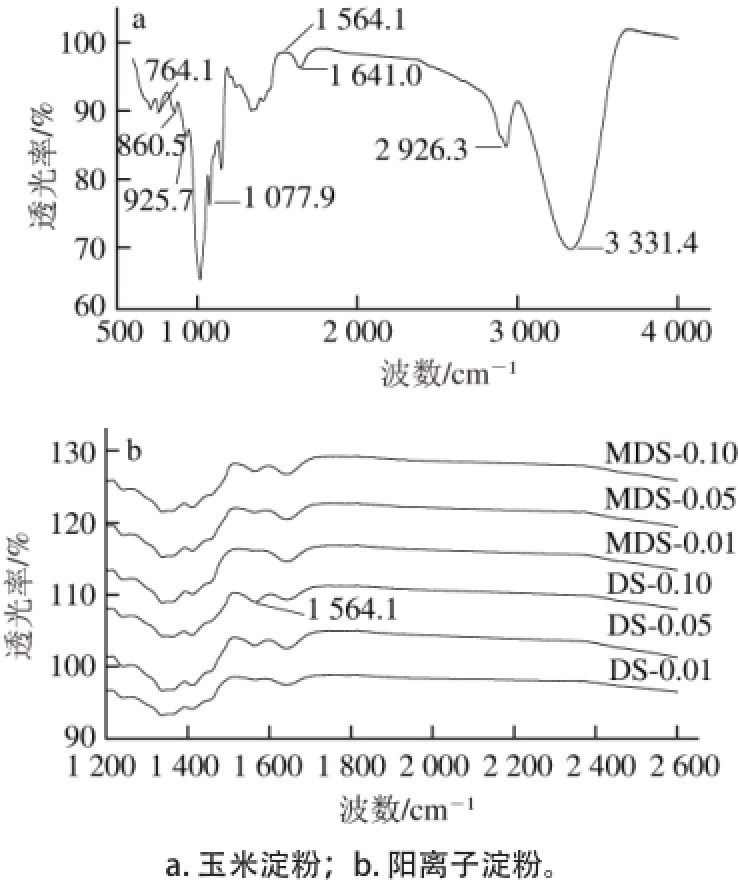
图1 阳离子淀粉的红外光谱
Fig. 1 Infrared spectra of cationic starches
天然玉米淀粉基本组成单位是α-D(+)-脱水葡萄糖单元,主要的特征基团为C连接的伯仲羟基、伯醇羟基以及α-D-吡喃环结构 [1]。由图1a可知,玉米淀粉在3 331.4 cm -1左右的吸收峰是由氢键缔合伸缩振动引起的;2 926.3 cm -1处的吸收峰对应着CH 2中C—H不对称的伸缩振动;1 641.0 cm -1及1 077.9 cm -1附近的吸收峰是与仲醇羟基相连接的C—OH的伸缩振动产生的;葡萄糖单元的环状结构的吸收峰在925.7、860.5、764.1 cm -1附近出现。
由图1b可知,改性后的玉米淀粉在1 564.1 cm -1处出现吸收峰,此吸收峰是由于阳离子试剂季铵基团上的C—N键的伸缩振动造成的,且吸收峰的强度随着取代度的增大而升高;而在天然玉米淀粉红外光谱(图1a)中没有出现这个吸收峰,这表明淀粉已经进行了醚化反应,结合了季铵基团,并且取代度越大,表明与淀粉结合的季铵基越多。并且,取代度相同的微波半干法阳离子淀粉和半干法阳离子淀粉在此处的吸收峰强度基本一致。
2.3 微波辐射对阳离子淀粉分子质量分布的影响

图2 阳离子淀粉分子质量分布曲线
Fig. 2 Molecular weight distribution curves of cationic starches
采用凝胶色谱法测定不同取代度的半干法及微波半干法阳离子淀粉的分子质量,研究微波辐射对淀粉分子质量分布的影响。根据凝胶色谱原理,保留时间越短,分子质量越大。由图2及分子质量分布结果可知,色谱流出曲线上第一个峰(P1)重均分子质量在10 7~10 8g/mol之间,为玉米淀粉的支链淀粉的分子质量分布峰,第二个峰(P2)重均分子质量在10 5~10 6g/mol之间,为直链淀粉及低分子质量淀粉链链的分子质量分布峰。随着取代度的增大,阳离子淀粉中支链淀粉峰面积所占比例逐渐减小,直链淀粉及低分子质量组分峰面积所占比例逐渐增加,且P1峰逐渐向分子质量减小(向右)的方向偏移,P2峰则向分子质量增大(向左)的方向偏移,分析原因可能是经过阳离子化反应过程,支链淀粉发生降解,逐渐转化为低分子质量淀粉链。与相同取代度的半干法阳离子淀粉相比,微波半干法阳离子淀粉的P1峰略偏右,P2峰略偏左,同时伴随着P1含量的降低和P2含量的升高。即微波半干法降解阳离子淀粉中支链淀粉分子的作用比半干法更加明显。宁芯等 [17]在研究微波对大米淀粉物化特性的影响中也发现,经微波辐射后大米淀粉中支链淀粉含量下降,直链淀粉含量上升。这可能是因为在微波电磁场中,随着电场正负极的高频改变,物质分子在进行有序的高频振动,并相互挤压、摩擦、碰撞,这对淀粉分子产生强机械作用,导致其支链化学键断裂而转化为直链淀粉或低分子质量淀粉链 [18]。支链淀粉分子的降解,可能会打破紧密的淀粉链结构,从而提高淀粉分子的反应活性。
2.4 微波辐射对阳离子淀粉颗粒形态的影响

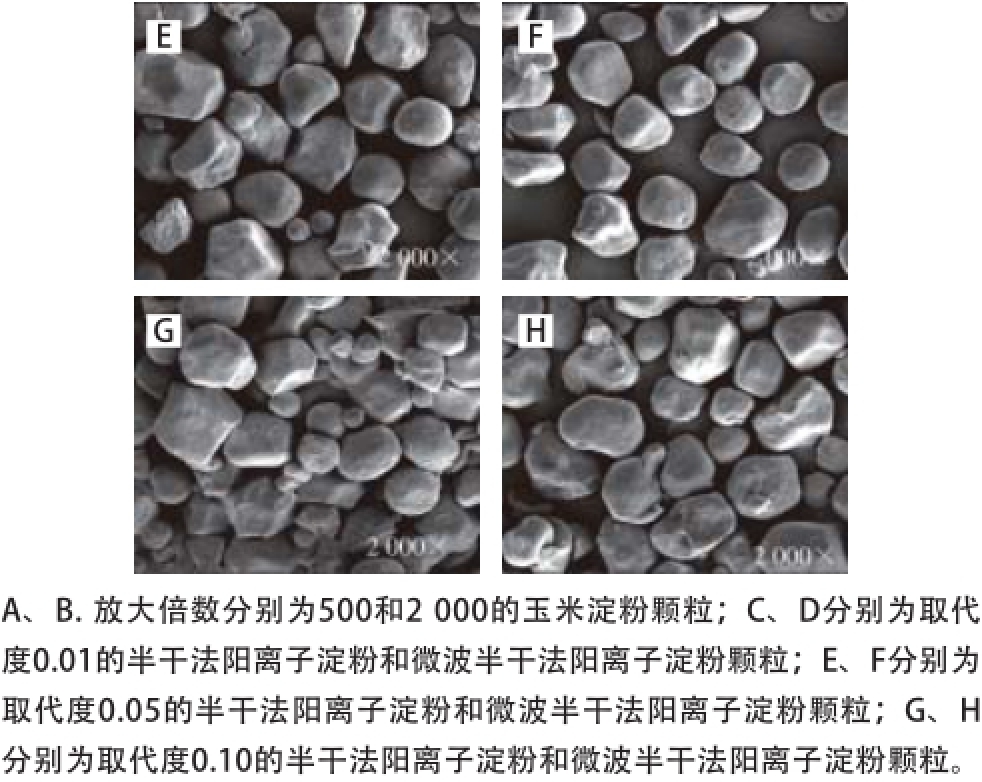
图3 阳离子淀粉扫描电子显微镜图
Fig. 3 SEM photomicrographs of cationic starches
由图3可知,天然玉米淀粉颗粒的形状比较规则,以圆形、椭圆形及多角形为主,颗粒形态完整且结构紧致、表面光滑、棱角分明。淀粉进行阳离子化改性后,淀粉颗粒出现不同程度的破坏。随着取代度增高,淀粉颗粒表面的粗糙程度越来越明显;取代度达到0.10时,半干法阳离子淀粉颗粒表面破坏成碎片,且大量黏连,微波半干法阳离子淀粉不仅表面粗糙,部分颗粒还出现了变形和凹坑。这与罗志刚等 [19]的研究结果相似,其采用微波处理蜡质玉米淀粉及马铃薯淀粉后,发现淀粉颗粒表面变得粗糙,且出现孔洞及凹坑。这可能是因为淀粉颗粒内部分子链结构较弱的部分,如以支链淀粉分支处为主的非结晶区,容易受到微波的热效应及非热效应的影响而造成氢键断裂,甚至淀粉链的断裂,造成淀粉颗粒形态的变化 [20-21]。这将有利于变性试剂通过孔隙进入淀粉链内部,激活淀粉羟基反应活性,从而引起淀粉变性的化学反应动力学变化 [22]。
2.5 微波辐射对阳离子淀粉的溶解度、透光率和凝沉值的影响
表2 阳离子淀粉溶解度、透光率和凝沉值
Table 2 Solubility, transmittance and retrogradation of cationic starches %

注:表中数据为
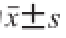 ;同列肩标不同字母表示差异显著(P<0.05)。下同。
;同列肩标不同字母表示差异显著(P<0.05)。下同。
17.42±0.93 d51.70±1.58 d2.19±0.07 aDS-0.0127.02±1.36 c81.75±2.25 c1.90±0.16 bDS-0.0569.51±2.44 b91.68±3.54 b1.25±0.08 cDS-0.1081.27±3.26 a96.72±3.13 a0.97±0.08 dMDS-0.0130.88±3.45 c81.82±4.41 c1.86±0.11 bMDS-0.0579.67±1.28 b92.14±2.56 b1.29±0.14 cMDS-0.1087.71±3.34 a98.98±3.00 a1.02±0.10 d样品溶解度透光率凝沉值S
由表2可知,天然玉米淀粉进行阳离子化改性后,在取代度0~0.10范围内,随着取代度的升高,溶解度和透光率明显提高。溶解度的大小反映了淀粉与水分子之间相互作用的强弱,取代度越大,淀粉颗粒结合的季铵基团越多,淀粉所带正电荷越多,越利于与水结合,从而使溶解度增大 [22]。这也使得淀粉链在糊液中的伸展、分散更加充分,淀粉团粒残余量减少,反射和散射光的能力变差,导致透光率提高。
当取代度相同时,微波半干法阳离子淀粉的溶解度和透光率高于半干法阳离子淀粉,这可能是因为淀粉经微波辐射后,支链淀粉分子结构被破坏,部分长链分解为短链,羟基外露,水分子更易与之结合,使淀粉链更易在水中溶解和分散 [20]。
与天然玉米淀粉相比,微波半干法阳离子淀粉及半干法阳离子淀粉的凝沉值随取代度的升高而逐渐减小。淀粉阳离子化改性后,季铵基团带来的静电效应和空间排斥效应延缓了淀粉链凝聚形成晶体的趋势,减少了凝沉 [17]。而微波半干法阳离子淀粉凝沉值与半干法样品的凝沉值差别不大。
2.6 微波辐射对阳离子淀粉冻融稳定性的影响
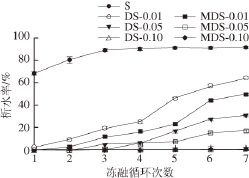
图4 阳离子淀粉冻融稳定性
Fig. 4 Freeze-thaw stability of cationic starches
由图4可知,原淀粉经过1 次冻融后变成海绵状结构,析出大量水分,说明其冻融稳定性较差;随着取代度的升高,阳离子淀粉的析水率逐渐下降,且水析出需要的冻融循环次数增多,说明取代度越高阳离子淀粉的冻融稳定性越好。淀粉糊液在冷冻过程中,随着时间的延长,凝胶淀粉分子间相互作用增大,在淀粉分子链平行取向形成凝胶束时,水分子被迫在凝胶中析出,导致淀粉糊持水性变差。阳离子基团的接入,增强了与水分子之间的结合力,淀粉分子不易重排、缔合,使冻融稳定性得到改善 [23]。相对于同一取代度下的半干法阳离子淀粉,微波半干法阳离子淀粉冻融稳定性更好。分析原因,可能是因为微波辐射使淀粉中部分长链段分解为低分子质量的淀粉链,增加了与水分子的结合,有利于淀粉冻融稳定性的改善。
2.7 微波辐射对阳离子淀粉糊化性质的影响
表3 阳离子淀粉糊化特性
Table 3 Pasting properties of cationic starches

样品峰值黏度/cP谷值黏度/cP衰减值/cP最终黏度/cP糊化温度/℃S1 844±11 g1 018±8 g8 26±13 g1 803±13 g19.57±0.49 aDS-0.014 337±16 e1 408±11 c2 929±17 d2 350±17 b16.37±0.16 bDS-0.056 291±15 a1 336±8 e4 955±7 a2 199±7 e9.80±1.00 cDS-0.105 945±29 f1 065±14 f4 880±9 c2 445±9 a5.63±0.26 dMDS-0.014 278±10 c1 372±16 b2 906±11 e2 317±11 d16.13±0.08 bMDS-0.056 220±11 b1 266±8 d4 954±13 b2 127±13 f9.83±0.26 cMDS-0.105 444±7 d1 030±6 a2 408±10 f2 328±10 c5.67±0.14 d
由表3可知,与天然玉米淀粉相比,阳离子淀粉的糊化温度明显降低,且随着取代度的升高逐渐下降。淀粉进行醚化反应后,结合了季铵基团,带有正电荷,淀粉颗粒与水分子间的亲和力大大提高,水分子易进入颗粒内部,从而使糊化温度下降 [17]。当取代度达到0.10时,阳离子淀粉的糊化温度低于6 ℃。相同取代度条件下,两种工艺制备的阳离子淀粉的糊化温度相差不大。
两种工艺制备的阳离子淀粉的峰值黏度明显高于天然玉米淀粉,且随取代度的升高呈先上升后下降的趋势;相同取代度的微波半干法阳离子淀粉峰值黏度、终黏度及衰减值相对半干法阳离子淀粉低。分析原因可能是微波辐射使淀粉中部分支链淀粉降解为直链淀粉及低分子质量淀粉链,降低了分子间相互作用力,导致淀粉糊液的黏度下降 [24]。衰减值反映了黏度稳定性,衰减值低说明微波半干法阳离子淀粉的糊液稳定性更好。
微波辐射对半干法阳离子淀粉的分子结构和糊液性质有明显影响:与半干法阳离子淀粉相比,微波半干法阳离子淀粉中支链淀粉降解更加明显,支链淀粉含量下降,直链淀粉含量升高,淀粉颗粒形态变化增大。分子结构的改变导致了淀粉糊液性质的变化,微波半干法阳离子淀粉较半干法样品的溶解度、透光率、冻融稳定性提高,糊液峰值黏度和终黏度降低,糊化温度差异不显著。
参考文献:
[1] 张力田. 变性淀粉[M]. 广州: 华南理工大学出版社, 1999: 58-96.
[2] 石海信, 罗婷, 李葵, 等. 微波辐射对淀粉化学变性反应的影响[J]. 广东化工, 2015, 42(7): 31-36. DOI:10.3969/ j.issn.1007-1865.2015.07.015.
[3] SHI Haixin, YIN Yangzhen, JIAO Shufei. Preparation and characterization of carboxymethyl starch under ultrasound-microwave synergistic interaction[J]. Journal of Applied Polymer Science, 2014,131(20): 409-416. DOI:10.1002/app.40906.
[4] 邱怡, 叶君, 熊犍. 微波辐射对淀粉结构及性质的影响[J]. 高分子通报, 2007(2): 57-62.DOI:10.3969/j.issn.1003-3726.2007.02.007.
[5] 何小维, 罗发兴, 罗志刚. 物理场改性淀粉的研究[J]. 食品工业科技,2005, 26(9): 172-174. DOI:10.3969/j.issn.1002-0306.2005.09.054.
[6] 陈 鹏, 黄霜, 李书艺, 等. 微波辐照对玉米淀粉及其改性淀粉理化特性的影响[J]. 食品科学, 2013, 34(1): 121-124.
[7] FAN Daming, MA Wenrui, WANG Liyun, et al. Determining the effects of microwave heating on the ordered structures of rice starch by NMR[J]. Carbohydrate Polymers, 2013, 92(2): 1395-1401.
[8] FAN Daming, WANG Liyun, CHEN Wei, et al. Effect of microwave on lamellar parameters of rice starch through small-angle X-ray scattering[J]. Food Hydrocolloids, 2014, 35: 620-626. DOI:10.1016/ j.foodhyd.2013.08.003.
[9] FAN Daming, WANG Liyun, MA Shenyan, et al. Structural variation of rice starch in response to temperature during microwave heating before gelatinization[J]. Carbohydrate Polymers, 2013, 92(2): 1249-1255. DOI:10.1016/j.carbpol.2012.10.053.
[10] 赵海波, 马涛, 张冶. 微波法制备醋酸酯淀粉的工艺及其性能的研究[J]. 食品科学, 2007, 28(8): 181-184. DOI:10.3321/ j.issn:1002-6630.2007.08.039.
[11] 丁筑红, 谭书明, 黄祥勇, 等. 微波条件对淀粉磷酸单酯取代度的影响及糊化性质研究[J]. 中国粮油学报, 2005, 20(4): 34-38; 43. DOI:10.3321/j.issn:1003-0174.2005.04.009.
[12] 兰冬梅, 林晓岚, 颜谊颖, 等. 微波联合干燥制备锥栗抗性淀粉[J]. 食品与发酵工业, 2015, 41(5): 144-148. DOI:10.13995/ j.cnki.11-1802/ts.201505026.
[13] HORCHANI H, CHA☒BOUNI M, GARGOURI Y, et al. Solventfree lipase-catalyzed synthesis of long-chain starch esters using microwave heating: optimization by response surface methodology[J]. Carbohydrate Polymers, 2010, 79(4): 466-474. DOI:10.1016/ j.carbpol.2009.09.003.
[14] BISWAS A, SHOGREN R L, KIM S, et al. Rapid preparation of starch maleate half-esters[J]. Carbohydrate Polymers, 2006, 64(3): 484-487. DOI:10.1016/j.carbpol.2005.12.013.
[15] DENG Y Z, CATCHMARK J M. Insoluble starch composite foams produced through microwave expansion[J]. Carbohydrate Polymers,2014, 111(13): 864-869. DOI:10.1016/j.carbpol.2014.04.090.
[16] American Association of Cereal Chemists. Approved Methods of the AACC-Method 76-21[S]. St. Paul: AACC, 2000.
[17] 宁芯, 程学勋, 赵思明, 等. 微波对大米淀粉物化特性的影响[J].华中农业大学学报, 2009, 28(3): 369-372. DOI:10.3321/ j.issn:1000-2421.2009.03.026.
[18] ZHAO S M, QIU C G, XIONG S B, et al. A thermal lethal model of rice weevils subjected to microwave irradiation[J]. Journal of Stored Products Research, 2007, 43(4): 430-434. DOI:10.1016/ j.jspr.2006.12.005.
[19] 罗志刚, 扶雄, 罗发兴. 微波辐射下蜡质玉米淀粉性质的变化[J].华南理工大学学报, 2007, 35(4): 34-38. DOI:10.3321/j.issn:1000-565X.2007.04.008.
[20] 陈秉彦, 郭泽镔, 许丽宾, 等. 微波处理对莲子淀粉理化性质的影响[J]. 现代食品科技, 2015, 31(3): 213-218. DOI:10.13982/ j.mfst.1673-9078.2015.3.036.
[21] BLASZCZAKA W, VALVERDE B, FOMAL J, et al. Changes in the microstructure of wheat, corn and potato starch granules during extraction of non-starch compounds with sodium dodecyl sulfate and mercaptoethanol [ J]. Carbohydrate Polymers, 2003, 53(1): 63-73. DOI:10.1016/S0144-8617(03)00004-3.
[22] 石海信, 方丽萍, 王爱荣, 等. 微波辐射下木薯淀粉结构与性质的变化[J]. 食品科学, 2015, 36(3): 68-72. DOI:10.7506/spkx1002-6630-201503013.
[23] 齐晓燕. 挤压法制备阳离子淀粉及其性能研究[D]. 泰安: 山东农业大学, 2012: 35-48.
[24] FAN D M, LIU Y X, HU B, et al. Influence of microwave parameters and water activity on radical generation in rice starch[J]. Food Chemistry, 2016, 196(4): 34-41. DOI:10.1016/ j.foodchem.2015.09.012.
Effect of Microwave Treatment on the Properties of Cationic Starch
ZHANG Hui, YIN Xunlan, HOU Hanxue, DONG Haizhou
*
(College of Food Science and Engineering, Shandong Agricultural University, Taian 271018, China)
Abstract:In order to improve the characteristics of cationic starch, the molecular structure and paste properties cationic starches prepared by semi-dry process alone and combined with microwave irradiation were comparatively evaluated in this study. The results indicated that the degradation of amylopectin in cationic starch prepared by microwave/semi-dry process was more obvious than in cationic starch prepared by semi-dry process. Electron micrographs showed no significant change in the shape of semi-dry cationic starch, except for the rough and ruptured surface of granules. However, deformation and pits were observed in the microwave/semi-dry cationic starch granules. Compared with cationic starch prepared by semidry process, cationic starch prepared by microwave/semi-dry process had higher solubility, transmittance and freeze-thaw stability, and lower peak viscosity and final viscosity.
Key words:cationic starch; microwave; molecular weight distribution; viscosity; starch properties
DOI:10.7506/spkx1002-6630-201615020
中图分类号:TS236
文献标志码:A
文章编号:1002-6630(2016)15-0118-06引文格式:
收稿日期:2016-04-14
基金项目:山东省自然科学基金项目(ZR2014CL037);山东省重点研发计划项目(2015GNC113008);泰安市科技发展计划项目(201540700)
作者简介:张慧(1980—),女,讲师,硕士,研究方向为粮油食品加工。E-mail:zhanghui@sdau.edu.cn
*通信作者:董海洲(1957—),男,教授,博士,研究方向为粮油食品加工。E-mail:hzhdong@sdau.edu.cn