表1 微波消解程序
Table 1 Conditions for microwave digestion of samples
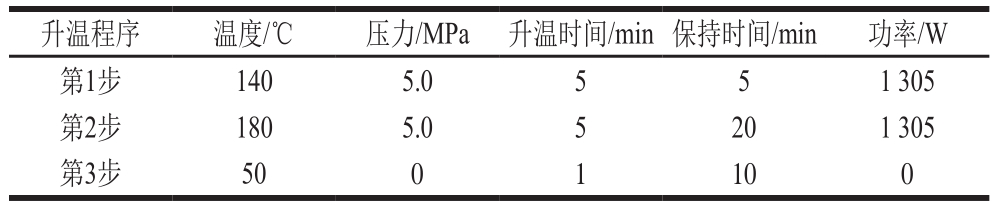
升温程序 温度/℃ 压力/MPa 升温时间/min保持时间/min 功率/W 第1步 140 5.0 5 5 1 305 第2步 180 5.0 5 20 1 305 第3步 50 0 1 10 0
孙玲玲,宋金明*,于 颖,孙 萱,温廷宇,林 强
(中国科学院海洋研究所分析测试中心,山东 青岛 266071)
摘 要:对微波消解-电感耦合等离子体发射光谱法测定牡蛎中锌含量的不确定度来源进行了分析,依据JJF 1059—1999《测量不确定度评定与表示》,量化了各不确定度分量,计算合成不确定度,最终得出测定结果的扩展不确定度。结果表明,测定结果的不确定度主要包括校准曲线拟合、测量重复性、标准溶液配制、样品称量以及样品定容体积,其相对标准不确定度分量分别为0.016、0.004 7、0.001 4、0.002 2和0.000 8。通过对不确定度分量的分析,指出校准曲线拟合是影响测定结果不确定度的主要因素,测量重复性、标准溶液配制以及样品称量和定容过程对最终结果不确定度影响亦不可忽略。测定结果的合成标准不确定度为13.29 mg/kg,扩展不确定度为26.58 mg/kg (k = 2)。因此,牡蛎中锌含量的测定结果为(781.98±26.58)mg/kg(k = 2,P = 95%)。
关键词:不确定度;锌;电感耦合等离子体发射光谱法;微波消解;牡蛎
牡蛎,俗称海蛎子或蚝,属牡蛎科(Ostreidae),牡蛎属(Ostrea)动物。牡蛎肉味鲜美,营养丰富,享有“海底牛奶”之美称 [1],是我国卫生部首批列为药食同源的保健疗效食品之一 [2]。研究表明,牡蛎不仅富含优质蛋白质、氨基酸、糖原和不饱和脂肪酸,还富含维生素及大量的活性微量元素,如铁、锌、钙、锰和硒等 [3-5],具有降血脂 [6-8]、降血糖 [9]、保肝 [10-13],提高人体免疫力 [14-16]等药理作用。值得注意的是,牡蛎中微量元素锌的含量高于一般海产品,人体每摄入10~20 g牡蛎肉就能满足我国营养协会推荐的锌日供给量 [17]。锌参与机体蛋白质与核酸代谢,对神经细胞至关重要,有助于儿童的发育,也是维持男性生殖系统健康的重要营养 [1]。因此,快速、准确地测定牡蛎中锌的含量,继而对检测结果进行正确的不确定度评定,对于提高检测结果的准确度及其合理开发利用有着极其重要的作用。
电感耦合等离子体发射光谱仪具有分析速度快、灵敏度高、准确性好、线性范围宽及多元素同时测定等优点,已成为重要的无机元素分析工具 [18],在海洋生物中微量元素的检测方面得到了广泛的应用 [19-23]。与传统消解技术相比,微波消解技术具有加热快、升温高、消解时间短、消解能力强、空白值低等优点,从而提高了样品的前处理效率,以及分析结果的准确度和精密度 [24-27]。
测量不确定度是表征合理的赋予被测量之值的分散性,是与测量结果相关联的参数,它描述了测量结果正确性的可疑程度或不肯定程度 [28-29]。测量不确定度作为衡量检测水平高低的统一尺度,在实验室质量管理和质量保证中尤为重要。本实验依据JJF 1059—1999《测量不确定度评定与表示》和《化学分析中不确定度的评估指南》的有关规定 [28-29],构建了一套相对合理、完整的评定方案,应用现代统计理论分析了微波消解-电感耦合等离子体发射光谱法测定牡蛎中锌含量的不确定度来源,对测定过程中的各不确定度分量进行评定,给出了测定结果合成标准不确定度和扩展不确定,使结果表达更加客观、真实,为正确评价和使用检测数据提供更为合理的科学依据,从而为微波消解-电感耦合等离子体发射光谱法测定微量元素的规范化操作和准确结果获取提供帮助。
1.1 材料、试剂与仪器
牡蛎样品取自大连近海。105 ℃烘干至质量恒定,将干燥好的牡蛎样品进行研磨,过40 目筛,贮藏于干燥器中备用。
HNO 3、H 2O 2(均为优级纯) 国药集团化学试剂有限公司;锌单元素标准溶液(1 000 μg/mL) 国家有色金属及电子材料分析测试中心;用于配制标准溶液与样品溶液的超纯水(电阻率18.2 MΩ·cm)。
Optima 7300 DV电感耦合等离子体发射光谱仪 美国PerkinElmer公司;SpeedWave MWS-4微波消解仪 德国Berghof公司;HG-9053A型热恒温鼓风干燥箱 上海精宏实验设备有限公司;Milli-Q Direct 8超纯水系统 美国Millipore公司;BS110电子天平 德国Sartorius公司。
1.2 方法
1.2.1 样品消解
准确称取0.055 5 g牡蛎干样于消解罐中,加入5.0 mL 浓HNO 3和1.0 mL H 2O 2,加盖预消解过夜。次日,将盛有样品的消解罐置于微波消解仪中,采用两步程序升温的微波消解程序(表1)。消解完全后,待消解罐内温度低于40 ℃时,取出,将消解液转移至高脚烧杯中,置于电热板上赶酸至近干,冷却后转移至25.00 mL容量瓶中,用超纯水洗涤高脚烧杯3~4 次,合并洗涤液,并以超纯水定容,摇匀备用。同法做试剂空白。
表1 微波消解程序
Table 1 Conditions for microwave digestion of samples

升温程序 温度/℃ 压力/MPa 升温时间/min保持时间/min 功率/W 第1步 140 5.0 5 5 1 305 第2步 180 5.0 5 20 1 305 第3步 50 0 1 10 0
1.2.2 电感耦合等离子体发射光谱仪器工作参数
等离子体气流量15.0 L/min,辅助气流量0.2 L/min,载气流量0.8 L/min,射频功率1.3 kW,溶液提升量1.5 mL/min,延迟时间20 s,积分时间5 s,观测方向轴向。1.2.3 标准曲线的绘制
将标准储备液进行逐级稀释,配制成质量浓度分别为0、1.00、2.00、3.00、4.00、5.00 mg/L的锌标准系列溶液。采用外标法,选择213.857 nm谱线对上述锌标准系列溶液重复测定3 次,用线性最小二乘法拟合校准曲线,得到回归方程为y = 73 420x+6 104.6,相关系数r = 0.999 486。
1.2.4 样品测定
在仪器选定的最佳工作条件下,对待测样品溶液中锌的含量进行10 次测量,测得结果分别为 1.704、1.718、1.709、1.713、1.712、1.746、1.774、1.752、1.751、1.777 mg/L,均值为1.736 mg/L,相对标准偏差为1.60%。
1.2.5 不确定度数学模型
根据实验原理,分析上述电感耦合等离子体发射光谱测定牡蛎中锌含量的过程,对检测结果和相关参数建立如式(1)函数关系:
式中:X为样品中锌的含量/(mg/kg);C为由工作标准曲线测得样品溶液中锌的含量/(mg/L);V为样品定容体积/mL;m为样品的质量/g。
2.1 测量不确定度来源分析
根据其数值评定方法的不同,测量结果的不确定度分量可分为A类不确定度和B类不确定度 [28-29]。A类评定是用对观测列数据进行统计分析的方法来评定标准不确定度,B类评定是用不同于对观测列数据进行统计分析的方法来评定标准不确定度 [28]。
从上述数学模型可看出,影响牡蛎中锌含量测定的不确定度分量包括:1)测定用样品溶液中锌含量的不确定度;2)样品定容体积的不确定度;3)样品称量质量的不确定度(图1)。
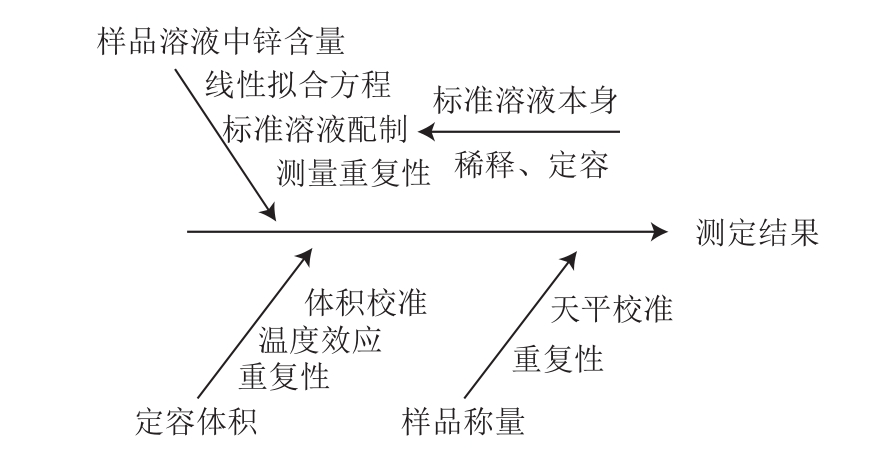
图1 不确定度来源分析
Fig. 1 Analysis of the sources of uncertainty
2.2 不确定度各分量的分析与计算
2.2.1 测量用样品溶液中锌含量的不确定度评定u(C)
测量用样品溶液中锌含量的不确定度,包括工作曲线拟合时引入的标准不确定度u(C 1)、标准溶液配制时引入的标准不确定度u(C 2)和重复性测定引入的不确定度u(C 3)有关。
2.2.1.1 锌标准溶液的质量浓度与光谱强度拟合直线方程求锌含量的不确定度评定u(C 1)(A类不确定度)
按1.2.3节方法,对锌标准系列溶液重复测定3 次,测定结果见表2。
表2 标准系列溶液测定结果
Table 2 Results for determination of standard solutions

标准溶液质量浓度/(mg/L)3 平均值0 940.9 878.4 867.9 895.7 1.00 84 433.4 88 725.6 87 589.1 86 916.0 2.00 152 366.0 153 721.7 156 327.2 154 138.3 3.00 220 484.5 224 843.1 229 444.9 224 924.2 4.00 297 996.3 299 469.7 302 539.5 300 001.8 5.00 364 832.4 373 732.2 377 197.8 371 917.5光谱发射强度1 2
用线性最小二乘法拟合校准曲线,得到回归方程为y = 73 420x+6 104.6,记为 y = ax+b,其中,a = 73 420,b = 6 104.6,相关系数 r = 0.999 486。
对样品溶液中锌含量进行10 次测定,均值为1.736 mg/L。
u(C 1)的标准不确定度由式(2)求得 [15]:
式中:s为标准曲线的剩余标准差,s=;y
i为仪器测得的各标准溶液质量浓度对应的光谱发射强度;
 i为由回归方
i为由回归方
![]() 程式y = ax+b计算出的各标准溶液质量浓度对应的光谱发射强度;a为斜率,a = 73 420;P为样品的测定次数,P = 10;N为标准系列溶液的测定次数,每个质量浓度进行3 次测量,共3×6 = 18,n = 18。
程式y = ax+b计算出的各标准溶液质量浓度对应的光谱发射强度;a为斜率,a = 73 420;P为样品的测定次数,P = 10;N为标准系列溶液的测定次数,每个质量浓度进行3 次测量,共3×6 = 18,n = 18。
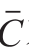 为样品溶液中锌含量的平均值,
为样品溶液中锌含量的平均值,
 = 1.736 mg/L。
= 1.736 mg/L。
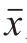 为标准系列溶液的平均质量浓度,
为标准系列溶液的平均质量浓度,
![]() 为标准系列溶液质量浓度的方差和,
为标准系列溶液质量浓度的方差和,
![]() 。
。
则工作曲线拟合引入的标准不确定度
![]() 。
。
工作曲线拟合引入的相对标准不确定度
![]() 。
。
2.2.1.2 锌标准溶液以及配制标准溶液时带来的不确定度评定u(C 2)
1)锌标准溶液的标准不确定度u(b)(B类不确定度)
锌国家标准溶液1 000 μg/mL(GSB04-1761—2 0 0 4)样品证书上注明其相对扩展不确定度为0.7%,按正态分布考虑,取置信水平为95%,包含因子k = 2,则由标准溶液本身引入的标准不确定度
![]() ,相对标准不确定度
,相对标准不确定度
![]() 。
。
2)标准溶液配制产生的不确定度u(B)
由1 000 μg/mL(即1 000 mg/L)标准溶液配制成标准系列溶液步骤如表3所示。
表3 标准系列溶液配制
Table 3 Preparation of standard solutions

浓度/(mg/L) 吸取体积/mL 定容体积/mL 所得溶液质量浓度/(mg/L)1 000 10 100 100 100 0.5 50 1.00 100 1.0 50 2.00 100 1.5 50 3.00 100 2.0 50 4.00 100 2.5 50 5.00标准溶液质量
由100 mg/L标准储备液配制成1.00、2.00、3.00、4.00、5.00 mg/L标准系列溶液带来的不确定度可忽略不计 [15]。由表3可知,从1 000 mg/L锌标准溶液配制成100 mg/L标准储备液过程中,需1 支100 mL容量瓶,1 支10.00 mL的移液管。
标准溶液配制产生的不确定度包括容量瓶、移液枪引入的不确定度。
a)容量瓶引入的不确定度u(B 1)
该项不确定度包括:①校准引入的不确定,②温度效应引入的不确定度,③定容时由体积重复性产生的不确定度。
①校准引入的不确定(B类不确定度)
根据国家标准,A级100 mL容量瓶的容量允差为±0.10 mL(20 ℃),按均匀分布考虑,包含因子
![]() ,其标准不确定度为:
,其标准不确定度为:
![]() 。
。
②温度效应引入的不确定度(B类不确定度)
该影响引起的不确定度可通过温度变化范围和体积膨胀系数来进行计算。玻璃的体积膨胀系数(9.75×10
-6℃
-1)明显小于液体的体积膨胀系数,因此可忽略。水的膨胀系数为2.1×10
-4℃
-1,实验室温度变化为±2℃,按均匀分布考虑,
![]() ,则100 mL容量瓶由温度效应产生的标准不确定度为
,则100 mL容量瓶由温度效应产生的标准不确定度为
![]() 。
。
③定容时由体积重复性产生的不确定度(A类不确定度)
通过对容量瓶的典型样品的重复性实验可以估算定容变动产生的不确定度。连续向100 mL容量瓶加纯水10 次并定容,用天平称量每次定容后的纯水质量,采用贝塞尔公式计算其实验标准偏差为0.012 mL,标准不确定度等于一倍标准偏差,即u(v 3)= 0.012 mL。
合成以上3 个不确定度分量,得100 mL容量瓶引入的标准不确定度:
100 mL容量瓶引入的相对标准不确定度:
b)移液管引入的不确定度u(B 2)
同100 mL容量瓶产生不确定度的计算相同,包括:①校准引入的不确定,②温度效应引入的不确定度,③体积重复性产生的不确定度。
①校准引入的不确定(B类不确定度)
根据国家标准,A级10.00 mL的移液管的容量允差为±0.02 mL(20 ℃),按均匀分布考虑,包含因子k=,其标准不确定度为:
![]() 。
。
②温度效应引入的不确定度(B类不确定度)
10.00 mL移液管由温度效应产生的标准不确定度为:
③体积重复性产生的不确定度(A类不确定度)
用10.00 mL移液管重复吸取纯水10.00 mL 10 次并称量其质量,得标准偏差为0.000 8 mL,即u(y 3)= 0.000 8 mL。
合成以上3 个不确定度分量,得10.00 mL 移液管引入的标准不确定度:
10.00 mL移液管引入的相对标准不确定度:
从1 000 mg/L锌标准溶液配制成100 mg/L标准储备液过程中,使用100 mL容量瓶1 次,10.00 mL移液管1 次。则标准溶液配制中由稀释因子产生的相对标准不确定度:
合成锌标准溶液以及配制标准溶液时产生的相对标准不确定度:
2.2.1.3 重复性测定引入的不确定度u(C 3)(A类不确定度)
为使测试结果可靠,一般采用重复测定的方式。对待测样品溶液中锌的含量连续进行10 次测定,结果见1.2.4节。
利用贝塞尔公式计算样品溶液中锌含量的标准偏差, 锌含量均值
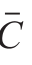 = 1.736 mg/L。
= 1.736 mg/L。
则重复性测定引入的相对标准不确定度:
![]()
2.2.1.4 测量用样品溶液中锌含量的合成不确定度u rel(C)
将以上3 项合成得出测量用样品溶液中锌含量的相对标准不确定度:
2.2.2 样品定容体积的不确定度u(V)
样品定容体积的不确定度与定容用容量瓶体积的校准不确定度u(V 1)、定容温度与校正温度不同引起的不确定度u(V 2)、容量瓶定容体积的不确定度u(V 3)有关。
2.2.2.1 样品定容用容量瓶体积校准引入的不确定度u(V 1)(B类不确定度)
根据国家标准,A级25.00 mL容量瓶的容量允差为±0.03 mL(20 ℃),属均匀分布,包含因子
![]() 。样品消解液定容用25.00 mL容量瓶1 个,该过程带来的标准不确定度为:
。样品消解液定容用25.00 mL容量瓶1 个,该过程带来的标准不确定度为:
![]() 。
。
2.2.2.2 定容温度与校正温度不同引起的不确定度u(V 2)(B类不确定度)
水的膨胀系数为2.1×1 0
-4℃
-1,实验室温度变化为±2 ℃,按均匀分布考虑,
![]() ,则25.00 mL容量瓶由温度效应产生的标准不确定度为
,则25.00 mL容量瓶由温度效应产生的标准不确定度为
![]() 。
。
2.2.2.3 容量瓶定容体积重复性的不确定度u(V 3)(A类不确定度)
连续向25.00 mL容量瓶加纯水10 次并定容,用天平称量每次定容后的纯水质量,计算其标准偏差为0.008 mL,则u(V 3)= 0.008 mL。
合成以上3 项,得样品定容体积的标准不确定度
![]() 。
。
样品定容体积的相对标准不确定度
![]() 。
。
2.2.3 样品称量质量的不确定度u(m)(B类不确定度)
天平的示值准确性受到环境温度、大气压、电源电压、电流、湿度等诸多因素影响。称量样品用十万分之一电子天平,根据天平的校准证书,天平的扩展不确定度为0.2 mg,按均匀分布,
![]() ,
,
![]() 。
。
样品称样质量为55.50 mg,其相对标准不确定度为:
![]() 。
。
2.3 合成标准不确定度的评定
根据以上分析和分步计算,各合成相对标准不确定度分量见表4。
表4 测量不确定度分量
Table 4 Components of relative standard uncertainty

不确定度分量 不确定度来源 分布 评定方式 合成相对标准不确定度标准工作曲线拟合 正态 A u(C) 标准溶液配制 均匀 B样品重复性测量 正态 A 0.017容量瓶体积校准 均匀 B温度误差 均匀 B定容体积重复性 正态 A u(m) 天平校准 均匀 B 0.002 2 u(V)0.000 8
各不确定度分量彼此独立,互不相关。合成以上各相对标准不确定度分量,得到样品中锌含量测定过程中的相对标准不确定度
![]() 。
。
牡蛎样品中锌含量为,则牡蛎样品中锌含量的标准不确定度u(X)= u rel(X)× X = 0.017×781.98 = 13.29 mg/kg。
2.4 扩展不确定度的评定
日常分析中仪器输出量的分布多为正态分布或近似正态分布,取置信水平P = 95%,扩展因子k = 2,则扩展不确定度U(X)= k×u(X)= 2×13.29 = 26.58 mg/kg。
2.5 锌含量测定结果
本实验方法测定牡蛎样品中的锌含量,称样质量为0.055 5 g,测定结果为(781.98±26.58)mg/kg,取置信水平P = 95%,扩展因子k = 2。
![]()
本实验以微波消解-电感耦合等离子体发射光谱测定牡蛎样品中锌含量为例进行了不确定度评定。通过比对各不确定度分量大小可以看出,不确定度来源主要为样品溶液中锌含量的不确定度,其次为样品称量质量产生的不确定度以及样品定容体积所引入的不确定度。
在样品溶液中锌含量的不确定度来源中,主要为标准曲线拟合产生的不确定度,其次为样品重复性测量和标准溶液配制引入的不确定度。因此,在实验中应增加标准曲线各点的测量次数,根据样品质量浓度调整标准曲线的质量浓度范围,使标准曲线的平均质量浓度接近样品的质量浓度,以减小由标准曲线产生的不确定度。重复性测量不确定度来自于测量仪器本身的性能和精度。在实际工作中,应对仪器定期进行核查、维护,使其保持最佳状态,以保证检测结果准确可靠。在标准溶液的配制过程中,应尽量减少稀释步骤,选择精度高的量器,以获得准确度高的标准品系列溶液。
参考文献:
[1] 陈惠源, 蔡俊鹏. 牡蛎的营养药用价值及其开发利用[J]. 中药材,2005, 28(3): 172-174. DOI:10.3321/j.issn:1001-4454.2005.03.004.
[2] 曾利荣, 张尔贤. 牡蛎的食用与药用价值及其开发利用[J]. 自然杂志, 1998, 20(6): 322-325.
[3] 毛文君, 李翊. 海洋功能食品的研究开发(二)[J]. 中国海洋药物,1997, 63(3): 50-53.
[4] 劳邦盛, 盛国英, 傅家谟, 等. 牡蛎中脂肪酸储藏过程中的稳定性[J].色谱, 2000, 18(4): 340-342.
[5] 汪何雅, 杨瑞金, 王璋. 牡蛎的营养成分及蛋白质的酶法水解[J]. 水产学报, 2003, 27(2): 163-168. DOI:10.3321/j.issn:1000-0615.2003.02.011.
[6] 谭乐义, 章超桦, 薛长湖, 等. 牛磺酸的生物活性及其在海洋生物中的分布[J]. 湛江海洋大学学报, 2000, 20(3): 75-79. DOI:10.3969/ j.issn.1673-9159.2000.03.017.
[7] 于娅, 杨瑞金, 王璋. 牡蛎功能短肽的制备及ACE抑制活性[J]. 无锡轻工大学学报, 2004, 23(2): 49-52.
[8] 缪元美, 张曼颖. “金牡蛎”治疗高脂血症的临床观察[J]. 中国海洋药物, 1994, 49(1): 40-41.
[9] 王世华, 于红霞, 王淑娥, 等. 牡蛎提取物对高血糖小鼠保护作用[J]. 中国公共卫生, 2006, 22(1): 80-81. DOI:10.3321/ j.issn:1001-0580.2006.01.041.
[10] 徐强, 桑希生, 梁伟. 牡蛎汤对四氯化碳所致实验性肝损伤的影响[J]. 中医药信息, 2007, 24(2): 57-58. DOI:10.3969/ j.issn.1002-2406.2007.02.024.
[11] 李旭, 苑隆国, 王晓辉. 牡蛎提取物对小鼠肝脏保护作用研究[J].医学研究通讯, 2005, 34(1): 51-52. DOI:10.3969/j.issn.1673-548X.2005.01.029.
[12] 何冬宁, 徐锡坤, 许娟华, 等. 牡蛎提取营养液对大剂量CCl4致小鼠急性肝损伤的保护作用[J]. 中国公共卫生学报, 1997, 16(3): 152-153.
[13] 范建高, 曾民德, 钟岚, 等. 牛磺酸、金牡蛎对大鼠酒精性肝损伤的防治作用[J]. 肝脏, 1999, 4(3): 154-156.
[14] 李江滨, 侯敢, 赖银璇. 牡蛎多糖抑制流感病毒增殖的实验研究[J]. 时珍国医国药, 2009, 20(6): 1346-1347. DOI:10.3969/ j.issn.1008-0805.2009.06.024.
[15] 李萌, 杜国威, 刘赛, 等. 牡蛎糖胺聚糖小鼠体内抗病毒作用的实验研究[J]. 中国海洋药物, 2008, 27(2): 50-52. DOI:10.3969/ j.issn.1002-3461.2008.02.012.
[16] 戴筱青, 陈江华, 刘玉生. 牡蛎提取物对小鼠T淋巴细胞功能的影响[J].第一军医大学报, 1997, 17(2): 149.
[17] 张红雨, 王笃圣, 王正伦. 渤海湾密鳞牡蛎营养成分分析[J]. 中国海洋药物, 1994, 52(4): 17-19.
[18] 辛仁轩. 等离子体发射光谱分析[M]. 北京: 化学工业出版社, 2005: 11-46.
[19] SHEPPARD B S, HEITKEMPER D T, GASTON C M. Microwave digestion for the determination of arsenic, cadmium and lead in seafood products by inductively coupled plasma atomic emission and mass spectrometry[J]. Analyst, 1994, 119(8): 1683-1686.
DOI:10.1039/an9941901683.
[20] 赵艳芳, 宁劲松, 尚德荣, 等. 牡蛎、缢蛏和菲律宾蛤仔中微量元素的分析研究[J]. 广东微量元素科学, 2009, 16(9): 50-54.
DOI:10.3969/j.issn.1006-446X.2009.09.010.
[21] SUN D H, WATERS J K, MAWHINNEY T P. Microwave digestion with HNO 3-H 2O 2-HF for the determination of total aluminum in seafood and meat by inductively coupled plasma atomic emission spectrometry[J]. Journal of Agricultural and Food Chemistry, 1997,45(6): 2115-2119. DOI:10.1021/jf960811f.
[22] 余焘. 微波消解 ICP-OES 法测定牡蛎中16 种无机元素含量[J]. 广西农业科学, 2010, 41(9): 991-993.
[23] 王莹, 康万利, 辛士刚, 等. 鲍鱼、海参中微量元素的分析研究[J].光谱学与光谱分析, 2009, 29(2): 511-514. DOI:10.3964/j.is sn.1000-0593(2009)02-0511-04.
[24] DOLAN S P, CAPAR S G. Multi-element analysis of food by microwave digestion and inductively coupled plasma-atomic emission spectrometry[J]. Journal of Food Composition and Analysis, 2002,15(5): 593-615. DOI:10.1006/jfca.2002.1064.
[25] KUSS H M. Applications of microwave digestion technique for elemental analyses[J]. Fresenius Journalof Analytical Chemistry, 1992,343(9/10): 788-793. DOI:10.1007/BF00633568.
[26] 张磊, 王晓艳, 李波. 微波消解技术在金属分析中的应用[J]. 光谱实验室, 2010, 27(3): 953-957. DOI:10.3969/j.issn.1004-8138.2010.03.034.
[27] 周勇义, 谷学新, 范国强, 等. 微波消解技术及其在分析化学中的应用[J].冶金分析, 2004, 24(2): 30-36. DOI:10.3969/ j.issn.1000-7571.2004.02.009.
[28] 国家质量技术监督局. JJF1059—1999 测量不确定度评定与表示[S].北京: 中国计量出版社, 1999.
[29] 中国实验室国家认可委员会. 化学分析中不确定度的评估指南[M].北京: 中国计量出版社, 2002.
Evaluation of Uncertainty for Zinc Determination in Oyster by Microwave Digestion-ICP-OES
SUN Lingling, SONG Jinming*, YU Ying, SUN Xuan, WEN Tingyu, LIN Qiang
(Analytical Center of Institute of Oceanology, Chinese Academy of Sciences, Qingdao 266071, China)
Abstract:The sources of uncertainty were analyzed for the determination of zinc in oyster by microwave digestioninductively coupled plasma optical emission spectrometry (ICP-OES). According to JJF 1059—1999, the sub-uncertainty was calculated and used to obtain combined uncertainty and expanded uncertainty of the measurement results. The results showed that the uncertainty was mainly derived from fitting to the standard curve, and repeated experiments of samples,preparation of the standard solution, and sample weighing and volume had a nonneligible effect on it with relative standard uncertainty values of 0.016, 0.004 7, 0.001 4, 0.002 2 and 0.000 8, respectively. In this study, the combined standard uncertainty of the measurement results was 13.29 mg/kg, and the expanded uncertainty was 26.58 mg/kg (k = 2). The final result of zinc content in oyster was (781.98 ± 26.58) mg/kg (k = 2, P = 95%).
Key words:uncertainty; zinc; ICP-OES; microwave digestion; oyster
DOI:10.7506/spkx1002-6630-201616030
中图分类号:O657.31
文献标志码:A
文章编号:1002-6630(2016)16-0187-06
引文格式:
孙玲玲, 宋金明, 于颖, 等. 微波消解-电感耦合等离子体发射光谱法测定牡蛎中锌的不确定度评定[J]. 食品科学, 2016,
37(16): 187-192. DOI:10.7506/spkx1002-6630-201616030. http://www.spkx.net.cn
SUN Lingling, SONG Jinming, YU Ying, et al. Evaluation of uncertainty for zinc determination in oyster by microwave digestion-ICP-OES[J]. Food Science, 2016, 37(16): 187-192. (in Chinese with English abstract) DOI:10.7506/spkx1002-6630-201616030. http://www.spkx.net.cn
收稿日期:2015-11-04
作者简介:孙玲玲(1982—),女,工程师,博士,研究方向为海洋环境分析。E-mail:sunll@qdio.ac.cn
*通信作者:宋金明(1964—),男,研究员,博士,研究方向为海洋生物地球化学和应用海洋化学。E-mail:jmsong@qdio.ac.cn