表1 梯度洗脱条件
Table1 Gradient elution conditions

时间/min流动相体积分数/% A乙腈B 0.02 mol/L乙酸铵溶液0 1090 1.01090 6.02872 12.03565 20.04555 24.04555 28.07525 32.07525 32.11090 39.01090
林 芳,李 涛*,王一欣,张 丽,刘海静
(陕西省食品药品检验所,陕西 西安 710065)
摘 要:建立超高效液相色谱法,同时测定降糖类保健食品中可能非法添加的13 种化学药物(盐酸二甲双胍、盐酸丁二胍、盐酸苯乙双胍、甲苯磺丁脲、格列吡嗪、格列齐特、格列波脲、盐酸罗格列酮、格列本脲、盐酸吡格列酮、格列美脲、瑞格列奈、格列喹酮)。样品采用甲醇提取,经ZORBAX SB-C 18色谱柱分离,乙腈和0.02 mol/L乙酸铵为流动相梯度洗脱,流速0.2 mL/min。采用二极管阵列检测器,采集波长235 nm处的色谱图进行初筛和定量。并通过与13 种降糖药物标准品的光谱比对进行确证。结果表明,13 种降糖药物在30 min内可有效分离,在0.3~90 μg/mL的线性范围内相关系数均大于0.999,平均回收率为83.2%~108.9%,相对标准偏差均不大于5.5%,检出限为0.2~0.6 ng。该方法前处理简单、分析时间相对较短、灵敏度高且重复性好,实现一个系统对13 种降糖药物的同时检测,可作为降糖类保健食品检测非法添加化学成分的参考方法。
关键词:保健食品;降糖类药物;非法添加;超高效液相色谱法
近年来,随着经济发展、生活水平的提高与生活节奏的加快,越来越多的人受到糖尿病、高血压等慢性病的困扰。保健食品作为一种新兴的功能性食品,常宣称含有天然、有机、中草药成分,具备辅助调节血糖、辅助降血压等功能,是具有一种功效或宣称功能的食品 [1-2]。同时,通过一些不良媒体宣传 [3],保健食品常被人们误认为可替代药物,快速治疗疾病且安全无副作用等。这种观念,被不良商家利用,在保健品中非法加入化学药物,以增强疗效、谋取暴利 [4]。很多添加的化学药物如果长期使用不当,将对人体造成极大的危害 [5-7]。2012年12月14日,国家食品药品监督管理局发布了《保健食品中可能非法添加的物质名单(第一批)》 [8],列出声称辅助降血糖(调节血糖)功能产品的中可能添加甲苯磺丁脲、格列苯脲、格列齐特等11 种降糖药物,同时公布了检验依据 [9],2014—2015年国家保健食品抽检监测工作要求对包括上述11 种降糖药物在内的共13 种降糖药物开展非法添加筛查,并增加了3 个推荐的依据 [10-12]。所有的检验依据需要4 个液相系统完成对13 种降糖药物的筛查,每个样品的仪器检测时间超过3 h,前处理还有所差异,检测周期较长,工作量及对试剂耗材的消耗均较大。若是能够简化检测方法,快速有效的完成对目标物的检测,将对检验工作的开展,加强市场监管及保障人民群众健康起到积极作用。
与传统的高效液相色谱相比 [13-15],超高效液相色谱具有更快的分离速率、更高的分辨率和灵敏度,可适用于复杂基质中药物的分离、分析 [16-21]。本实验利用超高效液相色谱的高分辨率和高灵敏度等特性,建立了一个液相系统同时较快速地检测盐酸二甲双胍、盐酸丁二胍、盐酸苯乙双胍、甲苯磺丁脲、格列吡嗪、格列齐特、格列波脲、盐酸罗格列酮、格列本脲、盐酸吡格列酮、格列美脲、瑞格列奈、格列喹酮共13 种降糖药物的方法。该方法结合二极管阵列检测器的光谱特征分析,可在一次运行中同时完成样品快速筛查、光谱确证和定量分析,线性关系、回收率、分离度均良好,检测简便、较国标推荐方法节约大量检测时间、灵敏度高且重复性好。该方法检测目标物覆盖了国家保健食品抽检监测工作降糖类保健食品要求筛查的所有药物种类,可作为降糖类保健食品检测非法添加化学成分的参考方法。
1.1 材料与试剂
检测样品为2015年陕西省国抽、省抽工作中从全省11 个市(区)抽取到的声称具有辅助降血糖功能的保健食品,共计30余批。
空白样品:本实验所用的空白样品为历次抽检中有代表性的固体、液体样品,辅料成分为硬脂酸镁、乳糖、预胶化淀粉、甜味剂、防腐剂等,经检测不含13 种降糖药物。
甲醇、乙腈(均为色谱纯) 德国Meker公司;乙酸铵(纯度≥99.0%) 美国Fluka公司;实验用水均为超纯水。
标准品:盐酸二甲双胍(含量100%,CAS号:1115-70-4)、盐酸苯乙双胍(含量99.7%,CAS号:834-28-6)、格列吡嗪(含量99.5%,CAS号:29094-61-9)、格列齐特(含量99.9%,CAS号:21187-98-4)、格列波脲(含量99.9%,CAS号:26944-48-9)、盐酸罗格列酮(含量91.3%,CAS号:302543-62-0)、格列本脲(含量99.9%,CAS号:10238-21-8)、盐酸吡格列酮(含量100%,CAS号:112529-15-4)、格列美脲(含量99.1%,CAS号:93479-97-1)、瑞格列奈(含量99.8%,CAS号:135062-02-1)、格列喹酮(含量99.5%,CAS号:33342-05-1) 中国食品药品检定研究院;盐酸丁二胍(含量100%,CAS号:1190-53-0)加拿大TRC公司;甲苯磺丁脲(含量99.0%,CAS号:64-77-7) 美国Fluka公司。
1.2 仪器与设备
1290 Infinity超高效液相色谱仪(配有1290二极管阵列检测器) 美国Agilent公司;8040液相色谱-质谱联用仪 日本岛津公司;AE-240双量程电子天平瑞士Mettlor Toledo公司;AS20500B超声波清洗器天津奥特赛恩斯仪器有限公司;Synergy型超纯水仪美国Millipore公司;数显恒温水浴 江苏省金华市荣华仪器制造有限公司。
1.3 方法
1.3.1 色谱及光谱条件
色谱柱:ZORBAX SB-C 18(150 mm×2.1 mm,1.8 μm);柱温35 ℃;流速0.2 mL/min;进样量2 μL;流动相A:乙腈,流动相B:0.02 mol/L乙酸铵溶液;梯度洗脱;检测波长235 nm。
光谱条件:光谱范围190~400 nm;光谱采集模式:全扫描。
1.3.2 标准品溶液的配制
准确称取13 种标准品各10~20 mg,分别置于10 mL容量瓶中,用甲醇定容至刻度,得单标储备液,质量浓度约为1 mg/mL。再从各单标储备液中准确移取0.5~1.5 mL,置于同一25 mL容量瓶中,用甲醇定容至刻度,得混合标准储备液。再由混合标准储备液梯度稀释成标准曲线各点,得13 种降糖类化学药物的系列混合标准曲线溶液,质量浓度为0.3~90 μg/mL。
1.3.3 样品前处理
样品前处理方法参考相关文献[14,22-24]、国家食品药品监督管理局批件2009029 [9]、2013001 [11]。固体样品:取样品5 次口服剂量(片剂除去包衣,胶囊剂取内容物),研细。精密称取相当于1 次口服剂量样品,置50 mL容量瓶中,加甲醇适量,超声处理20 min,冷却,加甲醇定容至刻度,摇匀,经0.22 μm滤膜过滤,取滤液作为供试品溶液。液体样品:准确移取相当于一次口服剂量的溶液,60 ℃旋蒸至近干,转移置50 mL容量瓶中,用甲醇定容至刻度,摇匀,经0.22 μm滤膜过滤,取滤液作为供试品溶液。同批样品均做2 份平行样,供试品溶液若检出药物含量过高,可根据具体情况再进行稀释。
1.3.4 回收率和精密度测定
分别选取固体(胶囊剂内容物)和液体(口服液)基质的空白样品。加入适量的混合标准工作液,使加标质量浓度达到方法检出限、4 倍定量限、20 倍定量限3 个添加水平。按1.3.3节方法进行处理,每种基质的每个添加水平平行做3 份样,每个样品重复测定2 次,计算样品的回收率。
取混合标准品溶液重复进样6 次,测定各个标准品的峰面积,按色谱条件以峰面积的相对标准偏差(relative standard deviation,RSD)表示精密度。
1.3.5 方法的稳定性及重复性测定
取混合标准曲线溶液分别在0、12、24、48、72 h进样,计算13 种降糖药物峰面积的RSD。同时,选取检出的阳性样品,按1.3.3节方法处理,分别在0、12、24、48、72 h相同条件进样,计算检出样品对应药物含量的RSD,考察方法的稳定性。
取同批次阳性样品6 份,按1.3.3节方法平行处理,得到供试品溶液并测定。以检出药物含量的RSD考察方法的重复性。
1.3.6 光谱确证分析
同时采集标准品和样品在波长190~400 nm处光谱,根据13 种降糖药物的特征吸收光谱建立光谱库,当检测到样品有与标准品保留时间一致的色谱峰时,即与该标准对照药物进行光谱匹配度检索,匹配度达90%以上且峰纯度较高(大于90%)时,可判断该类保健食品中添加了某种降糖药物(必要时可用质谱进行确证),同时可计算出该类药物的添加量。
1.3.7 方法的验证
为了验证本方法的可靠性,选取一份检测阳性样品,进行质谱确证。
液相及质谱条件 [9,22,25-26]:液相条件:流动相,甲醇、0.02 mol/L乙酸铵溶液,流速0.2 mL/min;质谱条件:电喷雾离子源;正离子模式;多反应监测模式;电离电压3.0 kV;锥孔电压25 V;源温度120 ℃;脱溶剂气温度250 ℃;碰撞气体(氩气):压力230 kPa;干燥气流速15 L/min;雾化气流速3 L/h。
2.1 色谱条件的优化
表1 梯度洗脱条件
Table1 Gradient elution conditions

时间/min流动相体积分数/% A乙腈B 0.02 mol/L乙酸铵溶液0 1090 1.01090 6.02872 12.03565 20.04555 24.04555 28.07525 32.07525 32.11090 39.01090
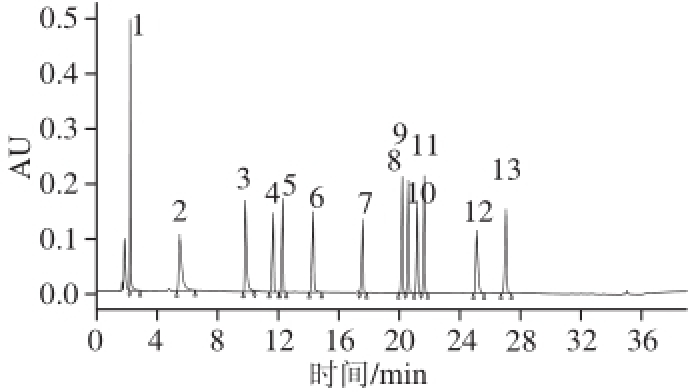
图1 13 种降糖药物混合标准溶液色谱图(20~60 μg/mL)
Fig.1 Chromatograms of mixed standard solution of 13 anti-diabetic drugs (20-60 μg/mL
1.盐酸二甲双胍(38 μg/mL);2.盐酸丁二胍(25 μg/mL);3.盐酸苯乙双胍(26 μg/mL);4.甲苯磺丁脲(40 μg/mL);5.格列吡嗪(40 μg/mL);6.格列齐特(50 μg/mL);7.格列波脲(20 μg/mL);8.盐酸罗格列酮(36 μg/mL);9.格列本脲(38 μg/mL);10.盐酸吡格列酮(42 μg/mL);11.格列美脲(35 μg/mL);12.瑞格列奈(60 μg/mL);13.格列喹酮(40 μg/mL)。
以ZORBAX SB-C 18色谱柱(2.1 mm×150 mm,1.8 μm)作为分析柱。以流动相A:乙腈,流动相B:0.02 mol/L乙酸铵溶液作为流动相 [22],梯度洗脱,调整流动相比例,优化洗脱条件。优化后的洗脱条件见表1,可使13 种降糖药物保持足够的分离度和良好的峰形,经相同色谱条件下的标准品单标溶液定位,可确定13 种降糖药物的出峰顺序和保留时间。同时在波长235 nm处,检测信号灵敏度较高,分离效果满足检测需要,此条件下所有降糖药物在30 min前出峰。13 种降糖药物混合标准溶液的色谱图见图1。
2.2 线性关系、定量限和检出限
将1.3.2节得到的13 种降糖药物的系列混合标曲溶液,按2.1节色谱条件进行检测,以对应的色谱图峰面积为纵坐标(y),质量浓度为横坐标(x,μg/mL)进行回归分析。如表2所示,13 种降糖药物在该范围内呈良好的线性关系,线性相关系数(r 2)均大于0.999,说明本方法适用于保健食品中非法添加的13 种降糖类药物的定量分析。
在本实验条件下,在空白样品中分别加入一定量的混合标准溶液,按供试品的处理方法同法处理,连续稀释至3 倍信噪比,作为本方法的检出限。检出限结合本方法进样体积(2 μL),得到本方法的检出限。本方法检出限为0.2~0.6 ng。连续稀释至10 倍信噪比作为本方法的定量限。定量限结合本方法进样体积(2 μL),得到本方法的定量限,本方法定量限为0.6~1.8 ng。
表2 13 种降糖药物的线性方程、相关系数、线性范围、定量限、检出限
Table2 Calibration curves, correlation coefficients (r
2), linear ranges,limits of quantification (LOQs), limits of detection (LODs) for 13 anti-diabetic drugs
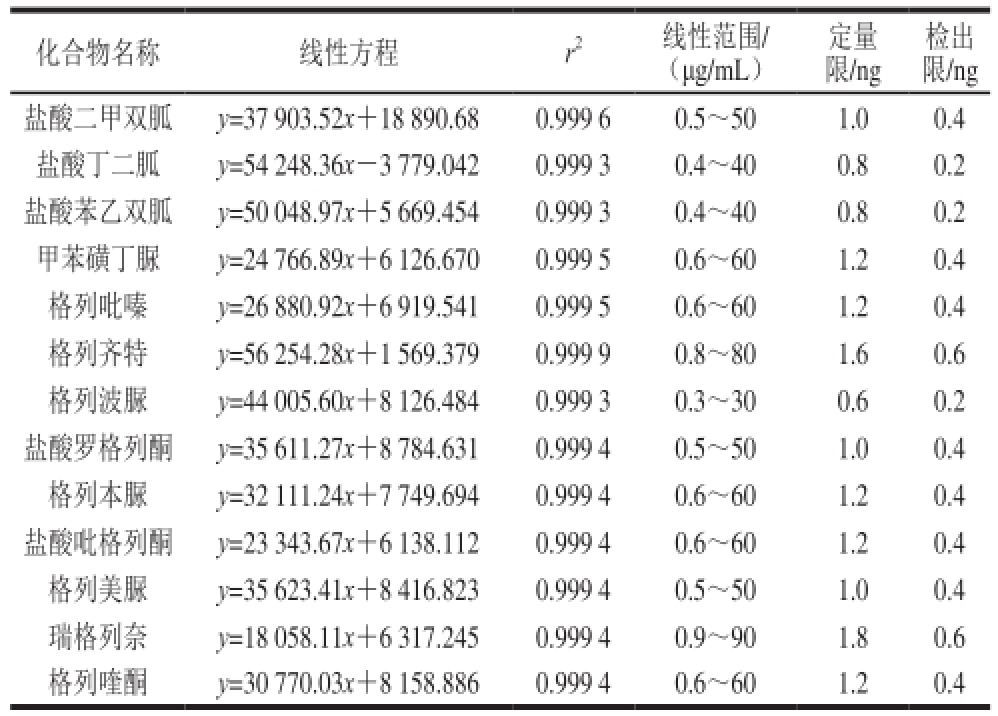
检出限/ng盐酸二甲双胍y=37 903.52x+18 890.680.999 60.5~501.00.4盐酸丁二胍y=54 248.36x-3 779.0420.999 30.4~400.80.2盐酸苯乙双胍y=50 048.97x+5 669.4540.999 30.4~400.80.2甲苯磺丁脲y=24 766.89x+6 126.6700.999 50.6~601.20.4格列吡嗪y=26 880.92x+6 919.5410.999 50.6~601.20.4格列齐特y=56 254.28x+1 569.3790.999 90.8~801.60.6格列波脲y=44 005.60x+8 126.4840.999 30.3~300.60.2盐酸罗格列酮y=35 611.27x+8 784.6310.999 40.5~501.00.4格列本脲y=32 111.24x+7 749.6940.999 40.6~601.20.4盐酸吡格列酮y=23 343.67x+6 138.1120.999 40.6~601.20.4格列美脲y=35 623.41x+8 416.8230.999 40.5~501.00.4瑞格列奈y=18 058.11x+6 317.2450.999 40.9~901.80.6格列喹酮y=30 770.03x+8 158.8860.999 40.6~601.20.4化合物名称线性方程r 2线性范围/(μg/mL)定量限/ng
2.3 回收率和精密度结果
如表3所示,按1.3.4节方法,13 种降糖药物的3 个添加水平在固体基质中回收率为86.1%~108.8%;液体基质中回收率为83.2%~108.9%,RSD不大于5.5%。
表3 13 种降糖药物不同基质保健食品中的加标回收率和精密度(n=6)
Table3 Recoveries and RSDs for 13 anti-diabetic drugs spiked in different health food matrices (n= 6)

化合物名称加标质量浓度/(μg/mL)固体基质液体基质回收率/%RSD/%回收率/%RSD/%盐酸二甲双胍0.2108.73.8104.53.2 2 95.52.7101.43.3 1099.82.198.63.0盐酸丁二胍0.186.15.083.25.2 1.6101.43.689.44.1 8 103.74.094.83.7盐酸苯乙双胍0.196.72.589.74.5 1.699.11.392.52.9 8 97.21.994.92.1甲苯磺丁脲0.290.23.785.35.5 2.492.03.590.64.3 1296.22.095.32.5格列吡嗪0.289.33.789.64.5 2.492.62.093.73.8 1298.81.696.32.7格列齐特0.3106.54.8108.95.5 3.2102.21.6104.32.5 1699.61.5101.12.1格列波脲0.187.05.987.85.4 1.294.12.992.34.2 6 97.71.996.52.3盐酸罗格列酮0.299.91.697.14.2 2 101.81.499.23.8 10100.62.498.52.2格列本脲0.2101.61.0103.02.8 2.4102.44.0101.72.8 12100.40.999.53.7盐酸吡格列酮0.296.01.893.92.8 2.4101.71.396.92.0 12100.51.997.11.8格列美脲0.299.72.696.23.9 2 101.20.997.92.4 10100.41.399.31.6瑞格列奈0.3108.81.4107.23.3 3.6104.02.6102.22.5 18101.71.798.32.1格列喹酮0.292.94.690.95.0 2.493.14.191.95.4 12101.53.096.82.6
2.4 精密度实验结果
按1.3.4节方法,盐酸二甲双胍、盐酸丁二胍、盐酸苯乙双胍、甲苯磺丁脲、格列吡嗪、格列齐特、格列波脲、盐酸罗格列酮、格列本脲、盐酸吡格列酮、格列美脲、瑞格列奈和格列喹酮平均峰面积的RSD分别为3.5%、3.8%、2.0%、3.2%、2.0%、3.5%、1.8%、2.3%、2.0%、3.0%、1.5%、2.5%、4.0%,表明仪器精密度良好。
2.5 方法的稳定性及重复性实验结果
按1.3.5节方法,计算13 种降糖药物混合标准曲线溶液在不同检测时间点峰面积的RSD在0.87%~4.82%之间。同时选取阳性样品,对应药物含量在不同检测时间点的RSD在1.02%~4.63%之间,说明标准品和样品在72 h内的稳定性良好。
按1.3.5节中的方法,同批次6 份阳性样品检出降糖药物含量的RSD为1.97%~4.77%,说明本方法重复性良好。2.6 实际样品检测与光谱确证分析
13 种降糖药物于波长190~400 nm处的特征吸收光谱如图2所示。某厂家样品胶囊按照1.3.3节方法前处理,2.1节色谱及光谱条件检测,如图3所示,峰1与盐酸罗格列酮保留时间一致,且光谱特征一致;峰2与盐酸比格列酮保留时间一致,且光谱特征一致,峰1与峰2光谱图见图3A、B,证实样品含有盐酸罗格列酮和盐酸比格列酮。



图2 13种降糖药物的特征吸收光谱图
Fig. 2 Characteristic absorption spectra of 13 anti-diabetic drugs
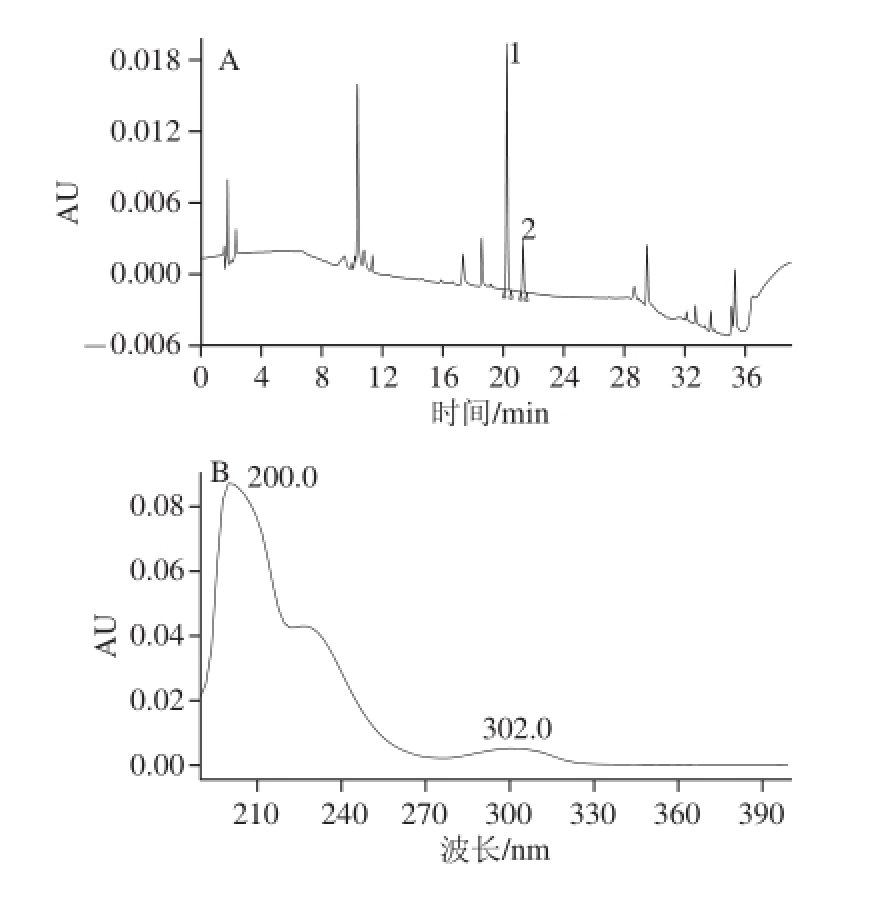

图3 阳性样品色谱图(A)、峰1(B)与峰2(C)的光谱图
Fig.3 Chromatogram of positive sample (A), and absorption spectra of peak 1 (B) and peak 2 (C)
2.7 质谱验证结果
表4 2 种非法添加化学物的质谱检测参数
Table4 Mass spectral parameters of 2 illegally added components

注:*.定量离子。
化合物名称扫描方式母离子子离子第一四极杆滤质器偏转电压/V碰撞电压/V第三四极杆滤质器偏转电压/V吡格列酮正离子模式357.00134.00*-17.0-29.0-25.0 119.05-17.0-40.0-23.0列酮正离子模式358.00135.00*-17.0-26.0-25.0 119.00-17.0-40.0-23.0罗格
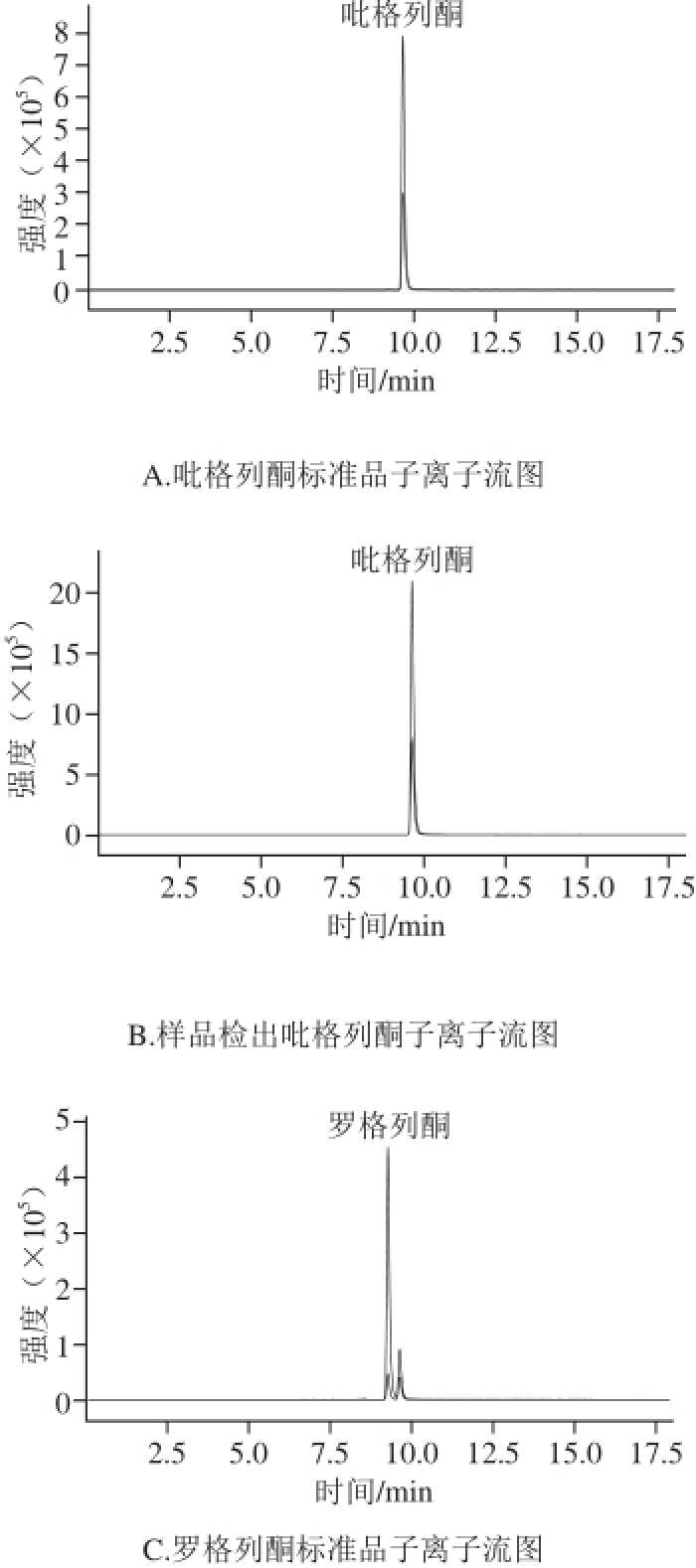

图4 阳性样品与标准品多反应监测模式图谱
Fig.4 MRM chromatograms of positive samples and standards
按1.3.7节方法,采用液相色谱-质谱联用方法验证本方法的可靠性,选取2.5节中阳性样品,检出2 种物质的离子信息如表4所示,样品中母离子和2对子离子均有检出,离子丰度比符合要求,再次确认检出物为罗格列酮与吡格列酮,如图4所示。
本研究建立了超高效液色谱结合二极管阵列检测器,同时测定降糖类保健食品中非法添加的13 种化学药物的方法。该方法将国标推荐的多液相系统检测方法简化为一个系统同时实现目标物的快速筛查、光谱确证和定量分析,大大节约检测时间与成本。该方法精密度和稳定性良好,灵敏度高,分离度满足要求,可作为降糖类保健食品检测非法添加化学成分的参考方法。
参考文献:
[1] 国家食品药品监督管理局. 保健食品注册管理办法(试行)[S].
[2] 国家卫生和计划生育委员会. GB 16740—2014 保健食品[S]. 北京:中国标准出版社, 2014.
[3] 宋迪. 保健食品消费行为和认知情况及存在问题的调查分析吉林大学[D]. 长春: 吉林大学, 2014.
[4] 黄海燕, 饶伟文, 钟建理. 降糖类中成药和保健食品中非法添加化学药品的研究概况[J]. 中国药业, 2014, 23(5): 94-96.
[5] 陈新谦, 金有豫. 新编药物学[M]. 17版. 北京: 人民卫生出版社,2011: 622.
[6] 董永成, 杜士明, 陈永顺, 等. 中成药及保健品非法添加化学成危害及对策[J]. 时珍国医国药, 2006, 17(8): 1601-1602.
[7] 颜杰, 刘志强, 程振田. 中成药及中药保健食品中非法添加化学药品现状与对策[J]. 中国药学杂志, 2007, 42(9): 716-718. DOI:10.3321/j.issn:1001-2494.2007.09.023.
[8] 国家食品药品监督管理局. 保健食品中可能非法添加的物质名单:第一批[EB/OL]. (2012-12-14)[2013-4-25]. http://www.sda.gov.cn/ WS01/CL1162/76614.html.
[9] 国家食品药品监督管理局. 药品检验补充检验方法和检验项目批准件2009029降糖类中成药中非法添加化学药品补充检验方法[S].
[10] 国家食品药品监督管理局. 药品检验补充检验方法和检验项目批准件2011008降糖类中成药中非法添加盐酸丁二胍补充检验方法[S].
[11] 国家食品药品监督管理局. 药品检验补充检验方法和检验项目批准件2013001降糖类中成药和辅助降血糖类保健食品中非法添加格列波脲的补充检验方法[S].
[12] 国家质量监督检验检疫总局. SN/T 3864—2014 出口保健食品中二甲双胍、苯乙双胍的测定[S].
[13] 隋海山, 王立娟, 谢菲. 高效液相色谱-二极管阵列检测器法测定保健食品和中成药中违法添加的10 种降糖类西药[J]. 中国药业,2015, 24(22): 110-112.
[14] 吴公平, 雷玉萍, 李荣玮, 等. 采用反相高效液相色谱法测定降糖类保健食品非法添加降糖化学药品检验方法的研究[J]. 中国现代医学杂志, 2010, 20(9): 1380-1382.
[15] JING Y, SHI Y Q, LI Z R, et al. Development of a RP-HPLC method for screening potentially counterfeit anti-diabetic drugs[J]. Journal of Chromatography B, 2007, 853(1/2): 254-259. DOI:10.1016/ j.jchromb.2007.03.022.
[16] 刘颖, 周建良, 李萍. 快速高效液相色谱分离技术在中药分析中的应用[J]. 色谱, 2009, 27(5): 682-689. DOI:10.3321/ j.issn:1000-8713.2009.05.021.
[17] 郝桂明, 唐素芳. 超高效液相色谱在药物分析中的应用[J]. 天津药学, 2009, 21(6): 64-69. DOI:10.3969/j.issn.1006-5687.2009.06.031.
[18] 赵明霞, 胡基埂, 吴方千, 等. 超高压液相色谱系统的研究进展[J].分析试验室, 2009, 28(b12): 137-140.
[19] 杜彦山, 李强, 吴春敏, 等. 超高效液相色谱-四极杆/静电场轨道阱高分辨质谱快速筛查及定量分析保健品中11 种非法添加降糖药物[J].色谱, 2015, 33(4): 371-376. DOI:10.3724/SP.J.1123.2014.11020.
[20] 曹进, 黄湘鹭, 张庆生, 等. 食品和保健食品中非法添加药物筛查策略的建立[J]. 食品科学, 2014, 35(19): 302-306. DOI:10.7506/ spkx1002-6630-201419060.
[21] 张晓光, 李强, 孙磊, 等. 超高效液相色谱-静电场轨道阱高分辨质谱快速筛查保健品中23 种非法添加西药成分[J]. 食品科学, 2015,36(14): 187-191. DOI:10.7506/spkx1002-6630-201514036.
[22] 朱峰, 阮丽萍, 马永建, 等. 超高效液相色谱-串联质谱联用法同时检测降糖类和减肥类保健品中20 种非法添加的化学降糖药物[J]. 色谱, 2014, 32(1): 13-20. DOI:10.3724/SP.J.1123.2013.08035.
[23] 黄湘鹭, 王静文, 曹进, 等. 降血糖类保健食品中非法添加的8 种药物检测及实例分析[J]. 食品科学, 2014, 35(10): 149-152. DOI:10.7506/spkx1002-6630-201410027.
[24] 余小平, 王也, 周静安, 等. 快速筛查检验保健食品及中成药中的12种化学降糖药[J]. 药物分析杂志, 2013, 33(6): 1003-1006.
[25] 曹梅荣, 李强, 张冬生. 超高效液相色谱-串联质谱法快速检测降糖类保健食品中的10 种非法添加物[J]. 分析试验室, 2015, 34(8): 896-901.
[26] 欧贝丽, 张红伟, 徐宏祥. UPLC-MS/MS法测定中成药及保健品中添加的36 种化学药物[J]. 药物分析杂志, 2013, 33(12): 2141-2147.
Simultaneous Determination of 13 Illegally Added Chemical Drugs in Hypoglycemic Health Foods by Ultra Performance Liquid Chromatography
LIN Fang, LI Tao*, WANG Yixin, ZHANG Li, LIU Haijing
(Shaanxi Institute for Food and Drug Control, Xi’an 710065, China)
Abstract:An ultra performance liquid chromatography (UPLC) method was developed for the simultaneous determination of 13 illegally added chemical drugs (metformin hydrochloride,buformin hydrochloride, phenformin hydrochloride,tolbutamide, glipizide, gliclazide, glibornuride, rosiglitazone hydrochloride, glibenclamide, pioglitazone hydrochloride,glimepiride, repaglinide and gliquidone) in hypoglycemic health foods. Samples were extracted by using methanol. ZORBAX SB-C 18column was applied with a mobile phase consisting of acetonitrile and 0.02 mol/L ammonium acetate by gradient elution at a flow rate of 0.2 mL/min. The illegally added chemical drugs were detected by a photodiode array detector and a chromatogram with detection wavelength of 235 nm was used for screening and quantification. The results were then confirmed by comparison with the spectra of 13 reference substances. It was shown that the 13 anti-diabetic agents could be effectively separated within 30 min. The correlation coefficients were all above 0.999 over the concentration range of 0.3-90 μg/mL. The average recoveries ranged from 83.2% to 108.9% with relative stand deviations (RSDs) all below 5.5%. The limits of detection (LODs) were all in the range of 0.2 to 0.6 ng. This method has the advantages of simple pre-treatment, fast detection, satisfactory recovery rate and good reproducibility, and it is suitable for the simultaneous determination of the 13 anti-diabetic agents and can be used as a reference in the detection of the illegally added chemical drugs in hypoglycemic health foods.
Key words:health foods; anti-diabetic drugs; illegally added; ultra performance liquid chromatography
DOI:10.7506/spkx1002-6630-201618029
中图分类号:O657.72
文献标志码:A
文章编号:1002-6630(2016)18-0178-07
引文格式:
林芳, 李涛, 王一欣, 等. 超高效液相色谱法同时测定降糖类保健食品中非法添加的13 种化学药物[J]. 食品科学, 2016,37(18): 178-184. DOI:10.7506/spkx1002-6630-201618029. http://www.spkx.net.cn
LIN Fang, LI Tao, WANG Yixin, et al. Simultaneous determination of 13 illegally added chemical drugs in hypoglycemic health foods by ultra performance liquid chromatography[J]. Food Science, 2016, 37(18): 178-184. (in Chinese with English abstract) DOI:10.7506/spkx1002-6630-201618029. http://www.spkx.net.cn
收稿日期:2016-03-14
基金项目:陕西省科技统筹创新工程项目(2014FWPT-01)
作者简介:林芳(1982—),女,主管药师,硕士,研究方向为食品、保健食品理化检验及安全性检测。E-mail:fanqiehuayuan@126.com
*通信作者:李涛(1978—),男,副主任药师,学士,研究方向为食品及保健食品检验。E-mail:westyx@126.com