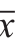 ±s表示。实验重复3 次,取其平均值。
±s表示。实验重复3 次,取其平均值。刘建华,陈新华,丁玉庭*
(浙江工业大学海洋学院,浙江 杭州 310014)
摘 要:为研究高温水煮和酸煮对猪骨硬度及化学成分的影响。以猪骨为实验对象,研究120 ℃条件下猪骨在水中煮制不同时间(40、50、60、70、80 min)和不同体积分数(0.0%、0.2%、0.4%、0.6%、0.8%、1.0%)的醋酸溶液中煮制80 min后猪骨硬度的变化。用凯氏定氮法和电感耦合等离子体原子发射光谱法测定未煮制猪骨、120 ℃条件下水中和1.0%醋酸溶液中煮制80 min后猪骨蛋白含量、钙、磷元素含量和钙、磷元素溶出量,用扫描电子显微镜观察猪骨粉碎后微观结构,测定猪骨红外吸收光谱,探究煮制后猪骨成分和结构的变化。结果表明,高温煮制能使猪骨硬度下降,水煮时间从40 min延长到80 min,猪骨硬度从(16 445±867) g下降到(10 995±546) g,醋酸溶液体积分数从0.0%增加到1.0%,猪骨硬度从(10 995±546) g下降到(6 003±153) g。高温煮制能使猪骨蛋白含量降低,猪骨表观钙、磷含量增加,钙、磷溶出量增加。水煮后猪骨蛋白含量为(28.5±2.3) g/100 g,降低了7.4%;猪骨表观钙、磷元素含量分别为(210.0±8.2) mg/g和(96.0±4.0) mg/g,分别增加了11.8%和8.9%;猪骨钙、磷含量溶出量分别为(0.57±0.04) mg/g和(0.17±0.01) mg/g。1.0%醋酸煮后猪骨蛋白含量为(25.9±0.9) g/100 g,降低了10.0%;猪骨表观钙、磷元素含量分别为(230.0±6.4) mg/g和(100.0±2.3) mg/g,分别增加了18.3%和14.8%;猪骨钙、磷元素溶出量分别为(1.73±0.01) mg/g和(0.75±0.01) mg/g。经扫描电子显微镜观测发现,煮制后的猪骨易粉碎,1.0%醋酸煮后的猪骨最容易粉碎。红外光谱发现,煮制后猪骨成分发生了变化,图谱的峰比未煮制简单,成分比未煮制猪骨单一,而加水煮制和加酸煮制后猪骨图谱的峰相似,煮制后猪骨红外光谱图更接近人工合成的羟基磷灰石晶体。高温水煮和酸煮均能引起猪骨蛋白、钙元素和磷元素等化学成分含量的变化,导致猪骨硬度显著下降(P<0.05)。
关键词:猪骨;醋酸;煮制;硬度;化学成分
中国是全球最大的猪肉生产国和消费国,拥有全球最大的猪肉市场,2014年中国猪肉总产量为5 671万t,占全球肉类市场主要参与国总产量的51.3%,2014年中国猪肉消费5 717万t,占全球肉类市场主要参与国的52%[1]。若以猪骨占猪肉的9%~14%计算[2],2014年我国因消费猪肉而产生的猪骨大约有514.5万~800.4万t。如此多的猪骨如果丢弃,不仅浪费了骨资源,而且也会为环境带来负担。猪骨的蛋白含量和灰分含量比较高,而脂肪含量比较低[3]。猪骨中的必需氨基酸含量高于猪肉,而且猪骨还含有8 种人体必需元素[4],其钙、磷含量尤为丰富。因此,猪骨是一种宝贵的食物资源,其营养非常丰富。
目前人们对猪骨的利用有:猪骨蛋白的提取[5-6],猪骨肽的研究[7-9],利用猪骨制备调味剂[10-11],猪骨产品的开发等[12]。猪骨质地坚硬、不易软化,利用猪骨前一般都需要粉碎,这大大增加了利用猪骨的成本,导致猪骨利用率不高。如果能通过某种工艺使猪骨硬度较大程度的下降,对猪骨的利用率会大幅上升。在骨软化方面,虽然人们对鱼骨软化研究的较多,但软化的方法可以借鉴。邱志超[13]、王阳光[14]、王建辉[15]、吴克刚[16]等研究了高压和酸处理对鱼骨硬度的影响,发现高压和酸处理能使鱼骨硬度下降。在猪骨软化方面,张崟[17]、陈丽尧[18]等研究了猪骨超微粉碎工艺,利用高压提高了畜禽骨的粉碎率,对研究猪骨软化工艺具有指导意义。本实验以猪排骨为对象,探究了猪排骨在不同处理方式下硬度的变化,并测定了不同处理方式下,猪排骨中无机物、有机物含量,观察了猪排骨微观结构,为猪骨软化工艺提供理论依据。
1.1 材料与试剂
从杭州市下城区世纪联华超市和平店购买的猪排
骨;酸、氢氧化钠、硼酸、硫酸、硝酸、硫酸铜、硫酸钾、溴化钾为分析纯,醋酸为食品级。
1.2 仪器与设备
XB220A型电子天平 瑞士普利赛公司;C21-FK2101型电磁炉 美的集团有限公司;YXQ-LS-50SII型立式压力蒸汽灭菌锅 上海博迅实业有限公司医疗设备厂;DHG-9070型电热恒温鼓风干燥箱 上海一恒科技有限公司;FLB-250型万能高速粉碎机 上海菲力食品机械有限公司;TA.XT. Plus型物性测试仪 英国STab Micro System公司;K9840自动凯氏定氮仪 济南海能仪器股份有限公司;S-4700(II)场发射扫描电子显微镜 株式会社日立制作所;IOAP6300型ICP-AES分析仪 美国铂金埃尔默公司;TENSOR傅里叶变换红外光谱仪德国布鲁克光谱仪器公司。
1.3 方法
1.3.1 猪排骨前处理
将切成长和宽均为2~3 cm的猪排骨清洗,放入沸水中煮制15 min,冷却至室温,边清洗边去除猪肉至骨肉完全分离。
1.3.2 实验流程
猪排骨前处理(去肉处理),120 ℃条件下在水中(煮制时间40、50、60、70、80 min)和醋酸酸(体积分数0.0%、0.2%、0.4%、0.6%、0.8%、1.0%)溶液中煮制,测煮制后溶液中钙、磷元素含量,取骨干制,测定硬度或粉碎测粉碎后骨粉的蛋白含量、钙磷元素含量及显微结构。
1.3.3 高压酸液软化处理
将前处理后不带肉的骨样品放入锥形瓶中,加入100 mL水或不同体积分数(0.0%、0.2%、0.4%、0.6%、0.8%、1.0%)的醋酸溶液,用纱布及牛皮纸封口,于事先预热的高压灭菌锅中高压煮制一定时间,取出锥形瓶冷却至室温,取出骨。
1.3.4 干燥与粉碎
骨于烘箱60 ℃干燥一定时间,于粉碎机中粉碎。
1.3.5 指标测定
1.3.5.1 硬度的测定
采用TA.XT.Plus物性测试仪进行测定。参考丘志超等[13]的方法,探头选用:HDP/BS,参数:模式选择:压缩力测量;选项:返回开始;测试前速率:1.5 mm/s;测试速率:2.0 mm/s;测试后速率:10.0 mm/s;下压距离:strain 90%;阈值:Auto~25 g;环境数据获得速率:400 pps。记录峰值读数(g)。
1.3.5.2 蛋白含量的测定
参考GB 5009.5—2010《食品中蛋白质的测定》[19]中的凯氏定氮法。
1.3.5.3 钙、磷含量的测定
采用电感耦合等离子体原子发射光谱法测定样品钙、磷含量。样品消化参考谭惠仁[20]的二步消解法:将0.200 g样品加入凯氏定氮管,加入20 mL硝酸,加热至140 ℃消化10 min,升温至200 ℃消化至溶液变成淡黄色的澄清溶液,冷却,用去离子水定容至50 mL备用。
分别测定煮制后猪骨中表观钙、磷含量及煮制溶液中钙、磷溶出量。
1.3.5.4 显微结构的观测
采用扫描电子显微镜观样品骨显微结构。参考马原辉等[21]的方法,将双面胶黏在用于观测的样品台,取适量样品散落于黏在样品台的双面胶上,用洗耳球吹去未黏住的样品。将载有样品的样品台放入溅射镀膜仪中镀膜。镀膜结束后,将样品台置于扫描电子显微镜的样品仓,调节放大倍数,观察样品的显微结构。
1.3.5.5 傅里叶变换红外光谱法
采用红外光谱仪测定猪骨红外吸收图谱,压片方法采用溴化钾压片法,将经过干燥的试样与纯KBr研细均匀,置于模具中压成透明薄膜进行测定。
1.4 数据处理
采用Microsoft Office Excel软件进行数据处理,图制作采用软件Origin 8.0。采用软件SPSS对实验中两两处理组的指标进行单因素方差分析。结果以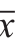 ±s表示。实验重复3 次,取其平均值。
±s表示。实验重复3 次,取其平均值。
2.1 不同时间煮制和不同体积分数醋酸溶液煮制对猪骨硬度的影响
在120 ℃条件下水中煮制不同时间后猪骨硬度变化结果如图1所示。在120 ℃条件下不同体积分数醋酸溶液中煮制80 min后骨硬度变化结果如图2所示。

图1 不同水煮制时间猪骨硬度的变化
Fig. 1 Change in hardness of pork bone cooked in water for different cooking times
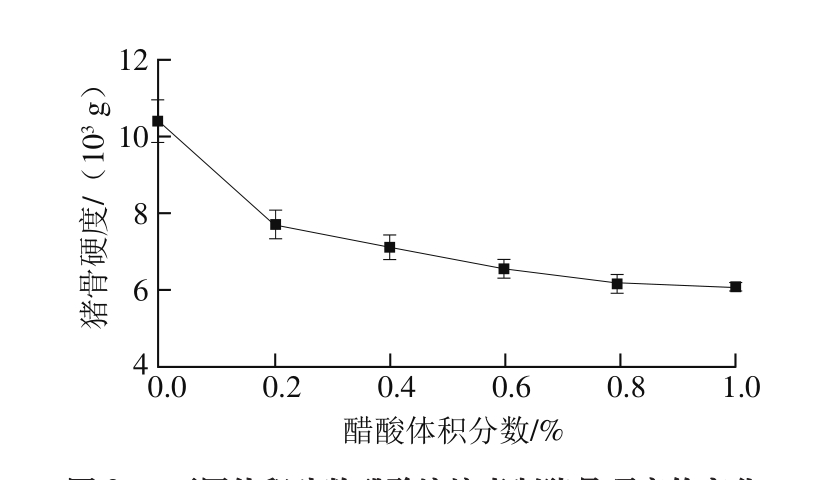
图2 不同体积分数醋酸溶液煮制猪骨硬度的变化
Fig. 2 Change in hardness of pork bone cooked with different concentrations of acetic acid
由图1可以看出,随着煮制时间延长,猪骨硬度显著下降(P<0.05)。加水煮制时间从40 min延长到80 min,猪骨硬度从(16 445±867) g下降到(10 995±546) g,说明高温煮制有利于猪骨软化。由图2可以看出,随着醋酸溶液体积分数的增加,煮制后猪骨硬度显著下降(P<0.05),但下降速率降低。醋酸溶液体积分数从0.0%(体积分数,下同)增加到1.0%,猪骨硬度从(10 995±546) g下降到(6 003±153) g,在醋酸溶液中煮制和在水中煮制相同时间后,在酸中煮制的猪骨硬度要小于在水中煮制的猪骨,说明醋酸溶液有利于猪骨的软化。
骨中含有丰富的人体必需营养物质,其中灰分含量45.0%、蛋白质含量35.7%、水分含量4.8%、脂肪含量10.3%,其他物质含量4.2%,其中蛋白质绝大部分为胶原,灰分为骨盐,其主要成分是碳酸钙和磷酸钙,其主要存在形式是羟基磷灰石结晶和无定形的磷酸钙混合物。骨磷灰石结晶在胶原网络内有序排列。无机物含量、微观结构和磷灰石晶体与胶原组成的网络结构对骨的硬度均有贡献,无机相提供硬度,有机相提供韧性和吸收力的能力[22]。所以,猪骨胶原蛋白的变性、溶解及降解和猪骨无机物的溶解等导致猪骨组成比例的改变和猪骨结构的破坏,可使猪骨机械强度发生变化。
2.2 不同处理方式对猪骨中蛋白含量的影响
图3为120 ℃条件下加水煮制和加1.0%醋酸溶液煮制80 min后猪骨蛋白含量,对照组为新鲜猪骨。可以看出,在120 ℃煮制80 min后,与未煮制的猪骨相比,煮制后的猪骨蛋白含量显著降低(P<0.05)。而且在醋酸溶液中煮制的猪骨的蛋白含量低于在水中煮制的猪骨。加水煮制后蛋白含量从(35.9±0.0)g/100 g降低到(28.5±2.3) g/100 g,降低了7.4%;醋酸溶液煮制后蛋白含量降低到(25.9±0.9)g/100 g,降低了10.0% 。在加热条件下,胶原蛋白的三条肽链之间的氢键断裂,紧密的三螺旋结构打开,形成单条肽链或是肽段,从高度有序的螺旋结构无规卷曲转变。酸溶液可以使胶原蛋白充分溶胀,提高胶原蛋白的溶解度[23]。Masanobu等[24]在研究醋酸蒸煮处理对鱼骨软化速率和有机物溶解速率影响发现,醋酸蒸煮处理可以使鱼骨中有机物含量减少,且鱼骨硬度与有机物含量的4 次方成正比。所以加酸又加热处理更能提高猪骨胶原蛋白的溶解度,从而影响猪骨的硬度。
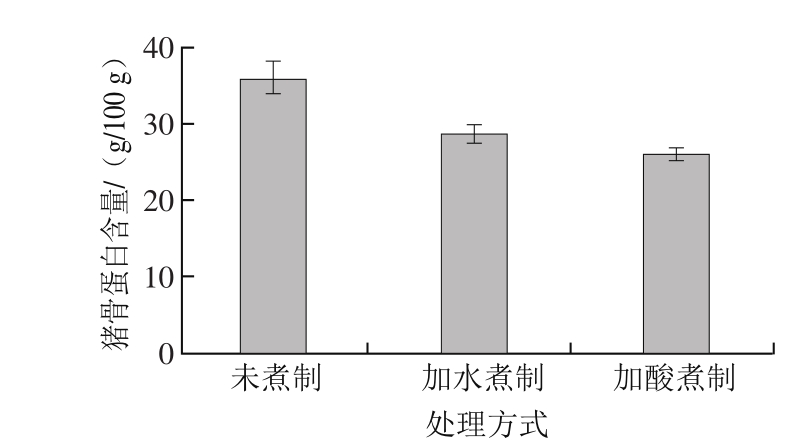
图3 不同处理方式对猪骨中蛋白含量的影响
Fig. 3 Effect of different cooking treatments on protein content in pork bone
2.3 不同处理方式对猪骨中钙、磷含量的影响
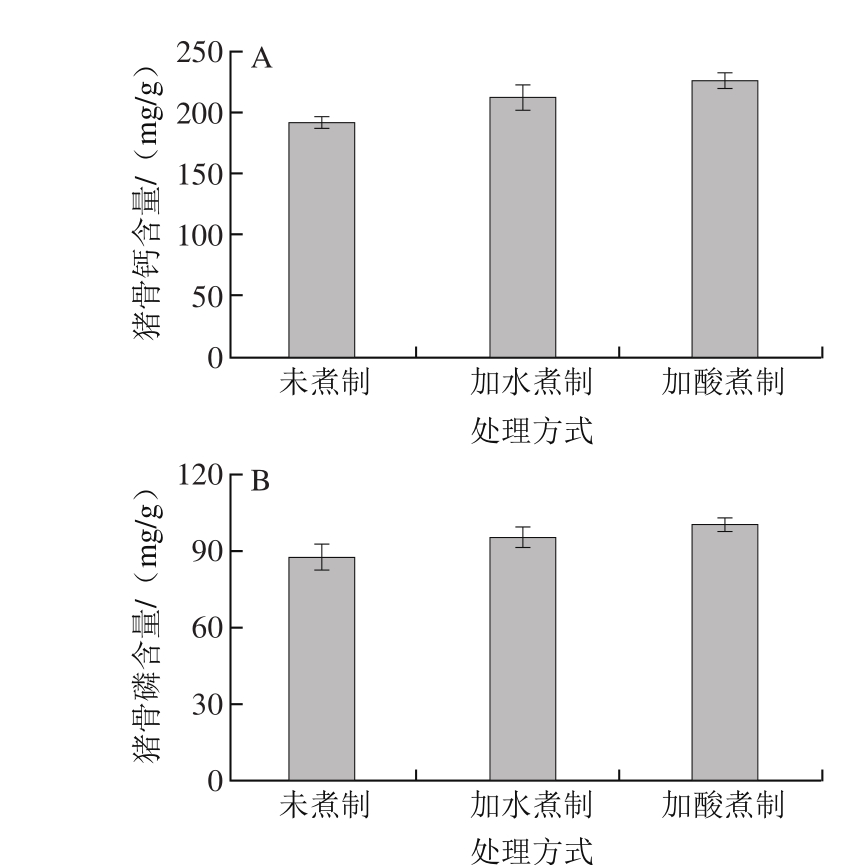
图4 不同处理方式对猪骨中钙含量(A)和磷含量(B)的影响
Fig. 4 Effect of different cooking treatments on calcium (A) and phosphorus (B) contents in pork bone
图4 为120 ℃条件下加水煮制和加1.0%醋酸溶液煮制80 min后表观猪骨钙、磷含量,对照组为新鲜猪骨。可以看出,跟未煮制的猪骨相比,煮制后猪骨表观钙、磷元素含量显著增加(P<0.05),而且在醋酸溶液中煮制后的猪骨表观钙、磷含量最高。加水煮制,猪骨表观钙含量从(190.0±5.4) mg/g增加到(210.0±8.2) mg/g,增加了11.8%;猪骨表观磷含量从(88.0±5.0) mg/g增加到(96.0±4.0) mg/g,增加了8.9%。加酸煮制后猪骨表观钙含量为(230.0±6.4) mg/g,增加了18.3%;猪骨表观磷含量为(100.0±2.3) mg/g,增加了14.8%。这是由于加水煮制或者加酸煮制后,虽然猪骨在水中煮制和醋酸溶液中煮制,无机物有一定量的溶出,但猪骨有机物减少量大于猪骨无机物减少量,导致猪骨无机物表观含量的增加。这与Shimosak等[25]在研究醋酸溶液处理下鱼骨物理特性和成分的变化中的结果一致。
2.4 不同处理方式对猪骨钙、磷元素溶出量的影响
图5为在水中、在酸中浸泡80 min,在120 ℃条件下加水煮制、加1.0%醋酸溶液煮制80 min后猪骨钙、磷溶出量。
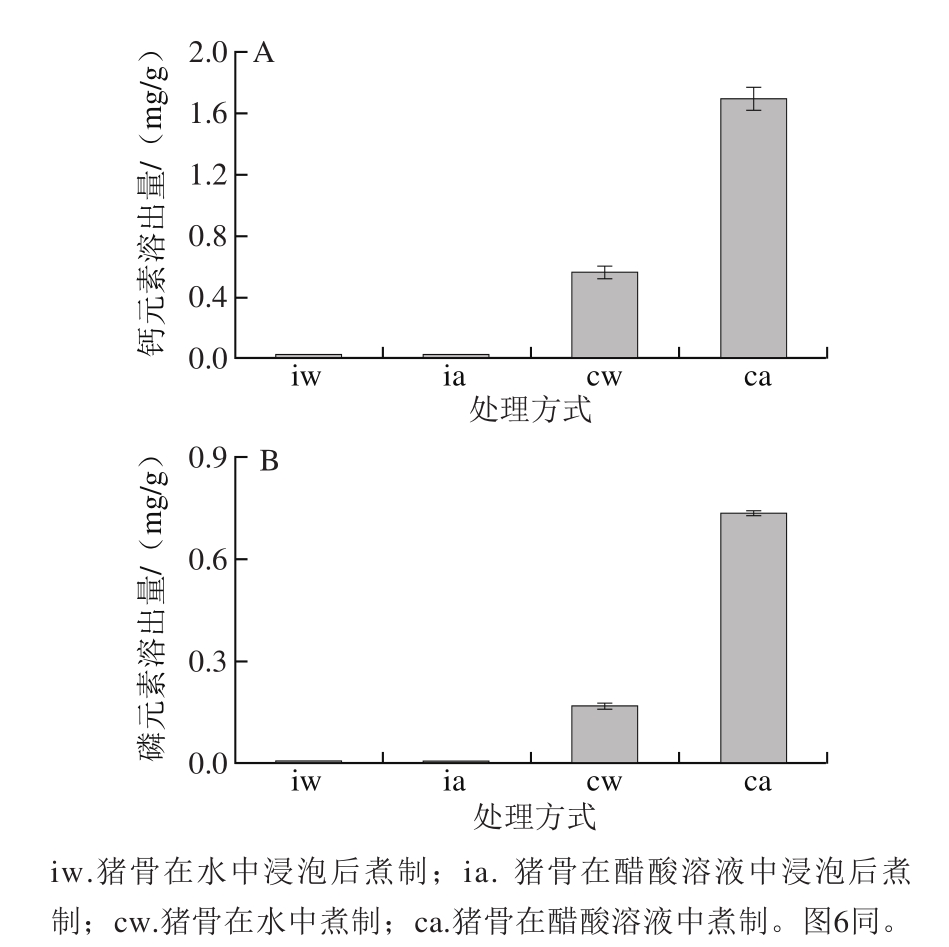
图5 不同处理方式对猪骨钙溶出量(A)和磷溶出量(B)的影响
Fig. 5 Effect of different cooking treatments on calcium release (A) and phosphorus release (B) from pork bone
从图5可以发现,在水中或在醋酸溶液中浸泡后,钙、磷元素几乎没有溶出,而在水中或醋酸溶液中煮制后,钙、磷元素溶出量显著增加(P<0.05),而且在醋酸溶液中煮制后猪骨钙、磷元素溶出量最高。在水中煮制后,猪骨钙、磷元素溶出量分别为(0.57±0.04) mg/g和(0.17±0.01) mg/g,在醋酸溶液中煮制后,钙、磷元素溶出量分别为(1.70±0.01) mg/g和(0.74±0.04) mg/g。这说明热处理和醋酸溶液均有利于猪骨钙、磷含量的溶出。这与赵钊等[26]在研究烹制骨汤中钙等矿物质含量的测定及营养评价中的结果一致。还可以发现,即使在醋酸溶液中煮制,猪骨钙、磷含量的溶出量还是极低的,所以只喝骨头汤补钙效果可能不大。
2.5 不同处理方式对猪骨显微结构的影响
利用扫描电子显微镜观察了不同处理方式下猪骨粉不同放大倍数的显微结构,以未处理组作为对照。观察结果如图6所示。

图6 不同处理方式对猪骨扫描电子显微镜图
Fig. 6 SEM photos of pork bone subjected to different cooking treatments
比较不同处理方式下放大300 倍和1 000 倍的猪骨粉电子显微镜图可以看出,在相同粉碎条件下,煮制后猪骨粉的颗粒度明显小于未煮制的,而且在醋酸溶液煮制后的猪骨粉的颗粒度是最小的,这说明煮制后的猪骨比未煮制的猪骨更容易粉碎,在醋酸溶液中煮制的猪骨最容易粉碎。这与柴向华等[27]在研究高压蒸煮对鸡骨架骨骼组成结构及硬度的影响结果一致。比较不同处理方式下放大5 000倍的猪骨粉电子显微镜图可以看出,煮制后的猪骨粉表面比未煮制的猪骨粉光滑,可以反映出煮制后猪骨的结构变化。
2.6 不同处理方式下猪骨红外吸收光谱分析
利用中红外光谱仪测定了不同处理方式下猪骨粉的红外吸收光谱,以人工合成的羟基磷灰石的红外光谱图作对照,结果如图7所示,与Haberko等[28]研究的热处理下天然羟基磷灰石中红外图谱相似。表1为不同处理方式下猪骨红外吸收光谱数据。
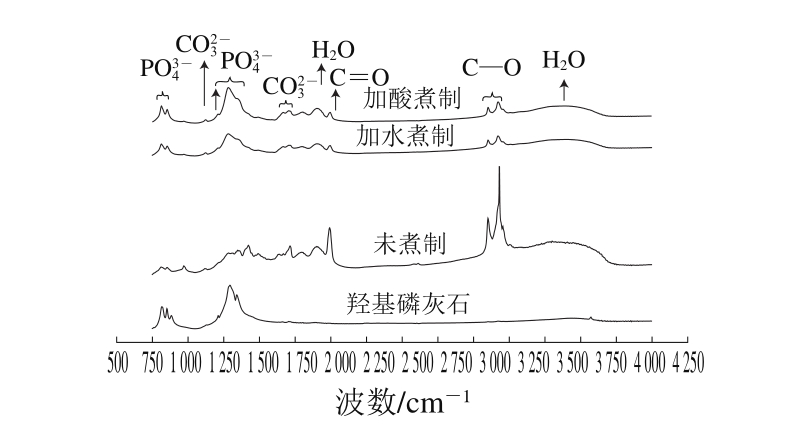
图7 不同处理方式下猪骨粉红外吸收光谱图
Fig. 7 Transmission infrared spectra of pork bone subjected to different cooking treatments
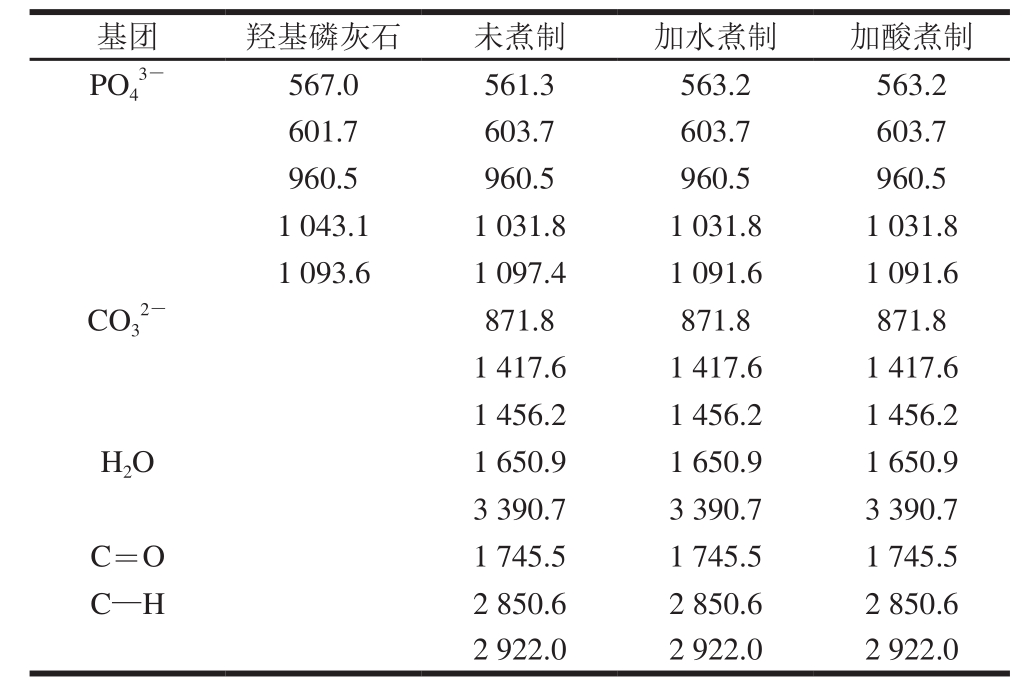
表1 不同处理方式下猪骨粉红外吸收光谱数据
Table 1 Infrared spectral data of pork bone subjected to different cooking treatments cm-1
从图7可以发现,未煮制的猪骨粉红外光谱图上的峰比较杂乱,说明未煮制的猪骨的成分复杂,原因是猪骨是由脂肪、蛋白质、无机成分等组成的复杂混合物。而相对于未煮制的猪骨粉,加水煮制或加酸煮制后的猪骨粉红外光谱图的峰相对比较清晰,与未煮制的猪骨粉红外光谱图存在明显不同,说明煮制后猪骨成分有所变化,且比未煮制猪骨成分简单,原因可能是煮制导致猪骨内物质的溶出。加水煮制和加酸煮制后,猪骨粉的红外光谱图极其相似,说明加酸或加水煮制后猪骨的所含成分相似。
C—H和C=O代表的是有机物的吸收峰,比较未煮制和煮制后猪骨粉的红外光谱图还可以发现,未煮制猪骨粉C—H和C=O红外吸收峰强度明显大于煮制后的,说明煮制可以降低煮骨中有机物含量,得到与前面相似的结果。
煮制后猪骨粉P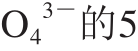 个红外吸收峰较未煮制的更加明显,说明煮制后猪骨组成与人工合成的羟基磷灰石晶体更接近,这与Shimosaka[29]在研究加热过程中鱼骨化学成分和晶体结构的变化的结果相似。
个红外吸收峰较未煮制的更加明显,说明煮制后猪骨组成与人工合成的羟基磷灰石晶体更接近,这与Shimosaka[29]在研究加热过程中鱼骨化学成分和晶体结构的变化的结果相似。
研究了高温水煮和酸煮对猪骨硬度及化学成分的影响,研究表明,煮制使猪骨硬度显著下降(P<0.05),达到软化、易粉碎的效果,在醋酸溶液中煮制效果更佳。煮制使猪骨蛋白含量显著降低(P<0.05),猪骨表观钙、磷元素含量显著增加和猪骨钙、磷含量溶出量显著增加(P<0.05);而加醋酸溶液煮制效果更佳。煮制使猪骨组成成分发生变化,加水煮制和加酸煮制后猪骨组成成分相似,煮制后的猪骨红外吸收图谱与人工合成的羟基磷灰石晶体更接近。利用中红外光谱法分析猪骨成分比较新颖,实验结果对提高猪骨利用率方面有一定贡献。在结构方面,还可以借助其他分析手段如X衍射图谱分析猪骨结构变化。
参考文献:
[1] 去年全球猪肉总消费1.1亿吨中国产量占52%[N/OL]. (2015-04-18).财经网, http://www.chinairn.com/news/20150418/101633387.shtml.
[2] 张崟, 卓勇贤, 张佳敏, 等. 猪骨利用的研究进展[J]. 农产品加工(学刊), 2010(11): 83-86. DOI:10.3969/j.issn.1671-9646(X).2010.11.021. [3] 朱莲珍. 人和动物的微量元素营养[M]. 青岛: 青岛出版社, 1994: 10-15.
[4] 安玉会, 杨松华, 晋佳路. 猪骨蛋白的氨基酸含量分析[J] . 河南医学研究, 2004, 13(3): 208-209. DOI:10.3969/j.issn.1004-437X.2004.03.003. [5] 刘安军, 石清, 朱振元, 等. 猪骨明胶的提取工艺研究[J]. 现代食品科技, 2010, 26(5): 519-522. DOI:10.3969/j.issn.1673-9078.2010.05.025.
[6] 刘立新. 猪骨蛋白水提工艺的优化[J]. 食品与机械, 2013(5): 220-222. DOI:10.3969/j.issn.1003-5788.2013.05.058.
[7] 刘小红, 李诚, 付刚, 等. 猪股骨头胶原蛋白降血压肽的分离纯化[J].食品科学, 2014, 35(6): 50-54. DOI:10.7506/spkx1002-6630-2014060010.
[8] 宗红, 诸葛斌, 秦斌钰, 等. 功能性猪骨泥发酵工艺研究[J]. 中国调味品, 2014(2): 31-35; 46. DOI:10.3969/j.issn.1000-9973.2014.02.008. [9] 彭慧莉. 酶解和乳酸菌发酵猪骨的工艺研究[D]. 成都: 西华大学, 2013: 11-12.
[10] 郇兴建. 利用猪骨制备天然肉味香精的研究[D]. 南京: 南京农业大学, 2012: 8-13. DOI:10.7666/d.Y2361610.
[11] 乔煦玮, 褚书丽. 凝固型猪骨浓汤调料的研制[J]. 中国调味品, 2011(7): 74-76. DOI:10.3969/j.issn.1000-9973.2011.07.020.
[12] 陈静怡, 肖厚荣, 张靖华, 等. 低温冷冻法生产牛骨粉的工艺研究[J]. 安徽农学通报, 2015(15): 127-129. DOI:10.3969/j.issn.1007-7731.2015.15.061.
[13] 邱志超, 曾庆孝. 醋酸浸泡蒸煮联合处理对干制罗非鱼骨质量的影响[J]. 现代食品科技, 2010, 26(6): 577-581. DOI:10.3969/j.issn.1673-9078.2010.06.007.
[14] 王阳光, 郦光. 高压软化青鲇整鱼肉中骨刺的工艺研究[J]. 现代农业科技, 2011(15): 370-371; 374. DOI:10.3969/j.issn.1007-5739.2011.15.223.
[15] 王建辉, 刘冬敏, 刘永乐, 等. 淡水鱼鱼骨软化工艺条件的优化[J]. 食品与机械, 2011(2): 109-111. DOI:10.3969/j.issn.1003-5788.2011.02.033.
[16] 吴克刚, 张文祥, 柴向华, 等. 高压蒸煮软化罗非鱼鱼骨的研究[J]. 食品工业科技, 2013, 34(15): 210-212. DOI:10.13386/ j.issn1002-0306.2013.15.022.
[17] 张崟, 王新惠, 王卫, 等. 高压和酶解辅助制备超微骨粉的工艺研究[J]. 现代食品科技, 2014, 30(10): 172-175; 250. DOI:10.13982/ j.mfst.1673-9078.2014.10.029.
[18] 陈丽尧. 猪骨骼超微粉碎工艺及新产品的开发[D]. 黑龙江: 东北农业大学, 2008: 2-4. DOI:10.7666/d.y1403730.
[19] 卫生部. 食品中蛋白质的测定: GB 5009.5—2010[S]. 北京: 中国标准出版社, 2010.
[20] 谭惠仁. ICP-AES、ICP-MS、AFS、IC分析技术在茶叶中微量元素的分析研究[D]. 深圳: 中山大学, 2013: 9-14.
[21] 马原辉, 陈学广, 刘哲. 扫描电子显微镜粉末样品的制备方法[J]. 实验室科学, 2011, 14(1): 148-150. DOI:10.3969/j.issn.1672-4305.2011.01.048.
[22] VIGUET-CAMIN S, GAMERO P, DELMAS P D. The role of collagen in bone strength[J]. Osteoporosis International, 2006, 17(3): 319-336. DOI:10.1007/s00198-005-2035-9.
[23] 卓素珍. 鮟鱇鱼皮胶原蛋白的性质、组成及应用研究[D]. 杭州: 浙江工商大学, 2009: 17-21. DOI:10.7666/d.Y1524164.
[24] MASANOBU I, SHOJI M, HISAHIKO W, et al. Effect of acetic acid on softening rate and solubilization rate of oganic matter from fish bone[J]. Journal of Food Processing and Preservation, 1989, 13(2): 123-132. DOI:10.1111/j.1745-4549.1989.tb00095.x.
[25] SHIMOSAKA C, SHIMOMURA M, TERAI M. Changes in the physical properties and composition of fish bone cured in an acetic acid solution[J]. Journal of Home Economics of Japan, 1998, 49(8): 873-879. DOI:10.11428/jhej1987.49.873.
[26] 赵钊, 钞虹, 吉爱国. 烹制骨汤中钙等矿物质含量的测定及营养评价[J]. 食品研究与开发, 2008(12): 126-129. DOI:10.3969/ j.issn.1005-6521.2008.12.037.
[27] 柴向华, 何文龙, 吴克刚, 等. 高压蒸煮对鸡骨架骨骼组成结构及硬度的影响[J]. 食品科学, 2013, 34(23): 103-107. DOI:10.7506/ spkx1002-6630-201323022.
[28] HABERKO K, BUĆKO M M, BRZEZIŃSKA-MIECZNIK J, et al. Natural hydroxyapatite-its behaviour during heat treatment[J]. Journal of the European Ceramic Society, 2006, 26(4/5): 537-542. DOI:10.1016/j.jeurceramsoc.2005.07.033.
[29] SHIMOSAKA C. Relationship between chemical composition and crystalline structure in fish bone during cooking[J]. Journal of Clinical Biochemistry and Nutrition, 1999, 26(3): 173-182. DOI:10.3164/ jcbn.26.173.
Effect of High Temperature Cooking in Water and Acetic Acid Solution on Hardness and Chemical Composition of Pork Bones
LIU Jianhua, CHEN Xinhua, DING Yuting*
(College of Ocean, Zhejiang University of Technology, Hangzhou 310014, China)
Abstract:The effect of high temperature cooking in water and acetic acid solution on the hardness of pork bones was studied under the conditions of 120 ℃ and different cooking times (40, 50, 60, 70 and 80 min) in water, and different acetic acid concentrations (0.0%, 0.2%, 0.4%, 0.6%, 0.8% and 1.0%, V/V) and 80 min in acetic acid solution. The protein content of raw and cooked pork bones were determined by the Kjeldahl method, and calcium and phosphorus contents as well as the amount of calcium and phosphorus release by inductively coupled plasma atomic emission spectrometry (ICP-AES). The microstructure of comminuted bones was examined by scanning electron microscope (SEM), and the structure of chemical components in bone powder samples was characterized by infrared spectroscopy. It was found that high temperature cooking resulted in a decrease in bone hardness, which decreased from (16 445 ± 867) to (10 995 ± 546) g with increasing the cooking time from 40 to 80 min, and from (10 995 ± 546) to (6 003 ± 153) g with increasing the acetic acid concentration from 0.0% to 1.0%. After cooking in water, the protein content in pork bone decreased by 7.4% to (28.5 ± 2.3) g/100 g, the apparent contents of calcium and phosphorus increased by 11.8% and 8.9% to (210.0 ± 8.2) and (96.0 ± 4.0) mg/g, respectively, and the amounts of calcium and phosphorus released were (0.57 ± 0.04) and (0.17 ± 0.01) mg/g, respectively. After cooking in acetic acid solution, the protein content decreased by 10.0% to (25.9 ± 0.9) g/100 g, the apparent contents of calcium and phosphorus increased by 18.3% and 14.8% to (230.0 ± 6.4) and (100.0 ± 2.3) mg/g, respectively, and theamounts of calcium and phosphorus released were (1.73 ± 0.01) and (0.75 ± 0.01) mg/g, respectively. Cooked pork bone was easily ground, especially the one cooked in acetic acid. The mid infrared absorption spectrum of cooked pork bone was simpler than that of the untreated one, with the former being similar to synthesized hydroxyapatite. Thus, the chemical components of pork bone were changed after cooking. We concluded that high temperature cooking in both water and acetic acid solution can change the contents of protein, calcium and phosphorus in pork bone, leading to a significant decrease in hardness (P < 0.05).
Key words:pork bone; acetic acid; cooking; hardness; chemical composition
收稿日期:2016-06-15
基金项目:国家自然科学基金青年科学基金项目(31301437)
作者简介:刘建华(1982—),男,副教授,博士,研究方向为功能性食品和水产品加工。E-mail:jhliu@zjut.edu.cn
*通信作者:丁玉庭(1963—),男,教授,博士,研究方向为水产品加工、贮藏和保鲜。E-mail:dingyt@mail.hz.zj.cn
DOI:10.7506/spkx1002-6630-201713004
中图分类号:TS251.94
文献标志码:A
文章编号:1002-6630(2017)13-0020-06
引文格式:
刘建华, 陈新华, 丁玉庭. 高温水煮和酸煮对猪骨硬度及化学成分的影响[J]. 食品科学, 2017, 38(13): 20-25. DOI:10.7506/spkx1002-6630-201713004. http://www.spkx.net.cn
LIU Jianhua, CHEN Xinhua, DING Yuting. Effect of high temperature cooking in water and acetic acid solution on hardness and chemical composition of pork bones[J]. Food Science, 2017, 38(13): 20-25. (in Chinese with English abstract)
DOI:10.7506/spkx1002-6630-201713004. http://www.spkx.net.cn