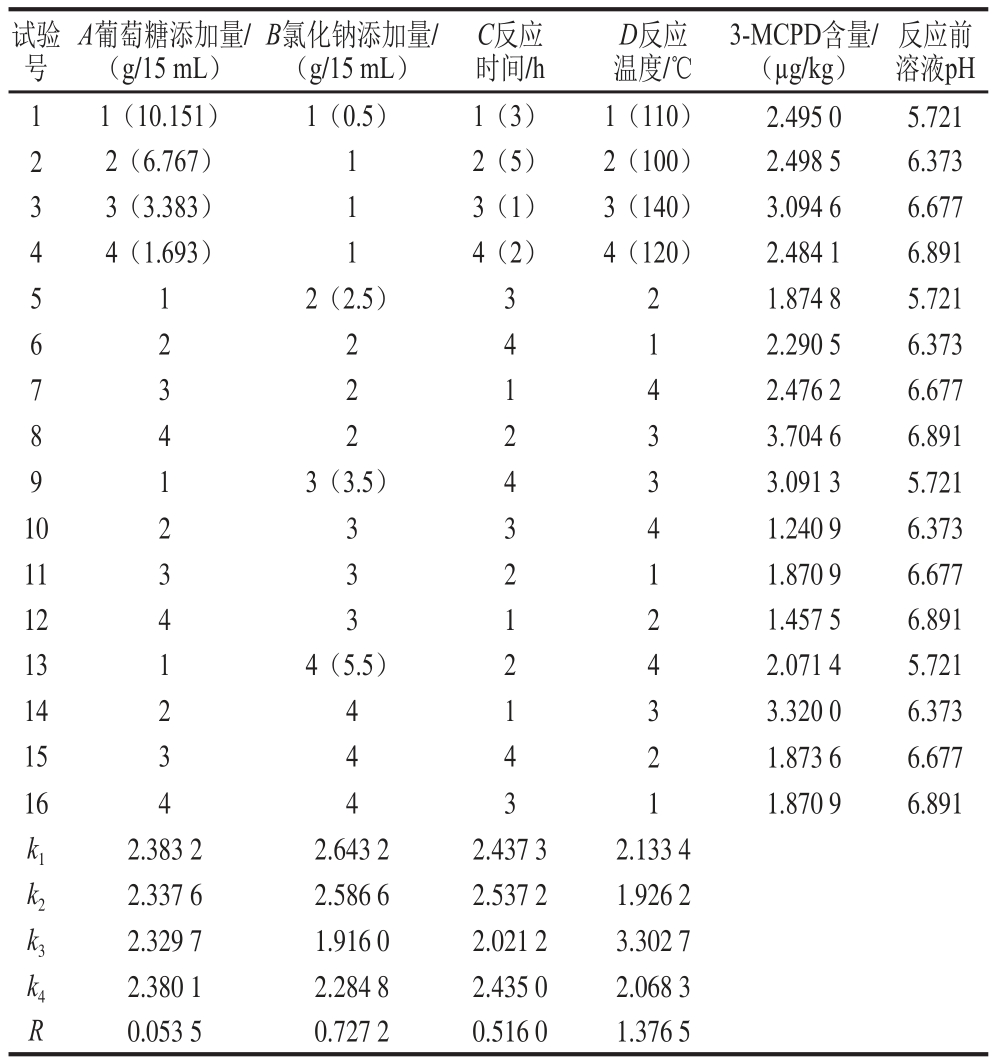
表1 “葡萄糖+氯化钠+水”模型反应正交试验结果
Table 1 Orthogonal array design with experimental results for 3-MCPD formation from glucose + sodium chloride model system
黄明泉,李 娟,邹青青,孙宝国,田红玉,张玉玉
(北京工商大学 北京市食品风味化学重点实验室,北京食品营养与人类健康高精尖创新中心,食品质量与安全北京实验室,北京 100048)
摘 要:以“单糖+氯化钠+水”为模型进行热反应,研究3-氯-1,2-丙二醇(3-monochloropropane-1,2-diol,3-MCPD)的形成机理和消长规律。结果表明,在“葡萄糖+氯化钠+水”模型反应中,反应温度对3-MCPD的形成影响最大,其次是氯化钠添加量、反应时间和葡萄糖添加量;在“单糖+氯化钠+水”模型中,6 种单糖都生成了3-MCPD,其中核糖和氯化钠反应生成的3-MCPD量最大(30.604 μg/kg),果糖生成的量最小(2.498 6 μg/kg);在“葡萄糖+氯化钠+水”模型中,反应后生成的挥发性成分5-羟甲基糠醛含量最大,然后是糠醛和2,5-二甲酰基呋喃。根据实验结果探讨3-MCPD的形成机理,提出在单糖模型反应中缩水甘油可能是关键的中间体。
关键词:单糖;3-氯-1,2-丙二醇;热反应模型;形成机理;缩水甘油
Abstract:The forma tion of 3-monochloropropane-1,2-diol (3-MCPD) was investigated in thermal reaction model systems consisting of one of six monosaccharides, sodium chloride and deionized water. Temperature had the most significant influence on 3-MCPD formation from the “glucose + sodium chloride” model system, followed by sodium chloride concentration, reaction time and glucose concentration. In addition, 3-MCPD could be formed from all six monosaccharides.The highest amount (30.604 μg/kg) of 3-MCPD was formed from the “ribose + sodium chloride” model system and the lowest amount (2.498 6 μg/kg) from the “fructose + sodium chloride” model system under the same reaction conditions.5-Hydroxymethyl furfural was the most abundant volatile compound detected from the “glucose + sodium chloride”model system, followed by furfural and 2,5-dimethyl acetyl furan. According to these results and the literature, the formation mechanism of 3-MCPD was discussed herein, and 3-epoxy-1-propanol (glycidol) was suggested to be as the key intermediate.
Key words:monosaccharides; 3-monochloropropane-1,2-diol; thermal reaction model; formation mechanism; glycidol
氯丙醇是丙三醇上的羟基被氯原子取代后产生的一类化合物,包括3-氯-1,2-丙二醇(3-monochloropropane-1,2-diol,3-MCPD)和2-氯-1,3-丙二醇(2-monochloropropane-1,3-diol,2-MCPD)以及双氯取代的1,3-二氯-2-丙醇(1,3-dichloropropan-2-ol,1,3-DCP)和2,3-二氯-1-丙醇(2,3-dichloropropan-1-ol,2,3-DCP)[1],常温条件下为液体,沸点大于100 ℃,可溶于水、乙醚、乙醇等[2]。在食品中可检测到的氯丙醇化合物中3-MCPD的含量是最高的,它具有生殖毒性[3]、致突变性、致癌性及一定的神经毒性[4]等。3-MCPD最初存在于酸水解植物蛋白液及配制酱油中[5-6],随后,又在许多食品中检测到一定含量的3-MCPD,如食用油[7]、咖啡[8]、啤酒[9]、奶酪[10]等。食品添加剂专家委员会2001年暂定人类对3-MCPD每日最大摄入量(provisional maximum tolerable daily intake,PMTDI)是2 μg/kg体质量[11]。
目前普遍认为食品中3-MCPD的产生机理是原料中油脂的降解产物与外来的氯离子发生了亲核取代反应生成,但Kuntzer等[12]在研究烟熏制品时发现烟熏所使用的木屑中的纤维素在高温条件下会发生裂解产生3-羟基丙酮,并认为3-羟基丙酮是3-MCPD形成的前体物。此外,文献[13-16]也相继报道了纤维素、葡萄糖等的裂解也会形成3-羟基丙酮。除了3-羟基丙酮,纤维素、葡萄糖及其他糖的裂解还会产生甘油醛[13,17]、1,3-二羟基-2-丙酮[18]、丙烯醛[19],这些化合物在一定的反应条件下和氯离子反应有可能生成3-MCPD。由此可推测,在氯化物的存在下,碳水化合物在加热条件下也可生成3-MCPD,但目前有关碳水化合物形成3-MCPD的研究鲜见报道。
本研究以葡萄糖为代表,建立“葡萄糖+氯化钠+水”热反应模型,研究葡萄糖热裂解产生3-MCPD的影响因素及形成机理,此外,还研究了其他5 种单糖对该单糖模型反应中形成3-MCPD的影响。本实验是对单糖形成3-MCPD的过程进行研究。本研究的热反应模型主要是对热反应肉味香精或含盐食品高温(高于100 ℃)加工处理的一种简单模拟,通过这个模型的研究,可为更好地控制3-MCPD在食品或相关产品中的污染提供参考。
1.1 材料与试剂
氯化钠(分析纯) 北京化工厂;D-果糖(纯度98%)、D-核糖(纯度98%)、苏氨酸、D-半乳糖、D-木糖(均为生化试剂)、正己烷、无水乙醚、D-甘露糖、葡萄糖、乙酸乙酯、无水硫酸钠、Celite545硅藻土(试剂级)、2,2,4-三甲基戊烷(纯度≥99.5%)国药集团化学试剂有限公司;七氟丁酰基咪唑(纯度97%)、3-MCPD(纯度99.5%)、d5-3-MCPD(纯度99.5%)、2-MCPD(纯度99.5%) 东京化成工业株式会社。
1.2 仪器与设备
气密针(1 mL) 美国Agilent公司;厚壁耐压管(15 mL,15#)、玻璃层析柱(有效柱长305 mm,内径26 mm) 北京欣维尔玻璃仪器有限公司;移液枪(20~200、1 000 μL) 法国Gilson公司;DF-101S集热式恒温加热磁力搅拌器 巩义市予华仪器有限责任公司;Jenway 3250 pH计 英国Bibby公司;N-EVAPTM11112位干浴氮吹仪 美国Organomation Associates公司;RE-52AA型旋转蒸发器上海亚荣生化仪器厂;TRACE ULTRA-DSQII气相色谱-质谱联用仪 美国Thermo Fisher公司。
1.3 方法
1.3.1 单糖与氯化钠的模型热反应及3-MCPD的检测
本实验以热反应香精的制备为参照配方[20-21],将葡萄糖、氯化钠、去离子水加入厚壁耐压管中,整体构成“葡萄糖+氯化钠+水”模型,混匀并溶解后密封,加热反应一段时间,然后测定反应液中3-MCPD的含量。水的用量15 mL固定不变,采用四因素四水平正交试验来考察葡萄糖添加量、氯化钠添加量、反应温度和反应时间对3-MCPD形成的影响。3-MCPD的检测方法参照GB/T 5009.191—2006《食品中氯丙醇含量的测定》[22]中的方法,同时采用内标法进行定量,相应的气相色谱-质谱联机分析条件如下。
色谱条件:毛细管色谱柱RTx-5(30 m×0.25 mm,0.25 μm),进样口:210 ℃,传输线:260 ℃;载气He,恒压模式41.4 kPa(6psi),不分流进样,进样1 μL,升温程序如下:50 ℃保持1 min,再以2 ℃/min升温至90 ℃,以40 ℃/min升温至260 ℃,保持6 min。
质谱条件:EI源,电压70 eV,离子源温度:230 ℃,溶剂延迟时间12 min,SIM扫描。定性离子:m/z253、275、289、291和453,定量离子:m/z253。
再将葡萄糖分别换成其他5 种等物质量单糖,构成“单糖+氯化钠+水”模型,研究这5 种单糖模型反应中形成3-MCPD的情况,并同时做空白反应和对比反应(以“葡萄糖+氯化钠+水”模型为对比),然后测定3-MCPD含量,平行测定3 次。
1.3.2 葡萄糖与氯化钠模型热反应液中挥发性成分的检测
1.3.2.1 葡萄糖模型热反应液中挥发性成分的提取
向分液漏斗中加入80 g反应液和40 mL重蒸二氯甲烷,振荡摇匀,静置5 min后,将有机相转到圆底烧瓶,然后将水相再重复萃取2 次,最后弃去水相,合并3 次萃取的有机相,加入无水硫酸钠冷冻干燥12 h,过滤除去无水硫酸钠。乙醚的萃取方法同二氯甲烷,最后合并两种溶剂的萃取液,旋转蒸发、氮吹至1.0 mL,待分析。
1.3.2.2 葡萄糖模型热反应液中挥发性成分的分析
将葡萄糖模型反应液的挥发性成分提取物进行气质分析,采用谱库检索(NIST 08)、标准品对照等手段定性,面积归一化法进行简单定量。相应的气相色谱-质谱联机分析条件如下。
色谱条件:RTX-5毛细管柱(60 m×0.25 mm,0.25 μm);载气为He,流速2.0 mL/min;不分流,进样0.2 μL,进样口:230 ℃;升温程序如下:35 ℃保持1 min,再以5 ℃/min升温至100 ℃,以15 ℃/min升温至200 ℃,保持2 min;再以20 ℃/min升温至270 ℃,保持10 min。
质谱条件:电压70 eV,离子源温度:250 ℃,四极杆温度:150 ℃,溶剂延迟时间7 min,扫描质量范围m/z29~450。
2.1 “葡萄糖+氯化钠+水”模型热反应中3-MCPD形成的影响因素
参考文献[23],设计正交试验,研究葡萄糖添加量、氯化钠添加量、反应时间和反应温度4 个因素对“葡萄糖+氯化钠+水”模型热反应中3-MCPD形成的影响。正交试验因素、水平设计及结果见表1,方差分析结果见表2。
表1 “葡萄糖+氯化钠+水”模型反应正交试验结果
Table 1 Orthogonal array design with experimental results for 3-MCPD formation from glucose + sodium chloride model system

表2 正交试验的方差分析结果
Table 2 Analysis of variance of the experimental results of orthogonal array design

注:*.影响显著(P<0.05)。
由表1可得,“葡萄糖+氯化钠+水”模型热反应中能生成3-MCPD;正交试验的4 个因素中反应温度对3-MCPD的产生量影响最大(RD=1.376 5),其次是氯化钠添加量(RB=0.727 2)、反应时间(RC=0.516 0)和葡萄糖添加量(RA=0.053 5)。从表2中方差分析结果中也可看出反应温度是影响3-MCPD生成的最大因素。
同时由表1可得,反应前溶液的pH值与葡萄糖的用量是相关的,当葡萄糖添加量从10.151 g/15 mL减少到1.693 g/15 mL时,反应前溶液的pH值从6.892减小到5.722。这表明pH值在6.892~5.722之间时,对体系中3-MCPD的产生的影响并不大。

图1 正交试验中各因素对模型反应中3-MCPD含量的影响
Fig. 1 Effects of different factors on the production of 3-MCPD in model system
由图1可知,随着氯化钠添加量的增加,反应产物中3-MCPD含量先减小后增加;随着葡萄糖添加量的增加,3-MCPD含量变化不大;但随着反应温度的上升,3-MCPD含量在不断上升,120 ℃上升更加明显;虽然3-MCPD含量在随着反应时间的延长而增加,但是2 h后,其含量增加缓慢。另外,由表2可知,组合A4B2C2D3(3.704 6 μg/kg)是正交试验中3-MCPD含量最大组,组合A2B3C3D4(1.240 9 μg/kg)是正交试验中3-MCPD含量最小组;但理论最大值组合为A1B1C2D3,最小值组合为A3B3C3D2。因此,对上述正交试验结果进行验证,结果见表3。
表3 葡萄糖与氯化钠模型反应正交试验验证结果
Table 3 Experimental verifi cation of reaction conditions for maximum and minimum production of 3-MCPD from glucose + sodium chloride model sysstteemm
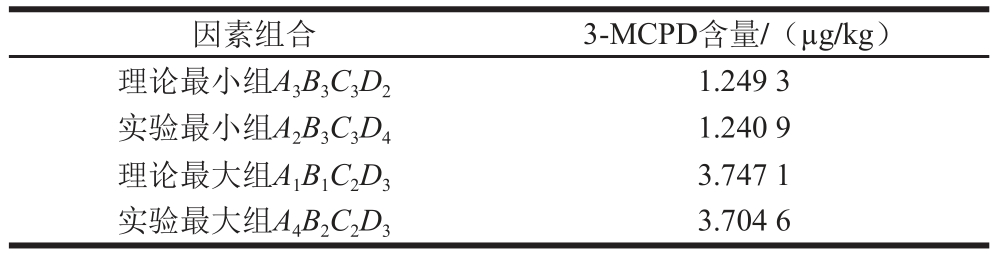
经验证,葡萄糖与氯化钠的模型反应中A2B3C3D4和A1B1C2D3分别是最小和最大因素组合,最大的因素组合是氯化钠添加量0.5 g/15 mL、葡萄糖添加量10.151 g/15 mL、反应温度140 ℃、反应时间5 h。
2.2 其他5 种单糖与氯化钠模型热反应中3-MCPD的形成
为了便于3-MCPD的检测分析,参照葡萄糖模型反应中3-MCPD产生量最大的因素组合,做其他单糖与氯化钠的模型热反应,具体的反应条件见表4,分析结果如图2所示。
表4 6 种单糖模型热反应条件
Table 4 Model systems consisting of glucose or one of fi ve additional monosaccharides and sodium chloride under the same reaction conditions
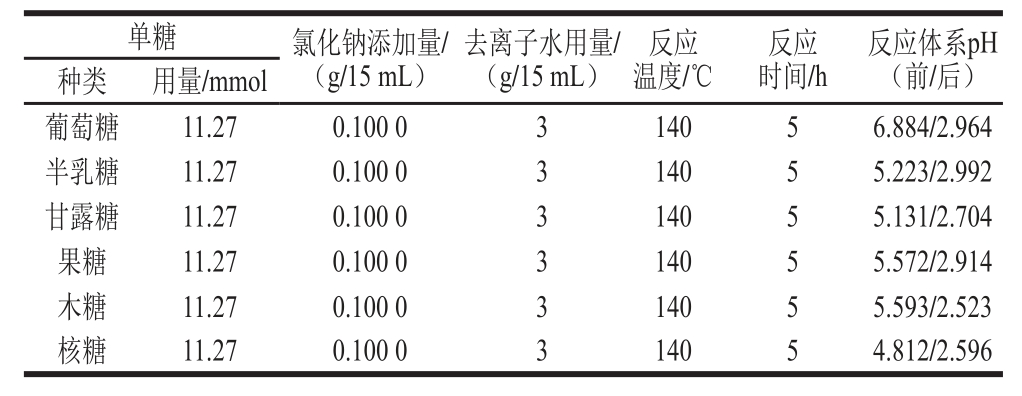
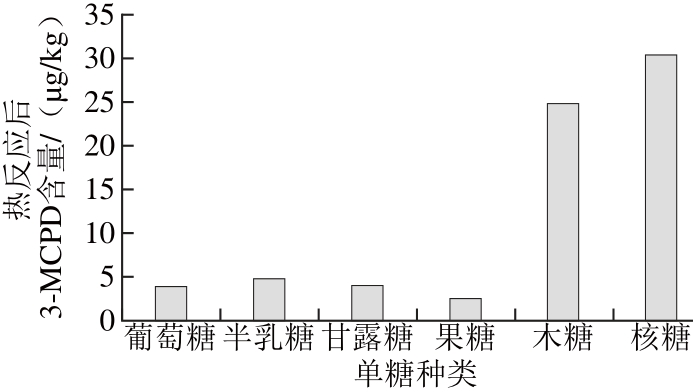
图2 6 种单糖与氯化钠模型反应产生3-MCPD的趋势
Fig. 2 3-MCPD concentrations in six different reaction models
由图2可知,6 种单糖模型热反应产物中都检测到3-MCPD,说明单糖裂解的产物在模型反应条件下能与氯化钠反应而产生3-MCPD;五碳糖的模型热反应产生3-MCPD的量比六碳糖更高,尤其是核糖,产生3-MCPD的量达到30.604 μg/kg;在六碳的单糖模型中,以半乳糖模型反应产生3-MCPD的量最高,为4.789 8 μg/kg。六碳糖与五碳糖之间生成3-MCPD的量差异可能与这两种单糖的裂解速率不同有关。通常在相同的条件下,五碳糖的裂解速率要快于六碳糖[24],因此五碳糖产生的中间产物要多于六碳糖,从而产生的3-MCPD的量比六碳糖多。
2.3 “葡萄糖+氯化钠+水”模型反应液中挥发性化合物的分析
采用正交试验中3-MCPD生成量最大因素组合,进行葡萄糖模型热反应,分别用乙醚和二氯甲烷萃取模型热反应后的溶液合并萃取液,干燥浓缩后,然后进气相色谱-质谱分析,结果如表5所示。
表5 “葡萄糖+氯化钠+水”模型反应溶液的气相色谱-质谱分析
Table 5 GC-MS analysis of volatile compounds formed from glucose + sodium chloride model system
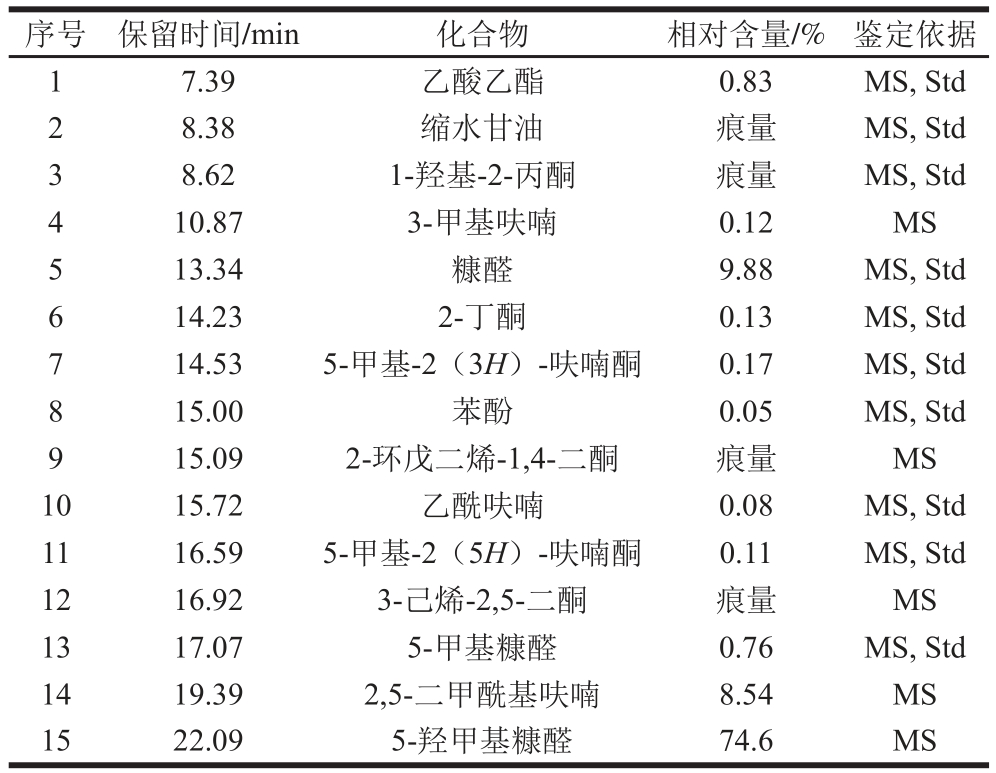
注:MS.谱库检索;Std.标准品定性。
由表5可知,葡萄糖模型热反应产物中共鉴定出15 种挥发性化合物,包括5 种呋喃类化合物,含量最大的是5-羟甲基糠醛(5-HMF,74.6%),其次是糠醛(9.88%)和2,5-二甲酰基呋喃(8.54%),而三碳类化合物缩水甘油(<0.01%)和1-羟基-2-丙酮(<0.01%)含量很少。由此可知糖裂解的主要途径是生成糠醛类物质,少量的三碳类裂解产物会形成3-MCPD。
2.4 “单糖+氯化钠+水”热反应模型3-MCPD的形成机理初探
目前,关于单糖与氯化钠模型反应中3-MCPD的形成机理鲜见报道。葡萄糖形成3-MCPD的过程可能与其三碳类裂解产物相关,故根据葡萄糖裂解的过程[12-13,15-16,18,25-30],初步推测单糖模型反应中3-MCPD的机理如图3所示。
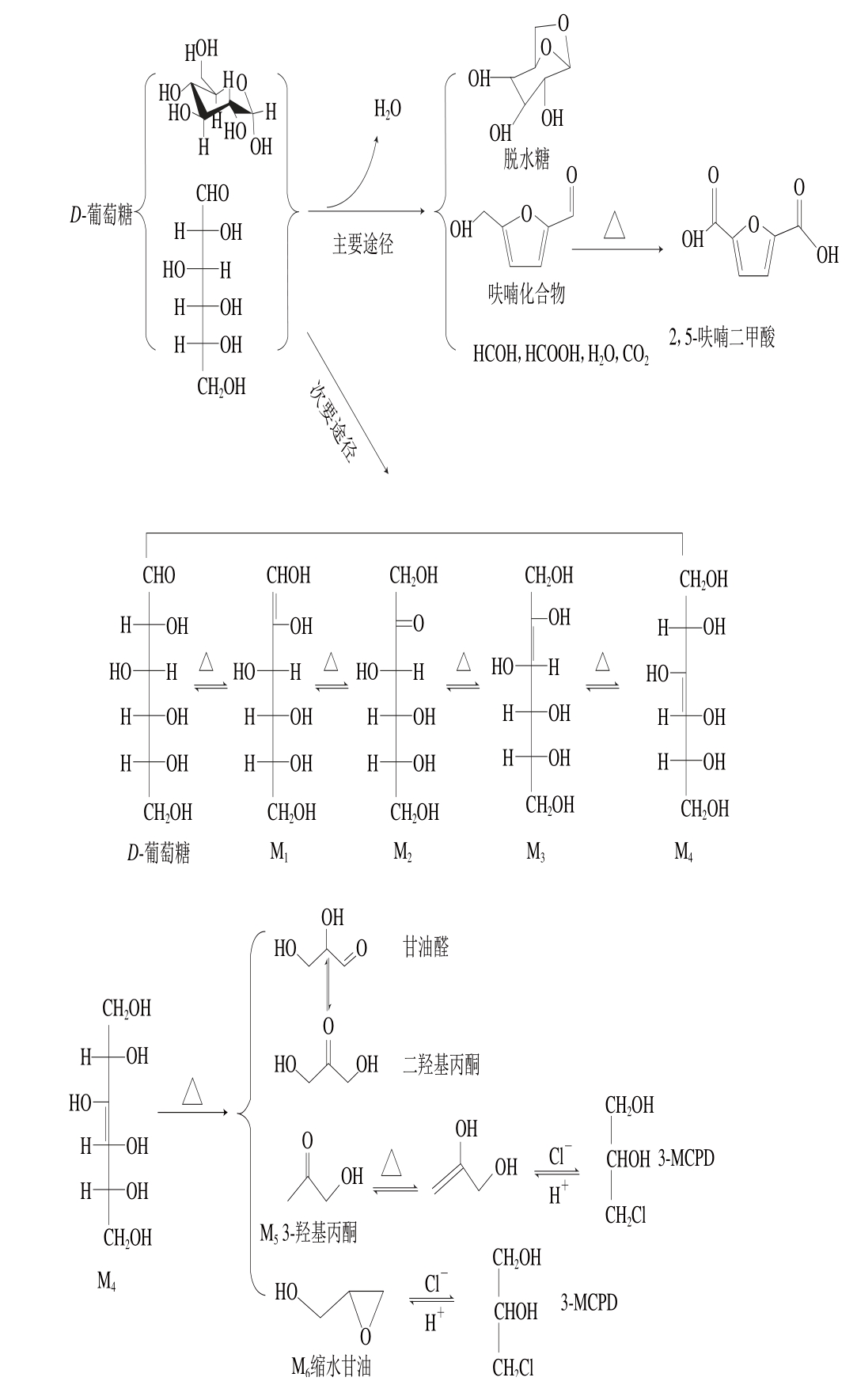
图3 葡萄糖与氯化钠热反应模型3-MCPD的形成机理
Fig. 3 Formation mechanism of 3-MCPD in thermal reaction model consisting of glucose and sodium chloride
由图3可知,在加热条件下,葡萄糖的裂解有两条途径,其中主要的途径是葡萄糖在高速率下脱水、脱羧生成糖苷、糠醛、呋喃类化合物、葡糖酸、甲酸、甲醛、二氧化碳和水[15-17,25]。在表5中挥发性成分的分析结果显示葡萄糖裂解的主要产物是呋喃类物质,在表4中模型反应后溶液pH值下降,即有酸生成,都可证实这一裂解途径。
在加热条件下,葡萄糖裂解的另一个途径是葡萄糖通过烯醇化、异构化依次形成中间产物M1、M2、M3和M4,中间产物M3和M4会通过双键氧化进一步裂解形成小分子化合物,而M4会裂解产生三碳类小分子化合物,如三羟基丙酮(M5)、缩水甘油(M6)。这些三碳类化合物,会与氯离子反应生成3-MCPD[12,31-32]。
由图3可知,葡萄糖在形成3-MCPD的过程中,M4裂解产生三碳类小分子化合物是3-MCPD生成的关键步骤。因为裂解涉及到双键的氧化断裂,需要的能量较大,所以温度是主要的影响因素,而葡萄糖用量影响不大。另外,温度也能加速葡萄糖裂解成3-MCPD的整个过程,从而影响3-MCPD的含量。可见,反应温度是3-MCPD形成的主要因素,这与前面正交试验设计分析结果一致。氯离子通过减少葡萄糖裂解产物呋喃的形成而增加小分子化合物的形成,从而影响葡萄糖的裂解速率和产物的分布[33],进而影响3-MCPD的量。其他的六碳糖产生3-MCPD的机理与葡萄糖相似,但由于它们在立体结构上有差异,所以生成3-MCPD的量有些差别。

图4 木糖与氯化钠热反应模型3-MCPD前体物的形成机理
Fig. 4 Formation mechanism of 3-MCPD precursors in thermal reaction model consisting of xylose and sodium chloride
五碳糖裂解形成3-MCPD前体物M5和M6的过程见图4。生成M5和M6的关键前体物是中间产物M7,与图3中M4类似,它的形成与裂解难易程度,决定了3-MCPD的生成量。M7由木糖经三次烯醇异构转化而成,而中间产物M4是由葡萄糖经四次烯醇异构转化而来的,所以在相同条件下,形成中间产物M7比M4更容易一些。此外,可能由于M4中的基团—CHOHCH2OH的给电子能力强于M7中的基团—CH2OH,因而M4中双键比M7中的双键更加稳定,即M7中的双键易断裂。综合以上两个原因,木糖模型反应中生成的中间产物M5和M6多于葡萄糖模型反应,同样3-MCPD的生成量也是木糖多于葡萄糖。核糖可能因为形成M7的顺式异构体,双键稳定性比M7差,所以裂解更容易些,3-MCPD的生成量也更高。
本实验研究报道了3-MCPD形成的新途径,即在加热条件下,单糖类碳水化合物裂解产生3-羟基丙酮和缩水甘油,这2 种三碳类小分子产物可以与氯离子反应生成3-MCPD;碳水化合物的用量对3-MCPD生成影响不大,反应温度、氯化物添加量、反应时间等因素会影响其生成,其中反应温度是影响最大的因素。3-羟基丙酮和缩水甘油相比较而言,由于缩水甘油更易与氯离子反应生成3-MCPD,所以缩水甘油可能是3-MCPD的主要前体物。
参考文献:
[1] 王悦宏. 快速测定HVP和酱油中3-MCPD方法的研究与应用[D].长春: 东北师范大学, 2008: 12-24.
[2] 傅武胜, 林升清, 黄剑锋. 氯丙醇的毒理学研究进展[J]. 现代预防医学, 2003, 30(2): 228-230. DOI:10.3969/j.issn.1003-8507.2003.02.043.
[3] 刘晓艳, 张妍. 发酵调味料中氯丙醇的危害与检测[J]. 中国调味品,2005(5): 7-12.
[4] KIM K. Differential expressions of neuronal and inducible nitric oxide synthase in rat brain after subchronic administration of 3-monochlorol,2-propanediol[J]. Food and Chemical Toxicology, 2008, 46: 955-960.DOI:10.1016/j.fct.2007.10.025.
[5] HAMLET C G, ASUNCION L, VELIÍŠEK J, et al. Formation and occurrence of esters of 3-chloropropane-1,2-diol(3-CPD) in foods:what we know and what we assume[J]. European Journal of Lipid Science and Technology, 2011, 113(3): 279-303.
[6] 李国基, 耿予欢. 关于中国传统酿造酱油中是否含有氯丙醇的考证报告[J]. 中国酿造, 2001, 20(5): 7-9
[7] ZELINKOVÁ Z, SVEJKOVSKÁ B, VELÍŠEK J, et al. Fatty acid esters of 3-chloropropane-1,2-diol in edible oils[J]. Food Additives and Contaminants, 2006, 23(12): 1290-1298.
[8] DOLEŽAL M, CHALOUPSKÁ M, DIVINOVÁ V, et al. Occurrence of 3-chloropropane-1,2-diol and its esters in coffee[J]. European Journal of Lipid Science and Technology, 2005, 221(3): 221-225.
[9] DIVINOVÁ V, DOLEŽAL M, VELIŠEK J. Free and bound 3-chloropropane-1,2-diol in coffee surrogates and malts[J]. Czech Journal of Food Science, 2007, 25(1): 39-47.
[10] KARŠULÍNOVÁ L, FOLPRECHTOVÁ B, DOLEŽAL M, et al.Analysis of the lipid fractions of coffee creamers, creamaerosols, and bouillon cubes for their health risk associated constituents[J]. Czech Journal of Food Science, 2007, 25(5): 257-264.
[11] Joint FAO/WHO Expert Committee on Food Additive (JECFA). Safety evaluation of certain food additives and containts prepared by the fi ftyseventh meeting of the Joint FAO/WHO Expert Committee on Food Additives (JECFA)[M], Genevs: WHO Food Additives Series 48,WHO, 2002: 401-432.
[12] KUNTZER J, WEIBHAAR R. The smoking process-a potent source of 3-chloropropane-1,2-diol (3-MCPD) in meat products[J]. Deutsche Lebensmittel-Rundschau, 2006, 9: 397-400.
[13] CARLSON T R, TOMPSETT G A, CONNER W C, et al. Aromatic production from catalytic fast pyrolysis of biomass-derived feedstocks[J]. Topics in Catalysis, 2009, 52(3): 241-252. DOI:10.1007/s11244-008-9160-6.
[14] 董宁宁. 碳水化合物的热裂解气相色谱-质谱研究[J]. 质谱学报,2004, 25(1): 24-28. DOI:10.3969/j.issn.1004-2997.2004.01.005.
[15] LU Qiang, YANG Xiaochu, DONG Changqing, et al. Influence of pyrolysis temperature and time on the cellulose fast pyrolysis products:analytical py-GC/MS study[J]. Journal of Analytical and Applied Pyrolysis, 2011, 92(2): 430-438. DOI:10.1016/j.jaap.2011.08.006.
[16] WANG Shurong, GUO Xiujuan, LIANG Tao, et al. Mechanism research on cellulose pyrolysis by py-GC/MS and subsequent density functional theory studies[J]. Bioresource Technology, 2012, 104:722-728. DOI:10.1016/j.biortech.2011.10.078.
[17] SASAKI M, OSHIKAWA T, WATANABE H, et al. Reaction kinetics and mechanism for hydrothermal degradation and electrolysis of glucose for producing carboxylic acids[J]. Research on Chemical Intermediates,2011, 37(2/3/4/5): 457-466. DOI:10.1007/s11164-011-0275-1.
[18] HU Xun, LIEVENS C, LARCHER A, et al. Reaction pathways of glucose during esterification: effects of reaction paraments on the formation of humin type polymers[J]. Bioresource Technology, 2011,102(21): 10104-10113. DOI:10.1016/j.biortech.2011.08.040.
[19] SHEN Chong, ZHANG I Y, FU Gang, et al. Pyrolysis ofD-glucose to acrolein[J]. Chinese Journal of Chemical Physics, 2011, 24(3): 249-252. DOI:10.1088/1674-0068/24/03/249-252.
[20] 张岱, 孙培培, 黄明泉, 等. 甘油与氯化钠模型热反应中生成3-氯-1,2-丙二醇的研究[J]. 食品工业科技, 2013, 34(9): 74-78.
[21] 黄明泉, 吴继红, 孙培培, 等. 甘油三酯与氯化钠模型反应中3-氯-1,2-丙二醇的形成研究[J]. 食品科学, 2014, 35(17): 8-11.DOI:10.7506/spkx1002-6630-201417002.
[22] 国家质量监督检验检疫总局, 中国国家标准化管理委员会. 食品中氯丙醇含量的测定: GB/T 5009.191—2006[S]. 北京: 中国标准出版社, 2006.
[23] SVEJKOVSKA B, DOLEZAL M, VELISEK J. Formation and decomposition of 3-chloropropane-1,2-diol esters in models simulating processed foods[J]. Czech Journal of Food Science, 2006, 24(4): 172-179.
[24] JALBOUT A F, ROY A K, SHIPAR A H, et al. Density functional computational studies on ribose and glycine Maillard reaction:formation of the amadori rearrangement products[J]. International Journal of Quantum Chemistry, 2008, 108(3): 589-597.
[25] CARLSON T R, JAE J, LIN Y C, et al. Catalytic fast pyrolysis of glucose with HZSM-5: the combined homogeneous andheterogeneous reactions[J]. Journal of Catalysis, 2010, 270: 110-124. DOI:10.1016/j.jcat.2009.12.013.
[26] DEMIRBAS A. Mechanism of liquefaction and pyrolysis reactions of biomass[J]. Energy Conversion and Management, 2000, 41: 633-646.DOI:10.1016/S0196-8904(99)00130-2.
[27] HAMLET C G, SADD P A. Kinetics of 3-chloropropane-1,2-diol (3-MCPD) degradation in high temperature model systems[J]. European Food Research and Technology, 2002, 215: 46-50.
[28] PISKORZ J, RADLEIN D, SCOTT D S. On the mechanism of rapid pyrolysis of cellulose[J]. Journal of Analytical and Applied Pyrolysis,1986, 9: 121-137. DOI:10.1016/0165-2370(86)85003-3.
[29] RADLEIN D, PISKORE J, SCOTT D S. Fast pyrolysis of natural polysaccharides as a potential industrial process[J]. Journal of Analytical and Applied Pyrolysis, 1991, 19: 41-63. DOI:10.1016/0165-2370(91)80034-6.
[30] SHEN D K, GU S. The mechanism for thermal decomposition of cellulose and its main products[J]. Bioresource Technology, 2009,100: 6496-6504. DOI:10.1016/j.biortech.2009.06.095.
[31] TESSER R, SANTACESARIA E, DI SERIO M, er al. Kinetics of glycerol chlorination with hydrochloric acid: a new route to alpha,gamma-dichlorohydrin[J]. Industrial & Engineering Chemistry Research, 2007, 46: 6456-6465. DOI:10.1021/ie070708n.
[32] HAMLET C G, SADD P A, CREWS C, et al. Occurrence of 3-chloropropane-1,2-diol (3-MCPD) and related compounds in food: a review[J]. Food Additives and Contaminants, 2002, 19: 619-631.DOI:10.1080/02652030210132391.
[33] HEYNS K, KLIER M. Browning reactions and fragmentation of carbohydrates[J]. Carbohydrate Research, 1968, 6(4): 436-448.
Formation of 3-Monochloropropane-1,2-diol in Thermal Reaction Model Systems Consisting of Monosaccharides and Sodium Chloride
HUANG Mingquan, LI Juan, ZOU Qingqing, SUN Baoguo, TIAN Hongyu, ZHANG Yuyu
(Beijing Key Laboratory of Flavor Chemistry, Beijing Advanced Innovation Center for Food Nutrition and Human Health,Beijing Laboratory for Food Quality and Safety, Beijing Technology and Business University, Beijing 100048, China)
DOI:10.7506/spkx1002-6630-201719001
中图分类号:TS207.3
文献标志码:A
文章编号:1002-6630(2017)19-0001-06
引文格式:
黄明泉, 李娟, 邹青青, 等. 单糖与氯化钠模型反应中3-氯-1,2-丙二醇的形成[J]. 食品科学, 2017, 38(19): 1-6.
DOI:10.7506/spkx1002-6630-20 1719001. http://www.spkx.net.cn
HUANG Mingquan, LI Juan, ZOU Qingqing, et al. Formation of 3-monochloropropane-1,2-diol in thermal reaction model systems consisting of monosaccharides and sodium chloride[J]. Food Science, 2017, 38(19): 1-6. (in Chinese with English abstract) DOI:10.7506/spkx1002-6630-201719001. http://www.spkx.net.cn
收稿日期:2016-04-18
基金项目:国家自然科学基金面上项目(31471665);北京市属高等学校高层次人才引进与培养计划项目(CIT & TCD 201404034)
作者简介:黄明泉(1977—),男,副教授,博士,研究方向为香料香精、食品检测与分析。E-mail:hmqsir@163.com