
图1 不同提取溶剂的回收率
Fig. 1 Recoveries of antibiotics with different extraction solvents
孙晓冬,郝 杰,毛 婷,史 娜,姜 洁*
(北京市食品安全监控和风险评估中心,北京 100041)
摘 要:使用超高效液相色谱-串联四极杆质谱仪结合快速高通量的前处理方法实现豆芽中51 种抗生素类药物的快速筛查测定。样品经乙腈提取,QuEChERS净化,采用ACQUITY BEH C18色谱柱分离,梯度洗脱,采用电喷雾-正离子多反应监测模式,外标法定量。结果表明:51 种抗生素类药物的定量限(RSN≥10)为0.5~5 μg/kg,高、中、低3 个添加水平平均回收率为62.93%~118.69%,相对标准偏差为0.29%~9.72%,该方法能够达到高通量、多组分、快速的筛查目的,可应用于豆芽中抗生素类药物的批量快速筛查。
关键词:豆芽;超高效液相色谱-串联四极杆质谱;抗生素类药物;快速筛查
Abstract: A rapid method was established for screening 51 antibiotic residues in bean sprouts using ultra performance liquid chromatography-tandem mass spectrometry (UPLC-MS/MS) after a rapid and high throughput pretreatment. Samples were extracted with acetonitrile and the extract was cleaned up by quick, easy, cheap, effective, rugged, and safe (QuEChERS)extraction. The target compounds were separated on BEH C18UPLC column with gradient elution, monitored using positive electrospray ionization in the multiple-reaction monitoring (MRM) mode and quantitated by the external standard method.The results showed that the limits of quantity (LOQs) for 51 antibiotics we re between 0.5 and 5 μg/kg. Average recoveries at 3 different spiked levels were 62.93%-118.69%, and the precision values expressed as relative standard deviations (RSDs)were 0.29%-9.72%. This method proved to be a rapid, high throughput, multi-component screening method for antibiotic residues in bean sprouts.
Key words: bean sprout; ultra performance liquid chromatography-tandem mass spectrometry (UPLC-MS/MS); antibiotics;rapid screening
DOI∶10.7506/spkx1002-6630-201720049
豆芽又称“活体蔬菜”,其品种丰富、营养全面、清香脆嫩,深受人们喜爱。但近几年,毒豆芽、问题豆芽等事件愈演愈烈[1-2],相关部门对豆芽食品安全的关注和监管[3-4]也越来越大,有报道指出在豆芽生产中可能会存在非法添加抗生素类药物的现象[5-7],如恩诺沙星、诺氟沙星、青霉素、土霉素等,其主要目的是用于杀菌消毒和防止根部腐烂。而抗生素类药物的滥用,易导致耐药性细菌的产生,极有可能在环境中传播和扩散,进而对人体健康构成潜在威胁[8-10]。
当前动物源性食品中抗生素类药物的检测方法文献较多[11-13],但是关于植物源性食品中抗生素类药物残留的检测方法报道较少,而且检测方法多为单个或几个化合物一个方法[14-18],前处理方法繁琐耗时长,不能满足食品安全突发事件快速处置工作所要求的高效率、多组分等要求,因此选择合适的提取方法和分析手段对解决多组分抗生素类药物残留量的同时测定尤为重要。
本实验使用超高效液相色谱-串联四极杆质谱进行豆芽中磺胺类、喹诺酮类、林可酰胺类、大环内酯类、β-内酰胺类、四环素族、硝基咪唑类[19-21]7 类共51 种抗生素类药物同时检测方法的研究,由于涉及的抗生素类药物种类比较多,舍去前处理常用的固相萃取柱的净化手段,选用QuEChERS(quick,easy,cheap,effective,rugged,safe)直接净化提取,其前处理简单、分析耗用时间短和较高灵敏度的优势增加了定性和定量的可靠性,满足了食品安全风险突发事件的快速应急处理工作中高通量、高可靠性确证和定量分析的要求,为相关工作提供了可靠的技术保障。
1.1 材料与试剂
豆芽抽检样品:从北京市各大市场、超市随机抽取的豆芽样品;豆芽质控样品:由实验室自行培育的阴性样品,添加标准溶液制备得到。
盐酸四环素(纯度98.0%,CAS号:64-75-5)、盐酸金霉素(纯度93.0%,CAS号:64-72-2)、盐酸强力霉素(纯度98.7%,CAS号:24390-14-5)、盐酸土霉素(纯度96.5%,CAS号:2058-46-0)、青霉素V钾(纯度98.8%,CAS号:132-98-9)、林可霉素(纯度98.0%,CAS号:154-21-2)、克林霉素(纯度98.0%,CAS号:18323-44-9)、泰乐菌素(纯度96.0%,CAS号:1401-69-0)、替米考星(纯度99.0%,CAS号:108050-54-0)、螺旋霉素(纯度97.0%,CAS号:8025-81-8)、吉他霉素(纯度92.0%,CAS号:232-429-6)、红霉素(纯度97.0%,CAS号:114-07-8)、竹桃霉素(纯度96.5%,CAS号:2751-09-9)、甲硝唑(纯度99.8%,CAS号:443-48-1)、替硝唑(纯度99.5%,CAS号:19387-91-8)、奥硝唑(纯度99.9%,CAS号:16773-42-5)、洛硝哒唑(纯度97.0%,CAS号:7681-76-7)、塞克硝唑(纯度95.3%,CAS号:3366-95-8)、异丙硝唑(纯度98.0%,CAS号:14885-29-1)、二甲硝咪唑(纯度99.0%,CAS号:551-92-8)、西诺沙星(纯度99.5%,CAS号:28657-80-9)、盐酸双氟沙星(纯度98.0%,CAS号:91296-86-5)、依诺沙星(纯度99.0%,CAS号:74011-58-8)、恩诺沙星(纯度99.0%,CAS号:93106-60-6)、氟甲喹(纯度98.3%,CAS号:42835-25-6)、盐酸洛美沙星(纯度99.0%,CAS号:98079-52-8)、麻保沙星(纯度99.0%,CAS号:115550-35-1)、萘啶酸(纯度98.0%,CAS号:389-08-2)、诺氟沙星(纯度99.0%,CAS号:70458-96-7)、氧氟沙星(纯度99.0%,CAS号:82419-36-1)、奥比沙星(纯度97.8%,CAS号:113617-63-3)、恶喹酸(纯度98.0%,CAS号:14698-29-4)、培氟沙星(纯度99.0%,CAS号:70458-92-3)、沙拉沙星盐酸盐(纯度97.0%,CAS号:91296-87-6)、司帕沙星(纯度98.9%,CAS号:111542-93-9)、磺胺嘧啶(纯度99.0%,CAS号:68-35-9)、磺胺二甲氧哒嗪(纯度99.0%,CAS号:122-11-2)、磺胺甲基嘧啶(纯度99.2%,CAS号:127-79-7)、磺胺对甲氧嘧啶(纯度98.0%,CAS号:651-06-9)、磺胺甲二唑(纯度98.5%,CAS号:144-82-1)、磺胺甲基异恶唑(纯度99.5%,CAS号:723-46-6)、磺胺甲氧哒嗪(纯度99.0%,CAS号:80-35-3)、磺胺间甲氧嘧啶(纯度98.0%,CAS号:1220-83-3)、磺胺吡啶(纯度99.0%,CAS号:144-83-2)、磺胺喹恶啉(纯度98.0%,CAS号:59-40-5)、磺胺噻唑(纯度99.5%,CAS号:72-14-0)、磺胺二甲异恶唑(纯度99.0%,CAS号:127-69-5)、磺胺氯哒嗪(纯度99.0%,CAS号:80-32-0) 德国Dr. Ehrenstofer GmbH公司;羟基甲硝唑(纯度99.2%,CAS号:4812-40-2) 德国Witega公司;环丙沙星(纯度98.0%,CAS号:85721-33-1) 加拿大TRC公司;交沙霉素(纯度100%,CAS号:16846-24-5)上海安普公司。
乙腈、甲醇(均为色谱纯) 美国Thermo Fisher公司;甲酸(色谱纯) 德国CNW Technology GmbH公司;QuEChERS提取管(内含4 g无水硫酸钠和1 g无水氯化钠) 美国安捷伦公司;实验用水为Milli-Q制备的超纯水。
1.2 仪器与设备
Acquity I-class UPLC超高效液相色谱系统、Xevo TQ-S三重四极杆质谱仪(配有电喷雾离子源及Masslynx 4.1 SCN803软件系统) 美国Waters公司;Milli-Q纯水仪 美国Millipore公司;3K18高速冷冻离心机 美国Sigma公司。
1.3 方法
1.3.1 标准溶液的配制
各标准品于10 mL棕色容量瓶中用甲醇溶解,并定容到刻度,配制成1 000 μg/mL的标准储备液,转入棕色样品瓶中于-20 ℃保存。
1.3.2 样品前处理
样品经处理均质后,称取5.00 g样品于离心管中,加入10 mL水和10 mL乙腈,涡旋振荡3 min至充分混匀,超声5 min后,加入QuEChERS粉末剧烈振荡1 min,于4 ℃、10 000 r/min离心5 min,取出上清液5 mL至收集管中,室温条件下氮气吹至近干,0.1%甲酸溶液-甲醇(9∶1,V/V)1 mL复溶,过0.22 μm滤膜,待仪器分析。
1.3.3 色谱条件
色谱柱:Waters Acquity UPLC BEH C18(100 mm×2.1 mm,1.7 μm);流速0.45 mL/min;柱温45 ℃;流动相:A为甲醇,B为0.1%甲酸溶液;梯度洗脱条件:0~0.25 min、98% A,0.25~12.25 min、98%~1% A,12.25~13.00 min、1% A,13.00~13.01 min、1%~98% A,13.01~17.00 min、98% A;进样量10 μL,进样温度10 ℃。
1.3.4 质谱条件
电喷雾离子源;毛细管电压0.80 kV;离子源温度150 ℃;锥孔电压40.0 V;锥孔气流量150 L/h;脱溶剂气温度450 ℃;脱溶剂气流量800 L/h。
2.1 前处理方法的优化
2.1.1 提取溶剂的优化
考虑到51 种抗生素类药物的快速筛查需要通用、快速、回收率优化的前处理方法,本研究考察的前处理方法需要均能有效净化基质中的干扰。选取总体回收率较差的四环素、青霉素V、红霉素、培氟沙星4 种化合物作为依据,样品在相同加标量5 μg/kg的情况下,分别考察乙腈、10%酸化乙腈(量取10 mL甲酸用乙腈定容至100 mL)、乙酸乙酯、乙腈-乙酸乙酯(1∶1,V/V)不同提取液的回收率,如图1所示。使用乙腈作为提取溶液时,青霉素V、红霉素、培氟沙星均可以达到较好和较为稳定的回收率,四环素的回收率也能达到70%以上。

图1 不同提取溶剂的回收率
Fig. 1 Recoveries of antibiotics with different extraction solvents
2.1.2 净化条件的优化
样品在使用相同提取试剂和相同加标量5 μg/kg的条件下,以总体回收率较差的四环素、青霉素V、红霉素、培氟沙星4 种化合物作为依据,分别考察QuEChERS 5982-0032(4 g Na2SO4、1g NaCl)、QuEChERS 5982-5550(4 g MgSO4、1 g NaCl)、QuEChERS 5982-5650(4 g MgSO4、1 g NaCl、1 g柠檬酸钠、0.5 g三水合二柠檬酸二钠)、5 g NaCl共4 种净化条件的效果比较,如图2所示。
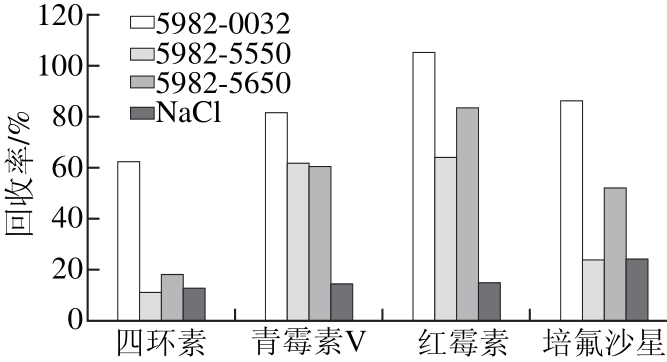
图2 不同净化条件的净化效果比较
Fig. 2 Comparison of effi ciency of different clean-up methods
如图2所示,样品使用QuEChERS 5982-0032净化处理后,回收率明显高于其他3 种,其中NaCl回收率最差,暂不做考虑。由于青霉素类和大环内酯类抗生素类药物热稳定性较差[22-24],前处理时加入QuEChERS 5982-5550和QuEChERS 5982-5650后有明显的发热现象,因此影响了青霉素V和红霉素的回收;而QuEChERS 5982-5550和QuEChERS 5982-5650中的Mg2+具有配位能力易与四环素族发生螯合作用从而影响提取回收率,也就体现了含Na+的QuEChERS 5982-0032较好提取效果的优势。
综上所述,使用乙腈作为提取溶剂,选择QuEChERS 5982-0032作为净化方法,可以达到51 种抗生素类药物较好的前处理提取净化效果,目标化合物的回收率均在60%以上。2.2 色谱-质谱分析
2.2.1 色谱条件的优化
由于51 种抗生素类化合物的电离方式均为正离子模式,在水相中加入一定比例的酸可以促进电离,所以选用较为常用的0.1%甲酸溶液作为流动相[25-27]。然后比较色谱分析方法中常用的甲醇和乙腈分别作为有机相时,对51 种抗生素类化合物色谱分离的影响。当使用乙腈作为有机相时,磺胺类化合物的响应和分离度明显降低,个别峰的峰形拖尾,导致化合物之间的干扰严重,灵敏度降低,尤其是对同分异构体的影响尤为明显, 51 种抗生素类化合物的总离子流色谱图见图3,3 种同分异构体磺胺甲氧哒嗪、磺胺间甲氧嘧啶、磺胺对甲氧嘧啶在有机相为甲醇时色谱分离图见图4。因此综合考虑,使用0.1%甲酸溶液-甲醇作为流动相体系,用于51 种抗生素类药物的色谱分离。

图3 51 种抗生素类化合物的总离子流色谱图
Fig. 3 Total ion chromatogram of 51 antibiotics

图4 3 种同分异构体的色谱分离图
Fig. 4 Chromatograms of sulfameter, sulfamonomethoxine, and sulfamethoxypyridazine
2.2.2 质谱条件的选择
2.2.2.1 母离子的选择
取100 ng/mL的各化合物标准溶液放在蠕动泵进样器上,设定流动相的速率为0.1 mL/min,蠕动泵流速20 μL/min,混合模式进样,调节毛细管电压、锥孔电压、脱溶剂气的温度、脱溶剂气的流速、锥孔气流速等质谱参数,尽可能得使目标物响应信号达到最高。
2.2.2.2 子离子的选择
使用仪器软件自动调谐功能为每个母离子自动筛选出最佳的锥孔电压和碰撞电压从而得到在该碎裂条件下的2 个子离子。对得到的子离子结合化合物的结构式和碎裂规律[28-30]进行再次分析,以验证仪器自动筛选的子离子功能的准确性。以磺胺甲基嘧啶为例,图5为磺胺甲基嘧啶的结构式和质谱碎裂分析图。磺胺甲基嘧啶母离子为m/z 265.1,仪器自动筛选出的两个子离子为m/z 92和156,满足该化合物碎裂规律。

图5 磺胺甲基嘧啶的结构式及质谱裂解
Fig. 5 Structure and fragmentation pathway of sulfamerazine
将51 种抗生素类药物的色谱及质谱采集参数见表1。
表1 51 种抗生素类药物的色谱及质谱采集参数
Table 1 Chromatogram and mass spectral parameters for 51 antibiotics

2.3 方法学验证
2.3.1 标准曲线的绘制
根据51 种抗生素类药物响应的强弱,配制系列质量浓度的混合标准工作溶液绘制标准曲线,如表2所示,51 种化合物的线性范围为0.5~20 ng/mL,相关系数均大于0.99。
表2 51 种抗生素类药物的线性方程、相关系数、线性范围
Table 2 Linear equations, correlation coeffi cients and linear ranges for 51 antibiotics

2.3.2 方法的检出限和回收率
取空白样品,添加不同系列水平的混合标准溶液,绘制基质加标工作曲线。在基质中加入不同量的混合标准溶液,制成加标阳性样品,进行前处理,将得到的样品上机检测,得到信噪比至少10∶1的目标化合物的最低加标量,即为本方法在基质中的定量限(limit of quantity,LOQ)。取空白基质,添加3 个不同水平的加标量,经过前处理并上机检测,每个水平做6 组平行实验,LOQ、回收率及相对标准偏差结果见表3。
表3 51 种抗生素类药物的方法LOQ、回收率和相对标准偏差
Table 3 LOQs, recoveries and RSDs for the antibiotics

2.4 方法应用
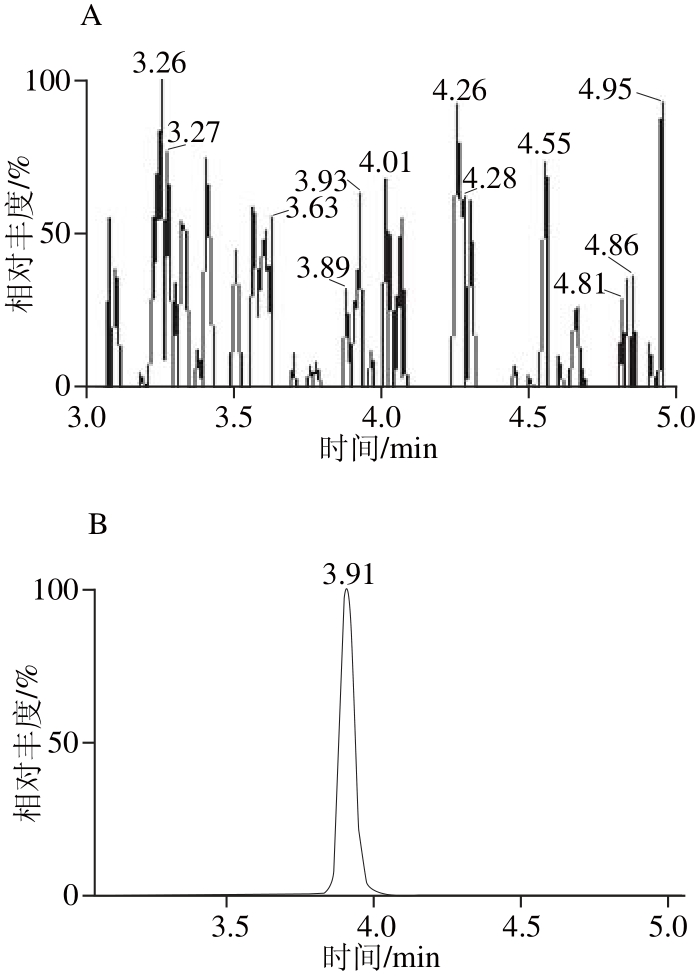
图6 豆芽样品空白(A)和质控样(B)恩诺沙星的色谱图
Fig. 6 Chromatogram of blank sample (A) and enrofl oxacin in quality control sample (B)


图7 豆芽样品空白和质控样土霉素、强力霉素的色谱图
Fig. 7 Chromatogram of blank sample and oxytetracycline and doxycycline in quality control sample

图8 豆芽样品空白和质控样磺胺嘧啶、磺胺吡啶的色谱图
Fig. 8 Chromatograms of blank sample and sulfadiazine and sulfapyridine in quality control sample
应用本方法对随机抽取的豆芽样品进行了筛查测定,共计50 个样品,同时做3 个质控样品。色谱图见图6~8。在3个质控样品中分别检出恩诺沙星含量为24.8 μg/kg,强力霉素含量为35.6 μg/kg,土霉素含量为34.4 μg/kg,磺胺嘧啶含量为6.7 μg/kg,磺胺吡啶含量为26.9 μg/kg,其余样品均未检出。
本实验利用QuEChERS净化手段,结合超高效液相色谱-串联四极杆质谱仪研究建立豆芽中磺胺类、喹诺酮类、林可酰胺类、大环内酯类、β-内酰胺类、四环素族、硝基咪唑类7 类共51 种抗生素类药物的快速筛查方法,该方法准确、快捷,并且进行了方法学验证应用。适合用于豆芽食品中安全风险突发事件的快速应急处置工作。
参考文献:
[1] 马坤明. “毒豆芽”溯源[J]. 农产品市场周刊, 2013(15)∶ 42-43.DOI∶10.3969/j.issn.1009-8070.2013.15.012.
[2] 京华. 北京某批发市场现毒豆芽∶ 含非法添加剂[J]. 广西质量监督导报, 2014(11)∶ 36. DOI∶10.3969/j.issn.1009-6310.2014.11.010.
[3] 王康友. 专家盘点2014年食品安全关键词[C]//科学媒介中心2015年推送文章全集(上). 北京∶ 中国科普研究所科学媒介中心, 2016∶ 20-28.
[4] 北京市食品药品监督管理局. 北京市食品药品监督管理局关于印发《工业化豆芽生产许可审查细则(2014版)》的通知[N]. 北京市人民政府公报, 2014-08-27(39).
[5] 吕世翔, 陈凯新, 李家磊, 等. 国内典型食品安全案例归类分析及对策[J]. 中国食物与营养, 2012, 18(11)∶ 16-19. DOI∶10.3969/j.issn.1006-9577.2012.11.005.
[6] 郝凤桐. “毒豆芽”及其危害治理[J]. 职业卫生与应急救援, 2013,31(5)∶ 285. DOI∶10.16369/j.oher.issn.
[7] 顾志翔, 庞昊. “毒豆芽”何时才能根除[N]. 检察日报, 2011-06-29(004).
[8] PRUDEN A, PEI R T, STORTEBOOM H, et al. Antibiotic resistance genes as emerging contaminants∶studies in northern Colorado[J].Environmental Science & Technology, 2006, 40(23)∶ 7445-7450.DOI∶10.1021/es0604131.
[9] ELENA M, CARMEN G, SIGRID S, et al. Environmental monitoring study of selected veterinary antibiotics in animal manure and soils in Austria[J]. Environmental Pollution, 2007, 148(2)∶ 570-579.DOI∶10.1016/j.envpol.2006.11.035.
[10] 胡洪营, 王超, 郭美婷. 药品和个人护理用品(PPCPs)对环境的污染现状于研究进展[J]. 生态环境, 2005, 14(6)∶ 947-952. DOI∶10.16258/j.cnki.1674-5906.2005.06.032.
[11] 郭黎明, 朱奎, 江海洋, 等. 超高效液相色谱-串联质谱法同时测定鸡肝中残留的四环素类、磺胺类和喹诺酮类药物[J]. 色谱, 2009,27(4)∶ 412-416. DOI∶10.3321/j.issn∶1000-8713.2009.04.006.
[12] 袁中珍. 动物源性食品中16 种磺胺类药物残留检测[D]. 重庆∶ 重庆医科大学, 2013.
[13] 宁海容, 彭瑛, 金兴良, 等. 牛奶中抗生素检测研究进展[J]. 中国畜牧兽医, 2012(8)∶ 227-230.
[14] 刘春生, 罗海英, 冼燕萍, 等. 超高效液相色谱-串联质谱法测定豆芽中7 种药物残留[J]. 质谱学报, 2014, 35(4)∶ 302-310. DOI∶10.7538/zpxb.youxian.2014.0023.
[15] 靳凤龙. 固相萃取-高效液相色谱法测定豆芽中土霉素的含量[J]. 现代农业科技, 2012(13)∶ 296-297. DOI∶10.3969/j.issn.1007-5739.2012.13.189.
[16] 李彦文, 张艳, 莫测辉, 等. 广州市蔬菜中喹诺酮类抗生素污染特征及健康风险初步研究[J]. 环境科学, 2010, 31(10)∶ 2445-2449.DOI∶10.13227/j.hjkx.2010.10.031.
[17] KUMAR K, GUPTA S C, BAIDOO S K, et al. Antibiotic uptake by plants from soil fertilized with animal manure[J]. Journal of Environmental Quality, 2005, 34(6)∶ 2082-2085. DOI∶10.2134/jep2005.0026.
[18] LILLENBERG M, LITVIN S V, NEI L, et al. Enrofloxacin and ciprofloxacin uptake by plants from soil[J]. Agronomy Research,2010, 8(1)∶ 807-814.
[19] 张致平. 抗生素与抗菌药发展史[J]. 首都医药, 2004(2)∶ 14-16.DOI∶10.3969/j.issn.1005-8257.2004.02.009.
[20] 黄艳芳. 抗生素的分类与应用[J]. 山东医药, 2006, 46(25)∶ 84-85.
[21] 赵子佳, 李晶峰, 姚梦杰, 等. 中国动物源性食品中抗生素残留的分类及检测方法[J]. 吉林中医药, 2016, 36(8)∶ 811-813. DOI∶10.13463/j.cnki.jlzyy.2016.08.017.
[22] 姜力群, 嵇元欣, 刘晶锦, 等. 青霉素类抗生素稳定性影响因素及有关物质测定方法[J]. 药学进展, 2008, 32(2)∶ 62-68.
[23] 李玮. 大环内酯类抗生素热稳定性及分解动力学研究[J]. 药物分析杂志, 2010, 30(8)∶ 1544-1547. DOI∶10.16155/j.0254-1793.2010.08.037.
[24] 薛哲, 李刚, 李少华, 等. β-内酰胺类抗生素对热的稳定性的研究[J]. 江西医学院学报, 2008, 48(4)∶ 42-46. DOI∶10.3969/j.issn.1000-2294.2008.04.013.
[25] 张洁, 严丽娟, 潘晨松. 超高效液相色谱/高分辨飞行时间质谱法同时检测乳制品中19 种抗生素[J]. 色谱, 2012, 30(10)∶ 1031-1036.DOI∶10.3724/SP.J.1123.2012.06026.
[26] 丁丽, 曾邵东, 魏晓奕. 超高效液相色谱-质谱发测定豆芽中多菌灵、2,4二氯苯氧乙酸、恩诺沙星残留[J]. 食品科学, 2014, 35(22)∶69-75. DOI∶10.7506/spkx1002-6630-201422032.
[27] 王培峰, 王凤美, 张鸿伟. 高效液相色谱-四极杆轨道阱高分辨质谱对动物源食品中抗生素类成分的快速筛查[J]. 食品安全质量检测学报, 2014, 12(5)∶ 3769-3777.
[28] 张海燕, 刘鑫, 严华, 等. 天然同位素信息在多级质谱裂解规律解析中的应用∶ 以磺胺类化合物为例[J]. 质谱学报, 2013, 34(5)∶ 300-307.DOI∶10.7538/zpxb.2013.34.05.0300.
[29] 俞振培, 赵亚军, 贺晓然, 等. 喹诺酮衍生物质谱碎裂规律的研究[J].质谱学报, 1996, 17(1)∶ 21-26.
[30] 陈兵, 陈辉, 吴丽阳, 等. N-(喹啉8-基)苯磺酰胺类化合物的合成及其电喷雾质谱裂解途径[J]. 广东药学院学报, 2015, 35(1)∶ 25-30.DOI∶10.3969/j.issn.1006-8783.2015.01.006.
Rapid Screening of 51 Antibiotic Residues in Bean Sprouts b y UPLC-MS/MS
SUN Xiaodong, HAO Jie, MAO Ting, SHI Na, JIANG Jie*
(Beijing Municipal Center for Food Safety Monitoring and Risk Assessment, Beijing 100041, China)
中图分类号:TS207.3
文献标志码:A
文章编号:1002-6630(2017)20-0327-07
引文格式:
孙晓冬, 郝杰, 毛婷, 等. 人工接种温州蜜柑后链格孢霉毒素的产生及分布规律[J]. 食品科学, 2017, 38(20)∶ 327-333.DOI∶10.7506/spkx1002-6630-201720049. http∶//www.spkx.net.cn
SUN Xiaodong, HAO Jie, MAO Ting, et al. Rapid screening of 51 antibiotic residues in bean sprouts by UPLC-MS/MS[J]. Food Science, 2017, 38(20)∶ 327-333. (in Chinese with English abstract) DOI∶10.7506/spkx1002-6630-201720049.http∶//www.spkx.net.cn
收稿日期:2016-11-03
作者简介:孙晓冬(1991—),女,本科,研究方向为食品安全。E-mail:1543757447@qq.com
*通信作者:姜洁(1972—),女,高级工程师,博士,研究方向为分析化学。E-mail:jybjj2004@126.com