赵 健1,范梦蝶1,甄大卫2,赵梦瑶1,肖群飞1,王天泽1,谢建春1,*
(1.北京食品营养与人类健康高精尖创新中心,食品质量与安全北京实验室,北京市食品风味化学重点实验室,北京工商大学,北京 100048;2.太原理工大学化学化工学院,山西 太原 030024)
摘 要:设计“氧化鸡脂-谷胱甘肽-葡萄糖”模型反应,于131 ℃和pH 6.5条件下反应5 h。采用溶剂辅助蒸发法萃取反应产物中的挥发性风味物质,并采用气相色谱-质谱仪、稀释法嗅闻分析。基于质谱、保留指数、气味特征、标准品,鉴定出89 种化合物;其中67 种化合物具有气味活性,主要为含硫化合物和醛类化合物。鉴定出由脂肪氧化降解与美拉德反应相互作用形成的带有烷基链的化合物10 种,包括2-戊基噻吩、2-庚基噻吩、2-戊基吡啶等,多数具有气味活性。除了2-甲基-3-呋喃硫醇、糠硫醇等产生于美拉德反应的化合物外,带烷基链的2-庚基噻吩、2-甲基吡啶、2-乙基吡啶等也具有较高的稀释因子(Log3FD≥5),表明在“氧化鸡脂-谷胱甘肽-葡萄糖”体系中,脂肪氧化降解与“谷胱甘肽”美拉德反应相互作用对肉香风味形成具有较大贡献,研究结果对“脂肪控制氧化-热反应”制备肉味香精有指导意义。
关键词:氧化鸡脂;谷胱甘肽;肉香味;香气活性化合物;美拉德反应;脂质氧化降解
肉香味形成反应主要包括美拉德反应、脂质氧化降解以及美拉德反应与脂质氧化降解相互作用[1]。熟肉及其制品中检测到的众多香味物质,在基于“半胱氨酸”的模式反应体系中已检测到,从而使肉香味的形成机制不断被揭示[1]。如在“半胱氨酸-核糖”[2]和“半胱氨酸-木糖”[3]反应体系中,鉴定出2-糠硫醇、2-甲基-3-呋喃硫醇、3-巯基-2-戊酮、2-甲基噻吩等含硫肉香物质。在“半胱氨酸-核糖-卵磷脂”[4]及“亚油酸或亚麻酸-半胱氨酸-核糖”[5]反应体系中,鉴定出脂肪氧化降解与美拉德反应发生作用产生的2-戊基噻喃、2-戊基噻吩、2-乙基吡啶、2-乙基-3-噻吩醛等带有烷基链的化合物。本课题组为研究热反应肉味香精制备中,调控氧化脂肪在肉香味形成中的作用,设计“半胱氨酸-葡萄糖-氧化鸡脂”反应体系,从中鉴定出脂肪氧化降解产物参与美拉德反应形成的带有烷基侧链的2-庚基噻吩、2,5-二丁基噻吩等重要风味物质[6]。
与半胱氨酸类似,谷胱甘肽也为重要肉香前体。有关“谷胱甘肽”模式反应体系的研究还主要限于“谷胱甘肽-还原糖”体系[7-8],而对脂质氧化存在条件下“谷胱甘肽-还原糖”反应体系的风味物质研究却鲜有报道。为此,本实验在前期对“半胱氨酸-葡萄糖-氧化鸡脂”反应体系研究基础上,设计“谷胱甘肽-葡萄糖-氧化鸡脂”反应体系,采用气相色谱-质谱(gas chromatographymass spectrometry,GC-MS)联机、香气提取稀释分析(aroma extract dilution analysis,AEDA)法和气相色谱-嗅闻(gas chromatography-olfactometry,GC-O)分析鉴定该反应体系产生的风味物质,并探讨风味化合物形成机制。研究结果对进一步认识肉香味形成机理,及完善“脂肪控制氧化-热反应”制备肉味香精工艺具有重要意义。
1.1 材料与试剂
L-谷胱甘肽、D-(+)-葡萄糖、C5~C29正构烷烃(均为色谱纯),二氯甲烷、无水Na2SO4(均为分析纯) 国药集团化学试剂北京有限公司;香料标准品:2-甲基-3-呋喃硫醇(纯度95%)、2-乙基噻吩(纯度98%)、糠硫醇(纯度98%)、2-甲基噻吩(纯度98%)、3-甲基噻吩(纯度99%)、2,5-二甲基噻吩(纯度98%)、四氢噻吩-3-酮(纯度98%)、2-噻吩硫醇(纯度97%)、2-乙酰基噻唑(纯度99%)、2-乙酰基噻吩(纯度99%)、5-甲基-2-噻吩醛(纯度98%)、3-甲基-2-噻吩醛(纯度97%)、2-戊基噻吩(纯度93%)、糠醇(纯度90%)、糠醛(纯度95%)、2-乙酰基呋喃(纯度95%)、2,5-二甲基-4-羟基-3(2H)-呋喃酮(纯度95%)、2-戊基呋喃(纯度98%)、戊醛(纯度95%)、己醛(纯度95%)、庚醛(纯度95%)、(E)-2-庚烯醛(纯度95%)、辛醛(纯度95%)、(E)-2-辛烯醛(纯度95%)、壬醛(纯度95%)、(E)-2-壬烯醛(纯度97%)、癸醛(纯度93%)、(E,E)-2,4-壬二烯醛(纯度95%)、(E)-2-癸烯醛(纯度93%)、(E,E)-2,4-癸二烯醛(纯度90%)、2-十一碳烯醛(纯度93%)、1-丁醇(纯度99.5%)、1-戊醇(纯度98%)、1-己醇(纯度98%)、乙偶姻(纯度95%)、2-庚酮(纯度98%)、1-辛烯-3-醇(纯度98%)、γ-己内酯(纯度95%)、γ-壬内酯(纯度90%) 北京百灵威化学有限公司。
氧化鸡脂,氧化指标为过氧化值为389 meq/kg,酸值为2.85 mg,其制备方法参照文献[6]。在装有电动搅拌器、回流冷凝管和温度计的2 000 m L四口烧瓶中加入500 g精炼鸡脂,不断搅拌通空气,空气流量为0.30m3/(h·kg)脂肪,维持温度130 ℃反应3 h,得样品。
1.2 仪器与设备
100 m L耐压瓶 北京欣维尔玻璃仪器有限公司;Parallel synthesis Poly-BLOCK4反应器 英国HEL公司;7890B-5975C型GC-MS联用仪、7890A GC 美国Agilent公司;气味嗅闻装置 美国DATU Inc.公司;N-EVAP-12干浴氮吹仪 美国Organomation Associates公司。
1.3 方法
1.3.1 模型反应
100 m L耐压密封管中,分别加入30 m L磷酸二氢钠-氢氧化钠缓冲溶液(0.2 mol/L,pH 6.5)、谷胱甘肽0.553 g(1.8 mmol)、葡萄糖0.324 g(1.8 mmol)、氧化鸡脂0.300 g(质量分数1%),放入平行反应器中。在温度131 ℃,磁力搅拌转速700 r/m in条件下,反应5 h。反应结束后,迅速用自来水冷却。反应液呈橘黄色,具有油脂和葱蒜香的气味。
每次实验平行做4 管反应液,将4 管反应液合并后作为一个样品,进行如下处理和分析。共2 次平行实验。
1.3.2 溶剂辅助蒸发(so lven t assisted f lavo r evaporation,SAFE)萃取
4 管合并得到的反应液,用120 m L二氯甲烷等体积萃取3 次,萃取液合并,按照文献[9]方法SAFE装置处理。SAFE处理时,恒温水槽温度及蒸馏头夹层回流水温度均为26 ℃,系统内压力10-5Pa,液氮冷凝。
收集馏出液,无水Na2SO4过夜干燥。Vigreux柱浓缩至1.5 m L,再氮吹浓缩至0.4 g左右,放入冰箱-18 ℃保存,待分析。
1.3.3 GC-MS分析
GC条件:DB-Wax色谱柱(30 m×0.25 mm,0.25 μm);升温程序:起始柱温35 ℃,保持2 m in,2 ℃/m in升至60 ℃,保持2 m in,最后4 ℃/m in升至230 ℃;载气(He),流速1 m L/m in;进样口温度250 ℃;不分流模式;进样1 μL。
MS条件:电子电离源;电子能量70 eV;离子源温度230 ℃;四极杆温度150 ℃;辅助加热线温度250 ℃;全扫描模式,质量扫描范围33~450 u;溶剂延迟时间4.7 min。
在相同GC-MS条件下进样C5~C23正构烷烃,计算保留指数(retention index,RI)。
式中:tn和tn+1分别为碳数为n、n+1的正构烷烃的保留时间/min;ti为在tn和tn+1之间的第i个化合物的保留时间/min。
1.3.4 GC-O分析
GC-O由配有氢火焰离子化检测器的7890A GC仪和嗅闻装置组成。HP-5毛细管柱(30 m×250 μm,0.25 μm);进样口温度250 ℃;升温程序:起始柱温40 ℃,以5 ℃/m in升到280 ℃;载气为氮气,流速1.0 m L/m in;不分流模式;进样1 μL。
采用AEDA法进行GC-O分析。样品用二氯甲烷按1∶3、1∶9、1∶27等逐级稀释并嗅闻分析,直到嗅闻不到任何气味物质时停止。每种气味化合物的最高稀释倍数即为稀释(flavor dilution,FD)因子。嗅闻过程中记录嗅闻到的气味特征,共3 名评价员完成,取其平均值作为结果。
本实验采用较为温和的SAFE方法萃取风味物质、GC-MS分析,并进一步采用AE DA法GC-O分析,然后基于质谱、RI、气味特征、标准品鉴定化合物,确保鉴定结果的准确性。根据AEDA法GC-O分析筛选出的香气活性化合物及其FD因子大小,判断化合物对总体香气的贡献及贡献大小。
所用氧化鸡脂是在通空气加热条件下将鸡脂氧化后制备,其含有未氧化的甘油酯、甘油酯氢过氧化物、小分子醛、酮等脂肪氧化降解产物[2]。“氧化鸡脂-谷胱甘肽-葡萄糖”反应体系中的风味物质,由产生于美拉德反应或脂肪氧化降解产物参与美拉德反应和产生于脂肪氧化降解的化合物构成,鉴定出89 种个化合物,其中67 种个化合物具有气味活性。一些化合物如甲硫醇、2,5-甲基-2,4-二羟基-3(2H)-噻吩酮等,虽在GC-O分析中检测到,但在GC-MS中却未检测到,可能是由于相对含量低于GC-MS联机检测限造成。
2.1 美拉德反应及脂肪氧化降解产物参与美拉德反应形成的化合物
表1 美拉德反应及脂肪氧化降解产物参与美拉德反应形成的化合物
Tab le 1 Volatile com pounds generated from M aillard reaction w ith and w ithout the presence of lipid oxidation and degradation products
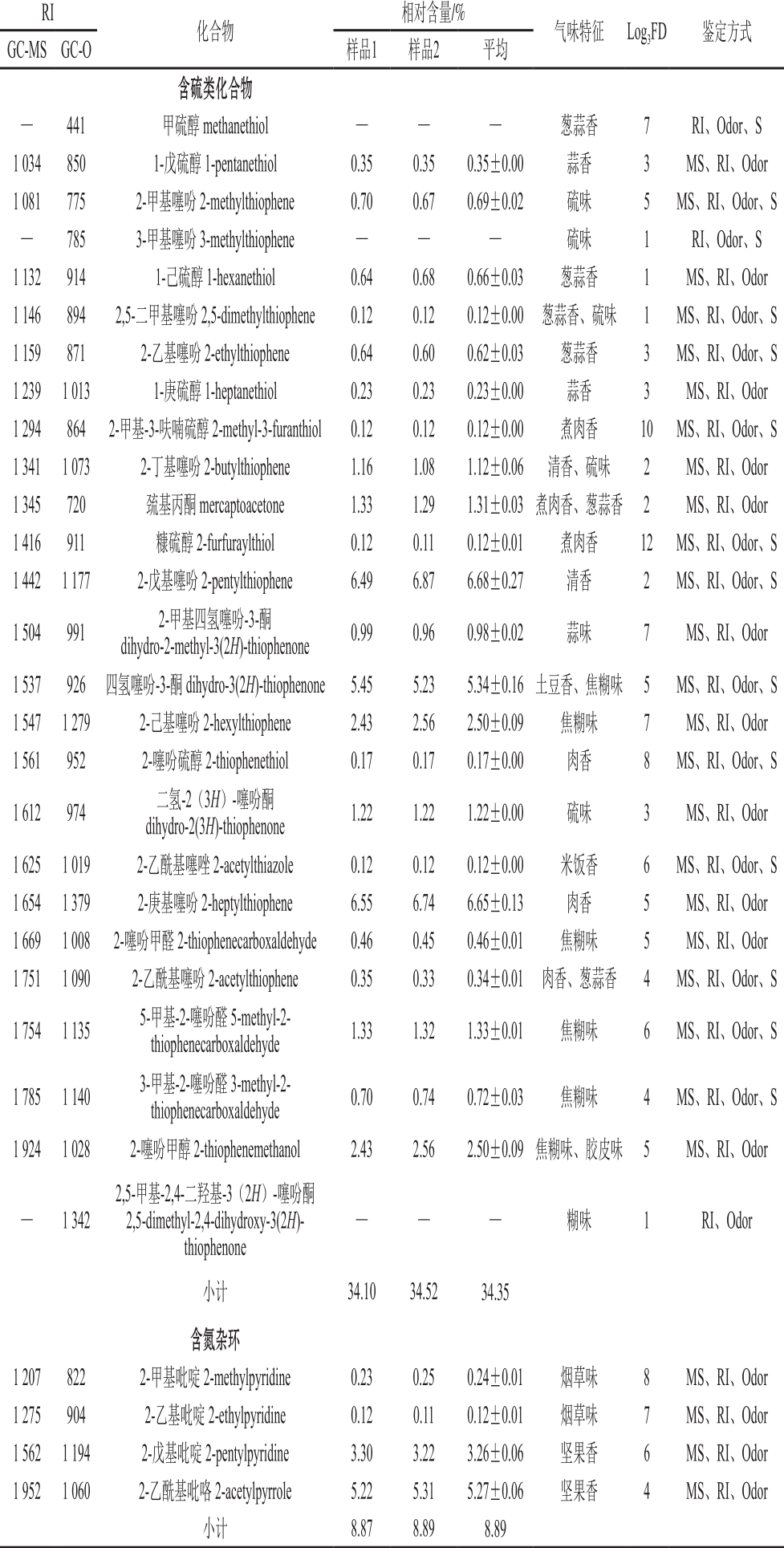
表1共鉴定出41 种化合物,相对含量较高(>5%)的为1-羟基-2-丙酮、2,3-二氢-3,5-二羟基-6-甲基-4H-吡喃-4-酮、糠醇、2-乙酰基呋喃、2-戊基噻吩、2-庚基噻吩、四氢噻吩-3-酮、2-乙酰基吡咯。表1中含硫化合物的数量最多(硫醇8 种、噻吩17 种、噻唑1 种)、其次为含氧杂环及醇酮类(11 种),而含氮杂环最少(烷基吡啶3 种、吡咯1 种)。但从相对含量看,含氧杂环及醇酮类相对含量最高,其次是含硫化合物和含氮杂环。
含氧杂环化合物和醇酮,是美拉德反应的重要中间产物,主要来源于糖的降解,在许多“还原糖-氨基酸”美拉德反应体系中可检测到[11-12]。另外,Watanabe等[13]在80 ℃加热的牛肉中,也发现了2,3-二氢-3,5-二羟基-6-甲基-4H-吡喃-4-酮的存在。由表1可知,尽管鉴定出的含氧杂环化合物和醇酮类相对含量高,但除了2-乙酰基呋喃、乙偶姻和糠醇外,其他FD因子都较小(Log3FD<3)。尤其相对含量大于12%的3 种化合物中,糠醇的FD因子(Log3FD)仅为3,1-羟基-2-丙酮、2,3-二氢-3,5-二羟基-6-甲基-4H-吡喃-4-酮却未检测到气味活性,这是因为含氧杂环和醇酮的气味阈值较高造成。据报道[14],糠醇在水体系中的气味阈值为20 mg/L。
含硫类化合物对肉香味有重要贡献[1]。表1鉴定出较多的含硫化合物,且多数的FD因子较大(Log3FD≥3)。与“半胱氨酸-还原糖”反应体系类似[15],本实验从“谷胱甘肽-葡萄糖-氧化鸡脂”反应体系中鉴定出的主要含硫化合物也为噻吩类,相对含量最高的为2-戊基噻吩,其次为2-庚基噻吩和四氢噻吩-3-酮。表1中,四氢噻吩-3-酮、2-噻吩甲醛等多数含硫化合物应来源于“谷胱甘肽-葡萄糖”间的美拉德反应。Lee[8]和Zhang Yuangang[15]等在“谷胱甘肽-葡萄糖”的体系中曾检测到2-甲基噻吩、5-甲基-2-噻吩醛、3-甲基-2-噻吩醛等噻吩类化合物。此外,Elmore等[16]从炖煮牛肉中也鉴定出2-乙酰基噻吩、2-噻吩醛、四氢噻吩-3-酮等噻吩类化合物。据报道[7],在加热条件下,谷胱甘肽可先断裂成谷氨酸和甘氨酸-半胱氨酸(Gly-Cys)二肽,Gly-Cys二肽再进一步断裂释放出半胱氨酸,半胱氨酸与还原糖发生反应则产生含硫化合物。
续表1

注:RI为DB-Wax色谱柱上的GC-MS保留指数或HP-5色谱柱上嗅闻保留指数;相对含量由表1中化合物面积归一化得到;样品1和样品2分别为2次平行实验制备,各由4 管反应液合并得到;—.未检测到。鉴定方式中MS为通过检索NIST 2011谱库鉴定,RI为保留指数鉴定,Odor为气味特征鉴定,S为与标准品比对鉴定。表2同。
表1中GC-O检测到的FD因子较大的(Log3FD≥5)含硫化合物为2-甲基-3-呋喃硫醇、糠硫醇、2-噻吩硫醇、甲硫醇等,均为硫醇类化合物。这与本实验模型反应是在弱酸性pH值、模拟煮肉条件下进行有关。硫醇对煮肉香气有重要贡献,本课题组研究炖煮猪肉[17]、鸡肉[18]和羊肉[19]的风味时,发现2-甲基-3-呋喃硫醇、糠硫醇、2-噻吩硫醇、甲硫醇等硫醇类化合物均是其关键香气成分。在较低pH值(酸性)发生美拉德反应,糠硫醇和2-噻吩硫醇等具有煮肉香气的硫醇类化合物易于形成[20]。Hofmann[21-22]等在弱酸性条件下进行“半胱氨酸-核糖”和“半胱氨酸与鼠李糖”反应,采用AEDA法GC-O分析鉴定出的关键肉香化合物也为糠硫醇、2-甲基-3-呋喃硫醇等硫醇类化合物。
本实验鉴定出的1-戊硫醇、2-戊基噻吩等带有烷基链的硫醇和噻吩类化合物,在已有的关于“谷胱甘肽-还原糖”模型反应文献报道中并未发现[7-8,15],这些化合物应是脂肪氧化降解产物参与美拉德反应形成。在Zhang Yuangang等[23]设计的“谷胱甘肽+2,4-癸二烯醛”pH 7.5和180 ℃反应体系中,也曾鉴定出多种具有烷基链的噻吩、噻啶和多硫烷类化合物如2-己基噻吩、甲基戊基噻吩、3-甲基-5-戊基-1,2,4,5-四硫烷等。另外,在脂质氧化存在的“半胱氨酸-还原糖”反应体系中,带有烷基链的含硫化合物常被检测到[4-6]。如图1所示,表1中检测到的带有烷基链化合物,2-戊基噻吩、2-己基噻吩、1-戊硫醇、1-庚硫醇等,可分别由2,4-壬二烯醛、2,4-癸二烯醛、戊醛、庚醛等脂肪氧化降解产物与硫化氢反应生成[1,24-25]。它们的FD因子比较高(Log3FD>3),表明对总体香气有较大贡献。Timón等[26]从煎培根肉和小腰肉中曾检测到2-丁基噻吩、2-戊基噻吩和2-(乙基丁基)噻吩。Elmore等[27]采用固相微萃取-GC-MS联机,在加热的猪肉中也检测到2-戊基噻吩。由本实验“谷胱甘肽-葡萄糖-氧化鸡脂”反应体系的风味分析结果可知,从肉中检测到的带有烷基链的含硫肉香味物质[24-25],可由脂肪氧化降解产物参与“半胱氨酸-还原糖”美拉德反应产生,还可由其参与“谷胱甘肽-还原糖”的美拉德反应产生。
含氮杂环化合物仅检测到4 种(3 种烷基吡啶,1 种吡咯),这也与本实验模拟了煮肉条件有关。在高温烤肉条件下,发生的美拉德反应易于生成含氮杂环化合物[1]。与测定的烷基噻吩类似,3 种烷基吡啶主要来源于脂肪氧化降解产物参与美拉德反应形成[1,10]。如图1所示,2,4-庚二烯醛、2,4-癸二烯醛与氨反应可形成2-乙基吡啶和2-戊基吡啶。
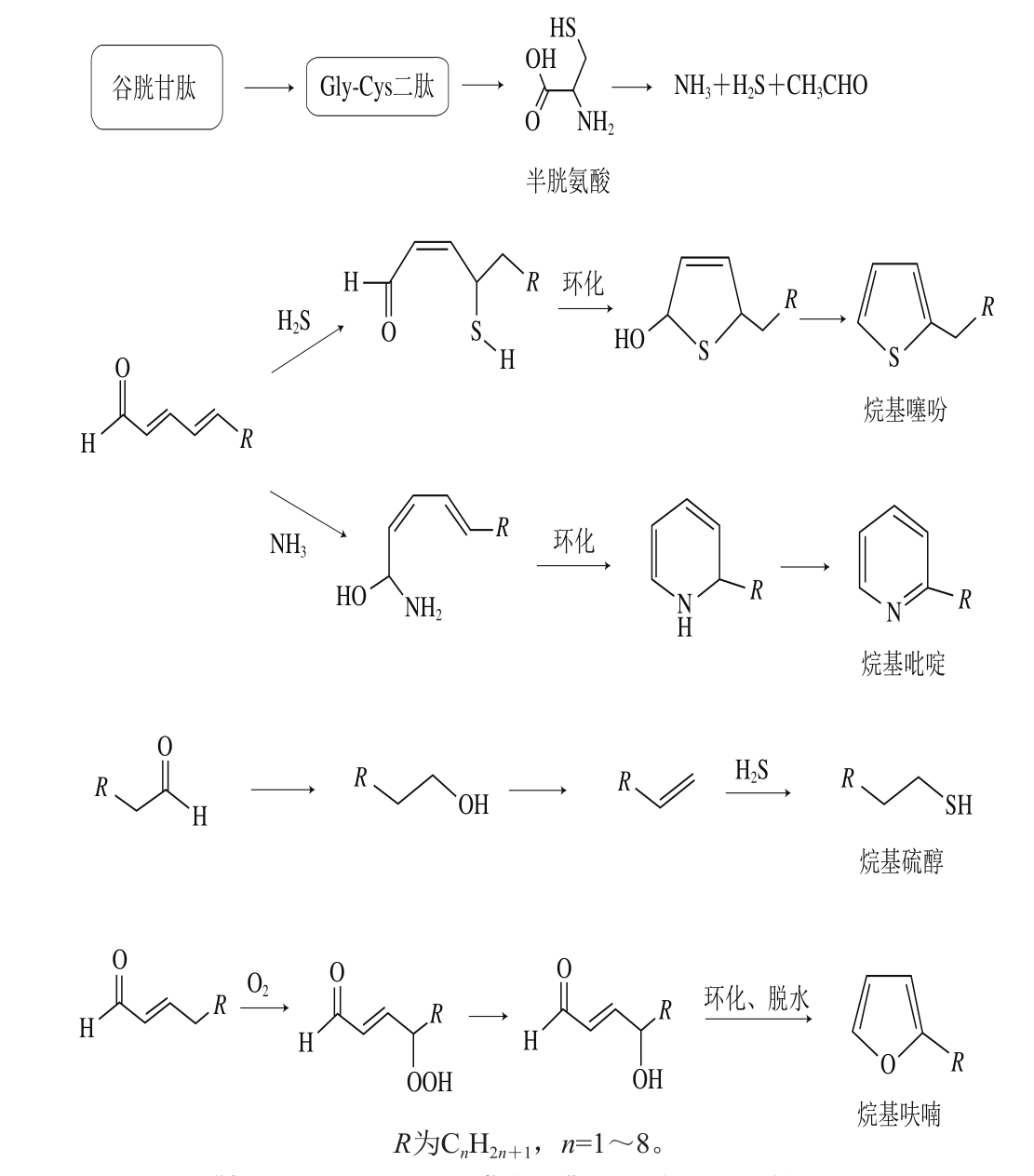
图1 “氧化鸡脂-谷胱甘肽-葡萄糖”体系中烷基链的噻吩、吡啶、硫醇和呋喃类化合物的可能生成途径
Fig. 1 Possib le reaction pathways for formation of alkyl-chain thiophenes, thiols, pyridines, and furans in the reaction system
2.2 脂肪氧化降解形成的化合物
表2 来源于氧化鸡脂的脂肪氧化降解化合物
Table 2 Volatile com pounds derived from lipid oxidization and degradation in chicken fat

续表2

由表2可知,检测到大量脂肪族化合物,包括醛类(15 种)、醇类(8 种)、酮类(4 种)、呋喃类(5 种)、酸类(8 种)、酯类(5 种)、烃类(3 种)。从相对含量上来看,醛类相对含量最高,其次为醇类、呋喃类,根据前期对氧化鸡脂组成[10]及氧化鸡脂添加于“半胱氨酸-葡糖糖”模型反应体系的挥发性成分研究[6],可知这些化合物应来源于氧化鸡脂本身或美拉德反应存在条件下氧化鸡脂进一步发生反应。
醛类化合物中,己醛、壬醛、辛醛等饱和醛的相对含量较高,而(E)-2-庚烯醛、(E,E)-2,4-癸二烯醛等不饱和醛的相对含量较低。这是因为不饱和醛反应活性高,易于参与美拉德反应造成。如2.1节所述,在美拉德反应存在条件下,2-庚烯醛、2,4-癸二烯醛等不饱和醛可与硫化氢或氨反应生成如带有烷基侧链的噻吩、硫醇或吡啶类化合物。
在美拉德反应存在条件下,检测到的来源于脂肪氧化的醇类化合物和烷基呋喃类化合物一般也较高[6,28]。对于醇类化合物而言,这是因为受到具有还原性的美拉德反应产物影响[11,24],使氧化脂肪中的醛类化合物还原成醇,及氧化脂肪中的甘油酯氢过氧化物也会改变降解途径生成具有还原性的醇。而烷基呋喃类化合物,可由α,β-不饱和醛在氨基酸或肽等含氨基化合物催化条件下环化生成[23,29]。如图1所示,2-壬烯醛、2-十一烯醛、2-庚烯醛环化可形成2-戊基呋喃、2-庚基呋喃和2-丁基呋喃。
总体上,表2的脂肪氧化降解产物中,检测到的FD因子较高的主要是醛类化合物,如壬醛、(E,E)-2,4-癸二烯醛、(E)-2-壬烯醛、(E)-2-癸烯醛、(E)-2-辛烯醛等。此外,醇类化合物中1-辛烯-3-醇(Log3FD=6)的FD因子也较高。这与烤小香猪肉[29]、炖煮猪后腿肉汤[17]、炖煮鸡胸肉[18]、炖煮羊肉[19]等肉风味分析的报道相一致。同时,文献中(E,E)-2,4-癸二烯醛、壬醛、己醛等醛类物质和1-辛烯-3-醇也为关键的香气活性物质。
本实验设计了“谷胱甘肽-葡萄糖-氧化鸡脂”反应体系,在模拟炖煮肉条件下进行热反应。采用SAFE结合GC-MS联机、GC-O鉴定出89 种化合物。相对含量较高的为1-羟基-2-丙酮、2,3-二氢-3,5-二羟基-6-甲基-4H-吡喃-4-酮、糠醇、2-乙酰基呋喃、2-戊基噻吩、2-庚基噻吩、2-戊基呋喃、己酸、己醛、1-戊醇、壬醛。具有气味活性且FD因子较大的主要为含硫化合物和脂肪醛,如2-甲基-3-呋喃硫醇、糠硫醇、壬醛、(E,E)-2,4-癸二烯醛等,它们分别来源于美拉德反应和脂肪氧化降解反应。另外,还鉴定出脂肪氧化降解与美拉德反应相互作用形成的带有烷基链的硫醇、噻吩、吡啶和呋喃类化合物。其中2-己基噻吩、2-乙基吡啶、2-戊基吡啶、2-庚基噻吩等具有较大的FD因子,表明脂质氧化产物与谷胱甘肽的美拉德反应相互作用,对肉香味形成具有较大贡献。
参考文献:
[1] MOTTRAM D S. Flavour formation in meat and meat products: a review[J]. Food Chem istry, 1998, 62(4): 415-424. DOI:10.1016/S0308-8146(98)00076-4.
[2] CERNY C, DAVIDEK T. Formation of aroma compounds from ribose and cysteine during the Maillard reaction[J]. Journal of Agricultural &Food Chem istry, 2003, 51(9): 2714-2721. DOI:10.1021/jf026123f.
[3] CERNY C. Origin of carbons in sulfur-containing aroma compounds from the Maillard reaction of xylose, cysteine and thiam ine[J]. LWTFood Science and Technology, 2007, 40(8): 1309-1315. DOI:10.1016/j.lw t.2006.09.008.
[4] MOTTRAM D S, WHITFIELD F B. Maillard-lipid interactions in nonaqueous systems: volatiles from the reaction of cysteine and ribose w ith phosphatidylcholine[J]. Journal of Agricultural & Food Chemistry, 1995, 43(5): 1302-1306. DOI:10.1021/jf00053a033.
[5] ELMORE J S, CAMPO M M, ENSER M, et al. Effect of lipid composition on meat-like model systems containing cysteine, ribose,and polyunsaturated fatty acids[J]. Journal of Agricultural & Food Chemistry, 2002, 50(5): 1126-1132. DOI:10.1021/jf0108718.
[6] YANG Z, XIE J, ZHANG L, et al. Aromatic effect of fat and oxidized fat on a meat-like model reaction system of cysteine and glucose[J]. Flavour &Fragrance Journal, 2015, 30(4): 320-329. DOI:10.1002/ffj.3248.
[7] WANG R, YANG C, SONG H. Key meat flavour com pounds formation mechanism in a glutathione-xylose M aillard reaction[J].Food Chem istry, 2012, 131(1): 280-285. DO I:10.1016/j.foodchem.2011.08.079.
[8] LEE S M, JO Y J, K IM Y S. Investigation of the aroma-active compounds formed in the Maillard reaction between glutathione and reducing sugars[J]. Journal of Agricultural & Food Chem istry, 2010,58(5): 3116-3124. DOI:10.1021/jf9043327.
[9] ZHAO J, WANG M, XIE J, et al. Volatile flavor constituents in the pork broth of black-pig[J]. Food Chem istry, 2017, 226: 51-60.DOI:10.1016/j.foodchem.2017.01.011.
[10] 曾慧英, 靳林溪, 虞芳妮, 等. 液-质联机分析氧化鸡脂中极性非(难)挥发性组分[J]. 精细化工, 2013, 30(10): 1122-1128.
[11] 朱文辉, 杨柳, 杨红燕, 等. TG-SPME-GC-MS研究谷氨酸和葡萄糖的固相美拉德反应[J]. 食品科学, 2010, 31(11): 91-96.
[12] YU X, ZHAO M, HU J, et al. Influence of pH on the formation and radical scavenging activity of volatile compounds produced by heating glucose w ith histidine/tyrosine[J]. European Food Research and Technology, 2012, 234(2): 333-343. DOI:10.1007/s00217-011-1644-0.
[13] WATANABE A, KAMADA G, IMANARI M, et al. Effect of aging on volatile compounds in cooked beef[J]. Meat Science, 2015, 107:12-19. DOI:10.1016/j.meatsci.2015.04.004.
[14] 苗菁, 苏慧敏, 张敏. 米饭中关键风味化合物的分析[J]. 食品科学,2016, 37(2): 82-86. DOI:10.7506/spkx1002-6630-201602014.
[15] ZHANG Y G, HO C T. Comparison of the volatile compounds formed from the thermal reaction of glucose w ith cysteine and glutathione[J].Journal of Agricultural & Food Chem istry, 1991, 39(4): 760-763.DOI:10.1021/jf00004a029.
[16] ELMORE J S, PAPANTONIOU E, MOTTRAM D S. A comparison of headspace entrainment on tenax w ith solid phase m icroextraction for the analysis of the aroma volatiles of cooked beef[J]. Advances in Experim ental M edicine & B io logy, 2001, 488: 125-132.DOI:10.1007/978-1-4615-1247-9_10.
[17] 王蒙, 侯莉, 曹长春, 等. 清炖猪肉汤香气物质的分析鉴定[J].食品科学, 2015, 36(24): 105-111. DOI:10.7506/spkx1002-6630-201524018.
[18] 梁晶晶, 曹长春, 王蒙, 等. 采用SDE结合SAFE分析炖煮鸡胸肉产生的风味物质[J]. 食品工业科技, 2016, 37(4): 57-67. DOI:10.13386/j.issn1002-0306.2016.04.003.
[19] 赵梦瑶, 赵健, 侯莉, 等. 炖煮羊肉香气物质分析鉴定[J]. 食品工业科技, 2016, 37(19): 284-293. DOI:10.13386/j.issn1002-0306.2016.19.047.
[20] TAI C Y, HO C T. Influence of glutathione oxidation and pH on thermal formation of Maillard-type volatile compounds[J]. Journal o f Agricu ltural & Food Chem istry, 1998, 46(6): 2260-2265.DOI:10.1021/jf971111t.
[21] HOFMANN T, SCHIEBERLE P. Evaluation of the key odorants in a thermally treated solution of ribose and cysteine by aroma extract dilution techniques[J]. Journal of Agricultural & Food Chem istry,1995, 43(8): 2187-2194. DOI:10.1021/jf00056a042.
[22] HOFMANN T, SCHIEBERLE P. Identification of potent aroma com pounds in thermally treated m ixtures of glucose/cysteine and rhamnose/cysteine using aroma extract dilution techniques[J].Journal of Agricultural & Food Chem istry, 1997, 45(3): 898-906.DOI:10.1021/jf960456t.
[23] ZHANG Y G, HO C T. Volatile compounds formed from thermal interaction of 2,4-decadienal w ith cysteine and glutathione[J].Journal of Agricultural & Food Chem istry, 1989, 37(4): 1016-1020.DOI:10.1021/jf00088a044.
[24] 靳林溪, 潘翠芳, 王石, 等. “氧化鸡脂-半胱氨酸”反应体系的肉香味物质及其形成机制[J]. 食品科学, 2011, 32(19): 1-6.
[25] HIDALGO F J, ZAMORA R. Am ino acid degradations produced by lipid oxidation products[J]. Critical Reviews in Food Science and Nutrition, 2016, 56(8): 1242-1252. DOI:10.1080/10408398.2012.761173.
[26] TIMÓN M L, CARRAPISO A I, ÁNGELA J, et al. A study of the aroma of fried bacon and fried pork loin[J]. Journal of the Science of Food & Agriculture, 2004, 84(8): 825-831. DOI:10.1002/jsfa.1740.
[27] ELMORE J S, MOTTRAM D S, HIERRO E. Tw o-fiber solidphase m icroextraction combined w ith gas chromatography-mass spectrometry for the analysis of volatile aroma compounds in cooked pork[J]. Journal of Chromatography A, 2001, 905(1/2): 233-240.DOI:10.1016/S0021-9673(00)00990-0.
[28] FARMER L J, MOTTRAM D S. Interaction of lipid in the maillard reaction betw een cysteine and ribose: the effect of a triglyceride and three phospholipids on the volatile products[J]. Journal of the Science of Food & Agriculture, 1990, 53(4): 505-525. DOI:10.1002/jsfa.2740530409.
[29] ADAMS A, BOUCKAERT C, VAN LANCKER F, et al. Am ino acid catalysis of 2-alkylfuran formation from lipid oxidation-derived α,β-unsaturated aldehydes[J]. Journal of Agricultural & Food Chem istry, 2011, 59(20): 11058-11062. DOI:10.1021/jf202448v.
[30] XIE J C, SUN B G, WANG S B. Volatile fl avor constituents in roasted pork of M ini-pig[J]. Food Science & Technology International, 2008,14(4): 329-340. DOI:10.1016/j.foodchem.2007.12.074.
Identification and Formation Mechanism of Volatile Flavor Compounds from Oxidized Chicken Fat-Glutathione-Glucose Model Reaction System
ZHAO Jian1, FAN Mengdie1, ZHEN Dawei2, ZHAO Mengyao1, XIAO Qunfei1, WANG Tianze1, XIE Jianchun1,*
(1. Beijing Advanced Innovation Center for Food Nutrition and Human Health, Beijing Laboratory for Food Quality and Safety,Beijing Key Laboratory of Flavor Chem istry, Beijing Technology & Business University (BTBU), Beijing 100048, China;2. College of Chemistry and Chemical Engineering, Taiyuan University of Technology, Taiyuan 030024, China)
Abstract:An oxidized chicken fat-glutathione-glucose model reaction system was designed and the reaction was allowed to proceed at 131 ℃ under pH 6.5 for 5 h. Volatile flavor compounds in the reaction products were extracted by solvent assisted flavor evaporation (SAFE) extraction, and analyzed by gas chromatography-mass spectrometry (GC-MS) and gas chromatography-olfactometry (GC-O) combined w ith aroma extract dilution analysis (AEDA). As a result, a total of 89 volatile compounds were identified, 67 of which were revealed to be aroma-active according to their mass spectra, linear retention indices and odor characteristics by co-injection w ith authentic standards. Among them, 10 alkyl-chain compounds were found, including 2-heptylthiophene, 2-pentylthiophene, and 2-pentylpyridine, which were formed by the interaction of lipid oxidation and degradation w ith the Maillard reaction. Besides, the compounds solely generated from the Maillard reaction such as 2-methyl-3-furanthiol and 2-furfurylthiol as well as most alkyl-chain compounds such as 2-heptylthiophene,2-methylpyridine and 2-ethylpyridine had a high dilution factor (Log3FD ≥ 5). Therefore, the interaction of lipid oxidization and degradation w ith the Maillard reaction of glutathione made a considerable contribution to the development of meaty flavor in the reaction system. These research results can provide a useful guidance for the preparation of meaty flavorings through controlled fat oxidization combined w ith thermal reaction.
Key words:oxidized chicken fat; glutathione; meaty flavor; odor-active compounds; Maillard reaction; lipid oxidization and degradation
DOI:10.7506/spkx1002-6630-201722023
中图分类号:TQ656.1
文献标志码:A
文章编号:1002-6630(2017)22-0149-07
收稿日期:2017-04-05
基金项目:国家自然科学基金面上项目(31671895;31371838);北京市自然科学基金面上项目(6172004);“十三五”国家重点研发计划重点专项(2017YFD0400106)
作者简介:赵健(1992—),男,硕士研究生,研究方向为食品风味化学。E-mail:jian3597@163.com
*通信作者:谢建春(1967—),女,教授,博士,研究方向为食品风味化学。E-mail:xjchun@th.btbu.edu.cn
引文格式:
赵健, 范梦蝶, 甄大卫, 等. “氧化鸡脂-谷胱甘肽-葡萄糖”反应体系风味物质鉴定及形成机制[J]. 食品科学, 2017,38(22): 149-155. DOI:10.7506/spkx1002-6630-201722023. http://www.spkx.net.cn
ZHAO Jian, FAN Mengdie, ZHEN Dawei, et al. Identification and formation mechanism of volatile flavor compounds from oxidized chicken fat-glutathione-glucose model reaction system[J]. Food Science, 2017, 38(22): 149-155. (in Chinese w ith English abstract)
DOI:10.7506/spkx1002-6630-201722023. http://www.spkx.net.cn