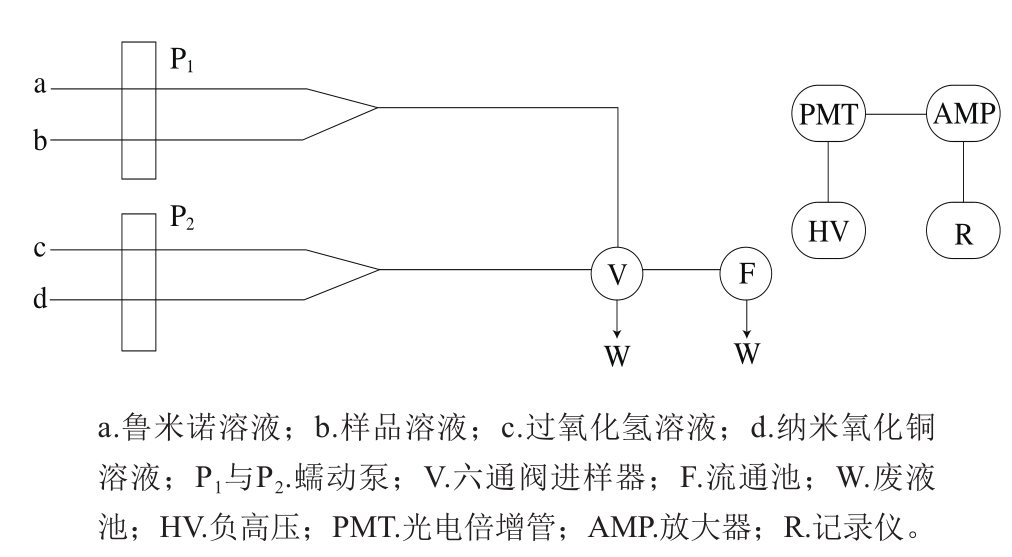
图1 流动注射化学发光流程图
Fig. 1 Schematic diagram of flow-injection chemiluminescence system
吴事正,张旭辉,杨盼盼,唐书泽*
(暨南大学理工学院食品科学与工程系,广东 广州 510632)
摘 要:利用黄绿青霉素对鲁米诺-过氧化氢-纳米氧化铜化学发光体系的抑制作用检测饮用水中可能出现的突发性污染,并对测定体系的条件进行单因素试验和响应面试验优化。结果表明:在优化的实验条件下,黄绿青霉素检测线性范围为0.005~3 mg/L,检出限为8.2×10-5mg/L。对质量浓度为0.005 mg/L的黄绿青霉素进行平行测定11 次,相对标准偏差为2.3%,黄绿青霉素加标回收率范围为78%~91%。该方法简便快捷、实用性强,可应用于饮用水中黄绿青霉素突发性污染在线快速检测。
关键词:流动注射;化学发光;黄绿青霉素;在线检测
水是人体生命活动的基本需求,因此饮用水的安全性对人体生命健康尤为重要[1]。安全的饮用水从水厂到居民饮用或到食品厂加工需经过一段较长的距离和许多环节[2],存在突发性污染或人为投毒的隐患,从而有可能导致饮用水和食物中毒事件的发生[3]。复旦大学曾经发生饮用水投毒案件,N-二甲基亚硝胺被投入饮用水中,造成受害学生死亡[4]。
饮用水中发生的突发性污染物主要是化学合成毒物如农药和工业有害化合物[5-7],因此对于这类化学合成毒物一般管控很严格,但是来自天然动植物的有毒物质可能导致的突发性污染或人为投毒隐患容易被忽视。大米发霉后产生的黄绿青霉素(citreoviridin,CIT)是一种容易被忽视的污染或人为投毒物质。CIT是黄绿青霉菌产生的生物活性代谢产物[8],对小白鼠的静脉注射和口服的LD50分别为2.0 mg/kg和29.0 mg/kg[9],毒性很强,容易被不法分子搜集富积利用导致恐怖袭击事件。本实验主要研究CIT在饮用水中可能存在的快速检测方法,利用该方法预警预防饮用水、食品加工用水及湖泊中CIT可能发生的饮用水中毒事件。
CIT的检测方法有高效液相色谱法[10]、薄层色谱法、气相色谱法、酶联免疫吸附法[11]等。高效液相色谱法效率高且选择性好,但是分析成本高,仪器昂贵。薄层色谱法方法简单且价格低廉,但是其灵敏度和特异性相对较差。气相色谱法和酶联免疫吸附法都具有较高的灵敏度[12],但难以在线检测。流动注射化学发光分析法具有灵敏度高、线性范围宽、分析速度快,可实现连续进样进行在线检测,已被广泛应用于食品科学、药物分析和环境监测等领域[13-16]。但是利用流动注射化学发光法检测CIT的研究少见文献报道。本实验主要研究流动注射化学发光法检测体系,探讨其在线快速检测饮用水、食品加工用水以及湖泊中CIT突发性污染的可行性。
1.1 材料、试剂与设备
实验用水均为采购于兴安超市的怡宝纯净水,以及加标回收实验中的珠江河水(采样于广州珠江)和明湖水(采样于暨南大学校内明湖)。
鲁米诺标准品(CAS:521-31-3;纯度98%)美国Sigma公司;过氧化氢溶液 广州东巨有限公司;纳米氧化铜分散液 宣城晶瑞新材料有限公司;CIT标准品(CAS:25425-12-1;纯度97%) 广州菲博生物科技有限公司。
IFIS-C型智能流动注射进样器 西安瑞迈分析仪器有限责任公司;BPCL-K型微弱发光测量仪 北京亚泊斯科技有限公司;UV-751GD紫外-可见分光光度计瑞利仪器分析有限公司;EL104 电子天平 上海梅特勒-托利多仪器有限公司;PHS-3C数字式pH计 上海精密科学仪器有限公司。
1.2 方法
1.2.1 进样方法
图1为流动注射化学发光流程图。a通道泵入鲁米诺溶液,b通道注入CIT溶液,在混合管路进行预先混合,c、d流路分别泵入过氧化氢溶液和纳米氧化铜溶液,各流路溶液在六通阀处混合反应产生荧光。发光信号由光电倍增管PMT检测,经放大器AMP放大后,再将光信号转换成电信号输送至计算机上以峰线图的形式显示。

图1 流动注射化学发光流程图
Fig. 1 Schematic diagram of flow-injection chemiluminescence system
1.2.2 化学发光反应动力学曲线
纳米氧化铜作为增敏剂[17-19]对鲁米诺-过氧化氢化学发光体系有很强的增敏作用,实验研究CIT对鲁米诺-过氧化氢-纳米氧化铜化学发光体系发光强度的影响,并绘制动力学曲线。
1.2.3 单因素试验
由于鲁米诺pH值、过氧化氢浓度、鲁米诺浓度、纳米氧化铜质量浓度对体系的发光强度有很大的影响,因此选取影响化学发光强度的4 个因素鲁米诺pH值、过氧化氢浓度、鲁米诺浓度、纳米氧化铜浓度进行单因素试验。在控制其他变量的情况下进行试验,考察4 个因素对体系化学发光强度的影响。
1.2.3.1 鲁米诺pH值对化学发光强度的影响
CIT质量浓度为0.005 mg/L时,鲁米诺浓度5×10-5mol/L、过氧化氢浓度0.02 mol/L、纳米氧化铜质量浓度20 mg/L条件下,考察鲁米诺pH值在12.2、12.5、12.8、13.1、13.4、13.7、14时对化学发光强度的影响。
1.2.3.2 过氧化氢浓度对化学发光强度的影响
CIT质量浓度为0.005 mg/L时,鲁米诺浓度5×10-5mol/L、鲁米诺溶液pH13.1、纳米氧化铜质量浓度20 mg/L条件下,考察过氧化氢浓度为0.02、0.03、0.04、0.05、0.06、0.07、0.08 mol/L时对化学发光强度的影响。
1.2.3.3 鲁米诺浓度对化学发光强度的影响
CIT质量浓度为0.005 mg/L时,鲁米诺pH13.1、过氧化氢浓度0.05 mol/L、纳米氧化铜质量浓度20 mg/L条件下,考察鲁米诺浓度在1×10-5、5×10-5、2×10-4、4×10-4、6×10-4、8×10-4、1×10-3mol/L时对化学发光强度的影响。
1.2.3.4 纳米氧化铜质量浓度对化学发光强度的影响
CIT质量浓度为0.005 mg/L时,鲁米诺浓度4×10-4mol/L、鲁米诺溶液pH13.1、过氧化氢浓度0.05 mol/L条件下,考察纳米氧化铜质量浓度为20、30、40、50、60、70、80 mg/L时对化学发光强度的影响。
1.2.4 响应面优化试验
在单因素试验的基础上,采用响应面分析法[20-22]得到最优的检测条件。根据Box-Behnken设计原理,进行四因素三水平响应面优化试验,采用29 个试验点进行响应面分析试验,其中共有24 个析因点,为减小误差,其中取5 组中心点,因素与水平见表1。
表1 响应面试验因素与水平
Table 1 Coded values and corresponding actual values of independent variables used in response surface analysis

1.2.5 共存物质的影响与加标回收率实验
饮用水中的金属离子及常见水体化学物质对CIT的测定结果可能有干扰作用[23-24]。在选定的最佳实验条件下,当CIT的质量浓度为0.005 mg/L时,考察一些常见的干扰物对CIT测定的影响。在选定的最佳实验条件下,测定珠江江水、明湖水、怡宝纯净水中CIT的含量,再进行质量浓度为0.05 mg/L和0.1 mg/L的CIT的加标回收实验。
1.2.6 标准曲线、精密度与检出限
在选定的最佳试验条件下,测定CIT质量浓度为0.005~3 mg/L的化学发光强度,绘制出标准曲线,并计算出检出限和精密度。检出限公式[25]表示为:
式中:CL为检出限;M为标准曲线在低质量浓度范围内的斜率;Sb为空白标准偏差;K为置信因子,一般取2或3。
1.2.7 反应机理探讨
为了探讨可能的化学发光反应机理,在200~700 nm波长范围内对鲁米诺-过氧化氢、鲁米诺-过氧化氢-纳米氧化铜、鲁米诺-过氧化氢-纳米氧化铜-CIT混合溶液进行紫外吸收扫描。
1.3 统计学分析
采用Design Expert 8.0软件进行响应面统计学分析(P<0.05),使用Origin 8.5软件绘制相关图表。
2.1 发光过程的动力学特征
如图2所示,比较曲线c、d,CIT对鲁米诺-过氧化氢体系有显著的抑制作用。观察曲线a、c,纳米氧化铜可以作为增敏剂加入到鲁米诺-过氧化氢体系中对体系的化学发光进行增敏。曲线a、b表明CIT对鲁米诺-过氧化氢-纳米氧化铜体系仍然有显著的抑制作用,因此,实验选择鲁米诺-过氧化氢-纳米氧化铜体系对CIT进行检测。
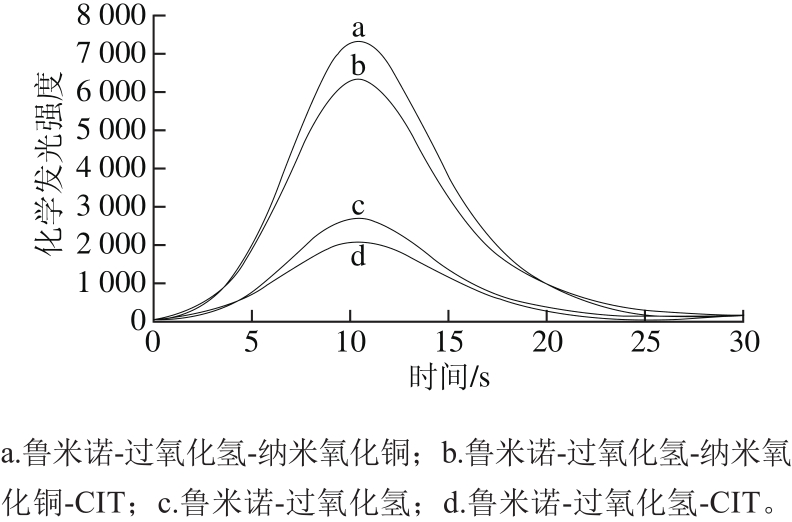
图2 CIT-鲁米诺-过氧化氢体系化学发光动力学曲线
Fig. 2 Kinetic curves of chemiluminescence of CIT-luminol-hydrogen peroxide systems
2.2 单因素试验结果
2.2.1 鲁米诺溶液pH值的选取
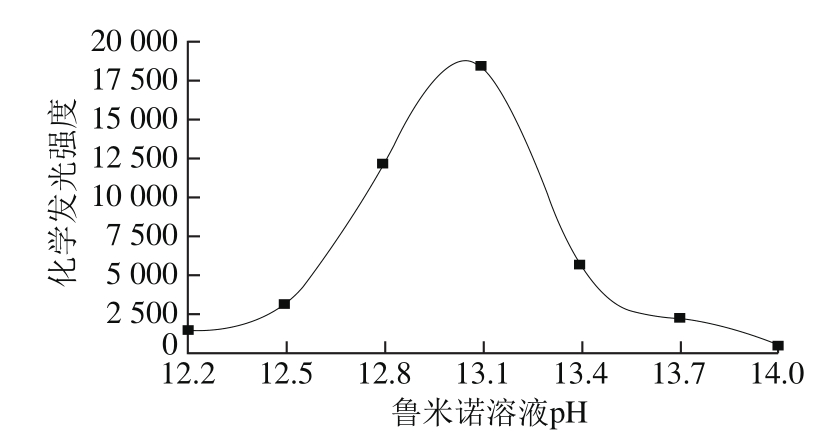
图3 鲁米诺溶液pH值与化学发光强度的关系
Fig. 3 Relationship between pH of luminal solution and chemiluminescence intensity
在碱性环境较弱的时候,碱性环境可增强鲁米诺化学发光体系的灵敏度[26]。如图3所示,当鲁米诺pH值为13.1时,化学发光强度最大。当碱性过强会抑制体系化学发光,可能是因为过多的氢氧根离子会阻碍鲁米诺与过氧化氢反应,因此选择鲁米诺溶液pH值为13.1。
2.2.2 过氧化氢浓度的选取
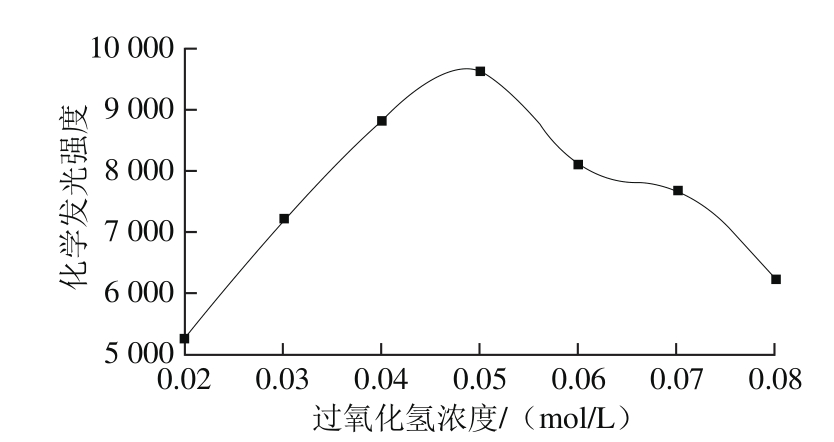
图4 过氧化氢浓度与化学发光强度的关系
Fig. 4 Relationship between hydrogen peroxide concentration and chemiluminescence intensity
如图4所示,在过氧化氢浓度为0.05 mol/L时,化学发光强度达到最大值。由于过氧化氢作为氧化剂在较小浓度范围内可快速氧化鲁米诺,当氧化剂浓度过大反而会抑制其与鲁米诺的化学反应。因此,实验选择过氧化氢溶液浓度为0.05 mol/L。
2.2.3 鲁米诺浓度的选取
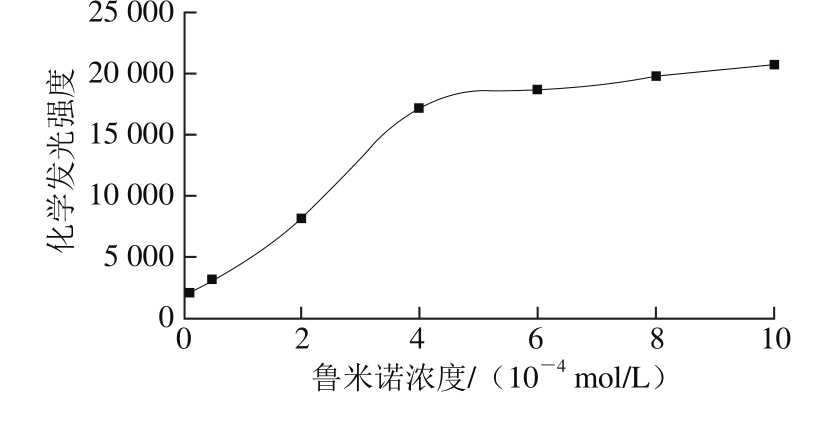
图5 鲁米诺浓度与化学发光强度的关系
Fig. 5 Relationship between luminol concentration and chemiluminescence intensity
如图5所示,随着鲁米诺浓度的增大,体系的化学发光强度随着增大。到达4×10-4mol/L后,随着鲁米诺浓度的增大,体系的化学发光强度增强缓慢,说明在此时体系中的过氧化氢大部分已经充分与鲁米诺反应。即使继续增大鲁米诺溶液的浓度,化学发光体系增加发光强度的幅度仍然很小,考虑到成本和环保,实验选定鲁米诺溶液浓度为4×10-4mol/L。
2.2.4 纳米氧化铜质量浓度的选取
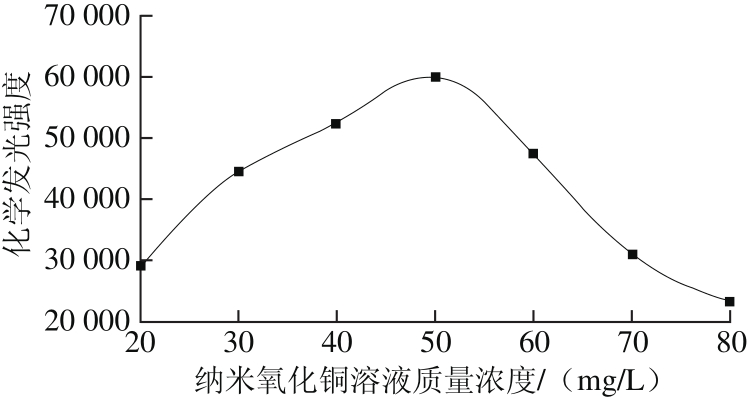
图6 纳米氧化铜质量浓度与化学发光强度的关系
Fig. 6 Relationship between nanometer copper oxide concentration and chemiluminescence intensity
如图6所示,在纳米氧化铜质量浓度为50 mg/L时,体系的化学发光强度达到最大。说明纳米氧化铜溶液作为增敏剂在此时的质量浓度最有助于增敏体系发光,当增敏剂质量浓度过大可能会阻止鲁米诺与过氧化氢的相互接触,从而导致发光强度的降低,因此实验选定纳米氧化铜质量浓度为50 mg/L。
2.3 响应面优化试验结果
2.3.1 响应面试验设计及结果
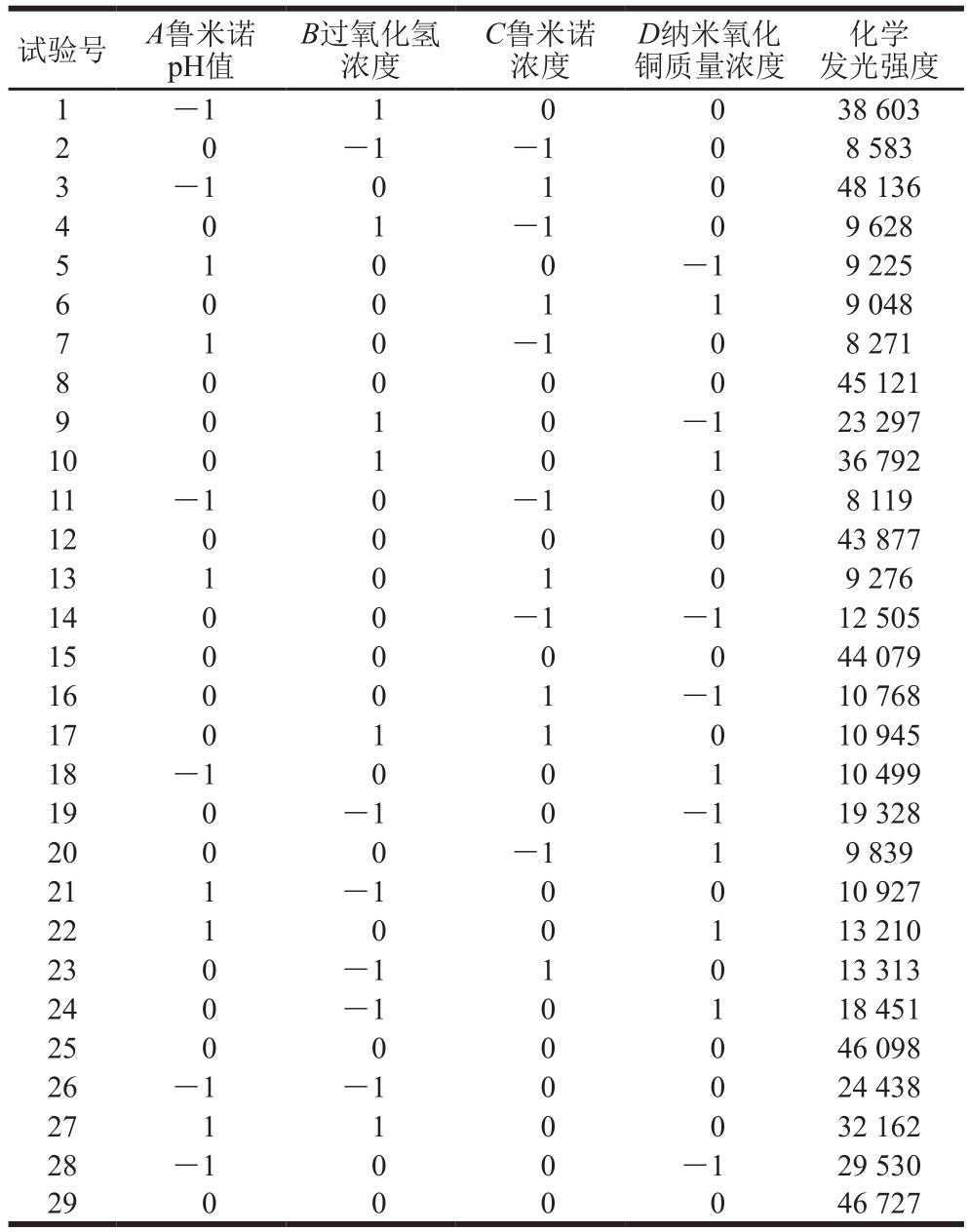
利用响应面对检测条件进行优化,响应面试验优化结果见表2。回归方程的方差分析结果见表3。P值的大小表明了模型及各因素之间的显著水平。P值小于0.05时,表明模型或各因素有显著影响;P值小于0.01时,表明模型或各因素极显著[27]。
表2 响应面试验设计与结果
Table 2 Box-Behnken design with experimental results for response surface analysis
2.3.2 模型拟合及回归方程的显著性检验
发光强度(y)和各因素变量的二次回归方程为:y=45 180.40-6 354.50A+4 698.92B+3 711.75C-567.83D+1 767.50AB-9 753.00AC+5 754.00AD-853.25BC+3 593.00BD+236.50CD-9 994.57A2-9 485.70B2-20 490.20C2-14 982.58D2。
表3 回归方程的方差分析结果
Table 3 Analysis of variance of regression equation
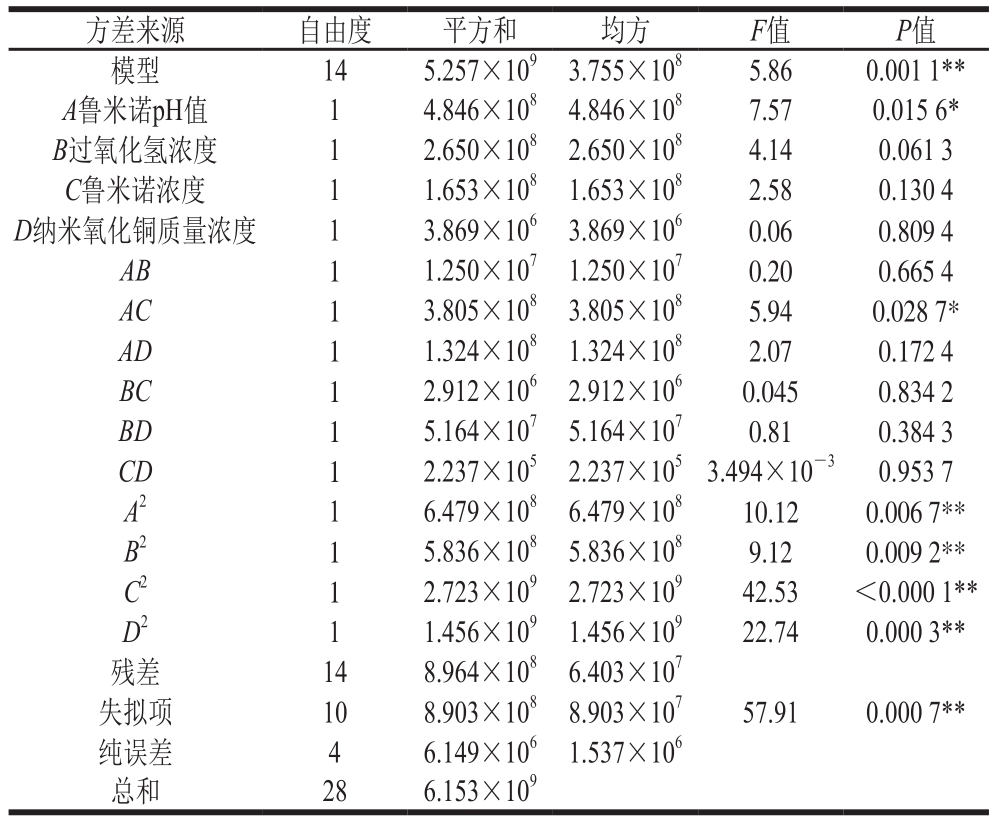
注:*.差异显著,P<0.05;**.差异极显著,P<0.01。
由表3可知,模型P值为0.001 1小于0.010 0,表明该拟合模型极显著。其中A和AC的影响显著,A2、B2、C2、D2的影响极显著,而B、C、D、AB、AD、BC、BD、CD均呈不显著。由图7可直观看出不同因素交互作用的显著性。

图7 各因素交互作用的响应面分析结果
Fig. 7 Response surface plots showing the interactive effects of four factors on response variable
2.3.3 响应面检测条件的预测与验证
结合软件的最优化预测功能,预测得到CIT的最佳检测条件为鲁米诺pH12.98、过氧化氢浓度0.05 mol/L、鲁米诺浓度4×10-4mol/L、纳米氧化铜质量浓度49.26 mg/L,发光强度为 47 295。最终确定修正后的检测条件为鲁米诺pH13.0、过氧化氢浓度0.05 mol/L、鲁米诺浓度4×10-4mol/L、纳米氧化铜质量浓度50 mg/L。在此条件下进行3 次平行检测实验,得到化学发光强度平均值为46 437,与理论值偏低1.8%,重复性好,说明采用响应面法优化的提取条件可靠。
2.4 共存物质的影响与加标回收率实验
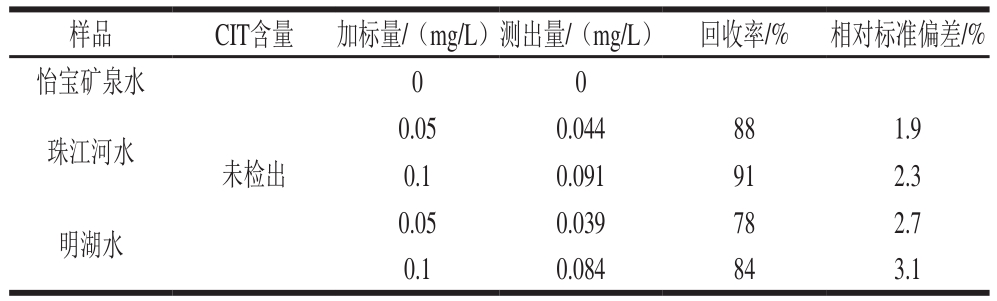
考虑到要将所建立的方法应用到实际样品的在线检测,实验评价了常见离子和共存组分对该化学发光体系的干扰情况。结果表明,在优化的实验条件下,当CIT质量浓度为0.005 mg/L,干扰允许误差为±5%时,500 倍的Na+、Cl-、Br-、CO32-、SO42-、CH3COO-、蔗糖、甲醛不干扰测定,300 倍的Ca2+、K+、Mg2+、乙醇、葡萄糖、酒石酸、糊精不干扰测定,100 倍的淀粉、乳酸、丙氨酸、醋酸不干扰测定,50 倍的Zn2+、Mn2+、Fe2+、Pb2+、苯甲酸钠、赖氨酸不干扰测定,10倍的乙二胺四乙酸二钠、硬脂酸、核黄素对实验无干扰,5 倍的抗坏血酸(VC)、柠檬酸、Fe3+、邻硝基苯酚不干扰测定。在优化的实验条件下,对不同水样进行3 次平行测定,取平均值报告测定结果。同时进行加标回收实验,每个加标水样平行测定3 次,取平均值报告回收率,结果见表4,回收率的平均值在78%~91%之间。
表4 加标回收率实验结果
Table 4 Results of recovery tests
2.5 标准曲线、检出限与精密度实验结果
在优化的实验条件下,以CIT溶液质量浓度为横坐标,化学发光强度为纵坐标,绘制标准曲线。化学发光强度与CIT的质量浓度在0.005~3 mg/L范围内有良好的线性关系,线性回归方程为y=-1 257.3x+38 026,相关系数R2为0.996 1。按照IUPAC组织的规定,以3 倍标准偏差计算的方法得到检出限为8.2×10-5mg/L,对质量浓度为0.005 mg/L的CIT进行平行测定11 次,相对标准偏差为2.3%,说明仪器的精密度良好。
2.6 反应机理探讨
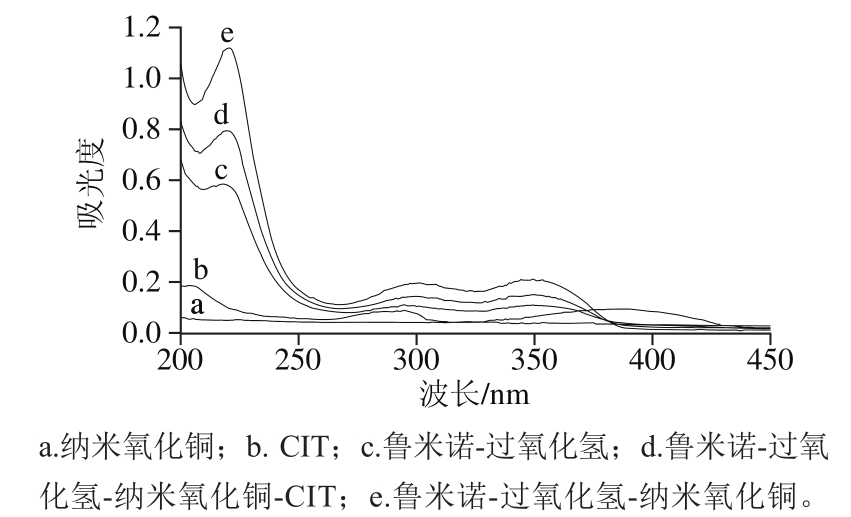
图8 紫外-可见吸收光谱图
Fig. 8 UV-Vis absorption spectra of CL systems
为探讨CIT对鲁米诺-过氧化氢-纳米氧化铜体系抑制作用的反应机理,采用紫外-可见分光光度计对不同溶液混合方式进行扫描,扫描后对紫外吸收光谱进行研究。紫外-可见光谱如图8所示,CIT的最大吸收峰在384 nm处(曲线a),曲线c、d、e 3 组溶液均在301 nm和351 nm处有两个吸收峰,由此说明将纳米氧化铜加入鲁米诺-过氧化氢体系后,并没有新的物质产生,可以推断纳米氧化铜在鲁米诺-过氧化氢体系中仅起到催化作用,并未参加反应。加入CIT之后发光体系吸收峰的位置并没有改变,也没有新的峰产生,说明CIT加入体系后并没有新的物质产生,曲线c、d、e 3 个体系的发光体仍然是激发态的氨基邻苯二甲酸根离子,激发态的氨基邻苯二甲酸根离子在返回基态的过程中以光子的形式释放出能量[28]。在水溶液中,鲁米诺氧化的最终产物是3-氨基邻苯二甲酸根离子,从鲁米诺到3-氨基邻苯二甲酸根的形成此过程中形成了一系列中间产物如·OH、O2-·[29-30]等,由于这些中间产物为氧化性自由基,推测这些氧化性自由基可能与CIT中的还原性基团作用形成了使激发态的3-氨基邻苯二甲酸根离子的数目减少的产物,导致鲁米诺化学发光体系的化学发光反应受到抑制。
基于CIT对鲁米诺-过氧化氢-纳米氧化铜化学发光体系具有显著的抑制作用,本实验将流动注射化学发光检测技术成功应用于饮用水中CIT的测定,建立了测定饮用水中的CIT的流动注射化学发光分析方法。测定方法灵敏度高、线性范围宽、运行费用低、分析速度快、仪器设备简单。可用于饮用水、食品加工用水以及湖泊中CIT突发性污染的快速检测,且效果显著,实用性强。
参考文献:
[1] COLLIVIGNARELLI C. Water safety: one of the primary objectives of our time[J]. 2016, 12(1): 1-7. DOI:10.4136/ambi-agua.1994.
[2] JI H W, LEE S I. Use of pollutant release and transfer register (PRTR)to assess potential risk associated with chemicals in a drinking water supply facility[J]. Desalination and Water Treatment, 2016, 57(60):29228-29239. DOI:10.1080/19443994.2016.1171170.
[3] 王延勇. 我国生活饮用水安全的现状与对策[J]. 中国初级卫生保健,2007, 21(1): 34-36.
[4] 金春波. 校园投毒事件报道分析[J]. 采写编, 2016(1): 85-86.
[5] YOST E E, STANEK J, BURGOON L D. A decision analysis framework for estimating the potential hazards for drinking water resources of chemicals used in hydraulic fracturing fluids[J]. Science of the Total Environment, 2016, 574: 1544-1558. DOI:10.1016/j.scitotenv.2016.08.167.
[6] MAINALI B, PHAM T T, NGO H H, et al. Maximum allowable values of the heavy metals in recycled water for household laundry[J].Science of the Total Environment, 2013, 452/453(5): 427-432.DOI:10.1016/j.scitotenv.2013.03.012.
[7] SAHA N, RAHMAN M S, AHMED M B, et al. Industrial metal pollution in water and probabilistic assessment of human health risk[J]. Journal of Environmental Management, 2017, 185: 70-78.DOI:10.1016/j.jenvman.2016.10.023.
[8] ZHUANG Z H, QUE S J, GAO Y M, et al. Artificial antigen synthesis and the development of polyclonal antibody-based immunoassay for citreoviridin determination.[J]. World Journal of Microbiology and Biotechnology, 2014, 30(1): 343-349. DOI:10.1007/s11274-013-1431-0.
[9] 侯海峰, 李群伟. 黄绿青霉素的研究进展[J]. 医学综述, 2005, 11(2):177-178.
[10] 李德安, 孙树秋, 李晓丹, 等. 黄绿青霉素的高效液相色谱法检测[J].中华地方病学杂志, 2004, 23(2): 160-162.
[11] 阙善进. 黄绿青霉素人工抗原的制备及酶联免疫吸附法的建立[D].福州: 福建农林大学, 2012.
[12] LING S, JIE P, YU J, et al. Preparation and identification of monoclonal antibody against fumonisin B1, and development of detection by Ic-ELISA[J]. Toxicon, 2014, 80(3): 64-72. DOI:10.1016/j.toxicon.2014.08.057.
[13] KHATAEE A, HASANZADEH A, LOTFI R, et al. Determination of dexamethasone by flow-injection chemiluminescence method using capped CdS quantum dots[J]. Spectrochimica Acta Part A Molecular &Biomolecular Spectroscopy, 2015, 150: 63-71. DOI:10.1016/j.saa.2015.05.047.
[14] 高向阳, 赵琛, 游新侠, 等. 流动注射化学发光法测定油炸食品中的丙烯酰胺[J]. 食品科学, 2013, 34(22): 239-242. DOI:10.7506/spkx 1002-6630-201322047.
[15] KHATAEE A, LOTFI R, HASANZADEH A, et al. A flow injection chemiluminescence method for determination of nalidixic acid based on KMnO4-morin sensitized with CdS quantum dots[J].Spectrochimica Acta Part A Molecular & Biomolecular Spectroscopy,2015, 154. DOI:10.1016/j.saa.2015.10.039.
[16] YAN Z, ZHANG Z, YU Y, et al. Chemiluminescence determination of potassium bromate in flour based on flow injection analysis[J]. Food Chemistry, 2016, 190: 20-24. DOI:10.1016/j.foodchem.2015.05.076.
[17] KHATAEE A R, FATHINIA M, HASANZADEH A, et al. Enhanced chemiluminescence of the luminol-KMnO4, system by CuO nanosheets and its application for determination of meropenem in water and human serum[J]. Journal of Luminescence, 2014, 149(5): 272-279.DOI:10.1016/j.jlumin.2014.01.038.
[18] KHATAEE A, IRANIFAM M, FATHINIA M, et al. Flow-injection chemiluminescence determination of cloxacillin in water samples and pharmaceutical preparation by using CuO nanosheets-enhanced luminol-hydrogen peroxide system[J]. Spectrochimica Acta Part A Molecular & Biomolecular Spectroscopy, 2015, 134: 210-217.DOI:10.1016/j.saa.2014.06.125.
[19] KHATAEE A R, HASANZADEH A, IRANIFAM M, et al. CuO nanosheets-enhanced flow-injection chemiluminescence system for determination of vancomycin in water, pharmaceutical and human serum[J]. Spectrochimica Acta Part A: Molecular and Biomolecular Spectroscopy, 2014, 122(6): 737-743. DOI:10.1016/j.saa.2013.12.014.
[20] DOBLADO-MALDONADO A F, JANSSEN F, GOMAND S V, et al.A response surface analysis of the aqueous leaching of amylose from maize starch[J]. Food Hydrocolloids, 2017, 63: 265-272. DOI:10.1016/j.foodhyd.2016.09.006.
[21] 侯学敏, 李林霞, 张直峰, 等. 响应面法优化薄荷叶总黄酮提取工艺及抗氧化活性[J]. 食品科学, 2013, 34(6): 124-128.
[22] D’ARCHIVIO A A, MAGGI M A. Investigation by response surface methodology of the combined effect of pH and composition of water-methanol mixtures on the stability of curcuminoids[J]. Food Chemistry, 2017, 219: 414-418. DOI:10.1016/j.foodchem.2016.09.167.
[23] KHATAEE A, LOTFI R, HASANZADEH A, et al. Flow-injection chemiluminescence analysis for sensitive determination of atenolol using cadmium sulfide quantum dots[J]. Spectrochimica Acta Part A Molecular & Biomolecular Spectroscopy, 2016, 157: 88-95.DOI:10.1016/j.saa.2015.12.015.
[24] KHATAEE A, HASANZADEH A, IRANIFAM M, et al. A novel flowinjection chemiluminescence method for determination of baclofen using L-cysteine capped CdS quantum dots[J]. Sensors & Actuators B Chemical, 2015, 215: 272-282. DOI:10.1016/j.snb.2015.03.066.
[25] 徐金龙, 刘中勇, 华斌, 等. 分析化学中检出限问题探讨[J]. 检验检疫学刊, 2012(6): 74-76.
[26] 朱定波, 马强, 燕廷, 等. 鲁米诺-铁氰化钾流动注射化学发光体系测定饮用水中a-茄碱[J]. 食品工业科技, 2012, 33(22): 84-86.DOI:10.13386/j.issn1002-0306.2012.22.006.
[27] 林建原, 季丽红. 响应面优化银杏叶中黄酮的提取工艺[J]. 中国食品学报, 2013, 13(2): 83-90.
[28] 石志敏. 流动注射化学发光法测定环境水中有机污染物的研究[D].新乡: 河南师范大学, 2012.
[29] CHAICHI M J, EHSANI M. Determination of glucose and cholesterol using a novel optimized luminol-CuO nanoparticles-H2O2, chemiluminescence method by box-behnken design[J]. Journal of Fluorescence, 2015, 25(4): 861-870. DOI:10.1007/s10895-015-1566-5.
[30] GUO J Z, CUI H, ZHOU W, et al. Ag nanoparticle-catalyzed chemiluminescent reaction between luminol and hydrogen peroxide[J].Journal of Photochemistry & Photobiology A Chemistry, 2008,193(2/3): 89-96. DOI:10.1016/j.jphotochem.2007.04.034.
On-Line Determination of Citreoviridin in Drinking Water by Flow Injection Chemiluminescence
WU Shizheng, ZHANG Xuhui, YANG Panpan, TANG Shuze*
(Department of Food Science and Engineering, College of Science and Technology, Jinan University, Guangzhou 510632, China)
Abstract:Based on the inhibition of citreoviridin (CIT) on luminol-hydrogen peroxide-nanometer copper oxide chemiluminescence system, a new method was proposed for the identification of sudden drinking water pollution. The detection system was optimized by one-factor-at-a-time and orthogonal array design methods. Results showed that under the optimized experimental conditions, the linear range for CIT determination was 0.005–3 mg/L. The limit of detection(LOD) of CIT was 8.2 × 10-5mg/L. The precision expressed as relative standard deviation (RSD) was 2.3% for 11 replicate determinations of 0.005 mg/L CIT, and the recoveries of spiked samples were 78%–91%. This online determination method showed the advantages of convenience and strong practicability and could have a great potential application in rapid detection of sudden citreovirid pollution in drinking water.
Key words:flow injection; chemiluminescence; citreoviridin; on-line monitoring
DOI∶10.7506/spkx1002-6630-201724041
中图分类号:TS201.6
文献标志码:A
文章编号:1002-6630(2017)24-0253-07
引文格式:
吴事正, 张旭辉, 杨盼盼, 等. 流动注射化学发光法对饮用水中黄绿青霉素的在线检测[J]. 食品科学, 2017, 38(24):253-259.
DOI:10.7506/spkx1002-6630-201724041. http://www.spkx.net.cn
WU Shizheng, ZHANG Xuhui, YANG Panpan, et al. On-line determination of citreoviridin in drinking water by flow injection chemiluminescence[J]. Food Science, 2017, 38(24)∶ 253-259. (in Chinese with English abstract) DOI∶10.7506/spkx1002-6630-201724041. http∶//www.spkx.net.cn
收稿日期:2016-12-29
基金项目:广东省公益研究与能力建设专项(2014A020218009)
作者简介:吴事正(1991—),男,硕士研究生,研究方向为食品安全与预警。E-mail:wszjnu@qq.com
*通信作者:唐书泽(1957—),男,教授,博士,研究方向为食品安全与预警。E-mail:tangsz@jnu.edu.cn