超高效液相色谱-串联质谱法测定猪肉中β-受体激动剂残留量的不确定度分析
宁 霄,金绍明,梁瑞强,曹 进*,张庆生
(中国食品药品检定研究院,北京 100050)
摘 要:采用超高效液相色谱-串联质谱法对猪肉中沙丁胺醇、盐酸克伦特罗和莱克多巴胺含量的不确定度进行评估。根据JJF 1135—2005《化学分析测量不确定度评定》和JJF 1059.1—2012《测量不确定度评定与表示》中的有关规定,建立测定猪肉中3 种β-受体激动剂残留量不确定度的数学模型,逐层对不确定度来源进行分析。通过对不确定度分量进行量化和合成,得出当猪肉中沙丁胺醇含量为1.99 μg/kg时,其扩展不确定度为0.25 μg/kg(k=2);当猪肉中盐酸克伦特罗含量为2.04 μg/kg时,其扩展不确定度为0.24 μg/kg(k=2);当猪肉中莱克多巴胺含量为1.97 μg/kg时,其扩展不确定度为0.24 μg/kg(k=2)。评定结果表明,影响检测结果的主要因素为标准溶液配制、标准曲线拟合和测量重复性等。
关键词:超高效液相色谱-串联质谱;沙丁胺醇;盐酸克伦特罗;莱克多巴胺;不确定度;猪肉
测量不确定度是表征合理地赋予被测量值的分散性、与测量结果相关性的参数
[1],其数值的大小反映了测量结果质量的高低,并直接与检验结果的合格判定相关。β-兴奋剂是一类合成化学兴奋剂。此类物质有较强的蛋白质同化作用,可提高蛋白质沉积,如果将其加入动物饲料中,能有效地促进肌肉的生长,降低脂肪比率
[2-3]。然而,现在医学实验已证明其残留会严重影响到人类的健康,如出现心慌、头痛、恶心等症状,甚至还会增加致癌、致畸的风险
[4-5]。鉴于此,人们开始越来越关注动物源性食品中存在的β-兴奋剂给人们身体健康所带来的影响,全世界所有国家均已禁止畜牧生产中应用此类药物
[6-8],但目前非法使用并造成严重食物中毒事件的报道仍然屡见不鲜
[9-12],对人体健康构成巨大威胁。动物源性食品成分复杂,兽药残留分析难度大,为了确保检测结果的可信度,必须进行测量不确定度的评定。目前有关气相色谱-质谱法
[13-14]和酶联免疫吸附测定法
[15-16]的不确定度评价方法已见报道,而液相色谱-串联质谱法的相关研究基本空缺。
本实验参照JJF 1135—2005《化学分析测量不确定度评定》
[17]和JJF 1059.1—2012《测量不确定度评定与表示》
[1],通过农业部1025号公告—18—2008《动物源性食品中β-受体激动剂残留检测 液相色谱-串联质谱法》
[1
8]评定猪肉中沙丁胺醇、盐酸克伦特罗和莱克多巴胺3 种β-受体激动剂残留检测的不确定度
[19-25],以期为实验室质量控制提供科学、准确的依据,同时为测量其他兽药残留量的不确定度评定提供参考。
1 材料与方法
1.1 材料与试剂
猪肉 市售。
沙丁胺醇(纯度为99.5%)、盐酸克伦特罗(纯度为98.5%)、莱克多巴胺(纯度为98.0%)标准品 德国Dr.E公司;β-盐酸葡萄糖醛苷酶 德国Merck公司;甲醇、乙腈均为色谱纯;甲酸、乙酸、异丙醇、乙酸铵、高氯酸、氢氧化钠、乙酸乙酯、叔丁基甲醚均为分析纯。
1.2 仪器与设备
1290-6460型超高效液相色谱-串联质谱仪 美国Agilent公司;AL204电子天平 瑞士Mettler Toledo公司;高速离心机 日本Hitach公司;涡旋振荡器 中国中科公司;恒温水浴振荡箱 上海森信科技有限公司;氮吹仪中国合众日盛公司;MCX固相萃取柱6 0 mg 美国Waters公司。
1.3 方法
1.3.1 样品前处理
按照农业部1025号公告—18—2008的要求,准确称取2 g均质的测试样品(精确至0.01 g)于50 mL离心管内,加入乙酸铵缓冲溶液8.0 mL,再加入β-盐酸葡萄糖醛苷酶40 μL,涡旋混匀,于37 ℃条件下避光水浴振荡16 h。酶解后涡旋混匀,10 000 r/min高速离心10 min,取上清液,用高氯酸调pH 1.0后高速离心,将上清液转移至另一50 mL离心管内,用NaOH溶液调p H 9.5后,用乙酸乙酯15 mL和叔丁基甲醚10 mL分别提取一次,合并两次提取有机相,50 ℃条件下氮气吹干,用2%甲酸溶液5 mL溶解,过MCX固相萃取柱净化,加入3%氨水-甲醇溶液2.5 mL洗脱,洗脱液氮气吹干后用甲醇-0.1%甲酸溶液(10∶90,V/V)定容至1 mL,涡旋混匀,0.22 μm滤膜过滤后,待超高效液相色谱-串联质谱测定。
1.3.2 色谱条件
色谱柱:Ag ilen t Eclip se XDB-C
18(4.6 mm× 150 mm,3.5μm);流动相:A相:甲醇;B相:0.1%甲酸溶液;梯度洗脱:0~2 min,维持80% A;2~12 min,80% A线性变化至40% A;12~12.1 min,40% A线性变至4% A;12.1~18 min,维持4% A;18~18.1 min,线性变至80% A;流速0.2 mL/min;柱温30 ℃;进样量2 μL。
1.3.3 质谱条件
离子源:电喷雾离子化正离子模式;气流温度:330 ℃;气流速率:8 L/min;喷雾气压力:30 psi;毛细管电压:3 500 V;多反应监测扫描采集参数见表1。
表1 超高效液相色谱-串联质谱采集参数
Table l Acquisition parameters of UPLC-MS/MS for analysis of salbutamol, clenbuterol hydrochloride and ractompaine

化合物母离子子离子驻留碎裂碰撞(m/z)(m/z)时间/ms电压/V能量/eV沙丁胺醇240.2 222.2 50 90 20 148.2 50 90 25盐酸276.9 259.1 50 90 5克伦特罗203.0 50 90 10莱克302.3 164.1 50 90 20多巴胺107.2 50 90 30
1.3.4 数学模型的建立
被测物残留量计算见式(1):
式中:X为试样中被测物残留量/(μg/kg);C为从标准工作曲线得到的试样溶液中被测组分的质量浓度/(ng/mL);V为试样溶液最终定容体积/mL;m为试样溶液所代表试样的质量/g。
2 结果与分析
2.1 不确定度来源分析
根据测定过程,对试样中β-受体激动剂残留量测定结果有影响的各种不确定的分量来源进行分析,从图1可见具体引入的不确定度来源。
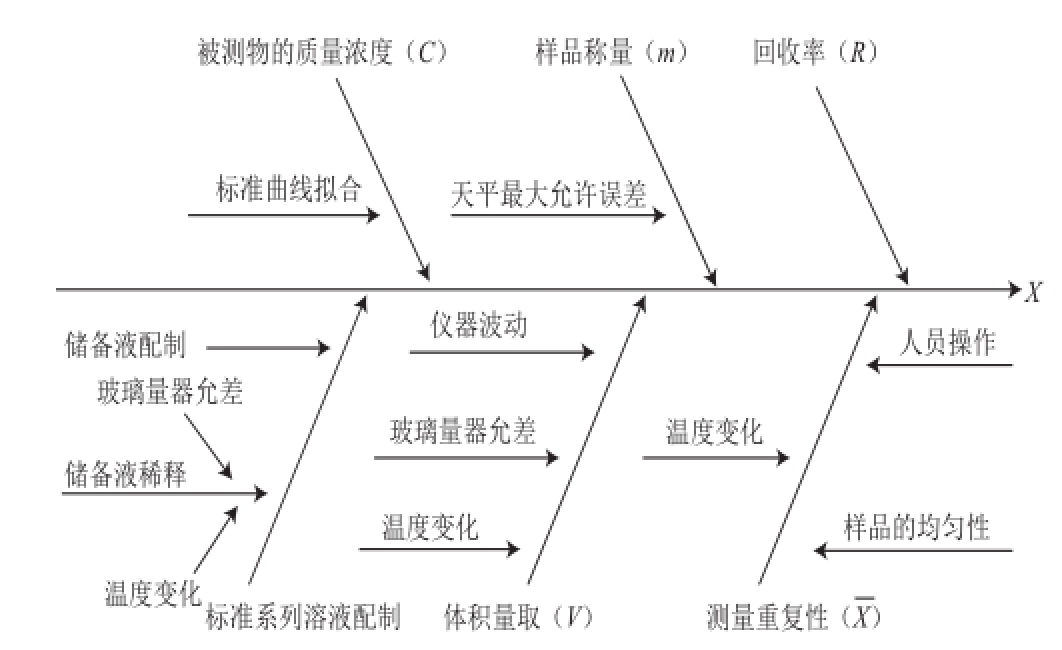
图1 超高效液相色谱-串联质谱测定猪肉中β-受体激动剂残留量的不确定度来源
Fig. l Uncertainty source for determination of three β-agonists in commercialized samples of pork with UPLC-MS/MS
2.2 不确定度的评定
2.2.1 被测物质量浓度(C)引入的不确定度
[26-28]
C的不确定度由标准系列溶液配制对C的测量产生的不确定度和由标准曲线拟合的直线求得C时带来的不确定度两部分组成。标准系列溶液配制又分为储备液的配制、储备液的稀释以及标准曲线溶液的配制3 个过程。
2.2.1.1 储备液配制过程产生的不确定度u(C-1)
分别准确称取1 0.4 mg沙丁胺醇(纯度99.5%)、10.1 mg盐酸克伦特罗(纯度98.5%)和10.6 mg莱克多巴胺(纯度98.0%)标准品,用甲醇溶解并定容至100 mL,得到质量浓度为100 mg/L的混合标准储备液。
标准品纯度引入的不确定度:根据标准证书,沙丁胺醇标、盐酸克伦特罗和莱克多巴胺准品的纯度误差分别为0.5%、0.5%和1%,按照均匀分布计算,由纯度引入的不确定度和相对不确定度分别为:沙丁胺醇:
 u(p)/p=0.2 8 9%/9 9.5%=0.0 0 2 9 0;盐酸克伦特
u(p)/p=0.2 8 9%/9 9.5%=0.0 0 2 9 0;盐酸克伦特
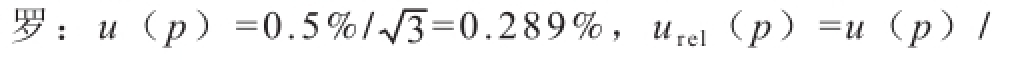 p=0.289%/98.5%=0.002 93;莱克多巴胺:
p=0.289%/98.5%=0.002 93;莱克多巴胺:
 0.577%,u
rel(p)=u(p)/p=0.577%/98.0%=0.005 89。
0.577%,u
rel(p)=u(p)/p=0.577%/98.0%=0.005 89。
标准品称量引入的不确定度:据鉴定证书,实验所用天平最大允许误差为±0.1 mg,按照均匀分布计算,由称量标准品引入的不确定度和相对不确定度分别为:沙丁胺醇:
 u
rel(m
1)=u (m
1)/m
1=0.057 7/10.4=0.005 55;盐酸克伦特罗:
u
rel(m
1)=u (m
1)/m
1=0.057 7/10.4=0.005 55;盐酸克伦特罗:
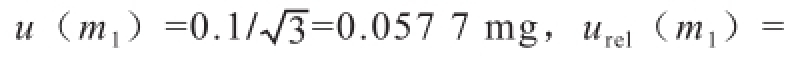 u(m
1)/m
1=0.0 57 7/1 0.3=0.0 05 7 2;莱克多巴胺:
u(m
1)/m
1=0.0 57 7/1 0.3=0.0 05 7 2;莱克多巴胺:
 m
1=0.057 7/10.4=0.005 45。
m
1=0.057 7/10.4=0.005 45。
标准储备液定容体积引入的不确定度:JJG 196— 2 0 0 6《常用玻璃量器》规定,2 0 ℃时1 0 0 m L A级容量瓶容量允差为±0.1 m L,假设为对称分布,其标准不确定度为
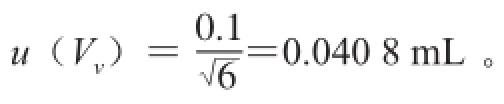 实验室的温度为(2 0±5)℃,甲醇的体积膨胀系数为1.1×10
-3℃
-1,假设温度波动呈均匀分布,
实验室的温度为(2 0±5)℃,甲醇的体积膨胀系数为1.1×10
-3℃
-1,假设温度波动呈均匀分布,
 故1 0 0 m L容量瓶由温度引起的体积不确定度为
故1 0 0 m L容量瓶由温度引起的体积不确定度为
 合成100 mL容量瓶定容体积引入的相对标准不确定度为:
合成100 mL容量瓶定容体积引入的相对标准不确定度为:
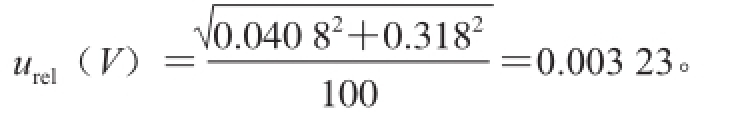
由储备液配制所产生的相对标准不确定度
 沙丁胺醇、盐酸克伦特罗和莱克多巴胺的u(C-1)分别为0.007 0、0.007 2和0.008 6。
沙丁胺醇、盐酸克伦特罗和莱克多巴胺的u(C-1)分别为0.007 0、0.007 2和0.008 6。
2.2.1.2 储备液稀释过程产生的不确定度u(C-2)
用1 mL单标线吸量管移取储备液1 mL于100 mL容量瓶(A级)中,用甲醇定容至刻度,摇匀,得到质量浓度为1 mg/L的混合标准溶液,再移取1 mL该标准溶液于100 mL容量瓶(A级)中,用0.2%甲酸溶液定容至刻度,得到质量浓度为0.01 mg/L的混合标准工作液。
按照均匀分布处理,玻璃器具及温度波动引入的不确定度见表2。
则由储备液稀释过程产生的相对标准不确定度为:
2.2.1.3 标准系列溶液配制过程产生的不确定度u(C-3)
准确称取2 g(精确至0.01 g)空白试样于50 mL离心管内,平行操作5 次。分别向其中添加50、100、200、500、100 μL混合标准工作液(0.01 mg/L),按照1.3.1节测试样品前处理步骤操作,得到含量为0.25、0.5、1、2.5、5 μg/kg的空白添加标准系列溶液。
移液器刻度误差参考JJG 646—2006《移液器检定规程》的要求,按照均匀分布处理,玻璃器具及温度波动引入的不确定度见表3。
则由标准系列溶液配制过程产生的相对标准不确定度为:
2.2.1.4 标准曲线拟合产生的不确定度u(C-4)
表4 标准曲线数据
Table 4 Results of standard curves
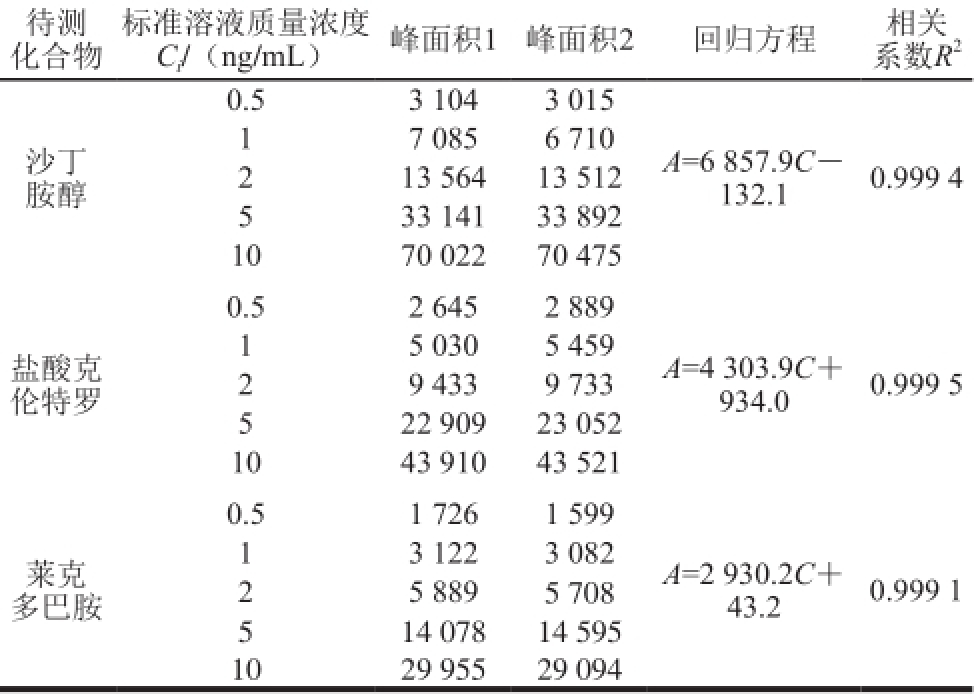
待测标准溶液质量浓度峰面积1峰面积2回归方程相关
2化合物C
i/(ng/mL)系数R 0.5 3 104 3 015沙丁17 085 6 710A=6 857.9C-胺醇213 564 13 512132.1 0.999 4 5 33 141 33 892 10 70 022 70 475 0.5 2 645 2 889盐酸克15 030 5 459A=4 303.9C+伦特罗29 433 9 733934.0 0.999 5 5 22 909 23 052 10 43 910 43 521 0.5 1 726 1 599莱克13 122 3 082A=2 930.2C+多巴胺25 889 5 70843.2 0.999 1 5 14 078 14 595 10 29 955 29 094
分别添加5 个水平的混合标准样品0.25、0.5、1、2.5、5 μg/kg,按照样品处理步骤操作后上机,取以上对应质量浓度为0.5、1、2、5、10 ng/mL的5 种标准系列溶液各2 μL分别重复测定2 次,通过Excel软件
[29]得到相应的色谱峰面积A
i,拟合而成的线性回归方程为A
i=aC
i+b,其中,a为斜率,b为截距,测定数据及计算结果如表4所示。取一阳性样品,对各待测化合物浓度C
0进行3 次重复检测,其结果见表5,则由标准曲线拟合产生的不确定度为:
式中:S
R为标准溶液峰面积残差的标准差,计算方法为:
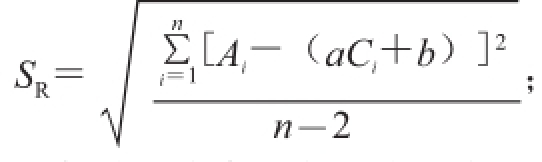 n为测试次数,本实验中5 个质量浓度重复测定2 次,n=5×2=10;p为对C
0的测定次数,
n为测试次数,本实验中5 个质量浓度重复测定2 次,n=5×2=10;p为对C
0的测定次数,
 为标准溶液的平均质量浓度,
为标准溶液的平均质量浓度,
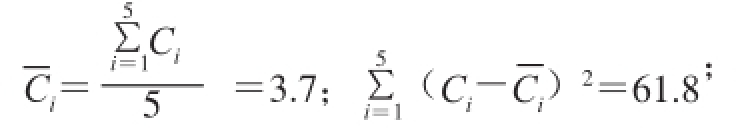 代入公式(2)则可计算出
代入公式(2)则可计算出
 根据
根据
 可计算出被测物质量浓度C引入的不确定度,相关量值见表6。
可计算出被测物质量浓度C引入的不确定度,相关量值见表6。
表5 阳性样品测量数据
Table 5 Results for determination of positive samples

待测化合物峰面积质量浓度/平均质量浓度(ng/mL)C/(ng/mL)28 734 4.167沙丁胺醇28 775 4.1724.111 27 513 3.993 19 840 4.393盐酸克伦特罗19 131 4.2284.298 19 327 4.274 11 660 3.965莱克多巴胺11 715 3.9833.925 11 262 3.829
表6 被测物质量浓度C引入的不确定度计算相关量值
Table 6 Calculation of uncertainty resulting from analyte concentration

待测化合物S a C/u
relu
relu
relu
relu
rel
R(ng/mL)(C-1)(C-2)(C-3)(C-4)(C)沙丁胺醇997 6857.9 4.111 0.007 05 0.008 0 0.056 6 0.023 3 0.062 1盐酸克伦特罗379 4303.9 4.298 0.007 19 0.008 0 0.056 6 0.013 5 0.059 2莱克多巴胺345 2930.2 3.925 0.008 65 0.008 0 0.056 6 0.019 8 0.061 1
2.2.2 测量重复性产生的不确定度

表7 猪肉中沙丁胺醇、盐酸克伦特罗和莱克多巴胺测定结果
Table 7 Results of determination of salbutamol, clenbuterol hydrochloride and ractompaine in commercialized samples of pork

注:相对不确定度无单位。
沙丁胺醇盐酸克伦特罗莱克多巴胺实验号称样量/g 质量浓度C/含量X/回收质量浓度C/含量X/回收质量浓度C/含量X/回收(ng/mL)(μg/kg)率R/%(ng/mL)(μg/kg)率R/%(ng/mL)(μg/kg)率R/% 1 2.09 3.867 1.850 90.4 4.103 1.963 95.0 4.007 1.917 92.8 2 2.03 3.792 1.868 88.6 4.217 2.077 97.6 4.059 2.000 94.0 3 2.05 4.006 1.954 93.6 4.083 1.992 94.5 4.004 1.953 92.7 4 2.06 3.854 1.871 90.0 4.077 1.979 94.4 3.921 1.903 90.8 5 1.97 3.746 1.902 87.5 4.119 2.091 95.3 3.896 1.978 90.2 6 2.02 3.958 1.959 92.5 4.138 2.049 95.8 3.975 1.968 92.0 7 1.99 3.817 1.918 89.2 4.115 2.068 95.3 3.886 1.953 90.0 8 2.03 3.799 1.871 88.8 4.073 2.006 94.3 4.010 1.975 92.8 9 2.01 3.817 1.899 89.2 4.089 2.034 94.7 3.994 1.987 92.5 10 1.98 3.688 1.863 86.2 4.052 2.046 93.8 4.093 2.067 94.7平均值2.023 3.834 1.896 89.6 4.107 2.031 95.1 3.985 1.970 92.2标准偏差0.037 0.094 0.038 2.190 0.046 0.044 1.071 0.067 0.045 1.555不确定度0.012 0.030 0.012 0.693 0.015 0.014 0.339 0.021 0.014 0.492相对不确定度0.005 9 0.007 7 0.006 4 0.007 7 0.003 6 0.006 8 0.003 6 0.005 3 0.007 3 0.005 3
在空白猪肉试样中添加2 μg/kg的沙丁胺醇、盐酸克伦特罗和莱克多巴胺混合标准溶液,平行测定10 次。将重复测定的平均含量
 ,标准偏差S(
,标准偏差S(
 结果分别代入公式
结果分别代入公式
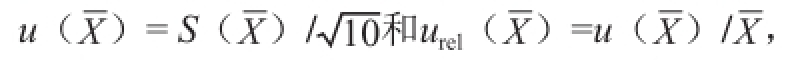 计算得到重复测量引入的不确定度和相对不确定度,如表7所示。
计算得到重复测量引入的不确定度和相对不确定度,如表7所示。
2.2.3 回收率产生的不确定度u(R)
取重复性实验中的 测量回收率结果列于表7,将平均回收率
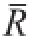 、标准偏差S(R)结果分别代入公式u(R)=
、标准偏差S(R)结果分别代入公式u(R)=
 计算得到回收率引入的不确定度和相对不确定度,
计算得到回收率引入的不确定度和相对不确定度,
2.2.4 样品称量产生的不确定度u(m)
称取2 g猪肉样品,天平校准证书说明最大允许误差为±0.005 g,按照均匀分布计算,其不确定度u(m)=
 相对不确定度u
rel(m)= u(m)/m= 0.002 9/2=0.001 4。
相对不确定度u
rel(m)= u(m)/m= 0.002 9/2=0.001 4。
2.2.5 体积量取产生的不确定度u(V)
量取体积产生的不确定度主要由定容体积和进样体积不确定度组成。
2.2.5.1 定容容量产生的不确定度u(V
1)
样品经过萃取、净化后用刻度试管定容至V
1为1 mL,其体积允许误差为±0.008 mL,按照均匀分布计算,其不确定度是:
 由温度变化产生的水容积变化为:u(V
1温)=1×5 ℃× β
水=0.001 05 mL,按照均匀分布计算,其不确定度是:
由温度变化产生的水容积变化为:u(V
1温)=1×5 ℃× β
水=0.001 05 mL,按照均匀分布计算,其不确定度是:

定容时引入的不确定度和相对不确定度为:
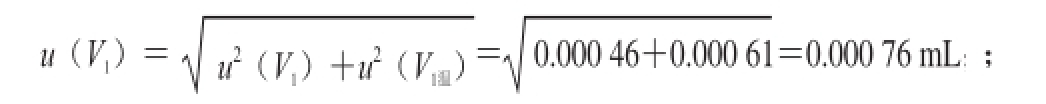 u
rel(V
1)= u(V
1)/1=0.000 76。
u
rel(V
1)= u(V
1)/1=0.000 76。
2.2.5.2 仪器进样体积产生的不确定度u(V
2)
该超高效液相色谱-串联质谱进样针容积的相对标准偏差为±1%,按均匀分布,则其相对不确定度u
rel(V
2)=

合成体积量取引入的相对不确定度为:

2.3 合成不确定度
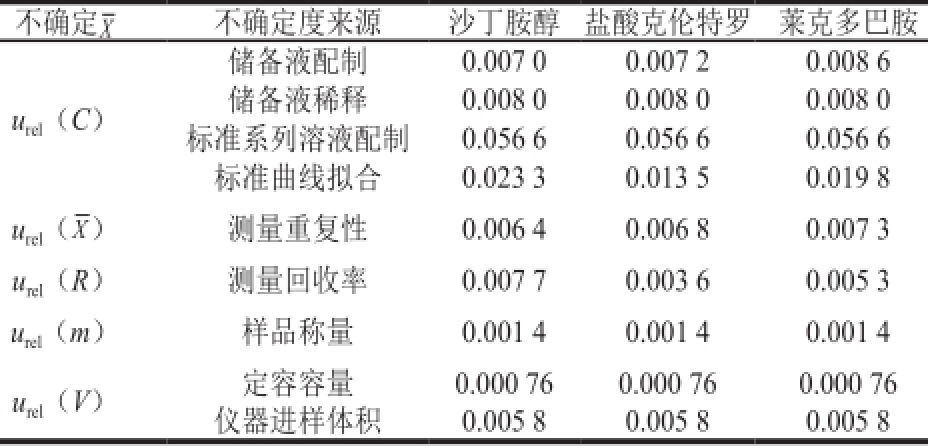
各β-受体激动剂相对不确定度分量见表8。
表8 各β-受体激动剂相对不确定度分量
Table 8 List of relative uncertainty components for three β-agonists
不确定
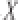 不确定度来源沙丁胺醇盐酸克伦特罗莱克多巴胺储备液配制0.007 0 0.007 2 0.008 6 u(C)储备液稀释0.008 0 0.008 0 0.008 0
rel标准系列溶液配制0.056 6 0.056 6 0.056 6标准曲线拟合0.023 3 0.013 5 0.019 8 u
rel(
不确定度来源沙丁胺醇盐酸克伦特罗莱克多巴胺储备液配制0.007 0 0.007 2 0.008 6 u(C)储备液稀释0.008 0 0.008 0 0.008 0
rel标准系列溶液配制0.056 6 0.056 6 0.056 6标准曲线拟合0.023 3 0.013 5 0.019 8 u
rel(
 )测量重复性0.006 4 0.006 8 0.007 3 u
rel(R)测量回收率0.007 7 0.003 6 0.005 3 u
rel(m)样品称量0.001 4 0.001 4 0.001 4 u(V)定容容量0.000 76 0.000 76 0.000 76
rel仪器进样体积0.005 8 0.005 8 0.005 8
)测量重复性0.006 4 0.006 8 0.007 3 u
rel(R)测量回收率0.007 7 0.003 6 0.005 3 u
rel(m)样品称量0.001 4 0.001 4 0.001 4 u(V)定容容量0.000 76 0.000 76 0.000 76
rel仪器进样体积0.005 8 0.005 8 0.005 8
由公式u
crel
 计算可得3 种β-受体激动剂的合成不确定度,结果列于表9。2.4 扩展不确定度及结果表示
计算可得3 种β-受体激动剂的合成不确定度,结果列于表9。2.4 扩展不确定度及结果表示
依据JJF 1135—2005,对于大多数测量采用包含因子k=2衡量,则β-受体激动剂含量的扩展不确定度U=
 由此得到超高效液相色谱-串联质谱法测定猪肉中3 种β-受体激动剂含量的结果,见表9。
由此得到超高效液相色谱-串联质谱法测定猪肉中3 种β-受体激动剂含量的结果,见表9。
表9 不确定度评定结果
Table 9 Uncertainty evaluation for the determination of threeβ-agonists

项目沙丁胺醇盐酸克伦特罗莱克多巴胺合成相对不确定度u
crel(X)0.063 2 0.060 0 0.062 1实测值
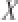 /(μg/kg)1.99 2.04 1.97扩展不确定度U/(μg/kg)0.25 0.24 0.24检测结果(k=2)/(μg/kg)1.99±0.25 2.04±0.24 1.97±0.24
/(μg/kg)1.99 2.04 1.97扩展不确定度U/(μg/kg)0.25 0.24 0.24检测结果(k=2)/(μg/kg)1.99±0.25 2.04±0.24 1.97±0.24
3 结 论
实验过程中,称量、提取、净化、质谱测定等过程均会引入不确定度,本实验通过对实验室温度、玻璃仪器、溶液配制、稀释、重复测定、回收率、质量、体积等因素的考虑,发现超高效液相色谱-串联质谱法测定猪肉中的3 种β-受体激动剂方法中,标准曲线拟合过程和标准溶液配制所产生的不确定最大,其次为测量重复性和体积量取引入的不确定度分量。因此,在实际操作过程中,可通过增加混合标准系列溶液的测定次数,增加平行样品测定,保持超高效液相色谱-串联质谱仪器较高的灵敏度,并定期对所涉仪器进行检定和提高操作人员的熟练水平,来减小测量不确定度,从而保证检测结果的准确性。
参考文献:
[1] 国家质量技术监督局. 测量不确定度评定与表示: JJF 1059.1—2012[S].北京: 中国计量出版社, 2012.
[2] DAESELEIRE E, VANDEPUTTE R, van PETEGHEM C. Validation of multiresidue methods for the detection of anabolic steroids by GCMS in muscle tissues and urine samples from cattle[J]. The Analyst, 1998, 123: 2595-2598.
[3] STOLKER A A M, ZOONTJES P W, van GINKELL L A. The use of super critical fluid extraction for the determination of steroids in animal tissues[J]. The Analyst, 1998, 123: 2671-2676.
[4] 邱阳生, 杨根海, 何方洋. β-兴奋剂沙丁胺醇及其检测技术研究进展[J]. 动物医学进展, 2002, 23(4): 50-52. DOI:10.3969/ j.issn.1007-5038.2002.04.013.
[5] 翟福丽, 赖克强, 张衍亮, 等. 动物性食品中β-兴奋剂残留概述[J]. 食品科学, 2011, 32(5): 351-356.
[6] 农业部. 禁止在饲料和动物饮用水中使用的药物品种录[B]. (2002-02-09).
[7] 农业部. 兽药管理条例实施细则[B]. (1988-06-30).
[8] 农业部. 关于严禁非法使用兽药的通知[B]. (1997-03-25).
[9] 张改平, 王选年, 肖肖. 瘦肉精的毒害作用及其试纸快速检测技术[J]. 中国动物检疫, 2011, 28(5): 1-6. DOI:10.3969/j.issn.1005-944X.2011.05.001.
[10] MITCHELL G A, DUNNAVAN G. Illegal use of beta-adrenergic agonists in the United States[J]. Canadian Journal of Animal Science, 1998, 76(1): 208-211.
[11] 赵思俊, 郑增忍, 曲志娜, 等. 瘦肉精的危害及监管检测技术[J].中国动物检疫, 2011, 28(4): 1-4.
[12] 路平, 肖肖, 张衍海, 等. 我国瘦肉精监管现状及监管建议[J]. 中国动物检疫, 2011, 28(4): 4-6.
[13] 赵晶晶, 李青山, 李云兰, 等. 气相色谱-质谱法测定动物组织中盐酸克伦特罗残留量不确定度影响因素的研究[J]. 分析实验室, 2009, 28(11): 63-67. DOI:10.3969/j.issn.1000-0720.2009.11.017.
[14] 吕燕, 王琦. 畜禽尿液中盐酸克伦特罗含量测定(GC-MS法)的不确定度的分析[J]. 中国测试技术, 2006, 32(3): 134-136.
[15] 王伟东, 陈圣, 任桂云, 等. ELISA法检测畜禽尿液中盐酸克伦特罗含量的不确定度分析[J]. 畜牧与兽医, 2008, 40(6): 45-46.
[16] 肖静, 赵健亚, 许世勇, 等. ELISA检测饲料中莱克多巴胺的不确定度分析[J]. 中国饲料, 2012, 14(7): 37-39.
[17] 国家质量技术监督局. 化学分析测量不确定度评定: JJF 1135—2005[S].北京: 中国计量出版社, 2005.
[18] 农业部. 动物源性食品中β-受体激动剂残留检测 液相色谱-串联质谱法: 农业部1025号公告—18—2008[S]. 2008.
[19] 张燕, 徐幸, 郭启新, 等. 高效液相色谱-串联质谱法测定牛奶中3 种磺胺类药物残留不确定度的评定[J]. 食品安全质量检测学报, 2015, 6(1): 303-309.
[20] 赵丹霞, 樊垚, 刘嘉亮, 等. 超高效液相色谱-串联质谱法测定调料中罂粟壳生物碱含量的不确定度的评定[J]. 中国调味品, 2013, 38(7): 87-92.
[21] 霍艳敏, 王艳丽, 王骏, 等. 高效液相色谱法测定婴幼儿乳粉中烟酰胺的不确定度评定[J]. 食品科学, 2011, 32(16): 330-333.
[22] 中国实验室国家认可委员会. 2006. 化学分析中不确定度的评估指南: CNAS-GL06: 2006[S]. 北京: 中国计量出版社, 2006.
[23] 合格评定国家认可委员会. 检测和校准实验室能力认可准则(ISO/ IEC 17025: 2005): CNAS-GL01[S]. 北京: 中国计量出版社, 2006: 18-19.
[24] 胡贝贞, 蔡海江, 宋伟华. 茶叶中氟虫腈等8 种农药残留的液相色谱-串联质谱法测定及不确定度评定[J]. 色谱, 2012, 30(9): 889-895.
[25] 崔向云, 张雪峰, 袁凤琴, 等. 超高效液相色谱-串联质谱法测定牛奶中土霉素残留的不确定度评估[J]. 食品安全质量检测学报, 2014, 5(2): 546-550.
[26] 国家质量技术监督局. 常用玻璃量器检定规程: JJF 196—2006[S].北京: 中国计量出版社, 2006.
[27] 李兰英, 丁敏, 徐勤, 等. LC-MS/MS测定猪尿中盐酸克伦特罗不确定度的评定[J]. 中国计量学院学报, 2012, 23(1): 7-12. DOI:10.3969/ j.issn.1004-1540.2012.01.002.
[28] 国家质量技术监督局. 移液器检定规程: JJF 646—2006[S]. 北京: 中国计量出版社, 2006.
[29] 范巧成. Excel在线性回归法测量不确定度评定中的应用[J].理化分析: 化学分册, 2 0 05, 41(9): 678-6 80. DOI:10.332 1/ j.issn:1001-4020.2005.09.021.
Uncertainty Evaluation for the Determination of β-Agonists in Pork by Ultra Performance Liquid Chromatography-Tandem Mass Spectrometry
VNING Xiao, JIN Shaoming, LIANG Ruiqiang, CAO Jin*, ZHANG Qingsheng
(National Institutes for Food and Drug Control, Beijing 100050, China)
Abstract:This study aimed to evaluate the uncertainty of measurement in the determination of salbutamol, clenbuterol hydrochloride and ractompaine in pork by ultra performance liquid chromatography-tandem mass spectrometry (UPLCMS/MS). According to JJF 1135-2005 Evaluation of Uncertainty in Chemical Analysis Measurement and JJF 1059.1-2012 Evaluation and Expression of Uncertainty in Measurement, a mathematical model was established for uncertainty evaluation. The sources of uncertainty that may be introduced were analyzed and each component of uncertainty was quantifi ed for the calculation of the combined uncertainty. The results showed that an expanded uncertainty of 0.25 μg/kg (k = 2) was obtained for the determination of the presence of 1.99 μg/kg salbutamol in pork, the expanded uncertainty was 0.24 μg/kg (k = 2) for the determination of pork samples containing 2.04 and 1.97 μg/kg salbutamol. The preparation of standard solution, curve fi tting and measurement repeatability were found to be the main sources of uncertainty.
Key words:ultra performance liquid chromatography-tandem mass spectrometry (UPLC-MS/MS); salbutamol; clenbuterol hydrochloride; ractompaine; uncertainty; pork
DOI:10.7506/spkx1002-6630-201706049
中图分类号:O657.7
文献标志码:A
文章编号:1002-6630(2017)06-0315-06
引文格式:
宁霄, 金绍明, 梁瑞强, 等. 超高效液相色谱-串联质谱法测定猪肉中β-受体激动剂残留量的不确定度分析[J]. 食品科学, 2017, 38(6): 315-320.
DOI:10.7506/spkx1002-6630-201706049. http://www.spkx.net.cn
NING Xiao, JIN Shaoming, LIANG Ruiqiang, et al. Uncertainty evaluation for the determination of β-agonists in pork by ultra performance liquid chromatography-tandem mass spectrometry[J]. Food Science, 2016, 38(6): 315-320. (in Chinese with English abstract) DOI:10.7506/spkx1002-6630-201706049. http://www.spkx.net.cn
收稿日期:2015-09-16
作者简介:宁霄(1985—),女,助理研究员,硕士,研究方向为食品及化妆品质量控制。E-mail:xiao200730079@hotmail.com
*通信作者:曹进(1970—),男,研究员,博士,研究方向为食品及化妆品质量控制。E-mail:caojin@tsinghua.org.cn



 0.100/
0.100/
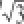 0.100/
0.100/
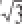 误差不确定度u(V
误差不确定度u(V
 β
β
 β
β
 不确定度u(V
不确定度u(V

 0.02/
0.02/
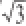 0.015/
0.015/
 0.01/
0.01/
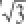 0.01/
0.01/
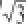 不确定度u(V
不确定度u(V
 0.01/
0.01/
 0.01/
0.01/
 0.005/
0.005/
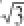 0.005/
0.005/
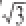 不确定度u(V
不确定度u(V
 β
β
 β
β
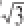 β
β
 β
β
 不确定度u(V
不确定度u(V



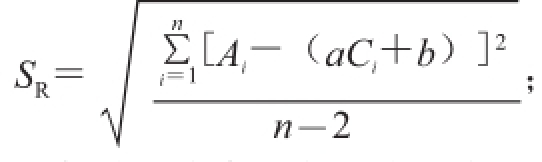 n为测试次数,本实验中5 个质量浓度重复测定2 次,n=5×2=10;p为对C
n为测试次数,本实验中5 个质量浓度重复测定2 次,n=5×2=10;p为对C



 ,标准偏差S(
,标准偏差S(
 结果分别代入公式
结果分别代入公式
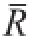 、标准偏差S(R)结果分别代入公式u(R)=
、标准偏差S(R)结果分别代入公式u(R)=

 不确定度来源沙丁胺醇盐酸克伦特罗莱克多巴胺储备液配制0.007 0 0.007 2 0.008 6 u(C)储备液稀释0.008 0 0.008 0 0.008 0
不确定度来源沙丁胺醇盐酸克伦特罗莱克多巴胺储备液配制0.007 0 0.007 2 0.008 6 u(C)储备液稀释0.008 0 0.008 0 0.008 0
 )测量重复性0.006 4 0.006 8 0.007 3 u
)测量重复性0.006 4 0.006 8 0.007 3 u

 /(μg/kg)1.99 2.04 1.97扩展不确定度U/(μg/kg)0.25 0.24 0.24检测结果(k=2)/(μg/kg)1.99±0.25 2.04±0.24 1.97±0.24
/(μg/kg)1.99 2.04 1.97扩展不确定度U/(μg/kg)0.25 0.24 0.24检测结果(k=2)/(μg/kg)1.99±0.25 2.04±0.24 1.97±0.24