
图1 小麦淀粉-油酸包合物的CCII值
Fig.1 Composite index (CI) of wheat starch-oleic acid complexes
徐澎聪 1,王雨生 1,2,陈海华 1,*,秦福敏 1,于 真 1
(1.青岛农业大学食品科学与工程学院,山东 青岛 266109;2.青岛农业大学学报编辑部,山东 青岛 266109)
摘 要:分别采用HCl/KOH法和快速黏度分析(rapid visco analyzer,RVA)法制备小麦淀粉-油酸包合物,并采用差示扫描量热仪、热重分析仪和X-射线衍射仪系统探讨两种制备方法对小麦淀粉-油酸包合物热性质及消化性质的影响规律。结果表明,制备方法影响小麦淀粉-油酸包合物的热性质和消化性质。两种方法制备的小麦淀粉-油酸包合物晶型均为V型;与HCl/KOH法相比,RVA法制备的小麦淀粉-油酸包合物的复合指数、玻璃化转变温度、热分解稳定性、颗粒表面短程结构有序度、慢速消化和抗性淀粉含量升高;相对结晶度、糊化起始温度、焓值、快速消化淀粉含量、水解度、相对消化率和预期血糖指数降低;两种方法制备的小麦淀粉-油酸包合物均属于中血糖指数食物。
关键词:HCl/KOH法;RVA法;小麦淀粉-油酸包合物;热性质;消化性质
淀粉是人类膳食中碳水化合物的主要来源,脂肪酸也是食品的重要成分,淀粉与脂肪酸通过疏水相互作用可形成稳定的、具有单链螺旋结构的淀粉-脂肪酸包合物 [1],能降低淀粉的消化速率,满足人们对低血糖食品的需要 [2]。
淀粉-脂肪酸包合物的制备方法有HCl/KOH法、二甲亚砜(dimethyl sulfoxide,DMSO)/H 2O法、蒸汽喷射蒸煮法、挤压蒸煮法、快速黏度分析(rapid visco analyzer,RVA)法等。Fanta等 [3]利用蒸汽喷射蒸煮法制备的高直链玉米淀粉-棕榈酸钠复合物具有V型晶体结构。Tang等 [1]利用RVA法制备的小麦淀粉-脂肪酸包合物为V型晶体结构。不同方法制备的淀粉-脂肪酸包合物理化性质有差异。Bhatnagar等 [4]利用挤压蒸煮法制备的玉米淀粉-脂肪酸包合物的复合程度,随脂肪酸碳链的延长而降低。Navarro等 [5]研究发现在玉米淀粉糊中添加脂肪酸后,低速冻结条件下可形成复合物。Zabar等 [6]利用HCl/KOH法制备的马铃薯直链淀粉-脂肪酸包合物的熔融温度随结晶温度的升高略有升高。谢涛等 [7]利用DMSO/ H 2O法制备的锥栗直链淀粉-脂肪酸复合物的糊化温度和糊化焓较原淀粉均有不同程度的升高。沙晨希 [8]利用蒸煮糊化法、HCl/KOH法和酒精碱法3 种方法制备了高直链玉米淀粉-乳化剂配合体,结果表明HCl/KOH法制备的样品络合率最高,蒸煮糊化法最低。李爽等 [9]采用热溶液复合-冷却沉淀法、热溶液复合-乙醇脱淀法和混合溶剂复合法制备了具有V型结晶结构的直链淀粉-月桂酸钠复合物,结果表明热溶液复合-冷却沉淀法制备的样品的结晶度最高,热溶液复合-乙醇脱淀法最低。Lalush等 [10]研究发现DMSO/H 2O法制备马铃薯直链淀粉-共轭亚油酸包合物的结晶度大于HCl/KOH法制备的样品。以上研究表明制备方法影响淀粉-脂肪酸包合物的性质,且目前研究较多集中于DMSO/H 2O法和HCl/NaOH法制备的淀粉-脂肪酸包合物的性质研究,关于HCl/KOH法和RVA法对小麦淀粉-油酸包合物结晶结构、热性质和消化性质影响规律的报道较少。
因此本实验分别采用HCl/KOH法和RVA法制备小麦淀粉-油酸包合物,从结晶结构、热性质、热分解稳定性、营养片段、消化规律等方面,系统探讨两种制备方法对小麦淀粉-油酸包合物热性质和消化性质的影响规律,为具有抗消化特性的小麦淀粉-油酸包合物的制备提供依据。
1.1 材料
小麦淀粉(wheat starch,WS,直链淀粉含量28%)南京甘汁园糖业有限公司;油酸(oleic acid,OA,纯度97%)天津巴斯夫化工有限公司;其余试剂均为分析纯。
1.2 仪器与设备
Starchmaster RVA分析仪 澳大利亚New-port公司;752型紫外-可见分光光度计 上海光谱仪器有限公司;DSC1型差示扫描量热仪、TGA1型热重分析仪 瑞士梅特勒-托利多公司;D8 ADVANCE X-射线衍射仪 德国布鲁克AXS有限公司;IS10型傅里叶红外变换光谱(Fourier transform infrared spectroscopy,FTIR)分析仪美国热电尼高力公司。
1.3 方法
1.3.1 样品制备
1.3.1.1 HCl/KOH法
参照陈海华等 [11]的方法,按WS与OA质量比为10∶1,利用HCl/KOH法在复合温度60 ℃条件下制备小麦淀粉-油酸包合物(WS-OA-A)。
1.3.1.2 RVA法
参照Tang等 [1]的方法,按WS与OA质量比为10∶1,利用快速黏度分析仪制备小麦淀粉-油酸包合物(WSOA-RVA)。
1.3.2 小麦淀粉-油酸包合物复合指数的测定
参照Tang等 [1]的方法,测定小麦淀粉-油酸包合物的复合指数(composite index,CI)。
1.3.3 小麦淀粉-油酸包合物的X-射线衍射分析
采用单色Cu-Ka射线,管电压为40 kV,管电流为40 mA进行连续扫描,2θ范围为4°~40°,扫描速率为5 °/min,测定WS-OA包合物的X-射线衍射图谱。样品的相对结晶度(relative crystallinity,RC)采用Jade5.0软件进行计算。
1.3.4 小麦淀粉-油酸包合物的FTIR分析
取1.3.1节中样品2 mg,按质量比为1∶100加入干燥的KBr混合置于玛瑙研钵中研磨均匀后压片,置于FTIR分析仪上测定WS-OA包合物的透光率随波数(400~4 000 cm -1)的变化。采用Omnic 9软件选取波数为800~1 200 cm -1区域的谱图,调整基线,设置半峰宽为30 cm -1和增强因子为1.5,对选取的谱图进行去卷积处理,计算1 047 cm -1和1 022 cm -1处的峰强度比值得到红外指数(R)。
1.3.5 小麦淀粉-油酸包合物热学性质的测定
参照Zabar等 [12]的方法,称取7 mg样品,再加21 mg水置于铝坩埚中,密封后于室温条件下平衡过夜,升温速率为5 ℃/min,扫描温度范围为30~135 ℃,测定WS-OA包合物的热性质。
1.3.6 小麦淀粉-油酸包合物玻璃化转变温度的测定
参照谢涛等 [7]的方法,测定WS-OA包合物的玻璃化转变温度(T g)。
1.3.7 小麦淀粉-油酸包合物热重分析
参照Mansaray等 [13]的方法,取1.3.1节中样品3~5 mg,置于氧化铝坩埚中,氮气速率为50 mL/min,升温速率为10 ℃/min,加热温度范围为30~800 ℃,测定WS-OA包合物的热分解曲线。采用STAR eV13.0软件分析处理热重数据,并主要分析230~380 ℃的热分解参数及最快反应速率对应温度。
1.3.8 小麦淀粉-油酸包合物的消化性测定
参照陈海华等 [11]的方法,测定WS-OA包合物中的快速消化淀粉(rapidly digested starch,RDS)、慢速消化淀粉(slow digestible starch,SDS)、抗性淀粉(resistant starch,RS)的含量;并测定WS-OA包合物的水解度,以小麦淀粉为参比,计算180 min时的相对消化率(relative digestibility,RD)和预期血糖指数(predicted glycemic index,pGI)。
1.4 数据处理
采用SPSS 17.0统计分析软件对数据进行方差分析。
2.1 小麦淀粉-油酸包合物的CI

图1 小麦淀粉-油酸包合物的CCII值
Fig.1 Composite index (CI) of wheat starch-oleic acid complexes
CI值的大小反映淀粉与脂肪酸的复合程度,通常CI值越大,淀粉与脂肪酸的复合程度越高 [1]。由图1可知,WS-OA-RVA包合物的CI值高于WS-OA-A包合物22%。这可能是因为RVA法制备包合物时,小麦淀粉在加热糊化过程中通过分子内氢键作用发生卷曲,形成螺旋的疏水腔,能与油酸络合形成包合物;而HCl/KOH法制备包合物时,淀粉是在热的KOH溶液中形成单螺旋,且KOH溶液可能会导致淀粉发生降解,使直链淀粉分子质量降低,而不利于油酸的络合 [14]。沙晨希 [8]利用蒸煮糊化法、HCl/KOH法和酒精碱法3 种方法制备了高直链玉米淀粉-乳化剂配合体,结果表明HCl/KOH法制备的样品络合率最高,蒸煮糊化法最低。本研究结果与其不一致,可能是由于所采用的脂质原料不同,前者采用的是乳化剂,相对分子质量和空间位阻比较大,而本研究采用的是油酸,相对分子质量和空间位阻较小。
2.2 小麦淀粉-油酸包合物的X-射线衍射图谱
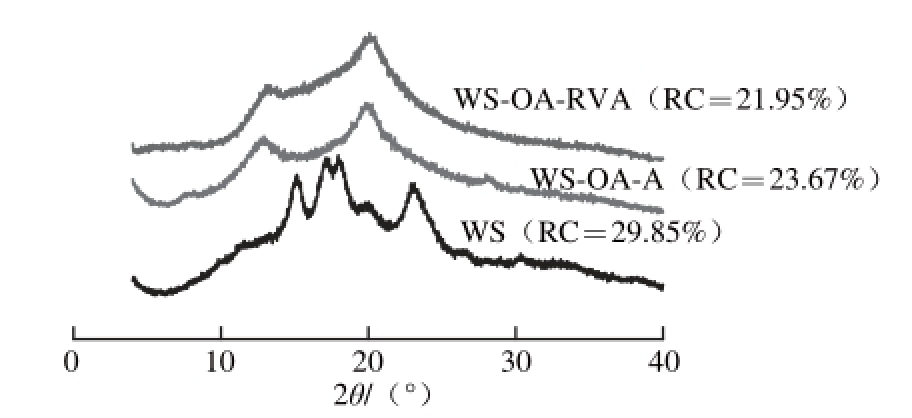
图2 小麦淀粉-油酸包合物的X-射线衍射图谱
Fig.2 X-ray diffraction patterns of wheat starch-oleic acid complexes
由图2可知,小麦淀粉在15.2°、23.1°处有衍射峰,在17.2°、18.1°处有双峰,属于典型的A型晶体结构。包合物WS-OA-A和WS-OA-RVA在13.1°、20.1°处均有衍射峰,属于典型的V型晶体结构,表明两种方法制备的WS-OA的晶体类型均发生改变。Lesmes等 [15]研究表明HCl/KOH法制备的马铃薯直链淀粉-脂肪酸复合物的结晶结构为V型。Tang等 [1]研究结果也表明RVA法制备的小麦淀粉-脂肪酸包合物为V型晶体结构。
与WS相比,两种方法制备的WS-OA包合物的RC均降低,降低了约8%。WS-OA-RVA的RC比WS-OA-A的略低,这可能是由于前者的CI值较高,对小麦淀粉重结晶的阻碍较大,导致包合物的结晶的致密性和有序度较低 [16]。Lalush等 [10]研究表明HCl/KOH法制备的马铃薯直链淀粉-共轭亚油酸包合物的RC比DMSO/H 2O法制备的样品高。
2.3 小麦淀粉-油酸包合物的FTIR分析

图3 小麦淀粉-油酸包合物的FTIRR结果
Fig.3 Fourier-transform infrared spectra of wheat starch-oleic acid complexes
由图3可知,WS和WS-OA-A的红外光谱峰形相似,但WS-OA-A在3 445 cm -1和1 636 cm -1处吸收峰的尖锐性和吸收强度均增强。与WS相比,WS-OA-RVA在3 445 cm -1和1 636 cm -1处吸收峰的尖锐性和吸收强度均减弱,400~600 cm -1的峰形不同。3 445 cm -1处是—OH的伸缩振动峰。WS-OA在3 445 cm -1处的峰向低波数方向移动,可能是由于油酸中的—OH与小麦淀粉中的—OH发生缔合叠加,使小麦淀粉在3 445 cm -1处的峰向低波数方向移动 [17]。WS-OA-RVA的—OH伸缩振动峰比WSOA-A降低了19 cm -1。1 636 cm -1处是O—H弯曲振动峰。与WS相比,WS-OA-A在1 636 cm -1处的吸收峰出峰波数变化不明显;WS-OA-RVA在此处的吸收峰向长波数方向移动,表明油酸的加入减少了样品中的结构水。
2 850 cm -1处是油酸的—CH 2伸缩振动峰。与WS相比,WS-OA包合物在此处出现了吸收峰,表明油酸与小麦淀粉形成了包合物,而不是油酸和小麦淀粉的混合物 [18]。与WS相比,WS-OA-A在1 081 cm -1处的吸收峰向低波数方向移动,表明油酸的加入使C—O数量增多;WS-OARVA在此处的吸收峰向长波数方向移动,表明油酸的加入使羟基数量减少。
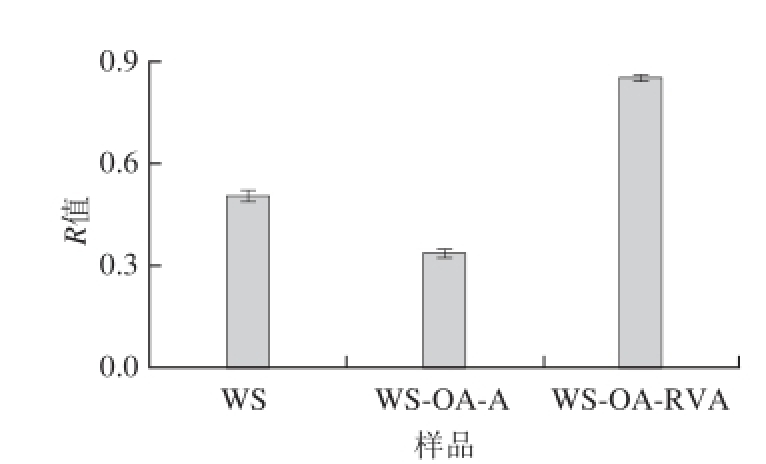
图4 小麦淀粉-油酸包合物的红外指数R值
Fig.4 FTIR index of wheat starch-oleic acid complexes
红外指数R值可反映淀粉颗粒表面的短程有序结构 [19]。由图4可知,WS-OA-A的R值比原淀粉低34%,表明KOH溶液可破坏小麦淀粉颗粒表面的短程有序结构;WS-OARVA的R值比原淀粉高68%,表明RVA法制备的包合物颗粒表面的有序度升高。WS-OA-A的R值比WS-OA-RVA低61%,表明HCl/KOH法制备的包合物颗粒表面的有序度较低,这可能是由于KOH溶液破坏了小麦淀粉颗粒表面的短程有序结构。
2.4 小麦淀粉-油酸包合物的热性质
表1 小麦淀粉-油酸包合物的热性质
Table1 Thermal properties of wheat starch-oleic acid complexes

注:同列肩标小写字母不同表示差异显著(P<0.05)。表4同。
样品T o/℃T p/℃T c/℃T c-T o/℃ΔH/(J/g)WS55.04±0.01 c60.44±0.18 b66.56±0.21 b11.52±0.20 b11.01±0.04 aWS-OA-A98.62±0.01 a100.43±1.75 a109.65±0.47 a11.03±0.46 b5.99±0.21 bWS-OA-RVA87.97±0.12 b96.60±0.07 a104.02±0.07 a16.06±0.05 a4.46±0.11 c
由表1可知,与WS相比,两种方法制备的WS-OA包合物的T o、T p和T c均显著升高,这可能是由于OA的加入抑制了WS的溶解和膨胀导致的 [1]。谢涛等 [7]研究表明锥栗直链淀粉-脂肪酸复合物的T o、T p和T c与原淀粉相比均升高。制备方法也影响WS-OA包合物的热性质。与WSOA-RVA相比,WS-OA-A的T o、T p和T c均升高。熔融温度范围(T c-T o)反映淀粉颗粒内部结晶体的多样化程度,通常(T c-T o)越大,结晶体的多样化程度越高 [20]。由表1可知,WS-OA-RVA的(T c-T o)高于WS-OA-A,表明RVA法制备的包合物中晶体同质性程度较低,形成了稳定性不同的结晶体 [8]。与WS相比,两种方法制备的WS-OA包合物的ΔH分别降低了5.02 J/g和6.55 J/g。这可能是由于糊化过程中小麦淀粉与油酸形成包合物释放热量,使得小麦淀粉的ΔH降低 [21]。WS-OA-RVA的ΔH比WS-OA-A低1.53 J/g,这可能是由于WS-OA-RVA的CI值高于WS-OA-A,因而加热过程中,WS-OA-RVA释放的热量多,对应的ΔH较低。Lalush等 [10]研究表明HCl/KOH法和DMSO/H 2O法对马铃薯直链淀粉-共轭亚油酸包合物的ΔH无显著影响。
2.5 小麦淀粉-油酸包合物的玻璃化转变温度
注:同行肩标小写字母不同表示差异显著(P<0.05)。
 样品WSWS-OA-AWS-OA-RVA T
g/℃-13.75±0.25
b-14.43±0.50
b-5.70±0.00
a
样品WSWS-OA-AWS-OA-RVA T
g/℃-13.75±0.25
b-14.43±0.50
b-5.70±0.00
a
玻璃化转变温度(T
g)是指在冷冻样品中固体基质(固体和未冻结水的混合物)发生玻璃化转变时的温度
[22]。T
g可以预测食品的质量稳定性,从而确定有效的加工和贮藏条件。由表2可知,WS-OA-A的T
g比原淀粉低0.7 ℃,这可能是由于KOH溶液使淀粉分子降解,淀粉分子质量下降,导致T
g降低
[23]。谢涛
[7]、Raphaelides
[24]等的研究均表明脂肪酸的加入能降低淀粉的T
g。WS-OA-RVA的T
g比原淀粉高8 ℃,Kibar等
[22]研究也发现玉米淀粉-油酸包合物的T
g高于原淀粉。WS-OA-RVA的T
g比WS-OA-A高8.73 ℃,这可能是因为WS-OA-RVA的CI值较高,因而含有较多的油酸,既能在淀粉颗粒周围形成不溶性膜,阻止水和包合物进出;同时又可阻止可溶性碳水化合物的渗出,降低有效水含量,从而降低水的增塑作用提高包合物的
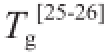 。
。
2.6 小麦淀粉-油酸包合物的热分解性质
表3 小麦淀粉-油酸包合物的230~380 ℃段热分解动力学参数
Table3 Thermal decomposition parameters of wheat starch-oleic acid complexes in the temperature range of 230-380 ℃

最快反应速率对应温度/℃WS251~34665.736.92313.0 WS-OA-A238~36168.275.55314.3 WS-OA-RVA258~38167.365.48312.7样品热分解温度范围/℃质量损失率/%平均降解速率/(%/min)
230~380 ℃的温度范围主要反映WS或WS-OA包合物的解聚和分解过程 [27]。从表3可以看出,WS和WS-OA包合物的平均降解速率为5~7 %/min,质量损失率为65%~68%。此温度范围内WS-OA-RVA的起始分解温度比WS-OA-A高约20 ℃,表明WS-OA-RVA热分解稳定性高于WS-OA-A。这可能是因为WS-OA-RVA的CI值较高而复合了较多的油酸,因此其热分解稳定性较高。WSOA-A的此温度范围的平均降解速率和质量损失率均高于WS-OA-RVA,表明WS-OA-A较易发生热分解。WS-OA-A的最快反应速率对应的温度比WS-OA-RVA高,这与DSC测定糊化温度的结果一致。
2.7 小麦淀粉-油酸包合物的体外消化性质
2.7.1 酶解后小麦淀粉-油酸包合物的营养片段分析
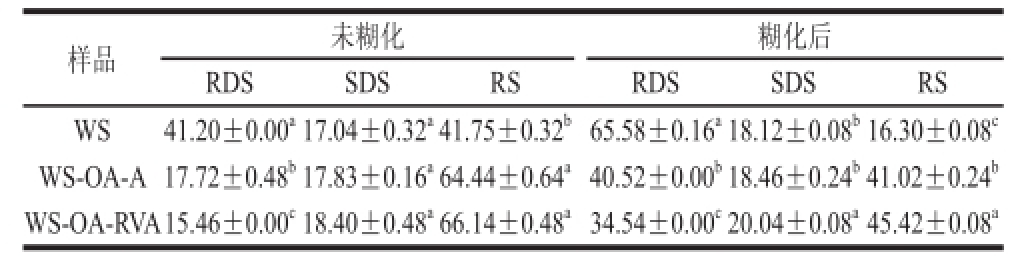
表4 小麦淀粉-油酸包合物中RDS、SDS、RS的含量
Table4 Contents of RDS, SDS and RS in wheat starch-oleic acid complexes %
?
由表4可知,与WS相比,糊化前及糊化后的WS-OA包合物中RDS的含量减小,RS含量增大,SDS含量变化不明显,表明包合物的形成抑制了小麦淀粉的消化,使其具有抗消化的特性。
糊化前及糊化后WS-OA-RVA的RDS含量分别比WSOA-A低2.26%、5.98%,表明RVA法制备的包合物对小麦淀粉消化的抑制程度较高。糊化前及糊化后WS-OARVA和WS-OA-A的SDS含量差异不显著。糊化前及糊化后WS-OA-RVA的RS含量分别比WS-OA-A高1.70%、4.40%,表明RVA法制备的包合物中抗性淀粉的含量较高,这可能是由于WS-OA-RVA的CI较高,对酶解的阻碍作用较大,抗消化程度较高 [28]。
2.7.2 小麦淀粉-油酸包合物的酶解动力学
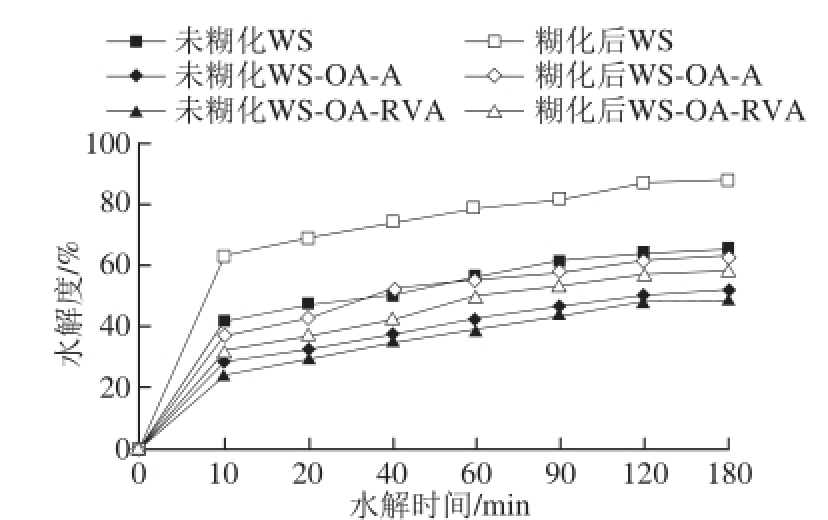
图5 糊化前后小麦淀粉-油酸包合物的水解度
Fig.5 Hydrolysis rate of wheat starch-oleic acid complexes before and after pasting
由图5可知,90 min内WS-OA包合物的水解度上升较快;90~180 min水解度增速减慢并逐渐达到平衡。与未糊化样品相比,糊化后的样品水解度增大,与营养片段测定结果相一致。这可能是因为样品糊化后,伸展的淀粉分子能够与酶的结合位点充分结合,促进淀粉酶酶解 [11]。与小麦淀粉相比,糊化前与糊化后WS-OA包合物的水解度均降低,表明包合物的形成抑制淀粉水解,与陈海华等 [11]的研究结果相一致。这可能是由于WS-OA包合物的糊化温度较高而不能充分糊化,包合物的形成抑制了淀粉颗粒的溶胀,从而降低淀粉的水解度 [2]。
WS-OA-RVA的水解度低于WS-OA-A,这可能是因为RVA法制备的包合物CI值较高,形成包合物的数量较多,对淀粉水解的抑制作用较强。
表5 小麦淀粉-油酸包合物的体外消化动力学参数
Table5 Kinetic parameters for in vittrroo digestibility of wheat starch-oleic acid complexes
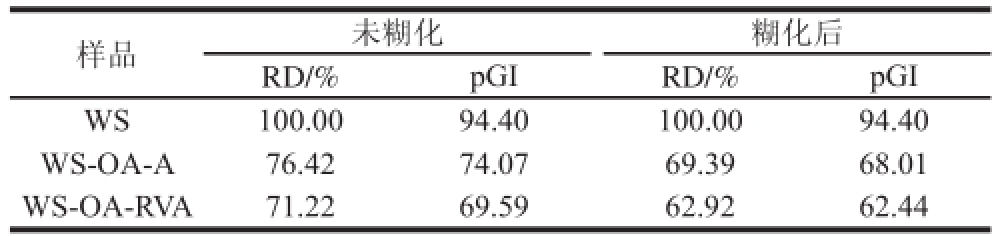
 样品
未糊化糊化后RD/%pGIRD/%pGI WS100.0094.40100.0094.40 WS-OA-A76.4274.0769.3968.01 WS-OA-RVA71.2269.5962.9262.44
样品
未糊化糊化后RD/%pGIRD/%pGI WS100.0094.40100.0094.40 WS-OA-A76.4274.0769.3968.01 WS-OA-RVA71.2269.5962.9262.44
RD表示水解180 min时的相对消化率。淀粉的pGI可以有效地预测摄入的淀粉基食物的血糖反应,根据食物的GI划分3 个等级,GI≥70的食物是高GI食物,55<GI<70的食物为中GI食物,GI≤55的食物是低GI食物 [29]。由表5可知,制备方法影响小麦淀粉-油酸包合物的体外消化动力学参数。糊化后的WS-OA包合物的RD和pGI均低于糊化前。这与陈海华等 [11]的研究结果相一致。糊化前WS-OA-RVA的RD和pGI分别比WS-OA-A低5.20%、4.48,糊化后WS-OA-RVA的RD和pGI分别比WSOA-A低6.47%和5.57,与水解度的测定结果相一致。由表5可以看出,糊化前及糊化后WS-OA包合物的pGI值均在55~75之间,属于中GI食物 [29-30]。
WS-OA-RVA的CI值高于WS-OA-A。WS-OA-RVA的RC低于WS-OA-A,两种包合物均为V型。与WS-OA-A相比,WS-OA-RVA的T o和ΔH降低。WS-OA-A的T g低于WSOA-RVA。WS-OA-RVA热分解稳定性高于WS-OA-A。FTIR图谱表明小麦淀粉与油酸形成了包合物。WS-OA-A的颗粒表面短程结构有序度低于WS-OA-RVA。与WSOA-A相比,WS-OA-RVA的RDS含量降低,SDS和RS含量升高。WS-OA-RVA的水解度低于WS-OA-A。糊化前及糊化后WS-OA-RVA的RD和pGI均低于WS-OA-A。
参考文献:
[1] TANG M C, COPELAND L. Analysis of complexes between lipids and wheat starch[J]. Carbohydrate Polymers, 2007, 67(1): 80-85. DOI:10.1016/j.carbpol.2006.04.016.
[2] AI Y, HASJIM J, JANE J L. Effects of lipids on enzymatic hydrolysis and physical properties of starch[J]. Carbohydrate Polymers, 2013, 92(1): 120-127. DOI:10.1016/j.carbpol.2012.08.092.
[3] FANTA G F, KENAR J A, BYARS J A, et al. Properties of aqueous dispersions of amylose-sodium palmitate complexes prepared by steam jet cooking[J]. Carbohydrate Polymers, 2010, 81(3): 645-651. DOI:10.1016/j.carbpol.2010.03.026.
[4] BHATNAGAR S, HANNA M A. Amylose-lipid complex formation during single-screw extrusion of various corn starches[J]. Cereal Chemistry, 1994, 71(6): 582-587.
[5] NAVARRO A S, MARTINO M N, ZARITZKY N E. Effect of freezing rate on the rheological behaviour of systems based on starch and lipid phase[J]. Journal of Food Engineering, 1995, 26(4): 481-495. DOI:10.1016/0260-8774(94)00074-J.
[6] ZABAR S, LESMES U, KATZ I, et al. Structural characterization of amylose-long chain fatty acid complexes produced via the acidif i cation method[J]. Food Hydrocolloids, 2010, 24: 347-357. DOI:10.1016/ j.foodhyd.2009.10.015.
[7] 谢涛, 张儒. 锥栗直链淀粉-脂肪酸复合物的热特性[J]. 中国粮油学报, 2012, 27(7): 38-41. DOI:10.3969/j.issn.1003-0174.2012.07.008.
[8] 沙晨希. 高直链玉米淀粉配合体的构建及其慢消化性研究[J]. 无锡:江南大学, 2013: 8-10.
[9] 李爽, 荆晓艳, 杨留枝, 等. V型直链淀粉-月桂酸钠复合物的制备方法研究[J]. 河南工业大学学报(自然科学版), 2014, 35(3): 37-44. DOI:10.16433/j.cnki.issn1673-2383.2014.03.012.
[10] LALUSH I, BAR H, ZAKARIA I, et al. Utilization of amylose-lipid complexes as molecular nanocapsules for conjugated linoleic acid[J]. Biomacromolecules, 2005, 6(1): 121-130. DOI:10.1021/bm049644f.
[11] 陈海华, 王雨生, 王慧云, 等. 脂肪酸碳链长度与不饱和度对脂肪酸-普通玉米淀粉包合物的体外消化性质的影响[J]. 现代食品科技, 2016, 32(2): 1-10. DOI:10.13982/j.mfst.1673-9078.2016.2.004.
[12] ZABAR S, LESMES U, KATZ I, et al. Studying different dimensions of amylose-long chain fatty acid complexes: molecular, nano and micro level characteristics[J]. Food Hydrocolloids, 2009, 23(7): 1918-1925. DOI:10.1016/j.foodhyd.2009.02.004.
[13] MANSARAY K G, GHALY A E. Determination of kinetic parameters of rice husks in oxygen using thermogravimetric analysis[J]. Biomass and Bioenergy, 1999, 17(1): 19-23. DOI:10.1016/S0961-9534(99)00022-7.
[14] HAHN D E, HOOD L F. Factors influencing corn starch-lipid complexing[J]. Cereal Chemistry, 1987, 64(2): 81-85.
[15] LESMES U, SHAHAR H C, YIZHAK S, et al. Effects of long chain fatty acid unsaturation on the structure and controlled release properties of amylose complexes[J]. Food Hydrocolloids, 2009, 23(3):667-675. DOI:10.1016/j.foodhyd.2008.04.003.
[16] BIENKIEWICZ G, KOŁAKOWSKA A. Effects of thermal treatment on fish lipids-amylose interaction[J]. European Journal of Lipid Science and Technology, 2004, 106(6): 376-381. DOI:10.1002/ ejlt.200300925.
[17] 钱志伟, 杨留枝, 秦令祥, 等. V-型直链淀粉-油酸复合物的制备与结构表征[J]. 食品科技, 2011, 36(7): 229-232. DOI:10.13684/j.cnki. spkj.2011.07.054.
[18] 刘晴晴, 胡飞, 李晓玺. 不同类型直链淀粉-硬脂酸复合物的微观特性[J]. 食品与发酵工业, 2013, 39(9): 18-21. DOI:10.13995/ j.cnki.11-1802/ts.2013.09.020.
[19] SOEST J J G V, TOURNOIS H, WIT D D, et al. Short-range structure in (partially) crystalline potato starch determined with attenuated total ref l ectance Fourier-transform IR spectroscopy[J]. Carbohydrate Research, 1995, 279: 201-214. DOI:10.1016/0008-6215(95)00270-7.
[20] CHAVAN U D, SHAHIDI F, HOOVER R, et al. Characterization of beach pea (Lathyrus maritimus L.) starch[J]. Food Chemistry, 1999, 65(1): 61-70. DOI:10.1016/S0308-8146(98)00158-7.
[21] MESTRES C, MATENCIO F, PONS B, et al. A rapid method for the determination of amylose content by using differential scanning calorimetry[J]. Starch-Stärke, 1996, 48(1): 2-6. DOI:10.1002/ star.19960480103.
[22] KIBAR E A A, GÖNENG I, US F. Effects of fatty acid addition on the physicochemical properties of corn starch[J]. International Journal of Food Properties, 2004, 17(1): 204-218. DOI:10.1080/10942912.2011.6 19289.
[23] 詹世平, 陈淑花, 刘华伟, 等. 分子量对淀粉玻璃化转变温度的影响[J]. 食品工业科技, 2006, 27(3): 55-57. DOI:10.3969/ j.issn.1002-0306.2006.03.015.
[24] RAPHAELIDES S N, ARSENOUDI K, EXARHOPOULOS S, et al. Effect of processing history on the functional and structural characteristics of starch-fatty acid extrudates[J]. Food Research International, 2010, 43(1): 329-341. DOI:10.1016/j.foodres.2009.10.016.
[25] HOOVER R, HADZIYEV D. Characterization of potato starch and its monoglyceride complexes[J]. Starch-Stärke, 1981, 33(9): 290-300. DOI:10.1002/star.19810330903.
[26] LONKHUYSEN H, BLANKESTIJN J. Inf l uence of monoglycerides on the gelatinization and enzymatic breakdown of wheat and cassava starch[J]. Starch-Stärke, 1976, 28(7): 227-233. DOI:10.1002/ star.19760280705.
[27] AGGARWAL P, DOLLIMORE D. A thermal analysis investigation of partially hydrolyzed starch[J]. Thermochimica Acta, 1998, 319(1):17-25. DOI:10.1016/S0040- 6031(98)00355-4.
[28] TESTER R F, DEBON S J J, SOMLNERVILLE M D. Annealing of maize starch[J]. Carbohydrate Polymers, 2000, 42(3): 287-299. DOI:10.1016/S0144-8617(99)00170-8.
[29] MIAO M, JIANG B, ZHANG T, et al. Impact of mild acid hydrolysis on structure and digestion properties of waxy maize starch[J]. Food Chemistry, 2011, 126(2): 506-513. DOI:10.1016/j.foodchem.2010.11.031.
[30] ANNOR G A, MARCONE M, CORREDIG M, et al. Effects of the amount and type of fatty acids present in millets on their in vitro starch digestibility and expected glycemic index (eGI)[J]. Journal of Cereal Science, 2015, 64: 76-81. DOI:10.1016/j.jcs.2015.05.004.
Effect of Preparation Methods on Thermal Properties and Digestibility of Wheat Starch-Oleic Acid Inclusion Complexes
XU Pengcong
1, WANG Yusheng
1,2, CHEN Haihua
1,*, QIN Fumin
1, YU Zhen
1
(1. College of Food Science and Engineering, Qingdao Agricultural University, Qingdao 266109, China; 2. Editorial Department of Journal of Qingdao Agricultural University, Qingdao 266109, China)
Abstract:The effect of two different preparation methods, namely HCl/KOH and rapid visco analyzer (RVA), on thermal properties and digestibility properties of wheat starch-oleic acid inclusion complexes was studied by differential scanning calorimetry, thermogravimetric analyzer and X-ray diffraction. The results indicated that different preparation methods affected thermal properties and digestibility properties of wheat starch-oleic acid inclusion complexes. The crystal types of wheat starch-oleic acid inclusion complexes prepared by both methods were type-V. Wheat starch-oleic acid inclusion complexes prepared by RVA method revealed an increase in complex index, glass transition temperature, thermal decomposition stability, ordered degree of short-range structure of particle surface, and the contents of slowly digestive starch and resistant starch and a decrease in relative crystallinity, onset temperature, gelatinization enthalpy, the content of rapidly digestive starch, hydrolysis degree, relative digestibility and predicted glycemic index compared with those prepared by HCl/KOH method. These two samples had a medium glycemic index.
Key words:HCl/KOH method; RVA method; wheat starch-oleic acid complex; thermal properties; digestibility
DOI:10.7506/spkx1002-6630-201703002
中图分类号:TS236
文献标志码:A
文章编号:1002-6630(2017)03-0007-06
引文格式:
徐澎聪, 王雨生, 陈海华, 等. 制备方法对小麦淀粉-油酸包合物的热性质及消化性质的影响[J]. 食品科学, 2017, 38(3):7-12. DOI:10.7506/spkx1002-6630-201703002. http://www.spkx.net.cn
XU Pengcong, WANG Yusheng, CHEN Haihua, et al. Effect of preparation methods on thermal properties and digestibility of wheat starch-oleic acid inclusion complexes[J]. Food Science, 2017, 38(3): 7-12. (in Chinese with English abstract)
DOI:10.7506/spkx1002-6630-201703002. http://www.spkx.net.cn
收稿日期:2016-04-05
基金项目:山东省自然科学基金项目(ZR2016CM17);国家自然科学基金面上项目(31671814);山东省高等学校中青年骨干教师国际合作培养项目(SD-20130825);青岛农业大学研究生创新计划项目(QYC201419)
作者简介:徐澎聪(1993—),男,硕士研究生,研究方向为食品化学。E-mail:1154421016@qq.com
*通信作者:陈海华(1973—),女,教授,博士,研究方向为食品化学。E-mail:haihchen@163.com