表 1 美国EPA公布的16 种优先控制的PAHs
Table 1 Sixteen priority-controlled PAHs listed by the USEPA
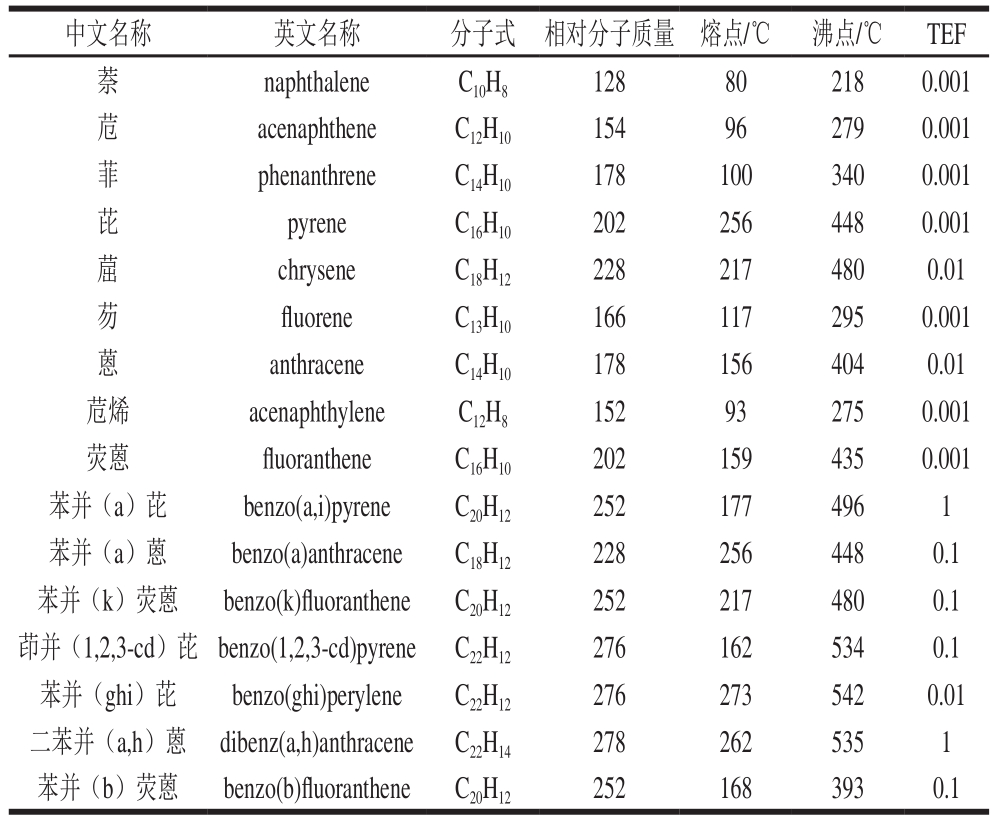
注:TEF.毒性当量因子(toxicity equivalency factor);表中假设苯并(a)芘的毒性当量因子为1,其他皆以此为参照。
聂 文1,屠泽慧1,占剑峰2,蔡克周1,*,姜绍通1,陈从贵1
(1.合肥工业大学食品科学与工程学院,安徽省农产品精深加工重点实验室,安徽 合肥 230009;2.黄冈师范学院生命科学学院,湖北 黄冈 438000)
摘 要:多环芳烃是一类对环境和食品极具危害的污染物。早期对环境中多环芳烃的检测、安全评价、食品加工过程中的污染及产生的机理和控制方法开展了大量的工作,本文重点对多环芳烃形成的化学机制及食品加工过程中多环芳烃的产生机制进行综述,并对研究现状进行简要总结,以期为食品中多环芳烃控制提供新思路。
关键词:多环芳烃;化学机制;食品加工过程;生成机理
多环芳烃(polycyclic aromatic hydrocarbons,PAHs)是一类分子中含有两个或两个以上苯环的碳氢化合物[1],最初是在化石燃料和木材等有机物燃烧烟雾中发现的[2],其广泛分布在自然环境中[3]。早期细胞和动物学实验研究发现4~6 环的稠环PAHs具有致癌、致畸和致突变毒性,这些稠环PAHs在体内的代谢产物可以与细胞中DNA分子共价结合,诱发DNA复制错误和增加突变的概率,从而导致癌症[4-5]。人类经常通过皮肤、呼吸、摄入受污染的水和食物接触到这些PAHs,其中有16 种PAHs已被美国国家环境保护局(Environmental Protection Agency,EPA)列为优先控制污染物[6](表1)。
根据流行病学研究显示,食品是人类摄入PAHs的主要途径之一,食品中的PAHs主要来源于环境污染和高温油炸、烧烤和烟熏等剧烈的加工行为[7]。烟熏食品是现有报道中PAHs含量最多的食品,烟熏食品中的PAHs污染程度与加工过程和条件密切相关,如烟熏木材的类型、氧气的供应、燃烧温度、与热源的距离、烟熏时间等[8-9]都会影响烟熏食品中PAHs的含量。烟熏过程中使用软木作为烟熏材料会导致产品中PAHs的含量增多[10]。烟熏产品自身特性如脂肪含量也对烟熏产品中PAHs的含量有所影响[11],这主要是由于PAHs具有亲脂性,脂肪含量偏高的食品,更容易扩散迁移到食品的里层[12]。
表 1 美国EPA公布的16 种优先控制的PAHs
Table 1 Sixteen priority-controlled PAHs listed by the USEPA

注:TEF.毒性当量因子(toxicity equivalency factor);表中假设苯并(a)芘的毒性当量因子为1,其他皆以此为参照。
近30 年来,国外对于环境和食品中PAHs的分离检测、安全评价、控制方法及产生机理等方面做了较为深入的研究,而我国对PAHs的研究起步较晚,并且大多集中在环境、化石燃料及PAHs的检测等方面,有关PAHs生成机理的研究较少。本文重点对PAHs形成的化学机制及食品加工过程中PAHs的产生机制进行综述,并对研究现状进行简要总结,以期为肉制品中PAHs控制提供新思路。
早在20世纪50年代末,澳大利亚学者Badger等[13]就对PAHs的生成机理进行了探索,并且对PAHs的生成机理做出大胆的假设:他首先猜想有机质在高温缺氧的条件会发生裂解生成碳氢自由基,这些碳氢自由基反应生成乙炔,乙炔分子经过聚合反应合成乙烯基乙炔或1,3-丁二烯,乙烯基乙炔或1,3-丁二烯再经过环化作用生成乙基苯,乙基苯进一步反应生成丁基苯和四氢化萘,丁基苯和四氢化萘结合反应生成中间体,最后由中间体合成苯并芘,具体过程如图1所示。
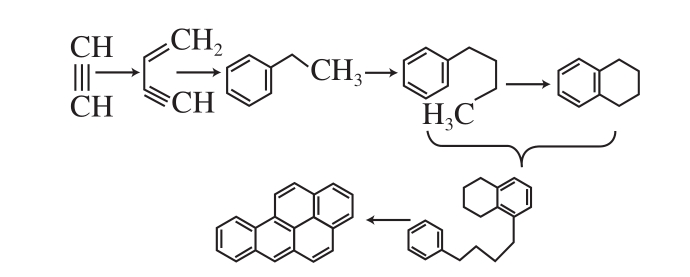
图 1 Badger提出的苯并芘可能的合成机理
Fig. 1 Possible synthesis mechanism of benzene proposed by Badger
Badger等的猜想是从含两个碳原子的化合物开始的,但是我国学者黄靖芬等[14]在研究烟熏食品中苯并芘的生成机理时发现苯并芘的合成不一定非要从两个碳原子的化合物开始,可以从任意中间体开始反应合成苯并芘。
Bittner等[15]在20世纪80年代初提出了PAHs生成的另一种可能性:首先苯环脱氢生成苯基,甲醛进行羟醛缩合等一系列反应生成乙烯,然后乙烯与苯基发生取代反应生成2-苯基乙烯基,苯乙烯基接着与甲醛反应生成苯丁烯基,最后通过环化生成萘。该反应机理在反应温度较低的情况下更容易实现。
Wang Hai和Frenklach[16]在20世纪90年代末研究发现,在温度较高时由Bitter-Howard机理产生的PAHs含量较少,因此他们提出了生成PAHs的第二个环的另一条途径:首先苯环脱氢形成苯基,苯基与1-丁烯-3-炔反应生成1-苯基-1,3-丁二烯基,接着进行一系列反应生成2-(2-甲基-1,3-丁二烯基)-1-苯基,最后经过环化作用生成萘。具体过程如图2所示。该机理可以很好地模拟在燃烧等高温条件下PAHs的生成机理。

图 2 生成PAHs第二个苯环的机理
Fig. 2 Formation mechanism of the second benzene ring of PAH
Wang Hai[16]和赵霏阳[17-18]等通过建立模型,较为完善地描述了从C2HX到C6HX的分子生长过程和苯环的形成,他们认为苯环一旦形成,就能根据分子大小顺序,通过HACA(氢原子脱除-乙炔分子添加)反应生成萘、菲和芘。研究发现可以通过以下基元反应生成苯环:1)—C≡C—CH3和—C≡C—CH3反应合成苯环;2)—CH=CH—CH=CH—和CH≡CH反应生成苯基;3)—CH=CH—CH=CH2和CH≡CH反应生成苯环;4)由—C≡C—CH=CH—CH=CH2直接生成苯基;5)IC6H6和氢反应生成苯环。形成苯环以后,苯环进行脱氢形成苯基,苯基和乙炔进行HACA反应生成苯乙烯,苯乙烯加氢再脱氢气形成2-乙炔基-1-苯基自由基,2-乙炔基-1-苯基自由基与乙炔发生HACA反应生成2-萘基,2-萘基和乙炔发生取代脱氢生成2-乙炔基萘,2-乙炔基萘进一步加氢脱氢气生成2-乙炔基-3-萘基,2-乙炔基-3-萘基重复与乙炔发生HACA反应,逐步实现芳香烃分子的生长和PAHs的环化,最终生成芘,具体反应过程如图3所示。
Tao Feng等[19]研究发现在HACA反应中,通过乙炔分子添加反应形成的4 个以上的苯环十分稳定,例如芘和六苯并芘等。而且HACA反应的吉布斯自由能变化较大,说明这些反应是不可逆的,从而就把反应机理引向了PAHs生成的方向,又因为PAHs是一个热动力学稳定的物质,所以可以通过HACA机理实现PAHs的不断生长。
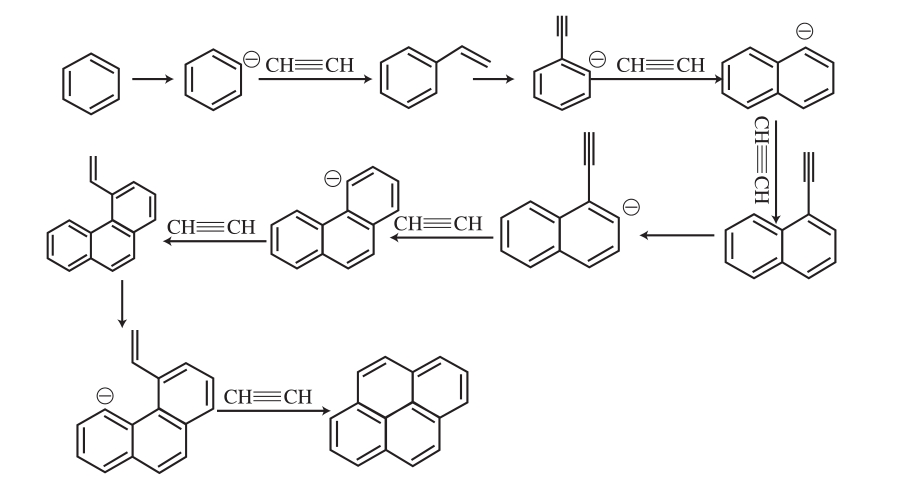
图 3 苯环通过HACA反应生成PAHs的过程
Fig. 3 Generation of PAHs by HACA reaction of benzene ring
2011年Hong Zekai等[20]以C10H22、C8H18为例较为详细地描述了PAHs的生成机理。以C10H22为例:首先C10H22脱氢生成C10H21,接着裂解产生C10H20、C2H5和C2H4,然后反应被分成两条路径:1)C10H20→C2H5+C3H6,C2H5→C2H4,C3H6→C3H5→C3H4→C3H3,期间C3H6→C2H3,C3H5、C3H4可以反应生成C2H2;2)C2H4经过一系列的反应脱氢生成C2H2,最终生成C3H3与上一条路径汇合。C3H3进一步发生反应,这时反应过程又被分成了5 条途径:1)C3H3→C5H5→Nap→Phe→Pyr;2)C3H3→Al→Nap→Phe→Pyr;3)C3H3→Al→Nap→Pyr;4)C3H3→A l→C9H8→C9H7→P h e→P y r;5)C3H3→Al→C9H8→C9H7→Pyr。由此可见,HACA是PAHs形成的重要步骤,C2H2和C3H3是形成PAHs的重要前体物。Chen等[21]研究发现苯类化合物可能也是PAHs合成的重要前体物之一。
食品中PAHs的形成是一个十分复杂的过程,烟熏食品中PAHs的来源主要有以下几个途径:1)烟熏燃料和食品在烟熏加工过程中发生高温热解,产生化学性质活泼的碳氢自由基和一些分子质量较小的低环类化合物,这是烟熏食品中PAHs生成的主要前体物,这些前体物在高温条件下可能按Badger-Howard机理发生环化聚合反应生成PAHs。2)食品本身含有的一些分子质量较低的不饱和烃类化合物,这些不饱和前体物可能按C2HX分子氧化机理发生芳构化形成苯环,然后在高温条件下按HACA分子生长机理经过一系列的缩合聚合形成PAHs。3)食品中存在一些单环化合物,在烟熏过程中苯环上的碳键断裂,然后可能按Frenklach机理经过一系列的缩合聚合形成PAHs。
Chen[21]和Lomanno[22]等研究发现PAHs的形成与脂肪有着很大的关系并且做出了大胆的假设:脂肪酸在被氧化的过程中可以生成氢过氧化物,氢过氧化物通过分子内环化生成环己烯等环状化合物,最终生成苯环,再通过HACA机理实现分子生长形成PAHs。
Uriarte[23]和Heinonen[24]等在研究油炸作用下PAHs的生成时发现,亚油酸和亚麻酸等多不饱和脂肪酸可以通过聚合反应生成环状单体,最终形成含有苯环的PAHs前体物。并且亚麻酸、亚油酸能够降解,分别产生甲苯和丁基苯。Cheng Weiwei等[25]在研究芝麻油加工过程中PAHs的形成时,发现在热压条件下芝麻油中PAHs的含量显著高于冷压条件下的,这说明温度是影响脂肪酸向PAHs转变的一个重要因素。Perelló等[26]也得出了同样的结论。
Cheng Weiwei等[25]研究发现在80~280 ℃条件下,通过添加芝麻子蛋白,PAHs数量急剧增加,这表明PAHs主要来自芝麻蛋白和甘油三酯的热解反应,并推测氨基酸可能是PAHs形成的重要前体物之一。Luo Yan等[27]的研究结果表明甘油三酯裂解过程中Diels-Alder反应和分子间及分子内烷基、烷烯基的自由基反应都会生成环状的烷烃化合物,所以Diels-Alder反应是PAHs生成过程中的重要反应,并且该反应对温度要求不高,符合肉制品在烟熏时的条件。
Chen等[21]研究加热模型血脂和食用油脂烟气中PAHs的形成时,发现脂肪酸降解产物中亚麻酸甲酯生成PAHs的含量最高,其次是亚油酸甲酯、油酸甲酯和甲基硬脂酸,造成这一结果可能是受不饱和程度的影响。Stumpe-Viksna等[28]在研究不同木材对烟熏肉中PAHs的影响时,发现软木作为烟熏材料时生成PAHs量高于硬木,可能是因为软木中含有较多的树脂,间接说明了脂肪类化合物是生成PAHs的重要前体物。Viegas等[29]在研究不同类型木炭烤肉中PAHs的形成时,发现鸡肉和猪肉中PAHs的含量较牛肉中多,这可能与原料肉中脂肪含量有关,脂肪滴在木炭上形成携带PAHs的烟雾并附着在肉制品的表面,导致烤肉中PAHs含量增多。Naccari[30]和Londoño[31]等通过研究奶制品经过高温热处理后PAHs含量的变化,发现牛奶样品中PAHs的含量顺序为:原料奶<巴氏杀菌奶<超高温半脱脂奶<超高温全脂奶,全脂奶和半脱脂奶在经过超高温处理后,PAHs的含量有所差异,这可能与牛奶中脂肪含量和甘油三酯的脂溶性活动有关。以上研究都说明了脂肪是食品中生成PAHs的主要成分。Luzardo[32]、Olatunji[33]和Kao[34]等也得出过一致的结论。
1992年Chiavari等[35]提出了氨基酸分解的4 种主要途径,如图4所示。
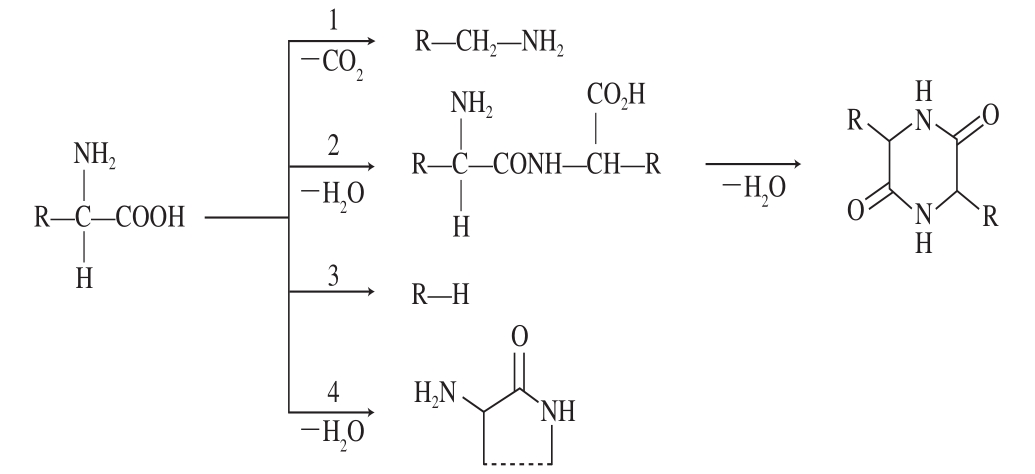
图 4 氨基酸分解的4 种主要途径
Fig. 4 Four major pathways of amino acid decomposition
Phillip等[36]在研究葡萄糖和脯氨酸对PAHs生成的影响时发现,蛋白质高温分解产生游离的氨基酸可以与还原糖(如葡萄糖)发生美拉德反应生成Amadori化合物,Amadori化合物经过高温分解产生PAHs。具体过程如图5所示。
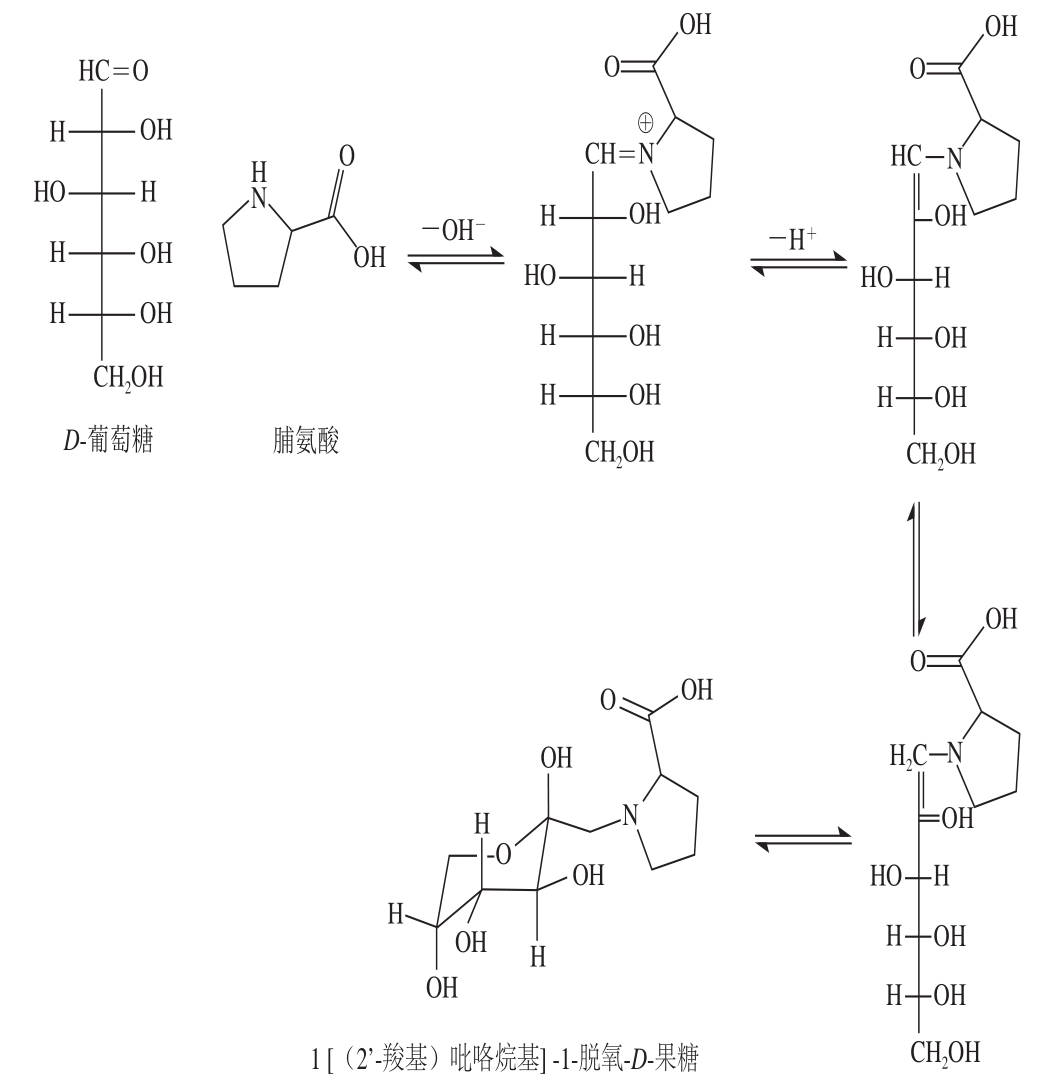
图 5 葡萄糖和氨基酸生成Amadori化合物的过程
Fig. 5 Generation of Amadori compounds from glucose and amino acids
Sharma等[37]在探究氨基酸热解形成低分子质量的杂环和PAHs的研究时发现,天冬氨酸和脯氨酸在高温下可降解产生菲等PAHs,同时高温处理色氨酸发现其不能降解产生PAHs。这说明某些氨基酸是生成PAHs的前体物。齐颖[38]在探究油炸肉制品加工过程中PAHs的形成时,发现连续性油炸导致蛋白质、氨基酸等化学组分热降解和环化缩合形成菲等PAHs。但Saito等[39]在研究热烹调对食物中PAHs形成影响时,分别对虾、玉米、鳟鱼、牛肉和猪肉进行研究,结果发现,玉米(主要成分是碳水化合物)中PAHs的含量为0.015 μg/m3;虾(主要成分是蛋白质)中PAHs的含量为0.003 9 μg/m3,这个水平低于或类似于大气中PAHs含量(0.004 4 μg/m3)的背景水平,所以食物中碳水化合物和蛋白质并不是生成PAHs的主要物质。鳟鱼、牛肉、猪肉中PAHs的含量分别为2.1、1.5 μg/m3和78 μg/m3。结果表明猪肉中PAHs的含量远高于虾、牛肉和鳟鱼,所以推测在食品热加工过程中脂肪才是产生PAHs的主要来源。Tanaka等[40-41]也得出过一致的结论。
McGrath等[42]在研究纤维素低温热解形成PAHs的机制时,发现纤维素在高温下脱水碳化、脱羰、脱羧、脱氢和交联等一系列的化学转化和重排最终形成PAHs。该研究还发现D-葡萄糖和蔗糖热解时生成PAHs的产量丝毫不逊色于纤维素。Horne[43]和Williams[44]等研究发现生物质在高温热解条件下发生继发反应生成PAHs的机制至少有两种:1)Diels-Alder反应;2)含氧芳香族化合物的脱氧作用。Stefanidis等[45]研究发现木聚糖和纤维素在混合热解过程中相互作用,可使PAHs的前体物——酚的产量增加。而Zhou Hui等[46]研究也证实了快速热解木聚糖和纤维素混合物生成PAHs的产量均比单个组分热解时高。以上两个报道都说明在生物质热解生成PAHs的过程中,物质成分之间的相互作用发挥了很大的作用。Wang Shurong等[47]研究发现当纤维素含量保持不变时,随着半纤维素含量增加,2,5-羟甲基糠醛浓度增加。此外,纤维素的存在促进了半纤维素生成乙酸和2-羟甲基糠醛。目前从生物质单组分热解的PAHs形成机制尚不清楚。Hosoya等[48]研究发现纤维素和木质素相互作用产生苯酚衍生物,一些化合物(如儿茶酚类化合物)生成量相比单组分热解预期结果是增加的,而另一些化合物(如邻甲酚)生成量与单组分预期结果相比却是降低的。Asmadi等[49-50]发现从木质素中热解产生的儿茶酚类化合物和酚可以形成PAHs,同时结果表明:木聚糖和纤维素热解产生的苯系物或酚是形成PAHs的重要前体物。明确生物成分的相互影响是一个复杂的过程,对于生物质各个组分相互作用对形成PAHs的影响和机制还需要进一步研究。
综上所述,烟熏等剧烈的食品热加工方式都会导致食品中PAHs的形成。用烟熏处理食品时,食品中的PAHs主要来自于烟熏燃料中纤维素的高温裂解,纤维素在高温下脱水碳化、脱羰、脱羧、脱氢和交联等一系列的化学转化和重排最终形成PAHs。通过对比不同食物在进行其他的热加工时PAHs的含量,可以推测PAHs形成主要是通过食品中脂肪的高温裂解和蛋白质的高温分解。脂肪裂解产物中亚麻酸甲酯、亚油酸甲酯、油酸甲酯和甲基硬脂酸和蛋白质降解产物中某些芳香族氨基酸是生成PAHs的重要前体物质。并且在PAHs的生成机制中,温度和氧气是两个重要的影响因素。目前从食品单个组分热解生成PAHs的机制尚不清楚,食品中PAHs的形成是各个组分相互作用的结果,是一个十分复杂的过程。笔者认为,首先需要从食品三大主要营养素(脂肪、蛋白质和碳水化合物)中逐一筛选出可以生成PAHs的单体成分,并分析其热解产生机制,然后进一步探索不同营养素之间是否存在相互作用以及如何作用导致最终PAHs的生成。
研究报道的PAHs生成机理大都集中在化石燃料和环境领域,对于食品中的PAHs生成机制的研究还处于初级阶段,所以对食品中PAHs的形成机制进行分子水平的深度探索是很有必要的,这对于更好地控制和减少食品中PAHs的生成有指导意义。
参考文献:
[1] HARITASH A K, KAUSHIK C P. Biodegradation aspects of polycyclic aromatic hydrocarbons (PAHs): a review[J]. Journal of Hazardous Materials, 2009, 169(1/2/3): 1-15. DOI:10.1016/j.jhazmat.2009.03.137.
[2] EDWARDS N T. Polycyclic aromatic hydrocarbons (PAH’s)in the terrestrial environment: a review[J]. Journal of Environmental Quality, 1983, 12(4): 427-441. DOI:10.2134/jeq1983.00472425001200040001x.
[3] ARIAS A H, VAZQUEZ-BOTELLO A, TOMBESI N, et al. Presence,distribution, and origins of polycyclic aromatic hydrocarbons (PAHs)in sediments from Bahía Blanca estuary, Argentina[J]. Environmental Monitoring and Assessment, 2010, 160(1/2/3/4): 301-314.DOI:10.1007/s10661-008-0696-5.
[4] BOSTRÖM C E, GERDE P, HANBERG A, et al. Cancer risk assessment, indicators, and guidelines for polycyclic aromatic hydrocarbons in the ambient air[J]. Environ Health Perspect, 2002,110(Suppl 3): 451-488. DOI:10.1289/ehp.02110s3451.
[5] IWEGBUE C M A, ONYONYEWOMA U A, BASSEY F I, et al.Concentrations and health risk of polycyclic aromatic hydrocarbons in some brands of biscuits in the Nigerian market[J]. Human and Ecological Risk Assessment: An International Journal, 2015, 21(2):338-357. DOI:10.1080/10807039.2014.916542.
[6] DAI Q J, JIANG X G, JIANG Y F, et al. Formation of PAHs during the pyrolysis of dry sewage sludge[J]. Fuel, 2014, 130(7): 92-99.DOI:10.1016/j.fuel.2014.04.017.
[7] SINGH L, VARSHNEY J G, AGARWAL T, et al. Polycyclic aromatic hydrocarbons’ formation and occurrence in processed food[J]. Food Chemistry, 2016, 199(2): 768-781. DOI:10.1016/j.foodchem.2015.12.074.
[8] ESSUMANG D K, DODOO D K, ADJEI J K. Effect of smoke generation sources and smoke curing duration on the levels of polycyclic aromatic hydrocarbon (PAH) in different suites of fish[J].Food and Chemical Toxicology, 2013, 58(7): 86-94. DOI:10.1016/j.fct.2013.04.014.
[9] DJINOVIC J, POPOVIC A, JIRA W. Polycyclic aromatic hydrocarbons (PAHs) in traditional and industrial smoked beef and pork ham from Serbia[J]. European Food Research & Technology,2008, 227(4): 1191-1198. DOI:10.1007/s00217-008-0836-8.
[10] GUILLÉN M D, SOPELANA P, PARTEARROYO M A. Polycyclic aromatic hydrocarbons in liquid smoke flavorings obtained from different types of wood. effect of storage in polyethylene flasks on their concentrations[J]. Journal of Agricultural and Food Chemistry,2000, 48(10): 5083-5087. DOI:10.1021/jf000371z.
[11] SIMKO P. Factors affecting elimination of polycyclic aromatic hydrocarbons from smoked meat foods and liquid smoke flavorings[J].Molecular Nutrition & Food Research, 2005, 49(7): 637-647.DOI:10.1002/mnfr.200400091.
[12] 曾健雄, 吴时敏, 王琳, 等. 高脂食品中多环芳烃研究[J]. 粮食与油脂, 2013, 26(10): 6-9. DOI:10.3969/j.issn.1008-9578.2013.10.002.
[13] BADGER G M, BUTTERY R G, KIMBER R W L, et al. The formation of aromatic hydrocarbons at high temperatures[J]. Journal of the Chemical Society, 1958, 498(3): 2449-2452. DOI:10.1039/jr9580002449.
[14] 黄靖芬, 李来好, 陈胜军, 等. 烟熏食品中苯并(a)芘的产生机理及防止方法[J]. 现代食品科技, 2007, 23(7): 67-70. DOI:10.3969/j.issn.1673-9078.2007.07.020.
[15] BITTNER J D, HOWARD J B. Composition profiles and reaction mechanisms in a near-sooting premixed benzene/oxygen/argon flame[J]. Symposium (International) on Combustion, 1981, 18(1):1105-1116. DOI:10.1016/s0082-0784(81)80115-4.
[16] WANG Hai, FRENKLACH M. A detailed kinetic modeling study of aromatics formation in laminar premixed acetylene and ethylene flames[J]. Combustion and Flame, 1997, 110(1/2): 173-201.DOI:10.1016/s0010-2180(97)00068-0.
[17] 赵霏阳. 柴油机低温燃烧实现超低碳烟排放的机理研究[D]. 天津:天津大学, 2013: 4-8.
[18] 赵霏阳, 于文斌, 苏万华. 基于碳烟表面活化程度预报柴油机预混燃烧中碳烟特性的多步现象学碳烟模型的构建与应用[C]//中国内燃机学会燃烧节能净化分会学术年会. 南宁: 中国内燃机学会, 2012.
[19] TAO Feng, CHOMIAK J. Numerical investigation of reaction zone structure and flame lift off of DI diesel sprays with complex chemistry[J]. SAE Technical Papers, 2002, 111(3): 1836-1854.DOI:10.4271/2002-01-1114.
[20] HONG Zekai, LAM K Y, DAVIDSON D F, et al. A comparative study of the oxidation characteristics of cyclohexane, methylcyclohexane and n-butylcyclohexane at high temperatures[J]. Combustion and Flame,2011, 158(8): 1456-1468. DOI:10.1061/j.combust flame.2010.12.019.
[21] CHEN B H, CHEN Y C. Formation of polycyclic aromatic hydrocarbons in the smoke from heated model lipids and food lipids[J]. Journal of Agricultural and Food Chemistry, 2001, 49(11):5238-5243. DOI:10.1021/jf0106906.
[22] LOMANNO S S, NAWAR W W. Effect of heating temperature and time on the volatile oxidative decomposition of linolenate[J].Journal of Food Science, 1982, 47(3): 744-746. DOI:10.1111/j.1365-2612.1982.tb12705.x.
[23] URIARTE P S, GUILLÉN M D. Formation of toxic alkylbenzenes in edible oils submitted to frying temperature: influence of oil composition in main components and heating time[J]. Food Research International, 2010, 43(8): 2161-2170. DOI:10.1016/j.foodres.2010.07.022.
[24] HEINONEN M, REIN D, SATUE-GRACIA M T, et al. Effect of protein on the antioxidant activity of phenolic compounds in a lecithinliposome oxidation system[J]. Journal of Agricultural and Food Chemistry, 1998, 46(3): 917-922. DOI:10.1021/jf970826t.
[25] CHENG Weiwei, LIU Guoqin, LIU Xuede, et al. Formation of benzo(a)pyrene in sesame seeds during the roasting process for production of sesame seed oil[J]. Journal of the American Oil Chemists’ Society, 2015, 92(11/12): 1725-1733. DOI:10.1007/s11746-015-2734-0.
[26] PERELLÓ G, MARTÍ-CID R, CASTELL V, et al. Concentrations of polycyclic diphenyl ethers, hexachlorobenzene and polycyclic aromatic hydrocarbons in various food stuffs before and after cooing[J].Food & Chemical Toxicology, 2009, 47(4): 709-715. DOI:10.1016/j.fct.2008.12.030.
[27] LUO Yan, AHMED I, KUBÁTOVÁ A, et al. The thermal cracking of soybean/canola oils and their methyl esters[J]. Fuel Processing Technology, 2010, 91(6): 613-617. DOI:10.1016/j.fuproc.2010.01.007.
[28] STUMPE-VĪKSNA I, BARTKEVIČS V, KUKĀRE A, et al.Polycyclic aromatic hydrocarbons in meat smoked with different types of wood[J]. Food Chemistry, 2008, 110(3): 794-797. DOI:10.1016/j.foodchem.2008.03.004.
[29] VIEGAS O, PANCRAZIO G, PRUCHA M, et al. Polycyclic aromatic hydrocarbons formation in different types of charcoal grilled meat[J]. International Symposium on Chemical & Non-Chemical Soil & Substrate Disinfestation, 2013, 8(2): 81-85.DOI:10.1361/10549710177033894.
[30] NACCARI C, CRISTANI M, GIOFRÈ F, et al. PAHs concentration in heat-treated milk samples[J]. Food Research International, 2011,44(3): 716-724. DOI:10.1016/j.foodres.2010.12.029.
[31] LONDOÑO V A G, GARCIA L P, SCUSSEL V M, et al. Polycyclic aromatic hydrocarbons in milk powders marketed in Argentina and Brazil[J]. Food Additives Contaminants, 2013, 30(9): 1573-1580.DOI:10.1080/19440049.2013.810347.
[32] LUZARDO O P, RODRIGUEZ-HERNANDEZ A, QUESADATACORONTE Y, et al. Influence of the method of production of eggs on the daily intake of polycyclic aromatic hydrocarbons and organochlorine contaminants: an independent study in the Canary Islands (Spain)[J]. Food and Chemical Toxicology, 2013, 60(10): 455-462. DOI:10.1016/j,fct.2013.08.003.
[33] OLATUNJI O S, FATOKI O S, XIMBA B J, et al. Polycyclic aromatic hydrocarbons (PAHs) in edible oil: temperature effect on recovery from base hydrolycysis product and health risk factor[J]. Food and Public Health, 2014, 4(2): 23-30. DOI:10.5923/j.fph.20140402.02.
[34] KAO T H, CHEN S, HUANG C W, et al. Occurrence and exposure to polycyclic aromatic hydrocarbons in kindling-free-charcoal grilled meat products in Taiwan[J]. Food and Chemical Toxicology, 2014,71(8): 149-158. DOI:10.1016/j.fct.2014.05.033.
[35] CHIAVARI G, GALLETTI G C. Pyrolysis-gas chromatography mass spectrometry of amino acids[J]. Journal of Analytical and Applied Pyrolysis, 1992, 24(2): 123-137. DOI:10.1016/0165-2370(92)85024-F.
[36] PHILLIP F, BRITT A C, BUCHANAN C V, et al. Does glucose enhance the formation of nitrogen containing polycyclic aromatic compounds and polycyclic aromatic hydrocarbons in the pyrolysis of proline?[J]. Fuel,2004, 83(11): 1417-1432. DOI:10.1016/j.fuel.2004.02.009.
[37] SHARMA R K, CHAN W G, SEEMAN J I, et al. Formation of low molecular weight heterocycles and polycyclic aromatic compounds(PACs) in the pyrolysis of α-amino acids[J]. Journal of Analytical and Applied Pyrolysis, 2003, 66(1/2): 97-121. DOI:10.1016/s0165-2370(02)00108-0.
[38] 齐颖. 油炸肉制品加工过程中多环芳烃的形成及控制研究[D]. 天津: 天津科技大学, 2015: 1-10.
[39] SAITO E, TANAKA N, MIYAZAKI A, et al. Concentration and particle size distribution of polycyclic aromatic hydrocarbons formed by thermal cooking[J]. Food Chemistry, 2014, 153(9): 285-291.DOI:10.1016/j,foodchem.2013.12.055.
[40] TANAKA N, TSUZAKI M, AKAI E, et al. Particle size distribution of oil-mist emitted from fish grilling and concentrations of polycyclic aromatic hydrocarbons[J]. Bunseki Kagaku, 2012, 61(11): 901-910.DOI:10.2116/bunsekikagaku.61.901.
[41] TANAKA N, OHTAKE K, TSUZAKI M, et al. Analysis of polycyclic aromatic hydrocarbons in oil-mist emitted from food grilling[J]. Bunseki Kagaku, 2012, 61(2): 77-86. DOI:10.2116/bunsekikagaku.61.77.
[42] MCGRATH T E, CHAN W G, HAJALIGOL M R. Low temperature mechanism for the formation of polycyclic aromatic hydrocarbons from the pyrolysis of cellulose[J]. Journal of Analytical and Applied Pyrolysis, 2003, 66(1): 51-70. DOI:10.1016/s0165-2370(02)00105-5.
[43] HORNE P A, WILLIAMS P T. Upgrading of biomass-derived pyrolytic vapours over zeolite ZSM-5 catalyst: effect of catalyst dilution on product yields[J]. Fuel, 1996, 75(9): 1043-1050.DOI:10.1016/0016--2361(96)00082-8.
[44] WILLIAMS P T, HORNE P A. The influence of catalyst type on the composition of upgraded biomass pyrolysis oils[J].Journal of Analytical & Applied Pyrolysis, 1995, 31(2): 39-61.DOI:10.1016/0165-2370(94)00847-T.
[45] STEFANIDIS S D, KALOGIANNIS K G, LLIOPOULOU E F, et al.A study of lignocellulosic biomass pyrolysis via the pyrolysis of cellulose, hemicellulose and lignin[J]. Journal of Analytical & Applied Pyrolysis, 2014, 105(5): 143-150. DOI:10.1016/j.jaap.2013.10.013.
[46] ZHOU Hui, WU Chunfei, MENG Aihong, et al. Effect of interactions of biomass constituents on polycyclic aromatic hydrocarbons (PAH)formation during fast pyrolysis[J]. Journal of Analytical and Applied Pyrolysis, 2014, 110(1): 264-269. DOI:10.1016/j.jaap.2014.09.007.
[47] WANG Shurong, GUO Xiujuan, WANG Kaige, et al. Influence of the interaction of components on the pyrolysis behavior of biomass[J].Journal of Analytical and Applied Pyrolysis, 2011, 91(1): 183-189.DOI:10.1016/j.jaap.2011.02.006.
[48] HOSOYA T, KAWAMOYO H, SAKA S. Solid liquid and vaporphase interactions between cellulose and lignin-derived pyrolysis products[J]. Journal of Analytical & Applied Pyrolysis, 2009, 85(1/2):237-246. DOI:10.1016/j.jaap.2008.11.028.
[49] ASMADI M, KAWAMOTO H, SAKA S. Gas and solidliquid-phase reactions during pyrolysis of softwood and hardwood lignins[J].Journal of Analytical & Applied Pyrolysis, 2011, 92(2): 417-425.DOI:10.1016/j,jaap.2011.08.003.
[50] ASMADI M, KAWAMOTO H, SAKA S. Thermal reactions of guaiacol and syringol as lignin model aromatic nuclei[J]. Journal of Analytical & Applied Pyrolysis, 2011, 92(1): 88-98. DOI:10.1016/j.jaap.2011.04.011.
Mechanism of Polycyclic Aromatic Hydrocarbon Formation in Food Processing: A Review
NIE Wen1, TU Zehui1, ZHAN Jianfeng2, CAI Kezhou1,*, JIANG Shaotong1, CHEN Conggui1
(1. Key Laboratory for Agricultural Products Processing of Anhui Province, School of Food Science and Engineering,Hefei University of Technology, Hefei 230009, China; 2. College of Life Sciences, Huanggang Normal University,Huanggang 438000, China)
Abstract:Polycyclic aromatic hydrocarbons (PAHs) are a class of pollutants hazardous to both the environment and foods.Previously, a lot of research efforts have been devoted to the detection and safety evaluation PAHs in the environment, the detection and control of PAHs contamination in food processing, and the study of the underlying mechanism. This review paper focuses on the chemical mechanism for the formation of PAHs and their formation mechanisms in food processing.Meanwhile, the current studies are briefly reviewed. This review is expected to provide new perspectives on the control of PAHs in food.
Keywords:polycyclic aromatic hydrocarbons; chemical mechanism; food processing; formation mechanism
DOI:10.7506/spkx1002-6630-201815039
收稿日期:2017-04-30
基金项目:国家自然科学基金青年科学基金项目(31501585)
第一作者简介:聂文(1993—),男,硕士研究生,研究方向为食品现代加工理论与方法。E-mail:1339059642@qq.com
*通信作者简介:蔡克周(1980—),男,副教授,博士,研究方向为肉品加工与质量控制。E-mail:kzcai@hfut.edu.cn
中图分类号:TS251.1
文献标志码:A
文章编号:1002-6630(2018)15-0269-06
引文格式:
聂文, 屠泽慧, 占剑峰, 等. 食品加工过程中多环芳烃生成机理的研究进展[J]. 食品科学, 2018, 39(15): 269-274.DOI:10.7506/spkx1002-6630-201815039. http://www.spkx.net.cn
NIE Wen, TU Zehui, ZHAN Jianfeng, et al. Mechanism of polycyclic aromatic hydrocarbon formation in food processing:a review[J]. Food Science, 2018, 39(15): 269-274. (in Chinese with English abstract) DOI:10.7506/spkx1002-6630-201815039. http://www.spkx.net.cn