表1 6 种降血脂化学药物的质谱采集参数
Table 1 Mass spectroscopic parameters for six antilipemic chemicals
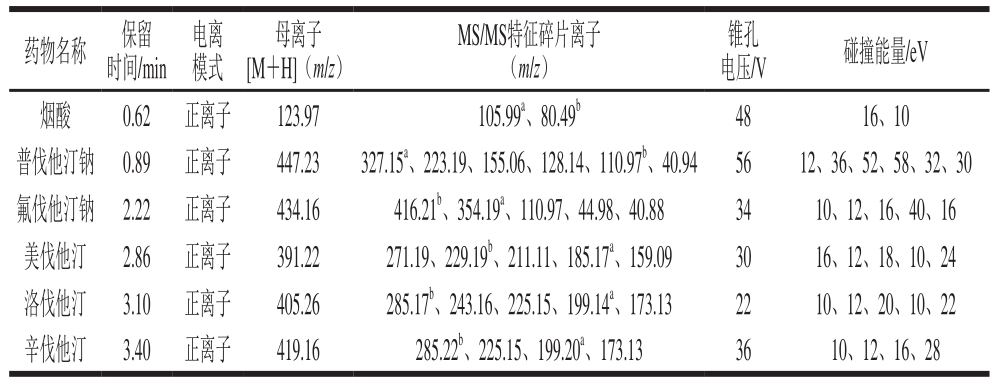
注:a.定量离子;b.定性离子。
李晓蕾 1 ,陈 军 2 ,杨朝芬 1 ,杨 俊 1
(1.昆明理工大学分析测试研究中心,云南 昆明 650000;2.中国林业科学研究院资源昆虫研究所,云南 昆明 650000)
摘 要: 建立超高效液相色谱-串联质谱法同时快速检测辅助降血脂类保健食品中6 种降血脂药物(烟酸、普伐他汀钠、氟伐他汀钠、美伐他汀、洛伐他汀、辛伐他汀)的方法。样品经甲醇提取,Waters Acquity BEH-C 18 色谱柱分离,0.1%甲酸-乙腈溶液梯度洗脱,流速0.2 mL/min,电喷雾离子源正离子模式扫描,多反应监测模式测定,外标法定量。结果表明:在实验条件下4 min内可快速、准确地定性定量分析6 种降血脂化学药物,分离度良好,方法检出限为4~39 µg/kg,加样回收率为80.2%~106.1%。利用本方法检测20 批降血脂类保健食品,其中3 批分别含有烟酸和洛伐他汀。本方法线性关系良好、快速、简便、准确,可作为辅助降血脂类保健食品中非法添加化学药物的定性定量检测方法。
关键词: 超高效液相色谱-串联质谱法;辅助降血脂;化学药物;保健食品;非法添加
近年,随着生活质量的显著提高,人们对自身健康越来越关注,保健品市场利益空间迅速增加。但是,随之而来的食品药品安全问题不断增多,一些不法分子为获取高额利益在保健食品中非法添加化学药物 [1-2] ,使其功效显著。此类非法添加随意性大,剂量不明确,标签上又未作说明,往往会导致消费者长期、超量服用而引起毒性反应,严重的甚至危及生命 [3] 。
目前,国内外对于保健食品中非法添加化学药的研究很多 [4-9] ,但降血脂类化学药物添加方面的研究尚不够深入。而近年发病率逐渐上升的高血脂症等心脑血管疾病,已成为严重危害我国人民健康的“隐形杀手” [10-11] ,辅助降血脂保健食品市场也呈飞速上升趋势。已有报道的检测方法有薄层色谱法 [12] 和高效液相色谱法 [13-14] ,但存在选择性差、定性能力弱和灵敏度低的问题;也有液相色谱-质谱联用法 [15-16] ,但检测成分较少、检测时间较长。国家食品药品监督管理局曾于2010年和2017年先后颁布了《辅助降血脂类保健食品违法添加药物的检测方法》 [17] 、《保健食品中75 种非法添加化学药物的检测》 [18] 、《食品中西布曲明等化合物的测定》 [19] ,方法中均含有降血脂类化学药成分的检测,但检测成分较少而检测时间较长,灵敏度也不够高。因此研究降血脂类化学药物的检测方法,对促进质量监督,保障食品安全和人民健康是十分有必要的。
本实验拟选取6 种临床上较常用,相对生产成本较低因而价格较低,易于非法添加的降血脂化学药物,采用超高效液相色谱-串联质谱法,以多反应监测模式(multi-reaction monitoring,MRM),建立快速、有效地定性、定量检测辅助降血脂保健食品中6 种非法添加降血脂药物成分的分析方法,并对20 批市售的辅助降血脂功能保健食品进行检测,拟为降血脂类保健食品安全监控提供理论依据。
辅助降血脂功能保健食品 市售。
对照品:烟酸(批号LF80N66,纯度99.5%)、普伐他汀钠(批号8-XJZ-27-1,纯度98.0%)、氟伐他汀钠(批号7-ABY-122-1,纯度98.0%)、美伐他汀(批号2-NYL-167-1,纯度98.0%)、洛伐他汀(批号LK10O58,纯度98.0%)、辛伐他汀(批号11-SCC-167-1,纯度98.0%) 中国食品药品检定研究院;实验用水为超纯水;样品处理所用甲醇为分析纯,其他试剂均为质谱纯。
ACQUITY UPLC Xevo TQD液相色谱-串联四极杆质谱联用仪(配有电喷雾离子源、Masslynx 4.1数据处理系统) 美国Waters公司;Advantage-10/Elix Milli-Q超纯水仪 美国Millopore公司;BP211D型电子天平德国Sartorius科学仪器有限公司;KQ-300DA型数控型超声波提取仪 上海波龙电子有限公司。
1.3.1 色谱条件
色谱柱:Waters Acquity BEH-C 18 色谱柱(2.1 mm×50 mm,1.7 µm);流动相:流动相A为0.1%甲酸溶液,流动相B为乙腈;梯度洗脱:0~2.5 min,50% B,2.5~3.0 min,60% B,3.0~3.5 min,100% B,3.5~4.0 min,50% B;流速0.2 mL/min;色谱柱温度30 ℃;进样量1 µL [20-22] 。
1.3.2 质谱条件
电喷雾离子源正离子模式扫描;毛细管电压2.68 kV;脱溶剂气温度500 ℃;脱溶剂气流量850 L/h;锥孔气流速50 L/h;碰撞气体为氩气;子离子扫描及MRM模式同时监测 [23-24] 。经质谱条件优化后,各物质的色谱保留时间、分子离子与特征碎片离子及其采集参数 [25] 见表1。
表1 6 种降血脂化学药物的质谱采集参数
Table 1 Mass spectroscopic parameters for six antilipemic chemicals

注:a.定量离子;b.定性离子。
1.3.3 溶液的制备
对照品溶液:分别精密称取烟酸、普伐他汀钠、氟伐他汀钠、美伐他汀、洛伐他汀、辛伐他汀适量(约1~5 mg),置于10 mL容量瓶中,加甲醇溶解并稀释至刻度,定容,摇匀,作为各标准品的标准储备液。各取单标储备液适量(0.1~1 mL),置于50 mL容量瓶,用甲醇稀释并定容配制成混合对照品溶液,使用时进一步稀释。
供试品溶液:将具有辅助降血脂功效的保健食品每个品种取10~20 粒油状样品内容物,混匀;或取10~20 片(丸或袋)固体样品,置研钵中研磨均匀呈粉末状。分别精密称取一次推荐服用量的样品,置于50 mL容量瓶中,加甲醇40 mL,超声提取15 min。冷却至室温后,用甲醇稀释定容,摇匀,直接作为供试品溶液,分析时上清液经0.22 µm微孔滤膜过滤后上样。
阴性样品溶液:取具有代表性的固体颗粒剂(和信茶)、胶囊剂(油状大豆磷脂胶囊、粉状三七胶囊)和片剂(阿胶含片)3 种剂型共4 种阴性样品,分别精密称取一次推荐服用量样品置于50 mL容量瓶,与供试品溶液同法制成阴性样品溶液。
色谱-质谱条件的优化:实验对流动相的组成(甲醇-水、甲醇-甲酸溶液、乙腈-水、乙腈-甲酸溶液)、流速(0.1、0.2、0.4 mL/min)和柱温(20、30、40 ℃)等条件分别进行考察。对流动相的考察发现,甲醇-水体系较乙腈-水体系分析时间长,峰形差,因此选用乙腈-水体系,而乙腈-水体系在水中添加0.1%的甲酸后峰形更好,因此选用0.1%甲酸-乙腈溶液做流动相。在流速为0.4 mL/min或温度为40 ℃时,由于烟酸、普伐他汀钠和洛伐他汀、辛伐他汀2 组成分的保留时间比较接近,不能很好地达到基线分离,而流速低(0.1 mL/min)或温度低(20 ℃)均会导致分析时间延长,故最终确定0.2 mL/min,柱温30 ℃为实验最佳条件。优化得到的最佳色谱条件可在4 min内高分离度、快速有效地分离6 种化学药物,均优于国家食品药品监督管理局发布的检测方法 [17-19] 及相关文献 [21-24] 方法。质谱部分在正离子、MRM模式下,用1 µg/mL的混合标准溶液手动调谐结合自动调谐,逐一选择并确定适合各化合物的准离子峰及母离子,采用子离子扫描方式进行二级质谱分析,对子离子进行优化选择,找出满足化合物碎裂规律的子离子,确定定量与定性离子,同时优化毛细管电压和锥孔电压、碰撞能量等质谱参数,使离子强度最大、分离度最佳。最后确定测定6 种化学药物的定性和定量离子对,共12 个离子检测通道。各化合物采集的总离子流见图1,定量离子对的MRM离子流见图2。
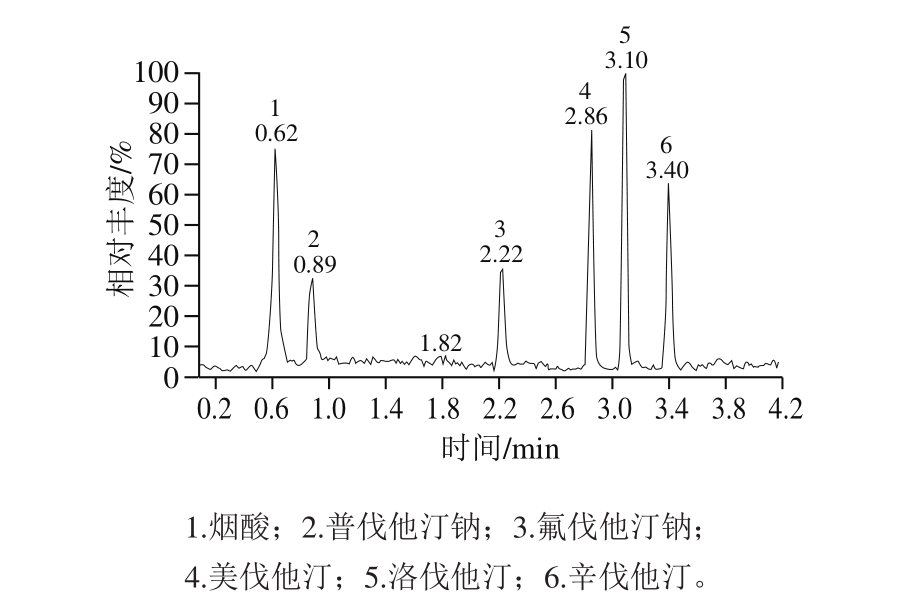
图1 6 种降血脂类化学药物的总离子流色谱图
Fig. 1 Total ion current chromatograms of six antilipemic drugs
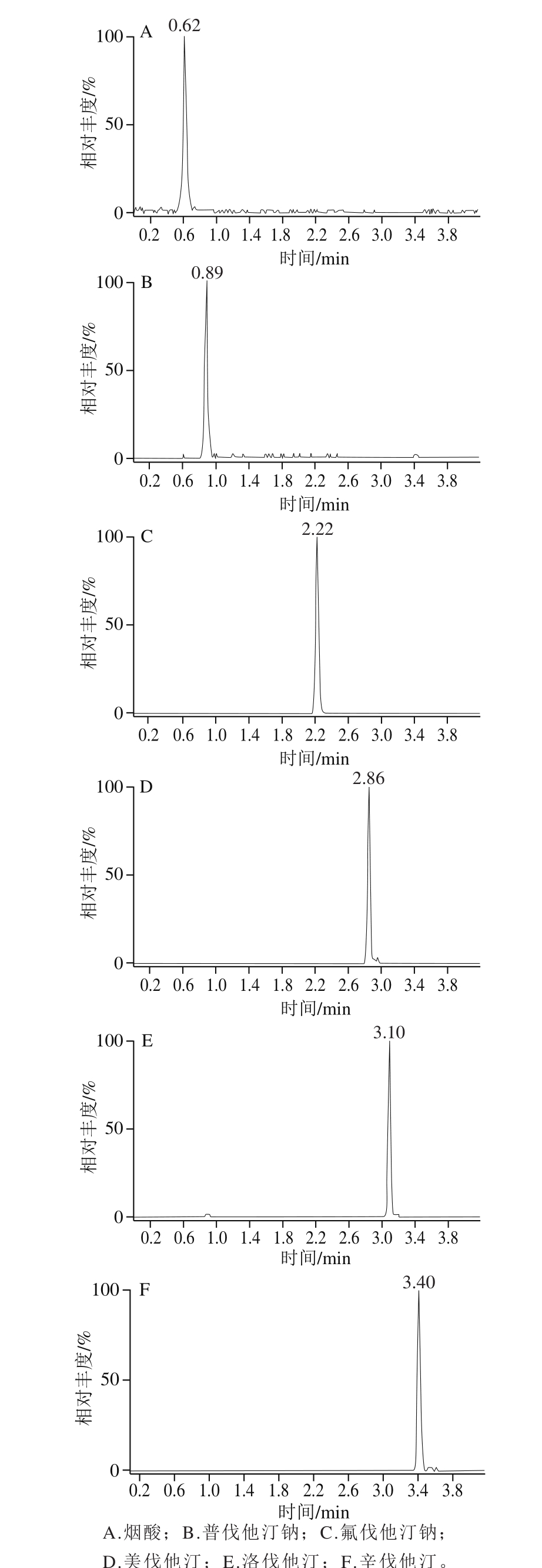
图2 6 种降血脂化学药对照品定量离子对的MRM色谱图
Fig. 2 MRM chromatograms of quantitative ions of 6 antilipemic drug standards
本实验选取具有代表性的4 种阴性样品基质:固体颗粒剂(和信茶)、胶囊剂(油状大豆磷脂胶囊、粉状三七胶囊)和片剂(阿胶含片)进行基质效应考察。基质效应根据基质空白配制标样响应值与同质量浓度溶剂标样响应值的比值进行评价 [26-27] ,大于1时为基质增强效应,小于1时为基质抑制效应。对于基质效应过强的样品,应采取相应的处理手段以减小其对测定的干扰。从实验结果可以看出,基质对烟酸、普伐他汀钠表现出基质增强效应,而对氟伐他汀钠、美伐他汀、洛伐他汀、辛伐他汀表现出基质抑制效应。本实验考察的基质效应在0.82~1.18之间,表明样品基质对目标成分响应干扰相对较小。
样品处理过程中,大部分基质较简单,前处理时采用甲醇超声提取过滤后即上样分析。但个别样品(如苦瓜洋参软胶囊和苍芎胶囊)基质相对比较复杂,对出峰时间较早的烟酸和普伐他汀钠基质增强效应大于1.3,影响数据正确性,且易污染质谱检测器离子源,故先将样品过WAX固相萃取柱净化处理后再上机分析 [28] 。苦瓜洋参软胶囊和苍芎胶囊净化后基质效应降至1.12和1.15,但净化后回收率降低至70.2%和65.4%,因此在基质影响相对较小的情况下并未对所有样品进行净化处理。
取具有代表性的固体颗粒剂(和信茶)、胶囊剂(油状大豆磷脂胶囊、粉状三七胶囊)和片剂(阿胶含片)3 种剂型共4 种阴性样品,按阴性样品溶液的制备方法处理后,依1.3.1节方法进样,按1.3.2节方法采集图谱,得到阴性样品的MRM离子流色谱图,12 个离子通道中均未见有干扰6 种目标物的色谱峰。结果表明,具有代表性的4 种阴性样品对所测6 种目标物均无干扰,方法专属性良好。
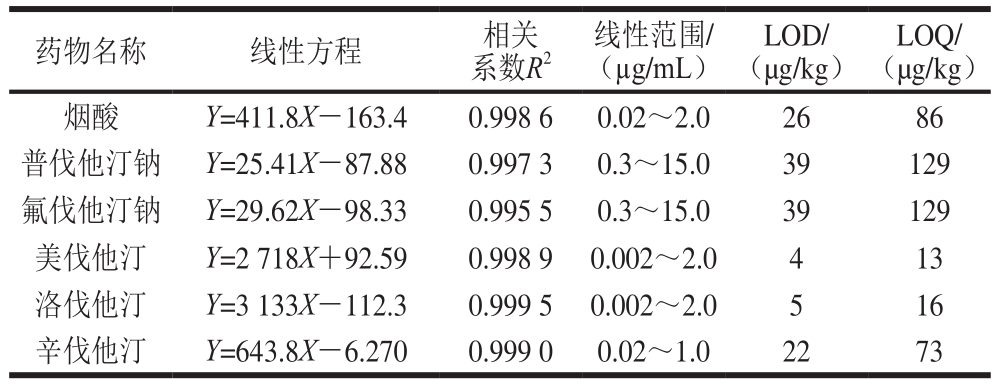
取混合对照品溶液,按1.3.1节和1.3.2节方法进样测定,以各组分定量离子对的峰面积(Y)对质量浓度(X)绘制标准曲线,得回归方程和相关系数(R 2 ),见表2。结果表明,6 种化学药物的线性关系在线性范围内良好,R 2 均在0.995 5以上。取阴性样品和信茶适量,置于50 mL容量瓶中,按1.0 mg/g的添加量加入混合对照品溶液,按供试品溶液同法经逐步稀释后进样,以3 倍信噪比时计算各化学药的LOD,为10 倍信噪比时计算各化学药的LOQ,其中洛伐他汀、美伐他汀和辛伐他汀的LOD降低至国家食品药品监督管理局发布检测方法 [18] 的12.5%以下。结果表明方法LOD均在4~39 µg/kg之间,说明方法具有较高的灵敏度。
表2 6 种降血脂化学药的线性方程、相关系数、回收率及LOD、LOQ
Table 2 Linear equations, correlation coefficients, linear ranges,LODs, and LOQs for six antilipemic drugs
取混合对照品溶液1 µL,按1.3.1节和1.3.2节色谱、质谱条件进样测定,连续测定6 次,计算烟酸、普伐他汀钠、氟伐他汀钠、美伐他汀、洛伐他汀、辛伐他汀定量离子对质谱峰面积的相对标准偏差(relative standard deviation,RSD)分别为1.16%、5.20%、2.26%、3.88%、2.12%、6.86%,均在7%以内,表明方法的精密度良好。
精密称取三七胶囊阴性样品6 份,每份为1 次日常服用量,分别精密加入对照品储备液适量,使含各种化学药含量均为1.0 mg/kg,按1.3.3节方法制成供试品溶液进样测定,计算各成分含量及其RSD。结果烟酸、普伐他汀钠、氟伐他汀钠、美伐他汀、洛伐他汀、辛伐他汀的含量分别为0.97、0.99、1.02、1.01、0.95、0.96 mg/kg;RSD分别为2.46%、2.49%、3.14%、1.86%、1.50%、1.57%,表明该方法重复性较好。
取供试品溶液1 份,在配制后避光冷藏放置0、2、4、6、8、12 h。根据6 种化学药的定量离子对峰面积计算其RSD分别为2.83%、1.75%、4.29%、2.58%、5.61%、1.87%,表明供试品溶液在12 h内稳定。
表3 3 种不同基质阴性样品中6 种降血脂化学药的加标回收率结果
Table 3 Recoveries of six antilipemic drugs in three different spiked matrixes
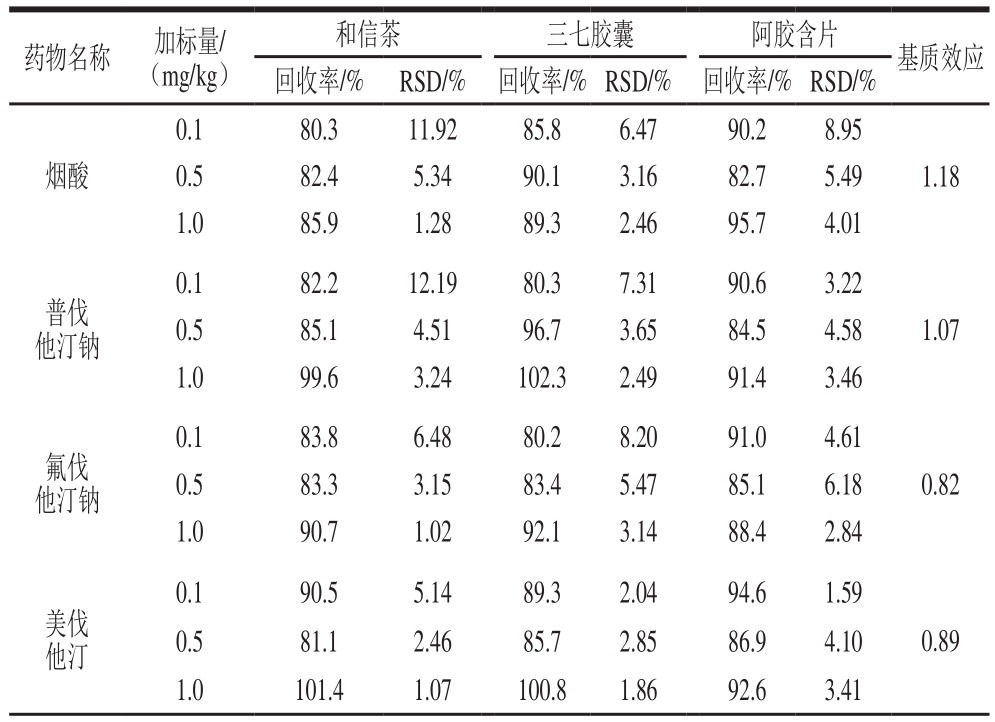
续表3
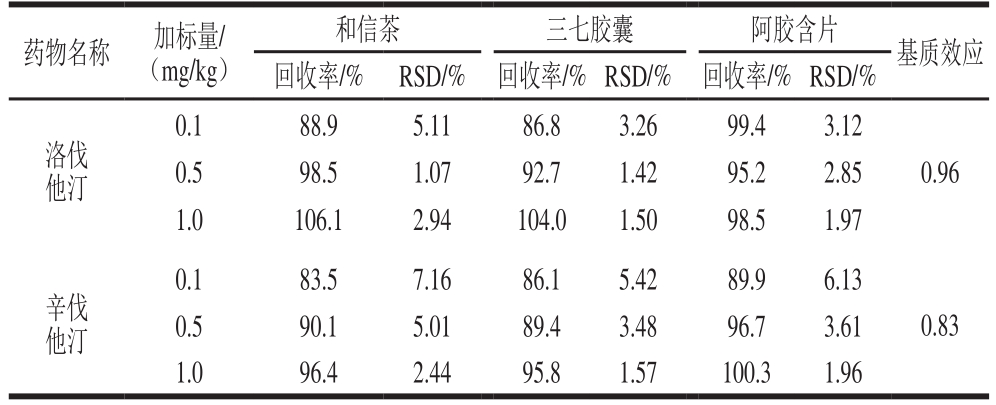
精密称取阴性样品和信茶、三七胶囊、阿胶含片各9 份,每份为1 次日常服用量,分为3 组,按1.3.3节方法制备成阴性样品溶液,分别进行定量限1、2、10 倍(0.1、0.2、1.0 mg/kg)3 个添加水平的回收率实验,结果见表3。6 种化学药物的加样平均回收率均在80.2%~106.1%之间。
本实验共收集辅助降血脂类功能性保健食品20 批,取各样品按1.3.3节方法制备供试品溶液,按1.3.1节和1.3.2节色谱、质谱条件进样测定,根据定量监测离子对的色谱峰面积,采用外标法计算样品中各化学药物成分的含量。结果发现,20 批辅助降血脂类保健食品中共检出3 批可能添加化学药物,分别检测出烟酸和洛伐他汀,含量分别为烟酸81.2、72.7 µg/g,洛伐他汀690 µg/g。
本实验建立辅助降血脂类保健食品中6 种非法添加降血脂化学药物(烟酸、普伐他汀钠、氟伐他汀钠、美伐他汀、洛伐他汀、辛伐他汀)的超高效液相色谱-串联质谱法,具有快速、准确、灵敏度高和专属性强等优点,可为药品监管及规范保健品市场提供理论依据。对于如何杜绝保健食品非法添加的情况,建议一方面大力发展更先进灵敏的检测技术,另一方面也需建立和完善非法添加有害化学成分的各种谱库信息,以利于对有害物进行筛查 [29-30] ,此外,从多方面加强监管以及增加惩罚力度也十分重要。
参考文献:
[1] 米建萍, 徐远金, 朱平川, 等. 液质联用技术在滥用食品添加剂及食品中违法添加物测定中的应用及研究进展[J]. 基因组学与应用生物学, 2015, 34(7): 1579-1586.
[2] LIU F Y, ZHANG X F, LI Y Q, et al. Simultaneous screening and determination of eight tetracycline antibiotics illegally adulterated in herbal preparations using HPLC-DAD combined with LC-MS-MS[J].Chromatographia, 2018, 81(2): 303-314. DOI:10.1007/s10337-017-3450-8.
[3] 赵超群. 液相色谱-串联质谱联用技术在测定食品中非法添加物的应用[D]. 杭州: 浙江工业大学, 2015: 1-8.
[4] HUANG J, LIANG P, XU J, et al. Qualitative and quantitative determination of coumarin using surface-enhanced Raman spectroscopy coupled with intelligent multivariate analysis[J]. RSC Advances, 2017, 77: 49097-49101. DOI:10.1039/c7ra09059e.
[5] GUO P Q, XU X Y, CHEN G N, et al. On-line two dimensional liquid chromatography based on skeleton type molecularly imprinted column for selective determination of sulfonylurea additive in Chinese patent medicines or functional foods[J]. Journal of Pharmaceutical and Biomedical Analysis, 2017, 146: 292-301. DOI:10.1016/j.jpba.2017.09.008.
[6] LI M J, MA H Y, GAO J L, et al. Rapid screening of nonsteroidal anti-inflammatory drugs illegally added in anti-rheumatic herbal supplements and herbal remedies by portable ion mobility spectrometry[J]. Journal of Pharmaceutical and Biomedical Analysis,2017, 145: 203-208. DOI:10.1016/j.jpba.2017.06.002.
[7] PAIG P, RODRIGUES M J E, CORREIA M, et al. Analysis of pharmaceutical adulterants in plant food supplements by UHPLC-MS/MS[J]. European Journal of Pharmaceutical Sciences, 2017, 99: 219-227. DOI:10.1016/j.ejps.2016.12.024.
[8] FU Y Q, ZHOU Z H, KONG H W, et al. Nontargeted screening method for illegal additives based on ultrahigh-performance liquid chromatography-high-resolution mass spectrometry[J].Analytical Chemistry, 2016, 88(17): 8870-8877. DOI:10.1021/acs.analchem.6b02482.
[9] 蒋丽萍, 屠婕红, 徐宏祥, 等. UPLC-MS/MS法测定抗疲劳类保健食品中非法添加的9 种壮阳类化学药物[J]. 中草药, 2015, 46(15):2238-2245. DOI:10.7501/j.issn.0253-2670.2015.15.011.
[10] 朱振宝, 张亚莉, 贾玮, 等. 超高效液相色谱-四极杆/静电场轨道离子阱质谱测定植物提取物中的7 种合成色素[J]. 食品科学, 2017,38(24): 196-201. DOI:10.7506/spkx1002-6630-201724031.
[11] 丁辉. 肥胖与高血脂病关系调查分析[J]. 中国卫生产业, 2017(17):183-184. DOI:10.16659/j.cnki.1672-5654.2017.17.183.
[12] 詹淑玉, 朱琦峰, 徐宏祥, 等. UPLC-MS/MS法快速测定减肥类中成药及保健食品中非法添加15 种化学药的研究[J]. 中草药, 2016,47(17): 3023-3031. DOI:10.7501/j.issn.0253-2670.2016.17.011.
[13] 丁宝月, 屠婕红, 薛磊冰, 等. UPLC-MS/MS法快速测定降压类中成药及保健食品中非法添加34 种化学药的研究[J]. 中草药, 2015,46(5): 688-696. DOI:10.7501/j.issn.0253-2670.2015.05.013.
[14] 黄越燕, 屠婕红, 徐宏祥, 等. UPLC-MS/MS法快速测定中药及保健食品中非法添加17 种抗炎镇痛类化学药的研究[J]. 中草药, 2016,47(2): 246-254. DOI:10.7501/j.issn.0253-2670.2016.02.012.
[15] 孙晓冬, 郝杰, 毛婷, 等. 超高效液相色谱-串联四极杆质谱快速筛查豆芽中51 种抗生素类药物的残留[J]. 食品科学, 2017, 38(20): 327-333. DOI:10.7506/spkx1002-6630-201720049.
[16] 薄海波, 星玉秀, 吉生军, 等. 固相萃取-超高效液相色谱-串联质谱法同时测定酸奶中55 种塑料添加剂[J]. 食品科学, 2017, 38(24):265-271. DOI:10.7506/spkx1002-6630-201724043.
[17] 国家食品药品监督管理局. 辅助降血脂类保健食品违法添加药物的检测方法: 国食药监办许[2010]114号[EB/OL]. (2010-04-27).http://www.instrument.com.cn/download/shtml/809955.shtml.
[18] 钮正睿, 曹进, 李珉, 等. 保健食品中75 种非法添加化学药物的检测: 国食药监办许[2017]138号[EB/OL]. (2017-10-17). http://samr.cfda.gov.cn/WS01/CL1933/217590.html.
[19] 胡青, 孙健, 勇艳华, 等. 食品中西布曲明等化合物的测定: 国食药监办许[2017]24号[EB/OL]. (2017-02-28). http://samr.cfda.gov.cn/WS01/CL1933/177667.html
[20] 王铁松, 仝禹, 郑洁, 等. 薄层色谱法快速筛查降脂、降压、止咳平喘类中药制剂中的29 种添加化学药物[J]. 中国药学杂志, 2010,45(11): 857-861.
[21] 孙亮, 张蓉, 邬国庆, 等. 高效液相色谱法同时测定保健食品中9种非法添加降脂类药物[J]. 食品安全质量检测学报, 2016, 7(8):3098-3102.
[22] 胡青, 崔益泠, 张甦, 等. 降血脂和降血糖类中药及保健食品中违禁添加17 种化学药物的液相色谱-离子阱质谱定性检测[J].中国医药工业杂志, 2009, 40(2): 124-127. DOI:10.3969/j.issn.1001-8255.2009.02.016.
[23] 郝刚, 顾炳仁. UPLC-MS/MS检测降血脂类保健食品中违法添加物[J].中国执业药师, 2014, 11(7): 20-24.
[24] 姜树银, 郭常川, 石峰, 等. Q-Orbitrap高分辨质谱用于降血脂类中成药和保健食品中非法添加物的快速筛查、鉴定和定量[J]. 药物分析杂志, 2015, 35(8): 1447-1452.
[25] 金美春, 郑朝阳. 液质联用分析美伐他汀的有关物质[J]. 分析测试学报, 2007, 26(增刊l): 84-86.
[26] 陈林, 温家欣, 吴霞, 等. 改良QuEChERS技术结合液相色谱-串联质谱联用法同时快速检测辣椒制品中14 种非法添加工业染料[J]. 食品科学, 2017, 38(8): 296-302. DOI:10.7506/spkx1002-6630-201708046.
[27] 郝杰, 姜洁, 余建龙, 等. 固相萃取-超高效液相色谱-串联质谱法同时测定动物源性食品中多种兽药残留[J]. 食品科学, 2017, 38(12):266-272. DOI:10.7506/spkx1002-6630-201712041.
[28] GBYLIK-SIKORSKA M, POSYNIAK A, SNIEGOCKI T, et al. Liquid chromatography-tandem mass spectrometry multiclass method for the determination of antibiotics residues in water samples from water supply systems in food-producing animal farms[J]. Chemosphere, 2015, 119: 8-15. DOI:10.1016/j.chemosphere.2014.04.105.
[29] FU Y Q, ZHAO C X, LU X, et al. Nontargeted screening of chemical contaminants and illegal additives in food based on liquid chromatographyehigh resolution mass spectrometry[J].Trends in Analytical Chemistry, 2017, 96: 89-98. DOI:10.1016/j.trac.2017.07.014.
[30] 马祖兵, 孙强, 李小芳, 等. 红曲降脂成分他汀类物质检测方法的研究进展[J]. 中国实验方剂学杂志, 2017, 23(23): 228-234.DOI:10.13422/j.cnki.syfjx.2017230228.
LI Xiaolei 1 , CHEN Jun 2 , YANG Chaofen 1 , YANG Jun 1
(1. Research Center of Analysis and Measurement, Kunming University of Science and Technology, Kunming 650000, China;2. Research Institute of Resources Insects, Chinese Academy of Forestry, Kunming 650000, China)
Abstract: A method for the simultaneous determination of six blood lipid regulating drugs (nicotinicacid, pravastatin sodium, fluvastatin sodium, mevastatin, lovastatin and simvastatin) illegally added to antilipemic functional foods by ultra-performance liquid chromatography-tandem mass spectrometry (UPLC-MS/MS) was established. The samples were extracted with methanol. The analytes were separated on a Waters Acquity BEH-C 18 column with a mobile phase consisting of 0.1% aqueous formic acid solution and acetonitrile using gradient elution at a flow rate of 0.2 mL/min, detected by multiple reaction monitoring (MRM) with an electrospray ionization source in the positive ion mode, and quantified by the external standard method. Under the experimental conditions in this study, all analytes were separated well, and they were quantified accurately and rapidly within 4 min. The limits of detection of the method ranged from 4 and 39 µg/kg,and the recoveries for spiked samples were 80.2%–106.1%. Twenty batches of antilipemic functional foods were tested by the method and out of these, 3 were found to contain nicotinic acid and lovastatin. This method exhibited good linear relationships and it was fast, simple and highly accurate, and thus could be used for the simultaneous determination of the six drugs illegally added in antilipemic functional foods.
Keywords: ultra-performance liquid chromatography-tandem mass spectrometry (UPLC-MS/MS); antilipemic; chemicals;healthy foods; illegal additives
Determination of Six Antilipemic Chemicals Illegally Added in Antilipemic Functional Foods by UPLC-MS/MS
LI Xiaolei, CHEN Jun, YANG Chaofen, et al. Determination of six antilipemic chemicals illegally added in antilipemic functional foods by UPLC-MS/MS[J]. Food Science, 2018, 39(18): 320-325. (in Chinese with English abstract)DOI:10.7506/spkx1002-6630-201818049. http://www.spkx.net.cn
李晓蕾, 陈军, 杨朝芬, 等. 超高效液相色谱-串联质谱法检测辅助降血脂保健食品中6 种非法添加化学药物[J]. 食品科学, 2018, 39(18): 320-325. DOI:10.7506/spkx1002-6630-201818049. http://www.spkx.net.cn
文章编号: 1002-6630(2018)18-0320-06
引文格式:
中图分类号: TS255.4
文献标志码: A
第一作者简介: 李晓蕾(1978—),女,副教授,博士,研究方向为食品药品质量分析和天然产物化学。E-mail:lixiaolei0726@hotmail.com
DOI: 10.7506/spkx1002-6630-201818049
基金项目: 昆明理工大学自然科学基金项目(KKSY201532062)
收稿日期: 2018-02-05