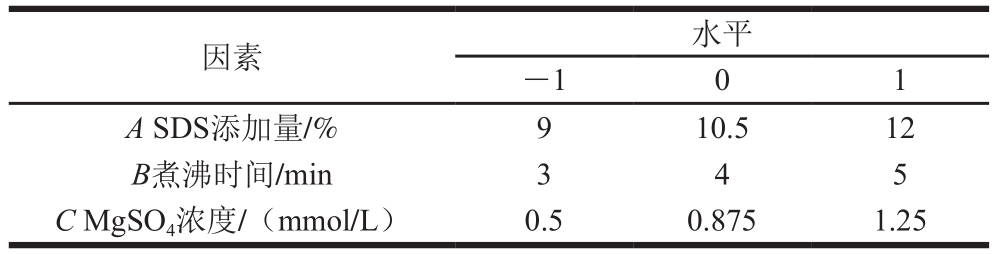
表1 响应面试验因素与水平
Table 1 Coded levels for independent variables used in response surface analysis
陈兰煊,杨 阳,易翠平*
(长沙理工大学化学与生物工程学院,湖南 长沙 410114)
摘 要:采用十二烷基硫酸钠(sodium dodecyl sulfate,SDS)缓冲体系分离提取碱洗籼米粉中的淀粉粒结合蛋白(starch granule-associated proteins,SGAPs),经高效液相色谱-串联质谱法鉴定表明:碱洗得到上、中、下层籼米淀粉中的SGAPs均主要为淀粉合成酶I(granule-bound starch synthase I,GBSS I),其他组分略有差别;其中以中层SGAPs含量最高,GBSS I达99.8%,谷蛋白质量分数仅为0.11%。采用响应面优化中层淀粉SGAPs的提取参数,得到最优条件为SDS添加量10.90%、煮沸时间4.10 min、MgSO4浓度0.90 mmol/L,此时SGAPs提取量为(1 028.61±0.05)μg/g。
关键词:籼米;淀粉粒结合蛋白(SGAPs);高效液相色谱-串联质谱法;淀粉合成酶I(GBSS I);响应面优化
淀粉粒结合蛋白(starch granule-associated proteins,SGAPs)是指紧密结合于淀粉表面及内部、具有显著特征的一类蛋白质[1],占籼米质量分数的0.2%~0.5%;它不同于普通蛋白,多以酶的形式存在于淀粉颗粒中决定其结构及形态[2],并对淀粉的糊化特性[3]、颗粒性质及整个谷物体系的品质有着重要影响[4],以颗粒淀粉合成酶(granule-bound starch synthase,GBSS)最为典型[5-6]。但由于籼米SGAPs含量低、组分复杂,又与淀粉颗粒结合紧密[7-8],相关研究不易开展,关于籼米中SGAPs研究鲜有报道,国内外研究主要集中在小麦和玉米等谷物中。目前,谷物SGAPs的分离主要采用NaCl溶液、2-丙醇、十二烷基硫酸钠(sodium dodecyl sulfate,SDS)和二硫苏糖醇等强极性溶液进行搅拌浸泡[9-12];但文献[13-15]指出,这种分离方法并不能将小麦SGAPs全部提取,Sargeant等[15]报道采用NaCl溶液仅能提取小麦总SGAPs的10%,Turnbull等[14]证明采用10% SDS溶液提取小麦SGAPs效率更高。因此,本研究拟采用SDS缓冲液提取籼米SGAPs,对所提取SGAPs进行十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(sodium dodecyl sulfate-polyacrylamide gel electrophoresis,SDS-PAGE)分离及高效液相色谱-串联质谱(high performance liquid chromatographtandem mass spectrometry,HPLC-MS/MS)鉴定;以响应面法优化SDS添加量、沸水浴时间、不同金属离子对籼米SGAPs分离纯化的工艺条件。为进一步分离及分析SGAPs组分对籼米基本品质的影响提供实验参考。
籼米:浙富802;SDS、丙三醇(甘油)、2-巯基乙醇、乙醇、三(羟甲基)氨基甲烷、溴酚蓝、甘氨酸、考马斯亮蓝G250、N,N-亚甲基丙烯酰胺、丙烯酰胺(均为分析纯) 国药集团化学试剂有限公司;过硫酸铵(分析纯) 西陇科学股份有限公司;乙酸、甲醇、磷酸(均为分析纯) 广东省化学试剂工程技术研究开发中心。
Triple TOF®5600 HPLC-MS/MS仪、Eksigent nanoLC-Ultra™ 2D纳升液相系统 美国AB SCIEX公司;5418R型高速冷冻离心机 德国Eppendorf公司;Savant DNA120离心浓缩仪 美国Thermo Fisher公司;UV-2800型分光光度计 尤尼柯(上海)仪器有限公司;AVY120型分析天平 北京赛多利斯天平有限公司;DK-2000-L型恒温水浴锅、FW100型万能粉碎机、HJ-1型磁力搅拌器 天津泰斯特仪器有限公司;DHG-9140A型鼓风干燥箱 上海一恒科学仪器有限公司;DYCZ型电泳仪 北京市六一仪器厂。
1.3.1 籼米淀粉制备
取过100 目的脱脂籼米粉,以0.045 mol/L NaOH溶液洗去蛋白,重复5 次,3 500 r/min离心,得到上层黄淀粉糊、中层白淀粉、下层黄淀粉(以下简称上、中、下层),用0.1 mol/L HCl溶液调pH值中性,洗涤、离心、低温烘干,4 ℃贮藏备用[16-17]。
1.3.2 SDS-PAGE分析蛋白亚基
根据Laemmli[18]的方法:采用不连续缓冲系统,分离胶12%,浓缩胶4%,胶板厚度1.0 mm,进样量15 μL,在80 V稳流电压下电泳,样品条带至胶板底部1 cm左右停止,采用考马斯亮蓝G250染色约4 h,脱色至条带清晰。
1.3.3 HPLC-MS/MS鉴定
样品经SDS-PAGE得到60 kDa亚基条带,经胰蛋白酶充分酶解得到上清液,离心浓缩干燥后得到胰酶切多肽[19-21]。将胰酶切多肽溶解入Nano-RPLC流动相A(0.1%甲酸溶液,2%乙腈溶液),装瓶上样到C18预柱(100 μm×3 cm,3 μm,150 Å),进行在线HPLC-MS/MS分析:流动相流速2 μL/min、10 min,液相采用C18反相色谱柱(75 μm×15 cm,3 μm,120 Å,Chrom XP Eksigent)分离,梯度洗脱为60 min内流动相B(0.1%甲酸,95%乙腈溶液)由5%升高至40%。质谱采用Triple TOF®5600系统结合纳升喷雾III离子源,喷雾电压为2.3 kV,气帘气压为30 psi,雾化气压为5 psi,加热温度为150 ℃,质谱扫描方式为信息依赖的采集工作模式下,一级飞行时间质谱单张图谱扫描时间为250 ms,每次采集工作模式循环下最多采集35 个电荷为2+到5+且单秒计数大于200 cps的二级图谱,每张二级图谱的累积时间为60 ms。每次循环时间固定为2.5 s,碰撞室能量设定适用于所有前体离子碰撞诱导解离,动态排除设置为12 s,约等于色谱半峰宽。
1.3.4 SGAPs的分离纯化
1.3.4.1 SGAPs的提取及测定
分别取1.0 0 g样品,加入S D S提取液(3%~12% SDS,5%巯基乙醇,10%甘油,62.5 mmol/L Tris,pH 6.9),搅拌均匀,沸水浴加热,冷却至室温后15 000 r/min离心15 min,考马斯亮蓝G250染色法测定上清液的蛋白含量[22]。
1.3.4.2 单因素试验
以样品煮沸时间3 min、MgSO4浓度0.75 mmol/L、SDS添加量9%为基本条件,改变SDS添加量:3%、5%、7%、9%、10%、12%,样品煮沸时间:1、2、3、4、5 min,浓度均为0.75 mmol/L的金属离子缓冲液:NaCl、MgCl2、KCl、CaCl2、Na2SO4、K2SO4、CaSO4、MgSO4,MgSO4浓度:0.25、0.5、0.75、1.00、1.25、1.50、2.00、2.50 mmol/L进行单因素试验。
1.3.4.3 响应面试验
在单因素试验的基础上,以提取SGAPs含量为响应值,选取SDS添加量、煮沸时间、MgSO4浓度3 个因素,设计3因素3水平的响应面分析试验。各因素与水平设计见表1。
表1 响应面试验因素与水平
Table 1 Coded levels for independent variables used in response surface analysis

实验数据采用Excel 2007、SPSS软件进行方差分析,Duncan新复极差法进行多重比较;HPLC-MS/MS鉴定采用Maxquant软件进行数据加工处理和检索分析,数据库为Uniprot的oryza sativa japonica物种蛋白数据库。
将籼米粉碱洗5 次后得到上、中、下层淀粉3 个样品,与籼米粉一起,分析其蛋白质量分数(表2)。结果表明,蛋白质量分数由低到高分别是中层、下层、上层、籼米粉,且经分离后的3层淀粉蛋白质量分数均低于0.5%,与Koziol等[23]报道SGAPs在籼米淀粉颗粒中质量分数为0.2%~0.5%一致,说明残留淀粉中的蛋白可能是SGAPs。
表2 碱处理籼米粉各组分的蛋白含量分析(n=3)
Table 2 Protein content of starch layers of alkali-washed indica rice fl our (dry basis, n= 3)
注:不同小写字母表示差异显著,P<0.05。

图1 籼米粉及不同籼米淀粉所提SGAPs的SDS-PAGE图
Fig. 1 SDS-PAGE image of SGAPs from indica rice fl our and different rice starch layers
将各层淀粉提取的SGAPs及籼米粉蛋白质进行电泳(图1),结果表明,与籼米粉蛋白亚基对照,3 层淀粉所提的SGAPs基本一致,均只有60 kDa亚基条带,说明多次碱洗后以SDS缓冲液提取能有效去除其他杂蛋白,得到较纯的SGAPs。其中,中层亚基颜色最深,下层次之,上层最浅,与上、中、下3 层淀粉中的蛋白含量呈相反趋势,说明上层淀粉蛋白中残留更多的与淀粉分子结合紧密的储藏蛋白,如谷蛋白、醇溶蛋白;中层淀粉SGAPs含量最高且更纯。
表3 SDS-PAGE条带HPLC-MS/MS鉴定结果
Table 3 HPLC-MS/MS analysis of the bands from SDS-PAGE
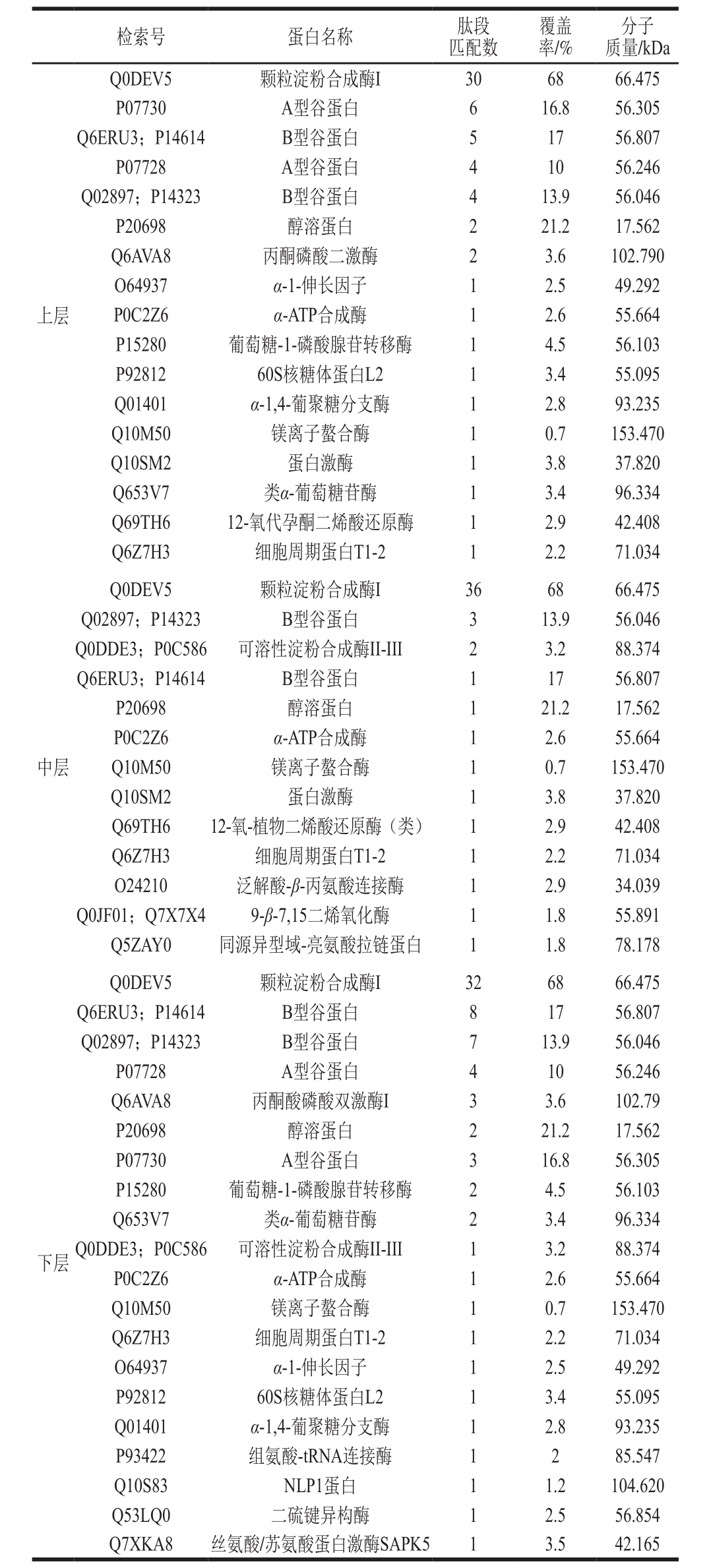
对电泳分离的60 kDa蛋白条带通过HPLC-MS/MS法进行鉴定[24],结果见表3,3层淀粉中的60 kDa蛋白均是以GBSS I为主的SGAPs,其中上层含A型谷蛋白0.58%、B型谷蛋白1.94%、醇溶蛋白0.15%、GBSS I 97.33%;中层淀粉SGAPs含量较为单一,GBSS I 99.80%、B型谷蛋白仅0.11%,可见SDS缓冲液能有效分离出中层淀粉SGAPs;下层淀粉仍以97.51%的GBSS I为主,A型谷蛋白0.15%、B型谷蛋白0.97%、醇溶蛋白0.06%,除此之外还含0.75%的α-ATP合成酶以及参与细胞代谢、能量调控及DNA转录和翻译的酶类和蛋白,如α伸长因子、60核糖体蛋白L2、NLP1蛋白、丙酮酸磷酸二激酶等。
HPLC-MS/MS结果表明,以SDS缓冲液从籼米淀粉中分离SGAPs的方式可行,能有效提取出SGAPs,且籼米中的SGAPs以GBSS I为主并以主要生物酶的形式负责谷物中的淀粉合成,影响直链淀粉与支链淀粉的比例[25]。上、中、下3 层淀粉中以中层淀粉的SGAPs含量最高最纯,因此选取中层淀粉进行SGAPs提取的优化试验。
2.4.1 SDS添加量对SGAPs提取量的影响

图2 SDS缓冲液添加量对SGAPs提取量的影响
Fig. 2 Effect of SDS buffer concentration on the extraction efficiency of SGAPs
如图2所示,SDS添加量对SGAPs提取量有显著影响(P<0.05),随着SDS添加量加大,SGAPs提取量逐渐升高,当SDS添加量为10%时达到最大提取量,随着SDS添加量继续升高,样品的SGAPs提取量开始有所下降,是由于SDS分子中的长链疏水基团与蛋白质分子内部的非极性基团相互作用,打破其原来有序结构[26],使蛋白质构象发生变化,目标蛋白变性,从而导致SGAPs的提取量降低。因此,提取籼米中SGAPs的最佳SDS添加量为10%。
2.4.2 煮沸时间对SGAPs提取量的影响
由于SGAPs紧密结合于淀粉颗粒内部,即便是盐浓度很高的提取液或缓冲液在低温下都很难进入到淀粉分子的内部与其作用[27]。利用高温条件下淀粉颗粒的糊化作用[28],淀粉颗粒的内部SGAPs缓慢膨胀并慢慢暴露,与反应试剂发生作用,由此可以分离纯化得到SGAPs[29]。因此煮沸时间对SGAPs的提取有重要影响。由图3可知,当煮沸时间为4 min时SGAPs提取量显著高于其他条件下提取量(P<0.05)。而随着煮沸时间的延长,SGAPs提取量逐渐下降。可能是由于一般淀粉颗粒在温度达到50 ℃时开始膨胀,反应试剂开始逐渐进入淀粉颗粒内部,当温度达到90 ℃时淀粉完全糊化[30],提取试剂最大程度与SGAPs接触,此时所用时间为4 min,随着煮沸时间延长,所提SGAPs由于高温作用已经发生热变性,导致在测定SGAPs提取量时呈逐渐减少趋势。

图3 煮沸时间对SGAPs提取量的影响
Fig. 3 Effect of heating time in boiling water bath on the extraction efficiency of SGAPs
2.4.3 金属离子对SGAPs提取量的影响

图4 金属离子对SGAPs提取量的影响
Fig. 4 Effect of metal ions on the extraction efficiency of SGAPs
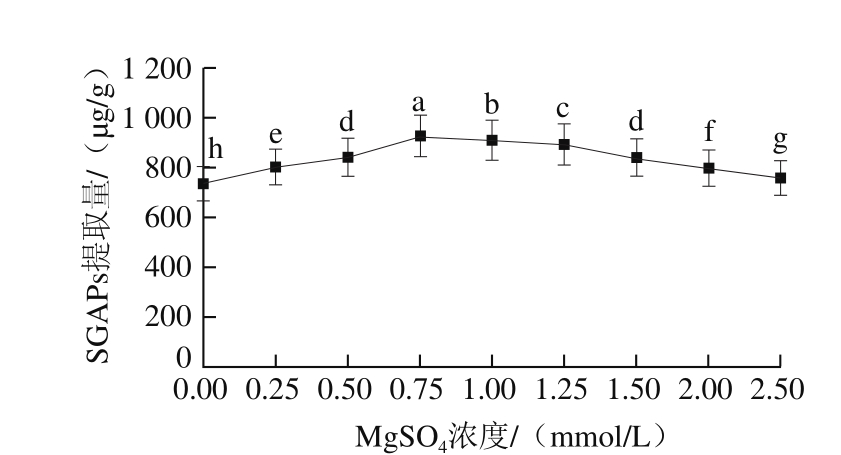
图5 MgSO4浓度对SGAPs提取量的影响
Fig. 5 Effect of magnesium ion concentration on the extraction efficiency of SGAPs
在SDS缓冲液中分别加入了Na+、K+、Mg2+和Ca2+等阳离子以及不同的阴离子Cl-和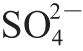 后,对淀粉颗粒上的SGAPs进行提取。如图4所示,不同金属离子对SGAPs的解离有显著影响(P<0.05),其中加入MgSO4后从淀粉颗粒上解离的SGAPs最多。由图5可知,随着MgSO4浓度的增大,SGAPs提取量呈先增大后减小的趋势。MgSO4浓度为0~0.75 mmol/L时,SGAPs提取量不断提高;浓度为0.75 mmol/L时,SGAPs提取量达到最大;当MgSO4浓度大于0.75 mmol/L后,SGAPs提取量逐渐下降。由于共价键不随离子类型与强度的变化而异[31],籼米SGAPs的解离随离子类型与强度的变化而变化,因此判断SGAPs结合力为非共价键。
后,对淀粉颗粒上的SGAPs进行提取。如图4所示,不同金属离子对SGAPs的解离有显著影响(P<0.05),其中加入MgSO4后从淀粉颗粒上解离的SGAPs最多。由图5可知,随着MgSO4浓度的增大,SGAPs提取量呈先增大后减小的趋势。MgSO4浓度为0~0.75 mmol/L时,SGAPs提取量不断提高;浓度为0.75 mmol/L时,SGAPs提取量达到最大;当MgSO4浓度大于0.75 mmol/L后,SGAPs提取量逐渐下降。由于共价键不随离子类型与强度的变化而异[31],籼米SGAPs的解离随离子类型与强度的变化而变化,因此判断SGAPs结合力为非共价键。
采用Design-Expert 8.0.6.1软件中的Box-Behnken设计试验,结果见表4。
表4 响应面试验设计与结果
Table 4 Experimental design and results for response surface analysis
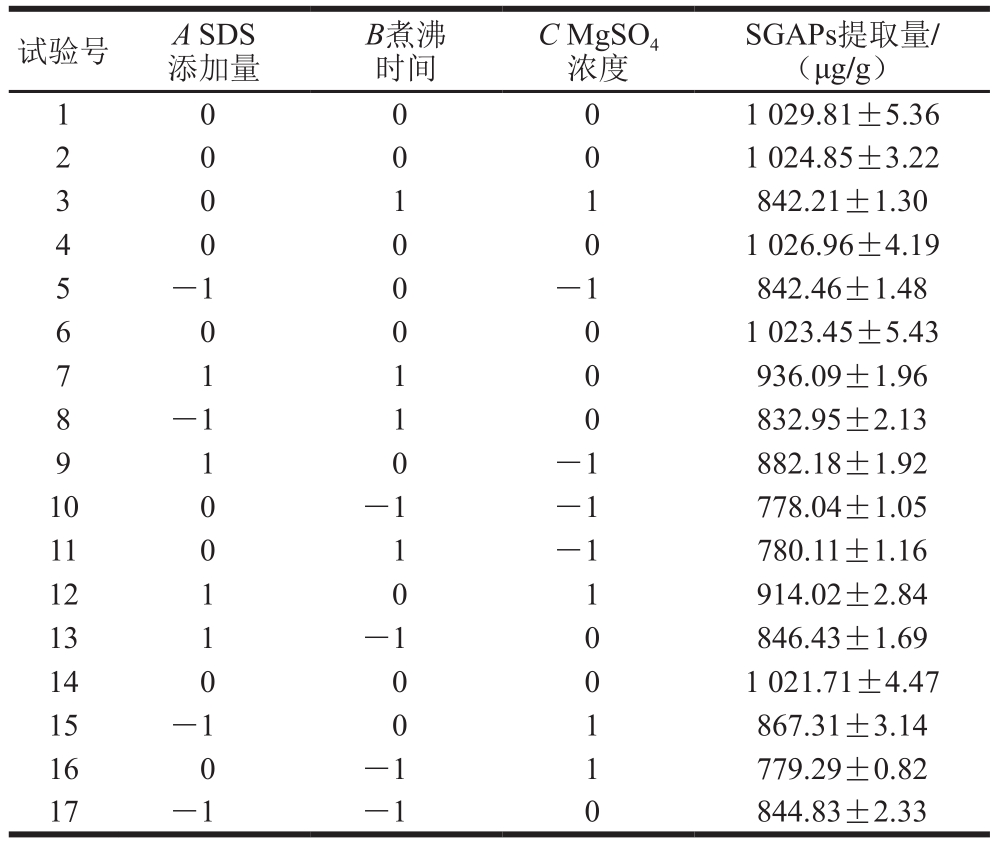
表5 中层籼米淀粉提取SGAPs回归模型方差分析
Table 5 Analysis of variance for the regression model describing the extraction efficiency of SGAPs
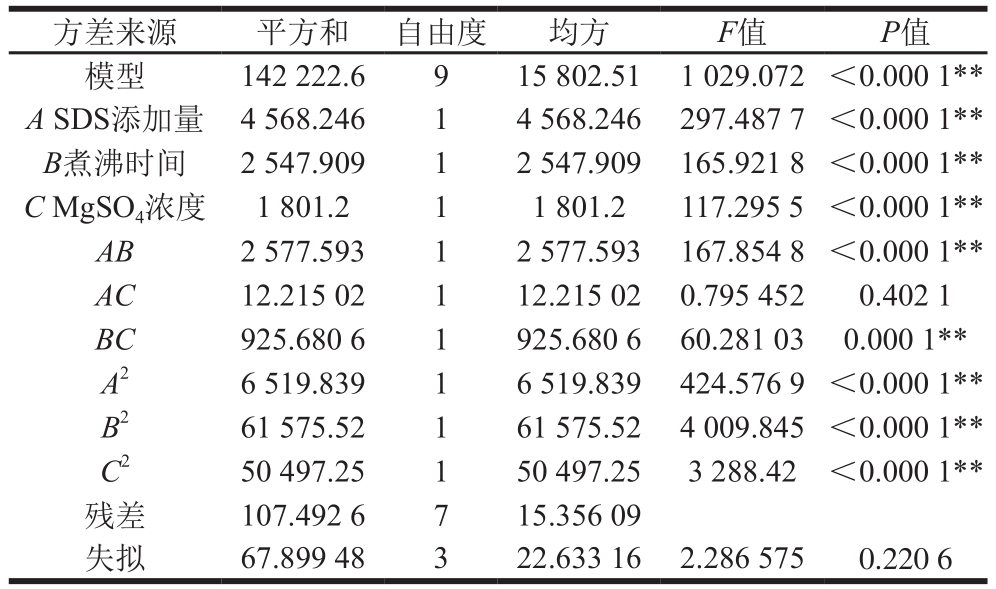
注:*. P<0.05,差异显著;**. P<0.01,差异极显著。
从表5可以看出,一次项A、B、C对SGAPs提取量的影响均达到极显著水平(P<0.01);交互项AB、BC达到极显著水平(P<0.01),交互项AC不显著(P>0.05),二次项A2、B2、C2、D2均达到极显著水平(P<0.01)。其中模型极显著(P<0.000 1),失拟项不显著(P=0.220 6>0.05),模型决定系数R2值为0.991 9,校正决定系数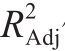 值为0.998 3,说明该模型能较好地反映SGAPs提取量与SDS添加量、煮沸时间、MgSO4浓度之间的关系,由此可见,这种试验方法是可靠的。
值为0.998 3,说明该模型能较好地反映SGAPs提取量与SDS添加量、煮沸时间、MgSO4浓度之间的关系,由此可见,这种试验方法是可靠的。
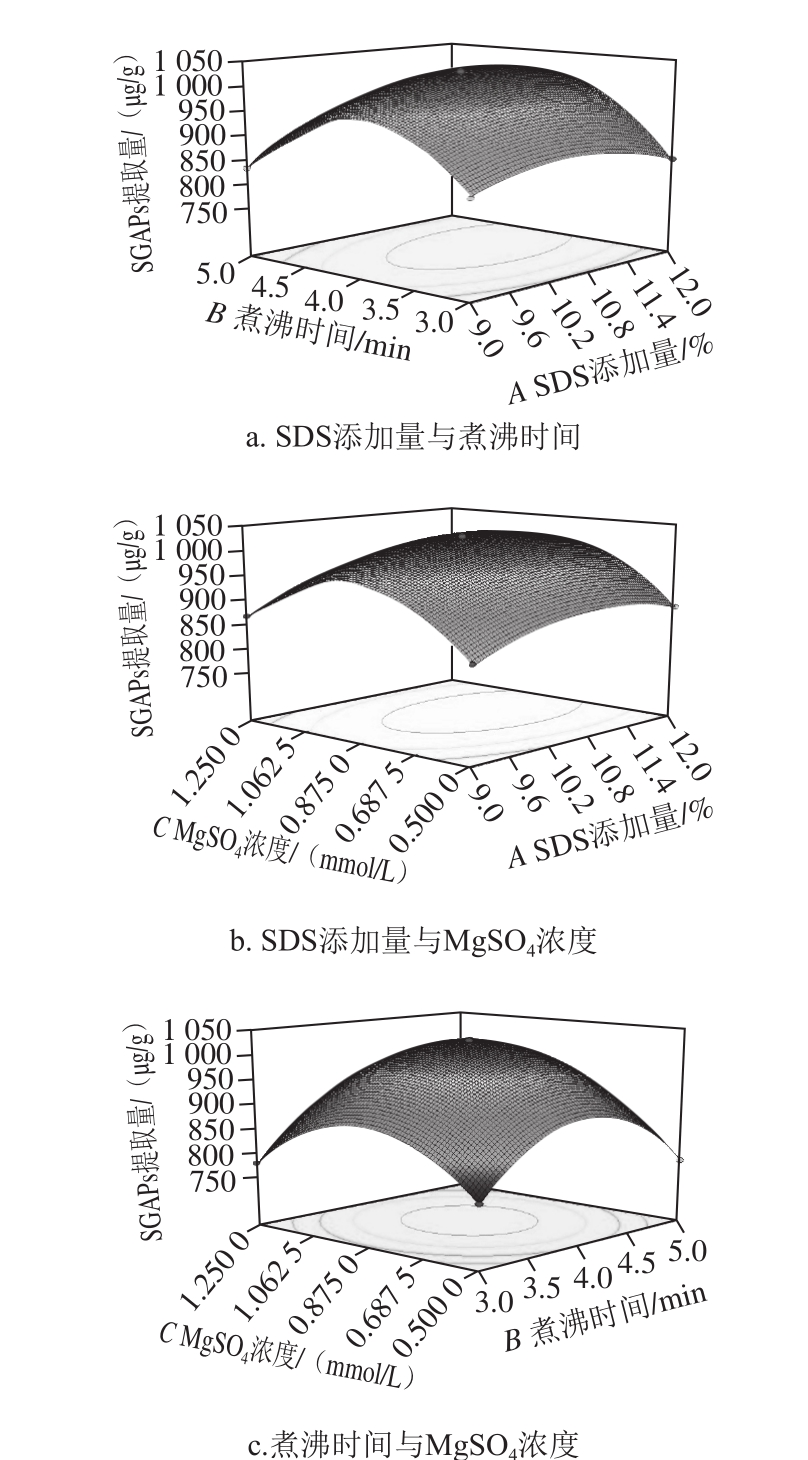
图6 因素交互作用对中层籼米淀粉SGAPs提取量的影响
Fig. 6 Response surface plots showing interactive effects of various factors on the extraction efficiency of SGAPs
由表5可知,SDS添加量、煮沸时间与MgSO4浓度均为影响淀粉SGAPs提取量的主要因素,各因素间交互影响分别如图6所示。SDS添加量与MgSO4浓度交互作用不显著(图6b),其余2 组交互显著,与表5方差分析结果一致。等高线呈椭圆形,表明煮沸时间与SDS添加量、MgSO4浓度间交互作用对SGAPs提取量有显著影响,此与单因素试验结果一致。
利用Design-Expert 8.0.6.1软件对样品提取SGAPs的工艺条件进行优化,得到SGAPs最优提取条件:SDS添加量10.95%、煮沸时间4.14 min、MgSO4浓度0.92 mmol/L。为方便工艺操作,将SGAPs提取最佳条件均修正为SDS添加量10.90%、煮沸时间4.10 min、MgSO4浓度0.90 mmol/L。在该条件下进行验证实验,分别得到SGAPs提取量实测值为(1 028.61±0.05)μg/g,与预测值1 037.28 μg/g非常接近。
碱洗籼米粉可以得到上、中、下3 层淀粉,SDS缓冲液提取、HPLC-MS/MS鉴定表明,不同淀粉层中的SGAPs均以GBSS I为主,其中以中层淀粉SGAPs含量最高,达99.80%。至于籼米粉中的GBSS I是否具有生理活性、在籼米的加工过程中能否因为其生理活性而对产品产生影响尚不得而知。响应面优化中层淀粉SGAPs提取参数,结果表明SDS添加量10.90%、煮沸时间4.10 min、MgSO4浓度0.90 mmol/L,SGAPs的提取量最大,达(1 028.61±0.05)μg/g。当然,这种条件下提取的SGAPs显然不可能是具有活性的酶,但同样可以考虑这种SGAPs仅作为蛋白质对于籼米基本品质的影响,至于具有酶活性的SGAPs分离提取方法,则需要进一步研究。
参考文献:
[1] BALDWIN P M. Starch granule-associated proteins and polypeptides:a review[J]. Starch-Stärke, 2015, 53(10): 475-503. DOI:10.1002/1521-379X(200110)53:10%3C475::AID-STAR475%3E3.0.CO;2-E.
[2] BARANOV Y O, SLISCHUK G I, VOLKOVA N E, et al.Bioinformatic analysis of maize granule-bound starch synthase gene[J]. Cytology & Genetics, 2014, 48(3): 150-154. DOI:10.3103/S0095452714030037.
[3] HAN X Z, HAMAKER B R. Partial leaching of granule-associated proteins from rice starch during alkaline extraction and subsequent gelatinization[J]. Starch-Stärke, 2002, 54(10): 454-460.
[4] NALUKENGE A, OBALLIM G, MAPHOSA M, et al. Contribution of granule bound starch synthase in kernel modification of quality protein maize[J]. Uganda Journal of Agricultural Sciences, 2013, 14(1): 101-109.
[5] CHO D H, HAN J A, LIM S T. Identification of botanical origin of starch by using peptide mass fingerprinting of granule-bound starch synthase[J]. Journal of Cereal Science, 2013, 57(3): 264-266.
[6] YU H, WANG T. Proteomic dissection of endosperm starch granule associated proteins reveals a network coordinating starch biosynthesis and amino acid metabolism and glycolysis in rice endosperms[J].Frontiers in Plant Science, 2016, 7: 707-716. DOI:10.3389/fpls.2016.00707.
[7] WATTOO J I, IQBAL M S, ARIF M, et al. Homology modeling,functional annotation and comparative genome analysis of GBSS enzyme in rice and maize genomes[J]. International Journal of Agriculture & Biology, 2015, 17(5): 1061-1065. DOI:10.17957/IJAB/15.0016.
[8] FUJITA N. Manipulation of rice starch properties for application[M].Tokyo, Japan: Springer, 2015. DOI:10.1007/978-4-431-55495-0_10.
[9] 郭华, 王宪泽, 李海雷, 等. 中国春小麦GBSS与淀粉颗粒结合特性的研究[J]. 作物学报, 2007, 33(2): 322-326. DOI:10.3321/j.issn:0496-3490.2007.02.023.
[10] SPENCER B. Soft wheat-view from great-britain[J]. Cereal Foods World, 1988, 33(8): 666.
[11] MORRISON W R, GREENWELL P, LAW C N, et al. Occurrence of friabilin, a low molecular weight protein associated with grain softness,on starch granules isolated from some wheats and related species[J].Journal of Cereal Science, 1992, 15(2): 143-149. DOI:10.1016/S0733-5210(09)80065-9.
[12] TAKAHASHI T, FUJITA N. Thermal and rheological characteristics of mutant rice starches with widespread variation of amylose content and amylopectin structure[J]. Food Hydrocolloids, 2017, 62: 83-93.DOI:10.1016/j.foodhyd.2016.06.022.
[13] BANCEL E, ROGNIAUX H, DEBITON C, et al. Extraction and proteome analysis of starch granule-associated proteins in mature wheat kernel (Triticum aestivum L.)[J]. Journal of Proteome Research,2010, 9(6): 3299-3310. DOI:10.1021/pr9010525.
[14] TURNBULL K M, RAHMAN S. Endosperm texture in wheat[J].Journal of Cereal Science, 2002, 36(3): 327-337. DOI:10.1021/pr9010525.
[15] LOWY G D, SARGEANT J G, SCHOFIELD J D. Wheat starch granule protein the isolation and characterization of a salt extractable protein from starch granules[J]. Journal of the Science of Food and Agriculture, 32(4): 371-377.
[16] 易翠平, 姚惠源. 高纯度大米蛋白和淀粉的分离提取[J]. 食品与机械, 2004, 20(6): 18-21. DOI:10.3969/j.issn.1003-5788.2004.06.008.
[17] YAMAMOTO K, SAWADA S, ONOGAKI T. Properties of rice starch prepared by alkali method with various conditions[J]. Journal of the Japanese Society of Starch Science, 2010, 20(3): 99-104.
[18] LAEMMLI U K. Cleavage of structural proteins during the assembly of the head of bacteriophage T4[J]. Nature, 1970, 227(5259): 680-685.DOI:10.1038/227680a0.
[19] YOOYANYONG A, DANWANICHAKUL D, DANWANICHAKUL P.The effect of remaining SDS on protein release in later leaching steps of deproteinized natural rubber[J]. KKU Engineering Journal, 2016,43(1): 41-46.
[20] RAUH M. LC-MS/MS for protein and peptide quantification in clinical chemistry[J]. Journal of Chromatography B, 2012, 884(4): 59-67.
[21] ZHAO Y, ZHANG W, KHO Y, et al. Proteomic analysis of integral plasma membrane proteins[J]. Analytical Chemistry, 2004, 76(7):1817-1823. DOI:10.1021/ac0354037.
[22] 赵倩倩, 冯艳玲, 贾小芳, 等. 免疫性肝纤维化大鼠肝非实质细胞蛋白质组分析[J]. 中国科学: 生命科学, 2013, 43(11): 928-914.
[23] KOZIOL A G, MARQUEZ B K, HUEBSCH M P, et al. The starch granule associated proteomes of commercially purified starch reference materials from rice and maize[J]. Journal of Proteomics, 2012, 75(3):993-1003. DOI:10.1016/j.jprot.2011.10.019.
[24] 齐耀程, 王宁, 程彦伟, 等. 水稻根尖质膜蛋白质组学研究方法的建立[J]. 中国水稻科学, 2008, 22(2): 111-117. DOI:10.3321/j.issn:1001-7216.2008.02.001.
[25] LUI D R, HUANG W X, CAI X L. Oligomerization of rice granulebound starch synthase 1 modulates its activity regulation[J]. Plant Science, 2013, 210(9): 141-150.
[26] SALAZAR-SALAS N Y, PINEDA-HIDALGO K V, CHAVEZONTIVEROS J, et al. Biochemical characterization of QTLs associated with endosperm modification in quality protein maize[J].Journal of Cereal Science, 2014, 60(1): 255-263. DOI:10.1016/j.jcs.2014.04.004.
[27] GOLDNER W R, BOYER C D. Starch granule-bound proteins and polypeptides: the inf l uence of the waxy mutations[J]. Starch-Stärke,2010, 41(7): 250-254. DOI:10.1002/star.19890410704.
[28] 李兆丰, 顾正彪, 洪雁. 稻米淀粉的研究进展[J]. 食品科学, 2004,25(12): 184-188. DOI:10.3321/j.issn:1002-6630.2004.12.041.
[29] AHMED J. Pasting properties of starch: effect of particle size,hydrocolloids and high pressure[M]. Safat: Chichester, UK, 2017.DOI:10.1002/9781118935682.ch16.
[30] MARSHALL W E, NORMAND F L, GOYNES W R. Effects of lipid and protein removal on starch gelatinization in whole grain milled rice[J]. Cereal Chemistry, 1990, 67(5): 458-463.
[31] 王镜岩, 朱圣庚, 徐长法. 生物化学[M]. 1版. 北京: 高等教育出版社,2002: 56-57.
Isolation and Identification of Starch Granule-Associated Proteins (SGAPs) from Indica Rice
CHEN Lanxuan, YANG Yang, YI Cuiping*(School of Chemistry and Biological Engineering, Changsha University of Science and Technology, Changsha 410114, China)
Abstract:Starch granule-associated proteins (SGAPs) from indica rice were isolated by sodium dodecyl sulfate (SDS) buffer from alkali washed rice fl our and then identified by high performance liquid chromatography-tandem mass spectrometry(HPLC-MS/MS). Results indicated that the SGAPs from the top, middle and bottom starch layers mainly consisted of granule-bound starch synthase I (GBSS I), which slightly varied with respect to other components. Among these layers, the content of SGAPs in the middle layer was the highest, with GBSS I accounting for up to 99.8% and gluten accounting for only 0.11% of the total. Using the response surface methodology, the optimized conditions for SGAPs extraction from the middle layer starch were obtained as follows: SDS 10.90%, boiling time 4.10 min and MgSO40.90 mmol/L. Under these conditions, the yield of SGAPs was (1 028.61 ± 0.05) μg/g.
Keywords:rice; starch granule-associated proteins; HPLC-MS/MS; granule-bound starch synthase I; response surface methodology
CHEN Lanxuan, YANG Yang, YI Cuiping. Isolation and identification of starch granule-associated proteins (SGAPs)from indica rice[J]. Food Science, 2018, 39(20): 240-245. (in Chinese with English abstract) DOI:10.7506/spkx1002-6630-201820035. http://www.spkx.net.cn
陈兰煊, 杨阳, 易翠平. 籼米中淀粉粒结合蛋白的分离鉴定及提取工艺优化[J]. 食品科学, 2018, 39(20): 240-245.DOI:10.7506/spkx1002-6630-201820035. http://www.spkx.net.cn
文章编号:1002-6630(2018)20-0240-06引文格式:
文献标志码:A
中图分类号:TS213
DOI:10.7506/spkx1002-6630-201820035
*通信作者简介:易翠平(1973—),女,教授,博士,研究方向为粮食深加工。E-mail:109823769@qq.com
第一作者简介:陈兰煊(1992—),女,硕士,研究方向为粮食、油脂与植物蛋白工程。E-mail:852945804@qq.com
基金项目:国家自然科学基金面上项目(31771899)
收稿日期:2017-09-09