王璐阳1,刘玉兰1,*,马宇翔1,黄会娜1,王风艳2,王满意2
(1.河南工业大学粮油食品学院,河南 郑州 450001;2.中粮营养健康研究院有限公司,北京 102200)
摘 要:对油脂脱臭用直接蒸汽水源中氯离子含量和待脱臭油脂中氯离子含量进行检测分析,并采用不同氯离子含量的直接蒸汽对油脂进行蒸馏脱臭,检测脱臭前后油脂中3-氯丙醇酯(3-monochloro-1,2-propanediol ester,3-MCPD酯)和缩水甘油酯(glycidyl esters,GEs)含量及氯离子含量,研究油脂脱臭过程氯离子含量对脱臭油脂中3-MCPD酯和GEs的影响。结果表明:油脂脱臭用直接蒸汽中氯离子含量随其水源中氯离子含量增加而升高,水源中氯离子含量在对应饱和蒸汽中的保留率约为0.1%;当油脂脱臭用直接蒸汽水源中氯离子质量浓度达到50~200 mg/L时,脱臭油脂中3-MCPD酯含量大幅升高至低质量浓度氯离子水源(1~10 mg/L)脱臭油脂中含量的2.6 倍,但脱臭油脂中氯离子含量并未升高;待脱臭油脂中氯离子含量升高会导致脱臭后油脂中3-MCPD酯和GEs含量的升高。在待脱臭油脂中添加质量浓度为100 mg/L的氯化钠溶液0.5~5 mL时(相当于油脂中添加量1~10 mg/kg),脱臭后油脂中3-MCPD酯和GEs生成量分别为4.49~7.84 mg/kg和14.88~19.84 mg/kg,是待脱臭油脂含量的5.5~9.5 倍和5.8~7.7 倍。因此,控制和减少油脂脱臭过程氯离子含量对降低脱臭油脂中3-MCPD酯和GEs含量有重要作用。
关键词:油脂;脱臭;氯离子;3-氯丙醇酯;缩水甘油酯
3-氯丙醇酯(3-monochloro-1,2-propanediol ester,3-MCPD酯)和缩水甘油酯(glycidyl esters,GEs)是近年来逐渐被关注的食用植物油中的安全风险成分[1-4]。3-MCPD酯在人体胃肠道内肠胰脂酶作用下分解成3-MCPD而对人体产生毒害作用[5-7]。根据世界卫生组织的评估报告,3-MCPD的最高摄入限量为2 μg/kg[8]。GEs是缩水甘油和游离脂肪酸的酯化产物,德国油脂科学协会将其定义为2类致癌物[9-11]。
目前,很多研究表明食用油中的3-MCPD酯和GEs主要产生于油脂的精炼过程,尤其是油脂高温蒸馏脱臭过程[12-16],且有研究发现3-MCPD酯的形成机制主要是由于氯离子的亲核攻击环酰氧鎓离子、甘油骨架上的酯基以及缩水甘油的环氧基所导致[17],若在脱臭过程中能消除氯离子则能中断GEs向3-MCPD酯的转化反应[18]。氯化物在棕榈油加工中形成3-MCPD酯的机制已有明确报道[19-21],但对氯离子引入量及其在油脂精炼过程形成3-MCPD酯和GEs的影响程度并不明确,因为油脂精炼过程中所使用加工助剂(如磷酸、烧碱、脱色白土、水、蒸汽等)均可能含有氯离子并将氯离子引入到油脂中[22]。
仅在油脂脱臭过程中,氯离子的来源可能有两个:一是脱臭用直接蒸气携带引入的氯离子;二是待脱臭油脂自身带入的氯离子,这些氯离子可能是植物油料含氯或脱臭之前的其他精炼工序引入的。因此,研究油脂脱臭过程直接蒸汽和待脱臭油中氯离子含量对3-MCPD酯和GEs形成的影响,对控制油脂脱臭过程3-MCPD酯和GEs的生成有重要意义。本实验通过对油脂脱臭用直接蒸汽及其水源中氯离子含量和待脱臭油脂中氯离子含量的检测分析,了解油脂脱臭过程氯离子的水平,并采用不同氯离子含量的直接蒸汽对油脂进行蒸馏脱臭,通过检测脱臭前后油脂中3-MCPD酯和GEs含量及氯离子含量,研究油脂脱臭过程氯离子含量对脱臭油脂中3-MCPD酯和GEs的影响。以期能通过控制氯离子含量来减少甚至避免精炼油脂中3-MCPD酯和GEs的生成。
待脱臭大豆油,取样于河南一大豆油加工企业的油脂精炼生产线;超纯水分别取自市售娃哈哈纯净水、实验室超纯水机自制的超纯水(电阻率大于18 MΩ•cm);蒸馏水由实验室蒸馏水机自制;自来水取自城市管网供水的实验室自来水管。
标准品:氘代油酸缩水甘油酯(纯度≥97%)、油酸缩水甘油酯(纯度≥97%)、3-油酸-氯丙醇酯(纯度≥97%)、1,2-二亚油酸-3-氯丙醇酯(纯度≥97%)、1,2-二月桂酸-3-氯丙醇酯-D5(纯度≥97%) 上海安普实验科技股份有限公司;苯基硼酸(纯度≥97%)、正己烷、甲醇、异丙醇、甲基叔丁基醚、乙酸乙酯,均为色谱纯;乙醚、溴化钠、硫酸(质量分数为98%)、硫酸钠、碳酸氢钠、无水硫酸镁,均为分析纯;氯化钠为优级纯。
Trace1310-ISO气相色谱-质谱联用仪、ICS-2100离子色谱仪 美国Thermo Fisher公司;MTN-2800W氮吹浓缩仪 天津奥得赛恩斯仪器有限公司;KQ3200DE数控超声波清洗器 昆山市超声仪器有限公司;LD5-10台式大容量离心机 北京京立离心机有限公司;ZD-85数显气浴恒温振荡器 江苏金坛市宏华仪器厂;QL-902涡旋均匀器 海门市其林贝尔仪器制造有限公司;SZCL-2数显智能控温磁力搅拌器 巩义市予华仪器有限责任公司;DF-101S集热式恒温加热磁力搅拌器 河南省予华仪器有限公司;2XZ-1旋片式真空泵 北京中兴伟业仪器有限公司;Moiresearch摩尔分析型超纯水器 重庆摩尔水处理设备有限公司;YAZD-5升全不锈钢断水自控蒸馏水器 绍兴市上虞道墟科析仪器厂。
1.3.1 不同氯离子含量的大豆油脂脱臭
1.3.1.1 利用不同氯离子质量浓度水源产生的直接蒸汽进行油脂脱臭
配制不同质量浓度氯离子水,置于蒸汽发生装置中,称取约50 g待脱臭大豆油于250 mL三口烧瓶内,并放入磁力转子和沸石,将三口瓶放入事先架制好的水蒸汽蒸馏脱臭装置中,启动真空泵,在系统绝对压力400 Pa以下时,将油缓慢加热至260 ℃,然后开启直接蒸汽导管旋塞,通入直接蒸汽,在不引起油飞溅的情况下,使通汽量最大且流量恒定,脱臭2 h后,关闭直接蒸汽旋塞,将油温降至室温后破除真空,取脱臭后油脂样品。
1.3.1.2 对不同氯离子溶液添加量的油脂进行脱臭
将配制好的100 mg/L氯离子溶液分别取0.5、2.5、5 mL分别添加到已准确称取好50 g油的三口烧瓶内,并放入磁力转子和沸石,将三口瓶放入事先架制好的水蒸汽蒸馏脱臭装置中,室温搅拌1 h。将氯离子视为全部溶解,则此时油脂中氯离子含量约为1、5、10 mg/kg。按照上述方法进行脱臭。取脱臭后油脂样品,检测脱臭前后油脂中氯离子、3-MCPD酯和GEs含量。
1.3.2 水源、蒸汽冷凝水及油脂中氯离子的检测
1.3.2.1 水源及蒸汽冷凝水中氯离子检测
参照GB/T 5750.5—2006《生活饮用水标准检验方法无机非金属指标》中离子色谱检测法。
色谱条件:色谱柱型号AS-16;保护柱型号AG-16;淋洗液25 mmol/L KOH;淋洗液流速1.0 mL/min;柱温30 ℃;进样体积10 µL。蒸气冷凝水中氯离子的保留率计算公式为:
1.3.2.2 油脂中氯离子的检测
前处理方法在晋榕等[23]测定地沟油中氯离子方法的基础上进行优化:称取5 g油于30 mL螺纹试管中,用10 mL正己烷溶解待脱臭油再加5 mL超纯水。拧紧试管盖,涡旋30 s使水与有机相充分接触。超声30 min以辅助萃取,然后4 500 r/min离心4 min。将试管中的下层水相过有机滤膜至10 mL容量瓶中,定容。用离子色谱仪测定氯离子含量,选择手动进样,进样时过0.22 μm水相滤膜和C18柱(C18柱依序用5 mL色谱纯甲醇、10 mL超纯水活化)进行测定。
经过前处理将油脂中的氯离子提取入水溶液中,因此检测方法参照水源及蒸汽冷凝水中氯离子检测。
1.3.2.3 氯离子标准曲线的绘制
配制100 mg/L的氯离子标准溶液:优级纯氯化钠在120 ℃烘干4 h,称取0.164 8 g,用超纯水定容至1 000 mL容量瓶中,作为氯离子标准溶液。
用超纯水将质量浓度为100 mg/L的氯离子标准溶液分别逐级稀释至质量浓度为5、2、0.8、0.4、0.1、0.06、0.03、0.01 mg/L,由低到高依次进样,绘制标准工作曲线。得到线性回归方程Y=0.306 3X+0.038,标准工作曲线的相关系数R2为0.999 7,表明氯离子在标准溶液的质量浓度范围内具有良好的线性关系。
1.3.3 油脂中3-MCPD酯和GEs的测定
参照GB 5009.191—2016《食品中氯丙醇及其脂肪酸酯含量的测定》以及苗雨田[24]、杨贵芝[25]等文献资料,采用酸水解的方法间接测定油脂中3-MCPD酯和GEs,以GC-MS法测定,采用同位素内标进行定量。
1.3.3.1 测定油脂中3-MCPD酯和GEs的前处理方法
酸水解:分别称取(100±5)mg待脱臭大豆油,加入3-MCPD酯和GEs氘代同位素内标溶液和甲基叔丁基醚,旋涡使其充分溶解并混匀。加溴化钠的酸性水溶液50 ℃反应15 min后,加入正己烷使油脂从水相中分离出来,氮吹干并用甲基叔丁基醚复溶。向复溶溶液中添加硫酸-甲醇溶液(1.8%,V/V),充分反应后,加入正己烷洗涤去脂,然后向水相中加入乙酸乙酯-乙醚混合溶液,混匀后取上层溶液转移至有少量无水硫酸镁的试管中,待衍生化。
衍生化:向待衍生化的溶液中加入苯基硼酸溶液,混匀后氮吹至干。加正己烷复溶,过滤膜至进样小瓶。
1.3.3.2 GC-MS测定条件
色谱条件:色谱柱,含5%苯基亚芳基聚合物或5%苯基-甲基聚硅氧烷的弱极性毛细管气相色谱-质谱柱(30 m×0.25 mm,0.25 μm),载气为氦气,流速1 mL/min,进样口温度250 ℃,进样量1 μL,不分流进样,不分流时间0.5 min,溶剂延迟时间5 min。程序升温:50 ℃保持1 min,以2 ℃/min升至90 ℃,再以40 ℃/min升至270 ℃,并保持5 min。
质谱条件:电子电离源,电离能量70 eV,离子源温度250 ℃,传输线温度280 ℃,扫描方式选择离子监测模式。
3-MCPD酯和GEs的出峰时间如图1所示,其中3-MCPD酯及其内标物的出峰时间分别为18.12 min和18.06 min,GEs及其内标物的出峰时间分别为19.69 min和19.62 min。

图1 GC-MS中3-MCPD酯和GEs出峰时间色谱图
Fig. 1 Chromatograms of 3-MCPD ester and GEs in GC-MS analysis
2.1.1 脱臭用直接蒸汽的水源中氯离子含量
表1 不同水源中氯离子含量
Table 1 Chloride contents in different water sources
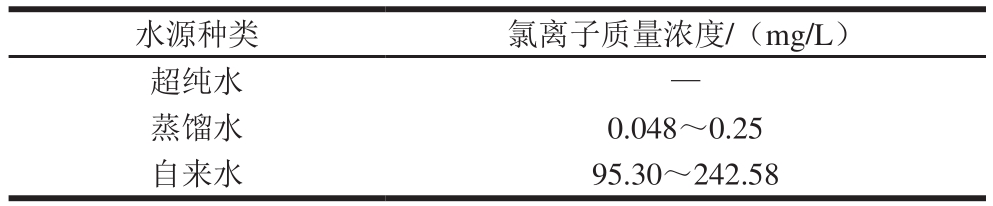
注:—.未检出。表2同。
由表1可知,在所取的超纯水中不论是娃哈哈纯净水还是超纯水机自制的超纯水中均未检测到氯离子。蒸馏水中氯离子含量与自来水相比含量明显差别较大,而蒸馏水是通过自来水蒸发冷凝得到的,由此可知自来水在蒸发过程中可能会携部分氯离子到冷凝水中。自来水中氯离子质量浓度最高可达到242.58 mg/L,在GB 5749—2006《生活饮用水卫生标准》中规定了生活饮用水中氯化物质量浓度不超过250 mg/L,可能是因为在自来水消毒处理处理过程中,常用的消毒水中除臭氧外均含有氯,所以导致消毒处理后的水中氯离子含量较高。
2.1.2 不同氯离子质量浓度水源的蒸汽冷凝水中氯离子含量及保留率
表2 不同氯离子质量浓度水源的蒸汽冷凝水中氯离子含量及保留率
Table 2 Chloride content in steam condensate of water sources with different chloride concentrations

根据常用水中氯离子的质量浓度范围,用超纯水配制氯离子质量浓度为20、50、100、200 mg/L的水样,加热蒸发并收集其蒸汽冷凝水,测定冷凝水中氯离子含量,计算其氯离子保留率,结果见表2。当水源中氯离子质量浓度为20 mg/L时,其对应蒸汽冷凝水中氯离子未能检出;当水源中氯离子质量浓度在50~200 mg/L时,蒸汽冷凝水中氯离子含量随水源中氯离子含量的增加而升高,氯离子的保留率约为0.1%。由此可知,在油脂脱臭过程中,当所用蒸汽的水源中氯离子质量浓度大于50 mg/L时,氯离子即会随着其蒸汽进入到待脱臭油中,可能与油脂中的某些物质发生反应生成3-MCPD酯和GEs。
2.1.3 水源中氯离子含量对脱臭油脂中3-MCPD酯的影响
根据常用水中氯离子的质量浓度范围,用超纯水配制氯离子质量浓度为1、5、20、50、100、200 mg/L的水样,根据工厂的油脂脱臭条件(绝对压力400 Pa以下、脱臭温度260 ℃、脱臭时间2 h)对脱色后的大豆油进行脱臭。
由图2可以看出,当水源中氯离子质量浓度在5 mg/L以下时,3-MCPD酯含量保持在1.66 mg/kg左右,没有随水源中氯离子质量浓度的增加而升高;当水源中氯离子达到20 mg/L时,脱臭油脂中3-MCPD酯含量稍有增加;当水源中氯离子超过50 mg/L时,脱臭油脂中3-MCPD酯含量大幅升高;水源中氯离子质量浓度达到200 mg/L时,脱臭油脂中3-MCPD酯含量更是升高至4.413 mg/kg,是低质量浓度氯离子水源(1~10 mg/L)脱臭油脂中含量的2.6 倍。结果明确显示出,油脂脱臭用直接蒸汽的水源中若含有高质量浓度的氯离子必然会造成脱臭油脂中3-MCPD酯含量的升高。这是因为脱臭用直接蒸汽携带的大量氯离子会与油脂中3-MCPD酯的前体物质进行反应[17,26],从而使3-MCPD酯含量升高。
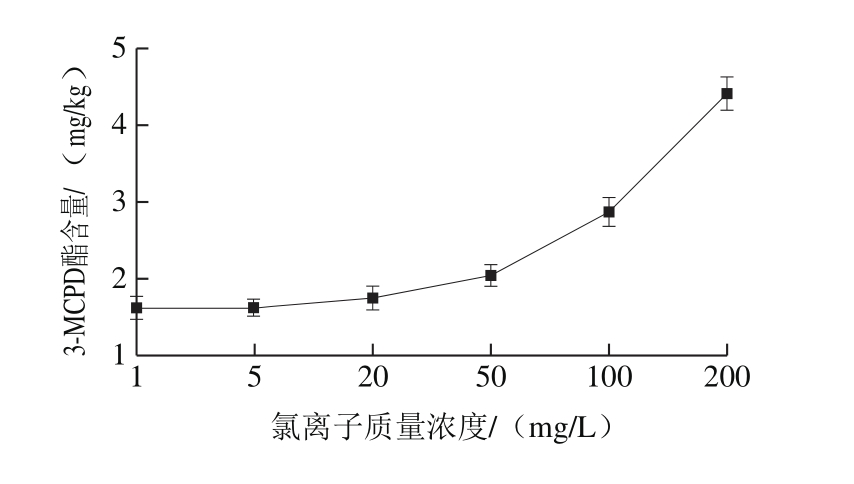
图2 水源中氯离子含量对脱臭油脂中3-MCPD酯的影响
Fig. 2 Effect of chloride ion content in water source on 3-MCPD ester content in deodorized oil
2.1.4 水源中氯离子含量对脱臭油脂中氯离子含量的影响

图3 水源中氯离子质量浓度对脱臭油脂中氯离子含量的影响
Fig. 3 Effect of chloride concentration in water source on chloride content in deodorized oil
分别采用氯离子质量浓度为1、5、20、50、100、200 mg/L水源产生的直接蒸汽对油脂脱臭,之后对脱臭前后油脂中氯离子含量进行检测分析,研究水源中氯离子含量对脱臭油中氯离子含量的影响,结果如图3所示。由图3可知,待脱臭油中氯离子含量为0.280 1 mg/kg,采用不同氯离子质量浓度的水源产生的直接蒸汽对油脂脱臭后,对应脱臭油中氯离子含量(0.2~0.25 mg/kg)均低于待脱臭油,并未随水源中氯离子质量浓度增大而造成脱臭油脂中氯离子含量升高,但脱臭油脂中3-MCPD酯含量却随水源中氯离子含量增大而呈现持续升高的现象。其原因可能是直接蒸汽引入到脱臭系统的氯离子并未呈游离态溶解在油脂中,而是在高温条件下与油脂中的某些组分发生反应形成了3-MCPD酯,且待脱臭油本身含有的氯离子在高温条件下也可能发生反应形成3-MCPD酯,以致最终造成脱臭油中氯离子含量比待脱臭油中的还要低。
2.2.1 待脱臭油中氯离子添加量的影响
在已准确称取的50 g待脱臭油中分别添加质量浓度为100 mg/L的氯化钠溶液0、0.5、2.5、5 mL[27]。用超纯水作为脱臭用直接蒸汽的水源对油脂进行脱臭,待脱臭油中氯离子溶液添加量对脱臭油中3-MCPD酯和GEs的影响如图4所示。

图4 待脱臭油中氯离子溶液添加量对脱臭油中3-MCPD酯和GEs的影响
Fig. 4 Effect of chloride sodium addition on 3-MCPD ester and GEs contents in deodorized oil
经测定,待脱臭油中3-MCPD酯和GEs含量分别为0.817 mg/kg和2.551 mg/kg。由图4可知,当待脱臭油脂中未添加氯化钠溶液时,脱臭后油脂中3-MCPD酯和GEs的含量分别为2.908 mg/kg和10.104 mg/kg,分别是待脱臭油的3.5 倍和3.9 倍。随着氯化钠溶液添加量的增加,脱臭油脂中3-MCPD酯的含量持续升高,即使0.5 mL的最小氯化钠溶液添加量,脱臭油中3-MCPD酯含量也达到4.49 mg/kg,是未添加脱臭油中生成量的1.5 倍,是待脱臭油的5.5 倍。当氯化钠溶液添加达到5 mL最大量时,3-MCPD酯的含量达到了7.84 mg/kg,是未添加脱臭油中生成量的2.7 倍,是待脱臭油的9.5 倍。而脱臭油中GEs的生成量,分别在氯化钠溶液添加量为0.5 mL和2.5 mL时,显著升高至16.36 mg/kg和19.85 mg/kg,分别是未添加脱臭油中生成量的1.6 倍和1.9 倍,是待脱臭油中含量的6.4 倍和7.7 倍。但当添加量达到5 mL的最大量时,脱臭油中GEs生成量增幅有所减小。有研究表明,脱臭油脂中10%~60%的3-MCPD酯可能是由GEs转化而成[28],或者氯离子的亲核作用所导致。随着反应的进行,氯离子、3-MCPD酯和GEs这3 种物质之间最终会达到动态平衡[29]。
2.2.2 油脂脱臭前后氯离子含量对比分析
当向待脱臭油脂中添加不同量的氯化钠溶液后,待脱臭油脂中氯离子含量发生变化,脱臭后油脂中氯离子含量与待脱臭油中氯离子含量对比如图5所示。未添加氯离子溶液时,脱臭油中氯离子含量低于待脱臭油,添加氯离子溶液后脱臭油中氯离子含量均比待脱臭油含量高,且均保持在0.35 mg/kg左右。这表明添加了氯离子溶液的油脂在脱臭过程中,氯离子部分用来生成了3-MCPD酯,未完全反应的氯离子则保留在脱臭油脂中,所以脱臭油中的氯离子相比于待脱臭油中的含量要高。此外,虽然溶解在油脂中的氯离子较少,但有研究表明有机酸具有一定的催化作用,能提高氯化反应生成3-MCPD酯,这是因为在形成3-MCPD酯的前体——酰基氧翁离子过程中,sn1位与sn2位的交联需要H+的催化[28,30]。因此,在油脂生产过程中应该尽可能控制氯离子引入,从而抑制3-MCPD酯和GEs的生成。

图5 待脱臭油中氯离子溶液添加量对脱臭油中氯离子含量的影响
Fig. 5 Effect of chloride sodium addition on chloride content in deodorized oil
油脂脱臭用直接蒸汽中氯离子含量随其水源中氯离子含量的增加而升高,但在水源中氯离子质量浓度为0~242.58 mg/L时,其对应饱和蒸汽中氯离子的保留率约为0.1%。当油脂脱臭用直接蒸汽水源中氯离子质量浓度达到50~200 mg/L时,脱臭油脂中3-MCPD酯含量大幅升高至低质量浓度氯离子水源(1~10 mg/L)脱臭油脂含量的2.6倍,但脱臭油脂中氯离子含量并未升高。当向待脱臭油中添加氯化钠溶液造成待脱臭油脂中氯离子含量升高时,均导致脱臭油中3-MCPD酯和GEs含量的升高。在添加质量浓度为100 mg/L的氯化钠溶液0.5~5 mL时(相当于在油脂中添加量为1~10 mg/kg),脱臭油中3-MCPD酯生成量为4.49~7.84 mg/kg,是待脱臭油含量的5.5~9.5 倍。脱臭油中GEs生成量为14.88~19.84 mg/kg,是待脱臭油含量的5.8~7.7 倍。但待脱臭油脂中氯离子含量的逐渐增加并未造成脱臭油中氯离子含量的升高,脱臭油中氯离子含量在0.35 mg/kg左右。研究结果显示,油脂脱臭用直接蒸汽中氯离子含量和待脱臭油脂中氯离子含量均会对脱臭油脂中3-MCPD酯和GEs的生成造成影响,因此根据研究结果显示,在实际生产中应将脱臭所用水源中的氯离子控制在5 mg/L以下,并同时尽可能脱除待脱臭油脂中的氯离子,且严格控制脱臭前精炼各步骤中氯离子的引入,使待脱臭油中氯离子控制在不被检出的范围内,从而降低脱臭油中3-MCPD酯和GEs生成量,确保和提升食用植物油的品质安全。
参考文献:
[1] 刘京, 王瑛瑶, 段章群, 等. 食用植物油中氯丙醇酯的形成途径与检测方法[J]. 食品科学, 2013, 34(21): 375-378. DOI:10.7506/spkx1002-6630-201321074.
[2] HAMLET C G, SADD P A, CREWS C, et al. Occurrence of 3-chloropropane-1,2-diol (3-MCPD) and related compounds in food:a review[J]. Food Additives & Contaminants, 2002, 19(7): 619-631.DOI:10.1080/02652030210132391.
[3] ZELINKOVÁ Z, SVEJKOVSKÁ B, VELÍŠEK J, et al.Fatty esters of 3-chloropropane-1,2-diol in edible oils[J].Food Additives & Contaminants, 2006, 23(12): 1290-1298.DOI:10.1080/02652030600887628.
[4] 金青哲, 王兴国. 氯丙醇酯-油脂食品中新的潜在危害因子[J].中国粮油学报, 2011, 26(11): 119-123. DOI:11-2864/TS.20110928.1450.002.
[5] 李健爽, 王森, 杜晓燕. 食品中3-氯-1,2-丙二醇脂肪酸酯研究进展[J].食品工业科技, 2013, 34(6): 385-388.
[6] SVEJKOVSK Á, DOLE M. Formation and decomposition of 3 chloropropane 1,2-diol esters in models simulating processed foods[J].Czech Journal of Foodences, 2006, 24(4): 172-179.
[7] LARSEN J C. 3-MCPD esters in food products[M]. Brussels: ILSI Europe a.i.s.b.l, 2009: 9-12.
[8] ORGANIZATION W H. Safety evaluation of certain food additives and contaminants: seventy-third meeting of the Joint FAO/WHO Expert Committee on Food Additives (JECFA)[M]. World Health Organization, 2011: 1-128.
[9] CRAIG A W. IARC monographs on the evaluation of the carcinogenic risk of chemicals to humans: International Agency for Research on Cancer. Lyon, 1986[J]. American Industrial Hygiene Association Journal, 1982, 41(5): 214.
[10] GÖEN T, ECKERT E, SCHÄFERHENRICH A, et al. Allocation of reliable analytical procedures for human biomonitoring published by the DFG senate commission for the investigation of health hazards of chemical compounds in the work area[J]. International Journal of Hygiene & Environmental Health, 2012, 215(2): 233-237.DOI:10.1016/j.ijheh.2011.08.013.
[11] IKEDA N, FUJII K, SARADA M, et al. Genotoxicity studies of glycidol fatty acid ester (glycidol linoleate) and glycidol[J]. Food &Chemical Toxicology an International Journal Published for the British Industrial Biological Research Association, 2012, 50(11): 3927-3933.DOI:10.1016/j.fct.2012.08.022.
[12] BAER I, CALLE B D L, TAYLOR P. 3-MCPD in food other than soy sauce or hydrolysed vegetable protein (HVP)[J]. Analytical &Bioanalytical Chemistry, 2010, 396(1): 443-456. DOI:10.1007/s00216-009-3177-y.
[13] IIKO V, ZELINKOVÁ Z, DOLEZAL M, et al. 3-Chloropropane-1,2-diol fatty acid esters in potato products[J]. Czech Journal of Food Sciences, 2011, 27(6): S421-S424.
[14] 吴少明, 傅武胜, 杨贵芝. 食用植物油中脂肪酸氯丙醇酯形成机制的研究进展[J]. 食品科学, 2014, 35(1): 266-270. DOI:10.7506/spkx1002-6630-201401053.
[15] FRANKE K, STRIJOWSKI U, FLECK G, et al. Influence of chemical refining process and oil type on bound 3-chloro-1,2-propanediol contents in palm oil and rapeseed oil[J]. LWT-Food Science and Technology, 2009, 42(10): 1751-1754. DOI:10.1016/j.lwt.2009.05.021.
[16] WEIßHAAR R. 3-MCPD-esters in edible fats and oils-a new and worldwide problem[J]. European Journal of Lipid Science &Technology, 2010, 110(8): 671-672. DOI:10.1002/ejlt.200800154.
[17] RAHN A K K, YAYLAYAN V A. What do we know about the molecular mechanism of 3-MCPD ester formation[J]. European Journal of Lipid Science and Technology, 2011, 113(3): 323-329.DOI:10.1016/j.fct.2012.08.022.
[18] 崔海萍, 吴炜亮, 王力清, 等. 食用油脂中GEs的生成机制及其检测方法研究进展[J]. 广东化工, 2014, 41(14): 129-130. DOI:10.3969/j.issn.1007-1865.2014.14.064.
[19] NAGY K, SANDOZ L, CRAFT B D, et al. Mass-defect filtering of isotope signatures to reveal the source of chlorinated palm oil contaminants[J]. Food Additives & Contaminants Part A Chemistry Analysis Control Exposure & Risk Assessment, 2011, 28(11): 1492-1500. DOI:10.1080/19440049.2011.618467.
[20] DESTAILLATS F, CRAFT B D, SANDOZ L, et al. Formation mechanisms of monochloropropanediol (MCPD) fatty acid diesters in refined palm (Elaeis guineensis) oil and related fractions[J]. Food Additives & Contaminants Part A Chemistry Analysis Control Exposure & Risk Assessment, 2012, 29(1): 29-37. DOI:10.1080/1944 0049.2011.633493.
[21] CRAFT B D, NAGY K, SANDOZ L, et al. Factors impacting the formation of monochloropropanediol (MCPD) fatty acid diesters during palm (Elaeis guineensis) oil production[J]. Food Additives &Contaminants Part A Chemistry Analysis Control Exposure & Risk Assessment, 2012, 29(3): 354-361. DOI:10.1080/19440049.2011.639034.
[22] 周红茹, 金俊, 杨娇, 等. 油脂中3-氯丙二醇酯形成的化学反应机制[J]. 中国粮油学报, 2012, 27(10): 118-122. DOI:10.3969/j.issn.1003-0174.2012.10.024.
[23] 晋榕. 地沟油的检测与鉴别研究[D]. 长春: 吉林大学, 2015.
[24] 苗雨田, 杨悠悠, 王浩, 等. 气相色谱-质谱法测定食用油中3-氯丙醇酯[J]. 中国粮油学报, 2016, 31(11): 135-139. DOI:10.3969/j.issn.1003-0174.2016.11.023.
[25] 杨贵芝. 食用油中氯丙醇酯和婴幼儿奶粉中结构化脂肪的检测方法研究[D]. 福州: 福建中医药大学, 2015.
[26] HAMLET C G, SADD P A, GRAY D A. Generation of monochloropropanediols (MCPDs) in model dough systems. 1.Leavened doughs[J]. Journal of Agricultural and Foodchemistry, 2004,52(7): 2067-2072. DOI:10.1021/jf035077w.
[27] FREUDENSTEIN A, WEKING J, MATTHÄUS B. Influence of precursors on the formation of 3-MCPD and glycidyl esters in a model oil under simulated deodorization conditions[J]. European Journal of Lipid Science & Technology, 2013, 115(3): 286-294. DOI:10.1002/ejlt.201200226.
[28] 杨娇, 金青哲. 食用植物油中3-氯丙醇酯的研究进展[J]. 中国油脂,2011, 36(9): 1-4.
[29] SHIMIZU M, VOSMANN K, MATTHÄUS B. Generation of 3-monochloro-1,2-propanediol and related materials from tri-, di-, and monoolein at deodorization temperature[J]. European Journal of Lipid Science & Technology, 2012, 114(11): 1268-1273. DOI:10.1002/ejlt.201200078.
[30] HAMLET C G, ASUNCION L. Single-laboratory validation of a method to quantify bound 2-chloropropane-1,3-diol and 3-chloropropane-1,2-diol in foodstuffs using acid catalysed transesterification, HFBI derivatisation and GC/MS detection[J].European Journal of Lipid Science & Technology, 2015, 113(3): 345-355. DOI:10.1002/ejlt.201000492.
Effect of Chloride Ion Content on 3-Monochloro-1,2-Propanediol Ester and Glycidyl Esters during Soybean Oil Deodorization
WANG Luyang1, LIU Yulan1,*, MA Yuxiang1, HUANG Huina1, WANG Fengyan2, WANG Manyi2
(1. College of Food Science and Technology, Henan University of Technology, Zhengzhou 450001, China;2. COFCO Nutrition & Health Research Institute, Beijing 102200, China)
Abstract:The purpose of the present study was to investigate the effect of chloride ion content on the contents 3-monochloro-1,2-propanediol esters (3-MCPD esters) and glycidyl esters (GES) during the deodorization of soybean oil.The chloride ion contents of the water source of steam used directly for the deodorization of soybean oil was analyzed. The deodorization was carried out by distillation with steams of different chloride ion contents and we determined the contents of chloride ion, 3-MCPD esters and GES in soybean oil before and after deodorization. The results showed that the chloride ion content in the steam increased with the increase of chloride ion content in the water, and the retention rate of chloride ion in the water was about 0.1%. When the content of chloride ion in the steam was increased from 1–10 to 50–200 mg/L,the content of 3-MCPD esters in deodorized oil was increased by 2.6 times, while the content of chloride ion in deodorized oil did not rise. Increasing chloride ion content in undeodorized oil resulted in increased contents of 3-MCPD ester and GEs after deodorization. The contents of 3-MCPD ester and GEs in deodorized oil were 4.49–7.84 and 14.88–19.84 mg/kg,respectively, when 0.5–5 mL of sodium chloride solution at a concentration of 100 mg/L (the fi nal concentration in the oil was 1–10 mg/kg) was added before deodorization, which were 5.5–9.5 and 5.8–7.7 times higher than in undeodorized oil. Therefore, controlling or reducing the chloride ion content during the deodorization process plays an important role in reducing the contents of 3-MCPD ester and GEs in deodorized oil.
Keywords:oil; deodorization; chloride ion; 3-chloro-1,2-propanediol esters; glycidyl ester
WANG Luyang, LIU Yulan, MA Yuxiang, et al. Effect of chloride ion content on 3-monochloro-1,2-propanediol ester and glycidyl esters during soybean oil deodorization[J]. Food Science, 2018, 39(20): 320-325. (in Chinese with English abstract)DOI:10.7506/spkx1002-6630-201820046. http://www.spkx.net.cn
引文格式:王璐阳, 刘玉兰, 马宇翔, 等. 油脂脱臭过程氯离子含量对3-氯丙醇酯和缩水甘油酯的影响[J]. 食品科学, 2018, 39(20):320-325. DOI:10.7506/spkx1002-6630-201820046. http://www.spkx.net.cn
文章编号:1002-6630(2018)20-0320-06
文献标志码:A
中图分类号:TS224.6
DOI:10.7506/spkx1002-6630-201820046
*通信作者简介:刘玉兰(1957—),女,教授,硕士,研究方向为油料油脂加工技术与产品质量安全。E-mail:liuyl7446@163.com
第一作者简介:王璐阳(1992—),女,硕士研究生,研究方向为油料油脂加工技术与产品质量安全。E-mail:934180482@qq.com
基金项目:“十三五”国家重点研发计划重点专项(2016YFD0401405)
收稿日期:2017-08-15