腌腊鱼是我国重要的传统腌干水产品,其风味独特,广受青睐。传统腌腊鱼一般采用日晒法制得,往往存在卫生条件差、生产不连续等弊端,目前已逐步被热风干燥和冷风干燥等现代化干制技术所替代[1]。然而,采用现代技术加工制得的腌腊鱼产品其香气品质不如传统日晒产品[1],其原因鲜见报道。
香气是腌腊鱼的重要感官评价指标之一,香气组分(挥发性风味物质)主要由脂类的氧化分解、蛋白质与糖类等的降解以及美拉德反应等产生[2]。腌腊鱼制作时多以草鱼、鲢鱼等为原料,鱼肉中不饱和脂肪酸(unsaturated fatty acid,UFA)含量丰富,在干制成熟过程中较易氧化、分解,从而形成制品的最终风味[3]。脂肪酸的氧化类型主要包括自动氧化、酶促氧化和光(敏)氧化[2]。自动氧化可在空气中自动进行,反应速率较慢[3];蔡秋杏等[4]指出酶促氧化不是引起腌腊鱼脂质氧化的主要原因。Tejero等[5]发现油酸的光氧化速率是其自动氧化的3 000 倍,多烯脂类光氧化的速度比其自动氧化快1 000~1 500 倍。腌腊鱼一般选择冬季晴日制作,气温较低且光照充足,十分利于脂肪光氧化反应的发生。除光照因素外,风干温度也会显著影响腌腊鱼香气品质:提高风干温度,一方面可提高脂肪酶活力,促进脂肪水解生成游离脂肪酸;另一方面能激活脂肪氧合酶,氧化游离脂肪酸进一步生成醇、醛、酮等香气物质[3]。目前,国内外已有研究者对多种腌腊鱼[6-10]的挥发性风味成分进行了鉴定,张进杰[1]比较了不同干制工艺对腌腊鱼脂肪氧化指标的影响;但鲜有研究者对两者的相关性展开深入探究,解析脂肪氧化对腌腊鱼香气形成的影响机制。
本研究以草鱼(Ctenpharyngodon idellus)为原材料,采用4 种干制工艺(调控光照、温度)制得腌腊鱼成品,探讨不同干制工艺对腌腊鱼脂肪氧化和挥发性风味成分的影响,初步解析腌腊鱼优良香气的形成机制,旨在为腌腊鱼相关生产企业提供理论参考。
鲜活草鱼(共10 尾,2 年龄,体长(60.5±5.2)cm,体宽(7.9±1.0)cm,体质量(2.1±0.5)kg),于2016年10月下旬购于杭州市下城区朝晖农贸市场,置于装水充氧的塑料袋中30 min内运回实验室。
食盐 中盐上海市盐业公司;2,4,6-三甲基吡啶(2,4,6-trimethylpyridine,TMP)、正己烷(均为色谱纯) 美国Sigma公司;琼脂培养基、石油醚、甲苯、异丙醇、氢氧化钾、氯仿、冰乙酸、盐酸、三氯乙酸、碘化钾(均为分析纯) 国药集团化学试剂有限公司;质量分数14%三氟化硼-甲醇溶液、C19脂肪酸甲酯标准品、37 种脂肪酸甲酯混标、氨丙基硅柱小柱 德国CNW Technologies公司。
HR 2860高速碎肉机 荷兰皇家飞利浦电子公司;BS223S电子精密天平 华东医药有限公司;CR21 GII高速冷冻离心机 日本日立公司;HYJD超纯水器 杭州永洁达净化科技有限公司;RE-2000A旋转蒸发仪上海亚荣生化仪器厂;K9840半自动凯氏定氮仪 济南海能仪器股份有限公司;MonoTrap RCC18固相萃取整体捕集剂(MTRCC18,规格5 mm×2.9 mm,1 mm) 日本GL Sciences公司;7890A-5975C气相色谱-质谱联用(gas chromatography-mass spectrometry,GC-MS)仪美国Aglient公司;Fox4000电子鼻 法国Alpha公司;MRX-150E人工气候调节箱 江苏中和实验仪器制造有限公司。
1.3.1 样品制备
预处理:鲜活草鱼以击头方式即杀死,剖开鱼腹,去除头、尾、内脏和黑膜,沿脊椎骨剖开制得鱼片,用清水洗净鱼片表面血污,室温下沥干。
腌制:根据前期预实验结果,添加质量分数9%的食盐进行腌制效果较佳。具体方法如下:称取鱼肉质量9%的食盐均匀涂抹鱼片。加盐后鱼片整齐堆码于不锈钢盆中,置于4 ℃冷藏柜中进行腌制,每隔12 h上下翻动一次,共腌制5 d。
干制:腌制结束后擦干鱼片表面盐和水分,在无菌操作台中将其切成6.0 cm×2.0 cm×1.5 cm的鱼块,将所有鱼块充分混合均匀后平铺于相对湿度为50%的人工气候调节箱中进干制加工。本研究共设置4 组干制工艺,依次为:热风光照组(温度50 ℃,光照强度15 000 lx,风速l m/s,连续干制20 h);热风避光组(温度50 ℃,无光照,风速l m/s,连续干制20 h);冷风光照组(温度10 ℃,光照强度15 000 lx,风速l m/s,连续干制60 h);冷风避光组(温度10 ℃、无光照、风速l m/s、连续干制60 h)。
1.3.2 指标测定
1.3.2.1 水分质量分数的测定
水分质量分数按照GB 5009.3—2016《食品安全国家标准 食品中水分的测定》[11]中的方法测定。
1.3.2.2 菌落总数的测定
菌落总数按照GB 4789.2—2016《食品安全国家标准食品微生物学检验 菌落总数测定》[12]中的方法测定。
1.3.2.3 总脂含量、脂肪酸组成的测定
总脂含量的测定:参考Folch等[13]的方法,称取5.0 g切碎的鱼肉于离心管中,加入40 mL氯仿-甲醇(2∶1,V/V)溶液15 mL,匀浆60 s,转移入具塞量筒中定容至100 mL,静置1 h。过滤除去蛋白、结缔组织,再加入0.2 倍体积的生理盐水,3 000 r/min离心15 min。吸净上层水与甲醇等液体杂质,下层脂质溶液转移至干燥称质量的旋蒸瓶中,在40 ℃下水浴真空旋蒸,得到浓缩脂质,称质量,并用公式(1)计算总脂含量。
式中:m1、m2分别为旋蒸瓶的初始质量与其旋蒸后的质量/g;m0为加入鱼肉样品质量(5 g)。
脂肪酸的甲酯化:参考Regueiro等[14]的方法并稍作修改,将分离后的脂质加入5 mL NaOH-甲醇溶液,于沸水中振荡5 min,再加入质量分数14%三氟化硼-甲醇溶液2 mL,沸水浴5 min。分别加入1 mL正己烷和蒸馏水,振荡1 min,静置分层后吸取上层液体过膜,加入25 μL C19脂肪酸甲酯标准溶液作为内标,以备色谱测定。
GC分析[3]:色谱柱:Superlco 2560(100 m×0.25 mm,0.25 μm);升温程序:初始温度90 ℃,保持2 min,以10 ℃/min升温至180 ℃,再以5 ℃/min升温至240 ℃,保持12 min;载气为高纯氮气,流量为1.0 mL/min,进样量1 μL,分流比1∶70,进样口温度230 ℃;火焰离子检测器温度240 ℃。根据37 种脂肪酸甲酯混标来确定各脂肪酸的保留时间,以C19脂肪酸甲酯为内标物质进行定量分析。
1.3.2.4 AV的测定
酸价(acid value,AV)的测定按照GB 5009.229—2016《食品安全国家标准 食品中酸价的测定》[15]的方法。AV以每克鱼肉所能中和的KOH质量表示。
1.3.2.5 POV的测定
过氧化值(peroxide value,POV)的测定按照GB 5009.227—2016《食品安全国家标准 食品中过氧化值的测定》[16]中的方法。
1.3.2.6 TBA含量的测定
硫代巴比妥酸(thiobarbituric acid,TBA)含量的测定参照Ulu[17]的方法并稍作修改。准确称取5.0 g试样,加入50 mL体积分数7.5%三氯乙酸溶液(内含质量分数0.1%乙二胺四乙酸),搅拌均匀并过滤。取5 mL滤液(空白对照用5 mL去离子水代替),向其中加入5 mL 0.02 mol/L TBA溶液,沸水浴中保温40 min。待冷却至室温后,于5 500 r/min条件下离心25 min。弃去沉淀,在上清液中加入5 mL氯仿,振荡摇匀,待静置分层后,取上层溶液分别在波长532 nm和600 nm处进行比色,记录吸光度,并用公式(2)计算TBA含量。
式中:A532nm、A600nm分别为532 nm、600 nm波长处的吸光度;155为丙二醛的摩尔吸光系数(在1 L溶液中含有1 mmol丙二醛时的吸光度);72.06为丙二醛的相对分子质量;5为样品质量(g)。
1.3.2.7 感官评定
参考张进杰[1]的方法,将腌制鱼块在纯水中浸泡15 min后蒸制15 min,待其冷却至40 ℃左右时进行感官评定。由10 名(4 名男性、6 名女性,平均年龄25 岁)有食品感官评定经验的人员组成评定小组,从咸味、香气、组织形态、口感和色泽5个方面对蒸熟后的鱼块进行评分,评价标准见表1。满分为100分,60分以下为不可接受。
表1 腌腊鱼的感官评定标准
Table1 Criteria for sensory evaluation of cured fish
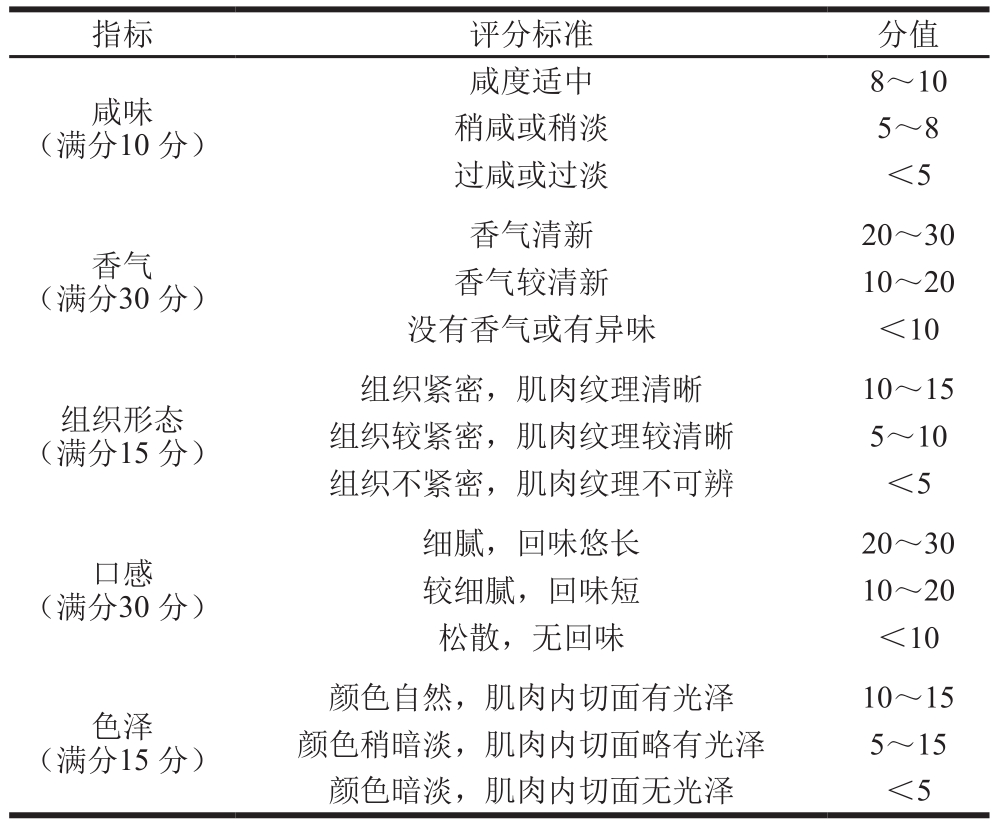
指标 评分标准 分值咸味(满分10 分)咸度适中 8~10稍咸或稍淡 5~8过咸或过淡 <5香气(满分30 分)香气清新 20~30香气较清新 10~20没有香气或有异味 <10组织形态(满分15 分)组织紧密,肌肉纹理清晰 10~15组织较紧密,肌肉纹理较清晰 5~10组织不紧密,肌肉纹理不可辨 <5口感(满分30 分)细腻,回味悠长 20~30较细腻,回味短 10~20松散,无回味 <10色泽(满分15 分)颜色自然,肌肉内切面有光泽 10~15颜色稍暗淡,肌肉内切面略有光泽 5~15颜色暗淡,肌肉内切面无光泽 <5
1.3.3 挥发性化合物的整体材料吸附萃取-GC-MS测定
1.3.3.1 萃取条件
参照顾赛麒等[18]的方法。用经消毒处理(刀口火焰灼烧10 s后再紫外辐照30 min)的绞肉机将腌制所得鱼块充分绞碎,精确称取(3.00±0.01)g绞碎后的鱼肉样品,装入20 mL棕色顶空瓶中。选取4 个MTRCC18(空心圆柱体),以固定装置串联后置于顶空瓶内鱼肉样品正上方。将内装样品的棕色顶空瓶置于恒温水浴锅中,于60 ℃下萃取1 h。待萃取完毕后,取下所有吸附子迅速装入热脱附管,再由前处理平台将热脱附管转移至热脱附器中进行热解吸进样。
1.3.3.2 仪器参数
热脱附器条件:不分流模式,初始温度40 ℃,以180 ℃/min升至240 ℃,保留5 min。冷进样系统条件:液氮制冷,起始温度-40 ℃,平衡30 s,以12 ℃/s升至270 ℃,保留15 min。
GC条件:DB-5MS毛细管柱(60 m×0.32 mm,1 μm),汽化室温度240 ℃,不分流模式进样。起始柱温40 ℃,以5 ℃/min升至100 ℃,再以2 ℃/min升至180 ℃,最后以5 ℃/min升至240 ℃,保留5 min。以99.999%高纯氦气为载气,流量1.0 mL/min。
MS条件:电子电离源为能量源,电子能量70 eV,全扫描模式,无溶剂延迟,扫描范围m/z 35~500,扫描速率3.0 scans/s,灯丝发射电流为200 μA,离子源温度220 ℃,四极杆温度为150 ℃,检测器温度250 ℃,传输线温度270 ℃,检测器电压1.2 kV。
1.3.3.3 定性方法
将检测得到的挥发物质谱图与NIST 2011和Wiley 9谱库中标准物质的质谱图进行比对,仅报道正反匹配度均大于800(最大值为1 000)的鉴定结果。
1.3.3.4 定量方法
将10 μL质量浓度为10-5g/mL的内标物TMP工作液加入到3 g充分绞碎的鱼肉样品中,通过计算待测挥发物与TMP峰面积的比值来求得各挥发性化合物的含量(绝对校正因子假定为1),其计算公式如式(3)所示。
式中:Ax、ATMP分别表示待测挥发物与内标物TMP的峰面积;CTMP为加入TMP的质量浓度(10-5g/mL);VTMP表示加入TMP的体积(10 μL);m0为加入鱼肉样品质量(3 g)。
1.3.3.5 OAV分析
气味活性值(odor activity value,OAV)反映了各挥发物对样品整体气味轮廓的贡献程度,计算公式如式(4)所示。
式中:Ci和OTi分别为挥发物i的含量/(ng/g)和气味阈值/(ng/g);OAV大于1的化合物具有气味活性,可定义为气味活性物质[15]。
采用SPSS 22.0和Origin 8.0软件进行数据分析与作图,差异显著性分析由单因素方差分析(One-way ANOVA)法完成,P<0.05表示差异显著。

图1 不同干制腌腊鱼的水分质量分数与菌落总数
Fig.1 Moisture content and aerobic plate count of cured fish produced by different drying methods
由图1可知,本研究中不同干制方法得到的腌腊鱼水分质量分数均降至40%左右,与张进杰[1]的结果相符。较低的水分质量分数可有效抑制鱼肉中内源酶活力与微生物生长繁殖速度,从而实现保藏作用[2]。热风光照组的菌落总数最低,为2.91(lg(CFU/g));而冷风避光组最高,为4.42(lg(CFU/g))。在相同光照(或避光)条件下,冷风组的菌落总数显著高于热风组,可能原因是冷风干燥温度较低(10 ℃)、干燥时间较长(60 h),虽未达到最适条件,但细菌仍旧处于缓慢增殖状态;对于热风干燥而言,长时间的高温处理(50 ℃、20 h),细菌的生长繁殖将受到严重抑制,甚至造成其部分失活。相同温度下,光照组的菌落总数略低于避光组,推测原因是在鱼肉肌红蛋白等光敏剂作用下,空气中原本处于基态的三线态氧(3O2)会转变生成激发态的单线态氧(1O2),后者氧化性极强,可能造成细菌的细胞膜发生氧化破坏,具体机制值得深入研究。张晓艳等[19]对5 个批次淡腌黄鱼中的菌落总数进行了测定,结果为4.56~6.19(lg(CFU/g)),略高于本研究,这可能与鱼种不同以及制作工艺差异有关。
如图2A所示,干制结束后,热风光照组样品中的总脂含量最低,为6.23 g/100 g;而冷风避光组的总脂含量最高,达7.87 g/100 g。热风光照组比冷风避光组样品总脂含量降低了20.84%,一方面可能源自脂肪热降解与光氧化的综合作用;另一方面,氧化过程中产生的自由基等中间产物可进一步加剧腌腊鱼脂肪氧化的程度。相同光照(或避光)条件下,热风组样品的总脂含量显著低于冷风组,表明其发生了更强烈的氧化分解反应。Zhang Jianhao等[20]的研究发现,提高风干(成熟)温度能够加快脂质氧化分解速率,有助于成品风味的形成,与本研究结果相符。相同温度下,光照组样品的总脂含量略低于避光组,但无显著性差异。
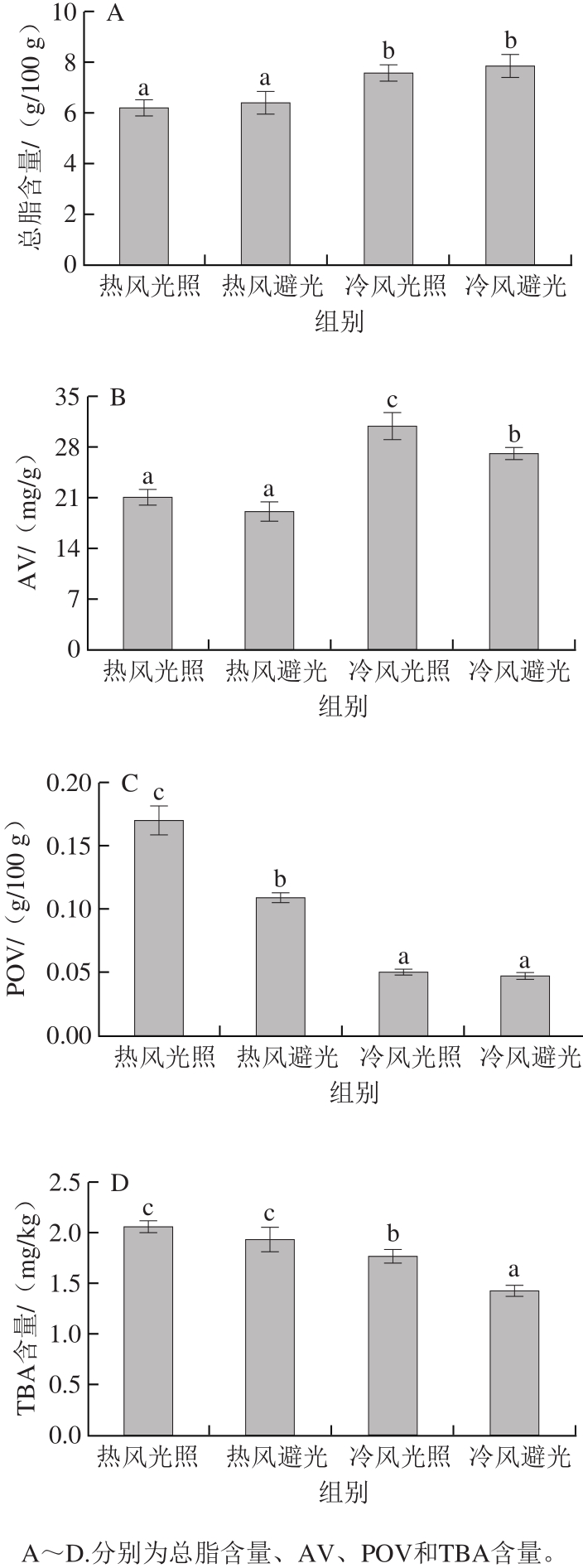
图2 不同干制腌腊鱼的总脂含量与脂质氧化指标
Fig.2 Total fat content and lipid oxidation indexes of cured fish produced by different drying methods
腌腊鱼脂质氧化过程可分为3 个阶段:首先,脂肪酸在脂肪酶的作用下从甘油三酯或磷脂上水解下来,成为游离脂肪酸,其含量可用AV表示;其次,游离态的UFA在脂肪氧化酶、单线态氧或烷基自由基等的作用下生成脂质氢过氧化物,其含量可用POV表示;再次,脂质氢过氧化物由于自身不稳定,会进一步分解成醛、酮、醇类等小分子挥发物。丙二醛是最具代表性的脂质氧化最终产物,其含量可用TBA含量表示。有研究者指出,脂肪的水解与氧化具有显著相关性,加强脂肪水解可以促进其氧化[21]。此外,脂质氢过氧化的生成与降解间隔时间极短,甚至可以同时发生[2]。
观察图2B~D可以发现:光照组样品的AV、POV、TBA含量均高于避光组,其中热风光照组POV较热风避光组具有显著性差异,而冷风光照组AV和TBA含量较冷风避光组具有显著性差异。综上分析可知,无论热风(50 ℃)还是冷风(10 ℃)条件下,光照均对腌腊鱼的脂肪氧化具有显著的促进作用,此结果与图2A中总脂含量变化规律互为印证。近年来,国内一些学者展开了相关方面的研究:高海等[22]探讨了光照对草鱼和三文鱼贮藏时脂肪氧化的影响,发现光照可以促进TBA含量的增加,加速脂质的氧化作用。霍晓娜等[23]研究了光照和避光条件对猪通脊肉肌内和皮下脂肪氧化程度的影响,发现光照可以明显加快脂肪氧化速率,并加深氧化程度。
除光照因素外,干制温度对腌腊鱼产品质量也有重要影响。由图2B~D可知,相同光照(或避光)条件下,热风组的POV和TBA含量均大于冷风组,而AV却呈相反规律。可能的原因如下:热风条件下,腌腊鱼脂肪的水解和氧化速率加快,水解生成的游离脂肪酸在短时间内被氧化生成氢过氧化物,因此热风组样品AV显著下降而POV急剧增加;冷风条件下,虽然脂肪酸持续不断地从各类脂质(甘油三酯和磷脂)上水解下来,但由于低温(10 ℃)下脂肪氧化酶活力受到抑制,导致生成的游离脂肪酸氧化降解速率减慢,因此与热风组相比,冷风组样品的POV较低。综上分析,较高的风干温度有利于腌腊鱼脂质的氧化降解。闫瑾[24]通过实验也证实,在一定温度范围内,提高风干温度,可以增加鱼肉中脂肪酶的活力,促进脂质的氧化分解。GB 10136—2015《食品安全国家标准 动物性水产制品》中对腌腊鱼产品的脂质氧化指标规定如下:POV≤0.6 g/100 g(以脂肪计)。本研究中制得的4 种腌腊鱼产品,其POV均远低于上述标准限量值,安全性较高。
由表2可知,腌腊鱼制品UFA含量十分丰富,主要包括MUFA与PUFA,两者含量分别占总脂肪酸含量的35%和40%左右。SFA含量占总脂肪酸含量的20%左右,主要以软脂酸(C16:0)和硬脂酸(C18:0)为主,其中软脂酸含量最多(约占SFA含量的一半左右),这与Wu Tao等[25]分析的草鱼脂肪酸成分基本一致,且软脂酸含量受光照因素影响显著。
表2 不同干制腌腊鱼脂肪酸组成与各因素显著性分析
Table2 Fatty acid composition of cured fish produced by different drying methods and significance analysis of various factors

注:MUFA.单不饱和脂肪酸(monounsaturated fatty acid);PUFA.多不饱和脂肪酸(polyunsaturated fatty acid);SFA.饱和脂肪酸(saturated fatty acid);同行肩标小写字母不同表示不同干制方法腌腊鱼间存在显著差异(P<0.05);—.相关数值未检出;*.差异显著(P<0.05);**.差异极显著(P<0.01);***.差异高度显著(P<0.001);下同。
脂肪酸相对含量/% 光照因素对比 温度因素对比脂肪酸类别 脂肪酸 热风光照组(A)热风避光组(B)冷风光照组(C)冷风避光组(D)热风(A & B)冷风(C &D)光照(A & C)避光(B &D)整体样品(A & B &C & D)SFA C12:0—a0.96±0.06b—a—a*** *** ***C14:01.17±0.04b1.63±0.06d0.87±0.03a1.28±0.06c*** *** ** ** ***C15:00.22±0.01b0.20±0.01ab0.21±0.01ab0.19±0.01aC16:012.24±0.57c10.03±0.56a12.16±0.33bc10.64±0.68a* * **C17:00.24±0.01b0.22±0.01b0.27±0.01c0.19±0.01a** * * ***C18:06.34±0.35ab5.64±0.32a8.66±0.55c6.91±0.19b** ** ** ***C20:00.20±0.01a0.25±0.01b0.26±0.02b0.18±0.01a** ** * ** **C22:02.34±0.06b2.63±0.07c0.13±0.01a0.06±0.01a** ** *** *** ***MUFA C18:1(n-9)34.79±1.61ab35.68±2.00b32.21±1.46a32.97±1.23abC20:1(n-9)1.48±0.08b1.68±0.11c1.28±0.03a1.67±0.06c* ** * **C18:2(n-6)20.58±1.14ab19.95±0.93a22.18±1.41ab22.51±0.84b*PUFA C18:3(n-6)0.41±0.01bc0.42±0.02c0.28±0.02a0.54±0.03d*** ** ** ***C18:3(n-3)1.47±0.10a2.11±0.14c1.88±0.08b2.26±0.11c** ** * ***C20:3(n-3)1.16±0.07c0.22±0.01a3.14±0.20d0.68±0.02b*** *** *** *** ***C20:3(n-6)2.03±0.06c0.49±0.02b0.25±0.01a2.60±0.07d*** *** *** *** ***C20:4(n-6)10.27±0.67a11.56±0.32b10.33±0.28a11.44±0.75b* * *C20:5(n-3)0.30±0.01a0.33±0.02ab0.34±0.01b0.39±0.01c** * * **C22:6(n-3)4.77±0.13a5.99±0.17c5.55±0.23b6.29±0.26c** * ** ***合计∑SFA 22.75±1.07b21.56±0.61b22.57±0.83b19.46±1.09a* * *∑MUFA 36.27±2.71a37.36±1.17a33.49±1.47a34.65±2.62a∑PUFA 40.98±2.00a41.08±1.62ab43.94±1.28bc45.89±1.78c* * *∑PUFA(n-3) 7.70±0.28a8.66±0.32b10.90±0.42c8.79±0.41b* ** *** ***∑PUFA(n-6) 33.28±1.64a32.42±1.94a33.04±1.91a37.10±1.45b* **∑n-3/∑n-6 0.23±0.01a0.27±0.01b0.36±0.02c0.24±0.01a* ** ** * ***
UFA是腌腊鱼脂肪酸的重要构成组分,除油酸(C18:1(n-9))与亚油酸(C18:2(n-6))外,4 组腌腊鱼样品其UFA在含量上均存在显著性差异。UFA由MUFA和PUFA构成,其中PUFA占UFA含量的50%以上,而花生四烯酸(C20:4(n-6))占PUFA含量的25%左右,是含量次高的PUFA(仅次于亚油酸)。花生四烯酸在生物体中广泛存在,是构成细胞膜磷脂的常见脂肪酸之一。由表2可知,腌腊鱼样品中花生四烯酸含量受光照因素影响显著,且基本不受温度因素影响,可能原因如下:与甘油三酯相比,构成磷脂的脂肪酸更易在光照条件下发生水解,而花生四烯酸正是后者的主要构成组分。近年来,随着人民生活水平的提高,n-3系PUFA因具有预防心脑血管疾病、促进大脑和视神经发育、防癌抗衰老等生理功效而备受关注[26],其种类包括:亚麻酸(C20:3(n-3))、二十碳五烯酸(C20:5(n-3))和二十二碳六烯酸(docosahexaenoic acid,DHA,C22:6(n-3))等。分析表2可知,腌腊鱼样品所含n-3系PUFA中,DHA含量最高(可作为典型代表),且无论是高温还是光照条件,均能促进DHA的氧化降解,造成其含量下降。
综上可知,光照因素对花生四烯酸、DHA等PUFA含量影响显著。不饱和程度越高、电子密度越大,在光照条件下就越容易受到单线态氧的攻击而发生氧化降解[27]。此外,光照不仅能够促进脂质水解释放出游离脂肪酸,还可以激发肌肉中的血色素蛋白(如肌红蛋白和血红蛋白)等光敏剂,促进单线态氧的生成,加速脂肪酸的光氧化降解[28],生成小分子的醛、酮、醇类等香气物质,因此有必要对其展开后续研究。
表3 不同干制腌腊鱼感官评分与各因素显著性分析
Table3 Sensory scores of cured fish produced by different drying methods and significant analysis of various factors

避光(B & D)咸味 8.6±0.4a8.4±0.2a8.4±0.4a8.3±0.2a香气 28.2±0.6c25.6±0.7b24.8±0.6b22.4±0.8a* * ** * ***组织形态 7.9±0.7a8.1±0.9a11.7±0.9b11.5±0.8b** * **口感 22.6±1.0ab20.5±0.9a26.1±0.9c24.8±0.9bc* * **色泽 9.8±0.5a9.2±0.6a10.8±0.9a10.7±0.7a总分 77.1±2.3b71.8±1.6a81.8±1.3c77.7±1.7b* ** ** ** **评分指标 热风光照组(A)热风避光组(B)感官评价得分 光照因素对比 温度因素对比 整体样品(A & B & C& D)冷风光照组(C)冷风避光组(D)热风(A & B)冷风(C & D)光照(A & C)
如表3所示,4 种腌腊鱼产品由于初始加盐量、最终水分质量分数基本一致,因此咸味评分无显著性差异。香气是腌腊鱼的重要感官评价指标,热风组和光照组样品的香气评分显著高于冷风组和避光组,表明高温和光照可以促进腌腊鱼香气的形成,这主要是因为高温可以加速脂质的热氧化分解,而光照则可引发脂质光氧化反应,使不饱和脂肪酸氧化成醛、酮等小分子挥发性物质,形成腌腊鱼的特有香气,这与Flores等[29]的研究结果一致。组织形态得分中热风组样品显著低于冷风组,推测原因与热风干制温度高,造成鱼肉失水过快、表面硬化有关。从口感角度分析,相同光照(或避光)条件下,热风组样品显著低于冷风组,可能是因为后者干制时间较长(60 h),产生了更多的游离氨基酸,故口感更佳;相同温度下,光照组和避光组样品无显著差异。另外,高温会加速蛋白质和脂质的氧化(图2)以及色素类物质的降解,因此热风组样品色泽评分略低于冷风组。从总体得分来看,冷风组和光照组相对较高,排序为:冷风光照组>冷风避光组>热风光照组>热风避光组。
采用整体材料吸附萃取-GC-MS法从不同干制工艺制得的腌腊鱼中共检出了8大类82 种挥发性风味成分(表4),其中热风光照、热风避光、冷风光照和冷风避光组样品中共分别检出了64、63、60、56 种化合物,所有挥发物中OAV大于1的气味活性物质分别有11、11、10、7 种,主要以醛类、醇类和杂环类为主。4 组样品共有的气味活性物质是己醛、庚醛、辛醛、壬醛、癸醛、正己醇和1-辛烯-3醇7 种,表明其可能是腌腊鱼典型的重要活性风味物质。进一步分析可知:相同温度下,光照组的挥发物总含量与OAV总和显著高于避光组,其中热风光照组数值最高,分别达542.07 ng/g和214.88,表明光照更有利于香气物质生成。
表4 不同干制腌腊鱼挥发性风味成分鉴别与各因素显著性分析
Table4 Volatile flavor components of cured fish produced by different drying methods and significant analysis of various factors

化合物种类 时间/min 化合物名称 阈值[30-31]/(ng/g)保留挥发物含量/(ng/g) OAV 光照因素对比 温度因素对比 整体样品(A & B & C& D)热风光照组(A)热风避光组(B)冷风光照组(C)冷风避光组(D)热风光照组(A)热风避光组(B)冷风光照组(C)冷风避光组(D)热风(A & B)冷风(C & D)光照(A & C)避光(B & D)醛类10.95 3-甲基丁醛▲1.1 1.60±0.08b—a—a—a1.45 — — — *** *** ***12.20 戊醛 9 1.28±0.08a1.19±0.07a1.60±0.06b1.16±0.01a0.14 0.13 0.18 0.13 ** ** **13.30 2-甲基-2-戊烯醛 290 —a—a—a1.11±0.07b— — — <0.01 *** *** ***15.84 己醛▲5 45.52±2.28c43.82±3.07bc30.15±2.41a40.47±3.64b9.10 8.76 6.03 8.09 *** *** ***19.89 庚醛▲2.8 55.58±4.45d19.88±0.99c7.83±0.23a6.12±0.55b19.85 7.10 2.80 2.19 *** ** *** *** ***22.43 2-庚烯醛 13.5 —a—a2.28±0.07c1.88±0.02b— — 0.17 0.14 ** *** *** ***23.14 苯甲醛 41.7 14.93±0.15c11.80±0.24b11.23±1.01b8.59±0.69a0.36 0.28 0.27 0.21 ** * ** ** ***24.59 辛醛▲0.587 2.34±0.16a4.45±0.04c2.62±0.16a3.18±0.22b3.98 7.58 4.46 5.42 *** ** ** ***27.41 2-辛烯醛 3 1.15±0.10a1.10±0.66a1.17±0.06a1.81±0.07b0.38 0.37 0.39 0.60 ** * ***28.54 4-甲基苯甲醛▲1.2 —a1.48±0.39b1.79±0.26b—a— 1.23 1.49 — *** *** *** *** ***29.77 壬醛▲1.1 10.27±0.51a17.48±1.05b20.36±0.81c11.52±0.81a9.34 15.89 18.51 10.47 *** ** *** *** ***32.75 2-壬烯醛▲0.08 7.52±0.45c—a1.76±0.04b—a94.05 — 22.06 — *** *** *** ***33.49 4-乙基苯甲醛 123.23 —a—a1.70±0.12b1.83±0.11b— — 0.01 0.01 *** *** ***35.13 癸醛▲0.1 3.71±0.18b2.07±0.12a4.90±0.15c2.06±0.12a37.07 20.68 49.00 20.61 *** *** ** ***43.97 2-丁基-2-辛烯醛 N.A. 1.02±0.03b—a—a2.85±0.14cN.A. — — N.A. *** *** *** *** ***合计 144.92±8.70c103.27±9.29b87.39±3.49a82.58±4.13a175.72 62.02 105.37 47.87 ** *** *** ***醇类酮类11.65 1-戊烯-3-醇 358.1 7.96±0.24a8.32±0.75a9.70±0.19b7.67±0.15a0.02 0.02 0.03 0.02 ** * **14.45 正戊醇 150.2 7.44±0.59b8.03±0.48b5.38±0.48a11.24±0.22c0.05 0.05 0.04 0.07 *** ** ** ***15.49 3-辛烯-1-醇 N.A. 1.48±0.10a1.88±0.05b3.08±0.22c1.50±0.06aN.A. N.A. N.A. N.A. ** *** *** ** ***18.35 正己醇▲5.6 26.68±0.53b31.35±1.25c15.07±1.33a45.25±2.71d4.76 5.60 2.69 8.08 * *** ** ** ***22.79 正庚醇 5.4 —a4.51±0.22c4.01±0.20b4.99±0.15d— 0.83 0.74 0.92 *** *** *** ** ***23.41 1-辛烯-3-醇▲1.5 44.25±2.21a63.49±3.81b39.71±1.59a63.09±1.26b29.50 42.32 26.47 42.06 ** *** ***25.70 2-乙基-1-己醇 300 4.95±0.44b3.98±0.04a4.18±0.12a5.04±0.35b0.02 0.01 0.01 0.02 * ** * * **26.55 4-乙基环己醇 N.A. —a2.75±0.14c2.48±0.12b2.73±0.19c— N.A. N.A. N.A. *** * *** ***27.68 2-辛烯-1-醇 20 3.06±0.06a5.37±0.05b2.77±0.14a5.51±0.11b0.15 0.27 0.14 0.28 ** *** ***合计 95.82±1.92b129.68±1.30c86.38±2.59a147.02±10.29d34.50 49.12 30.12 51.45 *** *** ** ** ***9.19 2-丁酮 35 400 2.17±0.06d1.29±0.02b1.85±011c—a<0.01 <0.01 <0.01 — *** *** * *** ***12.11 3-戊酮 40 1.07±0.10c0.79±0.04b1.07±0.02c—a0.03 0.02 0.03 — * *** *** ***15.33 2-己酮 560 1.67±0.02b—a—a—a<0.01 — — — *** *** ***19.30 2-庚酮 141 5.11±0.46c3.91±0.35b2.20±0.20a3.51±0.21b0.04 0.03 0.02 0.02 ** *** *** ***23.62 6-甲基-5-庚烯-2-酮 68 2.62±0.18ab2.86±0.06b3.45±0.31c2.46±0.22a0.04 0.04 0.05 0.04 * ** * **23.68 3-辛酮 21.4 3.54±0.10d3.20±0.16c—a2.11±0.08b0.17 0.15 — 0.10 * *** *** ** ***23.86 2-辛酮 50.2 —a11.19±0.45d2.75±0.25b4.18±0.33c— 0.22 0.05 0.08 *** *** *** *** ***28.28 苯乙酮 65 3.22±0.13c1.90±0.13a2.25±0.09b2.22±0.20ab0.05 0.03 0.03 0.03 *** *** ***29.21 3,5-辛二烯-2-酮 150 2.70±0.05c1.74±0.07b0.35±0.02a2.76±0.22c0.02 0.01 <0.01 0.02 *** *** *** *** ***合计 22.10±1.98c26.88±2.15d13.92±0.42a17.24±1.37b0.35 0.50 0.18 0.29 * * *** *** ***杂环类12.32 2-乙基呋喃▲2.3 3.30±0.26c2.54±0.20b1.79±0.39d1.63±0.11a1.43 1.11 0.77 0.71 * *** *** ** ***13.88 吡啶 2 000 —a—a1.72±0.16b—a— — <0.01 — *** *** ***15.05 2-甲基噻吩 N.A. 1.43±0.08d0.98±0.05c—a0.82±0.03bN.A. N.A. — N.A. ** *** *** * ***16.52 3-甲基吡啶 N.A. 1.30±0.09b1.44±0.08b—a1.31±0.05bN.A. N.A. — N.A. *** *** ***18.74 2-乙基噻吩 N.A. 1.57±0.04d1.23±0.11c—a0.87±0.08bN.A. N.A. — N.A. ** *** *** *** ***20.16 2-乙基吡啶 57 —a0.80±0.04b0.80±0.02b—a— 0.01 0.01 — *** *** *** *** ***25.85 2,5-二乙基噻吩 N.A. —a1.97±0.04c0.80±0.02b—a— N.A. N.A. — *** *** *** *** ***20.75 3-乙基-1H-吡咯 N.A. —a—a1.84±0.14b—a— — N.A. — *** *** ***24.49 2-(2-戊烯基)呋喃 N.A. —a—a0.90±0.06b—a— — N.A. — *** *** ***27.93 2-丁基噻吩 N.A. 3.97±0.31c4.06±0.24c—a2.27±0.09bN.A. N.A. — N.A. *** *** ** ***33.26 2-戊基噻吩 5.8 0.85±0.02b—a—a—a0.15 — — — *** *** ***34.12 3-甲基-1H-吲哚▲0.13 —a0.70±0.02b0.94±0.05c—a— 5.38 7.23 — *** *** *** *** ***34.99 2-戊基吡啶▲0.6 —a1.17±0.08b—a—a— 1.95 — — *** *** ***合计 12.42±0.62b14.89±1.34c8.79±1.43d6.90±0.62a1.58 8.45 8.01 0.71 * *** *** *** ***
续表4

注:N.A..相关数值无法获得;▲.该化合物为腌腊鱼的气味活性物质(OAV>1)。
化合物种类 时间/min 化合物名称 阈值[30-31]/(ng/g)保留挥发物含量/(ng/g) OAV 光照因素对比 温度因素对比 整体样品(A & B & C& D)热风光照组(A)热风避光组(B)冷风光照组(C)冷风避光组(D)热风光照组(A)热风避光组(B)冷风光照组(C)冷风避光组(D)热风(A & B)冷风(C & D)光照(A & C)避光(B & D)芳香类11.28 苯 3 630 60.69±1.21b64.67±4.52b163.64±4.91c41.74±0.83a0.02 0.02 0.05 0.01 *** *** *** ***14.89 甲苯 1 550 8.71±0.26b7.42±0.30a8.42±0.42ab7.52±0.07a0.01 <0.01 0.01 <0.01 *18.57 乙苯 2 205.25 5.55±0.11c6.93±0.41b4.82±0.29a6.79±0.47b<0.01 <0.01 <0.01 <0.01 ** ** ** ***18.91 对二甲苯 1 000 8.28±0.66c7.04±0.42 1.16±0.05a1.49±0.10 0.01 0.01 <0.01 <0.01 * ** *** *** ***18.99 间二甲苯 1 000 4.08±0.16c1.44±0.09b1.64±0.11b0.89±0.08a<0.01 <0.01 <0.01 <0.01 *** *** *** ** ***19.97 邻二甲苯 450.23 3.66±0.07b3.51±0.07b1.56±0.08a1.27±0.08a0.01 0.01 <0.01 <0.01 *** *** ***22.70 丙苯 177.12 12.44±0.61c5.00±0.25a6.89±0.21b5.79±0.34a0.07 0.03 0.04 0.03 *** * *** ***24.68 1,3,5-三甲基苯 500 18.07±1.08d4.66±0.14c3.03±0.27a3.76±0.04b0.04 0.01 0.01 0.01 *** ** *** ** ***26.15 1,2,4-三甲基苯 500 7.88±0.55d2.29±0.16c1.17±0.07a1.57±0.14b0.02 <0.01 <0.01 <0.01 *** * *** ** ***26.28 2-丙烯基苯 N.A. 2.31±0.09b1.93±0.06a1.89±0.17a1.75±0.09aN.A. N.A. N.A. N.A. * * **27.02 二氢化茚 10 2.32±0.02b—a2.75±0.06c—a0.23 — 0.27 — *** *** * ***27.77 丁苯 100 6.80±0.47b8.58±0.77c4.76±0.43a9.55±0.10d0.07 0.09 0.05 0.10 ** *** *** ** ***31.20 1,2,3,4-四甲基苯 N.A. 2.01±0.16b—a—a—aN.A. — — — *** *** ***31.35 1-丁烯基苯 N.A. 2.99±0.16a4.32±0.09b5.43±0.05c5.03±0.45cN.A. N.A. N.A. N.A. *** *** * ***33.04 戊苯 6 000 1.55±0.08a3.13±0.06c1.76±0.11b4.67±0.28d<0.01 <0.01 <0.01 <0.01 *** *** * *** ***35.37 萘 60 19.22±1.54c2.00±0.16a3.86±0.31b3.29±0.20b0.32 0.03 0.06 0.05 *** *** * ***36.66 1-戊烯基苯 N.A. —a—a—a1.41±0.03b— — — N.A. *** *** ***38.51 己苯 4 200 —a—a—a1.53±0.09b— — — <0.01 *** *** ***41.27 2-甲基萘 4 1.59±0.14b—a—a—a0.40 — — — *** *** ***合计 168.15±8.41c122.92±1.23b212.78±19.15d98.05±3.92a1.18 0.20 0.49 0.22 *** *** * *** ***烃类7.75 1,3-戊二烯 2 500 1.86±0.13c1.93±0.12c1.19±0.02a1.58±0.11b<0.01 <0.01 <0.01 <0.01 ** * ** ***9.35 己烷 1 500 8.07±0.72b5.54±0.11a11.30±0.79c5.11±0.15a0.01 <0.01 0.01 <0.01 ** *** ** ***10.07 2,4-己二烯 3 000 —a—a0.74±0.06b—a— — <0.01 — *** *** ***12.77 1,4-环己二烯 N.A. 1.66±0.10a4.06±0.12c7.43±0.44d2.39±0.19bN.A. N.A. N.A. N.A. *** *** *** *** ***16.02 2-辛烯 2 000 2.73±0.25c2.24±0.18b2.47±0.02c—a<0.01 <0.01 <0.01 — * *** *** ***16.36 3-辛烯 N.A. 1.07±0.07b1.34±0.09c2.17±0.06d—aN.A. N.A. N.A. — * *** *** *** ***16.81 1,3-辛二烯 5 600 41.05±0.41c48.12±4.33b7.60±0.53a49.10±2.45b0.01 0.01 <0.01 0.01 * *** *** ***17.89 2,4-辛二烯 20 000 4.95±0.40c6.15±0.18b1.83±0.09a6.02±0.12b<0.01 <0.01 <0.01 <0.01 * *** *** ***19.11 1,3,5-辛三烯 N.A. 2.64±0.08c2.40±0.10b1.71±0.12a1.81±0.07aN.A. N.A. N.A. N.A. * *** * ***21.93 蒎烯▲2.2 2.70±0.05b—a—a—a1.23 — — — *** *** ***26.44 柠檬烯 10 2.15±0.15b—a—a—a0.22 — — — *** *** ***51.52 2,6,10-三甲基十四烷 N.A. 5.83±0.29c0.78±0.02b—a—aN.A. N.A. — — *** *** *** ***54.09 十七烷 N.A. 2.27±0.11c0.88±0.07b—a—aN.A. N.A. — — *** *** *** ***合计 85.29±5.97d77.64±6.99c37.94±1.14a68.49±2.74b1.46 0.01 0.01 0.01 * *** *** ** ***酯类9.60 乙酸乙酯 5 —a0.82±0.06b—a—a— 0.16 — — *** *** ***20.69 己酸甲酯 70 0.82±0.01b0.86±0.08b—a—a0.01 0.01 — — *** *** ***47.24 邻苯二甲酸二甲酯 330 7.49±0.37c2.52±0.05b1.50±0.04a2.48±0.22b0.02 0.01 <0.01 0.01 *** *** *** ***合计 8.31±0.38d3.38±0.20c1.50±0.04a2.48±0.22b0.03 0.18 <0.01 0.01 *** *** *** ** ***其他 8.15 二硫化碳 95.5 5.06±0.10d2.69±0.10c—a1.23±0.08b0.05 0.03 — 0.01 *** *** *** ** ***总计 542.07±21.68c482.17±14.46b448.7±37.14ab423.99±38.16a214.88 120.67 144.18 100.56 *** * * **
醛类因其阈值较低,通常对腌腊鱼的整体香气具有重要贡献。光照条件下,热风组和冷风组样品中醛类化合物OAV占比分别高达81.78%和67.48%,而避光条件下该数值显著下降至51.39%和47.60%,表明光照对醛类物质的生成有极显著的影响。腌腊鱼中C6~C10的饱和直链醛主要来自油酸、亚油酸、亚麻酸和花生四烯酸等不饱和脂肪酸的氧化降解[32]。其中,己醛、庚醛、辛醛、壬醛、癸醛5 种饱和直链醛在4 组腌腊鱼中同时存在且含量相对较高,但由于干制条件的不同,其含量间也存在显著差异。吴燕燕[10]和Chung[7]等分别在腌干咸带鱼和腌干白鳕鱼中也检出了这5 种饱和直链醛,证实其是重要的挥发性风味成分。烯醛主要产自亚麻酸酯和亚麻酸酯氢过氧化物的降解,具有清香、果香、坚果香和奶酪香等香气[33]。本研究发现,2-壬烯醛是光照组样品特有的醛类,值得注意的是,在热风光照组中其OAV占醛类OAV的50%以上,表明高温光照条件十分有利于该物质的生成。郭雅[2]和曾令彬[34]分别在风干鳊鱼和腌干白鲢中也检出了2-壬烯醛,但未对其产生机制展开进一步探讨。
醇类可能由脂肪酸的二级氢过氧化物的分解、脂肪氧化酶作用或由羰基化合物还原生成[35],其OAV占比仅次于醛类,本研究检出正己醇和1-辛烯-3-醇两种醇类化合物具有气味活性,其中1-辛烯-3-醇被报道具有青草味、泥土味和蘑菇味[35],可能对腌腊鱼的清香特征有一定贡献,且其含量与光照因素显著相关。吴燕燕等[8]在腌红牙䱛中也检测出这两种醇类,并指出1-辛烯-3-醇是一种具有浓郁植物芳香味的成分,能够产生清淡的香气,使发酵后的鱼肉更加柔和清香。
酮类主要由PUFA热氧化降解、醇类氧化和氨基酸降解生成[35],4 组腌腊鱼中酮类含量占比在3%~6%之间,由于酮类阈值较高,其OAV总和小于1,气味活性较弱,对腌腊鱼整体香气的贡献程度低于醛类。然而,有学者研究发现,酮类对抑制腥味具有一定效果[36]。2-庚酮是含量最高的酮类化合物,刘昌华[6]在风干鲈鱼中检测出的2-庚酮含量达3.91%,并推测其对产品风味可能起一定的修饰作用。
杂环类多数属于美拉德反应产物,在高温下较易生成,因此本研究中检出的杂环类物质主要集中在热风干制的两组。杂环类一般阈值较低,在4 组腌腊鱼样品中共检出了3 种具有气味活性(OAV>1)的杂环类物质:2-乙基呋喃、3-甲基-1H-吲哚和2-戊基吡啶,其中2-乙基呋喃在4 组样品中均有检测出,但仅在热风处理组中OAV大于1,说明高温对其生成有显著的促进作用。贡慧等[36]报道2-乙基呋喃为硫胺素的热降解产物,具有强烈的焦香味,在熟秋刀鱼中的相对含量为0.11%。
芳香类来源较为复杂,部分可能由带苯环的氨基酸降解产生,部分也可能来自外界环境,如萘被报道来源于水产品所处的水体环境[35]。本研究共检出19 种芳香类物质,但由于其阈值普遍较大,无一具备气味活性(OAV<1),表明芳香类化合物可能对腌腊鱼整体香气贡献较小。烃类主要来自脂肪酸烷氧自由基的裂解[10],其阈值较高,一般认为其对腌腊鱼整体香气贡献不大。本研究仅在热风光照组中检出一种具有气味活性的烃类物质——蒎烯,但对于其形成机制有待进一步研究。酯类可赋予腌制水产品独特的酯香味[10],本研究共检出3 种酯类物质,虽然酯类阈值较低,但这3 种酯类物质检出含量极低,因此均不具备气味活性。
比较4 种不同干制方法(热风光照、热风避光、冷风光照、冷风避光)得到的腌腊鱼产品,发现冷风避光组腌腊鱼样品的菌落总数最高,而热风光照组最低。光照条件下制得的腌腊鱼脂质氧化指标(AV、POV、TBA含量)均高于避光组,但两者总脂含量无显著差异;热风条件下制得腌腊鱼的POV和TBA含量均显著高于冷风组,而AV和总脂含量却显著低于冷风组。腌腊鱼中的PUFA占总脂肪酸的40%左右,无论是温度还是光照因素,均对以DHA为代表的n-3系PUFA影响显著。从总体感官得分来看,冷风组和光照组相对较高。采用整体材料吸附萃取-GC-MS法从4 种腌腊鱼样品中检出了82 种挥发性物质,确定了14 种气味活性物质。相同温度下,光照组的挥发物总含量与OAV总和显著高于避光组,其中热风光照组数值最高,分别达542.07 ng/g和214.88。
[1] 张进杰. 中国南方传统腊鱼加工、品质及安全性研究[D]. 杭州: 浙江大学, 2012: 15-31.
[2] 郭雅. 不同腌制工艺对风干鳊鱼品质影响研究[D]. 南京: 南京师范大学, 2016: 30-42.
[3] SHAHIDI F. Flavor of meat, meat products and seafoods[M]. London:Blackie Academic & Professional, 1998: 1-13.
[4] 蔡秋杏, 吴燕燕, 李来好, 等. 黄花鱼腌制加工过程的脂肪氧化分析[J].食品安全质量检测学报, 2014, 5(12): 4079-4084.
[5] TEJERO I, GONZÁLEZ-LAFONT A, LLUCH J M, et al. Photooxidation of lipids by singlet oxygen: a theoretical study[J].Chemical Physics Letters, 2004, 398(4): 336-342. DOI:10.1016/j.cplett.2004.09.093.
[6] 刘昌华. 鲈鱼风干成熟工艺及其脂质分解氧化和风味品质特性研究[D]. 南京: 南京农业大学, 2012: 4-20.
[7] CHUNG H Y, YEUNG C W, KIM J S, et al. Static headspace analysisolfactometry (SHA-O) of odor impact components in salted-dried white herring (Ilisha elongata)[J]. Food Chemistry, 2007, 104(2): 842-851. DOI:10.1016/j.foodchem.2006.08.036.
[8] 吴燕燕, 游刚, 李来好, 等. 低盐乳酸菌法与传统法腌干鱼制品的风味比较[J]. 水产学报, 2014, 38(4): 600-611. DOI:10.3724/SP.J.1231.2014.49049.
[9] 王雪锋. 低盐高水分草鱼的风味品质变化研究[D]. 杭州: 浙江工商大学, 2015: 70-76.
[10] 吴燕燕, 王悦齐, 李来好, 等. 基于电子鼻与HS-SPME-GC-MS技术分析不同处理方式腌干带鱼挥发性风味成分[J]. 水产学报, 2016,40(12): 1931-1940. DOI:10.11964/jfc.20160410346.
[11] 国家卫生和计划生育委员会. 食品安全国家标准 食品中水分的测定: GB 5009.3—2016[S]. 北京: 中国标准出版社, 2016: 1-6.
[12] 国家食品药品监督管理总局. 食品安全国家标准 食品微生物学检验 菌落总数测定: GB 4789.2—2016[S]. 北京: 中国标准出版社,2016: 1-5.
[13] FOLCH J, LEES M, SLOANE S G H. A simple method for the isolation and purification of total lipides from animal tissues[J].Journal of Biological Chemistry, 1957, 226(1): 497-509.
[14] REGUEIRO J A G, GIBERT J, DÍAZ I. Determination of neutral lipids from subcutaneous fat of cured ham by capillary gas chromatography and liquid chromatography[J]. Journal of Chromatography A, 1994,667(1/2): 225-233. DOI:10.1016/0021-9673(94)89071-4.
[15] 国家卫生和计划生育委员会. 食品安全国家标准 食品中酸价的测定: GB 5009.229—2016[S]. 北京: 中国标准出版社, 2016: 1-13.
[16] 国家卫生和计划生育委员会. 食品安全国家标准 食品中过氧化值的测定: GB 5009.227—2016[S]. 北京: 中国标准出版社, 2016: 1-6.
[17] ULU H. Evaluation of three 2-thiobarbituric acid methods for the measurement of lipid oxidation in various meats and meat products[J].Meat Science, 2004, 67(4): 683-687. DOI:10.1016/j.meatsci.2003.12.014.
[18] 顾赛麒, 吴娜, 张晶晶, 等. MMSE-GC-O结合OAV法鉴定蒸制崇明地区中华绒螯蟹中关键气味物质[J]. 食品安全质量检测学报, 2014,5(3): 877-888.
[19] 张晓艳, 郭全友, 杨宪时, 等. 淡腌黄鱼制品品质评价及细菌菌相分析[J]. 湖南农业科学, 2011(15): 120-123. DOI:10.16498/j.cnki.hnnykx.2011.15.003.
[20] ZHANG Jianhao, JIN Guofeng, WANG Jiamei, et al. Effect of intensifying high-temperature ripening on lipolysis and lipid oxidation of Jinhua ham[J]. LWT-Food Science and Technology, 2011, 44(2):473-479. DOI:10.1016/j.lwt.2010.07.007.
[21] COUTRON-GAMBOTTI C, GANDEMER G. Lipolysis and oxidation in subcutaneous adipose tissue during dry-cured ham processing[J].Food Chemistry, 1999, 64(1): 95-101. DOI:10.1016/S0308-8146(98)00079-X.
[22] 高海, 蔡欢欢, 朱志伟. 光照和温度对草鱼和三文鱼鱼肉贮藏品质的影响[J]. 食品科学, 2017, 38(15): 244-249. DOI:10.7506/spkx1002-6630-201715039.
[23] 霍晓娜, 李兴民, 谢辉, 等. 光照对猪肉脂肪氧化影响的研究[J]. 食品工业科技, 2006, 27(3): 90-92; 94. DOI:10.13386/j.issn1002-0306.2006.03.023.
[24] 闫瑾. 草鱼腌制、风干工艺及其加工过程中脂质氧化研究[D]. 杨凌: 西北农林科技大学, 2014: 27-30.
[25] WU Tao, MAO Linchun. Influences of hot air drying and microwave drying on nutritional and odorous properties of grass carp(Ctenopharyngodon idellus) fillets[J]. Food Chemistry, 2008, 110(3):647-653. DOI:10.1016/j.foodchem.2008.02.058.
[26] WONG K W. Clinical efficacy of n-3 fatty acid supplementation in patients with asthma[J]. Journal of the American Dietetic Association,2005, 105(1): 98-105. DOI:10.1016/j.jada.2004.10.009.
[27] TONGNUANCHAN P, BENJAKUL S, PRODPRAN T. Roles of lipid oxidation and pH on properties and yellow discolouration during storage of film from red tilapia (Oreochromis niloticus) muscle protein[J]. Food Hydrocolloids, 2011, 25(3): 426-433. DOI:10.1016/j.foodhyd.2010.07.013.
[28] FENNEMA O R, 王璋, 许时婴, 等. 食品化学[M]. 北京: 中国轻工业出版社, 2003: 222-223.
[29] FLORES M, SPANIER A M, TOLDRA F. Flavor analysis of drycured ham[M]. USA: Aspen Publishers, Inc., 1998: 320-341.
[30] SCHIFFMAN S S, BENNETT J L, RAYMER J H. Quantification of odors and odorants from swine operations in North Carolina[J].Agricultural and Forest Meteorology, 2001, 108(3): 213-240.DOI:10.1016/S0168-1923(01)00239-8.
[31] GIRI A, OSAKO K, OHSHIMA T. Identification and characterisation of headspace volatiles of fish miso, a Japanese fish meat based fermented paste, with special emphasis on effect of fish species and meat washing[J]. Food Chemistry, 2010, 120(2): 621-631.DOI:10.1016/j.foodchem.2009.10.036.
[32] SABIO E, VIDAL-ARAGÓN M C, BERNALTE M J, et al. Volatile compounds present in six types of dry-cured ham from south European countries[J]. Food Chemistry, 1998, 61(4): 493-503. DOI:10.1016/S0308-8146(97)00079-4.
[33] 陈德慰. 熟制大闸蟹风味及冷冻加工技术的研究[D]. 无锡: 江南大学, 2007: 1-7.
[34] 曾令彬. 腊鱼加工中微生物菌群、理化特性及挥发性成分的研究[D].武汉: 华中农业大学, 2008: 15-42.
[35] 顾赛麒, 陶宁萍, 吴娜, 等. 一种基于ROAV值鉴别蟹类关键特征性风味物的方法[J]. 食品工业科技, 2012, 33(13): 410-416.DOI:10.13386/j.issn1002-0306.2012.13.051.
[36] 贡慧, 杨震, 刘梦, 等. 秋刀鱼热加工后挥发性风味成分变化的分析[J]. 肉类研究, 2017, 31(1): 25-31. DOI:10.7506/rlyj1001-8123-201701005.
Effects of Different Drying Methods on Lipid Oxidation and Volatile Flavor Components of Cured Grass Carp