表1 正交试验因素水平表
Table1 Factors and levels used for orthogonal array design

水平 A超声时间/min B超声功率/W C蛋清液体积分数/%1 10 120 30 2 15 150 40 3 20 180 50
鸡蛋是日常生活中一种常见的蛋白质源食物,包括人体需要的8 种必需氨基酸,易被人体消化和吸收,消化率高达98%,位于食源蛋白质的第一位[1]。鸡蛋清是包裹在蛋黄周围的由蛋白质组成的透明淡黄色胶状物质,约占鸡蛋总质量的60%[2],其中蛋白质占蛋清质量的11%~13%。鸡蛋营养成分全面,烹饪方法多样,易被消化吸收,且产量丰富,因此蛋制品的研究已有上百年的历史。传统的蛋制品包括咸蛋、皮蛋、鸡蛋干等产品,现在越来越多的企业开始对鸡蛋进行深加工,以开发出新的蛋制品如蛋粉、蛋液,从而拓宽蛋品的应用领域。
蛋清粉具有起泡性、凝胶性和乳化性等加工特性,是食品工业中一种优质的加工辅料,功能性蛋清粉因为具有良好的加工特性且运输贮存方便而被广泛研究。Erem等[3]利用蛋清蛋白的高起泡性来改善面包质构。Bonet[4]和Wilderjans[5]等研究了蛋清蛋白的凝胶性在面团和蛋糕中发挥的作用,并猜测很可能是由于蛋清蛋白与其他蛋白形成混合网络结构改善了面团和蛋糕的性能。Lee等[6]的研究表明,使用木瓜蛋白酶水解液态蛋清后制得的蛋清粉起泡性有显著提升。迟玉杰[7]和赵薇[8]等分别对蛋清蛋白进行糖基化和磷酸化改性处理,干燥得到的蛋清粉凝胶强度和持水性增强。范蓓等[9]发明了一种高起泡性蛋清粉,将大豆分离蛋白与蛋清液混合后调节pH值至8~10,干燥后可得到高起泡性蛋清粉,且操作简单。但是这些研究普遍都是对蛋清粉的凝胶性、起泡性等性质进行改良,对于蛋清粉的溶解性、速溶性研究较少。蛋清粉良好的溶解性是实现其他加工特性的基础,开发速溶性蛋清粉不仅可以提高其溶解性和分散性,也可以改善其他功能特性。有学者使用酶解和磷酸化改性来制备溶解性良好的蛋清粉,同时其起泡性、凝胶性都有所改善[10]。柴萍萍等[11]对比了多种方法制备速溶蛋黄粉,其中以乙二胺四乙酸络合和磷脂酶A水解两种方法效果最好,但是考虑到食品的安全性,最后确定以内源蛋白酶和外加蛋白酶水解的方法更适合实际的生产。然而酶解法最大的问题就是酶解后会产生苦味[12],样品易吸湿[13],且灭酶条件要求高。
超声处理以其高效节能、绿色环保、对产品品质和营养破坏率低等优势受到越来越多的关注,在食品工业中应用越来越广[14]。食品加工中常使用16~100 kHz的超声波来改变食品的物理化学性质[15-16],研究发现超声功率、时间、物料浓度等因素会对蛋白质的溶解度、乳化性、凝胶性、起泡性等产生影响[17-19]。因此,本实验中使用不同的超声时间、功率以及蛋清液体积分数来处理蛋清蛋白,并研究各不同处理方法对喷雾干燥制得的蛋清粉速溶性质的影响,以探求适宜的超声条件,为速溶蛋清粉的制备提供理论依据。
新鲜海兰褐鸡蛋 湖北省农科院畜牧所;一水柠檬酸(食品级) 英轩实业有限公司;十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(sodium dodecyl sulphatepolyacrylamide gel electrophoresis,SDS-PAGE)试剂盒(生化试剂) 武汉谷歌生物有限公司;蛋白质电泳预染Marker(生化试剂) 美国Thermo Scientific公司;SDS(化学纯)、冰醋酸、无水乙醇(分析纯) 国药集团化学试剂有限公司;考马斯亮蓝R-250 武汉飞扬生物有限公司;Tris-base、甘氨酸、SDS-PAGE 5×蛋白上样缓冲液、磷酸盐缓冲液(phosphate buffered saline,PBS) 中国Biosharp生物技术有限公司。
HJ-4多头磁力加热搅拌器 常州国华电器有限公司;DF-101S集热式恒温加热磁力搅拌器 上海科尔仪器设备有限公司;FE20数显pH计、MS104S/01分析天平上海梅特勒-托利多仪器有限公司;YP502N电子天平上海精密仪器科技有限公司;FS-600N超声波细胞粉碎仪 上海生析超声仪器有限公司;Nanodrop 2000c紫外-分光光度计 美国Thermo Scientific公司;20 目标准检验筛 浙江上虞市五四纱筛厂制造;ALPHAI1-4真空冷冻干燥机 德国Christ公司;DYY-12电泳仪 北京六一仪器厂;JSM-6390扫描电子显微镜 日本NTC公司;Mastersizer 2000激光粒度分布仪 英国Malvern仪器有限公司;J-810圆二色光谱仪 日本JASCO公司。
1.3.1 蛋清液的制备
挑取新鲜的鸡蛋清洗晾干,使用分蛋器将蛋清和蛋黄分开,挑出蛋清中的系带,使用磁力搅拌器低速搅拌,将蛋清液的浓厚蛋白和稀薄蛋白搅拌均匀,形成黏度均一、无蛋白团块的蛋清液后在干净的环境中自然发酵24 h。使用柠檬酸溶液调节蛋清液的pH值,边搅拌边调节pH值至接近7.5,缓慢加入蒸馏水将蛋清液稀释到实验所需体积分数,搅拌均匀后将pH值调节到7.5左右。
1.3.2 超声处理
使用超声波细胞粉碎仪对经过预处理的蛋清液进行超声处理。在500 mL的烧杯中倒入300 mL待超声蛋清液,将超声探头深入到液面之下3 cm左右,调节超声时间和功率进行超声实验。整个超声过程中烧杯都置于冰水浴中以保持蛋清液的温度基本不变,防止超声产生的热效应使蛋清液局部温度过高从而使蛋白变性。
1.3.3 单因素试验设计
试验中采用连续超声模式,超声频率固定为20 kHz。在单因素试验中,以蛋清粉的分散性、溶解度和稳定系数为评价指标,研究不同超声时间、功率和超声时蛋清液体积分数对制得蛋清粉的速溶性能的影响。固定超声功率为120 W、蛋清液体积分数为20%,设置超声时间分别为0、5、10、15、20、25、30 min;固定超声时间15 min、蛋清液体积分数为20%,设置超声功率为0、90、120、150、180、210、240 W;在固定超声时间为15 min、超声功率为150 W的条件下对体积分数分别为20%、30%、40%、50%、60%、70%的蛋清液进行超声处理。
1.3.4 超声条件正交优化试验设计
根据单因素试验结果设计正交试验,因素水平设计如表1所示。正交试验以分散性、溶解度和稳定系数为考察指标,综合对比确定超声处理蛋清液的最优参数。
表1 正交试验因素水平表
Table1 Factors and levels used for orthogonal array design

水平 A超声时间/min B超声功率/W C蛋清液体积分数/%1 10 120 30 2 15 150 40 3 20 180 50
1.3.5 不同处理方式蛋清粉的制备
将未经超声处理的蛋清原液和经过最优超声条件处理后的蛋清液分别加入蒸馏水稀释到蛋清液体积分数20%后,用20 目筛网过滤掉溶液中的不溶物质,进行喷雾干燥。喷雾干燥条件为进风温度170 ℃,流量1 200 mL/h[20-21]。同时,将未经超声处理的蛋清原液和经过最优超声条件处理后的蛋清液分别进行真空冷冻干燥制成蛋清冻干粉,收集喷雾干燥和冷冻干燥制得的不同样品,标注信息并密封保存用于后续实验指标的测定。
1.3.6 蛋清粉分散性的测定
参考李佳宁[22]的方法并作改进,在100 mL烧杯中加入30 mL蒸馏水后放于恒温水浴锅中保温,温度设定为40 ℃。称取1.00 g蛋清粉样品均匀缓慢地倒入烧杯中,使用磁力搅拌器以中等转速匀速搅动,同时记录从搅拌开始到蛋清粉结块组织全部润湿分散所需的时间。实验重复3 次,取其平均值作为分散时间来评价蛋清粉的分散性。
1.3.7 蛋清粉溶解度的测定
参考马爽[23]和GB 5413.29—2010《食品安全国家标准 婴幼儿食品和乳品中溶解性的测定》的方法并稍作修改。称取2.00 g蛋清粉,用30 mL 25~30 ℃的蒸馏水分数次将蛋清粉溶解于50 mL离心管中,加塞。将离心管置于30 ℃蒸馏水中保温5 min,取出后摇动3 min。以9 000 r/min离心10 min,使不溶物沉淀。倾去上清液,再加入25~30 ℃的水30 mL,加塞,上下振荡,使沉淀悬浮,再次离心10 min,倾去上清液,移入110 ℃烘箱中干燥至恒质量(最后两次质量差不超过2 mg)。同时参照GB 5009.3—2016《食品安全国家标准 食品中水分的测定》中的方法测定蛋清粉样品的水分含量,实验重复3 次。样品溶解度按公式(1)计算。
式中:m为样品质量/g;m1为离心管质量/g;m2为离心管和不溶物干燥后质量/g;B为样品水分含量/(g/g)。
1.3.8 蛋清粉稳定系数的测定
参考叶蕾等[24]的方法测定稳定系数,取0.50 g蛋清粉样品用蒸馏水配制成5 mg/mL溶液,取一定体积的蛋清粉溶液于50 mL离心管中,3 000 r/min离心20 min,取1 mL上清液稀释10 倍后置于1 cm比色皿中,以蒸馏水作为空白对照,测定280 nm波长处的吸光度A1和离心前的吸光度A2,稳定系数按公式(2)计算,实验重复3 次。
1.3.9 蛋清粉的SDS-PAGE分析
SDS-PAGE参考胡珊[25]的方法,使用质量分数12%分离胶和5%浓缩胶。将不同处理方法制成的蛋清粉用50 mmol/L、pH 7.0的PBS配成质量浓度为1 mg/mL的蛋清粉溶液。取80 μL样液加入200 μL离心管中,加入20 μL 5×蛋白上样缓冲液(含β-巯基乙醇),混匀后沸水浴加热3~5 min,冷却备用,用微量进样针取15 μL样液和蛋白Marker分别加入样品槽后电泳,浓缩胶电压80 V,分离胶电压120 V。胶板用固定液固定30 min,染色液染色30 min,然后用脱色液多次脱色将背景颜色脱除。
1.3.10 蛋清粉的扫描电子显微镜观察
取一定量的蛋清粉样品粘于样品台上并喷镀金电导层,在高分辨率扫描电子显微镜下放大200 倍观察4 种粉体的形态差异,并进一步放大500 倍和2 000 倍观察喷雾干燥制得的蛋清粉的形态结构。
1.3.11 蛋清粉的粒径分析
使用激光纳米粒度分析仪测定不同蛋清粉样品的粒径和分布状况,每个样品重复测定3 次,记录平均粒径。
1.3.12 蛋清粉表面疏水性的测定
使用8-苯胺-1-萘磺酸(8-anilino-1-naphthalenesulfonic acid,ANS)荧光探针法测定蛋清粉的表面疏水性。用PBS(10 mmol/L、pH 7.2)配制浓度为8 mmol/L的ANS溶液,同时将样品稀释为不同质量浓度(0.1、0.2、0.3、0.4、0.5 mg/mL)的溶液。取不同质量浓度的稀释液10 mL,使用荧光分光光度计,在390 nm激发波长和470 nm发射波长处分别测定样品的荧光强度FI0和样品加入20 μL ANS溶液后的荧光强度FI1,FI1和FI0的差值记为FI,以蛋白质量浓度为横坐标、FI为纵坐标作图,曲线初始阶段的斜率记为蛋白质分子的表面疏水性指数。将未超声的蛋清冻干粉的表面疏水性假定为1.0,其余样品与其的比值记作表面疏水性相对指数。
1.3.13 蛋清粉的圆二色光谱测定
取不同方法制备的蛋清粉溶于蒸馏水中配制成0.2 mg/mL溶液,扫描波长范围190~250 nm,扫描速率100 nm/min,光谱间隔0.1 nm,平行测定3 次。
使用Origin 8.0软件作图,使用SPSS 17.0软件进行正交试验的方差分析和多重比较分析,以P<0.05表示差异显著。
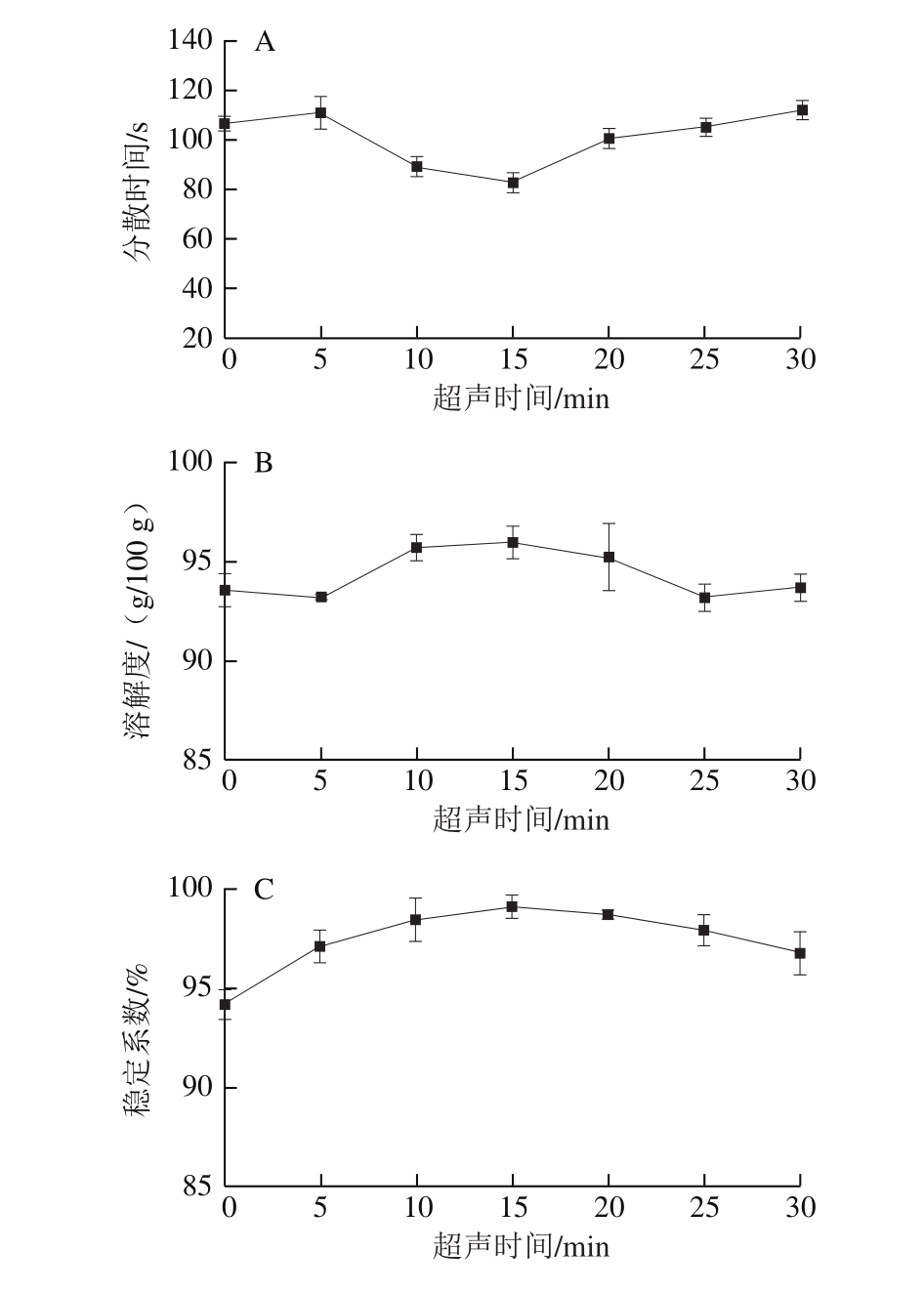
图1 超声时间对蛋清粉分散时间(A)、溶解度(B)和稳定系数(C)的影响
Fig.1 Effect of ultrasonic treatment time on dispersion time (A),solubility (B) and stability coefficient (C) of egg white powder
由图1可知,随着超声时间的延长,超声后制得蛋清粉的分散时间在超声前5 min没有明显变化,之后随超声时间的延长明显降低,超声15 min时分散时间最短,为(82.67±4.16)s,然后其又继续随超声时间的延长逐渐延长。而随着超声时间的延长,超声后制得蛋清粉的溶解度缓慢增加,在超声10 min时最高,为(95.69±0.68)g/100 g,此后到20 min时溶解度基本维持稳定,变化不明显,20 min之后明显开始下降。随着超声时间的延长,蛋清粉稳定系数都优于未超声的蛋清粉,其中超声15 min时稳定系数最高,达(99.10±0.58)%。这可能是因为一定时间的超声可以破坏蛋白质聚集,使蛋白质复合物解离分散,从而使更多的可溶性蛋白质分散到溶液中[26],但是蛋清蛋白质对外力的作用变化十分敏感,所以短时间的超声即可使聚集的蛋清蛋白质分散开,超声时间过长会造成蛋白质的再聚集,使其疏水性增加,分散性和溶解度下降,溶液中的不溶性蛋白质含量增加,溶液的稳定系数也就相应的降低。Jambrak等[27]用超声处理大豆分离蛋白和大豆浓缩蛋白的溶液后得到了相似的结果;孙英杰[28]用超声处理大豆蛋白的时候也发现随着超声时间的延长,大豆蛋白的溶解度出现了先增加后降低的趋势。因此,选择超声时间10、15、20 min进行正交试验。
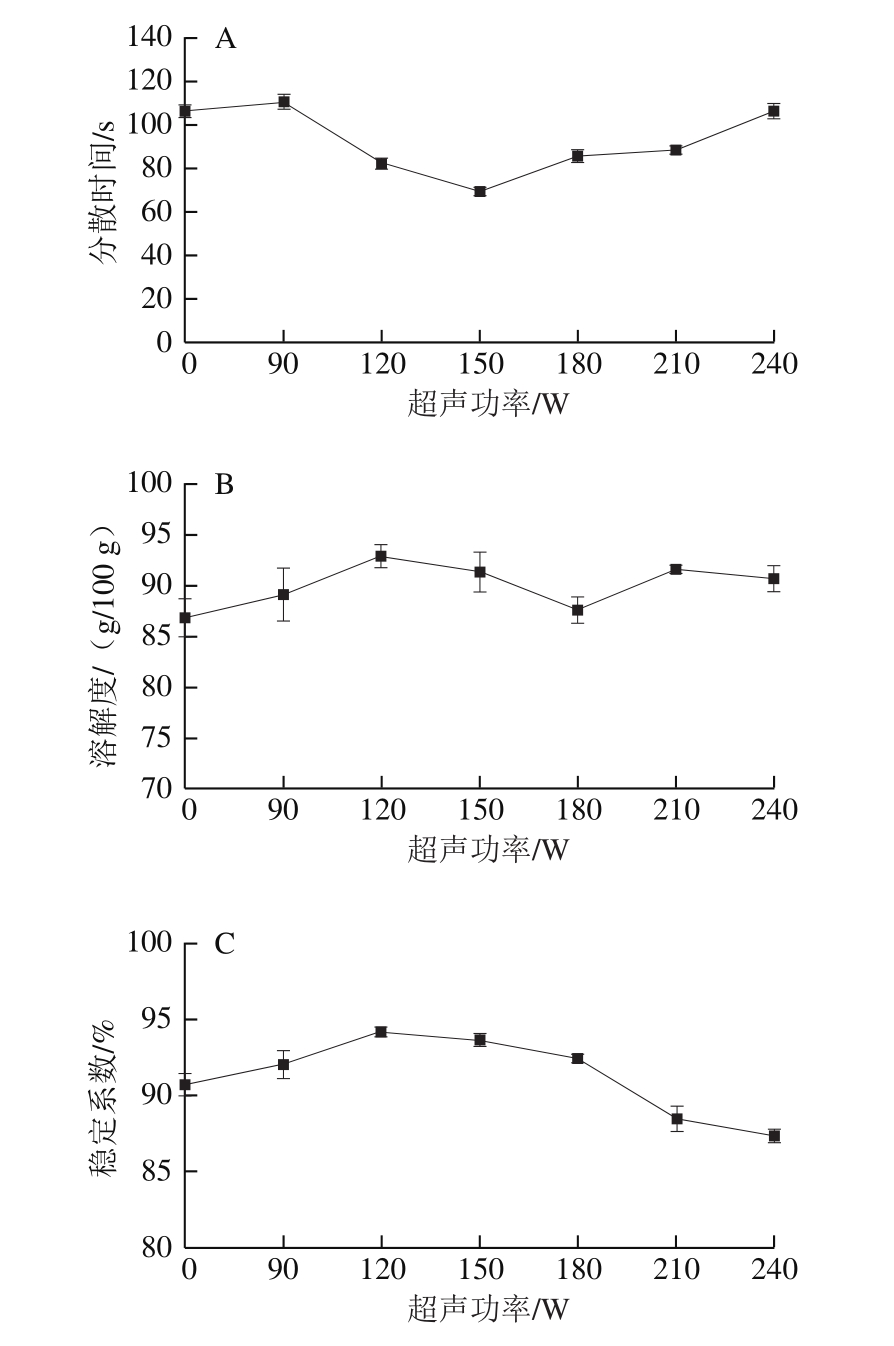
图2 超声功率对蛋清粉分散时间(A)、溶解度(B)和稳定系数(C)的影响
Fig.2 Effect of ultrasonic power on dispersion time (A), solubility (B)and stability coefficient (C) of egg white powder
从图2中可以看出,超声功率为90 W时蛋清粉的分散时间与未超声蛋清粉没有明显差异。超声功率升高到150 W时分散时间缩短至(69.33±2.08)s,分散性明显优于其他样品。在超声功率120 W和150 W时制得蛋清粉的稳定系数明显高于其他功率下制备的样品,分别为(94.20±0.32)%和(93.69±0.42)%,这主要与超声的空化效应破坏不稳定的蛋白聚集形成小的可溶性物质有关[29]。随着超声功率的升高,蛋清粉的溶解度在120 W时最高,为(92.96±1.11)g/100 g,功率继续升高时溶解度在87~91 g/100 g间波动。推测可能是在高功率超声处理时,蛋白质的溶解度虽然增加,但是分散性和稳定系数并没有改善,这可能也与蛋白质的再聚集有关。蛋白质聚集形成大的蛋白质分子,再聚集的过程中部分可溶性蛋白质与不溶性蛋白质结合,虽然最终溶解度可能略有增加,但是分散时间延长且聚合物不稳定,所形成溶液的稳定系数也仍会降低。Jiang Lianzhou等[29]在研究超声处理黑豆分离蛋白时发现,随着超声功率的增加,蛋白质的溶解度会增加,但是进一步增加超声功率和延长时间,溶解度反而会降低;他们认为超声波可能使蛋白质部分解折叠,从而使蛋白质与水分子间的相互作用增加,当超声强度增加时,蛋白分子通过非共价相互作用形成聚合物使溶解性降低。综合考虑分散性、溶解性和稳定系数后选择在超声功率120、150、180 W进行正交试验。
如图3所示,体积分数50%时蛋清粉分散时间为(76.44±0.19)s,分散性明显优于其他体积分数样品;而蛋清粉的溶解度没有发生明显变化,在蛋清液体积分数70%的时候有所下降;在蛋清液体积分数低于50%时,蛋清粉的稳定系数没有明显变化,都高于90%,体积分数高于50%时,蛋清粉稳定系数开始有明显的降低趋势。随着蛋清液体积分数的增加,溶液中的蛋白质分子含量增加,超声波对蛋白质分子的作用增强,空化作用使更多的蛋白质分子结构发生改变,分子结构变得疏松展开,蛋白质分子的亲水基团暴露。同时,卵黏蛋白及溶菌酶等蛋白质聚合形成的难溶聚合体被分散,更多的可溶性蛋白质被释放到水溶液中,蛋清粉所需要的分散时间缩短。蛋清是一种胶体物质,自身黏度很大,蛋清液体积分数超过50%时,超声产生的热效应会使局部温度快速升高,不能及时通过冰水浴散热降温。而蛋清蛋白质的变性温度为65 ℃[30],温度过高会使蛋清蛋白质发生变性凝胶化,尤其是一些可溶性蛋白质如卵白蛋白、卵转铁蛋白等遇热易变性[31],在喷雾干燥前被过滤掉,降低了蛋白粉中可溶性蛋白质的比例。汤虎[32]在研究超声改性小麦面筋蛋白时也发现,随着底物体积分数的增加,小麦面筋蛋白的溶解度明显提高,当体积分数超过10%时,在相同时间内超声的空化效应减弱,蛋白质结构的改变变小,可溶性蛋白质含量减少,溶解度下降。一定范围内体积分数的变化所产生的超声强度的变化并不明显,所以蛋清粉速溶特性的提高并不明显,但是考虑到实际生产加工过程中的能耗成本等因素,选择相对较高的蛋清液体积分数可以有效地节省成本、提高生产效率,故选择超声时蛋清液的体积分数为30%、40%和50%进行正交试验。

图3 蛋清液体积分数对蛋清粉分散时间(A)、溶解度(B)和稳定系数(C)的影响
Fig.3 Effect of egg white concentration on dispersion time (A), solubility (B)and stability coefficient (C) of egg white powder
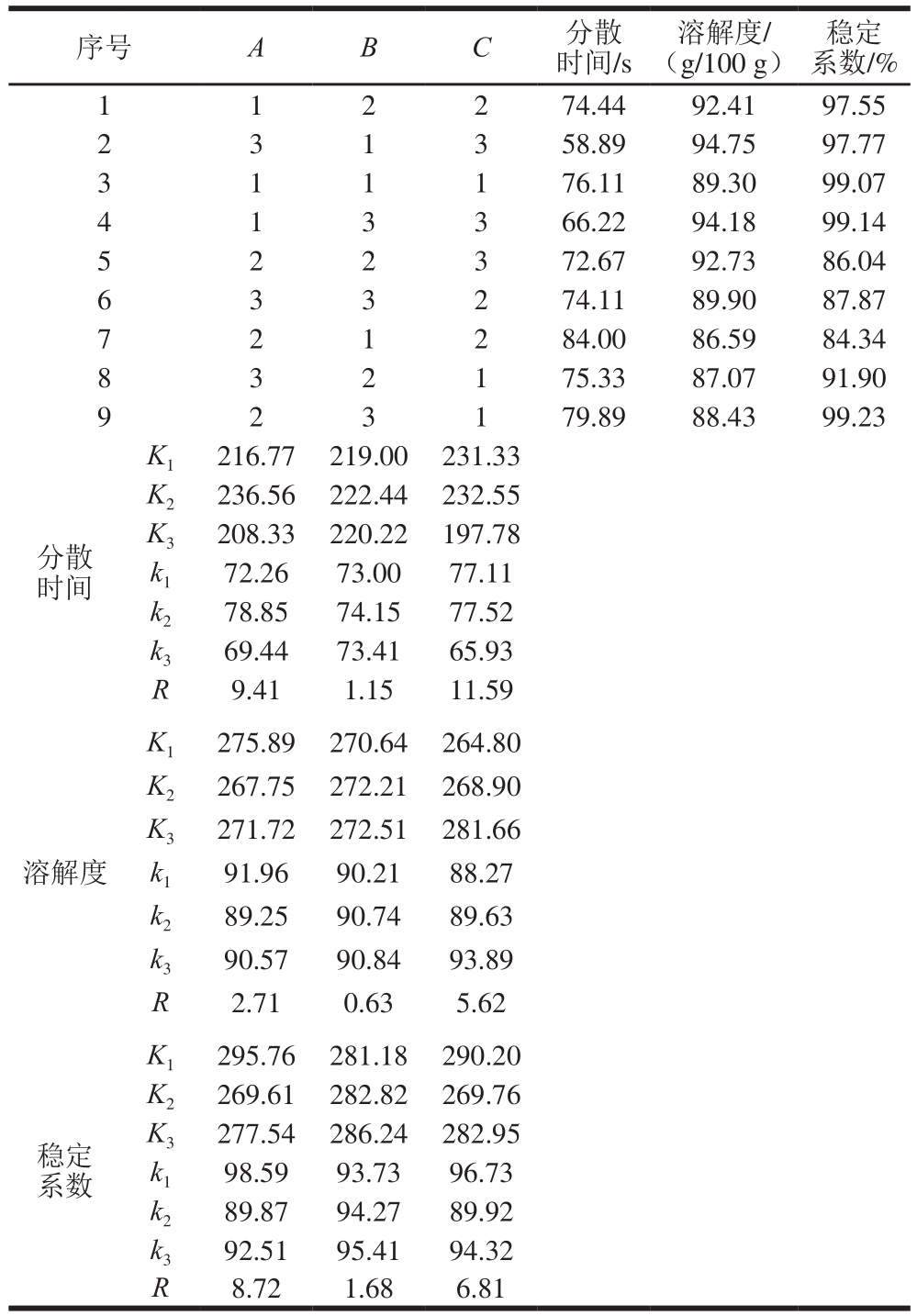
从表2可以看出,影响蛋清粉分散性的因素主次顺序为:C>A>B,分散时间最短的最优水平是A3B1C3,即超声时间20 min、超声功率120 W、蛋清液体积分数50%;影响蛋清粉溶解度的因素主次顺序为C>A>B,溶解度最优的水平组合为A1B3C3,即超声时间10 min、超声功率180 W、蛋清液体积分数50%;影响蛋清粉稳定系数的因素主次顺序为:A>C>B,稳定系数最高的水平组合为A1B3C1,即超声时间10 min、超声功率180 W、蛋清液体积分数30%。从表3可以看出,超声时间和超声时蛋清液体积分数对蛋清粉的速溶性(分散时间、溶解度、稳定系数)影响显著(P<0.05),超声功率的影响不显著。结合表4可以得到蛋清粉分散时间、溶解度和稳定系数的正交试验最优的超声条件组合是A1B1C3。综合考虑实验结果以及实际生产过程中的能耗成本等因素,最终确定速溶性蛋清粉的超声处理条件为A1B1C3,即超声时间10 min、超声功率120 W、蛋清液体积分数为50%。
表2 正交试验结果及极差分析
Table2 Orthogonal array design with range analysis of experimental results
序号 A B C 分散时间/s稳定系数/%1 1 2 2 74.44 92.41 97.55 2 3 1 3 58.89 94.75 97.77 3 1 1 1 76.11 89.30 99.07 4 1 3 3 66.22 94.18 99.14 5 2 2 3 72.67 92.73 86.04 6 3 3 2 74.11 89.90 87.87 7 2 1 2 84.00 86.59 84.34 8 3 2 1 75.33 87.07 91.90 9 2 3 1 79.89 88.43 99.23溶解度/(g/100 g)分散时间K1216.77 219.00 231.33 K2236.56 222.44 232.55 K3208.33 220.22 197.78 k172.26 73.00 77.11 k278.85 74.15 77.52 k369.44 73.41 65.93 R 9.41 1.15 11.59溶解度K1275.89 270.64 264.80 K2267.75 272.21 268.90 K3271.72 272.51 281.66 k191.96 90.21 88.27 k289.25 90.74 89.63 k390.57 90.84 93.89 R 2.71 0.63 5.62稳定系数K1295.76 281.18 290.20 K2269.61 282.82 269.76 K3277.54 286.24 282.95 k198.59 93.73 96.73 k289.87 94.27 89.92 k392.51 95.41 94.32 R 8.72 1.68 6.81
表3 正交试验结果方差分析
Table3 Analysis of variance for the experimental results from orthogonal array design

注:*.差异显著(P<0.05),**.差异极显著(P<0.01);下同。
指标 变异来源 平方和 自由度 均方 F P分散时间A 419.780 2 209.890 22.240 0.000**B 6.119 2 3.060 0.324 0.727 C 779.217 2 389.608 41.284 0.000**误差 188.747 20 9.437溶解度A 33.105 2 16.553 5.295 0.014*B 2.022 2 1.011 0.323 0.727 C 154.728 2 77.364 24.747 0.000**误差 62.524 20 3.126 A 0.036 2 0.018 6.942 0.005**B 0.006 2 0.003 1.117 0.347 C 0.021 2 0.011 4.148 0.031*误差 0.052 20 0.003稳定系数
表4 正交试验多重比较结果
Table4 Multiple comparison of the experimental results from orthogonal array design

注:大写字母不同表示同一指标、同一因素的不同水平之间差异极显著(P<0.01);小写字母不同表示同一指标、同一因素的不同水平之间差异显著(P<0.05)。
指标 因素A 因素B 因素C水平1水平3水平2 水平1水平2水平3 水平3水平1水平2分散时间a b b a a a a ab b A AB B A A A A A A a a b a a a a b b A A B A A A A B B溶解度 a ab b a a a a b b A AB B A A A A B B稳定系数
在该超声条件下对蛋清液进行验证实验,最终制备蛋清粉的平均分散时间为56.67 s,平均溶解度为93.56 g/100 g,>平均稳定系数为97.29%,优于正交试验中的结果。

图4 不同方法制备的蛋清粉的SDS-PAGE图
Fig.4 SDS-PAGE of egg white powder prepared by different methods
从图4中可以看出,蛋清经过超声处理后,喷雾干燥制得的蛋清粉的蛋白质组分与纯蛋清粉相比差异不明显,这表明超声没有改变蛋白质的一级结构,Karki[33]和Zhang Qiuting[34]等在研究超声处理大豆分离蛋白和花生分离蛋白的SDS-PAGE时也得到了相似的结果。但是对比样品A、D可以看到,分子质量大于100 kDa时样品A中有3 条条带,而样品D中只存在1 条条带,这说明超声使一些分子质量大于100 kDa的蛋白质发生解离,这主要是因为超声空化作用破坏了蛋白质的聚集(主要是卵黏蛋白聚集物)。样品B、C都是经过喷雾干燥制得的蛋清粉,由于在喷雾干燥前会进行加水稀释并过滤,一些卵黏蛋白及其聚集物在喷雾干燥前就已被除去,通过对比可以看到超声处理之后的蛋清粉在约35 kDa处的蛋白含量增多,这也进一步证实超声主要破坏了蛋白质的聚集。Jambrak等[35]研究乳清蛋白也发现了类似的结果,20 kHz超声会使局部分子间的疏水相互作用被破坏,乳清蛋白颗粒尺寸和分子质量减小。

图5 不同方法制备的蛋清粉扫描电子显微镜图(×200)
Fig.5 Scanning electron microscopy images of egg white powder prepared by different methods (× 200)
从蛋清粉样品的扫描电子显微镜观察结果可以看出不同方法制备的蛋清粉之间的形态差距较大。冻干粉呈片状结构,形态和大小分布不均(图5A、D),超声前后的形态变化主要与外力挤压破碎有关。而喷雾干燥后的蛋清粉颗粒形状规则、粒径较小(图5B、C),这主要与喷雾干燥过程造粒有关。

图6 超声前后喷雾干燥制备的蛋清粉的扫描电子显微镜图
Fig.6 Scanning electron microscopy images of egg white powder prepared by spray drying with and without ultrasonic pretreatment
从图6可以看出,经过喷雾干燥后的蛋清粉成带孔颗粒状,超声之后的蛋清粉颗粒小于未超声样品,且分散均匀,颗粒间的聚集程度较低(图6C),这些结构都有助于蛋清粉在水中的快速分散溶解。通常认为分散系中的颗粒越小对应的溶解度越高[36],郭武汉等[37]研究超微粉碎处理小麦面筋蛋白时也发现处理后随着粉体粒径的减小,溶解度整体明显增加。
从图7可以看出,不同方法制备的蛋清粉溶液的粒径分布差别明显。与原蛋清冻干粉相比较,超声处理和喷雾干燥都会使蛋白质的粒径减小,对比样品A、D可以看到,超声的主要作用为减少大粒径的蛋白质分子,说明超声会使大分子蛋白质发生裂解,与SDS-PAGE分析结果(图6)对应。样品B、C是经过喷雾干燥制得的蛋清粉,由于喷雾干燥过程中伴随着造粒,所以粒径均小于1 000 nm,样品B、C中粒径大于和小于100 nm的部分约占36%和64%,但超声处理后制得的样品更倾向于向较小的粒径范围分布,粒径的减小有利于蛋清粉在水中的分散。
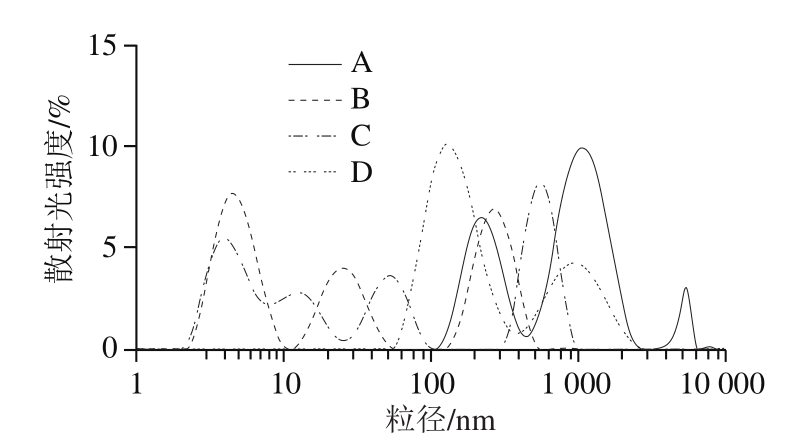
图7 不同方法制备的蛋清粉溶液的粒径分布
Fig.7 Particle size distribution of egg white powder prepared by different methods
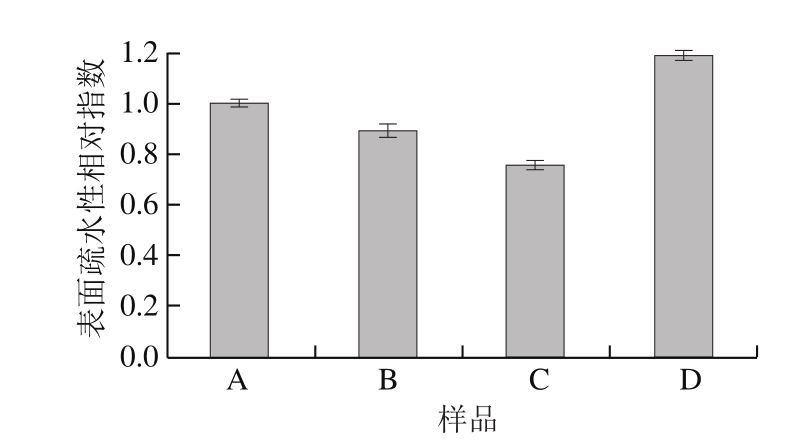
图8 不同方法制备的蛋清粉的表面疏水性相对指数
Fig.8 Relative hydrophobicity indices of egg white powder prepared by different methods
经过超声和喷雾干燥处理后制得的蛋清粉与蛋清冻干粉相比表面疏水性发生了明显变化,这主要是因为超声和高温会使蛋白质结构发生变化。比较图9中样品A、D和B、C可以看出,超声可以增加蛋白质的表面疏水性,这主要与超声的空化作用有关,超声会破坏蛋白质大分子聚集物,使其疏水基团暴露,表面疏水性增加,溶解度增大[26]。与样品A、D相比可以看出,喷雾干燥的高温会使样品B、D的蛋白质变性,一部分疏水基团被包裹起来,疏水性有所降低,但是结合图5中蛋清粉形态差异分析,喷雾干燥带来的速溶性的提高也与蛋清粉颗粒疏松多孔的结构有关。
图9显示超声和喷雾干燥都会使蛋白质的二级结构发生不同程度的变化。α-螺旋和β-折叠结构中含有较多的氢键,超声的空化作用和高温都会使蛋白质氢键的取向发生不同程度的重排。由表5对比样品A、D可以看出,超声使蛋白质的α-螺旋比例减少,β-折叠比例增多,蛋白质结构趋于无序状态,对比样品B、C也可以看到超声使蛋白质结构中的α-螺旋比例减少,β结构(包括β-折叠和β-转角)比例稍有增加。这表明蛋白质在超声作用下结构会趋于展开,发生分子伸展[17],同时导致其表面疏水性增加[38],这也与2.8节表面疏水性的结果一致,这些因素综合作用使得蛋白质的溶解度增加。

图9 不同方法制备的蛋清粉的圆二色光谱图
Fig.9 Circular dichroism spectra of egg white powder prepared by different methods
表5 不同方法制备的蛋清粉的二级结构组成
Table5 Protein secondary structure contents of egg white powder prepared by different methods

注:A.蛋清冻干粉;B.蛋清超声后喷雾干燥粉;C.蛋清喷雾干燥粉;D.蛋清超声后冻干粉。
无规卷曲比例/%A 31.8 36.3 7.2 24.7 B 30.5 41.0 5.0 23.5 C 31.2 40.7 4.3 23.8 D 26.4 48.1 3.5 21.9组别 α-螺旋比例/%β-折叠比例/%β-转角比例/%
本研究中采用超声对蛋清进行预处理后喷雾干燥,以期得到速溶性能良好的蛋清粉。影响超声作用效果的因素主要有超声时间、功率和样品体积分数,通过正交试验优化得到了超声处理的最优水平组合为超声时间10 min、超声功率120 W、蛋清液体积分数50%。在该超声条件下制备的蛋清粉的平均分散时间为56.67 s,平均溶解度为93.56 g/100 g,平均稳定系数为97.29%,比未经超声处理的蛋清液制备的蛋清粉的平均分散时间缩短了49.83 s,平均溶解度提高了3.34 g/100 g,平均稳定系数提高了4.85%。SDS-PAGE和粒径分析显示超声可以分散蛋清中的大分子蛋白聚集物,扫描电子显微镜观察结果显示超声后喷雾干燥制备的蛋清粉颗粒较小、分散均匀,同时超声可以增加蛋清粉蛋白质的表面疏水性和无序结构含量,有助于蛋清粉在水中的分散溶解。本研究表明超声改性蛋清可以提高蛋清粉的速溶性能,且实验操作环保安全,为蛋清粉的开发利用提供了实验依据。
[1] 李勇. 营养与食品卫生学(北京大学医学教材)[M]. 北京: 北京大学医学出版社, 2005: 34-57.
[2] KOVACS-NOLAN J, PHILLIPS M, MINE Y. Advances in the value of eggs and egg components for human health[J]. Journal of Agricultural and Food Chemistry, 2005, 53(22): 8421-8431.DOI:10.1021/jf050964f.
[3] EREM F, SONTAG-STROHM T, CERTEL M, et al. Functional characteristics of egg white proteins within wheat, rye, and germinatedrye sourdoughs[J]. Journal of Agricultural and Food Chemistry, 2010,58(2): 1263-1269. DOI:10.1021/jf903228x.
[4] BONET A, BLASZCZAK W, ROSELL C M. Formation of homopolymers and heteropolymers between wheat flour and several protein sources by transglutaminase-catalyzed cross-linking[J]. Cereal Chemistry, 2006, 83(6): 655-662. DOI:10.1094/CC-83-0655.
[5] WILDERJANS E, LUYTS A, BRIJS K, et al. Ingredient functionality in batter type cake making[J]. Trends in Food Science and Technology,2013, 30(1): 6-15. DOI:10.1016/j.tifs.2013.01.001.
[6] LEE W C, CHEN T C. Functional characteristics of egg white solids obtained from papain treated albumen[J]. Journal of Food Engineering,2002, 51(4): 263-266. DOI:10.1016/S0260-8774(01)00066-8.
[7] 迟玉杰, 胥伟, 洪煜淼. 糖基化处理对蛋清粉凝胶性与物化特性的影响[J]. 食品科学, 2013, 34(7): 82-85. DOI:10.7506/spkx1002-6630-201307018.
[8] 赵薇, 迟玉杰. 磷酸化改性提高蛋清粉凝胶性的研究[J]. 食品与发酵工业, 2011, 37(9): 79-83. DOI:10.13995/j.cnki.11-1802/ts.2011.09.024.
[9] 范蓓, 卢嘉, 卢晓明, 等. 一种高起泡性蛋清粉及其制备方法:CN104544283A[P]. 2015-04-29 [2017-08-20].
[10] 刘丽莉, 王焕, 杨协力, 等. 一种酶解和磷酸化改性协同制备蛋清粉的工艺方法: CN104839760A[P]. 2015-08-19 [2017-08-20].
[11] 柴萍萍, 鲍鲁生, 金杨, 等. 不同方法制备速溶蛋黄粉溶解特性研究[J].食品科技, 2015, 40(1): 73-76. DOI:10.13684/j.cnki.spkj.2015.01.016.
[12] LEKSRISOMPONG P P, MIRACLE R E, DRAKE M A.Characterization of flavor of wheyprotein hydrolysates[J]. Journal of Agricultural and Food Chemistry, 2010, 58(10): 6318-6327.DOI:10.1021/jf100009u.
[13] YANG S, MAO X Y, LI F F, et al. The improving effect of spraydrying encapsulation process on the bitter taste and stability of whey protein hydrolysate[J]. European Food Research and Technology,2012, 235(1): 91-97. DOI:10.1007/s00217-012-1735-6.
[14] JIANG Z M, YAO K, YUAN X Y, et al. Effects of ultrasound treatment on physicochemical, functional properties and antioxidant activity of whey protein isolate in the presence of calcium lactate[J].Journal of the Science of Food and Agriculture, 2018, 98(4): 1522-1529. DOI:10.1002/jsfa.8623.
[15] CHEMAT F, ZILL-E-HUMA, KHAN M K. Applications of ultrasound in food technology: processing, preservation and extraction[J]. Ultrasonics Sonochemistry, 2011, 18(4): 813-835.DOI:10.1016/j.ultsonch.2010.11.023.
[16] AWAD T S, MOHARRAM H A, SHALTOUT O E, et al.Applications of ultrasound in analysis, processing and quality control of food: a review[J]. Food Research International, 2012, 48(2): 410-427. DOI:10.1016/j.foodres.2012.05.004.
[17] HU H, WU J H, LI-CHAN E C Y, et al. Effects of ultrasound on structural and physical properties of soy protein isolate (SPI)dispersions[J]. Food Hydrocolloids, 2013, 30(2): 647-655.DOI:10.1016/j.foodhyd.2012.08.001.
[18] LI Y, LIU B H, JIANG N, et al. Effects of ultrasound treatment on gelling properties of black bean protein isolate[J]. Journal of Chinese Institute of Food Science and Technology, 2017, 17(1): 161-169.DOI:10.16429/j.1009-7848.2017.01.021.
[19] O’SULLIVAN J, MURRAY B, FLYNN C, et al. The effect of ultrasound treatment on the structural, physical and emulsifying properties of animal and vegetable proteins[J]. Food Hydrocolloids,2015, 53: 141-154. DOI:10.1016/j.foodhyd.2015.02.009.
[20] 刘静波, 马爽, 刘博群, 等. 喷雾干燥条件对高铁蛋粉溶解特性的影响[J]. 农业工程学报, 2011, 27(11): 365-371. DOI:10.3969/j.issn.1002-6819.2011.11.068.
[21] 孙临政, 迟玉杰, 王欢, 等. 喷雾干燥条件对蛋清粉冲调效果的影响[J].中国家禽, 2014, 36(2): 29-33. DOI:10.3969/j.issn.1004-6364.2014.02.008.
[22] 李佳宁. 多元素营养粉的冲调性改良[D]. 无锡: 江南大学, 2009:5-10.
[23] 马爽. 蛋粉冲调特性及复合型功能蛋粉的研究与开发[D]. 长春: 吉林大学, 2012: 39-42.
[24] 叶蕾, 郭本恒, 龚广予, 等. 钙强化豆奶稳定性研究[J]. 安徽农业科学,2009, 37(17): 8175-8176; 8183. DOI:10.3969/j.issn.0517-6611.2009.17.143.
[25] 胡珊. 不同禽蛋蛋清及蛋黄差异蛋白质组学研究[D]. 武汉: 华中农业大学, 2016: 13-18.
[26] 王一博. 高起泡性蛋清液制备与应用研究[D]. 武汉: 华中农业大学,2016: 29-30.
[27] JAMBRAK A R, LELAS V, MASON T J, et al. Physical properties of ultrasound treated soy proteins[J]. Journal of Food Engineering, 2009,93(4): 386-393. DOI:10.1016/j.jfoodeng.2009.02.001.
[28] 孙英杰. 超声波处理对大豆分离蛋白结构和功能性质影响研究[D].哈尔滨: 东北农业大学, 2014: 24-39.
[29] JIANG Lianzhou, WANG Jing, LI Yang, et al. Effects of ultrasound on the structure and physical properties of black bean protein isolates[J].Food Research International, 2014, 62(6): 595-601. DOI:10.1016/j.foodres.2014.04.022.
[30] LIU Y B, MARUVADA S, HERMAN B A, et al. Temperaturedependent physical properties of egg white for HIFU applications[J]. American Institute of Physics, 2012, 1481: 216-220.DOI:10.1063/1.4757337.
[31] 马美湖. 禽蛋蛋白质[M]. 北京: 科学出版社, 2016: 21-23.
[32] 汤虎. 超声波及琥珀酰化法改性小麦面筋蛋白的研究[D]. 武汉: 华中农业大学, 2008: 9-19.
[33] KARKI B, LAMSAL B P, GREWELL D, et al. Functional properties of soy protein isolates produced from ultrasonicated defatted soy flakes[J]. Journal of the American Oil Chemists Society, 2009, 86(10):1021-1028. DOI:10.1007/s11746-009-1433-0.
[34] ZHANG Qiuting, TU Zongcai, XIAO Hui, et al. Influence of ultrasonic treatment on the structure and emulsifying properties of peanut protein isolate[J]. Food and Bioproducts Processing, 2014, 92(1): 30-37.DOI:10.1016/j.fbp.2013.07.006.
[35] JAMBRAK A R, MASON T J, LELAS V, et al. Effect of ultrasound treatment on particle size and molecular weight of whey proteins[J].Journal of Food Engineering, 2014, 121(1): 15-23. DOI:10.1016/j.jfoodeng.2013.08.012.
[36] TANG C H, WANG X Y, YANG X Q, et al. Formation of soluble aggregates from insoluble commercial soy protein isolate by means of ultrasonic treatment and their gelling properties[J].Journal of Food Engineering, 2009, 92(4): 432-437. DOI:10.1016/j.jfoodeng.2008.12.017.
[37] 郭武汉, 关二旗, 卞科. 超微粉碎处理对小麦面筋蛋白性质的影响[J]. 中国粮油学报, 2017, 32(5): 13-18. DOI:10.3969/j.issn.1003-0174.2017.05.003.
[38] WANG X S, TANG C H, LI B S, et al. Effects of high-pressure treatment on some physicochemical and functional properties of soy protein isolates[J]. Food Hydrocolloids, 2008, 22(4): 560-567.DOI:10.1016/j.foodhyd.2007.01.027.
Effect of Ultrasonic Treatment on Instant Solubility of Egg White Powder