亚麻籽是一种在干旱和半干旱冷凉地区广泛种植和生产的油料植物,世界上常年有50 个国家出产亚麻籽,近年来总产量维持在260万 t左右。亚麻籽是一种植物油料,也是在很多国家或地区的食品法典中列入的食用油料,其主要可食用部分为亚麻籽油,因此亚麻籽目前最主要用途是压榨加工制取亚麻籽油。亚麻籽油是一种富含ω-3系列多不饱和脂肪酸α-亚麻酸的功能性油脂,其功能已有大量研究报道[1-7],并已获得广泛应用。亚麻籽压榨制油后副产物占亚麻籽质量60%~65%的亚麻饼是一种由亚麻籽蛋白、膳食纤维(其中包括纤维素和可溶性膳食纤维亚麻籽胶)、碳水化合物、残留亚麻籽油、亚麻木酚素(secoisolariciresinol diglucoside,SDG)和微量物质构成的混合物[8-9]。目前亚麻饼主要用于制备喂养动物的蛋白饲料,由于含有生氰糖苷毒素、抗VB6物质和较高含量不被动物消化利用的亚麻籽胶等[10-14],饲喂动物前需进行脱毒处理或只能以少量比例添加到饲料中,用途受到限制,且利用率不稳定,需要开展使其更富价值的利用途径研究。如何高效利用亚麻籽饼成为亚麻籽加工的研究热点,目前的研究集中在两个方面:第一是对其所具有的单一活性物质功能开展研究,重点是亚麻SDG,文献报道SDG具有抗氧化、清除自由基能力从而改善糖尿病和心脑血管疾病症状,在抗肿瘤方面也具有一定效果[15-22];第二是直接利用亚麻饼,主要是将其加工成部分脱脂亚麻籽粉(partially defatted flaxseed meal,PDFM)后进行功能研究,证实饮食中摄入一定比例PDFM,具有润肠通便、改善高脂饮食动物的血脂指标、提高动物体内抗氧化活性、增强动物生产能力等作用[23-28]。
糖尿病是全球威胁人类健康的三大慢性非传染性疾病之一,近年来中国糖尿病患病人数已稳居世界第一[29]。糖尿病与饮食结构具有极其紧密的关系,通过合理的饮食结构调整预防并控制糖尿病及其并发症发生、发展一直是科研关注方向之一。膳食纤维能够润肠通便、增加肠道内有益微生物、减少厌氧菌、产生饱腹感,对高血糖人群的血糖控制和肥胖人群的体质量控制具有一定帮助[30-31]。PDFM含有丰富的膳食纤维类物质亚麻纤维素、亚麻胶和SDG,但饮食摄入PDFM对血糖的影响鲜见报道;因此本实验以PDFM干预高脂高糖饲料饮食SD大鼠,通过检测血糖、糖化血红蛋白等指标,系统评估PDFM对实验动物血糖的影响,以期检验PDFM是否具有调节血糖的功能作用,从而为其用作健康功能产品开发提供基础性数据支持。
SPF级雄性SD大鼠54 只,体质量180~220 g,购自湖南斯莱克景达实验动物有限公司,许可证号:SCXK(湘)2009-0012。
亚麻籽购自甘肃金昌,为大粒黄色亚麻籽;猪油为实验室自制;AIN-93M饲料(玉米淀粉62%(质量分数,下同)、干酪素14%、蔗糖10%、纤维素5%、大豆油4%、复合盐3.5%、复合维生素1%、氯化胆碱0.2%、DL-蛋氨酸0.3%) 江苏美迪森生物医药有限公司;白砂糖 上海市糖业烟酒(集团)有限公司。
阿卡波糖片 拜耳医药保健有限公司;低密度脂蛋白胆固醇(low density lipoprotein cholesterol,LDL-C)试剂盒、高密度脂蛋白胆固醇(high density lipoprotein cholesterol,HDL-C)试剂盒、总甘油三酯(total triglyceride,TG)试剂盒、总胆固醇(total cholesterol,TC)试剂盒、糖化血红蛋白(hemoglobin A1c,HbA1c)试剂盒 北京利德曼生化股份有限公司;肝糖原试剂盒 南京建成生物工程研究所;血糖试纸罗氏制药有限公司。
超低温冰箱 青岛海尔特种冰柜有限公司;D-37520 Osterode台式冷冻离心机 美国Thermo公司;微型离心机 美国Beckman Coulter公司;ML303/02电子天平 瑞士Mettler Toledo公司;EnSpire酶标仪 美国PerkinElmer公司;血糖测试仪 罗氏制药有限公司;CA59G榨油机 德国Komet公司。
1.3.1 PDFM的制备方法
鉴于亚麻籽中含有较高含量的毒性物生氰糖苷,而研究报道微波处理是一种能够高效率脱除生氰糖苷的方法[32-34],为尽可能降低PDFM中的生氰糖苷含量,保证产品在动物饮食制品中的安全,本实验采用微波技术脱毒,PDFM生产方法如下:每次将清理除杂的400 g亚麻籽加水润湿并保存4 h,以800 W功率微波处理5 min,调水分至质量分数7%左右,经CA59G榨油机两次压榨得到亚麻饼,将亚麻饼用粉碎机粉碎,过60 目筛,取样检测其成分并密封保存备用。
1.3.2 动物分组及处理
将SD大鼠以常规饲料进行环境适应性喂养7 d后随机分为6 组,每组9 只,分别为正常对照组(饲喂AIN-93M饲料)、高糖高脂模型组(饲喂AIN-93M饲料65.5%(质量分数,下同)、猪油12%、白砂糖20%、胆固醇2%、胆酸钠0.5%)和PDFM低(高脂高糖组饲料95%、PDFM 5%)、中(高脂高糖组饲料90%、PDFM 10%)、高(高脂高糖组饲料80%、PDFM 20%)剂量组以及阳性治疗对照组(按每1 kg加阿卡波糖片0.15 g配制)。各组饲料均经膨化造粒制成颗粒饲料。每日记录摄食量,每周称体质量2 次。
喂养8 周后,将大鼠隔夜禁食,进行葡萄糖糖耐量实验。继续喂养1 d,隔夜禁食,用质量分数3%戊巴比妥钠麻醉、断头处死后,腹部解剖,用采血管采取腹部主动脉血液,静置1 h,4 000 r/min离心10 min后分离血清。取血完毕后,分别摘取肝脏、肾脏、胰腺、脾、腹部脂肪,用冷冻生理盐水冲洗后,滤纸吸干,电子天平称取各脏器湿质量。分离的血清和脏器均于-80 ℃保存备检。
1.3.3 理化指标、动物生理生化指标检测及计算
1)PDFM的水分、灰分、蛋白质、脂肪、膳食纤维、氰化物含量检测,分别参照GB 5009.3—2016《食品安全国家标准 食品中水分的测定》、GB 5009.4—2016《食品安全国家标准 食品中灰分的测定》、GB 5009.5—2016食品安全国家标准 食品中蛋白质的测定、GB 5009.6—2016《食品安全国家标准 食品中脂肪的测定》、GB 5009.88—2014《食品安全国家标准 食品中膳食纤维的测定》和GB 5009.36—2016《食品安全国家标准 食品中氰化物的测定》方法执行。碳水化合物质量按照GB/Z 21922—2008《食品营养成分基本术语定义》进行减量计算获得,即:食品总质量为100 g,减去蛋白质、脂肪、水分、灰分和膳食纤维的质量即为碳水化合物的质量。SDG参照臧茜茜等[35]的方法检测。
2)动物体质量增长率按式(1)计算。
式中:m0为初始体质量/g;m为最终体质量/g。
3)脏器指数按式(2)计算。
式中:mi为对应脏器湿质量/g;m为动物体质量/g。
4)空腹血糖值:断尾采尾血,采用血糖仪和血糖试纸条检测。
5)HbA1c、血清TC、TG、LDL-C、HDL-C浓度分别参照相应试剂盒说明书进行检测。
所有测定结果均以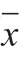 ±s表示,采用SPSS 16.0软件包对结果进行分析,组间用方差分析进行显著性检验,以P<0.05判断差异有统计学意义。
±s表示,采用SPSS 16.0软件包对结果进行分析,组间用方差分析进行显著性检验,以P<0.05判断差异有统计学意义。
经检测,PDFM主要成分包括:水分8.07%(质量分数,下同)、总灰分6.0%、膳食纤维40.1%、油脂5.0%、蛋白质34.1%、碳水化合物6.7%、SDG 28.8 mg/g、生氰糖苷6.80 mg/kg。从生氰糖苷检测结果上看,低于主要含有这类毒性物食品原料的控制指标值,如食用木薯淀粉控制生氰糖苷含量(以HCN计)指标为10 mg/kg以下,本实验所得的实验材料PDFM生氰糖苷含量为6.80 mg/kg,初步认为对摄食动物是安全的。这也说明所采用的微波处理方法达到了脱毒目的。膳食纤维这种认为能产生饱腹感、不能被胃肠道消化吸收但具有增加肠蠕动、控制能量吸收的物质质量分数高达40.1%。研究认为SDG这种具有生理活性物质的含量为28.8 mg/g。
动态观察动物生长情况,正常对照组大鼠营养状态良好、食欲佳,活动正常,饮水饮食规律,大便状态正常;高糖高脂模型组大鼠大便较稀、腥臭,饮水量大,易怒好斗,精神萎靡,后期出现明显的多食、多饮和多尿等症状;阳性治疗对照组(阿卡波糖组),摄食量减少,活动正常;添加PDFM各组,生长都正常,大便形态也正常。实验期间各组均未出现实验动物非正常死亡。
动物解剖观察,除正常对照组外,其他各组均出现一定程度脂肪肝,这是高脂高糖食物饲喂动物的一种普遍现象。重点观察添加PDFM各组,未出现动物内脏损伤情况,说明PDFM在所添加的剂量范围内对动物是安全的。
表1 PDFM对大鼠体质量的影响(n=9)
Table1 Effect of PDFM on body mass of rats (n= 9)
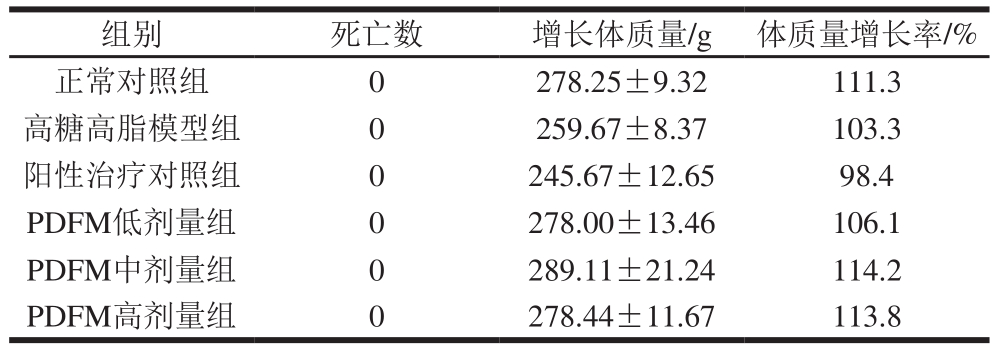
组别 死亡数 增长体质量/g 体质量增长率/%正常对照组 0 278.25±9.32 111.3高糖高脂模型组 0 259.67±8.37 103.3阳性治疗对照组 0 245.67±12.65 98.4 PDFM低剂量组 0 278.00±13.46 106.1 PDFM中剂量组 0 289.11±21.24 114.2 PDFM高剂量组 0 278.44±11.67 113.8
各组大鼠因是随机分组,初始体质量基本一致。通过体质量监测,经8 周喂养后,大鼠体质量增加值见表1。PDFM中剂量组大鼠体质量最大,增长率最高;PDFM高剂量组与正常对照组大鼠增长率其次,且相差不大;阳性治疗对照组体质量增长率较低,可能是因为动物对高脂高糖饲料口感不适应,加之药物阿卡波糖的作用,摄食量减少,而添加PDFM显著改善高脂高糖饲料适口性,体质量增长与高脂高糖模型组和阳性治疗对照组都无显著性差异(P>0.05)。
表2 PDFM对大鼠空腹血糖及糖耐量的影响(n=9)
Table2 Effect of PDFM on fasting blood glucose of rats (n = 9)mmol/L

注:a.正常对照组、各剂量组与高糖高脂模型组相比差异显著(P<0.05);b.正常对照组、各剂量组与阳性治疗对照组相比差异显著(P<0.05)。
组别 0 min 15 min 30 min 60 min 120 min正常对照组 4.46±0.13a8.73±1.05 9.03±21.38 7.34±0.56 5.93±0.44高糖高脂模型组 7.15±1.22 13.2±2.09 12.78±1.53 11.08±2.74 8.10±1.26阳性治疗对照组 5.14±0.33 9.45±1.27 8.51±1.36 7.21±2.01 6.04±0.55 PDFM低剂量组 6.34±0.48ab10.80±1.72 10.16±2.03 9.65±1.45 6.88±0.69 PDFM中剂量组 5.82±0.36a9.83±1.27 9.87±2.05 6.64±0.66 6.29±0.40 PDFM高剂量组 5.03±0.32a10.30±1.68 8.99±1.90 7.12±1.35 6.57±0.95
由表2可知,按照实验动物空腹血糖值超过7.0 mmol/L为糖尿病判定标准,本实验高糖高脂模型组大鼠血清空腹血糖值为(7.15±1.22)mmol/L,其中空腹血糖值超过7.0 mmol/L大鼠数量比例为5/9,明显高于正常对照组大鼠空腹血糖值(4.46±0.13)mmol/L,说明高脂高糖饮食加速诱导动物患糖尿病的模型造模获得成功。从0、15、30、60、120 min动态监测大鼠尾血血糖数据来看,各组大鼠腹部注射葡萄糖后0~15 min空腹血糖值急剧升高达到峰值,然后随着时间延长血糖值下降,高糖高脂模型组各个时间阶段的空腹血糖值都高于其他组,PDFM低、中、高剂量组大鼠空腹血糖值与剂量呈负相关关系,其中PDFM低剂量组已有动物空腹血糖值超过7.0 mmol/L的情况,数量比例为1/9,实验结果说明PDFM具有显著抑制血糖升高作用,但低剂量PDFM抑制血糖升高的活性较低,要达到一定的抑制血糖升高的活性,需要给予合适的剂量。
HbA1c是血液中红细胞内的血红蛋白与血糖结合的产物,HbA1c越高表示血糖与血红蛋白结合越多,糖尿病病情也越重。HbA1c在糖尿病监测中有重要意义,与血糖值呈正相关,血糖值越高,HbA1c就越高,所以能反映血糖控制水平。因为生成缓慢,短暂的血糖值升高不会引起HbA1c的升高,但一旦生成不易分解,所以HbA1c不能反映短期内的血糖波动,但却能很好地反映较长时间的血糖控制情况,并反映出平均血糖水平。
表3 PDFM对HbA1c和肝糖原浓度的影响(n=9)
Table3 Effects of PDFM on HbA1c and liver glycogen contents of rats (n= 9)

注:a.各剂量组与高糖高脂模型组相比差异显著(P<0.05);b.各剂量组与阳性治疗对照组相比差异显著(P<0.05)。下同。
肝糖原浓度/(mmol/L)正常对照组 169.25±10.88 8.75±1.68高糖高脂模型组 200.78±11.48 2.65±0.34阳性治疗对照组 173.67±7.77 4.34±0.69 PDFM低剂量组 193.75±10.89 3.27±0.55aPDFM中剂量组 168.89±13.74a3.98±0.72aPDFM高剂量组 159.5±11.99a4.16±0.84a组别 HbA1c浓度/(μmol/L)
由表3可知,添加中、高剂量PDFM到饲料中,明显抑制了动物血液HbA1c浓度升高,达到并超过阳性治疗对照组抑制HbA1c浓度升高的效果。机体血糖主要是通过神经、肝脏和激素对血糖的调节作用,从而使其保持在一个 比较稳定的范围内。合成肝糖原是血糖的消耗途径之一,肝糖原与血糖值呈负相关,当肝糖原增加时,血糖值下降,反之肝糖原分解增加时,血糖值上升。本实验中高脂高糖模型组肝糖原浓度最低,为(2.65±0.34)mmol/L,与高糖高脂模型组比较,PDFM中、高剂量组和阳性治疗对照组肝糖原浓度明显增加。PDFM具有增加肝糖原合成、减少肝糖原分解的作用。
比较稳定的范围内。合成肝糖原是血糖的消耗途径之一,肝糖原与血糖值呈负相关,当肝糖原增加时,血糖值下降,反之肝糖原分解增加时,血糖值上升。本实验中高脂高糖模型组肝糖原浓度最低,为(2.65±0.34)mmol/L,与高糖高脂模型组比较,PDFM中、高剂量组和阳性治疗对照组肝糖原浓度明显增加。PDFM具有增加肝糖原合成、减少肝糖原分解的作用。
本实验对血脂和脏器指数检验是附带检验,主要是观察高脂高糖饮食以及采用PDFM干预对动物血脂和一些脏器的影响,观察这些指标与血糖变化的相关性。
表 4 PDFM对血清TG、TC、HDL-C、LDL-C浓度的影响(n=9)
Table4 Effects of PDFM on serum TG, TC, HDL-C and LDL-C of rats (n= 9)mmol/L

组别 TG浓度 TC浓度 HDL-C浓度 LDL-C浓度正常对照组 0.38±0.05 1.99±0.11 1.38±0.08 0.26±0.03高糖高脂模型组 0.65±0.06 2.93±0.12 1.36±0.04 0.82±0.07阳性治疗对照组 0.37±0.06 2.63±0.07 1.57±0.04 0.67±0.08 PDFM低剂量组 0.60±0.07ab2.49±0.14ab1.48±0.06 0.64±0.10aPDFM中剂量组 0.53±0.06ab2.28±0.13ab1.28±0.05 0.54±0.05abPDFM高剂量组 0.44±0.07a2.44±0.20ab1.39±0.09 0.53±0.08ab
由表4可知,与正常对照组相比较,长期高脂高糖饮食导致动物脂质代谢紊乱,大鼠血液中TG和TC显著升高。与高脂高糖模型组比较,在高脂高糖饲料中添加PDFM进行干预,对动物血脂升高具有显著的抑制作用,且呈现出非常明显的剂量效应关系,PDFM添加比例越高,动物血浆TG、TC和LDL-C浓度就越低,而对HDL-C浓度的影响则高低不一致。
由表5可知,与正常对照组比较,采用高脂高糖饲料喂养动物,各组动物的腹部脂肪指数、肝脏指数都有升高,差异显著(P<0.05)。与阳性治疗对照组比较,PDFM中、高剂量组肝脏指数和腹部脂肪指数均有显著差异(P<0.05)。腹部脂肪指数越大反映大鼠肥胖体质越明显,肝脏指数一定程度上反映肝脏肿大程度,说明中、高剂量PDFM的干预具有一定的抑制动物向肥胖和脂肪肝发展的作用。各组之间胰指数差异不显著(P>0.05)。
表5 PDFM对大鼠各脏器指数的影响(n=9)
Table5 Effects of PDFM on organ indexes of rats (n= 9)%
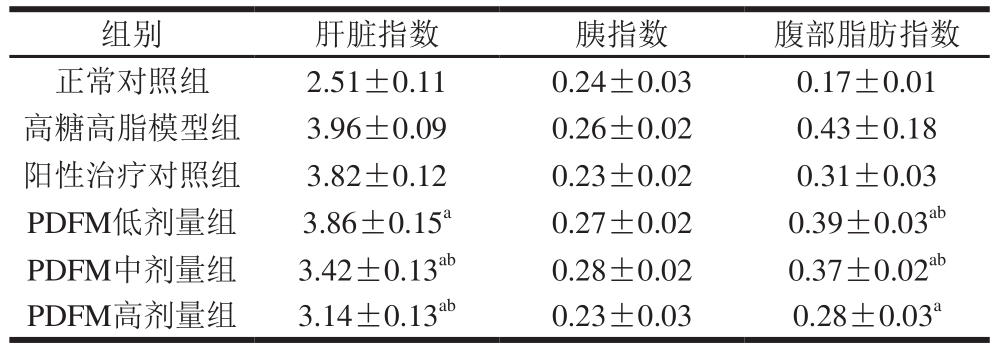
组别 肝脏指数 胰指数 腹部脂肪指数正常对照组 2.51±0.11 0.24±0.03 0.17±0.01高糖高脂模型组 3.96±0.09 0.26±0.02 0.43±0.18阳性治疗对照组 3.82±0.12 0.23±0.02 0.31±0.03 PDFM低剂量组 3.86±0.15a0.27±0.02 0.39±0.03abPDFM中剂量组 3.42±0.13ab0.28±0.02 0.37±0.02abPDFM高剂量组 3.14±0.13ab0.23±0.03 0.28±0.03a
综上可知,PDFM在抑制血脂升高、动物肥胖及脂肪肝方面的表现与抑制血糖升高方面具有一致性。
将微波处理亚麻籽生产的PDFM添加于动物饲料饲喂动物,实验动物生长发育正常,未出现急性和慢性中毒症状,无实验动物异常死亡情况发生,动物解剖未观察到内脏损伤,说明PDFM在所采用的剂量范围内是安全的。高脂高糖饲料组与正常对照组的动物空腹血糖值、HbA1c浓度升高显著(P<0.05),形成高脂高糖饮食诱导的大鼠高血糖糖尿病模型,而在高脂高糖饲料中添加PDFM干预后,中、高剂量PDFM组空腹血糖值和HbA1c浓度显著低于高脂高糖饲料组(P<0.05),从PDFM添加量不同动物的空腹血糖值、HbA1c浓度变化看出,抑制动物血糖升高的效果与PDFM添加量之间存在剂量-效应关系。中、高剂量PDFM组的血糖和HbA1c水平与添加常用糖尿病治疗药物阿卡波糖的阳性治疗对照组没有显著性差异(P>0.05),但从水平数值上看,PDFM达到甚至好于阿卡波糖抑制血糖升高的效果。同时通过检测发现PDFM对动物血脂、肝脏指数、腹部脂肪指数等升高也具有明显抑制作用。
实验所采用的PDFM是一种由亚麻籽蛋白、膳食纤维(包括纤维素和亚麻籽胶)、碳水化合物、残留的亚麻籽油、SDG等组成的复混体系,既具备食品原料的基本要素,又具有膳食纤维和SDG含量高的显著特点,动物实验检验PDFM对高脂高糖饮食动物血糖升高具有显著的抑制作用,具备成为辅助降血糖功能食品原料的潜力。本实验将为进一步开展PDFM深度开发利用提供科研数据支持。
[1] VIJAIMOHAN K, JAINU M, SABITHA K E, et al. Beneficial effects of alpha linolenic acid rich flaxseed oil on growth performance and hepatic cholesterol metabolism in high fat diet fed rats[J]. Life Sciences, 2006, 79(5): 448-454. DOI:10.1016/j.lfs.2006.01.025.
[2] BARCELÓ-COBLIJN G, MURPHY E J. Alpha-linolenic acid and its conversion to longer chain n-3 fatty acids: benefits for human health and a role in maintaining tissue n-3 fatty acid levels[J].Progress in Lipid Research, 2009, 48(6): 355-374. DOI:10.1016/j.plipres.2009.07.002.
[3] 黄庆德, 刘列刚, 郭萍梅, 等. 亚麻籽油降脂作用的实验研究[J]. 食品科学, 2004, 25(3): 162-165.
[4] NESTEL P J, POMEROY S E, SASAHARA T, et al. Arterial compliance in obese subjects is improved with dietary plant n-3 fatty acid from flaxseed oil despite increased LDL oxidizability[J].Arteriosclerosis Thrombosis and Vascular Biology, 1997, 17(6): 1163-1170. DOI:10.1161/01.ATV.17.6.1163.
[5] 谢华, 徐丹凤, 陈艳秋, 等. 亚麻籽油对高脂诱导肥胖小鼠血糖和胰升血糖素样肽-1分泌影响的研究[J]. 中国糖尿病杂志, 2015, 23(4):356-359.
[6] 杨野仝, 张桂英, 刘雅娟, 等. 亚麻籽油对糖尿病大鼠辅助降血糖功能的研究[J]. 安徽农业科学, 2015, 43(9): 22-23; 45. DOI:10.13989/j.cnki.0517-6611.2015.09.134.
[7] 邓乾春, 禹晓, 黄庆德, 等. 亚麻籽油的营养特性研究进展[J]. 天然产物研究与开发, 2010, 22(4): 715-721. DOI:10.16333/j.1001-6880.2010.04.018.
[8] 赵艺, 田立波. 亚麻饼营养价值评定及其应用的研究[J]. 当代畜牧,1997(2): 26-28.
[9] THOMPSON L U, BOUCHER B A, LIU Z, et al. Phytoestrogen content of foods consumed in Canada, including isoflavones, lignans,and coumestan[J]. Nutrition and Cancer, 2006, 54(2): 184-201.DOI:10.1207/s15327914nc5402_5.
[10] 周青娥, 彭大惠. 亚麻饼中氢氰酸与粗蛋白质含量的探讨[J]. 饲料研究, 1987(12): 16-18.
[11] 周小洁, 车向荣, 于霏. 亚麻籽及其饼粕的营养学和毒理学研究进展[J]. 饲料工业, 2005, 26(19): 46-50.
[12] 张忠军, 赵金根, 闫江林. 绵羊亚麻籽饼中毒病例[J]. 中国兽医杂志,2006, 42(11): 59.
[13] 吴桂瑞. 亚麻饼引起产蛋鸭大量死亡[J]. 饲料研究, 1994(12): 29-30.[14] 孔庆雷, 唐咏琴, 邢锦珊. 亚麻籽饼对鸡的毒性实验[J]. 草与畜杂志,1989(2): 17-19.
[15] PRASAD K. Oxidative stress as a mechanism of diabetes in diabetic BB prone rats: effect of secoisolariciresinol diglucoside (SDG)[J].Molecular and Cellular Biochemistry, 2000, 209(1/2): 89-96.DOI:10.1023/A:1007079802459.
[16] KITTS D D, YUAN Y V, WIJEWICKREME A N, et al. Antioxidant activity of the flaxseed lignin secoisolariciresinol diglycoside and its mammalian lignan metabolites enterodiol and enterolactone[J].Molecular and Cellular Biochemistry, 1999, 202(1): 91-100.DOI:10.1023/A:1007022329660.
[17] MOREE S S, RAJESHA J. Investigation of in vitro and in vivo antioxidant potential of secoisolariciresinol diglucoside[J]. Molecular and Cellular Biochemistry, 2013, 373(1/2): 179-187. DOI:10.1007/s11010-012-1487-4.
[18] THOMPSON L U, SEIDL M M, RICKARD S E, et al.Antitumorigenic effect of amammalian lignan precursor from flaxseed[J]. Nutrition and Cancer, 1996, 26(2): 159-165.DOI:10.1080/01635589609514472.
[19] 刘珊, 王小兵, 李爱东, 等. 亚麻籽木酚素预防乳腺癌及与雌激素的关系[J]. 中国比较医学杂志, 2012, 22(6): 43-47; 88.
[20] WESTEOTT N D, MUIR A D. Flax seed lignan in desease prevention and health promotion[J]. Phytochemitry Reviews, 2003, 2(3): 401-417.DOI:10.1023/B:PHYT.0000046174.97809.b6.
[21] PRASAD K. Secoisolariciresinol diglucoside from flaxseed delays the development of type 2 diabetes in Zucker rat[J]. Journal of Laboratory and Clinical Medicine, 2001, 138(1): 32-39. DOI:10.1067/mlc.2001.115717.
[22] PRASAD K. Hydroxyl radical-scavenging property of secoisolariciresinol diglucoside (SDG) isolated from flax-seed[J].Molecular and Cellular Biochemistry, 1997, 168(1/2): 117-123.DOI:10.1023/A:1006847310741.
[23] XU J Q, ZHOU X Q, CHEN C, et al. Laxative effects of partially defatted flaxseed meal on normal and experimental constipated mice[J]. BMC Complementary and Alternative Medicine, 2012, 12(1):1-5. DOI:10.1186/1472-6882-12-14.
[24] JENKINS D J A, KENDALL C W C, VIDGEN E, et al. Health aspects of partially defatted flaxseed, including effects on serum lipids,oxidative measures, and ex vivo androgen and progestin activity:a controlled crossover trial[J]. The American Journal of Clinical Nutrition, 1999, 69(3): 395-402.
[25] SANO T, ODA E, YAMASHITA T, et al. Antithrombic and antiatherogenic effects of partially defatted flaxseed meal using a laser-induced thrombosis test in apolipoprotein E and low-density lipoprotein receptor deficient mice[J]. Blood Coagulation Fibrinolysis,2003, 14(8): 707-712. DOI:10.1097/00001721-200312000-00003.
[26] COLLINS T F X, SPRANDO R L, BLACK T N, et al. Effects of flaxseed and defatted flaxseed meal on reproduction and development in rats[J]. Food and Chemical Toxicology, 2003, 41(6): 819-834.DOI:10.1016/S0278-6915(03)00033-4.
[27] 曹伟伟, 黄庆德, 邓乾春. 亚麻籽粉食品的开发利用研究进展[J]. 食品研究与开发, 2017, 38(7): 200-205.
[28] 曹伟伟, 黄庆德, 田光晶, 等. 脱毒亚麻饼粉对馒头品质的影响[J]. 现代食品科技, 2016, 32(11): 190-196. DOI:10.13982/j.mfst.1673-9078.2016.11.029.
[29] 廖涌. 中国糖尿病的流行病学现状及展望[J]. 重庆医科大学学报,2015, 40(7): 1042-1045. DOI:10.13406/j.cnki.cyxb.000693.
[30] 游太空, 陈自然. 膳食纤维与疾病的关系[J]. 内江师范学院学报,2011, 26(10): 45-49.
[31] WHISTLER R L, BEMILLER N. Industrial gums[M]. New York:Academic Press, 1993: 232-235.
[32] 赵春, 许继取, 黄庆德, 等. 亚麻籽饼对饲喂高脂日粮大鼠血浆中脂质及氧化应激改善作用的研究[J]. 中国油脂, 2015, 40(30): 36-39.
[33] 杨宏志, 毛志怀. 不同处理方法降低亚麻籽中氰化氢含量的效果[J].中国农业大学学报, 2004, 9(6): 65-67.
[34] 李次力, 缪铭. 亚麻籽粕不同脱毒方法的比较研究[J]. 食品科学,2006, 27(12): 280-282.
[35] 臧茜茜, 魏晓珊, 陈鹏, 等. 不同品种亚麻籽木酚素多聚体水解物的组成及含量[J]. 中国油料作物学报, 2017, 39(2): 253-259.DOI:10.7505/j.issn.1007-9084.2017.02.017.
Effect of Partially Defatted Flaxseed Meal on Blood Glucose in Rats Fed with High-Fat High-Sugar Diet