
鱼油是n-3系列不饱和脂肪酸的主要来源,其对人体健康和疾病预防方面的作用在多年前就已被验证,尤其以二十碳五烯酸(eicosapentaenoic acid,EPA)和二十二碳六烯酸(docosahexaenoic acid,DHA)的生理活性最为突出[1]。EPA与DHA仅存在于水产品中,对增强人体神经系统、生殖系统及视觉的功能有着重要作用[2-3]。然而,n-3系列不饱和脂肪酸极易被氧化,导致鱼油中营养成分流失并产生难闻的腥臭异味[4]。故鱼油品质与n-3系列不饱和脂肪酸含量及抗氧化稳定性密切相关,且光线、温度、空气及金属离子等外界环境的变化都会加速其氧化[5]。
目前,国内外学者对油脂抗氧化稳定性及其品质变化研究较多。Fontagné等[6]将鱼油在50 ℃下鼓风氧化48 h后,并测定其过氧化值,以模拟鱼油动态变化规律;结果表明,过氧化值随氧化时间的延长而显著升高(P<0.05)。吕军伟[7]通过将DHA藻油置于(60±1)℃的烘箱中存放12 d,并定期测定藻油的过氧化值、硫代巴比妥酸值及藻油中DHA残留率,以研究DHA藻油的抗氧化稳定性。然而目前对鱼油在贮藏期品质变化规律的研究较少,尤其是对在不同贮藏温度下其稳定性变化的研究更少。考虑到实际生活中食品的贮藏条件,本实验选定35、25、15、5 ℃为温度梯度进行研究,通过将粗鱼油与精制鱼油分别置于不同温度条件下,定期检测其理化指标(酸价、过氧化值与茴香胺值)、脂肪酸组成及挥发性风味的变化,探究其在贮藏期品质变化规律,为提高贮藏稳定性和延长货架期提供参考。
粗制鱼油(由金枪鱼与鳀鱼加工下脚料提炼制得)购于浙江舟山奥旭鱼油制品有限公司。
脂肪酸甲酯(标准品) 美国Sigma公司;其他试剂均购于西陇化工股份有限公司。
50/30 μm二乙烯基苯/碳分子筛/聚二甲基硅氧烷(divinylbenzene/carboxen/polydimethylsiloxane,DVB/CAR/PDMS)涂层萃取头 美国Supelco公司;7890A气相色谱(gas chromatography,GC)仪 美国Agilent公司;Trace GC Ultra GC仪、DSQ II质谱(mass spectrometry,MS)仪 美国Thermo Fisher Scientif i c公司;ROTINA 420R离心机 德国Hettich科学仪器公司;LRH-150-S恒温恒湿培养箱 广东省医疗器械厂。
1.3.1 样品处理
粗制鱼油经脱胶、脱酸、脱色和脱臭工艺[8-11]处理制得精制鱼油。(主要工艺参数如下:酸法脱胶,体积分数85%磷酸,添加量为油质量的1%;碱法脱酸,约20 g/100 mL NaOH溶液,添加量(m/g)与样品酸价有关(具体关系见式(1)~(3));吸附脱色,活性白土用量约为油质量的10%;真空脱臭)。并将粗制鱼油与精制鱼油分装于200 mL带盖玻璃瓶中,各4 瓶,分别置于35、25、15、5 ℃恒温箱中贮藏120 d。每隔15 d取样测定样品酸价、过氧化值、茴香胺值;每隔30 d取样测定脂肪酸组成及挥发性风味成分的变化。为防止促进鱼油氧化,取样时动作尽量快速。

1.3.2 酸价的测定
参考GB 5009.229—2016《食品安全国家标准 食品中酸价的测定》[12]中的冷溶剂指示剂滴定法测定酸价。
1.3.3 过氧化值的测定
参考GB 5009.227—2016《食品安全国家标准 食品中过氧化值的测定》[13]中的滴定法测定过氧化值。
1.3.4 茴香胺值的测定
参考GB/T 24304—2009《动植物油脂 茴香胺值的测定》[14]中的方法测定茴香胺值。
1.3.5 脂肪酸组成分析
1.3.5.1 鱼油甲酯化
称取0.1 g鱼油样品于具塞试管中,加入2 mL 0.5 mol/L的NaOH-CH3OH溶液,充分摇匀,65 ℃水浴加热30 min,取出后自然冷却,再加入2 mL 体积分数15% BF3-CH3OH溶液,充分摇匀,65 ℃水浴加热3 min,取出后自然冷却,加入2 mL正己烷提取,同时加入2 mL饱和NaCl溶液水洗,静置分层,取上层清液并加入1/10体积的无水Na2SO4去除溶液中痕量的水,将处理好的上层清液过有机相滤膜后用GC仪进行脂肪酸相对含量测定[15]。
1.3.5.2 GC检测
GC检测条件:HP-88氰丙基色谱柱(30 m×0.25 mm,0.20 μm);载气:H2;不分流进样;进样量1 μL;检测温度220 ℃;程序升温:起始柱温设定为70 ℃,以15 ℃/min升至120 ℃,保持1 min,再以5 ℃/min升至175 ℃,保持10 min;最后以5 ℃/min升至220 ℃,保持5 min。
1.3.6 挥发性风味物质测定
1.3.6.1 固相微萃取条件
称取5 g样品置于15 mL顶空进样瓶中,60 ℃下平衡10 min,并将老化好的50/30 μm DVB/CAR/PDMS涂层萃取头插入进样瓶顶空部分,60 ℃下吸附30 min,取出后插入GC进样口,250 ℃解吸3 min。
1.3.6.2 GC-MS检测条件
GC条件:色谱柱为TR-35 MS(30 m×0.25 mm,0.25 μm);载气:高纯氦气;进样口温度250 ℃,不分流进样;升温程序:初始温度40 ℃,保持3 min,以5 ℃/min升至90 ℃,再以10 ℃/min升至230 ℃,保持7 min。
MS条件:离子源温度200 ℃;电子离子源;电子能量70 eV;传输线温度250 ℃;检测器温度280 ℃;质量扫描范围m/z 30~500。
实验数据定性分析时,通过NIST 2.0谱库做自动检索确认定性,且仅当正反匹配度(SI/RSI)均大于800(最大值为1 000)的鉴定结果才予以保留。定量分析时采用峰面积归一化法求得各挥发性成分在样品中的相对含量[16],测定数据以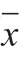 ±s表示。采用SPSS 21.0软件Duncan检验对脂肪酸相对含量的各组数据进行显著性分析,P<0.05表示有显著性差异。
±s表示。采用SPSS 21.0软件Duncan检验对脂肪酸相对含量的各组数据进行显著性分析,P<0.05表示有显著性差异。
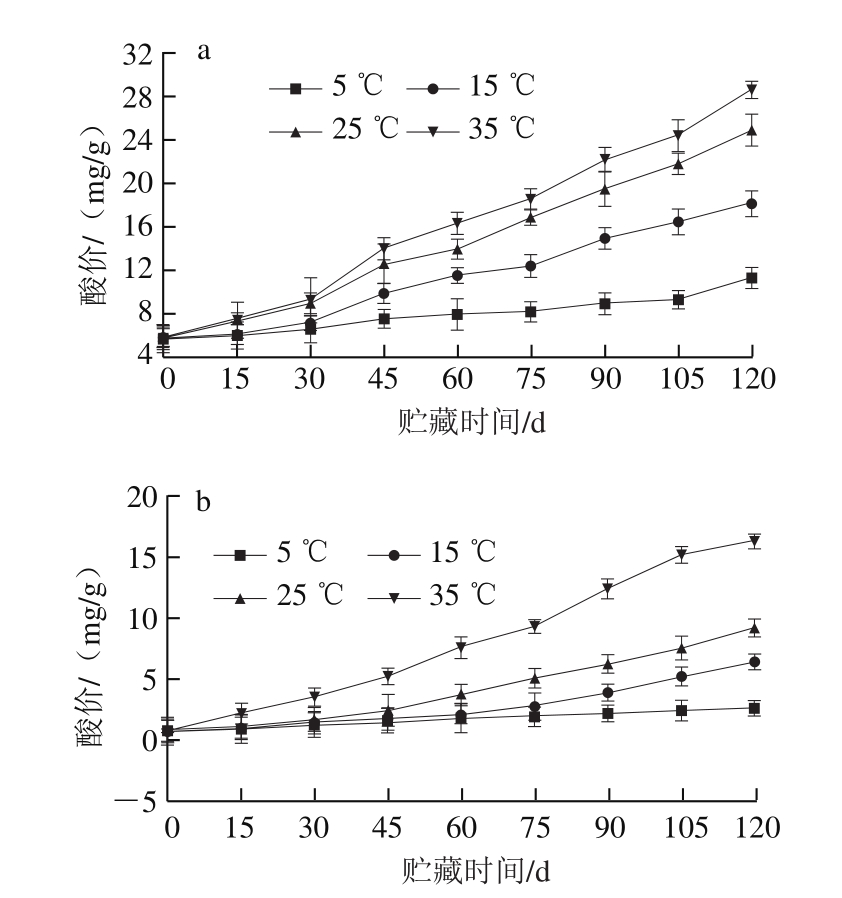
图1 粗制鱼油(a)和精制鱼油(b)在贮藏过程中的酸价变化
Fig.1 Changesin acid values of crude (a) and refined (b) fish oil over time at different temperatures
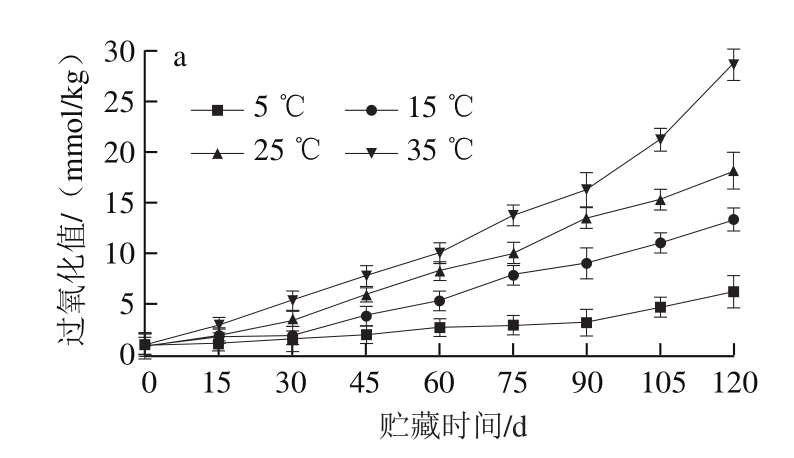
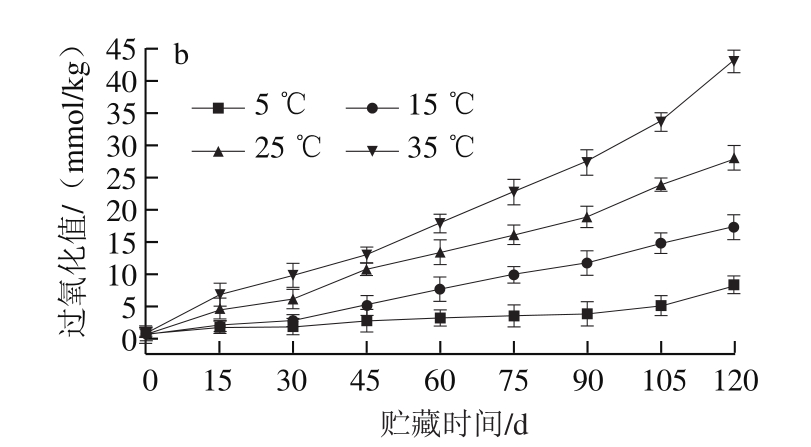
图2 粗制鱼油(a)和精制鱼油(b)在贮藏过程中的过氧化值变化
Fig.2 Changes in peroxide values of crude (a) and refined (b) fish oilover time at different temperatures
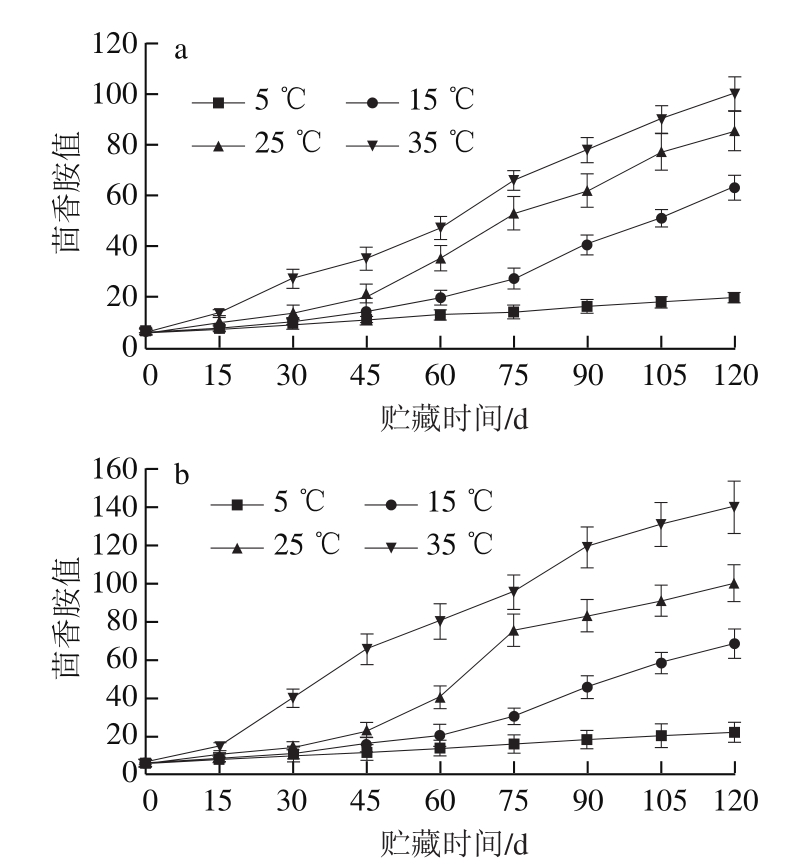
图3 粗制鱼油(a)和精制鱼油(b)在贮藏过程中茴香胺值的变化
Fig.3 Changes in anisidine values of crude (a) and refined (b) fish oil over time at different temperatures
由图1~3可知,在贮藏期内,酸价、过氧化值、茴香胺值均显著升高,且相同温度条件下,粗制鱼油与精制鱼油间也存在较大差异。粗制鱼油初始酸价为5.79 mg/g,过氧化值为0.98 mmol/kg,茴香胺值为6.18。经精制处理后,大量游离脂肪酸、色素、部分脂类及挥发性成分等杂质被有效清除[17],使鱼油品质得到有效提升。该精制鱼油初始酸价为0.65 mg/g,过氧化值为0.75 mmol/kg,茴香胺值为5.02。
在贮藏初期,分别置于35、25、15、5 ℃恒温箱中的粗制鱼油与精制鱼油,其酸价、过氧化值及茴香胺值变化均不大,此时鱼油正处于氧化诱导阶段,稳定性较好[18]。随贮藏时间的延长,酸价、过氧化值和茴香胺值逐渐增大,且温度越高,增幅越明显,氧化作用越显著。
酸价的高低与鱼油中游离脂肪酸含量多少密切相关[19]。氧化作用导致油脂中酯键断裂而产生大量游离脂肪酸,故鱼油酸价升高。在35℃条件下,贮藏120 d时,粗制鱼油酸价高达28.58 mg/g,远高于精制鱼油。董小林等[20]研究发现,将鱼油分别敞口置于室温、30、45、60、100 ℃条件下贮藏56 d,在100 ℃条件下酸价变化最为显著,初始时(0 d)其酸价为0.38 mg/g,贮藏56 d后,酸价上升至22.24 mg/g。而在本实验中,鱼油均加盖贮藏,具有良好的气密性,且每次尽量快速取样以避免鱼油氧化。故在整个贮藏期间,鱼油酸价变化不是特别大。
过氧化值是判断鱼油品质优劣的重要指标,其主要反映鱼油中氢过氧化物的含量。氢过氧化物是油脂氧化产生的初级氧化产物。随温度升高,鱼油氧化作用加剧,过氧化值变化更显著;这是由于温度对甘油三酯及其他物质的异构化、分解等有一定的诱导作用,且温度越高,诱导速率越快[21]。在鱼油氧化过程中,氢过氧化物的分解速率与其生成速率之间的关系也会影响过氧化值的变化规律。另外,氢过氧化物能被进一步分解成小分子酮、醛类等次级氧化产物。
茴香胺值可表征油脂中醛、酮、醌等次级氧化产物含量的多少,主要表示油脂中醛类化合物的含量[22-23]。在贮藏期间,鱼油茴香胺值的变化规律与过氧化值相似。在贮藏后期,在35 ℃条件下鱼油茴香胺值的增长速率有所减缓,此现象在精制鱼油中更为明显,这与鱼油中具有挥发性的次级氧化产物含量减少有关[24]。
此外,经对比分析在不同贮藏温度条件下粗制鱼油与精制鱼油酸价、过氧化值及茴香胺值的变化规律,发现精制鱼油的贮藏稳定性较差,更易受环境条件影响,品质破坏严重。这可能是由于精制过程中,在去除鱼油中有害杂质的同时也将部分抗氧化活性成分带走,导致鱼油自身抗氧化能力下降[25-26]。
根据鱼油行业标准SC/T 3502—2016《中华人民共和国水产行业标准 鱼油》[27],以酸价和过氧化值作为一级鱼油是否变质的评判标准。一级与二级鱼油理化指标的规定标准如表1所示。
表1 鱼油理化指标[27]
Table1 Physicochemical characteristics of fish oil[27]
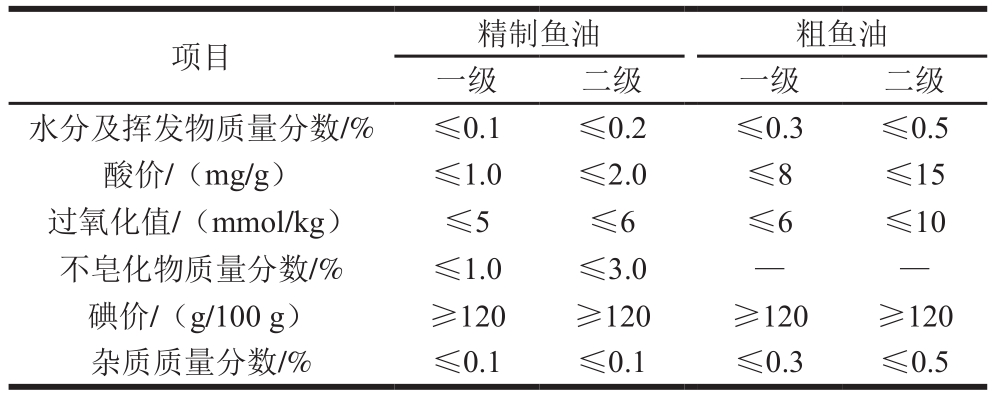
注:—.无明确规定。
项目 精制鱼油 粗鱼油一级 二级 一级 二级水分及挥发物质量分数/% ≤0.1 ≤0.2 ≤0.3 ≤0.5酸价/(mg/g) ≤1.0 ≤2.0 ≤8 ≤15过氧化值/(mmol/kg) ≤5 ≤6 ≤6 ≤10不皂化物质量分数/% ≤1.0 ≤3.0 — —碘价/(g/100 g) ≥120 ≥120 ≥120 ≥120杂质质量分数/% ≤0.1 ≤0.1 ≤0.3 ≤0.5
精制鱼油初始酸价为0.65 mg/g,过氧化值为0.75 mmol/kg;粗制鱼油初始酸价为5.79 mg/g,过氧化值为0.98 mmol/kg,均达到一级标准。参照上述标准可知:35 ℃时精制鱼油的保质期约为20 d,粗制鱼油约为40 d;25 ℃时精制鱼油的保质期约为40 d,粗制鱼油约为65 d;15 ℃时精制鱼油的保质期约为65 d,粗制鱼油约为80 d;5 ℃时精制鱼油的保质期约为115 d,而粗制鱼油在120 d贮藏期内未变质。
在整个贮藏期间,鱼油中饱和脂肪酸(saturated fatty acid,SFA)总含量增加,不饱和脂肪酸(unsaturated fatty acid,UFA)总含量降低,使整体不饱和度下降。鱼油中主要脂肪酸有肉豆蔻(C14∶0)、十五酸(C15∶0)、棕榈酸(C16∶0)、十七酸(C17∶0)、十七碳一烯酸(C17∶0)、硬脂酸(C18∶0)、油酸(C18∶1)、亚油酸(C18∶2cis)、花生四烯酸(C20∶4)、EPA和DHA[28]。由表2可知,在35 ℃条件下,鱼油主要脂肪酸相对含量变化最为显著。贮藏后,粗制鱼油与精制鱼油中SFA总量分别增加了20.99%和30.81%,单不饱和脂肪酸(monounsaturated fatty acid,MUFA)总量分别增加了19.94%和19.30%,而多不饱和脂肪酸(polyunsaturated fatty acid,PUFA)总量则分别下降了46.15%和47.46%,其中EPA与DHA总量分别减少了36.60%和36.62%。鱼油中PUFA较MUFA更易被氧化,其减少速率比MUFA快,而MUFA氧化成为SFA的速率又相对较慢,故使得MUFA占比增大。该结果与李文佳[18]研究的鱼油贮藏过程中脂肪酸变化的趋势相接近,即整个贮藏过程中,鱼油中饱和脂肪酸总量增加而导致整体不饱和度下降。此外,精制鱼油稳定性更差,这与其理化指标的变化规律相一致。由表3~5可知,随着贮藏温度的降低,鱼油中脂肪酸相对含量变化不大。故低温条件能有效保护鱼油品质,延长贮藏期。
表2 35 ℃贮藏条件下粗制鱼油与精制鱼油在贮藏过程中主要脂肪酸相对含量的变化
Table2 Changes in relative contents of main fatty acids in crude and refined fish oil over time at 35 ℃%
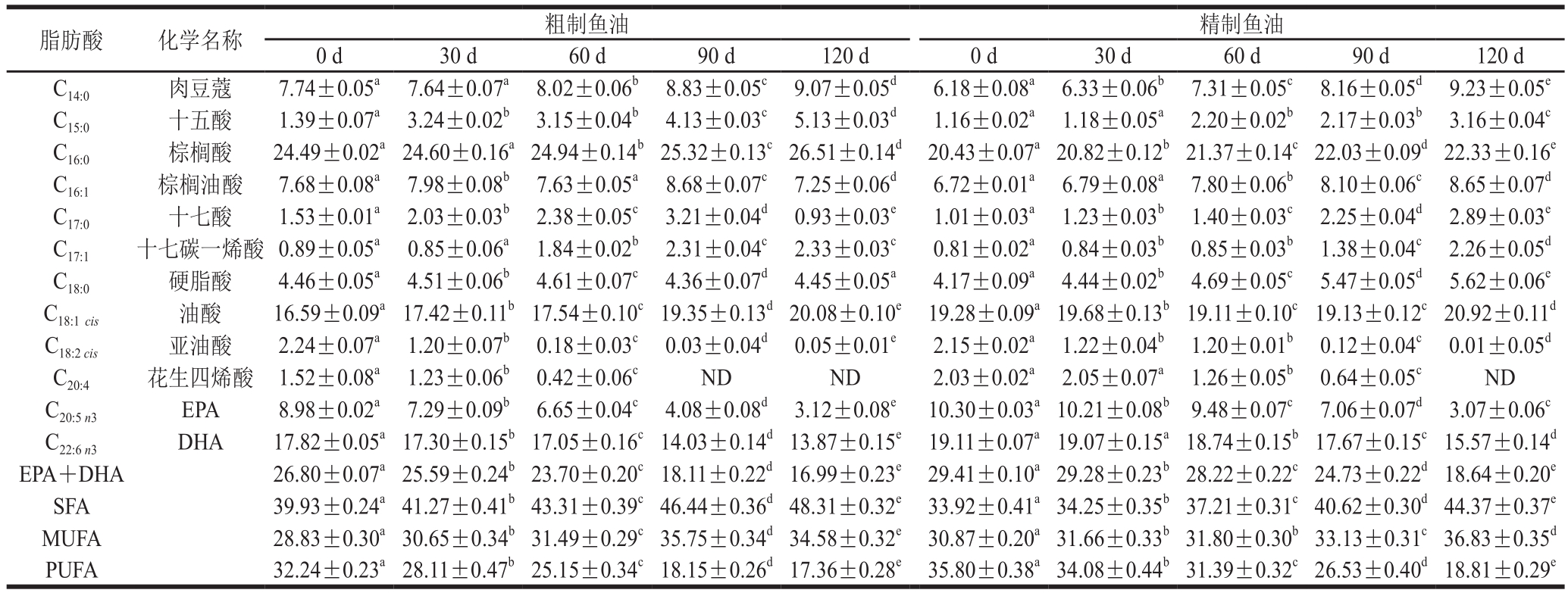
注:同一处理组,同行肩标小写字母不同表示差异显著(P<0.05);ND.未检出。下同。
精制鱼油0 d 30 d 60 d 90 d 120 d 0 d 30 d 60 d 90 d 120 d C14:0肉豆蔻 7.74±0.05a7.64±0.07a8.02±0.06b8.83±0.05c9.07±0.05d6.18±0.08a6.33±0.06b7.31±0.05c8.16±0.05d9.23±0.05eC15:0十五酸 1.39±0.07a3.24±0.02b3.15±0.04b4.13±0.03c5.13±0.03d1.16±0.02a1.18±0.05a2.20±0.02b2.17±0.03b3.16±0.04cC16:0棕榈酸 24.49±0.02a24.60±0.16a24.94±0.14b25.32±0.13c26.51±0.14d20.43±0.07a20.82±0.12b21.37±0.14c22.03±0.09d22.33±0.16eC16:1棕榈油酸 7.68±0.08a7.98±0.08b7.63±0.05a8.68±0.07c7.25±0.06d6.72±0.01a6.79±0.08a7.80±0.06b8.10±0.06c8.65±0.07dC17:0十七酸 1.53±0.01a2.03±0.03b2.38±0.05c3.21±0.04d0.93±0.03e1.01±0.03a1.23±0.03b1.40±0.03c2.25±0.04d2.89±0.03eC17:1十七碳一烯酸 0.89±0.05a0.85±0.06a1.84±0.02b2.31±0.04c2.33±0.03c0.81±0.02a0.84±0.03b0.85±0.03b1.38±0.04c2.26±0.05dC18:0硬脂酸 4.46±0.05a4.51±0.06b4.61±0.07c4.36±0.07d4.45±0.05a4.17±0.09a4.44±0.02b4.69±0.05c5.47±0.05d5.62±0.06eC18:1cis油酸 16.59±0.09a17.42±0.11b17.54±0.10c19.35±0.13d20.08±0.10e19.28±0.09a19.68±0.13b19.11±0.10c19.13±0.12c20.92±0.11dC18:2cis亚油酸 2.24±0.07a1.20±0.07b0.18±0.03c0.03±0.04d0.05±0.01e2.15±0.02a1.22±0.04b1.20±0.01b0.12±0.04c0.01±0.05dC20:4花生四烯酸 1.52±0.08a1.23±0.06b0.42±0.06cND ND 2.03±0.02a2.05±0.07a1.26±0.05b0.64±0.05cND C20:5n3EPA 8.98±0.02a7.29±0.09b6.65±0.04c4.08±0.08d3.12±0.08e10.30±0.03a10.21±0.08b9.48±0.07c7.06±0.07d3.07±0.06cC22:6n3DHA 17.82±0.05a17.30±0.15b17.05±0.16c14.03±0.14d13.87±0.15e19.11±0.07a19.07±0.15a18.74±0.15b17.67±0.15c15.57±0.14dEPA+DHA 26.80±0.07a25.59±0.24b23.70±0.20c18.11±0.22d16.99±0.23e29.41±0.10a29.28±0.23b28.22±0.22c24.73±0.22d18.64±0.20eSFA 39.93±0.24a41.27±0.41b43.31±0.39c46.44±0.36d48.31±0.32e33.92±0.41a34.25±0.35b37.21±0.31c40.62±0.30d44.37±0.37eMUFA 28.83±0.30a30.65±0.34b31.49±0.29c35.75±0.34d34.58±0.32e30.87±0.20a31.66±0.33b31.80±0.30b33.13±0.31c36.83±0.35dPUFA 32.24±0.23a28.11±0.47b25.15±0.34c18.15±0.26d17.36±0.28e35.80±0.38a34.08±0.44b31.39±0.32c26.53±0.40d18.81±0.29e脂肪酸 化学名称 粗制鱼油
表3 25 ℃贮藏条件下粗制鱼油与精制鱼油主要脂肪酸相对含量随时间的变化
Table3 Changes in relative contents of main fatty acids in crude and refined fish oil over time at 25 ℃%
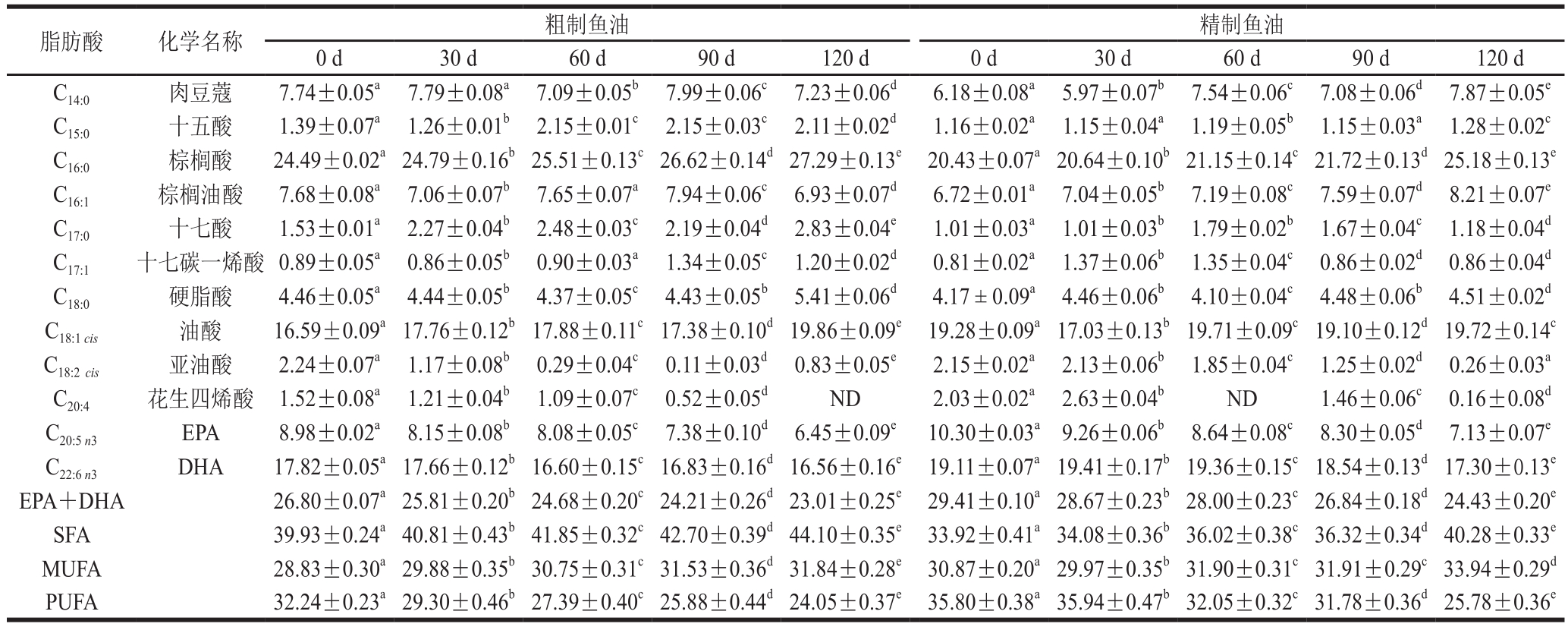
脂肪酸 化学名称 粗制鱼油精制鱼油0 d 30 d 60 d 90 d 120 d 0 d 30 d 60 d 90 d 120 d C14:0肉豆蔻 7.74±0.05a7.79±0.08a7.09±0.05b7.99±0.06c7.23±0.06d6.18±0.08a5.97±0.07b7.54±0.06c7.08±0.06d7.87±0.05eC15:0十五酸 1.39±0.07a1.26±0.01b2.15±0.01c2.15±0.03c2.11±0.02d1.16±0.02a1.15±0.04a1.19±0.05b1.15±0.03a1.28±0.02cC16:0棕榈酸 24.49±0.02a24.79±0.16b25.51±0.13c26.62±0.14d27.29±0.13e20.43±0.07a20.64±0.10b21.15±0.14c21.72±0.13d25.18±0.13eC16:1棕榈油酸 7.68±0.08a7.06±0.07b7.65±0.07a7.94±0.06c6.93±0.07d6.72±0.01a7.04±0.05b7.19±0.08c7.59±0.07d8.21±0.07eC17:0十七酸 1.53±0.01a2.27±0.04b2.48±0.03c2.19±0.04d2.83±0.04e1.01±0.03a1.01±0.03b1.79±0.02b1.67±0.04c1.18±0.04dC17:1十七碳一烯酸 0.89±0.05a0.86±0.05b0.90±0.03a1.34±0.05c1.20±0.02d0.81±0.02a1.37±0.06b1.35±0.04c0.86±0.02d0.86±0.04dC18:0硬脂酸 4.46±0.05a4.44±0.05b4.37±0.05c4.43±0.05b5.41±0.06d4.17 ± 0.09a4.46±0.06b4.10±0.04c4.48±0.06b4.51±0.02dC18:1cis油酸 16.59±0.09a17.76±0.12b17.88±0.11c17.38±0.10d19.86±0.09e19.28±0.09a17.03±0.13b19.71±0.09c19.10±0.12d19.72±0.14cC18:2cis亚油酸 2.24±0.07a1.17±0.08b0.29±0.04c0.11±0.03d0.83±0.05e2.15±0.02a2.13±0.06b1.85±0.04c1.25±0.02d0.26±0.03aC20:4花生四烯酸 1.52±0.08a1.21±0.04b1.09±0.07c0.52±0.05dND 2.03±0.02a2.63±0.04bND 1.46±0.06c0.16±0.08dC20:5n3EPA 8.98±0.02a8.15±0.08b8.08±0.05c7.38±0.10d6.45±0.09e10.30±0.03a9.26±0.06b8.64±0.08c8.30±0.05d7.13±0.07eC22:6n3DHA 17.82±0.05a17.66±0.12b16.60±0.15c16.83±0.16d16.56±0.16e19.11±0.07a19.41±0.17b19.36±0.15c18.54±0.13d17.30±0.13eEPA+DHA 26.80±0.07a25.81±0.20b24.68±0.20c24.21±0.26d23.01±0.25e29.41±0.10a28.67±0.23b28.00±0.23c26.84±0.18d24.43±0.20eSFA 39.93±0.24a40.81±0.43b41.85±0.32c42.70±0.39d44.10±0.35e33.92±0.41a34.08±0.36b36.02±0.38c36.32±0.34d40.28±0.33eMUFA 28.83±0.30a29.88±0.35b30.75±0.31c31.53±0.36d31.84±0.28e30.87±0.20a29.97±0.35b31.90±0.31c31.91±0.29c33.94±0.29dPUFA 32.24±0.23a29.30±0.46b27.39±0.40c25.88±0.44d24.05±0.37e35.80±0.38a35.94±0.47b32.05±0.32c31.78±0.36d25.78±0.36e
表4 15 ℃贮藏条件下粗制鱼油与精制鱼油主要脂肪酸相对含量随时间的变化
Table4 Changes in relative contents of main fatty acids in crude and refined fish oil over time at 15 ℃ storage condition%
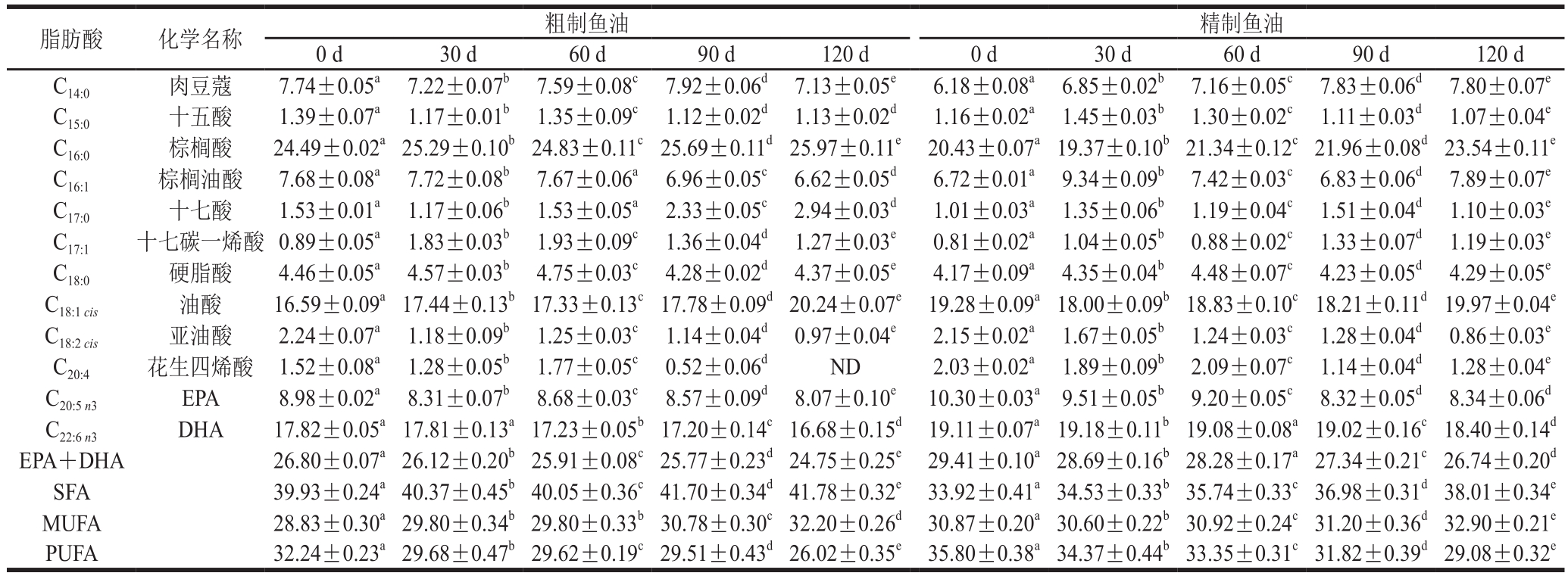
脂肪酸 化学名称 粗制鱼油精制鱼油0 d 30 d 60 d 90 d 120 d 0 d 30 d 60 d 90 d 120 d C14:0肉豆蔻 7.74±0.05a7.22±0.07b7.59±0.08c7.92±0.06d7.13±0.05e6.18±0.08a6.85±0.02b7.16±0.05c7.83±0.06d7.80±0.07eC15:0十五酸 1.39±0.07a1.17±0.01b1.35±0.09c1.12±0.02d1.13±0.02d1.16±0.02a1.45±0.03b1.30±0.02c1.11±0.03d1.07±0.04eC16:0棕榈酸 24.49±0.02a25.29±0.10b24.83±0.11c25.69±0.11d25.97±0.11e20.43±0.07a19.37±0.10b21.34±0.12c21.96±0.08d23.54±0.11eC16:1棕榈油酸 7.68±0.08a7.72±0.08b7.67±0.06a6.96±0.05c6.62±0.05d6.72±0.01a9.34±0.09b7.42±0.03c6.83±0.06d7.89±0.07eC17:0十七酸 1.53±0.01a1.17±0.06b1.53±0.05a2.33±0.05c2.94±0.03d1.01±0.03a1.35±0.06b1.19±0.04c1.51±0.04d1.10±0.03eC17:1十七碳一烯酸 0.89±0.05a1.83±0.03b1.93±0.09c1.36±0.04d1.27±0.03e0.81±0.02a1.04±0.05b0.88±0.02c1.33±0.07d1.19±0.03eC18:0硬脂酸 4.46±0.05a4.57±0.03b4.75±0.03c4.28±0.02d4.37±0.05e4.17±0.09a4.35±0.04b4.48±0.07c4.23±0.05d4.29±0.05eC18:1cis油酸 16.59±0.09a17.44±0.13b17.33±0.13c17.78±0.09d20.24±0.07e19.28±0.09a18.00±0.09b18.83±0.10c18.21±0.11d19.97±0.04eC18:2cis亚油酸 2.24±0.07a1.18±0.09b1.25±0.03c1.14±0.04d0.97±0.04e2.15±0.02a1.67±0.05b1.24±0.03c1.28±0.04d0.86±0.03eC20:4花生四烯酸 1.52±0.08a1.28±0.05b1.77±0.05c0.52±0.06dND 2.03±0.02a1.89±0.09b2.09±0.07c1.14±0.04d1.28±0.04eC20:5n3EPA 8.98±0.02a8.31±0.07b8.68±0.03c8.57±0.09d8.07±0.10e10.30±0.03a9.51±0.05b9.20±0.05c8.32±0.05d8.34±0.06dC22:6n3DHA 17.82±0.05a17.81±0.13a17.23±0.05b17.20±0.14c16.68±0.15d19.11±0.07a19.18±0.11b19.08±0.08a19.02±0.16c18.40±0.14dEPA+DHA 26.80±0.07a26.12±0.20b25.91±0.08c25.77±0.23d24.75±0.25e29.41±0.10a28.69±0.16b28.28±0.17a27.34±0.21c26.74±0.20dSFA 39.93±0.24a40.37±0.45b40.05±0.36c41.70±0.34d41.78±0.32e33.92±0.41a34.53±0.33b35.74±0.33c36.98±0.31d38.01±0.34eMUFA 28.83±0.30a29.80±0.34b29.80±0.33b30.78±0.30c32.20±0.26d30.87±0.20a30.60±0.22b30.92±0.24c31.20±0.36d32.90±0.21ePUFA 32.24±0.23a29.68±0.47b29.62±0.19c29.51±0.43d26.02±0.35e35.80±0.38a34.37±0.44b33.35±0.31c31.82±0.39d29.08±0.32e
表5 5 ℃贮藏条件下粗制鱼油与精制鱼油主要脂肪酸相对含量随时间的变化
Table5 Changes in relative contents of main fatty acids in crude and refined fish oil over time at 5 ℃ storage condition%
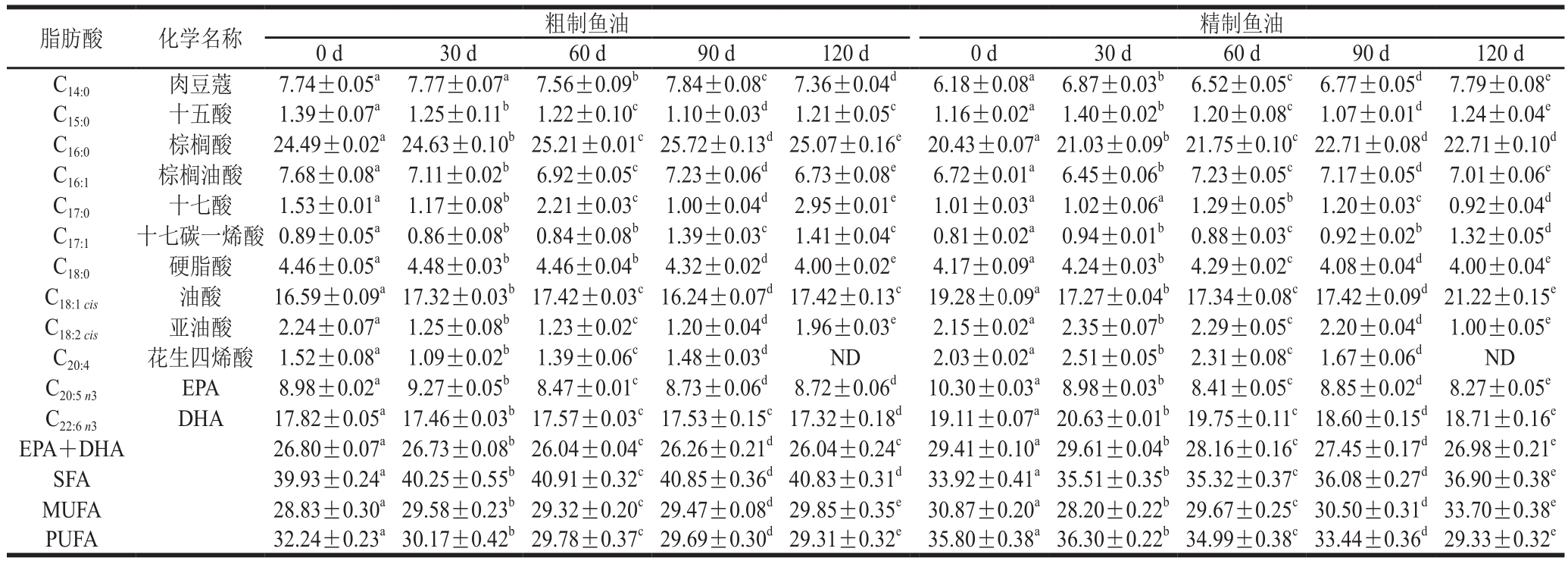
脂肪酸 化学名称 粗制鱼油精制鱼油0 d 30 d 60 d 90 d 120 d 0 d 30 d 60 d 90 d 120 d C14:0肉豆蔻 7.74±0.05a7.77±0.07a7.56±0.09b7.84±0.08c7.36±0.04d6.18±0.08a6.87±0.03b6.52±0.05c6.77±0.05d7.79±0.08eC15:0十五酸 1.39±0.07a1.25±0.11b1.22±0.10c1.10±0.03d1.21±0.05c1.16±0.02a1.40±0.02b1.20±0.08c1.07±0.01d1.24±0.04eC16:0棕榈酸 24.49±0.02a24.63±0.10b25.21±0.01c25.72±0.13d25.07±0.16e20.43±0.07a21.03±0.09b21.75±0.10c22.71±0.08d22.71±0.10dC16:1棕榈油酸 7.68±0.08a7.11±0.02b6.92±0.05c7.23±0.06d6.73±0.08e6.72±0.01a6.45±0.06b7.23±0.05c7.17±0.05d7.01±0.06eC17:0十七酸 1.53±0.01a1.17±0.08b2.21±0.03c1.00±0.04d2.95±0.01e1.01±0.03a1.02±0.06a1.29±0.05b1.20±0.03c0.92±0.04dC17:1十七碳一烯酸 0.89±0.05a0.86±0.08b0.84±0.08b1.39±0.03c1.41±0.04c0.81±0.02a0.94±0.01b0.88±0.03c0.92±0.02b1.32±0.05dC18:0硬脂酸 4.46±0.05a4.48±0.03b4.46±0.04b4.32±0.02d4.00±0.02e4.17±0.09a4.24±0.03b4.29±0.02c4.08±0.04d4.00±0.04eC18:1cis油酸 16.59±0.09a17.32±0.03b17.42±0.03c16.24±0.07d17.42±0.13c19.28±0.09a17.27±0.04b17.34±0.08c17.42±0.09d21.22±0.15eC18:2cis亚油酸 2.24±0.07a1.25±0.08b1.23±0.02c1.20±0.04d1.96±0.03e2.15±0.02a2.35±0.07b2.29±0.05c2.20±0.04d1.00±0.05eC20:4花生四烯酸 1.52±0.08a1.09±0.02b1.39±0.06c1.48±0.03dND 2.03±0.02a2.51±0.05b2.31±0.08c1.67±0.06dND C20:5n3EPA 8.98±0.02a9.27±0.05b8.47±0.01c8.73±0.06d8.72±0.06d10.30±0.03a8.98±0.03b8.41±0.05c8.85±0.02d8.27±0.05eC22:6n3DHA 17.82±0.05a17.46±0.03b17.57±0.03c17.53±0.15c17.32±0.18d19.11±0.07a20.63±0.01b19.75±0.11c18.60±0.15d18.71±0.16eEPA+DHA 26.80±0.07a26.73±0.08b26.04±0.04c26.26±0.21d26.04±0.24c29.41±0.10a29.61±0.04b28.16±0.16c27.45±0.17d26.98±0.21eSFA 39.93±0.24a40.25±0.55b40.91±0.32c40.85±0.36d40.83±0.31d33.92±0.41a35.51±0.35b35.32±0.37c36.08±0.27d36.90±0.38eMUFA 28.83±0.30a29.58±0.23b29.32±0.20c29.47±0.08d29.85±0.35e30.87±0.20a28.20±0.22b29.67±0.25c30.50±0.31d33.70±0.38ePUFA 32.24±0.23a30.17±0.42b29.78±0.37c29.69±0.30d29.31±0.32e35.80±0.38a36.30±0.22b34.99±0.38c33.44±0.36d29.33±0.32e
鱼油挥发性成分主要由醛、醇、酮、酸和烃类组成。醛类化合物主要源自不饱和脂肪酸的氧化降解[29],其感觉阈值一般都很低,对整体风味贡献大[30];醇类一般被认为是羰基化合物还原或是脂肪酸二级氢过氧化物降解而生成[31];酮类化合物来源于不饱和脂肪酸的热氧化降解等作用[32];而烃类化合物则可能是由于烷基自由基的自氧化作用产生,各种烃类(C8~C20)的感觉阈值通常较高,对鱼油整体风味几乎没有作用。
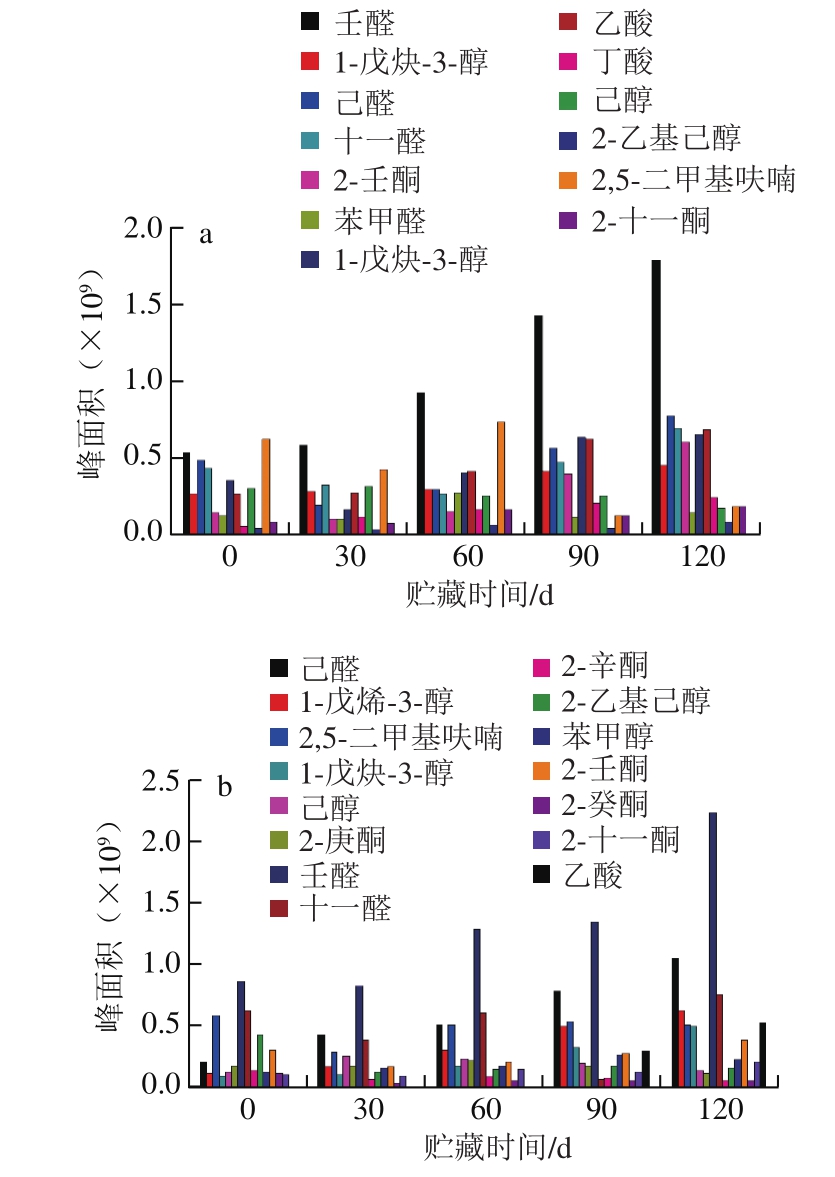
图4 35 ℃贮藏条件下粗制鱼油(a)与精制鱼油(b)主要挥发性风味成分随时间的变化
Fig.4 Changes in main volatile flavor components in crude (a) and refined (b) fish oil over time at 35 ℃
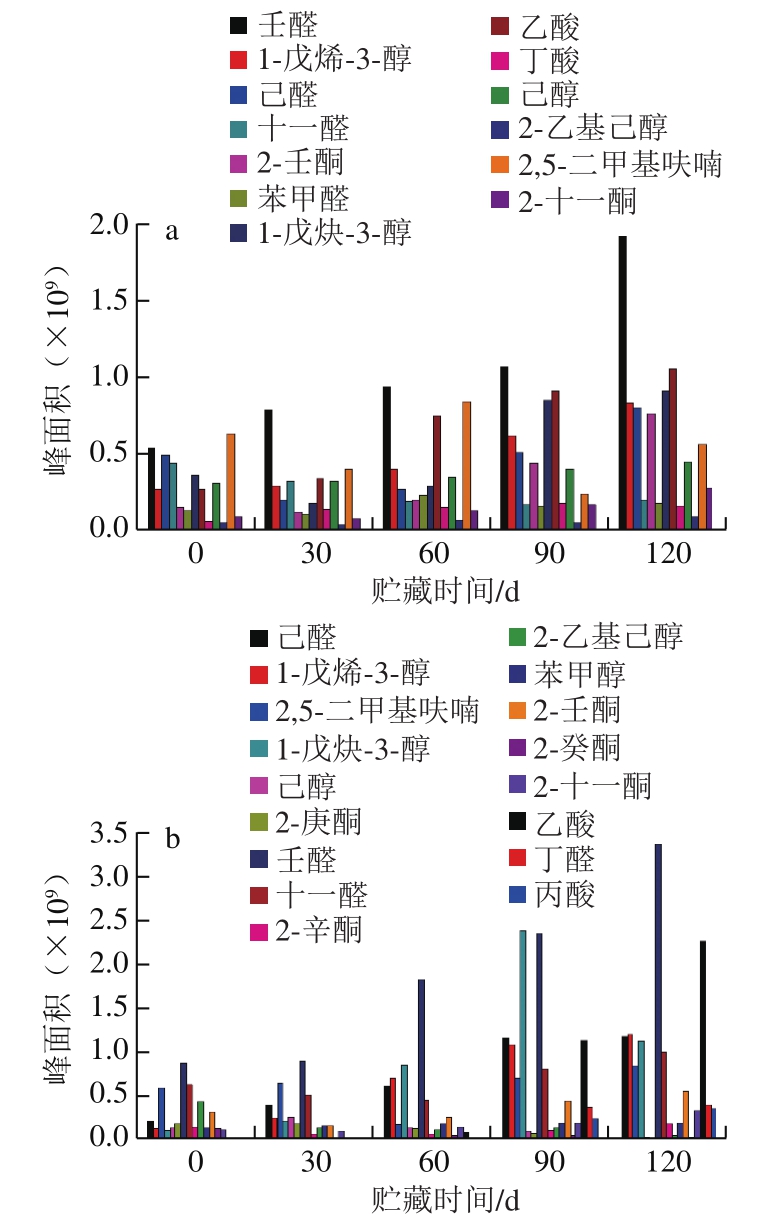
图5 25 ℃贮藏条件下粗制鱼油(a)与精制鱼油(b)主要挥发性风味成分随时间的变化
Fig.5 Changes in main volatile flavor components in crude (a) and refined (b) fish oil over time at 25 ℃
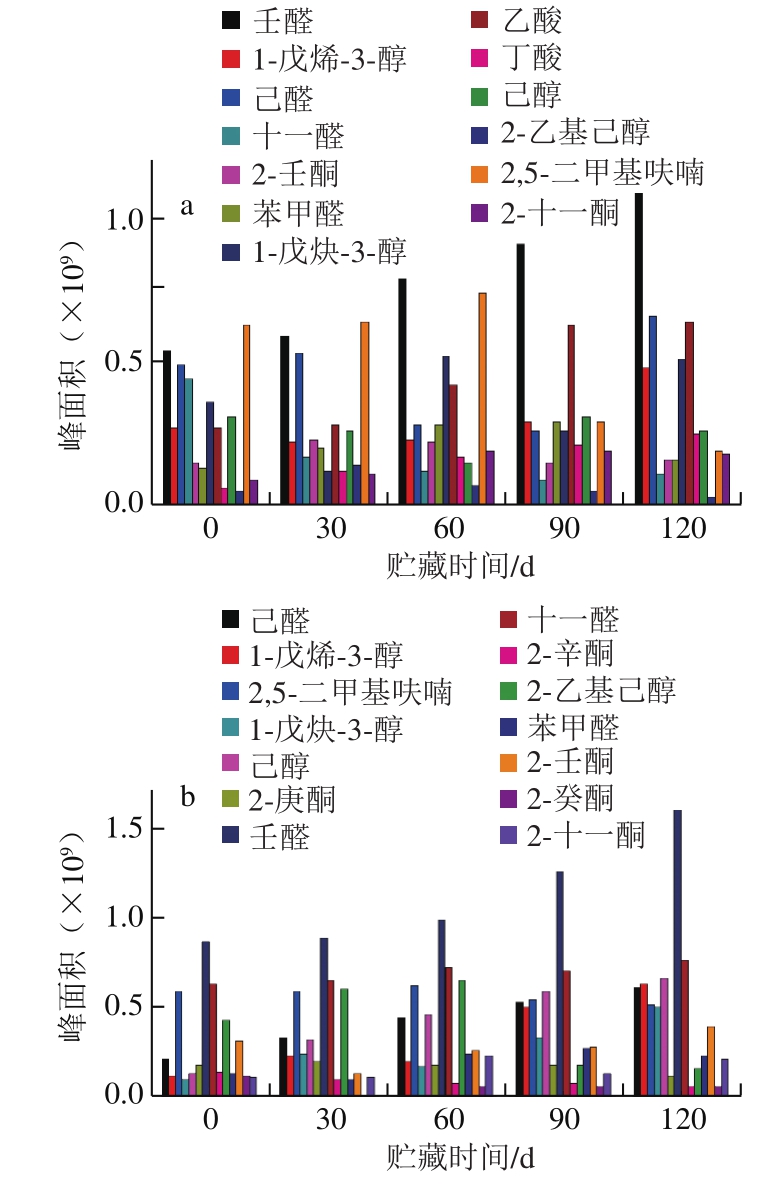
图6 15 ℃贮藏条件下粗制鱼油(a)与精制鱼油(b)主要挥发性风味成分随时间的变化
Fig.6 Changes in main volatile flavor components in crude (a) and refined (b) fish oil over time at 15 ℃condition
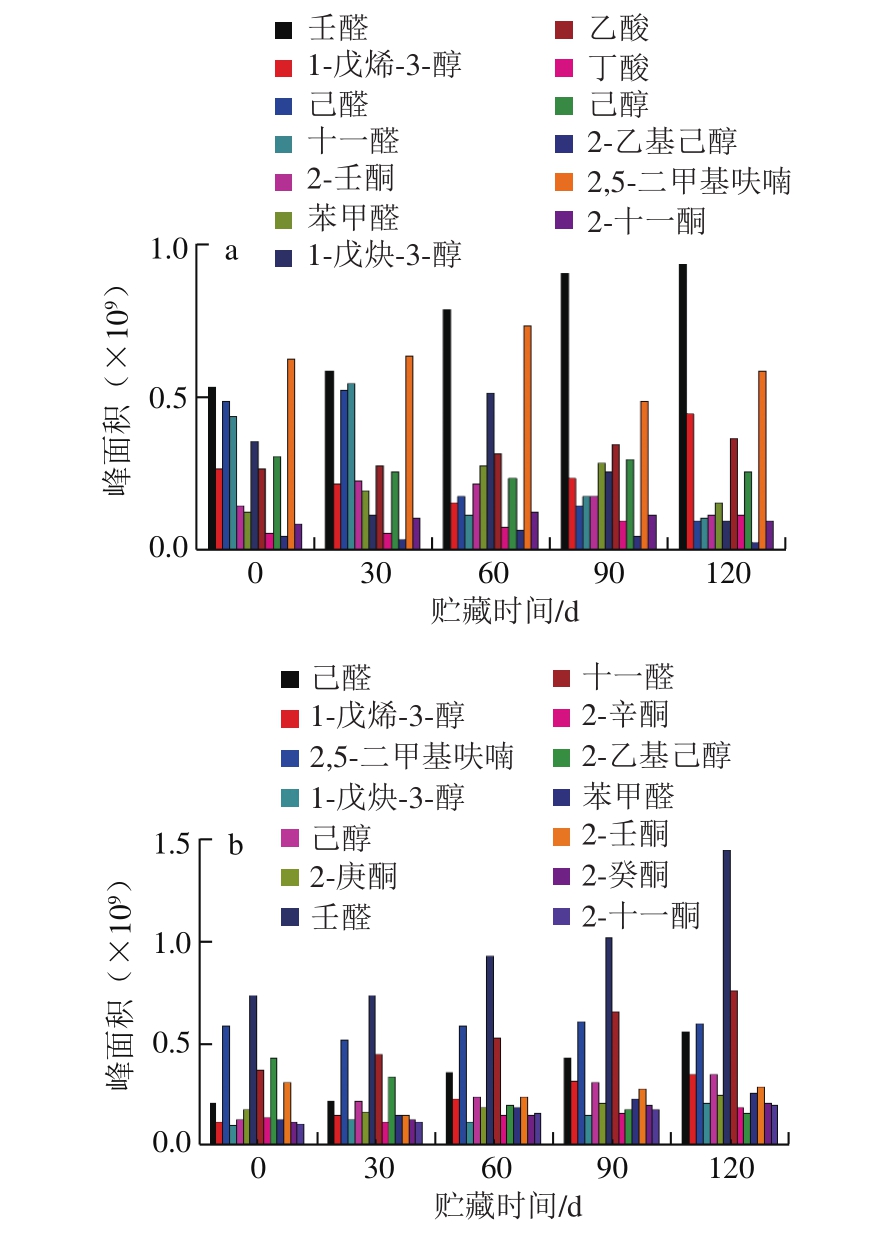
图7 5 ℃贮藏条件下粗制鱼油(a)与精制鱼油(b)主要挥发性风味成分随时间的变化
Fig.7 Changes in main volatile flavor components in crude (a) and refined (b) fish oil over time at 5 ℃
由图4~7可知,壬醛、1-戊烯-3-醇、己醛、十一醛、2-壬酮、苯甲醛、1-戊炔-3-醇、乙酸、丁酸、2-乙基己醇、2,5-二甲基呋喃及2-十一酮是粗鱼油中主要的挥发性风味物质。随贮藏时间延长,挥发性化合物总含量增加,且受温度影响较大,温度越高,其含量增加越多,变化越明显。在贮藏前期,挥发性化合物的增长速率较慢,这与鱼油过氧化值及茴香胺值在贮藏前期的变化规律趋近。到贮藏中期,由于脂肪酸氧化加剧致挥发性氧化产物大量增加,鱼油已产生较严重的脂肪酸败味,并有较强的腥臭味。在整个贮藏期间,壬醛的含量变化最为显著。壬醛是油酸氧化的主要特征产物,且感觉阈值为1 μg/kg,对鱼油整体风味贡献很大,赋予鱼油脂肪味[33]。1-戊烯-3-醇的含量变化也较明显,阈值较小,是粗鱼油中的主要腥味物质[34]。己醛含量也随着贮藏时间的延长而呈现有规律的变化,其是亚油酸氧化的主要特征产物[35]。另外,2-壬酮、2,5-二甲基呋喃和2-十一酮的含量都明显增加,且感觉阈值低,对鱼油整体风味贡献大,而乙酸的含量可表征鱼油氧化酸败剧烈程度[24]。
粗鱼油经过脱胶、脱酸、脱色与脱臭处理后,大量胶脂类、色素、痕量金属以及具有不良气味的醛类、酮类、醇类和碳氢化合物等挥发性成分被去除[36-38],使得鱼油风味明显改善。精制鱼油中主要挥发性化合物有己醛、1-戊烯-3-醇、2,5-二甲基呋喃、己醇、2-庚酮、壬醛、十一醛、2-辛酮、2-乙基己醇、苯甲醇、2-壬酮、2-癸酮、2-十一酮、乙酸、丁醛和丙酸。由图4可以看出,粗鱼油经精制处理后,其腥味物质含量明显减少,鱼油品质明显提升。精制鱼油中挥发性成分含量的变化规律与粗鱼油相近,受温度影响大。在贮藏前期,风味物质的含量变化不大,即处于氧化诱导阶段。随着时间延长,精制鱼油氧化酸败严重,己醛、1-戊烯-3-醇、壬醛及乙酸的含量显著提高,且含量远超于同温度条件下粗鱼油中该物质的含量,说明在相同环境条件下,精制鱼油比粗鱼油的贮藏稳定性更差,其主要原因是精制鱼油中脂肪酸的不饱和度高,更易被氧化分解。
鱼油在不同贮藏温度条件下品质变化规律显著。随温度升高,酸价、过氧化值及茴香胺值均明显升高;大量PUMA被氧化,使其含量减少,而SFA含量增加;壬醛、1-戊烯-3-醇、己醛等物质含量增加使鱼油有强烈的腥臭异味,温度对其贮藏稳定性的影响大,且精制鱼油贮藏稳定性较粗制鱼油差。35 ℃时精制鱼油的保质期约为20 d,粗制鱼油约为40 d;25 ℃时精制鱼油的保质期约为40 d,粗制鱼油约为65 d;15 ℃时精制鱼油的保质期约为65 d,粗制鱼油约为80 d;5 ℃时精制鱼油的保质期约为115 d,而粗制鱼油在120 d的贮藏期内未变质。对于如何更好地提高鱼油贮藏稳定性将是一个新的研究方向;在后续实验中,将研究通过添加抗氧化剂、气调贮藏、调节温度等措施以期达到提高鱼油贮藏稳定性及延长货架期的目的。
[1] MERKLE S, GIESE E, ROHN S, et al. Impact of fish species and processing technology on minor fi sh oil components[J]. Food Control,2017, 73: 1379-1387. DOI:10.1016/j.foodcont.2016.11.003.
[2] ELTWERI A M, THOMAS A L, METCALFE M, et al. Potential applications of fi sh oils rich in omega-3 polyunsaturated fatty acids in the management of gastrointestinal cancer[J]. Clinical Nutrition, 2016,36: 65-78. DOI:10.1016/j.clnu.2016.01.007.
[3] ENDO J, ARITA M. Cardioprotective mechanism of omega-3 polyunsaturated fatty acids[J]. Journal of Cardiology, 2016, 67(1): 22-27. DOI:10.1016/j.jjcc.2015.08.002.
[4] TANEJA A, ZHU X. The trouble with omega-3 oils[J]. Function Ingredient, 2016, 2006: 26-28.
[5] HONOLD P J, NOUARD M L, JACOBSEN C. Oxidative stability during storage of fi sh oil from fi lleting by-products of rainbow trout(Oncorhynchus mykiss) is largely independent of the processing and production temperature[J]. European Journal of Lipid Science and Technology, 2016, 118(6): 967-973. DOI:10.1002/ejlt.201500344.
[6] FONTAGNÉ S, BAZIN D, BRÈQUE J, et al. Effects of dietary oxidized lipid and vitamin A on the early development and antioxidant status of Siberian sturgeon (Acipenser baeri) larvae[J]. Aquaculture,2006, 257: 400-411. DOI:10.1016/j.aquaculture.2006.01.025.
[7] 吕军伟. DHA 藻油抗氧化特性研究[D]. 上海: 上海海洋大学, 2015:13-14.
[8] 李冲冲, 李子豪, 柳余莉, 等. 鱼粉加工副产物中鱼油的精炼及其脂肪酸组成分析[J]. 食品科学, 2015, 36(20): 190-193. DOI:10.7506/spkx1002-6630-201520036.
[9] 朱建龙, 薛静, 宋恭帅, 等. 响应面法优化杂鱼油脱酸工艺[J]. 中国食品学报, 2017, 17(1): 154-160. DOI:10.16429/j.1009-7848.2017.01.020.
[10] 朱建龙, 薛静, 宋恭帅, 等. 响应面法优化杂鱼油脱色工艺[J]. 中国食品学报, 2017, 17(2): 119-126. DOI:10.16429/j.1009-7848.2017.02.016.
[11] DE OLIVEIRA D A S B, MINOZZO M G, LICODIEDOFF S, et al.Physicochemical and sensory characterization of refined and deodorized tuna (Thunnus albacares) by-product oil obtained by enzymatic hydrolysis[J]. Food Chemistry, 2016, 207: 187-194.DOI:10.1016/j.foodchem.2016.03.069.
[12] 国家卫生和计划生育委员会. 食品安全国家标准 食品中酸价的测定: GB 5009.229—2016[S]. 北京: 中国标准出版社, 2016: 1-2.
[13] 国家卫生和计划生育委员会. 食品安全国家标准 食品中过氧化值的测定: GB 5009.227—2016[S]. 北京: 中国标准出版社, 2016: 1-2.
[14] 中国国家标准化管理委员会. 动植物油脂 茴香胺值的测定: GB/T 24304—2009[S]. 北京: 中国标准出版社, 2006: 1-3.
[15] 王亚男, 季晓敏, 黄健, 等. CO2超临界萃取技术对金枪鱼油挥发性成分的分析[J]. 中国粮油学报, 2015, 30(6): 74-78; 100. DOI:1003-0174(2015)06-0074-0.
[16] 王霞, 黄健, 侯云丹, 等. 电子鼻结合气相色谱-质谱联用技术分析黄鳍金枪鱼肉的挥发性成分[J]. 食品科学, 2012, 33(12) : 268-272.DOI:1002-6630(2012)12-0268-05.
[17] MENEGAZZO M L, PETENUCI M E, FONSECA G G. Production and characterization of crude and refined oils obtained from the co-products of Nile tilapia and hybrid sorubim processing[J]. Food Chemistry, 2014, 157: 100-104. DOI:10.1016/j.foodchem.2014.01.121.
[18] 李文佳. 水酶法淡水鱼油提取及鱼油腥味成分分析研究[D]. 无锡:江南大学, 2014: 40-41.
[19] CREXI V T, MONTE M L, DE SOUZA SOARES L A, et al.Production and refinement of oil from carp (Cyprinus carpio)viscera[J]. Food Chemistry, 2010, 119(3): 945-950. DOI:10.1016/j.foodchem.2009.07.050.
[20] 董小林, 董桂芳, 朱晓鸣, 等. 不同温度条件下鱼油氧化的动态变化[J].中国油脂, 2012, 37(7): 36-40.
[21] RAMAKRISHNAN T V, FRANCIS F J. Coupled oxidation of carotenoids in fatty acid esters of varying unsaturation[J]. Journal of Food Quality,1979, 2(4): 277-287. DOI:10.1111/j.1745-4557.1979.tb00679.x.
[22] SULLIVAN J C, BUDGE S M. Fish oil sensory properties can be predicted using key oxidative volatiles[J]. European Journal of Lipid Science and Technology, 2012, 114(5): 496-503. DOI:10.1002/ejlt.201100330.
[23] 栾霞, 祖丽亚, 樊铁. 食用油脂中p-茴香胺值的测定[J]. 中国油脂,2006, 31(11): 38-40.
[24] 王世成. 影响油脂茴香胺值和过氧化值的因素[J]. 粮食与油脂,1996(4): 58.
[25] 李桂玲, 金庆华. 淡水鱼加工下脚料中VD和EPA及DHA的测定[J].武汉化工学院学报, 1998, 20(3): 19-21.
[26] 李永刚. 鱼油是珍贵的饲料资源[J]. 饲料与畜牧, 1992(4): 11-12.
[27] 农业部. 中华人民共和国水产行业标准 鱼油: SC/T 3502—2016[S].北京: 中国标准出版社, 2006: 2-3.
[28] ÖZOGUL Y, ÖZOGUL F, ÇIÇEK E, et al. Fat content and fatty acid compositions of 34 marine water fi sh species from the Mediterranean sea[J]. International Journal of Food Sciences and Nutrition, 2009,60(6): 464-475.
[29] JOSEPHSON D B, LINDSAY R C, STUIBER D A. Volatile compounds characterizing the aroma of fresh Atlantic and Pacific oysters[J]. Journal of Food Science, 1984, 50(1): 5-9. DOI:10.1111/j.1365-2621.1985.tb13265.x.
[30] 徐星. 植物油氧化过程中脂肪酸和挥发性成分变化的研究[D].杭州: 浙江工商大学, 2013: 41-43.
[31] 张娜, 袁信华, 过世东, 等. 中华绒螯蟹挥发性物质的研究[J]. 食品与发酵工业, 2008, 34(3): 141-144; 148.
[32] GALAN A, 张威, 苏秀榕, 等. 浒苔和龙须菜营养成分的研究[J]. 水产科学, 2010, 29(6): 329-333.
[33] SUZUKI J, ICHIMURA N, ETOH T. Volatile components of boiled scallop[J]. Food Reviews International, 1990, 6(4): 537-552.DOI:10.1080/87559129009540891.
[34] DUFLOS G, COIN V M, CORNU M, et al. Determination of volatile compounds to characterize fish spoilage using headspace/mass spectrometry and solid-phase microextraction/gas chromatography/mass spectrometry[J]. Journal of the Science of Food and Agriculture,2006, 86(4): 600-611.
[35] KALUA C M, ALLEN M S, BEDGOOD D R, et al. Olive oil volatile compounds, flavour development and quality. a critical review[J]. Food Chemistry, 2007, 100(1): 273-286. DOI:10.1016/j.foodchem.2005.09.059.
[36] ANTONIASSI R, ESTEVES W, MEIRELLES J A. Pretreatment of corn oil for physical refining[J]. Journal of the American Oil Chemists Society, 1998, 75(10): 1411-1415. DOI:10.1007/s11746-998-0191-8.
[37] BERDEAUX O, FOURNIER V, LAMBELET P, et al. Isolation and structural analysis of the cyclic fatty acid monomers formed from eicosapentaenoic and docosahexaenoic acids during fish oil deodorization[J]. Journal of Chromatography A, 2007, 1138: 216-224.DOI:10.1016/j.chroma.2006.10.061.
[38] HAFIDI A, PIOCH D, AJANA H. Membrane-based simultaneous degumming and deacidification of vegetable oils[J]. Innovative Food Science and Emerging Technologies, 2005, 6(2): 203-212.DOI:10.1016/j.ifset.2004.12.001.
Quality Changes in Crude and Refined Fish Oil at Different Storage Temperatures