蛹虫草的活性成分和药理作用及其应用研究进展
左锦辉,贡晓燕,董银卯,李 丽*
(北京工商大学 北京市植物资源研究开发重点实验室,北京 100048)
摘 要:本文对蛹虫草中的活性成分,如核苷类、虫草多糖、虫草多肽、甾醇类、有机酸类等的化学结构进行总结。并综述了近年来国内外关于蛹虫草药理活性的研究,主要包括其免疫调节作用、抑菌作用、抗病毒作用、抗肿瘤作用、神经保护作用、性功能保护作用以及抗辐射作用等。最后对蛹虫草在食品、医药保健品中的应用进行了概括。
关键词:蛹虫草;活性成分;药理作用;应用
蛹虫草(Cordyceps militaris L. Link),又称北冬虫夏草、北虫草,是一种常用的食药用真菌,属子囊菌亚门(Ascomycotina)、麦角菌科(Clavicipitaceue)、虫草属(Cordyceps),与冬虫夏草属于同属真菌[1]。虽然野生的蛹虫草资源比较稀少,但经过多年的技术研究,蛹虫草已经实现了较大规模的人工培养。此外,不少研究也表明,人工培养的蛹虫草具有和冬虫夏草相似的药理活性[2-3],有些活性成分如虫草素的含量甚至比冬虫夏草更高[4-5],蛹虫草已逐渐成为冬虫夏草的理想替代品,为了进一步推进蛹虫草功效的开发与应用,本文对近年来国内外关于蛹虫草药理活性的研究进行了总结。
目前关于蛹虫草活性成分的综述,大多缺乏对某一类物质中单体活性物质的化学结构进行系统整理。蛹虫草的化学成分不像冬虫夏草等有现成可查询的中药数据库(TCMSP、TCM@TAIWAN等),所以很多文献往往把蛹虫草的化学成分和冬虫夏草等其他虫草属的混在一起总结[3,6-7]。此外,近年来关于蛹虫草多糖和多肽等的结构研究有了不少的新进展,所以急需对蛹虫草活性成分的化学结构进行一个系统的整理。本文通过查阅大量国内外相关文献和化学结构数据库(PubChem),分别对蛹虫草中的核苷类、虫草多糖、虫草多肽、甾醇类、有机酸类等的化学结构进行了系统整理。
蛹虫草的培养方法大体可分为液体发酵培养和固体发酵培养[8],蛹虫草固体发酵可以得到子实体,而液体发酵主要得到的是菌丝体,此外还可以利用一些中药材作为培养基,与蛹虫草共同发酵得到药用菌质[9-10],这些发酵产物可以通过制成出不同的剂型广泛地应用于医药、食品和保健品中。
1 蛹虫草的活性成分
1.1 核苷类成分
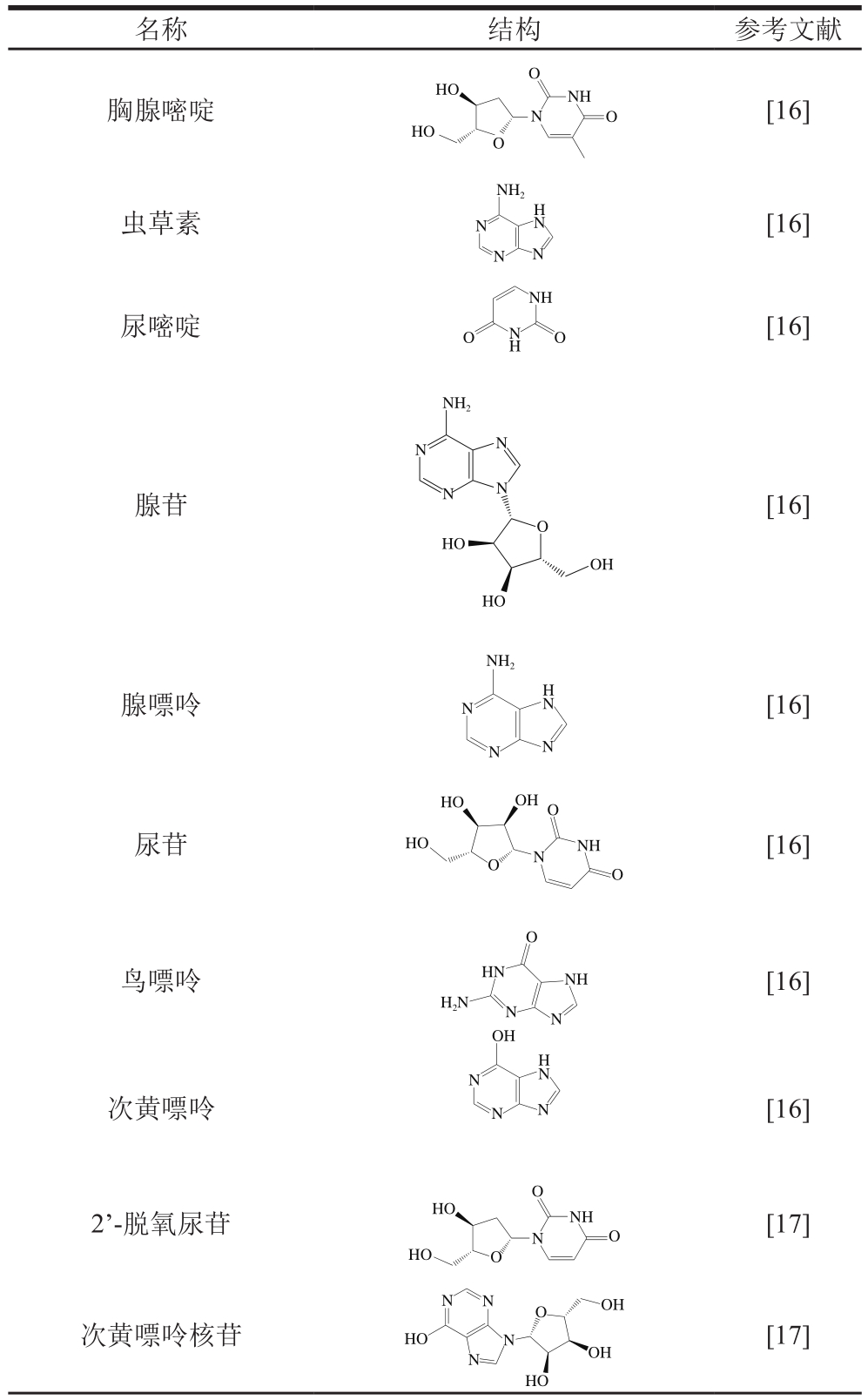
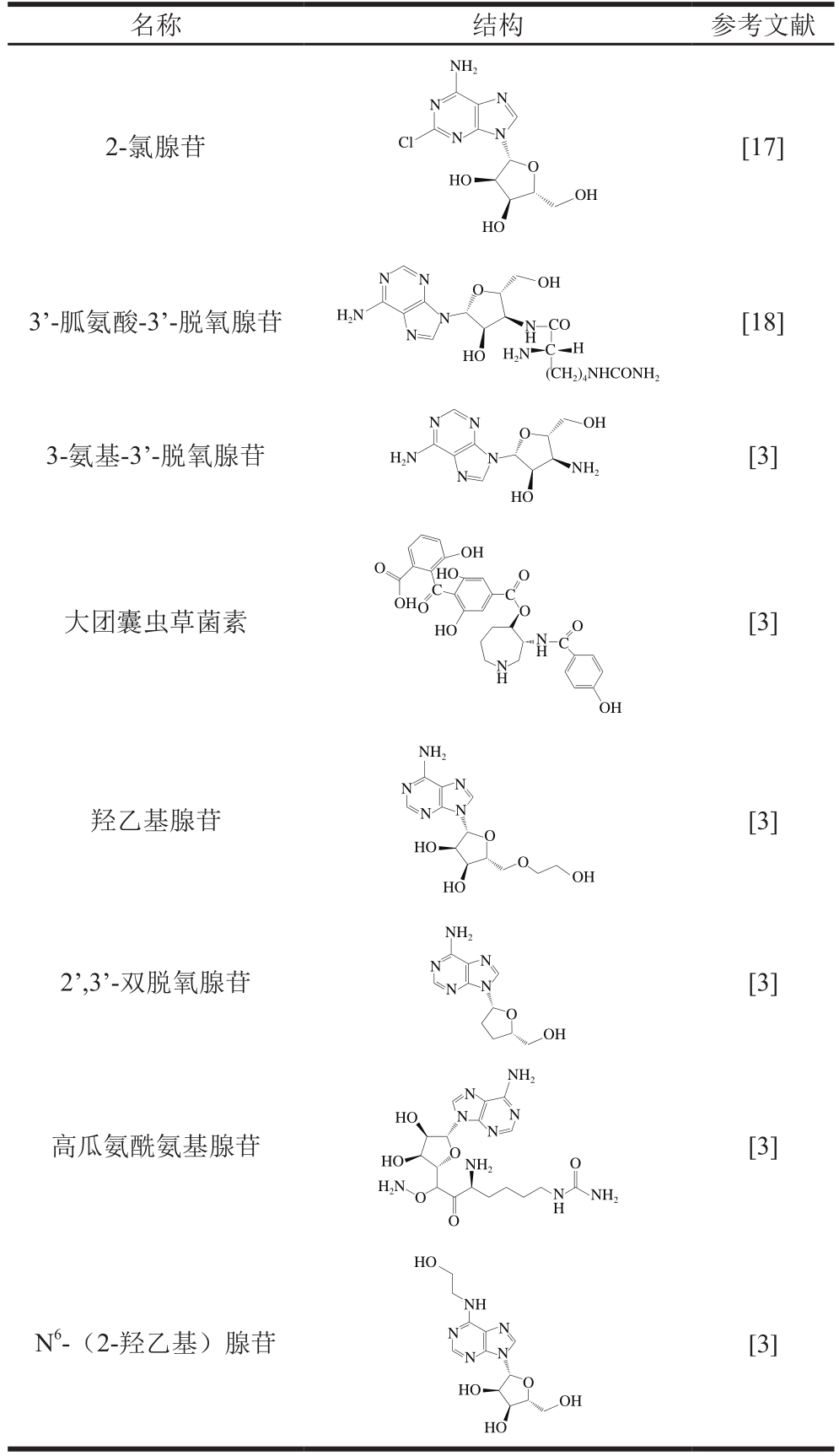
核苷类物质为蛹虫草的主要活性成分之一,具有广泛的生理功能。蛹虫草核苷包括虫草素、腺苷、腺嘌呤、尿嘧啶、尿苷、鸟嘌呤、次黄嘌呤核苷和胸腺嘧啶等,具体结构如表1所示。其中虫草素作为蛹虫草中具有代表性的核苷类物质,是第一个从真菌中分离出来的核苷类抗生素[11],虫草素在蛹虫草发酵菌丝体中的含量远远高于冬虫夏草,蛹虫草是目前已报道的300余种虫草菌中唯一能大量形成虫草素的菌种[4-5,12]。虽然现在虫草素能以腺苷、3’-O-对硝基苯磺酰基腺苷等为原料进行化学合成[13],但由于产率很低,价格依旧十分昂贵。此外也有研究者通过优化培养基,诱导突变菌种选育使蛹虫草的虫草素产量不断提高[14-15]。
表1 蛹虫草中的核苷类成分
Table1 Nucleosides in C. militaris
名称 结构 参考文献O HO胸腺嘧啶NHHONO[16]O NH2虫草素NHN [16]N N NH尿嘧啶OONH[16]NH2N N腺苷NNHOO[16]OH HO NH2腺嘌呤H N N [16]N N HO OH O尿苷HOO N NH [16]O O鸟嘌呤HNH2N[16]N NH N OH N次黄嘌呤NH N N [16]O 2’-脱氧尿苷HONHNO[17]HO O N N O OH次黄嘌呤核苷HON[17]N OH HO
续表1
名称 结构 参考文献NH2N N Cl N 2-氯腺苷NHOO[17]OH HO N N O OH 3’-胍氨酸-3’-脱氧腺苷H2NNN NHCO [18]HO H2N C H(CH2)4NHCONH2N N O OH 3-氨基-3’-脱氧腺苷H2N N N NH2HO[3]OH O HO C C大团囊虫草菌素OHOO O HO O NH[3]C NH OH羟乙基腺苷NH2N N N NHOO[3]O HO OH NH2N N N 2’,3’-双脱氧腺苷N[3]O OH NH2N HO N N高瓜氨酰氨基腺苷NHO O NH2O [3]H2N O NH2O NH HO N6-(2-羟乙基)腺苷NH N N NN[3]HO O OH HO
1.2 虫草多糖类化合物
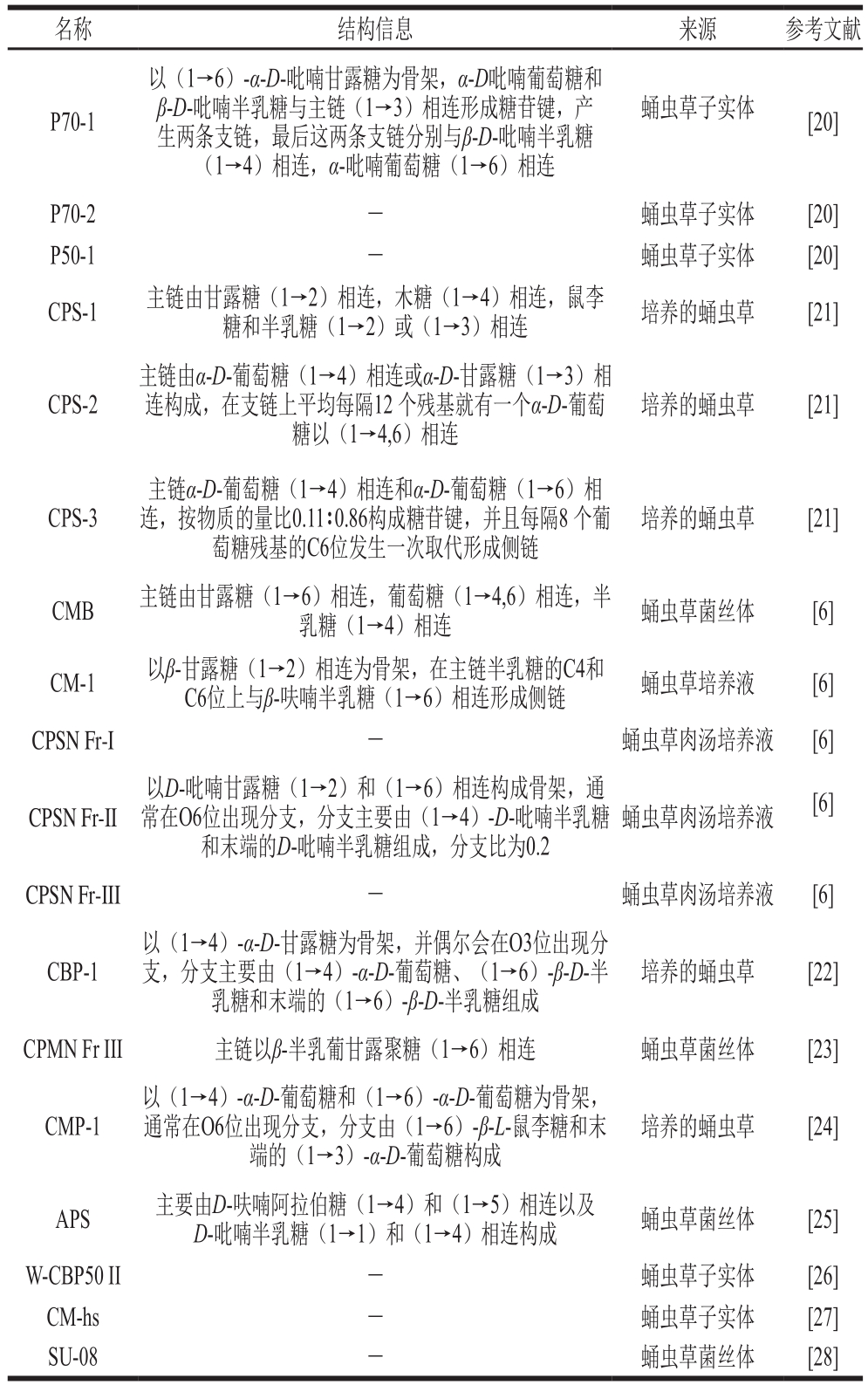
虫草多糖是蛹虫草中含量最丰富、也是最重要的生物活性成分之一,蛹虫草中多糖的含量为4%~10%,在蛹虫草真菌的子座、僵虫体、菌丝体及发酵液中均含有多糖[12]。来永斌等[19]的研究表明,蛹虫草多糖在蛹虫草不同部位含量差异较大。通过对不同培养基栽培的蛹虫草多糖含量测定发现:多糖含量最多的是大米培养基菌丝体,然后依次是深层发酵液菌丝体、以大米为培养基的人工栽培蛹虫草子座、以蚕蛹为培养基质的人工栽培蛹虫草子座,而野生蛹虫草子座多糖的含量最低。目前关于蛹虫草多糖的报道大多仅限于含量分析、单糖的组成分析,或是糖苷键连接方式的分析,真正解析清楚的多糖结构还比较有限。通过对已经报道的文献整理,蛹虫草中提取出的多糖有:P70-1、P70-2、P50-1、CPS-1、CPS-2、CPS-3、CMB、CM-1、CPSN Fr-I、CPSN Fr-II、CPSN Fr-III、CBP-1、CPMN Fr III、CMP-1等,其具体信息如表2所示。酸的含量不如野生蛹虫草和人工培育的蛹虫草。证明蛹虫草较蛋白质和氨基酸含量丰富的蚕蛹更能为人体提供必需氨基酸,表3总结了一些目前在蛹虫草中发现的多肽类物质。
表2 蛹虫草中的多糖类成分
Table2 Polysaccharide components in C. militaris
注:-.结构不清。
名称 结构信息 来源 参考文献P70-1以(1→6)-α-D-吡喃甘露糖为骨架,α-D吡喃葡萄糖和β-D-吡喃半乳糖与主链(1→3)相连形成糖苷键,产生两条支链,最后这两条支链分别与β-D-吡喃半乳糖(1→4)相连,α-吡喃葡萄糖(1→6)相连蛹虫草子实体 [20]P70-2 - 蛹虫草子实体 [20]P50-1 - 蛹虫草子实体 [20]CPS-1 主链由甘露糖(1→2)相连,木糖(1→4)相连,鼠李糖和半乳糖(1→2)或(1→3)相连 培养的蛹虫草 [21]CPS-2主链由α-D-葡萄糖(1→4)相连或α-D-甘露糖(1→3)相连构成,在支链上平均每隔12 个残基就有一个α-D-葡萄糖以(1→4,6)相连培养的蛹虫草 [21]CPS-3主链α-D-葡萄糖(1→4)相连和α-D-葡萄糖(1→6)相连,按物质的量比0.11∶0.86构成糖苷键,并且每隔8 个葡萄糖残基的C6位发生一次取代形成侧链培养的蛹虫草 [21]CMB 主链由甘露糖(1→6)相连,葡萄糖(1→4,6)相连,半乳糖(1→4)相连 蛹虫草菌丝体 [6]CM-1 以β-甘露糖(1→2)相连为骨架,在主链半乳糖的C4和C6位上与β-呋喃半乳糖(1→6)相连形成侧链 蛹虫草培养液 [6]CPSN Fr-I - 蛹虫草肉汤培养液 [6]CPSN Fr-II以D-吡喃甘露糖(1→2)和(1→6)相连构成骨架,通常在O6位出现分支,分支主要由(1→4)-D-吡喃半乳糖和末端的D-吡喃半乳糖组成,分支比为0.2蛹虫草肉汤培养液 [6]CPSN Fr-III - 蛹虫草肉汤培养液 [6]CBP-1以(1→4)-α-D-甘露糖为骨架,并偶尔会在O3位出现分支,分支主要由(1→4)-α-D-葡萄糖、(1→6)-β-D-半乳糖和末端的(1→6)-β-D-半乳糖组成培养的蛹虫草 [22]CPMN Fr III 主链以β-半乳葡甘露聚糖(1→6)相连 蛹虫草菌丝体 [23]CMP-1以(1→4)-α-D-葡萄糖和(1→6)-α-D-葡萄糖为骨架,通常在O6位出现分支,分支由(1→6)-β-L-鼠李糖和末端的(1→3)-α-D-葡萄糖构成培养的蛹虫草 [24]APS 主要由D-呋喃阿拉伯糖(1→4)和(1→5)相连以及D-吡喃半乳糖(1→1)和(1→4)相连构成 蛹虫草菌丝体 [25]W-CBP50 II - 蛹虫草子实体 [26]CM-hs - 蛹虫草子实体 [27]SU-08 - 蛹虫草菌丝体 [28]
表3 蛹虫草中的多肽物质
Table3 Polypeptides in C. militaris
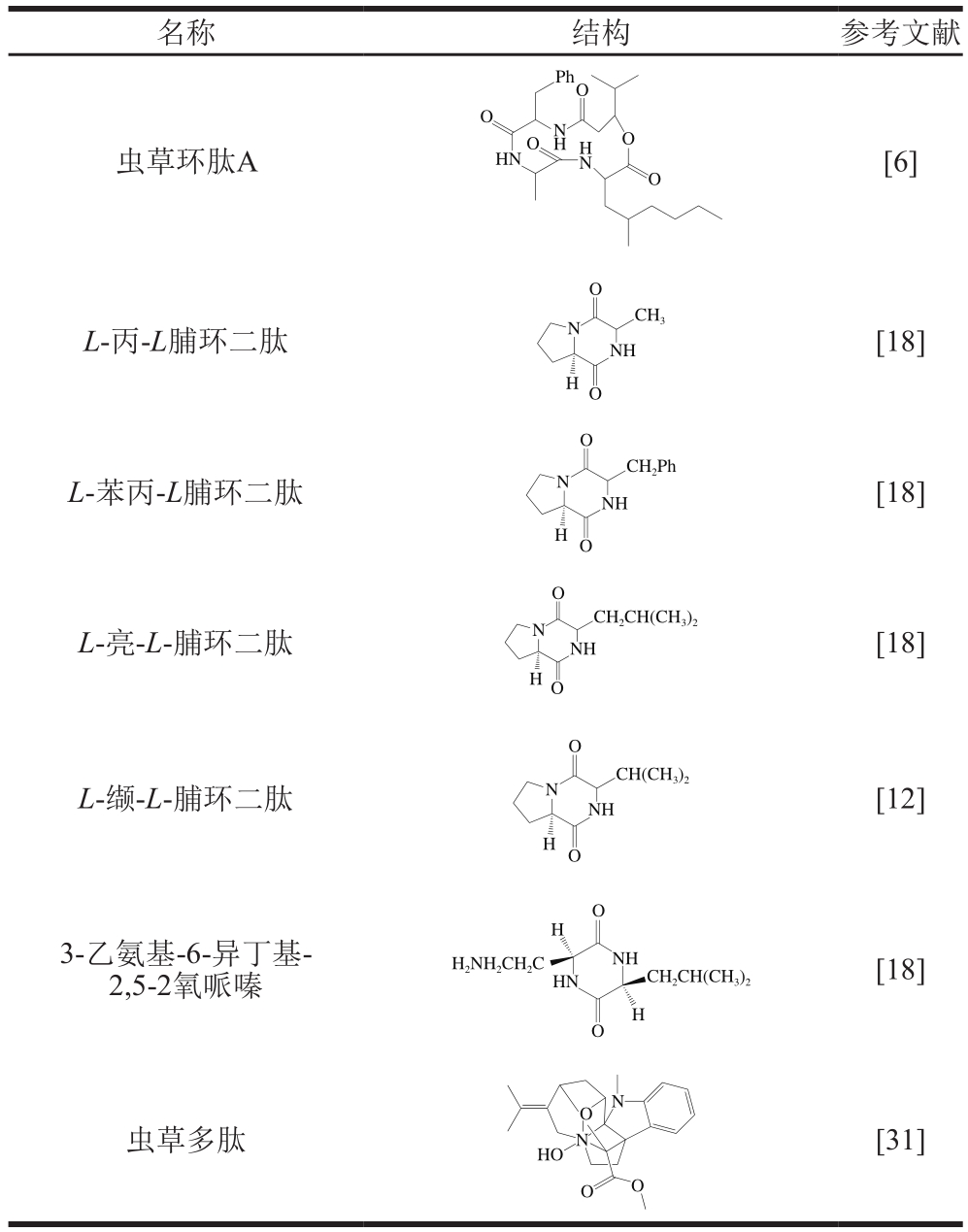
名称 结构 参考文献Ph O O O虫草环肽A HNONHHNO[6]L-丙-L脯环二肽L-苯丙-L脯环二肽L-亮-L-脯环二肽L-缬-L-脯环二肽3-乙氨基-6-异丁基-2,5-2氧哌嗪O N CH3NH H O O N CH2Ph NH H O O N NH CH2CH(CH3)2H O O N CH(CH3)2NH H O O H H2NH2CH2C CH2CH(CH3)2NH HN O H[18][18][18][12][18]O N虫草多肽HON [31]O O
1.3 蛋白质、多肽和氨基酸
无论是天然虫草还是人工培养的蛹虫草菌丝体或子实体,均含有丰富的氨基酸。Chan等[29]对蛹虫草CBS-132098的子实体和液体发酵得到的菌丝体中的氨基酸种类和含量进行研究,发现蛹虫草子实体中含有的氨基酸包括谷氨酸、色氨酸、精氨酸、赖氨酸、天冬氨酸、组氨酸、络氨酸、丙氨酸、苏氨酸、缬氨酸、丝氨酸、亮氨酸、甘氨酸、苯丙氨酸、异亮氨酸、磺基丙氨酸和蛋氨酸,而在菌丝体中除了检测不到磺基丙氨酸和蛋氨酸,其他氨基酸均可检测到。在子实体中,含量最高的氨基酸是谷氨酸、赖氨酸和天冬氨酸,而在菌丝体中,含量最高的氨基酸是甘氨酸和丙氨酸。陈策[30]通过对野生蛹虫草与人工培养蚕蛹虫草(全草)、大米培养蛹虫草子实体、蚕蛹的氨基酸含量进行测定,结果表明:野生蛹虫草中所含有的各种氨基酸,在不同培养基的人工培养虫草子实体及寄主蚕蛹中都有存在,虽然作为宿主的蚕蛹的总氨基酸含量最高,但其人体必需氨基
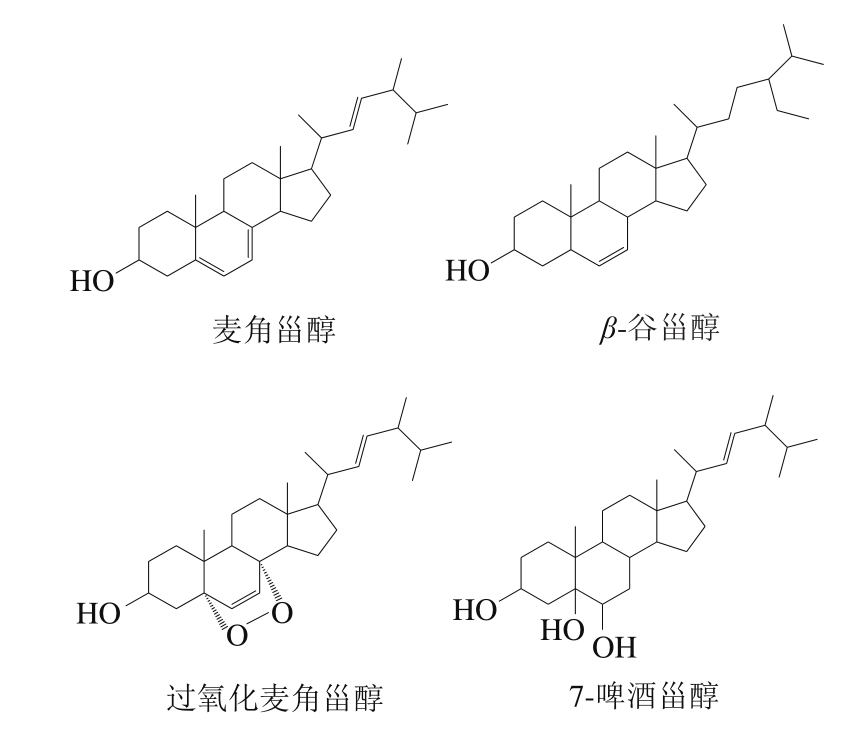
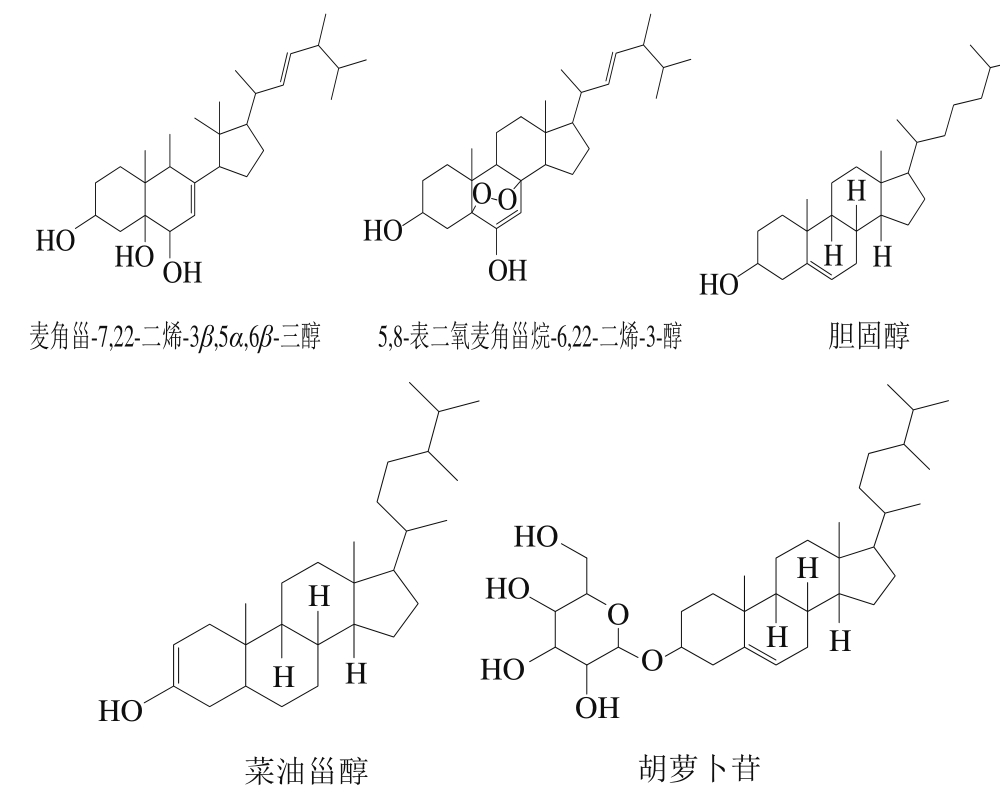
1.4 虫草甾醇和糖醇类成分
蛹虫草中具有代表性的甾醇类成分主要是麦角甾醇,其在虫草属真菌中含量相对恒定,通常作为蛹虫草质量控制指标之一。此外,在蛹虫草中发现的甾醇类物质还有β-谷甾醇、过氧化麦角甾醇、7-啤酒甾醇和麦角甾-7,22-二烯-3β,5α,6β-三醇等,如图1所示。
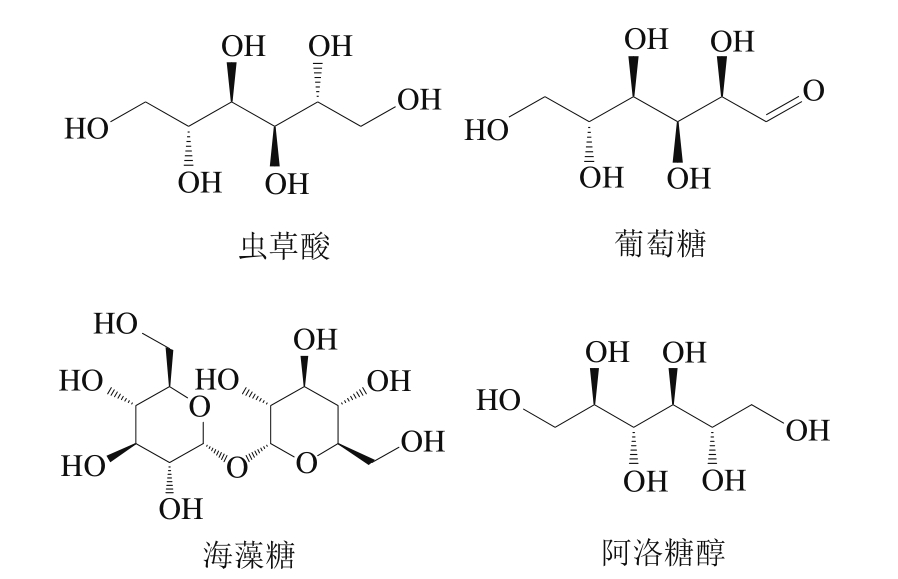
而蛹虫草中的糖醇主要为虫草酸,即D-甘露糖醇,是虫草类真菌中的主要有效成分之一,此外在蛹虫草中还发现葡萄糖、阿洛糖醇、海藻糖等糖醇,如图2所示。
1.5 酶类
虫草菌为了能够更好地侵入寄主体内并有效利用寄主的营养成分,往往会分泌出多种生物酶类,这些酶类一方面可以通过分解昆虫表皮和体壁来帮助菌体进入寄主体内;另一方面还能通过降解寄主中的一些大分子营养物质,为菌体的生长提供营养[34]。目前在蛹虫草中发现的生物酶类主要有纤维蛋白溶解酶[35]、几丁质酶[34]、超氧化物歧化酶(superoxide dismutase,SOD)[36]、类胰岛素蛋白[37]、淀粉酶[38]、多酚氧化酶、过氧化氢酶(catalase,CAT)、脱氢酶等[39]。
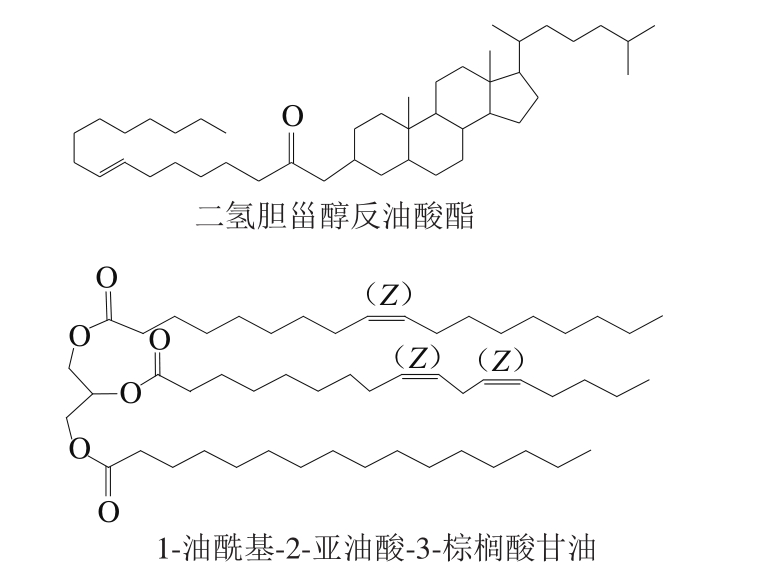
1.6 有机酸类成分
在蛹虫草中能够检测到多种有机酸类物质,包括棕榈酸、棕榈油酸、硬脂酸、油酸、亚油酸、亚麻酸、花生酸、琥珀酸[40],以及一些有机酸衍生物,如二氢胆甾醇反油酸、1-油酰基-2-亚油酸-3-棕榈酸甘油等,结构如图3所示。
1.7 色素
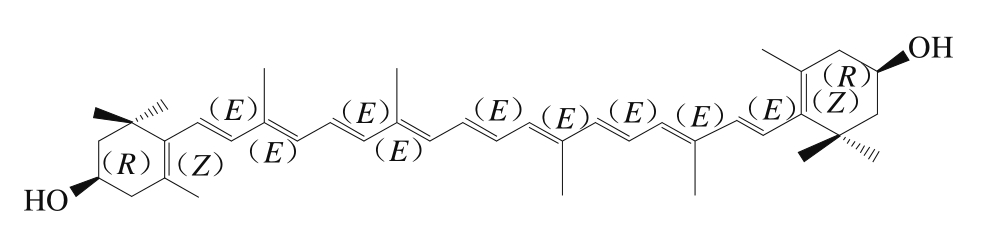
Dong等[41]从蛹虫草的子实体分离纯化得到了4 种水溶性极强的类胡萝卜素,并分别命名为北虫草黄素-I(Cordyxanthin-I)、北虫草黄素-II(Cordyxanthin-II)、北虫草黄素-III(Cordyxanthin-III)和北虫草黄素-IV(Cordyxanthin-IV)。这4 种类胡萝卜素的量占蛹虫草中总类胡萝卜素的86.7%。水溶性类胡萝卜素,与传统的类胡萝卜素相比,其理论上具有更强的潜在生理活性。此外,陈策[30]采用薄层色谱法、紫外-可见吸收光谱分析法、液相色谱-质谱联用等多种鉴定方法,对人工蛹虫草氯仿层提取物中的化合物进行了鉴定,最终鉴定为玉米黄素,结构如图4所示。
1.8 维生素和微量元素
蛹虫草中还含有多种维生素,包括VA、VB1、VB2、VB6、VB12、VC、VD、VE、烟酸和胡萝卜素等。蛹虫草中含有30多种无机元素,其中含量较高的元素有钾、磷、硫、镁、钙、钠、铁、铜等元素。从野生蛹虫草和人工培养的蛹虫草均能检出这些微量元素的存在[42]。此外,目前研究较热的蛹虫草富硒培养,通过在培养基中添加硒,可以大大提高蛹虫草中虫草素、腺苷、多糖和虫草酸的含量[43-44],同时增强某些生理活性,如抗氧化性、神经保护性等[45-46]。
1.9 其他成分
蛹虫草中还含有其他类成分,如含氮杂环化合物[18,40,47-48]、含氧杂环化合物[49]、内酯化合物[50]、黄酮类化合物[18]、神经酰胺类化合物[51],详见表4。
表4 蛹虫草中其他类化合物
Table4 Other compounds in C. militaris
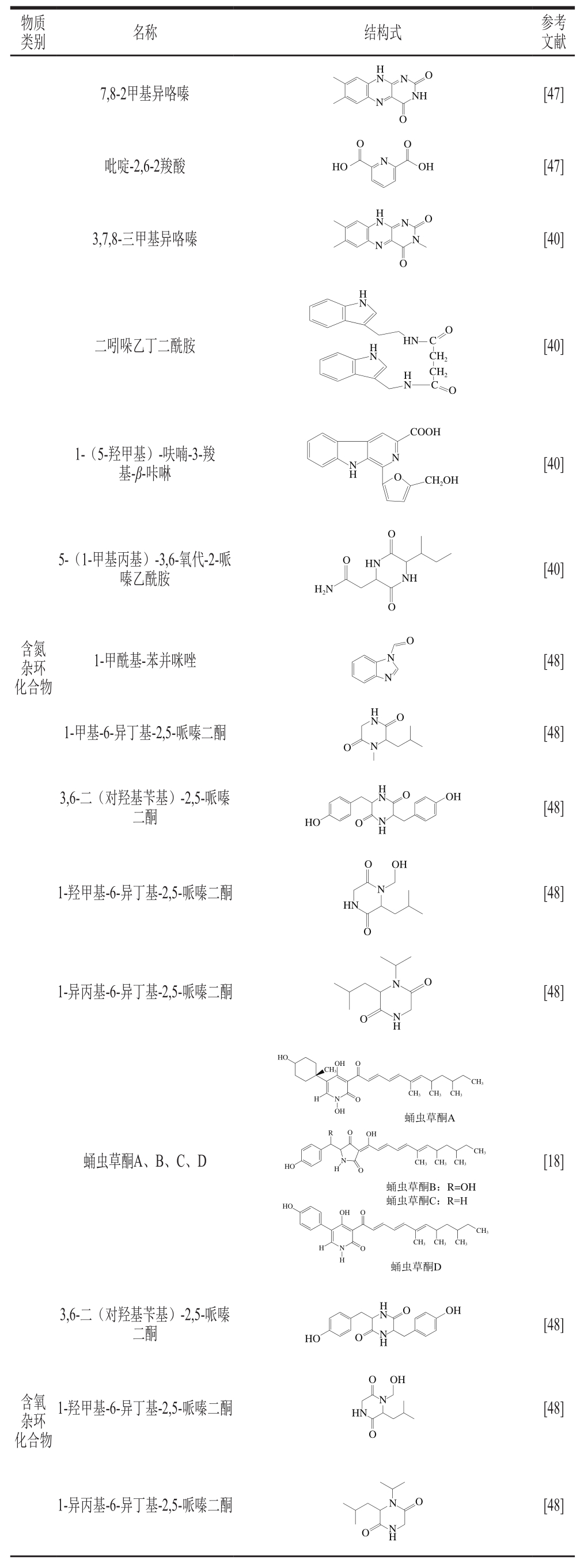
类别 名称 结构式 参考文献物质HN 7,8-2甲基异咯嗪NN O NH O[47]O O吡啶-2,6-2羧酸HO N OH [47]HN 3,7,8-三甲基异咯嗪NN O N O[40]HN二吲哚乙丁二酰胺H N HNC O CH2HN CH2C O[40]1-(5-羟甲基)-呋喃-3-羧基-β-咔啉NH COOH N O CH2OH[40]5-(1-甲基丙基)-3,6-氧代-2-哌嗪乙酰胺含氮杂环化合物1-甲酰基-苯并咪唑1-甲基-6-异丁基-2,5-哌嗪二酮3,6-二(对羟基苄基)-2,5-哌嗪二酮O O HN NH H2N O O N N H N O O N O HO O HN NH[40][48][48]OH[48]O OH 1-羟甲基-6-异丁基-2,5-哌嗪二酮NHN[48]O 1-异丙基-6-异丁基-2,5-哌嗪二酮O[48]O N NH HO OH CH3O H N O CH3CH3CH3CH3OH蛹虫草酮A R O OH CH3蛹虫草酮A、B、C、DHONH CH3CH3CH3O [18]HO OH蛹虫草酮B:R=OH蛹虫草酮C:R=H O H N O CH3CH3CH3CH3H蛹虫草酮D 3,6-二(对羟基苄基)-2,5-哌嗪二酮O OH [48]HO O HN NH O OH含氧杂环化合物1-羟甲基-6-异丁基-2,5-哌嗪二酮NHN[48]O 1-异丙基-6-异丁基-2,5-哌嗪二酮O[48]O N NH
续表4
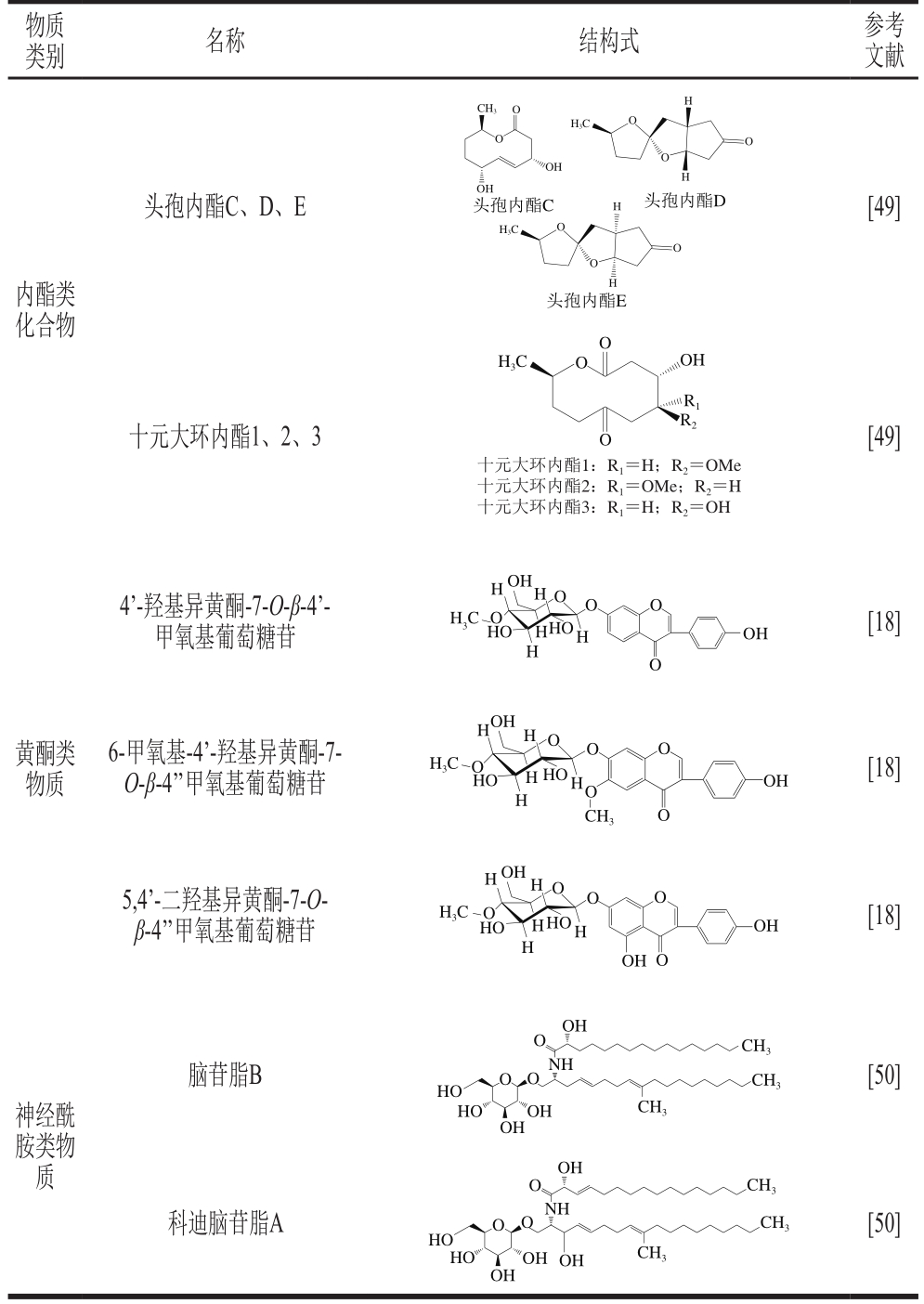
物质类别 名称 结构式 参考文献CH3H O H3C O O O OH O H头孢内酯C 头孢内酯D OH头孢内酯C、D、E H[49]H3C O O O内酯类化合物H头孢内酯E O H3C O OH R1十元大环内酯1、2、3R2O [49]十元大环内酯1:R1=H;R2=OMe十元大环内酯2:R1=OMe;R2=H十元大环内酯3:R1=H;R2=OH 4’-羟基异黄酮-7-O-β-4’-甲氧基葡萄糖苷OH H3C O H O O H O HO HO H H H OOH[18]黄酮类物质6-甲氧基-4’-羟基异黄酮-7-O-β-4’’甲氧基葡萄糖苷OH H3C O H O H O O HO HO H HHO CH3OOH[18]5,4’-二羟基异黄酮-7-O-β-4’’甲氧基葡萄糖苷OH H3C O H O O HO H O HO HOH[18]H H OHO OOH脑苷脂B CH3NH HO OO [50]神经酰胺类物质HO OH CH3CH3OH OH O CH3NH科迪脑苷脂A HO OO CH3[50]HO OH CH3OH OH
2 蛹虫草的生理活性
2.1 免疫调节作用
蛹虫草的免疫作用主要与虫草多糖有关。Liu Jingyu等[51]分别对雌雄昆明小鼠各24 只进行不同剂量的蛹虫草多糖(cordyceps militaris polysaccharides,CMP)灌胃给药。术后30 d发现,CMP给药组的白细胞水平,胸腺和脾脏的质量与对照组比较有明显提高,CMP在小鼠体内具有显著的抗氧化活性,并能够降低丙二醛(malondialdehyde,MDA)水平和上调肿瘤坏死因子-α、干扰素-γ和白细胞介素-1β mRNA的表达,与对照组相比有显著性差异。所以可以推断,蛹虫草对机体免疫功能的提高,可能与CMP对氧化应激的保护有关。而Song Jingjing等[52]的进一步研究表明,这种氧化应激保护作用与核因子(nuclear factor-κB,NF-κB)通路被抑制有关。此外,Li Yan等[53]发现蛹虫草中的虫草素对脂多糖(lipopolysaccharide,LPS)诱导的髓核细胞和椎间盘基质的降解和巨噬细胞浸润有保护作用。蛋白质印迹和荧光素酶测定结果表明,这种保护作用与抑制LPS诱导NF-κB通路的激活有关。
2.2 抗氧化及延缓衰老作用
Yu等[54]研究发现蛹虫草的抗氧化能力与其虫草素和腺苷的含量没有很明显的关系,其抗氧化能力可能是因为蛹虫草中的虫草多糖、多酚和类黄酮等物质具有清除自由基的能力。不少研究也显示,在相同多糖质量浓度条件下,蛹虫草胞外多糖粗品的清除效果均稍优于纯化品[55-56]。这可能与蛹虫草胞外多糖粗品中可能还含有类胡萝卜素和硒等成分有关,它们可能对蛹虫草胞外多糖的抗氧化效果产生协同增效作用。王奇[57]通过给老年Wistar大白鼠喂服蛹虫草,结果发现蛹虫草对老年大鼠血清、脑组织中的氧自由基和过氧化脂质体(lipid peroxides,LPO)有明显的清除作用,SOD和CAT的活性显著提升。此外还发现,蛹虫草对衰老大鼠的运动机能、内脏器官机能,以及生殖能力均有一定的改善功效。
2.3 抑菌作用
蛹虫草具有良好的抑菌作用,其主要抑菌成分虫草素已被证实对枯草芽孢杆菌、鸟结核杆菌、牛型结核分枝杆菌、链球菌、鼻疽杆菌、炭疽杆菌、葡萄球菌等病原细菌,以及一些皮肤致病性真菌如小芽孢癣菌及须疮癣菌等的生长具有抑制作用[58]。除此之外,Yu Rongmin等[59]提取得到的虫草多糖CPS-1,Kim等[60]从子实体中分离出的丝氨酸蛋白酶,Park等[61]从子实体中分离纯化出的蛋白CMP以及Wong等[62]从蛹虫草发酵液中分离得到的多肽Cordymin等,均具有一定的抑菌功效。高燕燕等[63]的研究发现,蛹虫草的水溶性提取物抑菌效果明显优于脂溶性提取物,推测这可能与水溶性提取物中含有较多的多糖,多肽和蛋白质类成分有关。
2.4 抗病毒、抗肿瘤作用
蛹虫草子实体和菌丝体的抗病毒、抗肿瘤的作用已被大量文献报道,其具体的作用机理也一直是人们关注和研究的热点。Bizarro等[64]为了进一步研究蛹虫草的抗肿瘤机制,采用非小细胞肺癌细胞系(NCI-H460)作为模型,经蛹虫草的醇提物作用后,癌细胞增殖减少,诱导G0/G1期细胞周期停滞,细胞凋亡增加,p53和p21的水平升高,并且指示DNA损伤的p-H2A.X和53BP1水平也升高。结果表明,该提取物通过涉及DNA损伤和p53激活的机制影响NCI-H460细胞活力。Song Jingjing等[65]对蛹虫草水提物在人乳腺癌细胞株MCF-7与人肝癌HepG2细胞的体内外模型中的抗肝癌和抗乳腺癌作用进行了研究,发现蛹虫草水提物对肝癌和乳腺癌的细胞毒性作用与半胱天冬氨酸依赖性的线粒体途径相关。
关于蛹虫草的抗病毒作用,杜秀菊等[66]对不同溶剂提取相(氯仿相、乙醇相、乙酸乙酯相)的蛹虫草子实体的抗病毒作用进行研究,发现仅氯仿相具有抗疱疹病毒HSV-I和HSV-II的活性,而无抗流感甲型病毒活性。随后的研究又发现,蛹虫草的7 个醇提物中仅有两个具有抗流感甲型病毒活性,而无抗抗疱疹病毒活性[67]。由此可见,蛹虫草的抗病毒活性与蛹虫草的来源及其提取的部位有着密切关系。
2.5 神经保护作用
蛹虫草的神经保护作用可能与其多糖和多肽类成分有关。Tsai等[68]利用超声辅助提取和DEAE-Sepharose CL-6B色谱柱分离和鉴定出了3 种蛹虫草多糖-肽类复合物(CPSP-F1、CPSP-F2、CPSP-F3),并发现它们对乙酰胆碱酯酶(acetylcholinesterase,AChE)具有一定的抑制活性,而对AChE的抑制增强了阿尔茨海默病患者的学习和认知能力。孙军德等[69]的研究也显示,蛹虫草多糖可以通过降低果蝇体内的氧化压力,来起到神经保护的作用。高峰等[70]用蛹虫草多肽对记忆障碍小鼠模型灌胃给药,持续45 d后,进行Morris水迷宫实验,并测定小鼠脑组织中AchE、Na+-K+-ATP酶、eNOS、γ-氨基丁酸(γ-aminobutyric Acid,GABA)和谷氨酸(glutamic acid,Glu)含量。结果表明:蛹虫草多肽能缩短小鼠寻找平台的潜伏期及增加穿越平台次数;降低小鼠脑组织AchE含量,升高Na+-K+-ATP、eNOS、GABA和Glu含量。说明蛹虫草多肽对记忆障碍小鼠学习记忆能力的改善可能与清除体内自由基、抗氧化损伤、保护神经系统等有关。此外,逄利等[71]发现,蛹虫草对脑缺血所致的神经细胞凋亡也有保护作用,其机制与抑制神经元凋亡、促进Bcl-2表达和抑制Bax表达有关。
2.6 性功能保护作用
虽然蛹虫草具有补益肝肾,壮阳益精的功效,临床上也常用来辅助治疗男性阳痿、早泄、遗精、遗尿、不育等性功能疾病,被誉为“男性能量补充剂”[72],但目前关于蛹虫草对性功能改善的直接证据并不多。Chang等[73]在7 周龄雄性Sprague-Dawley(SD)大鼠的饮食中添加蛹虫草菌丝体,与不添加蛹虫草的对照组相比,蛹虫草添加组大鼠体内的虫草素含量,以及附睾中精子的质量和数量都有明显提高,血清中的睾酮和雌二醇的浓度也有所上升。Sohn等[74]的研究也表明虫草素对年龄导致的SD大鼠睾丸功能下降有潜在的治疗作用。在不给虫草素的对照组中,中年组小鼠(12 月龄)与年轻组小鼠(2 月龄)相比,显示出附睾质量下降,精子活力下降,精子发生减少。但通过4 个月的虫草素治疗后,中年大鼠的附睾质量明显增加,且随虫草素剂量依赖性增加,精原细胞也具有更加良好的排列方式,曲细精管的精液中成熟精子数量明显增多。
2.7 降血脂保肝作用
蛹虫草的保肝、降血脂作用主要与其中的多糖、多肽以及一些酶类有关。侯金鑫等[75]对蛹虫草的液体发酵产物进行冻干处理,其冻干粉中主要含有一些粗纤维、粗多糖、粗三萜及黄酮类物质,能有效降低脂肪肝模型组小鼠血液中天冬氨酸氨基转移酶(aspartate aminotransferase,AST)与丙氨酸氨基转移酶(alanine aminotransferase,ALT)水平,并推测其保肝作用可能与降低肝脏中的氧化损伤有关。蛹虫草多肽可有效降低脂肪肝大鼠血清AST、ALT、总胆固醇(total cholesterol,TC)、甘油三酯(triglyceride,TG)及低密度脂蛋白(low density lipoprotein,LDL)含量,降低肝匀浆中MDA含量,提高SOD活力,同时改善血液流变学变化,对肝脏起保护作用[76]。蛹虫草残留多糖SU-12可以降低小鼠血液和肝脏脂质,并提高谷氨酸丙酮酸转氨酶和抗氧化活性。小鼠肝组织病理学观察表明,SU-12可以减轻肝细胞损伤[77]。此外,丛珊滋等[78]发现,含纤溶酶的蛹虫草培养液可有效降低具有高血脂倾向动物血液中TC、TG、LDL水平,同时可升高高密度脂蛋白水平,降低肝脏指数,对肝脏具有一定保护作用。
2.8 降血糖作用
蛹虫草具有良好的降血糖作用,其作用机制可能与清除体内自由基,提高机体和胰腺的抗氧化能力,修复受损的胰岛B细胞有关。徐雷雷等[79]将蛹虫草经超微粉碎后得精粉,用蒸馏水配制成悬浮液对糖尿病模型小鼠进行灌服,发现蛹虫草能显著降低糖尿病大鼠空腹血糖值,提高葡萄糖耐量,降低糖化血红蛋白和糖化血清蛋白含量。并且糖尿病模型大鼠肝脏和胰腺中的抗氧化酶SOD、CAT和谷胱甘肽过氧化物酶活力在经蛹虫草治疗后得到了提高。此外,对模型组胰岛组织的显微和亚显微结构观察,显示出蛹虫草对胰岛B细胞具有保护作用。Yu等[80]将蛹虫草的子实体和菌丝体粉末进行了组合,用C57BL/6J小鼠作为模型,评估蛹虫草组合物对高脂肪饮食诱导的Ⅱ型糖尿病的潜在降低血糖效应。通过测量体质量、空腹血糖、口服葡萄糖耐量实验和血液生化指标,发现蛹虫草组合物通过增加胰岛素敏感性来降低血糖水平,无明显体质量变化。此外,骨骼肌和脂肪组织中胰岛素受体底物-1、磷酸化胰岛素受体底物-1、蛋白激酶B、磷酸化蛋白激酶B、葡萄糖转运蛋白-4表达增加,进一步表明胰岛素信号传导恢复。
2.9 抗辐射作用
黄雅琴等[81-82]发现,适宜质量分数的蛹虫草粉能够修复紫外辐射对果蝇造成的中轻度损伤,并能通过抗氧化的途径来减轻紫外线给机体带来的氧化损伤。李华等[83]用8-甲氧补骨脂素联合长波紫外线制备小鼠皮肤光老化模型,在造模前给皮肤涂抹虫草多糖溶液,造模后24 h内取皮肤组织,进行苏木精-伊红染色和电子显微镜观察,并检测组织羟脯氨酸含量。结果发现,光老化组皮肤真皮层明显增厚,炎细胞浸润,皮脂腺不规则增生,纤维组织疏松紊乱,常见断裂,成纤维细胞形态不规则,内质网少;虫草多糖保护组明显改善,羟脯氨酸含量较光老化组明显增加。虫草多糖对皮肤的光老化的保护作用可能是通过影响TGF-β/Smad信号来实现的[84-85]。
3 蛹虫草发酵产物的应用
3.1 在食品方面的应用
在2009年,国家卫生部第3号文件正式批准蛹虫草为新资源食品。目前蛹虫草功能性食品的研发已经涉及多种类型食品,如虫草饮料[86-87]、虫草酸奶[88]、虫草酒[89]、虫草面包[90]、虫草酱油[91]、虫草八宝粥[92]等。蛹虫草发酵产物的应用形式大体上可以分为如下几种:蛹虫草子实体、固体培养基浸提液、深层发酵液或其匀浆、分离发酵液与菌丝体。这些制得的食品在保留原有的基本风味的基础上又增添了蛹虫草的独特风味,同时营养价值和保健功效也都得到了明显提升。此外,由于蛹虫草中的虫草素具有很好地抗菌功效,可以作为天然的防腐剂,进而减少配方中防腐剂的添加。
3.2 在医药保健品方面的应用
蛹虫草不仅具有很高的营养价值,同时也具有明显的药用价值,在医药和保健品中主要是用来补充机体能量,提高免疫能力,改善性功能以及抗疲劳等。蛹虫草的应用剂型也很丰富,并且常和一些具有保健功效的中药进行配伍,以增强其功效。如于汇等[93]将人参、玛卡等与蛹虫草配伍在一起,经过酵母菌发酵制得保健酒。安军[94]将枸杞粉、黄精粉、蛹虫草粉和蔗糖按一定比例混合制成片剂和胶囊剂;韩连云[95]将蛹虫草水提液与白砂糖、蜂蜜、果胶等调配制得的糖浆型口服液;徐亮[96]将蛹虫草与西洋参、桑葚配伍制得的颗粒剂;傅磊等[97]采用纳米粉碎技术,大幅度提高了蛹虫草中所含虫草素、虫草酸、虫草多糖、腺苷等的药效,虫草素含量达0.5%,腺苷含量达0.5%,且更易被人体吸收。此外,也有研究者将蛹虫草子实体提取物用于治疗乳腺癌的保健品或药品开发,并且经乳腺癌化疗患者的临床实验证明,该提取物具有较好的促进化疗病人白细胞增生作用,可用于制备辅助治疗肿瘤的保健食品和药品[98]。
4 结 语
本文系统地总结了蛹虫草中核苷类、虫草多糖、虫草多肽、甾醇类、有机酸类、黄酮类以及内酯类等成分的化学结构,这一方面有助于通过这些结构来推测其构效关系,开发新的药品或保健品;另一方面有助于推动蛹虫草结构信息数据库的建立。活性成分种类的多样性也造就了蛹虫草具有多种药理作用,如免疫调节作用、抑菌作用、抗病毒、抗肿瘤作用、神经保护作用、性功能保护作用,以及抗辐射作用等,并能够广泛地应用于食品、医药、保健品中。
目前关于蛹虫草活性成分结构的研究仍然存在很多不足,如蛹虫草中的多糖类和多肽类结构解析清楚的单体还十分有限,而且两者往往是以复合体的形式发挥活性功效,其具体的结合方式以及比例也有待进一步地研究。尽管蛹虫草相比于冬虫夏草有很多应用优势,如蛹虫草的原料成本更低,培育周期远短于冬虫夏草,已经通过人工培育实现了规模化生产,并且最近发表在Cell Chemical Biology上的一项研究表明,蛹虫草能够合成具有抗癌活性的药物喷司他丁,该化合物被用来保护所合成虫草素的结构稳定性,而冬虫夏草中无此活性成分[99]。虽然蛹虫草中虫草素远高于冬虫夏草,但蛹虫草并未因此而具有更强的抗肿瘤作用,多年来其仍然作为冬虫夏草的替代品而使用。与西药相比,中草药的功效是多途径、多靶点、多种活性物质共同作用的结果,所以必须加强完善蛹虫草中药指纹图谱和相关结构信息数据库的建立,同时可以借助计算机分子模拟的手段[100],对蛹虫草中的化学成分进行多途径和多靶点的研究,以进一步揭示蛹虫草的活性成分与其功效的关系,为其推广和应用提供更加科学的指导。
参考文献:
[1] 王奇. 蛹虫草功效成分研究进展[J]. 辽宁师专学报(自然科学版),2011, 13(3): 103-106.
[2] 姜雪, 王春月, 李兰洲, 等. 蝙蝠蛾拟青霉及蛹虫草与野生冬虫夏草活性比较[J]. 长春中医药大学学报, 2017, 33(4): 544-547.DOI:10.13463/j.cnki.cczyy.2017.04.010.
[3] ZHAO J, XIE J, WANG L Y, et al. Advanced development in chemical analysis of Cordyceps[J]. Journal of Pharmaceutical and Biomedical Analysis, 2014, 87: 271-289. DOI:10.1016/j.jpba.2013.04.025.
[4] 梅雪艳, 李媛媛, 沈于兰. 冬虫夏草、虫草菌丝体及蛹虫草中核苷类成分的测定[J]. 药学与临床研究, 2015, 23(1): 27-29.DOI:10.13664/j.cnki.pcr.2015.01.009.
[5] 汪宇, 杨光照, 康万军, 等. 高效液相色谱法测定天然冬虫夏草和蛹虫草及其人工培养物中3 个核苷类化合物含量[J]. 中国医院药学杂志, 2015, 35(9): 805-808. DOI:10.13286/j.cnki.chinhosppharmacyj.2015.09.11
[6] YUE K, YE M, ZHOU Z, et al. The genus Cordyceps: a chemical and pharmacological review[J]. The Journal of Pharmacy and Pharmacology, 2013, 65(4): 474-493. DOI:10.1111/j.2042-7158.2012.01601.
[7] 孟泽彬, 陈林会, 韩近雨, 等. 蛹虫草化学活性成分的研究进展[J]. 分子植物育种, 2015, 13(9): 2147-2154. DOI:10.13271/j.mpb.013.002147.
[8] 黄宝菊. 蛹虫草人工栽培研究进展[J]. 福建农业科技, 2015(1): 75-77. DOI:10.13651/j.cnki.fjnykj.2015.01.031.
[9] 田蕾. 三七双向发酵技术的研究[D]. 大连: 大连工业大学, 2015: 11-14.
[10] 王琳, 邱野, 徐瑶, 等. 参草菌质的发酵工艺研究[J]. 人参研究, 2014,26(2): 45-47. DOI:10.19403/j.cnki.1671-1521.2014.02.014.
[11] 李虎臣, 孙平, 冯成强. 蛹虫草中活性成分虫草素的研究进展[J]. 井冈山大学学报(自然科学版), 2010, 31(2): 93-96.
[12] 樊慧婷, 林洪生. 蛹虫草化学成分及药理作用研究进展[J]. 中国中药杂志, 2013, 38(15): 2549-2552. DOI:10.4268/cjcmm20131532.
[13] 易娟. 2’,3’-双脱氢-2’,3’-双脱氧腺苷和虫草素的化学合成研究[D].广州: 广东工业大学, 2013: 49-50.
[14] DAS S K, MASUDA M, HATASHITA M, et al. A new approach for improving cordycepin productivity in surface liquid culture of Cordyceps militaris using high-energy ion beam irradiation[J]. Letters in Applied Microbiology, 2008, 47(6): 534-538. DOI:10.1111/j.1472-765X.2008.02456.
[15] 施明珠. 昆虫激素对蛹虫草液体发酵培养的调控作用及蛹虫草菌丝体的药理学研究[D]. 合肥: 安徽农业大学, 2008: 11-15.
[16] 刘艳芳, 唐庆九, 杨焱, 等. 蛹虫草及其培养基中主要核苷类成分的分析比较[J]. 食品科学, 2010, 31(4): 139-142. DOI:1002-6630(2010)04-0139-04.
[17] ZONG S Y, HAN H, WANG B, et al. Fast simultaneous determination of 13 nucleosides and nucleobases in Cordyceps sinensis by UHPLCESI-MS/MS[J]. Molecules, 2015, 20(12): 21816-21825. DOI:10.3390/molecules201219807.
[18] 胡丰林, 李增智. 虫草及相关真菌的次生代谢产物及其活性[J]. 菌物学报, 2007, 26(4): 607-632. DOI:10.13346/j.mycosystema.2007.04.016.
[19] 来永斌, 王琦, 孙月. 蛹虫草多糖含量的测定与分析[J]. 中成药,2001, 23(7): 51-52. DOI:1001-1528(2001)07-0517-02.
[20] YU R M, YANG W, SONG L Y, et al. Structural characterization and antioxidant activity of a polysaccharide from the fruiting bodies of cultured Cordyceps militaris[J]. Carbohydrate Polymers, 2007, 70(4):430-436. DOI:10.1016/j.carbpol.2007.05.005.
[21] WANG Y, YIN H P, LÜ X B, et al. Protection of chronic renal failure by a polysaccharide from Cordyceps sinensis[J]. Fitoterapia, 2010,81(5): 397-402. DOI:10.1016/j.f i tote.2009.11.008.
[22] YU R M, YIN Y, YANG W, et al. Structural elucidation and biological activity of a novel polysaccharide by alkaline extraction from cultured Cordyceps militaris[J]. Carbohydrate Polymers, 2009, 75(1): 166-171.DOI:10.1016/j.carbpol.2008.07.023.
[23] LEE J S, KWON J S, YUN J S, et al. Structural characterization of immune stimulating polysaccharide from cultured mycelia of Cordyceps militaris[J]. Carbohydrate Polymers, 2010, 80(4): 1011-1017. DOI:10.1016/j.carbpol.2010.01.017.
[24] JING Y S, CUI X L, CHEN Z Y, et al. Elucidation and biological activities of a new polysaccharide from cultured Cordyceps militaris[J]. Carbohydrate Polymers, 2014, 102: 288-296.DOI:10.1016/j.carbpol.2013.11.061.
[25] WU F, YAN H, MA X, et al. Comparison of the structural characterization and biological activity of acidic polysaccharides from Cordyceps militaris cultured with different media[J]. World Journal of Microbiology & Biotechnology, 2012, 28(5): 2029-2038.DOI:10.1007/s11274-012-1005-6.
[26] CHEN X L, WU G H, HUANG Z L. Structural analysis andantioxidant activities of polysaccharidesfrom cultured Cordyceps militaris[J].International Joumal of Biological Macromolecules, 2013, 58: 18-22.DOI:10.1016/j.ijbiomac.2013.03.041.
[27] WU G H, HU T, HUANG Z L, et al. Characterization of water and alkali-soluble polysaccharides from Pleurotus tuber-regium sclerotia[J]. Carbohydrate Polymers, 2013, 96(1): 284-290.DOI:10.1016/j.carbpol.2013.03.036.
[28] FAN K M, MENG G Y, ZHOU B, et al. Intracellular polysaccharide and its antioxidant activity by Cordyceps militaris SU-08[J]. Journal of Applied Polymer Science, 2011, 120(3): 1744-1751. DOI:10.1002/app.33367.
[29] CHAN J S L, BARSEGHYAN G S, ASATIANI M D, et al. Chemical composition and medicinal value of fruiting bodies and submerged cultured mycelia of caterpillar medicinal fungus Cordyceps militaris CBS-132098 (Ascomycetes)[J]. International Journal of Medicinal Mushrooms, 2015, 17(7): 649-659. DOI:10.1615/IntJMedMushrooms.v17.i7.50.
[30] 陈策. 人工蛹虫草的化学成分研究[D]. 长春: 吉林农业大学, 2012:13-41.
[31] WONG K L, WONG R N, ZHANG L, et al. Bioactive proteins and peptides isolated from Chinese medicines with pharmaceutical potential[J]. Chinese Medicine, 2014, 9(19): 1-14. DOI:10.1186/1749-8546-9-19.
[32] DAS S K, MASUDA M, SAKURAI A, et al. Medicinal uses of the mushroom Cordyceps militaris: current state and prospects[J].Fitoterapia, 2010, 81(8): 961-968. DOI:10.1016/j.f i tote.2010.07.010.
[33] WANG S, YANG F Q, FENG K, et al. Simultaneous determination of nucleosides, myriocin, and carbohydrates in Cordyceps by HPLC coupled with diode array detection and evaporative light scattering detection[J]. Journal of Separation Science, 2009, 32(23/24): 4069-4076. DOI:10.1002/jssc.200900570.
[34] 顾宇翔, 李素霞, 袁勤生. 发酵蛹虫草菌丝体胞外几丁质酶活性研究[J]. 食品与发酵工业, 2009, 35(1): 48-52. DOI:10.13995/j.cnki.11-1802/ts.2009.01.004.
[35] 白伟芳, 郭丽琼, 林俊芳, 等. 蛹虫草产纤溶酶活性菌株的筛选及产酶条件的研究[J]. 现代食品科技, 2013, 29(5): 1014-1018.DOI:10.13982/j.mfst.1673-9078.2013.05.030.
[36] 周荣芬, 朱婧, 黄磊, 等. 蛹虫草中超氧化物歧化酶提取工艺的研究[J].现代预防医学, 2015, 42(20): 3770-3773.
[37] HATTORI M, ISOMURA S, YOKOYAMA E, et al. Extracellular trypsin-like proteases produced by Cordyceps militaris[J]. Journal of Bioscience and Bioengineering, 2005, 100(6): 631-636. DOI:10.1263/jbb.100.631.
[38] 张曦文, 赵博, 张国财, 等. 富硒对蛹虫草菌丝干重及胞内酶活性的影响[J]. 食品工业科技, 2017, 38(14): 151-155. DOI:10.13386/j.issn1002-0306.2017.14.030.
[39] 宋好倩. 蛹虫草生长营养特性及胞外酶活性的研究[D]. 新乡: 河南科技学院, 2017: 12-13.
[40] 马骁驰, 苟占平, 张宝璟, 等. 蛹虫草培养液成分研究II[J]. 现代生物医学进展, 2009(20): 3958-3961. DOI:10.13241/j.cnki.pmb.2009.20.018.
[41] DONG J Z, WANG S H, AI X R, et al. Composition and characterization of cordyxanthins from Cordyceps militaris fruit bodies[J]. Journal of Functional Foods, 2013, 5(3): 1450-1455.DOI:10.1016/j.jff.2013.06.002.
[42] 郑壮丽, 黄春花, 梅彩英, 等. 蛹虫草国内外研究的新进展[J]. 环境昆虫学报, 2011, 33(2): 225-233. DOI:10.3969/j.issn.1674-0858.2011.02.015.
[43] 贲松彬, 黄子琪, 王莹, 等. 蛹虫草富硒条件优化及硒对其中主要活性成分的影响[J]. 食品科学, 2009, 30(17): 266-269.
[44] 翁梁, 温鲁. 硒和钙对蛹虫草活性物质含量的影响[J]. 北方园艺,2012(22): 159-161.
[45] 邵颖, 袁凤健, 陈安徽, 等. 富硒蛹虫草活性成分及抗氧化作用分析[J].食品工业, 2013, 34(4): 126-129.
[46] 孙军德, 侯静, 杨逸. 富硒蛹虫草多糖对鱼藤酮诱导伤害果蝇的保护功效[J]. 食品科学, 2013, 34(7): 266-269.
[47] 苏亮, 楼凤昌, 赵守训. 虫草头孢菌丝体化学成分的研究[J]. 药学进展, 2001, 25(1): 43-44.
[48] 郑健, 张宝璟, 舒晓宏, 等. 蛹虫草培养液成分研究[J]. 现代生物医学进展, 2009(16): 3125-3127.
[49] RUKACHAISIRIKUL V, PRAMJIT S, PAKAWATCHAI C, et al.10-membered macrolides from the insect pathogenic fungus Cordyceps militaris[J]. Journal of Natural Products, 2004, 67(11): 1953-1955.DOI:10.1021/np0401415.
[50] CHIU C P, LIU S C, TANG C H, et al. Anti-inf l ammatory cerebrosides from cultivated Cordyceps militaris[J]. Journal of Agricultural and Food Chemistry, 2016, 64(7): 1540-1548.
[51] LIU Jingyu, FENG Cuiping, LI Xing, et al. Immunomodulatory and antioxidative activity of Cordyceps militaris polysaccharides in mice[J]. International Journal of Biological Macromolecules, 2016, 86:594-598. DOI:10.1016/j.ijbiomac.2016.02.009.
[52] SONG Jingjing, WANG Yingwu, LIU Chungang, et al. Cordyceps militaris fruit body extract ameliorates membranous glomerulonephritis by attenuating oxidative stress and renal inf l ammation via the NF-κB pathway[J]. Food & Function, 2016, 7(4): 2006-2015. DOI:10.1039/c5fo01017a.
[53] LI Yan, LI Kang, MAO Lu, et al. Cordycepin inhibits LPS-induced inf l ammatory and matrix degradation in the intervertebral disc[J]. Peer J, 2016, 4: 1-21. DOI:10.7717/peerj.1992.
[54] YU H M, WANG B S, HUANG S C, et al. Comparison of protective effects between cultured Cordyceps militaris and natural Cordyceps sinensis against oxidative damage[J]. Journal of Agricultural and Food Chemistry, 2006, 54(8): 3132-3138. DOI:10.1021/jf053111w.
[55] 叶文姣, 冯武, 黄文, 等. 蛹虫草胞外多糖的体外抗氧化活性分析[J].华中农业大学学报, 2014, 33(5): 105-110. DOI:10.13300/j.cnki.hnlkxb.2014.05.043.
[56] 张俊生, 陈莉华, 朱士龙, 等. 节节草多糖的体外抗氧化活性[J]. 食品科学, 2013, 34(5): 86-89.
[57] 王奇. 蛹虫草的生物学特性及抗衰老功效研究[D]. 武汉: 华中农业大学, 2010: 70-73.
[58] 刘桂君, 周思静, 杨素玲, 等. 蛹虫草中虫草素的研究进展[J]. 食品科学, 2013, 34(21): 408-413. DOI:10.7506/spkx1002-6630-201321080.
[59] YU Rongmin, SONG Liyan, ZHAO Yu, et al. Isolation and biological properties of polysaccharide CPS-1 from cultured Cordyceps militaris[J]. Fitoterapia, 2004, 75(5): 465-472. DOI:10.1016/j.f i tote.2004.04.003.
[60] KIM J S, SAPKOTA K, PARK S E, et al. A fi brinolytic enzymefrom the medicinal mushroom Cordyceps militaris[J]. The Journal of Microbiology, 2006, 44(6): 622-631.
[61] PARK B T, NA K H, JUNG E C, et al. Antifungal and anticanceractivities of a protein from the mushroom Cordyceps militaris[J]. Korean Journal Physiology Pharmacology, 2009, 13: 49-54. DOI:10.4196/kjpp.2009.13.1.49.
[62] WONG J H, NG T B, WANG H, et al. Cordymin, an antifungal peptide from the medicinal fungus Cordyceps militaris[J]. Phytomedicine,2011, 18(5): 387-392.
[63] 高燕燕, 周礼红, 潘肇仪, 等. 蛹虫草抗菌活性物质的初步研究[J].广东农业科学, 2013, 40(11): 183-185; 238. DOI:10.16768/j.issn.1004-874x.2013.11.043.
[64] BIZARRO A, FERREIRA I C F R, SOKOVIC M, et al. Cordyceps militaris (L.) link fruiting body reduces the growth of a nonsmall cell lung cancer cell line by increasing cellular levels of p53 and p21[J]. Molecules, 2015, 20(8): 13927-13940. DOI:10.3390/molecules200813927.
[65] SONG Jingjing, WANG Yingwu, TENG Meiyu, et al. Cordyceps militaris induces tumor cell death via the caspase dependent mitochondrial pathway in HepG2 and MCF7 cells[J]. Molecular Medicine Reports, 2016, 13(6): 5132-5140. DOI:10.3892/mmr.2016.5175.
[66] 杜秀菊, 张劲松, 蔡连捷, 等. 北虫草体外抗病毒、抗肿瘤活性部位的筛选[J]. 食品科学, 2011, 32(17): 313-316.
[67] 杜秀菊, 张劲松, 贾薇, 等. 北虫草醇提物体外抗肿瘤和抗病毒活性的比较研究[J]. 食品工业, 2012, 33(1): 121-123.
[68] TSAI C H, YEN Y H, YANG J P. Finding of polysaccharidepeptide complexes in Cordyceps militaris and evaluation of its acetylcholinesterase inhibition activity[J]. Journal of Food and Drug Analysis, 2015, 23(1): 63-70. DOI:10.1016/j.jfda.2014.05.006.
[69] 孙军德, 侯静, 杨逸. 富硒蛹虫草多糖对鱼藤酮诱导伤害果蝇的保护功效[J]. 食品科学, 2013, 34(7): 266-269.
[70] 高峰, 谢丽亚, 苑广信, 等. 蛹虫草多肽提高小鼠学习记忆能力的作用及机制[J]. 中国继续医学教育, 2017, 9(2): 207-208. DOI:10.3969/j.issn.1674-9308.2017.02.119.
[71] 逄利, 凡文博, 董宁, 等. 蛹虫草对脑缺血损伤大鼠神经细胞凋亡的影响[J]. 中国中医药科技, 2016, 23(1): 37-39.
[72] 韦会平, 肖波, 胡开治. 蛹虫草药用价值考[J]. 中药材, 2004, 27(3):215-217.
[73] CHANG Y, JENG K C, HUANG K F, et al. Effect of Cordyceps militaris supplementation on sperm production, sperm motility and hormones in Sprague-Dawley rats[J]. The American Journal of Chinese medicine, 2008, 36(5): 849-859.
[74] SOHN S H, LEE S C, HWANG S Y, et al. Effect of long-term administration of cordycepin from Cordyceps militaris on testicular function in middle-aged rats[J]. Planta Medica, 2012, 78(15): 1620-1625. DOI:10.1055/s-0032-1315212.
[75] 侯金鑫, 张金秀, 赵晓静, 等. 蛹虫草液体发酵产物冻干粉的抗氧化活性及保肝作用[J]. 药物评价研究, 2014, 37(1): 25-29.DOI:10.7501/j.issn.1674-6376.2014.01.006.
[76] 蔡琦. 蛹虫草多肽对脂肪肝大鼠血脂及血流变的影响[D]. 长春: 吉林大学, 2016: 14-16; 24.
[77] WANG L Q, XU N, ZHANG J J, et al. Antihyperlipidemic and hepatoprotective activities of residue polysaccharide from Cordyceps militaris SU-12[J]. Carbohydrate Polymers, 2015, 131: 355-362.DOI:10.1016/j.carbpol.2015.06.016.
[78] 丛珊滋, 刘晓兰, 张雯舒, 等. 含纤溶酶的蛹虫草深层培养液抗脂功能性初探[J]. 农产品加工(学刊), 2014(10): 1-4. DOI:10.3969/jissn.1671-9646.
[79] 徐雷雷, 王静凤, 唐筱, 等. 蛹虫草降血糖作用及其机制研究[J].中国药理学通报, 2011, 27(9): 1331-1332. DOI:10.3969/j.issn.1001-1978.2011.09.037.
[80] YU S H, CHEN S Y, LI W S, et al. Hypoglycemic activity through a novel combination of fruiting body and mycelia of Cordyceps militaris in high-fat diet-induced type 2 diabetes mellitus mice[J]. Journal of Diabetes Research, 2015, 2015: 1-10. DOI:10.1155/2015/723190.
[81] 黄雅琴, 李尽哲, 段鸿斌, 等. 蛹虫草对紫外诱导果蝇氧化损伤的保护作用[J]. 食品科学, 2015, 36(21): 258-262. DOI:10.7506/spkx1002-6630-201521048.
[82] 黄雅琴, 李尽哲, 段鸿斌, 等. 蛹虫草对果蝇紫外辐照的保护作用[J]. 食用菌学报, 2014, 21(4): 45-48. DOI:10.16488/j.cnki.1005-9873.2014.04.005.
[83] 李华, 叶䁎杰, 李伯勤, 等. 虫草多糖对小鼠皮肤光老化的保护作用[J].时珍国医国药, 2008, 19(11): 2679-2681.
[84] KIM J A, AHN B N, KONG C S, et al. Chitooligomers inhibit UV-A-induced photoaging of skin by regulating TGF-β/Smad signaling cascade[J]. Carbohydrate Polymers, 2012, 88(2): 490-495.DOI:10.1016/j.carbpol.2011.12.032.
[85] CHEN T J, HOU H. Protective effect of gelatin polypeptides from Pacific cod (Gadus macrocephalus) against UV irradiation-induced damages by inhibiting inflammation and improving transforming growth factor-beta/Smad signaling pathway[J]. Journal of Photochemistry and Photobiology B: Biology, 2016, 162: 633-640.DOI:10.1016/j.jphotobiol.2016.07.038.
[86] 李尽哲, 黄雅琴, 叶兆伟. 蛹虫草银杏叶保健饮料的研制[J]. 中国酿造, 2015, 34(12): 175-178. DOI:10.11882/j.issn.0254-5071.2015.12.039.
[87] 钟艳梅, 罗新强, 郑清梅. 利用蛹虫草培养残基制作发酵型含乳饮料的研究[J]. 广东农业科学, 2011, 38(11): 121-123. DOI:10.16768/j.issn.1004-874x.2011.11.009.
[88] 樊琴, 邓功成, 张娟, 等. 蛹虫草发酵酸奶研制试验[J]. 现代农业科技, 2015(11): 307-309.
[89] 钟艳梅, 徐智斌, 曾宪录. 利用蛹虫草培养残基酿制保健型发酵酒的工艺研究[J]. 现代食品科技, 2011, 27(5): 555-558. DOI:10.13982/j.mfst.1673-9078.2011.05.027.
[90] 朱蕴兰, 宋慧, 周卫东, 等. 蛹虫草面包的研制[J]. 食品科技, 2009,34(4): 136-137. DOI:10.13684/j.cnki.spkj.2009.04.031.
[91] 李林波, 边红杰, 崔建东. 蛹虫草保健酱油的工艺研究[J]. 中国调味品, 2016, 41(7): 100-103. DOI:10.3969/j.issn.1000-9973.2016.07.021.
[92] 何洋, 刘林德, 苏志坚, 等. 蛹虫草八宝粥的研制[J]. 安徽农业科学, 2011, 39(19): 11973-11974; 11983. DOI:10.13989/j.cnki.0517-6611.2011.19.053.
[93] 于汇, 徐斌, 宫敬利, 等. 人参玛卡蛹虫草壮阳酒:201610084650.8[P]. 2016-04-13[2017-10-09].
[94] 安军. 一种益肾养生、强身健体的保健品及制备方法:201410219675.5[P]. 2014-08-27[2017-10-09].
[95] 韩连云. 虫草口服液及其制备方法: 201010228002.8[P]. 2010-11-24[2017-10-09].
[96] 徐亮. 一种增强免疫力的蛹虫草颗粒及其制备方法:201610727741.9[P]. 2016-12-07[2017-10-09].
[97] 傅磊, 徐宇虹, 李晓波, 等. 提高虫草素、多糖、腺苷生物利用率的纳米蛹虫草粉制法: 201310139088.0[P]. 2013-08-07[2017-10-09].
[98] 吴美兰, 吴更余, 李秋洋, 等. 蛹虫草子实体提取物在制备促进乳腺癌患者白细胞增生功能保健品或药品中的应用:201210121285.5[P]. 2012-08-01[2017-10-09].
[99] XIA Y L, LUO F F, SHANG Y F, et al. Fungal cordycepin biosynthesis is coupled with the production of the safeguard molecule pentostatin[J]. Cell Chemical Biology, 2017, 24(12): 1-11.DOI:10.1016/j.chembiol.2017.09.001.
[100] 乔连生, 张燕玲. 计算机辅助药物设计在天然产物多靶点药物研发中的应用[J]. 中国中药杂志, 2014, 39(11): 1951-1955. DOI:10.4268/cjcmm20141101.
Research Achievements in Bioactive Components, Pharmacological Effects and Applications of Cordyceps militaris
ZUO Jinhui, GONG Xiaoyan, DONG Yinmao, LI Li*
(Beijing Key Laboratory of Plants Resource Research and Development,Beijing Technology and Business University, Beijing 100048, China)
Abstract:In this paper, the structures of bioactive components in Cordyceps militaris, such as nucleosides, polysaccharides,polypeptides, sterols and organic acids, are summarized. The recent domestic and oversea studies on pharmacological effects of Cordyceps militaris are reviewed, focusing on immunoregulatory, antibacterial, antiviral, antitumor, neuroprotective,sexual function-enhancing, and anti-radiation effects. Finally, the applications of Cordyceps militaris in the fields of food,medicine, health care and cosmetics are summarized.
Keywords:Cordyceps militaris; bioactive component; pharmacological effect; application
ZUO Jinhui, GONG Xiaoyan, DONG Yinmao, et al. Research achievements in bioactive components, pharmacological effects and applications of Cordyceps militaris[J]. Food Science, 2018, 39(21): 330-339. (in Chinese with English abstract)DOI:10.7506/spkx1002-6630-201821049. http://www.spkx.net.cn
引文格式:左锦辉, 贡晓燕, 董银卯, 等. 蛹虫草的活性成分和药理作用及其应用研究进展[J]. 食品科学, 2018, 39(21): 330-339.DOI:10.7506/spkx1002-6630-201821049. http://www.spkx.net.cn
文章编号:1002-6630(2018)21-0330-10
文献标志码:A
中图分类号:TS201.1
DOI:10.7506/spkx1002-6630-201821049
*通信作者简介:李丽(1980—),女,副教授,博士,研究方向为化妆品植物原料。E-mail:lily2212@126.com
第一作者简介:左锦辉(1994—),男,硕士研究生,研究方向为化妆品植物原料。E-mail:843720054@qq.com
收稿日期:2017-10-09