表1 Plackett-Burman试验设计因素与水平
Table 1 Factors and their coded values used for Plackett-Burman design
于 平,黄星星,张一舒
(浙江工商大学食品与生物工程学院,浙江 杭州 310035)
摘 要:通过响应面法对枯草芽孢杆菌ZJS18发酵生产γ-聚谷氨酸的培养条件进行优化。首先采用Plackett-Burman试验设计筛选出对γ-聚谷氨酸产量有显著影响的3 个关键因素,即蔗糖、酵母粉和谷氨酸钠;然后通过Box-Behnken试验设计和响应面法对这3 个关键因素的用量进行优化。响应面优化后的3 个关键因素的最佳质量浓度为蔗糖64.40 g/L、酵母粉7.10 g/L和谷氨酸钠57.96 g/L。枯草芽孢杆菌ZJS18发酵生产γ-聚谷氨酸的最佳培养条件为蔗糖用量64.40 g/L、酵母粉用量7.10 g/L、谷氨酸钠用量57.96 g/L,氯化钠用量30 g/L,MgSO4用量0.3 g/L、K2HPO4用量2 g/L,初始pH 7.5,接种量5%,装液量40 mL/250 mL,温度37 ℃,摇床转速200 r/min,发酵时间36 h。在上述条件下,γ-聚谷氨酸产量为13.20 g/L。与未优化前相比,产量提高了1.88 倍。
关键词:枯草芽孢杆菌;γ-聚谷氨酸;培养条件;响应面法;优化
γ-聚谷氨酸是由L-谷氨酸和(或)D-谷氨酸通过α-氨基和γ-羧基之间的酰胺键连接而成[1]的一种水溶性、可生物降解和无毒性的生物高分子物质[2-4]。γ-聚谷氨酸通常由上千个谷氨酸单体组成,分子质量大约在1~200万 Da之间[5]。不同菌种产生的γ-聚谷氨酸的分子质量有所差异。γ-聚谷氨酸的特殊化学结构使其具有优良的保水性能,在农业上可用作保水剂[6]。此外,由于γ-聚谷氨酸的最终代谢产物为氨基酸,因此具有可生物降解、对人体无害无毒和无致免疫性的特点[7-8],已被广泛应用于环保、化妆品、食品[9]和医疗等行业,成为理想的绿色材料。
γ-聚谷氨酸的生产方法主要有化学合成法、酶转化法和微生物发酵法,微生物发酵法是目前最常用的方法之一。与其他方法相比,该法具有生产条件可工业化、生长周期相对较短、目标产物较易获得以及产量高等优点[10-12]。但目前我国通过微生物发酵法制备γ-聚谷氨酸存在生产成本高以及提取工艺复杂等缺点,难以实现大规模工业化生产和应用[13-14],因此筛选优良的生产菌株和优化其发酵条件仍是我国目前微生物发酵生产γ-聚谷氨酸主要研究热点之一。
在前期研究中,课题组从豆豉中筛选了一株能够合成γ-聚谷氨酸的枯草芽孢杆菌ZJS18,该菌株能够生产7.2 g/L的γ-聚谷氨酸。本研究拟通过响应面法对筛选的枯草芽孢杆菌ZJS18发酵生产γ-聚谷氨酸的培养条件进行优化,旨在进一步提高γ-聚谷氨酸产量,降低生产成本,从而为其工业化生产和应用提供指导。
实验所用菌株为枯草芽孢杆菌ZJS18,由课题组从豆豉中筛选获得,能够生产γ-聚谷氨酸。
蔗糖、酵母粉、氯化钠、无水乙醇、氢氧化钠、十六烷基三甲基溴化铵 生工生物工程(上海)有限公司;磷酸氢二钾、硫酸镁、谷氨酸钠 英国BBI公司;γ-聚谷氨酸标准品 南京赛泰斯生物技术有限公司;其他试剂均为分析纯。
Luria-Bertani(LB)液体培养基:蛋白胨10 g/L,酵母粉5 g/L,氯化钠10 g/L。种子培养基:葡萄糖20 g/L,酵母粉5 g/L,谷氨酸钠10 g/L,磷酸氢二钾2 g/L,硫酸镁0.25 g/L。基础发酵培养基:蔗糖60 g/L,酵母粉8 g/L,谷氨酸钠60 g/L,硫酸镁0.3 g/L,磷酸氢二钾2 g/L。
立式全自动高压灭菌锅 上海博讯实业有限公司;SKY-200B恒温摇床 上海苏坤实业有限公司;2K15型高速低温离心机 德国Sigma公司;UV-320PC紫外分光光度计 英国Mapada公司;SW-CJ-1FD型超净工作台苏州市金净净化设备科技有限公司;pH计 Mettler-Toledo仪器(上海)有限公司;Infinite M200多功能酶标仪美国Tecan公司。
1.3.1 种子培养
将200 µL甘油管保存的菌液接种于装有10 mL LB培养基的试管中,200 r/min、37 ℃恒温振荡培养12 h。按2%(体积分数,下同)的接种量将新鲜培养液接种于装有40 mL种子培养基的250 mL摇瓶中,200 r/min、37 ℃恒温振荡培养24 h,制备种子培养液。
1.3.2 摇瓶发酵培养
将种子培养液以5%的接种量接种于装有40 mL发酵培养基的250 mL摇瓶中进行发酵培养,37 ℃、200 r/min恒温振荡培养36 h。
1.3.3 Plackett-Burman试验设计
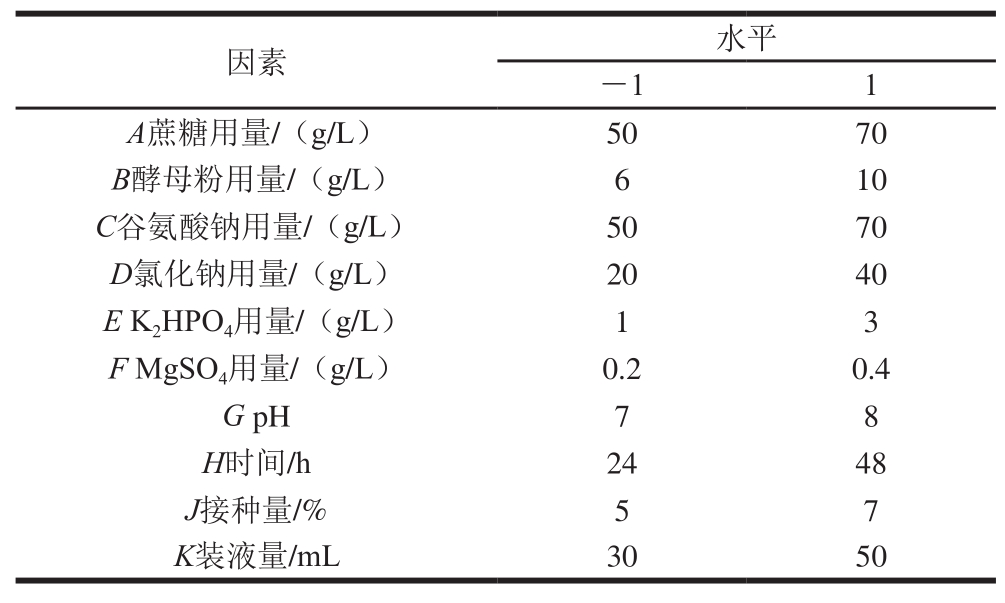
在前期单因素试验的基础上,选取对γ-聚谷氨酸产量影响较大的10 个因素,利用Design Expert 8.0软件对其进行N为12的Plackett-Burman试验设计,每个因素选高低2 个水平,以(-1,1)编码各值,以γ-聚谷氨酸产量作为响应值。每组试验设置3 个平行以减少试验误差[15]。Plackett-Burman试验设计的因素和水平如表1所示。
表1 Plackett-Burman试验设计因素与水平
Table 1 Factors and their coded values used for Plackett-Burman design

1.3.4 最陡爬坡试验确定响应面因素水平的中心点
根据表1试验数据的分析结果,可以从众多影响因素中筛选出3 个影响γ-聚谷氨酸产量的最显著因素,以此确定各因素的水平,表现为正效应的因素取高水平、负效应的因素取低水平。根据这3 个因素效应的大小设定变化的方向和步长,进行试验设计确定响应面分析的中心点。
1.3.5 Box-Behnken试验
根据Plackett-Burman试验分析结果和最陡爬坡试验确定的3 个显著影响因素用量的取值区间,进一步设计3因素3水平共17 个试验点的Box-Behnken响应面试验,其中12 个点是析因点,5 个点是中心复合点[16]。以3 个显著影响因素为响应面设计自变量,以γ-聚谷氨酸产量为响应值,每个因素的3 个水平以(-1,0,1)编码,每个试验点进行3 次平行减小试验误差[17-18]。其他因素的高低水平根据Plackett-Burman试验分析结果确定,表现为正效应的因素取高水平、负效应的因素取低水平。Box-Behnken试验设计的因素及水平如表2所示。
表2 Box-Behnken试验设计的因素与水平
Table 2 Factors and their coded values used for Box-Behnken design

1.3.6 摇瓶发酵实验
将200 µL甘油管保存的枯草芽孢杆菌ZJS18菌种接种于装有10 mL LB液体培养基的试管中,于37 ℃、200 r/min培养12 h后,以2%的接种量转接于装有40 mL种子培养基的250 mL摇瓶中,于37 ℃、200 r/min摇床中培养10 h。按5%的接种量将种子液接种到装有500 mL发酵培养基的1 L摇瓶中,于37 ℃、200 r/min的摇床中培养,每隔4 h取样测定发酵液中γ-聚谷氨酸产量。
1.3.7 γ-聚谷氨酸标准曲线的制作
γ-聚谷氨酸与十六烷基三甲基溴化铵-NaOH溶液反应会形成混悬液。配制2%的NaOH溶液,并以此为溶剂,加入十六烷基三甲基溴化铵,配制成5 g/L的十六烷基三甲基溴化铵溶液。
精确称取γ-聚谷氨酸,配制成8、16、24、32、40 μg/mL和48 μg/mL的γ-聚谷氨酸标准液,加入等体积的十六烷基三甲基溴化铵溶液,反应3 min后,用分光光度计测定反应液在250 nm波长处吸光度,绘制γ-聚谷氨酸的标准曲线[17-18]。
1.3.8 发酵液中γ-聚谷氨酸产量的测定
取1 mL发酵液,4 ℃、4 800 r/min离心25 min。取上清液250 μL,加入3 倍体积的无水乙醇,摇匀后4 ℃静置过夜,然后于8 000 r/min离心15 min。取沉淀,加入与发酵液等体积的蒸馏水溶解,即为样液。将样液稀释适当倍数后,测定其在250 nm波长处的吸光度[13]。将吸光度代入γ-聚谷氨酸标准曲线,得到相应γ-聚谷氨酸产量,再乘以稀释倍数,即发酵液中γ-聚谷氨酸产量。
Plackett-Burman试验设计、最陡爬坡试验设计以及Box-Behnken试验设计均采用Design Expert 8.0软件,数据处理采用Excel 2010软件,数据作图采用Origin 8.5.0软件。
以γ-聚谷氨酸标准溶液质量浓度为横坐标,吸光度(A250nm)为纵坐标,绘制γ-聚谷氨酸的标准曲线。对标准曲线进行回归模拟,得到方程:y=21.187 5x+0.001 1,R2=0.999 2,该标准曲线线性关系良好。
根据前期单因素试验结果,选取10 个对γ-聚谷氨酸产量影响较大的因素,通过Design Expert 8.0软件进行N为12的Plackett-Burman试验设计,试验设计及结果如表3所示。
表3 Plackett-Burman试验设计和结果
Table 3 Plackett-Burman design with experimental results

利用Design Expert 8.0软件对表3试验数据进行方差分析,结果如表4所示。
表4 Plackett-Burman 试验设计方差分析
Table 4 Analysis of variance (ANOVA) for the Plackett-Burman design
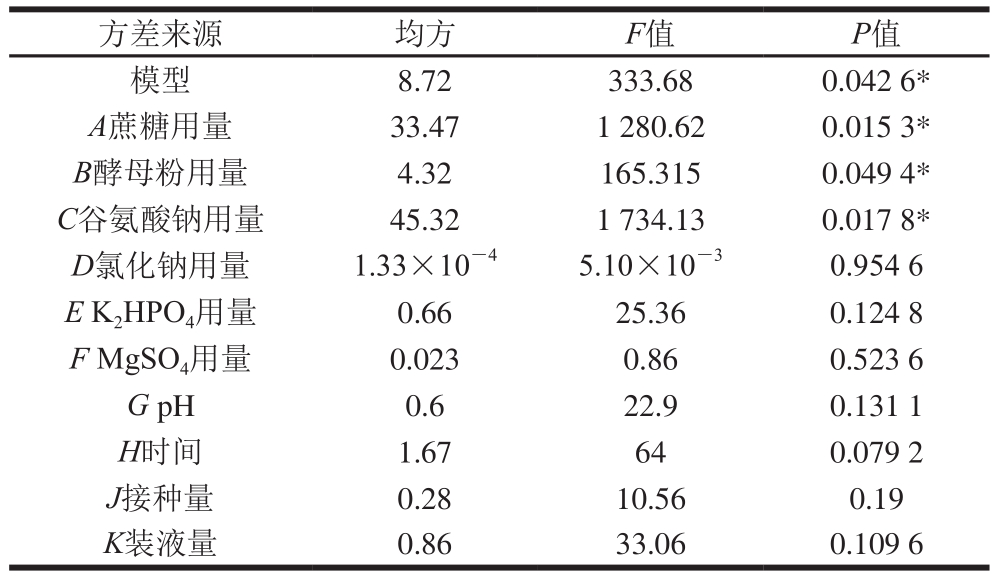
注:*.差异显著,P<0.05,表8同。
由表4可知,试验模型的P值小于0.05,表明该模型影响显著。蔗糖用量、酵母粉用量和谷氨酸钠用量3 个因素通过F检验后所得的P值均小于0.05,说明它们对γ-聚谷氨酸产量有显著影响,其中蔗糖用量的影响最为显著,因此选取这3 个因素为显著影响因素。此外,从表4还可以看出,酵母粉用量对γ-聚谷氨酸产量的影响呈现负效应,而蔗糖用量和谷氨酸钠用量的影响呈现正效应。
根据Plackett-Burman试验结果分析,确定蔗糖用量、谷氨酸钠用量和酵母粉用量3 个因素为影响γ-聚谷氨酸产量的显著性因素。根据这3 个因素效应的大小设定变化的方向及步长,进行最陡爬坡试验,确定中心点。最陡爬坡的试验设计及结果见表5。
表5 最陡爬坡试验设计及结果
Table 5 Steepest ascent design with experimental results
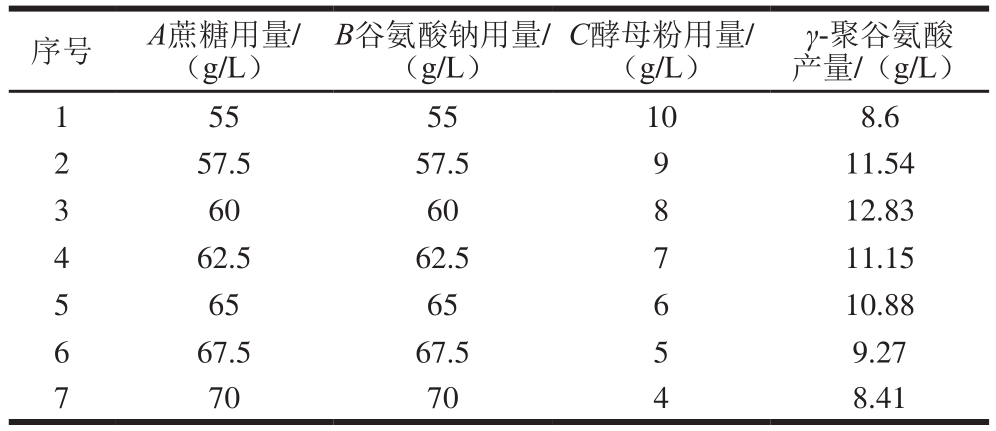
由表5可知,随着蔗糖、谷氨酸钠和酵母粉用量的变化,γ-聚谷氨酸产量呈现先上升后下降的趋势。当蔗糖、谷氨酸钠和酵母粉用量分别为60、60 g/L和8 g/L时,γ-聚谷氨酸产量最大,因此选择这3 个因素质量浓度为中心点,进行响应面分析。
通过Plackett-Burman试验筛选出了蔗糖、酵母粉和谷氨酸钠用量3 个主要影响因素,然后通过最陡爬坡试验确定主要影响因素的具体质量浓度的取值区间。以蔗糖、酵母粉和谷氨酸钠用量3 个显著影响因素作为响应面设计的自变量,以γ-聚谷氨酸产量作为响应值进行Box-Behnken试验,结果如表6所示。
表6 Box-Behnken试验设计与结果
Table 6 Box-Behnken design with experimental results

利用Design Expert 8.0软件对表6数据进行方差分析,结果如表7所示,回归模型的方差分析如表8所示。
表7 Box-Behnken试验结果分析
Table 7 Analysis of the experimental results of Box-Behnken design

表8 回归模型的方差分析
Table 8 Analysis of variance for regression model
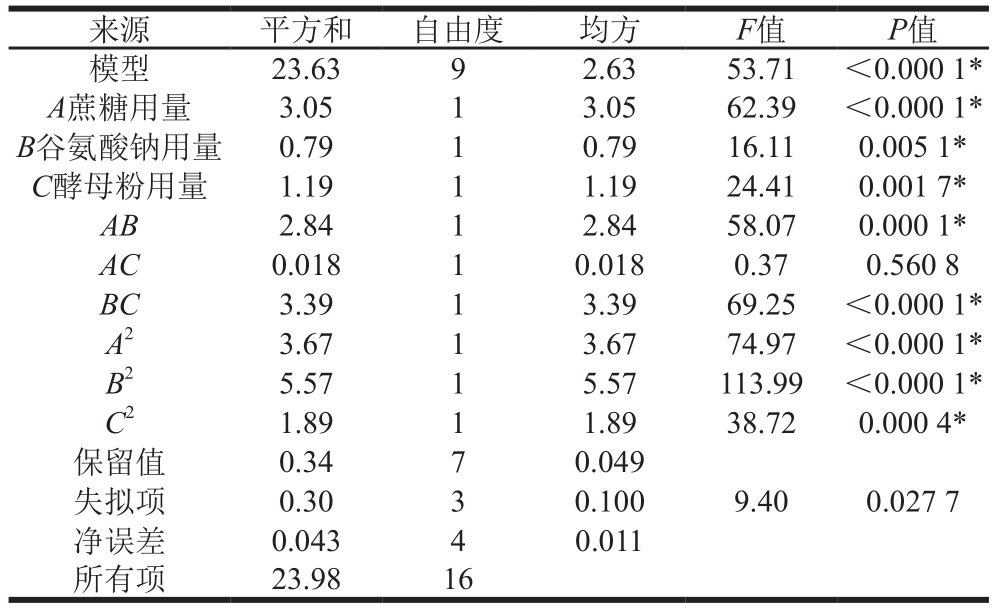
由表7、8可知,回归模型的R2值为0.985 7,F值为53.71,显著性水平P值小于0.000 1,说明该试验模型的自变量和因变量之间的函数关系显著,在P值为0.05的水平上足够拟合试验数据。失拟项的F值为9.40(P值0.027 7>0.01),说明失拟项不显著,即回归模型显著,该试验模型可信度高,可用来分析及预测最大值。校正系数为0.967 4,说明该模型能够解释96.74%的γ-聚谷氨酸产量的变化,模型拟合度好。
由表8可知,蔗糖、谷氨酸钠和酵母粉用量的P值均小于0.05,说明这3 个因素对γ-聚谷氨酸产量影响的线性效应显著,其中蔗糖用量的影响最为显著。AB、BC的P值也小于0.05,说明蔗糖和谷氨酸钠用量以及谷氨酸钠和酵母粉用量之间的交互作用显著。应用Design Expert 8.0软件对表6中的试验数据进行二次多项回归拟合,得到回归方程:Y=13.06+0.62A+0.31B-0.39C-0.84AB-0.067AC+0.92BC-0.93A2-1.15B2-0.67C2。
根据二次回归方程可以得到相应的响应面图以及等高线图,如图1所示。
响应面的等高线图可直观地反映出各因素的交互作用对响应值的影响,以便找出最佳工艺参数以及各参数之间的相互作用。如果等高线的形状是椭圆形,表示两因素的交互作用显著,而越接近圆形则表示不显著[19-20];并且在一条线上,所有的试验方案都可以得到相同的数值。响应面三维立体图能够反映出各因素之间的交互作用对响应值的影响,坡度越陡,影响越显著[21-22]。
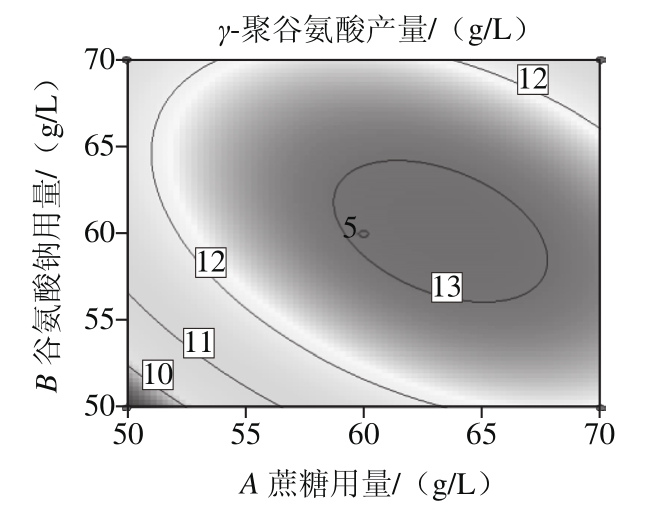
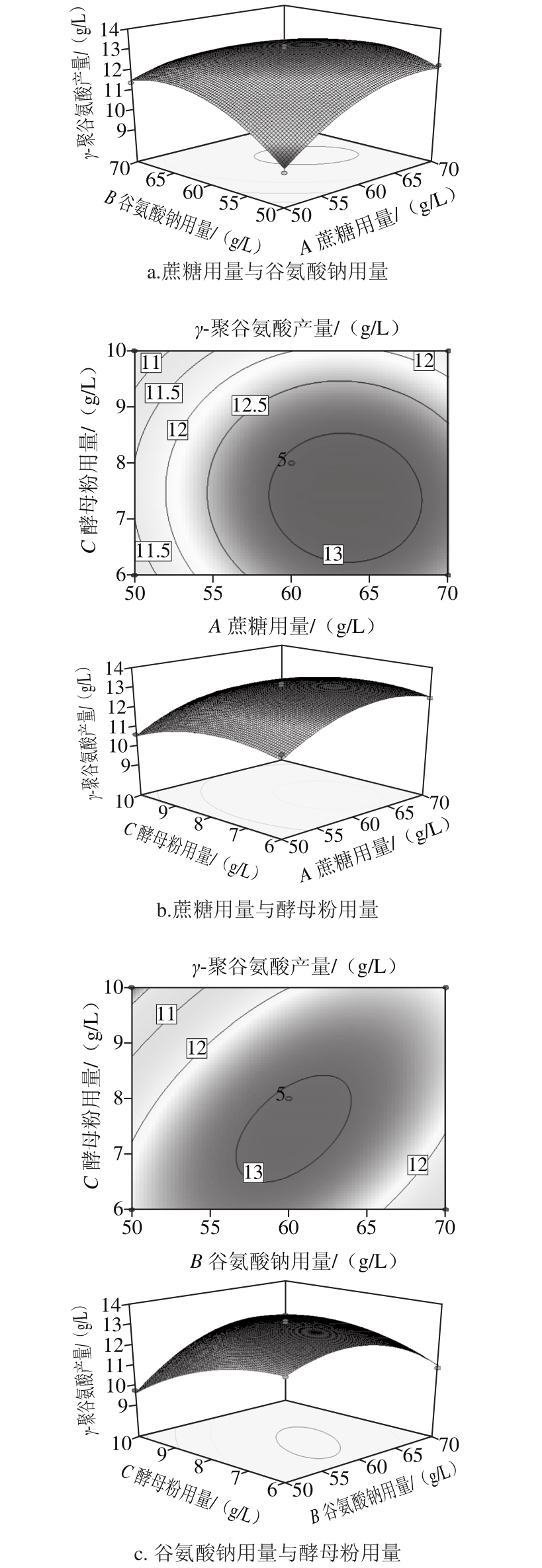
图1 任意两因素对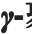 聚谷氨酸产量交互影响的响应面及等高线图
聚谷氨酸产量交互影响的响应面及等高线图
Fig. 1 Response surface plot and contour plot showing the interactive effects of various factors on the production of poly γ-glutamic acid
由图1可知,谷氨酸钠用量与酵母粉用量对γ-聚谷氨酸产量的交互作用最为显著,蔗糖与谷氨酸钠用量对γ-聚谷氨酸产量的交互作用显著,蔗糖用量与酵母粉用量的交互作用不显著。在一定范围内,随着蔗糖用量、谷氨酸钠用量和酵母粉用量的增加,γ-聚谷氨酸产量随之增加。当达到最大值后,随着各因素用量的继续增加,γ-聚谷氨酸产量逐渐减小。说明只有在各因素用量适宜的条件下,γ-聚谷氨酸产量才会达到最大值。响应面图显示了两个因素之间存在着交互作用,说明它们之间对γ-聚谷氨酸产量的影响并不是简单的线性关系,而是存在交互作用,共同影响着γ-聚谷氨酸的生物合成。
基于上述模型,通过Design Expert 8.0 软件对回归方程求极值,由二次多项回归方程得出3 个因素的最佳值为谷氨酸钠用量57.96 g/L、蔗糖用量64.40 g/L和酵母粉用量7.10 g/L。在上述条件下,预测的γ-聚谷氨酸产量的最大值为13.25 g/L。在最佳培养条件下进行3 次平行实验,获得的γ-聚谷氨酸产量的平均值为13.20 g/L,与理论预测值接近,说明该模型能较好地反映枯草芽孢杆菌ZJS18发酵合成γ-聚谷氨酸的实际情况。
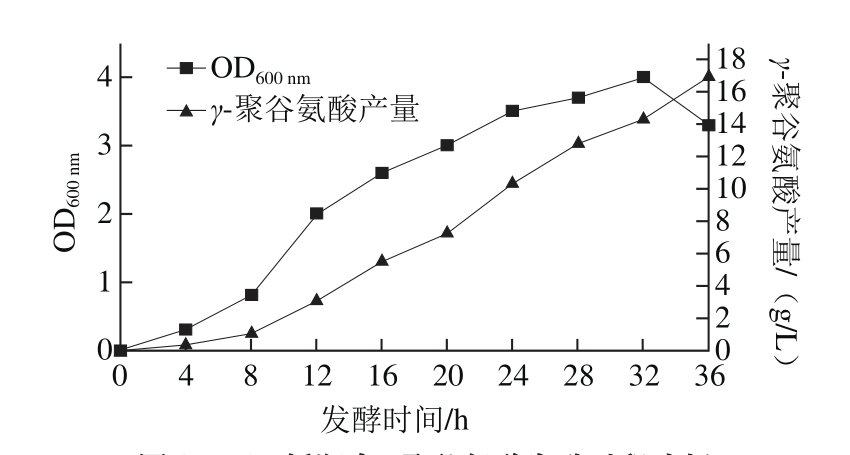
图2 1 L摇瓶中γ-聚谷氨酸发酵过程分析
Fig. 2 Time-course analysis of γ-PGA fermentation in a 1-L shake fl ask
由图2可以看出,菌株在0~8 h时处于延迟期;8~20 h处于对数生长期,由OD600nm表示的菌体生长量由0.87快速增加到3.24,发酵液中的γ-聚谷氨酸也在这个阶段大量积累,从0.31 g/L增加到6.98 g/L;20~32 h菌体处于稳定生长期,但发酵液中γ-聚谷氨酸产量仍在迅速积累,从6.98 g/L增加到14.12 g/L;之后菌体生长进入衰亡期,菌体量下降,但γ-聚谷氨酸的积累仍在进行。由发酵过程的参数变化还可以看出,枯草芽孢杆菌ZJS18在菌体生长进入对数期后,其合成γ-聚谷氨酸的速率增加较快,且与细胞生长呈现相关性。
通过以上研究结果可以看出,在一定范围内,随着蔗糖和谷氨酸钠用量的增加,能够取得较高的γ-聚谷氨酸产量,说明蔗糖和谷氨酸钠用量对γ-聚谷氨酸的影响呈现正效应,也说明碳源和前体物质相互影响,促进菌体合成γ-聚谷氨酸;但当两者用量增加到一定数值后,γ-聚谷氨酸产量开始降低。当谷氨酸钠用量不变时,随着蔗糖用量的增加,γ-聚谷氨酸产量也随之增加;但随着酵母粉用量的变化,γ-聚谷氨酸产量变化较小,这可能是因为酵母粉对γ-聚谷氨酸的合成呈现负效应。上述结果说明碳源和氮源虽然都能影响γ-聚谷氨酸的生物合成,但两者之间并没有太大的交互影响。随着谷氨酸钠用量的增加和酵母粉用量的减小,γ-聚谷氨酸产量增加,说明前体物和氮源之间存在交互作用,共同影响着γ-聚谷氨酸的生物合成。
与已报道的文献[23-25]相比,本研究发现γ-聚谷氨酸发酵培养基的最优碳源是蔗糖,而不是葡萄糖,其中的原因可能是因为葡萄糖效应的产生,使得细菌对葡萄糖摄取的生物能转换受到了限制,细菌生长也因此受到抑制。本实验筛选的枯草芽孢杆菌ZJS18在发酵36 h时,γ-聚谷氨酸产量达到最高值,为16.9 g/L。文献报道的其他高产γ-聚谷氨酸的菌株,如枯草芽孢杆菌RKY3[26]、地衣芽孢杆菌ATCC9945[27-28]和地衣芽孢杆菌NCIM 2324[29]等,其γ-聚谷氨酸产量为15~20 g/L,但培养时间为72~96 h,时间较长。另外,现在大部分报道的提高产物发酵产量的方法是通过菌种诱变[30-31],但该法具有不确定性,且费时费力。随着分子生物学和代谢工程的发展,如果想从根本上大量生产γ-聚谷氨酸,必须深入探究其生物合成途径,因此下一步拟研究枯草芽孢杆菌ZJS18合成γ-聚谷氨酸的生物合成途径,并通过代谢工程的方法对其进行改造,进一步提高γ-聚谷氨酸产量。
本实验主要研究了枯草芽孢杆菌ZJS18发酵生产γ-聚谷氨酸的最优培养条件。通过Plackett-Burman试验设计,筛选出蔗糖、酵母粉和谷氨酸钠用量3 个因素对γ-聚谷氨酸产量具有显著影响的因素,并通过最陡爬坡试验进一步确定了它们的取值范围,最后通过Box-Behnken试验进行响应面设计,确定了发酵培养基的最佳配方:谷氨酸钠用量57.96 g/L、蔗糖用量64.40 g/L、酵母粉用量7.1 g/L、氯化钠用量30 g/L、MgSO4用量0.3 g/L、K2HPO4用量2 g/L;最佳发酵条件:接种量5%、装液量40 mL/250 mL、温度37 ℃、转速200 r/min、培养时间36 h。在上述条件下,γ-聚谷氨酸产量为13.20 g/L。与原始发酵条件相比,产量提高了1.88 倍。
参考文献:
[1] YOON S H, DO J H, LES S Y, et al. Production of poly γ-glutamic acid by fed-batch culture of Bacillus licheniformis[J]. Biotechnology Letters, 2000, 22: 585-588.
[2] TROY F A. Chemistry and biosynthesis of the poly (γ-D-glutamyl)capsule in Bacillus lichenoformis[J]. Journal of Biological Chemistry,1973, 248(1): 305-315.
[3] TROY F A. Peptide antibiotics biosynthesis and functions: enzymatic formation of bioactive peptides and related compounds[M]. New York:Walter de Gruyter, 1982: 49-83.
[4] 陈永竹, 孙启玲. γ-聚谷氨酸的性质、发酵生产及其应用[J].微生物学通报, 2004, 31(1): 56-58. DOI:10.13344/j.microbiol.china.2004.01.029.
[5] 施庆珊. γ-聚谷氨酸的微生物合成与应用[J]. 精细与专用化学品,2004, 12(11): 20-23. DOI:10.3969/j.issn.1008-1100.2004.11.005.
[6] 鞠蕾, 马霞, 张佳. γ-聚谷氨酸的发酵及保水性能[J]. 中国酿造, 2011,30(7): 57-60. DOI:10.3969/j.issn.0254-5071.2011.07.016.
[7] 王欣, 陈国广, 韦萍. 添加剂对聚谷氨酸-明胶生物胶凝剂和组织黏附性的影响[J]. 南京工业大学学报, 2005, 27(3): 32-35.
[8] 曹名锋, 金映虹, 解慧, 等. γ-聚谷氨酸的微生物合成、相关基因及应用展望[J]. 微生物学报, 2011, 38(3): 388-395.
[9] OGAWA Y, YAMAGUCHI F, YUASA K. Efficient production of γ-polyglutamic acid by Bacillus licheniformis (natto) in jar fermenters[J]. Journal of Fermentation and Bioengineering, 1997,61(10): 1684-1687. DOI:10.1271/bbb.61.1684.
[10] 贺阳阳, 曾伟, 王青龙, 等. γ-聚谷氨酸发酵工艺的优化[J]. 食品科学,2013, 34(9): 1-6. DOI:10.7506/spkx1002-6630-201409030.
[11] ASHIUCHI M. Analytical approaches to poly-γ-glutamate:quantification, molecular size determination, and stereochemistry investigation[J]. Journal of Chromatography B, 2011, 173(5): 1-6.DOI:10.1016/j.jchromb.2011.03.029.
[12] 王辉, 董超, 史延茂, 等. 多聚谷氨酸发酵的响应面法优化[J].食品研究与开发, 2011, 32(17): 150-155. DOI:10.3969/j.issn.1005-6521.2011.12.044.
[13] 游庆红, 张新民, 陈国广, 等. γ-聚谷氨酸的生物合成及应用[J]. 现代化工, 2002, 22(12): 56-59. DOI:10.3321/j.issn:0253-4320.2002.12.016.
[14] 桑莉, 徐虹, 李晖, 等. γ-聚谷氨酸生产菌的筛选及发酵条件[J]. 过程工程学报, 2004, 4(5): 426-466. DOI:10.7666/d.y672146.
[15] 杜沛, 朱丽娟, 陈双喜. 响应面法优化Bacillus subtilis HD-F9产γ-聚谷氨酸发酵培养基[J]. 河南大学学报, 2010, 40(5): 488-503.DOI:10.3969/j.issn.1003-4978.2010.05.014.
[16] 姚梦吟, 刘晓风, 袁月祥, 等. 响应面分析法优化白腐菌Y10产漆酶培养基研究[J]. 广东农业科学, 2009(12): 12-17. DOI:10.3969/j.issn.1004-874X.2009.12.004.
[17] CHENG X, WANG Q J, ZHANG S, et al. Determination of four kinds of carbamate pesticides by capillary zone electrophoresis with amperometricdetection at a polyamide-modified carbon paste electrode[J]. Talanta, 2007, 71: 1083-1087. DOI:10.1016/j.talanta.2006.06.001.
[18] 张庆庆, 金鑫强, 陈剑翔, 等. 发酵液中γ-聚谷氨酸含量快速测定方法研究[J]. 食品工业科技, 2012, 33(19): 294-300.
[19] 慈美琳, 陈燕, 张潇, 等. 响应面法优化蓝莓花青素提取工艺及其抗氧化活性[J]. 食品工业, 2014, 35(4): 39-44.
[20] BEZERRA M A, SANTELLI R E, OLIVEIRA E P, et al. Response surface methodology (RSM) as a tool for optimization in analytical chemistry[J]. Talanta, 2008, 76(5): 965-977. DOI:10.1016/j.talanta.2008.05.019.
[21] 尹园, 马佳歌, 倪春蕾, 等. 居间驹形氏杆菌发酵大豆糖蜜生产细菌纤维素条件的优化[J]. 食品科学, 2017, 38(8): 8-16. DOI:10.7506/spkx1002-6630-201718002.
[22] BILGI E, BAYIR E, SENDEMI R, et al. Optimization of bacterial cellulose production by Gluconacetobacter xylinus using carob and haricot bean[J]. International Journal of Biological Macromolecules,2016, 90: 2-10. DOI:10.1016/j.ijbiomac.2016.02.052.
[23] THORNE C B, MOINAR D M. D-amino acid transamination in Bacillus anthracis[J]. Journal of Biotechnology, 1955, 70: 420-426.
[24] KUNIOKA M, GOTO A. Biosynthesis of poly (γ-glutamic acid) from L-glutamic acid, citric acid, and ammonium sulfate in Bacillus subtilis IF03335[J]. Applied Microbiology and Biotechnology, 1994, 40: 867-872. DOI:10.1007/s002530050589.
[25] INATSU Y, NAKAMURA N, YURIKO Y, et al. Characterization of Bacillus subtilis strains in Thua nao, a traditional fermented soybean food in northern Thailand[J]. Letters in Applied Microbiology, 2006,43(3): 237-242. DOI:10.1111/j.1472-765X.2006.01966.x.
[26] JEONG J, KIM J, WEE Y, et al. The statistically optimized production of poly (gamma-glutamic acid) by batch fermentation of a newly isolated Bacillus subtilis RKY3[J]. Bioresource Technology, 2010,101(12): 4533-4539. DOI:10.1016/j.biortech.2010.01.080.
[27] GARDNER J M, TROY F A. Chemistry and biosynthesis of the poly(gamma-D-glutamyl) capsule in Bacillus licheniformis activation,racemization, and polymerization of glutamic acid by a membranous polyglutamyl synthetase complex[J]. Journal of Biological Chemistry,1979, 254(14): 6262-6268.
[28] SHIH I L, WU P J, SHIEH C J. Microbial production of a poly (γ-glutamic acid) derivative by Bacillus subtilis[J]. Process Biochemistry, 2005, 40(8):2827-2832. DOI:10.1016/j.procbio.2004.12.009.
[29] CHENG C, ASADA Y, AIDA T. Production of gamma-polyglutamic acid by Bacillus licheniformis A35 under denitrifying conditions[J].Agricultural and Biological Chemistry, 1989, 53(9): 2369-2375.
[30] 吴学超, 曹新江, 冀志霞, 等. 聚γ-谷氨酸高产菌的选育与培养基优化[J]. 微生物学通报, 2008, 35(10): 1527-1531.
[31] ABBASI A, AMIRI S. Emulsifying behavior of an exopolysaccharide produced by Enterobacter cloacae[J]. African Journal of Biotechnology, 2008, 7(10): 1574-1576.
Optimization of Culture Conditions for Poly γ-Glutamic Acid Production by Bacillus subtilis ZJS18
YU Ping, HUANG Xingxing, ZHANG Yishu
(College of Food Science and Biotechnology, Zhejiang Gongshang University, Hangzhou 310035, China)
Abstract:The culture conditions for poly γ-glutamic acid production by Bacillus subtilis ZJS18 were optimized by response surface methodology (RSM). Three factors that had a significant influence on the yield of poly γ-glutamic acid, namely sucrose, yeast powder and sodium glutamate, were screened out by the Plackett-Burman design. The levels of the three medium components were further optimized to be 64.40, 7.10 and 57.96 g/L, respectively using Box-Behnken design with RSM. The optimal culture conditions for the production of poly γ-glutamic acid were as follows: sucrose 64.40 g/L, yeast powder 7.10 g/L, sodium glutamate 57.96 g/L, NaCl 30 g/L, KH2PO42 g/L, MgSO40.3 g/L, initial pH 7.5, inoculum size 5%,medium volume 40 mL/250 mL, temperature 37 ℃, shaking speed 200 r/min, and fermentation time 36 h. Under the above conditions, the yield of poly γ-glutamic acid was up to 13.20 g/L, which was increased by 2.88 folds as compared to that under the original conditions.
Keywords:Bacillus subtilis; poly γ-glutamic acid; culture conditions; response surface methodology; optimization
YU Ping, HUANG Xingxing, ZHANG Yishu. Optimization of culture conditions for poly γ-glutamic acid production by Bacillus subtilis ZJS18[J]. Food Science, 2018, 39(22): 87-92. (in Chinese with English abstract) DOI:10.7506/spkx1002-6630-201822014. http://www.spkx.net.cn
引文格式:于平, 黄星星, 张一舒. 枯草芽孢杆菌ZJS18发酵生产γ-聚谷氨酸培养条件的优化[J]. 食品科学, 2018, 39(22): 87-92.DOI:10.7506/spkx1002-6630-201822014. http://www.spkx.net.cn
文章编号:1002-6630(2018)22-0087-06
文献标志码:A
中图分类号:Q815
DOI:10.7506/spkx1002-6630-201822014
第一作者简介:于平(1974—),男,教授,博士,研究方向为食品生物技术。E-mail:yup9202@hotmail.com
基金项目:国家自然科学基金面上项目(31171658);食品科学与工程浙江省重中之重一级学科项目(2017SIAR214)
收稿日期:2017-10-16