大豆分离蛋白(soybean protein isolate,SPI)是以低温脱脂大豆粕为原料生产的一种植物蛋白产品,主要由清蛋白和球蛋白组成,其中清蛋白约占5%、球蛋白约占90%[1]。SPI具有良好的乳化能力,是非常好的天然水包油型乳化稳定剂[2],已在甜品、香肠、汤料等的生产加工中发挥重要作用。
改性是进一步拓展SPI应用范围的重要措施。到目前为止,文献已经报道了大量可用于SPI改性的方法,包括物理法、化学法、酶法等[3]。在物理法中,超声处理已经引起了部分学者的关注,已被证实可使SPI的结构更加舒展并可显著改善其溶解[4-6]、乳化[7-9]、流变[10]、凝胶[11-14]和感官[15]等多种功能性质。美拉德反应是另外一种非常有潜力的SPI改性方法,与麦芽糊精[16-17]、葡聚糖[18-19]、阿拉伯树胶[20]、羧甲基纤维素钠[21]、乳糖[22]等多糖发生美拉德反应后,SPI的乳化活性及其他功能性质均有显著提高。
超声处理可以加速SPI与多糖之间的美拉德反应并提高所得美拉德反应产物(Maillard reaction products,MRPs)的乳化性质。比如,王喜波等[23-24]利用超声辅助SPI与葡聚糖之间的美拉德反应,所得MRPs的乳化活性及乳液的冻融稳定性均有了显著的提高;穆利霞等[25]就超声对加速SPI与多糖接枝反应的机理进行探讨,发现超声处理可显著增加SPI肽链的伸展度、分子内部自由氨基的暴露程度及无规则卷曲的数量。
上述研究表明,超声处理与美拉德反应结合可以显著提高SPI的乳化活性及所得乳液的稳定性,但是目前鲜见关于SPI单独经超声处理后与还原糖的美拉德反应规律及所得MRPs乳化活性的报道。因此,本实验先在一定功率下超声处理SPI不同时间,然后使其与木糖(xylose,XYL)在湿热条件下发生美拉德反应,研究SPI超声处理对其与XYL美拉德反应及MRPs部分性质的影响,最后再对利用MRPs制备的乳液在不同食品加工条件下的稳定性进行研究。本实验对于推动超声处理在SPI生产、进一步拓展SPI的应用范围具有一定的意义。
大豆分离蛋白 临邑禹王植物蛋白有限公司;D-木糖 上海蓝季生物有限公司;大豆油 益海粮油工业有限公司;十二烷基硫酸钠(sodium dodecyl sulfate,SDS)、磷酸二氢钾、盐酸、氢氧化钠等均为国产分析纯。
电热恒温水浴锅 龙口市先科仪器公司;UV-2000紫外分光光度计 上海尤尼科仪器有限公司;分析天平、Delta320 pH计 梅特勒-托利多仪器(上海)公司;90-1型恒温磁力搅拌器 上海沪西分析仪器厂有限公司;LG10-2.4A高速离心机 北京医用离心机厂;NicoleIR200傅里叶红外光谱仪 赛默飞世尔科学仪器公司;Zetasizer Nano ZS激光粒度分析仪英国马尔文实验设备公司;ZDG-0.25真空冷冻干燥机烟台冰轮股份有限公司;KQ-500B型超声波清洗器昆山市超声仪器有限公司;FJ200-SH型数显高速分散均质机 上海标本模型厂;F-2700荧光分光光度计天美(中国)科学仪器有限公司。
1.3.1 MRPs的制备
取5 份4.000 0 g SPI分别加入96.000 0 g蒸馏水,用恒温磁力搅拌器充分搅拌得到质量浓度为4 g/100 mL的溶液,然后置于超声清洗机中在25 ℃、16 000 Hz条件下分别处理20、40、60、80、100 min。预实验发现,SPI与XYL在混合质量比4∶1、反应体系pH 8.0及水浴温度90 ℃反应6 h后所得MRPs的溶解性最好,因此本实验中的美拉德反应均在此条件下进行。超声处理结束后,向各SPI溶液中分别加入1.000 0 g XYL,搅拌均匀,调节溶液pH 8.0,然后置于90 ℃水浴锅内反应6 h,得到各种MRPs(记为SPI(Ult)-XYL-MRPs)。另外,将未经超声处理的SPI与XYL按上述条件混合、溶解(所得混合物记为SPI-XYL-Mix)后在相同条件下反应得到美拉德反应产物(记为SPI-XYL-MRPs),作为实验对照。
1.3.2 MRPs的表征
1.3.2.1 美拉德反应程度的测定
美拉德反应的中间产物在294 nm波长处具有特征吸收,最终产物在420 nm波长处具有特征吸收[26],因此可通过检测这两个波长下的吸收揭示SPI与XYL的美拉德反应程度。
将SPI-XYL-MRPs、SPI(Ult)-XYL-MRPs、SPIXYL-Mix于4 000 r/min离心20 min,收集上清液,用蒸馏水分别稀释100 倍和15 倍后用紫外-可见分光光度计测定其在294 nm和420 nm波长处的吸光度。
1.3.2.2 红外光谱分析
将各MRPs冷干后与KBr按质量比100∶1混合、研磨均匀,用压片机压制成均匀的薄片,将压片置于红外光谱仪在波数4 000~400 cm-1进行扫描分析,以空白KBr作为背景对照。
1.3.2.3 Zeta电位的测定
取SPI-XYL-MRPs、SPI(Ult)-XYL-MRPs和SPIXYL-Mix各1 mL,加入9 mL蒸馏水稀释,振荡均匀后用激光粒度分析仪测定电位。
1.3.2.4 荧光分析
将SPI-XYL-MRPs、SPI(Ult)-XYL-MRPs和SPIXYL-Mix冻干后准确称取一定量的粉末,用10 mmol/L的pH 7.0磷酸缓冲液稀释至SPI质量浓度为1 mg/mL。将稀释液加入到荧光光度计的比色皿中,设置激发波长为334 nm,按5 nm/min的速率在350~500 nm范围内扫描,测定荧光强度。
1.3.3 乳化性的测定
将SPI-XYL-MRPs、SPI(Ult)-XYL-MRPs和SPI-XYL-Mix冻干,用0.1 mol/L pH 6.5磷酸缓冲液溶解,使溶液中的SPI质量浓度达到1 mg/mL,然后按照体积比3∶1加入大豆油,于10 000 r/min高速搅拌5 min得到均匀的O/W乳状液。
取1 mL上述乳状液用蒸馏水稀释5 倍,另取1 mL乳状液与39 mL 1 g/L的SDS溶液混合均匀,以相同质量浓度的SDS溶液为空白,测定500 nm波长处的吸光度(A500nm),按式(1)计算乳化活性[27]:
式中:L为光路长度,此处为1 cm;N为稀释倍数。
同时测定乳液在该时刻(T0)及放置10 min后在500 nm波长处的浊度(T10),按照式(2)计算乳化稳定性:
1.3.4 乳状液稳定性的测定
选择超声处理时间20、40、80 min研究SPI超声处理对SPI(Ult)-XYL-MRPs稳定乳液稳定性的影响。
1.3.4.1 对离子强度的稳定性
将1.3.1节中所得的SPI-XYL-MRPs、SPI(Ult)-XYLMRPs和SPI-XYL-Mix溶液各取3 份,向溶液中加入大豆油,使大豆油的体积分数为25%,于10 000 r/min搅拌5 min得到均匀的O/W大豆油乳状液,然后加入一定量的NaCl固体,使NaCl质量浓度分别达到0、0.15 mg/mL和0.20 mg/mL,将其置于4 ℃贮藏12 h,测定乳液的粒径及分层指数。
1.3.4.2 热稳定性
将1.3.1节中所得的SPI-XYL-MRPs、SPI(Ult)-XYLMRPs和SPI-XYL-Mix溶液各取3 份,加入大豆油,使大豆油的体积分数为25%,于10 000 r/min高速搅拌5 min得到均匀的O/W大豆油乳状液,分别在60、80、90 ℃加热15min,降至室温后测定乳液的粒径及分层指数。
1.3.4.3 对盐和加热的协同稳定性
将1.3.1节中所得的SPI-XYL-MRPs、SPI(Ult)-XYLMRPs和SPI-XYL-Mix溶液各取3 份,向溶液中加入大豆油,使大豆油的体积分数为25%,于10 000 r/min搅拌5 min得到均匀的O/W大豆油乳状液,加入一定量的NaCl固体,使NaCl的质量浓度分别达到0、0.15 mg/mL和0.20 mg/mL,然后分别在60、80、90 ℃加热15 min,降至室温后测定乳液的粒径及分层指数。
1.3.4.4 pH值稳定性
将1.3.1节中所得的SPI-XYL-MRPs、SPI(Ult)-XYLMRPs和SPI-XYL-Mix溶液各取3 份,向溶液中加入大豆油,使大豆油的体积分数为25%,于10 000 r/min搅拌5 min得到均匀的O/W大豆油乳状液,用1 mol/L的NaOH或HCl溶液分别调节pH 3.0、4.5、7.0。将所得乳液置于4 ℃贮藏12 h,测定乳液的粒径及分层指数。
1.3.4.5 乳状液粒径
当乳液发生聚集时粒径会增大,因此其相对变化可以反映乳液对环境条件的稳定性。取0.5 mL乳状液于玻璃试管中,用去离子水稀释10 倍,然后用激光粒度仪测定乳状液的粒径。
1.3.4.6 乳状液分层指数
将乳状液进行静置观察,测量分层后底层清液的高度与总高度,根据式(3)计算分层指数[28]:
每个实验重复3 次,结果以 ±s表示,采用SPSS 17.0(美国SPSS公司)进行统计分析。组间差异显著性分析采用方差分析中的最小显著性差异法测试,P<0.05,差异显著。
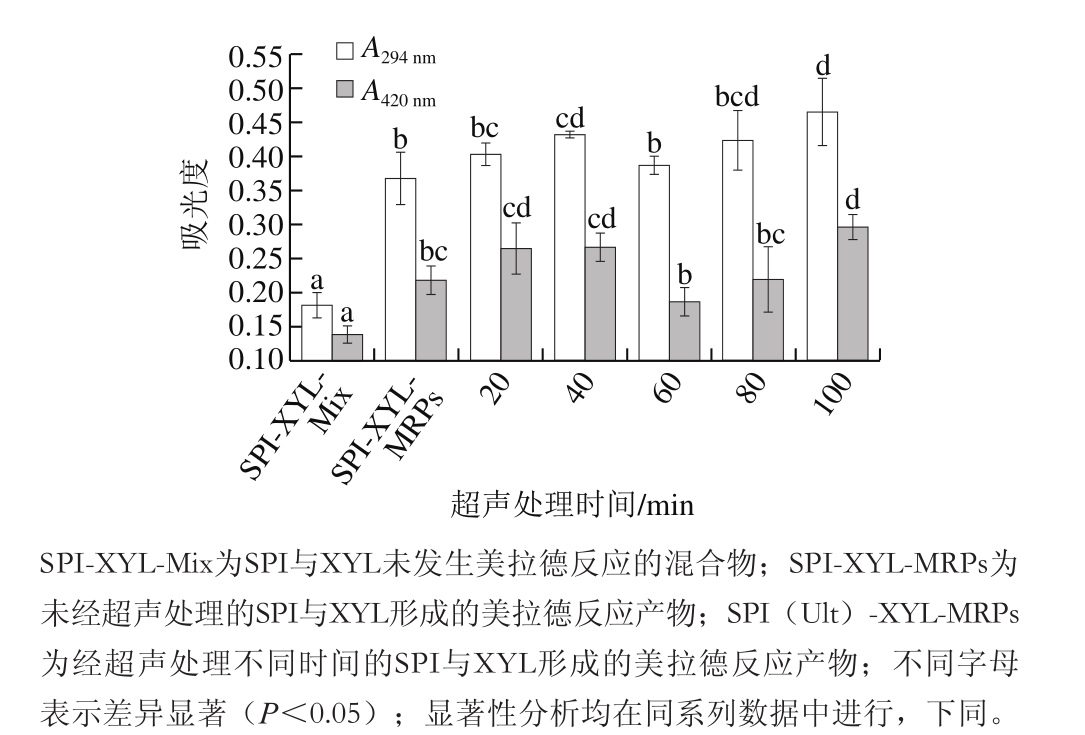
图1 SPI超声处理时间对其与XYL美拉德反应的影响
Fig. 1 Effect of ultrasonication time of SPI on its Maillard reaction with XYL
如图1所示,MRPs溶液的A294nm和A420nm值均高于SPI与XYL的混合物溶液(SPI-XYL-Mix),表明两者之间发生了美拉德反应。SPI超声处理对其与XYL之间的美拉德反应有重要影响,且该影响与处理时间有关。当超声处理时间为20 min和40 min时,所得MRPs溶液在294 nm和420 nm波长处的吸光度均高于SPI-XYL-Mix(但处理时间为20 min时差异不显著)。这可能是由于SPI经超声处理后更多的氨基暴露出来,同时溶解性增加,使得其与XYL的美拉德反应增强;当SPI的超声处理时间延长至60 min时,所得MRPs溶液在2 个波长处的吸光度与40 min
时相比均显著下降,但是随着SPI超声处理时间的进一步延长,吸光度又开始显著增加。这可能是由于此时SPI的三级结构发生了更加剧烈的变化,该变化更加有利于SPI与XYL发生美拉德反应[25]。因此,SPI超声处理可以增强其与XYL美拉德反应的程度。在随后的研究中,选择SPI超声处理时间20、40、80 min进行进一步的研究。
2.2.1 红外光谱检测结果

图2 SPI超声处理对其与XYL形成的MRPs红外光谱的影响
Fig. 2 Effect of ultrasonication time of SPI on the FTIR pattern of MRPs
如图2所示,醛基的特征吸收峰出现在3 750 cm-1处,此处各种SPI(Ult)-XYL-MRPs的强度大于SPI-XYLMRPs和SPI-XYL-Mix,证明SPI超声处理可以促进含醛基中间产物的生成。1 560 cm-1处为C—N伸缩与N—H弯曲的吸收峰,SPI-XYL-MRPs在此处的强度要高于SPI-XYLMix,表明美拉德反应使得更多的—NH2暴露出来,SPI超声处理使得该处的强度进一步增加,但是随着超声处理时间的延长,吸收强度逐渐降低,表明SPI与XYL之间发生了美拉德反应,且SPI超声处理可以增强其与XYL之间的美拉德反应,这与图1中的结果一致。
2.2.2 Zeta电位
由图3可以看出,在选定的浓度下,SPI与XYL混合物(SPI-XYL-Mix)的Zeta电位仅为-13 mV;发生美拉德反应后,MRPs的Zeta电位仍为负值,但其绝对值提高到24.7 mV;SPI超声处理进一步增加了相应MRPs的Zeta电位,但是不同处理时间之间没有显著的差异。这可能是美拉德反应产生了带有负电荷的中间产物,同时超声处理使得SPI中更多的羧基暴露出来,从而导致MRPs电位绝对值增加。MRPs电位绝对值在一定范围内的提高可加强乳滴之间的静电排斥作用,因此有望用于提高乳液的稳定性[29]。

图3 SPI超声处理时间对其与XYL所得MRPs Zeta电位的影响
Fig. 3 Effect of ultrasonication time of SPI on the Zeta potential of MRPs
2.2.3 荧光特性

图4 SPI超声处理时间对其与XYL所得MRPs荧光特性的影响
Fig. 4 Effect of ultrasonication time of SPI on the fluorescence characteristics of MRPs
由图4可见,在激发波长为334 nm的情况下,超声处理40 min后得到的MRPs的荧光强度最大,其次为80 min和20 min,再次为SPI-XYL-MRPs,SPI与XYL两者的混合物的荧光强度最低。这表明,美拉德反应可以增强SPI的荧光强度,且SPI超声处理可以进一步提高该参数,这与SPI与阿拉伯胶干热处理后荧光强度降低的现象不一致[30]。这可能是由于超声处理会使SPI结构更为舒展,使更内部更多荧光性基团暴露出来,同时美拉德反应还生成了新的荧光物质。超声处理80 min时的荧光强度较40 min时低,这可能是由于长时间的超声处理使SPI结构发生剧烈变化所致。
2.2.4 乳化活性
由图5可以看出,美拉德反应可以显著增强SPI的乳化活性。当未经超声处理的SPI与XYL发生美拉德反应后(SPI-XYL-MRPs),其乳化活性与两者的混合物(SPIXYL-Mix)相比增加了18.48%,这与大部分现有的报道一致[15,21]。SPI超声处理进一步增强了所得MRPs的乳化活性。当处理时间为20 min和40 min时,所得MRPs的乳化活性分别为两者混合物的1.59 倍和1.74 倍。但是当SPI超声处理时间进一步延长时,所得MRPs的乳化活性又显著下降,且与SPI-XYL-Mix之间无显著差异。这可能是由于SPI的结构变化过于剧烈,削弱了其在油水两界面的吸附作用,使得乳化活性略有降低。SPI超声处理对其与XYL形成的MRPs的乳化稳定性没有显著影响。
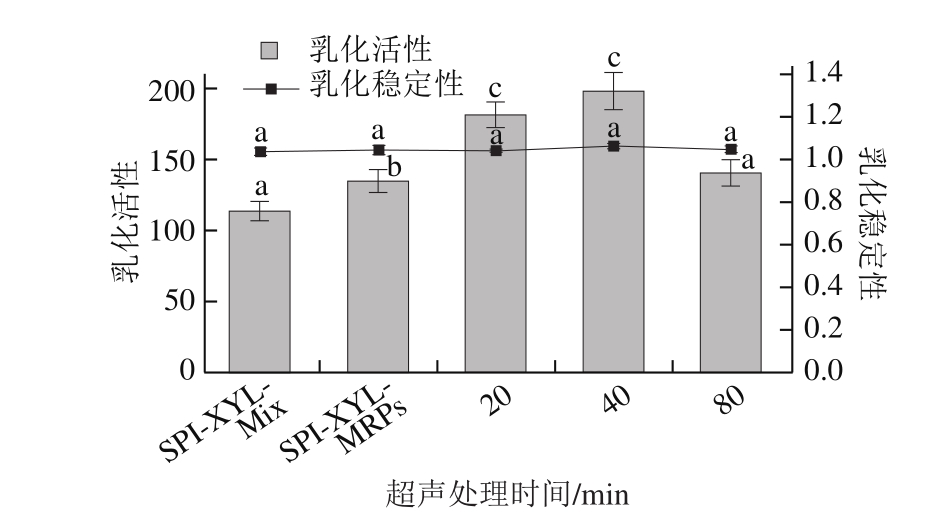
图5 SPI超声处理时间对其与XYL所得MRPs乳化性能的影响
Fig. 5 Effect of ultrasonication time of SPI on the emulsifying properties of MRPs
本实验根据乳液粒径的变化及分层指数[24]评价乳液在不同离子强度、温度及pH值下的聚集特性及稳定性。
2.3.1 对离子强度的稳定性
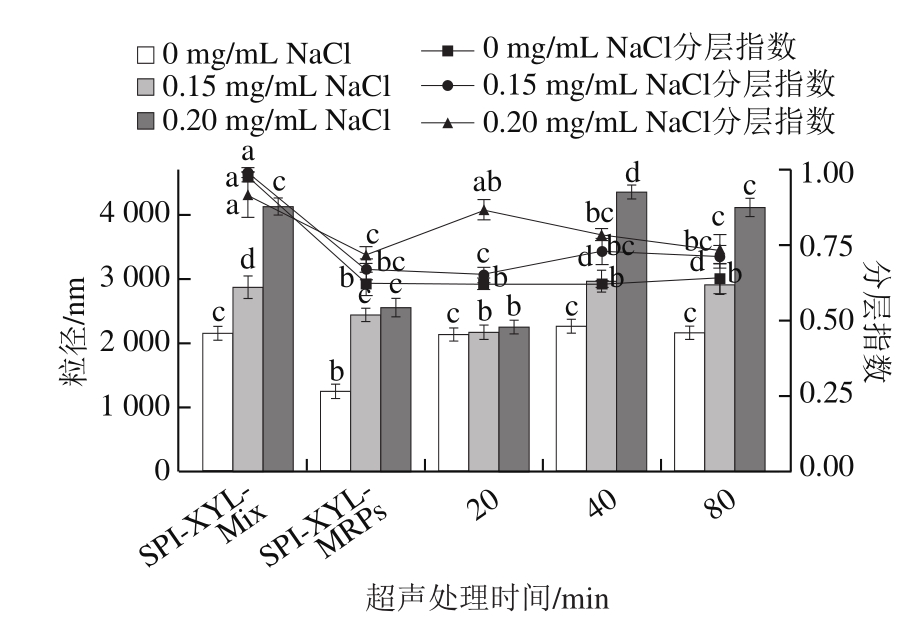
图6 SPI超声处理对相应SPI(Ult)-XYL-MRPs稳定乳液离子强度稳定性的影响
Fig. 6 Effect of SPI ultrasonication time on the stability of MRPs-stabilized emulsions at different ionic strengths
如图6所示,随着溶液中NaCl质量浓度的升高,SPIXYL-Mix稳定乳液的粒径随之增大,与未添加NaCl时相比,添加0.15 mg/mL和0.20 mg/mL NaCl后,乳液的粒径分别增加了33%和91%,说明NaCl屏蔽了乳滴之间的静电斥力,导致乳滴之间发生了聚集。SPI-XYL-MRPs稳定乳液的粒径略低于SPI-XYL-Mix;当向乳液中添加两个浓度的NaCl后,粒状液的粒径分别增加了94%和103%,变化幅度要高于SPI-XYL-Mix稳定乳液,表明乳液对离子强度的抗性有所减弱。
与SPI-XYL-MRPs相比,各种SPI(Ult)-XYL-MRPs稳定乳液的粒径均有所提高,这可能是由于美拉德反应使得SPI分子质量变大所致。SPI超声处理对乳液粒径的变化有显著影响,且该影响与超声处理时间相关。当SPI超声处理20 min时乳状液在各NaCl溶液中的粒径没有显著变化;当超声处理时间延长至40 min和80 min时,所得乳液的粒径随NaCl质量浓度的升高显著增加,与未添加NaCl时相比,两种乳液在两个NaCl质量浓度下的粒径分别增加了31%、92%和35%、90%,表明此时乳液发生了聚集,但是与SPI-XYL-MRPs稳定乳液相比对离子诱导的聚集的抗性仍有所增强。
SPI-XYL-Mix稳定乳液的分层指数最高,美拉德反应显著降低乳液在水溶液中的分层指数,但SPI是否进行超声处理对该指数没有显著影响。乳液中添加NaCl后,乳状液的分层指数均升高,表明NaCl能够破坏乳滴使油析出。与SPI-XYL-MRPs相比,SPI超声处理对乳液的分层指数没有明显的改善作用。
2.3.2 热稳定性
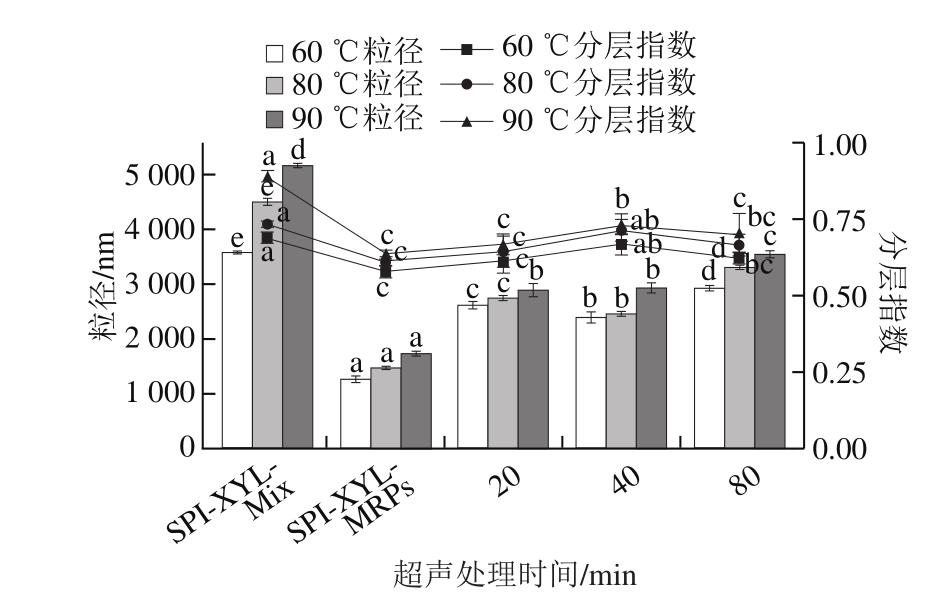
图7 SPI超声处理对相应SPI(Ult)-XYL-MRPs稳定乳液热稳定性的影响
Fig. 7 Effect of SPI ultrasonication time on the thermal stability of MRPsstabilized emulsions
由图7可以看出,所有乳液的粒径均随着贮藏温度的升高而增加,表明高温贮藏会引起乳液的聚集,这可能是由于高温削弱了静电斥力及增强了SPI分子之间的疏水性相互作用。美拉德反应显著降低了乳液在高温下的粒径,但是与SPI-XYL-MRPs相比,对SPI进行超声处理会引起相应乳液粒径的增加,这与图6的结果一致。当将乳液的贮藏温度由60 ℃提高至80 ℃和90 ℃时,SPI-XYL-Mix稳定乳液的粒径分别增加了24%和44%,SPI-XYL-MRPs稳定乳液的粒径分别增加了16%和36%,说明美拉德反应可以削弱由环境温度升高引起的乳液聚集;将SPI超声处理20、40 min和80 min后,该增加值分别为5%、11%和3%、23%及13%、21%。因此,对SPI进行超声处理可以进一步提高乳液对高温贮藏的抗性。这可能是由于美拉德反应增强了MRPs的Zeta电位(图3)从而使得相应乳液在高温下仍可保持较强的静电斥力所致。
SPI-XYL-MRPs和各种SPI(Ult)-XYL-MRPs稳定乳液在3 个选定温度下的粒径和分层指数均小于SPI-XYL-Mix,表明美拉德反应可以提高乳液的热稳定性,但是SPI超声处理对该指标没有进一步的提升作用。
2.3.3 对温度和离子强度的协同稳定性

图8 SPI超声处理对相应SPI(Ult)-XYL-MRPs稳定乳液热和离子协同稳定性的影响
Fig. 8 Effect of SPI ultrasonication time on the synergetic stability of MRPsstabilized emulsions under varying conditions of temperature and ionic strength
如图8所示,当加入0.15 mg/mL的NaCl后,所有乳液的粒径和分层指数均随着贮藏温度的升高而变大,乳状液的稳定性逐渐变差;所有SPI-XYL-MRPs稳定乳液在所选条件下的粒径和分层指数均小于SPI-XYL-Mix,表明美拉德反应可以显著提高乳液在高温高盐条件下的稳定性,这与图7的结果一致。
当将含0.15 mg/mL NaCl乳液的贮藏温度由60 ℃提高至80 ℃和90 ℃时,SPI-XYL-Mix稳定乳液的粒径分别增加了7%和13%,SPI-XYL-MRPs稳定乳液的粒径分别增加了4%和25%;将SPI超声处理20、40 min和80 min后,该增加值分别为3%、18%和5%、10%及16%、27%。这表明,对SPI进行适度的超声处理可以提高乳液对高温和高盐贮藏环境的抗性。
与SPI-XYL-MRPs相比,SPI(Ult)-XYL-MRPs稳定乳液分层指数均有所增加,且在超声处理时间为40 min时稳定性最差。因此,对SPI进行超声处理并不能进一步提高相应乳液在盐离子和高温贮藏下的稳定性,这与图6和图7的结果一致。
2.3.4 pH值稳定性
SPI在等电点(pH 4.5)下乳化性差是影响其应用的重要因素之一[17],本实验也观察到该现象。由图9可知,所有乳液在pH 4.5下的粒径最大,这是由于在等电点附近,SPI的溶解度降低;同时乳滴表面的电荷量较低,粒子间的静电排斥力降弱,乳状液发生絮凝或聚合,导致乳状液失稳、粒径变大。另外,所有乳液在pH 7.0下的粒径最小,这是因为该pH值远离SPI的等电点,因此乳液表面的电荷数量最大,静电斥力更强,导致聚集现象最弱。美拉德反应显著降低了乳液在所选pH值下的粒径,表明该反应可以提高SPI在各pH值、尤其是等电点下的乳化能力,并可有效避免乳滴之间发生聚集。
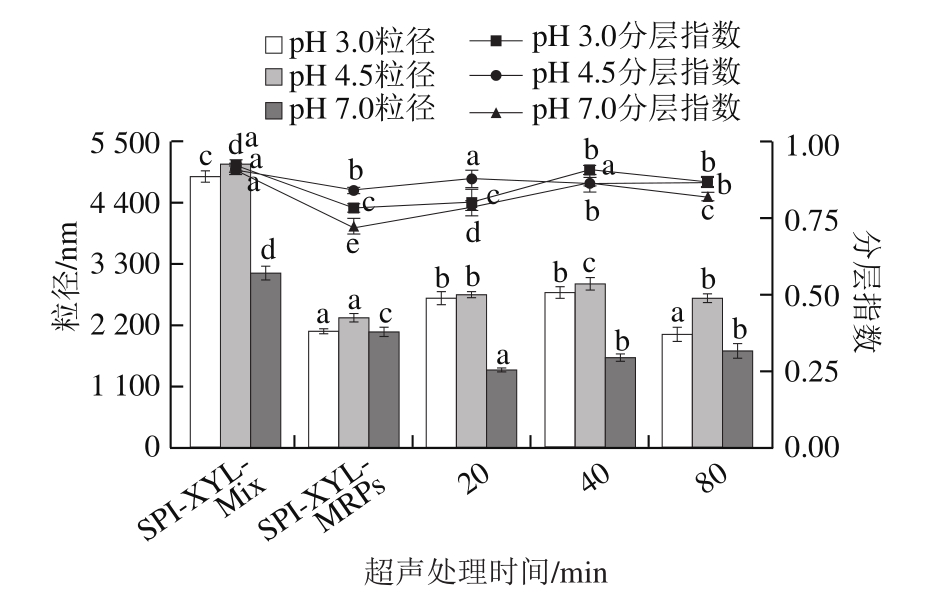
图9 SPI超声处理对相应SPI(Ult)-XYL-MRPs稳定乳液pH值稳定性的影响
Fig. 9 Effects of SPI ultrasonication time on the pH stability of MRPsstabilized emulsions
当将乳液的贮藏pH值由3.0提高至4.5~7.0时,SPI-XYL-Mix粒径分别增加了4%,减小了35%,SPI-XYL-MRPs稳定乳液的粒径分别增加了11%,减小了6%;将SPI超声处理20、40 min和80 min后,该值分别增加2%、减小48%和增加5%、减小42%及增加31%、减小15%。因此,对SPI进行适度的超声处理可以提高乳液对环境pH值变化的抗性,且该效应在pH值为7.0时尤为明显。
与SPI-XYL-Mix相比,SPI-XYL-MRPs稳定乳液的分层指数明显下降,但是对SPI进行超声处理对该指标没有进一步的促进作用。
本实验先对SPI进行超声处理,然后使其与XYL发生美拉德反应,并对所得MRPs的乳化活性及乳液稳定性进行研究。结果表明,对SPI进行超声处理可以显著促进其与XYL之间的美拉德反应;与未进行超声处理的SPIXYL-MRPs相比,超声处理显著提高了相应MRPs的Zeta电位、荧光强度及乳化能力。与天然SPI相比,其经超声处理后再与XYL发生美拉德反应显著降低了相应MRPs稳定乳液在环境离子强度、加热及pH值发生变化时的聚集程度,但是对乳液的分层情况没有明显的改善作用。
[1] HATTORI M, OKADA Y, TAKAHASHI K. Functional changes in β-lactoglobulin upon conjugation with carboxymethyl cyclodextrin[J].Journal of Agricultural & Food Chemistry, 2000, 48(9): 3789-3794.DOI:10.1021/jf001028x.
[2] 胡敏, 张伟, 赵谋明, 等. 乳化稳定剂在改性大豆分离蛋白冰淇淋中的应用研究[J]. 食品与发酵工业, 2003, 29(2): 49-53. DOI:10.3321/j.issn:0253-990X.2003.02.011.
[3] 黄友如, 华欲飞. 大豆分离蛋白的改性及其对功能性质的影响[J]. 中国油脂, 2003, 28(4): 35-38. DOI:10.3321/j.issn:1003-7969.2003.04.012.
[4] 孙燕婷, 黄国清, 肖军霞, 等. 超声处理对大豆分离蛋白溶解性和乳化活性的影响[J]. 中国粮油学报, 2011, 26(7): 22-26.
[5] 袁道强, 杨丽. 超声波改性提高大豆分离蛋白酸性条件下溶解性的研究[J]. 粮食与饲料工业, 2008(1): 27-28. DOI:10.3969/j.issn.1003-6202.2008.01.012.
[6] 刘国琴, 李琳, 李冰, 等. 超声和超高压处理对大豆分离蛋白特性影响的研究[J]. 河南工业大学学报(自然科学版), 2005, 26(3): 1-4.DOI:10.16433/j.cnki.issn1673-2383.2005.03.001.
[7] 宋旸, 朱秀清 吴海波, 等. 超声-烷基化对大豆分离蛋白乳化稳定性的影响[J]. 中国食品学报, 2016, 16(7): 184-191. DOI:10.16429/j.1009-7848.2016.07.025.
[8] 李磊, 迟玉杰, 王喜波, 等. 超声-琥珀酰化复合改性提高大豆分离蛋白乳化性的研究[J]. 食品工业科技, 2011, 32(3): 123-126.DOI:10.13386/j.issn1002-0306.2011.03.069.
[9] 朱建华, 杨晓泉, 邹文中, 等. 超声处理对大豆分离蛋白功能特性的影响[J]. 食品工业科技, 2004, 25(4): 56-59. DOI:10.3321/j.issn:1002-6630.2004.07.008.
[10] 朱建华, 杨晓泉. 超声处理对大豆分离蛋白流变学性质的影响[J]. 食品科学, 2005, 26(12): 52-57. DOI:10.3321/j.issn:1002-6630.2005.12.007.
[11] 胡坦, 张珮珮, 郑婷, 等. 高场强超声-加热联用增强大豆分离蛋白冷凝胶凝胶特性[J]. 农业工程学报, 2016, 32(20): 306-314.DOI:10.11975/j.issn.1002-6819.2016.20.040.
[12] 朱建华, 杨晓泉, 熊犍. 超声处理对大豆分离蛋白热致凝胶功能性质的影响[J]. 食品与生物技术学报, 2006, 25(1): 15-20. DOI:10.3321/j.issn:1673-1689.2006.01.004.
[13] 李杨, 刘宝华, 姜楠, 等. 超声处理对黑豆蛋白凝胶性能的影响[J].中国食品学报, 2017, 17(1): 161-169. DOI:10.16429/j.1009-7848.2017.01.021.
[14] 唐传核, 姜燕, 杨晓泉, 等. 超声处理对商用大豆分离蛋白凝胶性能的影响[J]. 中国粮油学报, 2005, 20(5): 72-77. DOI:10.3321/j.issn:1003-0174.2005.05.016.
[15] 张宏伟, 张立娟, 邢天丽, 等. 超声处理对大豆分离蛋白凝胶和感官特性影响[J]. 食品研究与开发, 2016, 37(12): 105-108. DOI:10.3969/j.issn.1005-6521.2016.12.024.
[16] ZHANG J, WU N, LAN T, et al. Improvement in emulsifying properties of soy protein isolate by conjugation with maltodextrin using hightemperature, short-time dry-heating Maillard reaction[J]. International Journal of Food Science & Technology, 2014, 49(2): 460-467.DOI:10.1111/ijfs.12323.
[17] 胡坤, 曾丽, 余思敏. 大豆分离蛋白与麦芽糊精的Maillard反应性及产物乳化性质研究[J]. 食品与发酵工业, 2007, 33(7): 22-25.DOI:0.13995/j.cnki.11-1802/ts.2007.07.039.
[18] DIFTIS N, KIOSSEOGLOU V. Physicochemical properties of dryheated soy protein isolate-dextran mixtures[J]. Food Chemistry, 2006,96(2): 228-233. DOI:10.1016/j.foodchem.2005.02.036.
[19] DIFTIS N, KIOSSEOGLOU V. Stability against heat-induced aggregation of emulsions prepared with a dry-heated soy protein isolate-dextran mixture[J]. Food Hydrocolloids, 2006, 20(6): 787-792.DOI:10.1016/j.foodhyd.2005.07.010.
[20] XUE F, LI C, ZHU X, et al. Comparative studies on the physicochemical properties of soy protein isolate-maltodextrin and soy protein isolate-gum acacia conjugate prepared through Maillard reaction[J]. Food Research International, 2013, 51(2): 490-495. DOI:10.1016/j.foodres.2013.01.012.
[21] DIFTIS N, KIOSSEOGLOU V. Improvement of emulsifying properties of soybean protein isolate by conjugation with carboxymethyl cellulose[J].Food Chemistry, 2003, 81(1): 1-6. DOI:10.1016/j.foodhyd.2012.01.006.
[22] GUAN J J, QIU A Y, LIU X Y, et al. Microwave improvement of soy protein isolate-saccharide graft reactions[J]. Food Chemistry, 2006, 97(4):577-585. DOI:10.1016/j.foodchem.2005.05.035.
[23] 王喜波, 张泽宇, 葛洪如, 等. 超声辅助制备抗冻融大豆分离蛋白工艺优化[J]. 农业工程学报, 2016, 32(14): 272-278. DOI:10.11975/j.issn.1002-6819.2016.14.036.
[24] 张泽宇, 王健, 葛洪如, 等. 超声糖基化大豆分离蛋白冻融稳定性的研究[J]. 现代食品科技, 2016(10): 198-204. DOI:10.13982/j.mfst.1673-9078.2016.10.030.
[25] 穆利霞, 赵谋明, 颜小平, 等. 超声强化大豆分离蛋白-糖接枝反应作用机理的初步探讨[J]. 食品工业科技, 2013, 34(7): 90-95.DOI:10.13386/j.issn1002-0306.2013.07.060.
[26] 葛伟, 李晓东, 夏琪娜, 等. 超声协同美拉德反应对酪蛋白乳化性和凝胶性的影响[D]. 哈尔滨: 东北农业大学. 2016, DOI:10.16429/j.1009-7848.2016.10.010.
[27] 赵剑飞. 大豆分离蛋白与糖基化分离蛋白乳化性的研究[J].食品工业科技, 2005, 26(12): 76-78. DOI:10.13386/j.issn1002-0306.2005.12.018.
[28] ZHANG J B, WU N N, YANG X Q, et al. Improvement of emulsifying properties of Maillard reaction products from β-conglycinin and dextran using controlled enzymatic hydrolysis[J]. Food Hydrocolloids, 2012,28(2): 301-312. DOI:10.1016/j.foodhyd.2012.01.006.
[29] LILLEY E M, ISERT P R, CARASSO M L, et al. The effect of the addition of lignocaine on propofol emulsion stability[J]. Anaesthesia,2010, 51(9): 815-818.
[30] XUE F, LI C, ZHU X W, et al. Comparative studies on the physicochemical properties of soy protein isolate-maltodextrin and soy protein isolate-gum acacia conjugate prepared through Maillard reaction[J]. Food Research International, 2013, 51: 490-495.DOI:10.1016/j.foodres.2013.01.012.
Effect of Ultrasonication of Soybean Protein on Its Maillard Reaction with Xylose and Emulsifying Property of the Resultant Products