表1 4 种酶的酶解条件
Table 1 Hydrolysis conditions of four enzymes

酶种类 pH 温度/℃ 时间/h对照组(不加酶) 常温 2中性蛋白酶 7.0 50 2木瓜蛋白酶 6.5 50 2复合蛋白酶 6.5 50 2风味蛋白酶 6.5 50 2
双孢蘑菇(Agaricus bisporus)又称白蘑菇、蘑菇、双孢菇,隶属于担子菌门、担子菌纲、伞菌目、蘑菇科、蘑菇属[1],是世界性栽培和消费的菇类之一。双孢蘑菇子实体具有高蛋白、低脂肪的特点,而且含有丰富的多糖、矿物质元素、核苷酸、膳食纤维等[2-3]。双孢蘑菇不但具有营养保健价值,而且具有特殊的风味,深受广大消费者的喜爱。为充分利用双孢蘑菇中的滋味物质,可将其加工成双孢蘑菇调味品,与传统调味品相比,可以大大减少日常生活中盐类、味精类调味品的使用,作为天然调味品的植物性来源,滋味丰富独特并且健康营养。因此,双孢蘑菇调味品的加工研究引起人们的关注,如刘晓艳等[4]以双孢蘑菇等4 种食用菌为主要原料,研究功能型复合食用菌调味品的开发工艺,但近年来对于食用菌调味品的研究采用的原料多为香菇[5],双孢蘑菇调味品的研究仍较少。
食用菌味道鲜美,含有丰富的鲜味氨基酸、核苷酸类、可溶性糖、醇类、有机酸等多种小分子水溶性物质[6],研究证明鲜味氨基酸及核苷酸具有一定的协同增鲜作用[7]。游离氨基酸是食用菌中重要的鲜味活性成分,食用菌中所含的氨基酸有25%~35%处于游离状态[8]。氨基酸种类、含量、组成不同,造就了不同食用菌的独特鲜香滋味[9]。目前市面上一些粗加工的产品,如干品、罐头等,虽然生产工艺比较简单,但其呈香呈味物质成分并不能够完全地被提取利用,造成了其中风味物质的浪费。食用菌鲜味物质的提取有很多方法,传统方法一般为热水浸提,在实际生产过程中,其提取效率较低、能耗大,现今生物酶解技术作为一种新型的制备工艺,已广泛应用于食用菌的加工处理中,通过蛋白酶进行酶解处理,双孢蘑菇细胞壁中的蛋白质得以降解,使得其细胞内部的风味物质溶出,且能将溶出的大分子蛋白降解成各种呈味的多肽或氨基酸,使其风味更佳。周超等[10]采用酶解技术对茶褐牛肝菌进行酶解,在最佳酶解条件下,酶解液中肽质量浓度高达9.27 mg/mL,酶解液为浅褐色,透明性良好,菌香浓郁,鲜味突出;赵立娜等[11]对双孢蘑菇进行蛋白酶酶解,酶解液再通过美拉德反应可制备成具有食用菌特有浓郁芳香味的呈味基料,并且味道鲜美适口、醇厚。因此,为提高双孢蘑菇中呈味氨基酸的提取利用,其酶解处理的研究成为重点。
本研究以水解液的可溶性固形物、游离氨基酸浓度、色差、滋味为指标,对4 种不同的蛋白酶酶解处理效果进行对比研究,筛选双孢蘑菇酶解处理的最佳蛋白酶,并以水解液游离氨基酸浓度为指标,结合单因素及正交试验方法研究最佳蛋白酶的最优水解工艺,由最佳工艺制备所得的双孢蘑菇水解液可为双孢蘑菇调味品的生产提供实验参考。
双孢蘑菇(Agaricus bisporus) 天润吴记高效生态农业有限公司;中性蛋白酶(酶活力50 000 U/g)、木瓜蛋白酶(酶活力100 000 U/g)、复合蛋白酶(酶活力100 000 U/g)、风味蛋白酶(酶活力30 000 U/g)北京索莱宝科技有限公司;纯碱、柠檬酸(均为食品级) 山东优索化工科技有限公司;总氨基酸(T-AA)含量测定试剂盒 南京建成生物科技有限公司。
FE20/EL20型pH计 梅特勒-托利多仪器(上海)有限公司;CM-5分光测色计 柯尼卡美能达控股株式会社;WYT型手持式折光仪 上海沪粤明科学仪器有限公司、L-8900全自动氨基酸分析仪 日本日立公司;味觉指纹分析仪 日本Insent公司。
1.3.1 酶解工艺流程
原料预处理(挑选、清洗、切片)→漂烫→匀浆→酶解→灭酶→过滤→取上清液待用
原料预处理:挑选菇体无腐烂、无霉变的新鲜双孢蘑菇,流水清洗,纵向切成约0.5 cm厚的薄片。漂烫:将切片后的双孢蘑菇于沸水中进行漂烫杀青处理,以杀死细菌及其他有害物质,并达到灭酶目的,结束后将双孢蘑菇捞出沥干待用。匀浆:取护色后的双孢蘑菇,按照料液比1∶5(g/mL)加入去离子水后进行匀浆,以达到破碎细胞结构、使其内部风味物质溶出的目的。酶解:采用食品级柠檬酸、纯碱调节匀浆pH值,测定蛋白酶活力后,按照其底物含量加入一定活力单位的酶,保持酶解温度恒定,在一定时间内进行酶解。灭酶:酶解结束后将水解液在100 ℃灭酶15 min。
1.3.2 不同蛋白酶的酶解
取一定量的新鲜双孢蘑菇,清洗、烫漂后按料液比1∶5(g/mL)加入去离子水后匀浆,分别采用中性蛋白酶、木瓜蛋白酶、复合蛋白酶、风味蛋白酶4 种酶对双孢蘑菇进行酶解处理,各种蛋白酶的酶解条件以及水解时间见表1,按照表1条件进行酶解,加酶量均为1 000 U/g,酶解结束后,将水解液在100 ℃加热灭酶15 min,3 500 r/min离心10 min,取适量上清液备用进行指标测定。
表1 4 种酶的酶解条件
Table 1 Hydrolysis conditions of four enzymes

酶种类 pH 温度/℃ 时间/h对照组(不加酶) 常温 2中性蛋白酶 7.0 50 2木瓜蛋白酶 6.5 50 2复合蛋白酶 6.5 50 2风味蛋白酶 6.5 50 2
1.3.3 指标的测定
1.3.3.1 可溶性固形物的测定
取水解液上清液滴在折光仪棱镜的毛玻璃上,采用WYT型手持折光仪进行测定,读取可溶性固形物质量分数,每个样品测定3 次,结果取平均值。
1.3.3.2 色泽测定
采用全自动色差仪测定水解液的色泽,使用三色协调系统测定L*、a*、b*。L*表示明度,黑色为0,白色为100。坐标原点的颜色为无色(a*=0,b*=0)。在水平轴上,+a*表示颜色红,-a*表示颜色绿。在纵轴上,+b*表示颜色黄,-b*表示颜色蓝。
1.3.3.3 游离氨基酸浓度的测定
采用总氨基酸(T-AA)试剂盒参照说明书进行测定。
1.3.3.4 游离氨基酸组成的测定
采用L-8900全自动氨基酸分析仪进行测定。酶解处理后的上清液采用0.02 mol/L HCl溶液进行稀释,过0.22 μm滤膜上机检测。
1.3.3.5 电子舌指纹分析
取酶解处理后的上清液进行电子舌指纹分析,以无酶解处理作为对照组进行比对,每个样品重复扫描4 次,所得数据用电子舌数据分析系统(SA402B)对样品的鲜味、咸味、苦味、涩味、酸味、丰富性、一次回味和二次回味进行分析。
1.3.4 风味蛋白酶工艺优化试验
1.3.4.1 单因素试验
取一定量的新鲜双孢蘑菇,按料液比1∶5(g/mL)加入去离子水后匀浆,分别控制pH值、酶解温度、加酶量和酶解时间4 个因素,酶解结束后,将水解液100 ℃加热灭酶15 min,3 500 r/min离心10 min,取适量上清液备用进行指标测定。
控制酶解温度50 ℃、加酶量1 000 U/g、酶解时间2 h、pH值分别取5.5、6.0、6.5、7.0、7.5,考察pH值对酶解效果的影响;控制pH 6.5、加酶量1 000 U/g、酶解时间2 h,而酶解温度分别取30、40、50、60、70 ℃,考察酶解温度对酶解效果的影响;控制pH 6.5、酶解温度50 ℃、酶解时间2 h,而加酶量分别取500、750、1 000、1 250、1 500 U/g,考察加酶量对酶解效果的影响;控制pH 6.5、酶解温度50 ℃、加酶量1 000 U/g,而酶解时间分别取1、1.5、2、2.5、3 h,考察酶解时间对酶解效果的影响。
1.3.4.2 正交试验
在单因素试验结果的基础上,选择pH值、酶解温度、加酶量和酶解时间4 个因素,每个因素选取3 个水平进行L9(34)正交试验,以水解液游离氨基酸质量浓度为指标,对风味蛋白酶酶解工艺进行优化。正交试验选取的因素和水平如表2所示。
表2 正交试验设计L9(34)因素和水平
Table 2 Independent variables and their levels chosen for L9(34) orthogonal array design

水平 因素A酶解时间/h B酶解温度/℃ C pH D加酶量/(U/g)1 2.0 40 6.0 1 000 2 2.5 50 6.5 1 250 3 3.0 60 7.0 1 500
所得数据均用SPSS 20.0进行处理和统计分析。
2.1.1 酶解处理对双孢蘑菇水解液可溶性固形物质量分数、游离氨基酸浓度的影响

图1 4 种酶解处理对双孢蘑菇水解液可溶性固形物含量、游离氨基酸浓度的影响
Fig. 1 Contents of soluble solids and free animo acids in A. bisporus hydrolysates obtained with four different proteases
与大部分植物的细胞壁不同,食用菌细胞壁由蛋白质、几丁质、葡聚糖等组成[12-15],并且这些多糖与其他成分形成复杂的网状结构,导致食用菌的细胞壁结构致密,细胞内的成分不易释放,实验过程中对双孢蘑菇进行匀浆处理,对原本致密的细胞壁结构造成一定的破碎,同时,蛋白酶处理也可以增强细胞壁的通透性,对细胞内部成分的溶出有一定的促进作用[16-17],从而使得蛋白酶能够作用的底物浓度大大增加。经过不同蛋白酶酶解处理后,如图1所示,相对于没有进行酶解处理的对照组,4 种蛋白酶酶解后所得水解液中可溶性固形物质量分数及游离氨基酸浓度均有显著提高。其中,4 种蛋白酶水解后的可溶性固形物质量分数相近,这说明经过酶解处理可以提高双孢蘑菇中可溶性物质的溶出率,然而4 种蛋白酶对细胞壁通透性的改善则区别不显著。但从水解液的游离氨基酸浓度可以发现,4 种蛋白酶对于溶出物质的降解程度具有显著的区别。游离氨基酸浓度越高,说明蛋白质的降解程度越高,其酶解效果越好,从图1可以看出,酶解效果从高到低依次为风味蛋白酶、中性蛋白酶、复合蛋白酶和木瓜蛋白酶。其中,中性蛋白酶属于内切酶,是一类在中性条件下作用于蛋白质肽键的蛋白酶,而复合蛋白酶则是为水解蛋白质而研制的杆菌蛋白酶复合体,其主酶是碱性蛋白酶;风味蛋白酶则包含了内切蛋白酶与外切肽酶2 种活性,因此蛋白质的水解较为彻底。
2.1.2 酶解处理对双孢蘑菇水解液游离氨基酸组成的影响由于蛋白酶的种类不同,其降解蛋白质的作用位点不同,其水解产物也会产生显著的差异,降解后所得游离态氨基酸不仅具有各种生理功能,而且大多数氨基酸及其盐具有甜味或苦味,少数几种具有鲜味或酸味[18],因此不同的游离氨基酸组成造成了食用菌不同的滋味[19]。谷氨酸、天冬氨酸、苯丙氨酸、丙氨酸、甘氨酸和酪氨酸这6 种氨基酸能够呈现出特殊的鲜味[20],其中L-谷氨酸钠盐是味精的主要成分,是天然氨基酸中鲜味最强的物质,其次为天冬氨酸及其钠盐。甘氨酸、丙氨酸为甜味氨基酸[21-22]。
表3 4 种酶解处理对双孢蘑菇水解液游离氨基酸组成的影响
Table 3 Amino acid compositions of A. bisporus hydrolysates obtained with four different proteases

注:同行不同小写字母表示差异显著,P<0.05。
氨基酸 游离氨基酸质量浓度/(mg/L)对照组 中性蛋白酶 木瓜蛋白酶 复合蛋白酶 风味蛋白酶天冬氨酸Asp 98.58±0.60c105.73±1.44b103.87±2.58b106.77±2.42b142.11±3.40a苏氨酸Thr 150.98±0.60b151.44±2.34b167.05±4.42a65.80±1.42d134.17±3.04c丝氨酸Ser 32.57±0.25d44.03±0.70b39.55±1.01c46.07±0.97b90.65±2.23a谷氨酸Glu 154.05±0.78c228.96±3.64b162.39±4.26c283.87±6.64a220.68±5.59b甘氨酸Gly 14.95±0.14e22.44±0.34c18.87±0.48d24.49±0.60b47.36±1.26a丙氨酸Ala 52.97±0.30d76.77±1.26b64.30±1.74c78.15±1.78b124.00±3.27a半胱氨酸Cys 6.17±0.12d8.23±0.13c6.36±0.16d8.58±0.10b10.31±0.32a缬氨酸Val 18.18±0.03e78.40±1.33b32.88±0.79d74.73±1.72c105.23±2.84a甲硫氨酸Met 4.55±0.25d28.80±0.48b11.44±0.43c29.47±0.64b39.18±0.97a异亮氨酸Ile 13.39±0.11d80.37±1.28b27.55±1.41c78.26±1.73b95.07±2.56a亮氨酸Leu 25.05±0.05d118.65±1.98b49.69±3.67c116.65±2.74b160.82±4.38a酪氨酸Tyr 16.65±0.05d42.43±0.85b24.32±5.39c43.22±1.29b84.50±2.20a苯丙氨酸Phe 25.96±0.344d154.78±2.78b67.85±14.11c160.23±3.26a145.18±3.82b赖氨酸Lys 87.74±0.58d117.33±1.84a95.92±6.99c118.95±2.73a106.79±2.74b组氨酸His 12.19±0.14d27.94±0.37b17.82±5.27c29.05±0.66b48.95±1.29a精氨酸Arg 17.56±0.32e70.78±0.99c45.32±2.43d81.93±2.34b122.73±3.23a脯氨酸Pro 57.38±0.79c65.62±0.85b66.14±1.52b64.85±2.05b74.33±0.73a总量 788.93±3.61d1 422.70±22.58b1 001.31±54.74c1 411.06±32.11b1 752.07±43.40a
从表3可以看出,4 种蛋白酶处理后,各游离氨基酸及其总量都显著提高,其中风味蛋白酶的水解效果最为显著,其水解液中的游离氨基酸质量浓度总计达到1 752.07 mg/L。同时,风味蛋白酶可使水解液形成独特的风味和减少水解造成的苦味,其水解液中呈鲜味的主要氨基酸为天冬氨酸和谷氨酸,且质量浓度分别达到142.11 mg/L和220.68 mg/L。甘氨酸对食用菌呈味效果影响较大[23],甘氨酸除了本身可以提供清香甜味以外,还能减少苦味并从食物中除去不快的滋味[24],风味蛋白酶水解后的甘氨酸含量也显著高于其他处理组。苏氨酸作为脂肪族氨基酸,稍具甜味[25],复合蛋白酶和风味蛋白酶酶解后苏氨酸质量浓度相对于无酶处理组反而显著下降,特别是复合蛋白酶,其苏氨酸质量浓度比无酶处理组降低了56.42%,风味蛋白酶酶解后苏氨酸质量浓度虽然也有所下降,但其仅降低了0.11%。因此可以得出,风味蛋白酶对双孢蘑菇的水解较为彻底,其水解液中游离氨基酸总量及呈味氨基酸质量浓度相对于其他处理组显著提高。
2.1.3 酶解处理对双孢蘑菇水解液色差的影响

图2 4 种酶解处理对双孢蘑菇水解液色差的影响
Fig. 2 Color parameters of A. bisporus hydrolysates obtained with four different proteases
酶解处理后,水解液中大分子物质分解成游离的小分子物质,水解液的颜色也会产生一定变化,同时水解液在后续的干燥及造粒工艺过程中,其最终所得的酶解粉末、颗粒颜色也会有所影响,根据实际生产要求,最终产品应避免过深的颜色。因此,实验对4 种不同酶解处理后所得水解液的色差进行测定,从图2可以看出,各种酶解处理均对水解液的色差值(L*、a*、b*)产生了影响。水解后,水解液的L*值均有显著上升,说明其亮度显著提高,水解液颜色变得更为明亮,其中风味蛋白酶酶解后水解液的L*值最高;从a*值可以看出,酶解处理会使得水解液的红绿色调产生显著变化,即红色减弱,绿色加强;从b*值可以看出,中性蛋白酶及风味蛋白酶对于水解液黄蓝色调的影响不显著。因此,可以得出,风味蛋白酶可以在基本保持其水解液原本色调的基础上,使水解液的亮度提高,水解液颜色清透明亮。
2.1.4 不同酶解处理电子舌分析结果
风味的分析通常采用感官评价法,但该方法易受环境条件和人体主观意识主导[26],影响最终结果的准确性,电子舌技术是模拟生物活体的味觉感受机理[27],通过检测各种味觉物质和人工脂膜之间的静电作用或疏水性相互作用产生的膜电势变化,实现对各种滋味的评价,食品中已广泛运用该技术对味觉进行表征,客观和准确地区分不同样品[28],在调味基料的制备工艺中也已有应用[29]。由图3可以直观地看出不同处理组之间的区别,结合表4方差分析可以看出,水解液的苦味、涩味、鲜味、丰富性和咸味之间存在极显著差异(P<0.01),而酸味、一次回味、二次回味则差异不显著。从图3可以看出,各酶解处理后,水解液滋味的丰富性都显著上升,其中,中性蛋白酶、木瓜蛋白酶和复合蛋白酶酶解后,水解液的苦味和涩味都显著上升,而鲜味和咸味则显著降低,反之,风味蛋白酶酶解处理后,水解液的苦味、涩味显著降低,鲜味和咸味则显著升高。由于不同的酶切断蛋白质的位点不同,水解后生成的呈味氨基酸、短肽链也有所不同,因此,即使水解度较高,其风味也会有所变化。呈味肽是指对食品风味具有一定贡献的寡肽类物质,通常分子质量小于5 000 u,可赋予食品微妙而细腻的风味。肽不仅可以直接呈味,而且可以与其他风味物质相互协同,增强或改变原有的味道,也可以作为挥发性风味物质的前体参与美拉德反应,形成特殊的芳香化合物[30-31]。苦味、涩味的形成可能是因为蛋白水解后形成了苦味肽,而风味蛋白酶则可以控制肽的苦味,其原理为通过内切蛋白酶切断多肽内部的肽键,形成短链肽,其中一些含有疏水氨基酸,因而成为苦肽,使用外切酶每一次从多肽链的末端切断释放一个氨基酸,从而把苦肽彻底降解为氨基酸。
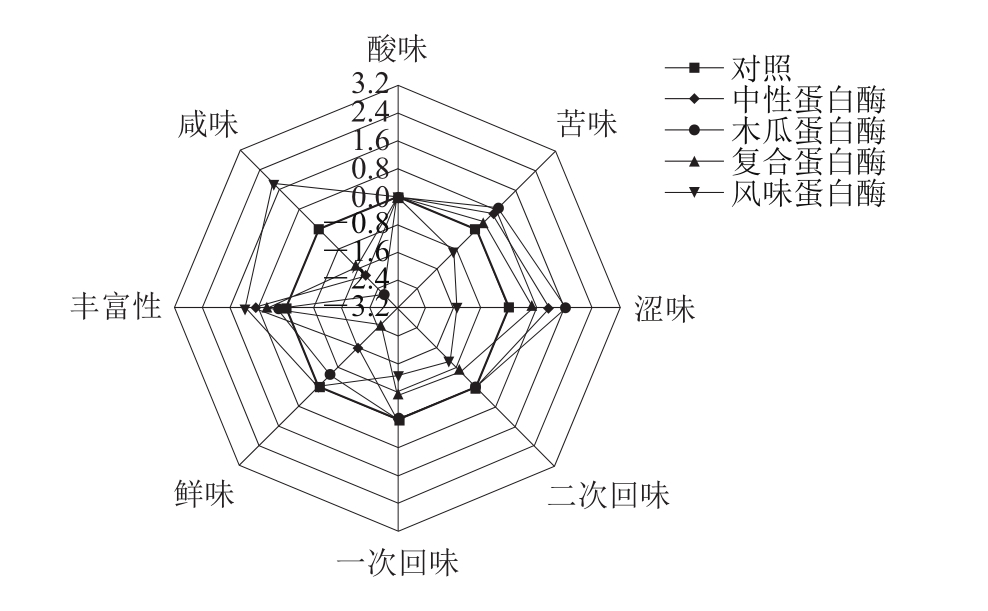
图3 4 种酶解处理对双孢蘑菇水解液滋味的影响
Fig. 3 Taste profiles of A. bisporus hydrolysates obtained with four different proteases
表4 4 种酶解处理电子舌方差分析
Table 4 Analysis of variance of the effect of four proteases on taste characteristics of A. bisporus hydrolysate

注:*.差异显著,P<0.05;**.差异极显著,P<0.01。表6同。
差异来源 项目 平方和 自由度 均方 F值 P值酸味组间 0.000 4 0.000 1.000 0.452组内 0.000 10 0.000总数 0.000 14苦味组间 5.708 4 1.427 19.550 <0.001**组内 0.730 10 0.073总数 6.438 14涩味组间 18.052 4 4.513 46.125 <0.001**组内 0.978 10 0.098总数 19.030 14二次回味组间 2.839 4 0.710 0.780 0.563组内 9.106 10 0.911总数 11.945 14一次回味组间 3.956 4 0.989 0.732 0.590组内 13.510 10 1.351总数 17.466 14鲜味组间 15.463 4 3.866 48.584 <0.001**组内 0.796 10 0.080总数 16.258 14丰富性组间 2.523 4 0.631 19.737 <0.001**组内 0.320 10 0.032总数 2.843 14组间 38.964 4 9.741 552.418<0.001**组内 0.176 10 0.018总数 39.140 14咸味
由不同蛋白酶水解双孢蘑菇实验结果可以得出,风味蛋白酶酶解处理后,双孢蘑菇水解液的可溶性固形物和游离氨基酸浓度均有显著升高,水解液颜色变亮,且其滋味较好,能够除去水解液中的苦味、涩味,并且可以显著提高其咸味和滋味的丰富性。因此,选择风味蛋白酶制备双孢蘑菇水解液,并采用单因素试验和正交试验对风味蛋白酶的酶解条件进行优化。
2.2.1 单因素试验结果

图4 不同因素对双孢蘑菇酶解效果的影响
Fig. 4 Effects of different factors on enzymatic hydrolysis of A. bisporus
从图4A可以看出,风味蛋白酶的最适pH值为6.5,在此pH值下,双孢蘑菇水解液的游离氨基酸浓度达到最高,同时,当pH值高于6.5时,游离氨基酸浓度呈显著下降趋势。因此,选择风味蛋白酶酶解的最佳pH值范围为6.0~7.0。
不同酶的最适温度不同,过高或过低的温度都会降低酶的催化效率,在适宜的温度范围内,温度每升高10 ℃,酶促反应速率可以相应提高1~2 倍;而过高的温度则会造成酶被破坏,发生不可逆的变性,即降低酶促反应速率。曹承旭等[32]评价了水解温度对风味蛋白酶活力的影响,证明在一定温度范围内,水解度随着水解温度升高而升高,本研究结果与之类似。从图4B可看出,当酶解温度从30 ℃上升到50 ℃时,双孢蘑菇水解液的游离氨基酸浓度有十分显著的上升趋势,但当酶解温度超过50 ℃时游离氨基酸浓度则出现了下降的趋势,此时酶活力受到抑制。因此确定风味蛋白酶的最佳酶解温度范围为40~60 ℃。
从图4C可以看出,当加酶量从500 U/g增加到1 250 U/g时,水解液的游离氨基酸浓度明显上升,水解度大幅增加,但当加酶量增加到1 500 U/g时,游离氨基酸浓度没有继续增加,这是由于当加酶量达到一定程度时,大部分底物参与反应,由于水解底物有限,即使加酶量继续增加,水解度也无法得到提高。因此,确定的最佳加酶量范围为1 000~1 500 U/g。
从图4D可以看出,随着酶解时间的延长,双孢蘑菇水解液的氨基酸浓度逐渐增大,当酶解时间达到2.5 h后,游离氨基酸达到较高的浓度,而后随着酶解时间的延长游离氨基酸浓度保持相对平稳,结合实际情况,过长的生产时间对工业生产带来不利,容易造成能耗过大、成本高的情况,因此选择2~3 h作为风味蛋白酶的最佳酶解时间范围。
2.2.2 正交试验结果
根据以上单因素试验结果,以pH值、酶解温度、加酶量、酶解时间为因素,以水解液游离氨基酸浓度作为考察指标,选取L9(34)正交试验,根据极差分析和方差分析的结果确定最佳的风味蛋白酶酶解工艺,其正交试验分析结果见表5,正交试验方差分析结果见表6。
表5 风味蛋白酶酶解L9(34)正交试验设计及结果
Table 5 L9(34) orthogonal array design with experimental results for optimization of enzymatic hydrolysis conditions
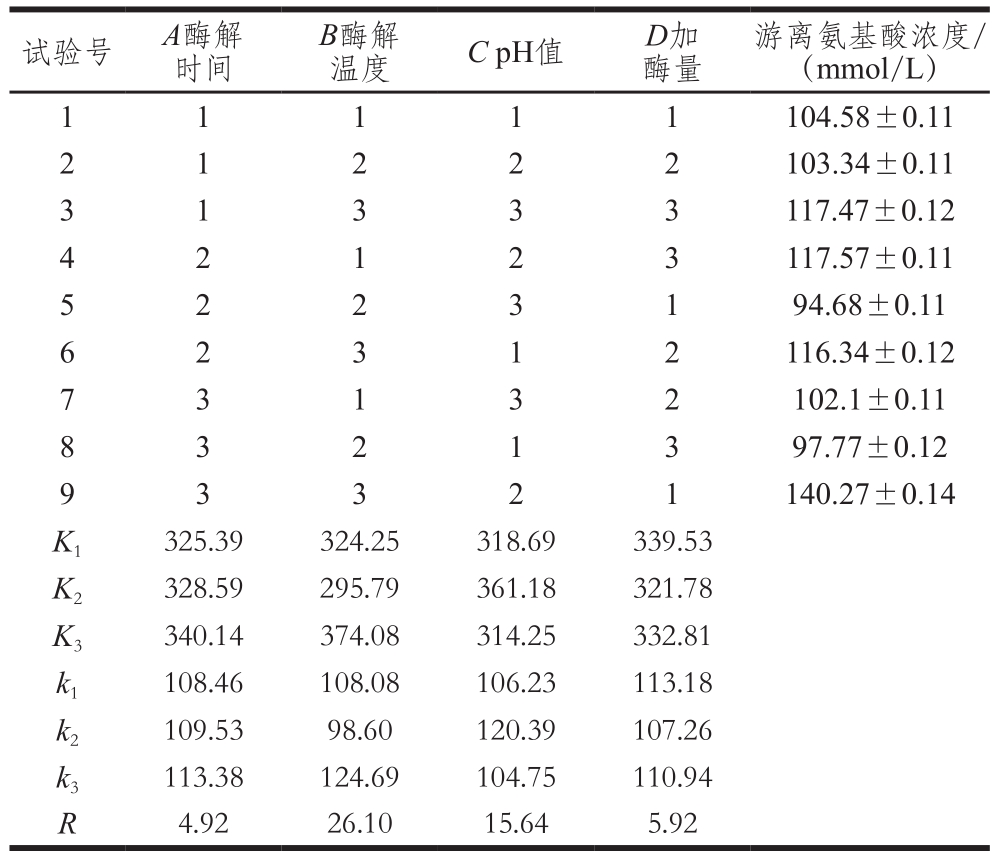
试验号 A酶解时间B酶解温度C pH值D加酶量游离氨基酸浓度/(mmol/L)1 1 1 1 1 104.58±0.11 2 1 2 2 2 103.34±0.11 3 1 3 3 3 117.47±0.12 4 2 1 2 3 117.57±0.11 5 2 2 3 1 94.68±0.11 6 2 3 1 2 116.34±0.12 7 3 1 3 2 102.1±0.11 8 3 2 1 3 97.77±0.12 9 3 3 2 1 140.27±0.14 K1325.39 324.25 318.69 339.53 K2328.59 295.79 361.18 321.78 K3340.14 374.08 314.25 332.81 k1108.46 108.08 106.23 113.18 k2109.53 98.60 120.39 107.26 k3113.38 124.69 104.75 110.94 R 4.92 26.10 15.64 5.92
比较表5中的4 个因素的极差R值可以发现各因素影响的大小依次为酶解温度、pH值、加酶量、酶解时间,从表6可以得出,酶解温度对风味蛋白酶酶解效果的影响达到极显著水平,pH值对风味蛋白酶的酶解效果达到显著水平,说明酶解温度和pH值是影响酶解效果的关键因素。由正交试验结果可以得出,最佳的风味蛋白酶酶解工艺条件组合为A3B3C2D1,即pH 6.5、酶解温度60 ℃、加酶量1 000 U/g、酶解时间3 h,在此条件下风味蛋白酶酶解效果最佳,游离氨基酸浓度为140.27 mmol/L。
表6 风味蛋白酶酶解条件方差分析
Table 6 Analysis of variance of the effect of hydrolysis conditions on free amino acid concentration
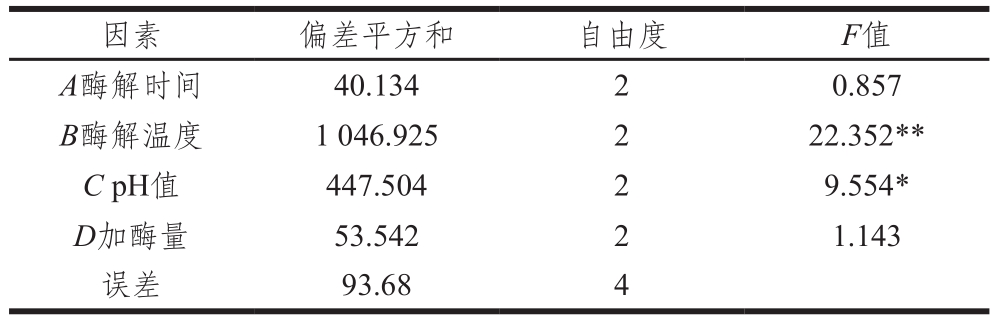
注:F0.05(2,4)=6.940;F0.01(2,4)=18.00。
因素 偏差平方和 自由度 F值A酶解时间 40.134 2 0.857 B酶解温度 1 046.925 2 22.352**C pH值 447.504 2 9.554*D加酶量 53.542 2 1.143误差 93.68 4
本实验采用4 种不同蛋白酶对双孢蘑菇进行酶解处理,通过对其酶解后所得水解液的可溶性固形物含量、游离氨基酸浓度、色泽及滋味特征进行研究,分析4 种酶对双孢蘑菇酶解效果的影响。结果发现,酶解处理可以显著提高水解液的可溶性固形物及游离氨基酸浓度。其中风味蛋白酶的水解效果最好,并且可以显著除去水解液的苦味、涩味,保持其鲜味,并显著提高其咸味和滋味的丰富性,在保持水解液原本色调的基础上,可以提高其颜色的亮度,为下一步加工双孢蘑菇调味品作基础。因此选择风味蛋白酶对双孢蘑菇进行酶解处理,并进一步对风味蛋白酶的酶解工艺进行优化。
以水解液游离氨基酸浓度为指标,对酶解时间、酶解温度、pH值和加酶量4 个因素进行单因素试验以及L9(34)正交试验,结果发现,各因素对水解液游离氨基酸浓度影响程度大小依次为酶解温度>pH值>加酶量>酶解时间,方差分析结果表明,酶解温度对风味蛋白酶酶解效果的影响达到极显著水平,pH值对风味蛋白酶的酶解效果达到显著水平。试验最终得出风味蛋白酶最佳酶解工艺为pH 6.5、酶解温度60 ℃、加酶量1 000 U/g、酶解时间3 h,游离氨基酸浓度为140.27 mmol/L。
[1] 李玉, 刘淑艳. 菌物学[M]. 北京: 科学出版社, 2015.
[2] 吴素玲, 孙晓明, 王波, 等. 双孢蘑菇子实体营养成分分析[J].中国野生植物资源, 2006, 25(2): 47-48. DOI:10.3969/j.issn.1006-9690.2006.02.016.
[3] 朱燕华, 王倩, 陈明杰, 等. 不同采摘期的双孢蘑菇子实体蛋白质营养评价[J]. 上海农业学报, 2016, 32(4): 29-34. DOI:10.15955/j.issn1000-3924.2016.04.07.
[4] 刘晓艳, 杨国力, 于纯淼. 功能型复合食用菌调味品的工艺开发研究[J]. 中国调味品, 2016(1): 121-123. DOI:10.3969/j.issn.1000-9973.2016.01.026.
[5] 沈文凤, 王文亮, 徐志祥, 等. 香菇调味料配方工艺研究[J].农产品加工, 2017(3): 24-27. DOI:10.16693/j.cnki.1671-9646(X).2017.02.008.
[6] ROTZOLL N, DUNKEL A, HOFMANN T. Quantitative studies,taste reconstitution, and omission experiments on the key taste compounds in morel mushrooms (Morchella deliciosa Fr.)[J].Journal of Agricultural & Food Chemistry, 2006, 54(7): 2705-2711.DOI:10.1021/jf053131y.
[7] CAIROLI P, PIERACCINI S, SIRONI M, et al. Studies on umami taste. synthesis of new guanosine 5’-phosphate derivatives and their synergistic effect with monosodium glutamate[J]. Journal of Agricultural & Food Chemistry, 2008, 56(3): 1043-1050.DOI:10.1021/jf072803c.
[8] 陈海强, 胡汝晓, 彭运祥, 等. 食用菌鲜味物质研究进展[J].现代生物医学进展, 2011, 11(19): 3783-3786. DOI:10.13241/j.cnki.pmb.2011.19.003.
[9] 曹世宁, 陈相艳, 崔文甲, 等. 食用菌中呈味物质的研究进展[J].食品工业, 2016(3): 231-234.
[10] 周超, 黄裕怡, 胡旭佳. 茶褐牛肝菌酶解制备呈味肽基料的工艺研究[J]. 昆明理工大学学报(自然科学版), 2017(4): 79-86.DOI:10.16112/j.cnki.53-1223/n.2017.04.013.
[11] 赵立娜, 陈紫红, 于志颖, 等. 利用双孢蘑菇蛋白酶解液制备呈味基料的研究[J]. 食品研究与开发, 2017, 38(23): 77-81. DOI:10.3969/j.issn.1005-6521.2017.23.014.
[12] FREE S J. Fungal cell wall organization and biosynthesis[J]. Advances in Genetics, 2013, 81: 33-82. DOI:10.1016/B978-0-12-407677-8.00002-6.
[13] MCCANN M C, BUSH M, MILIONI D, et al. Approaches to understanding the functional architecture of the plant cell wall[J].Phytochemistry, 2001, 57(6): 811-821. DOI:10.1016/S0031-9422(01)00144-3.
[14] KLIS F M, MOL P, HELLINGWERF K, et al. Dynamics of cell wall structure in Saccharomyces cerevisiae[J]. FEMS Microbiology Reviews,2002, 26(3): 239-256. DOI:10.1016/S0168-6445(02)00087-6.
[15] 段秀辉, 黄文, 李露, 等. 生物酶技术在食用菌加工中的应用[J].食用菌, 2014, 36(6): 3-5. DOI:10.3969/j.issn.1000-8357.2014.06.002.
[16] 郭耀华, 尚鑫茹, 岳兰昕, 等. 3 种蛋白酶对鲶鱼骨肉泥中多肽得率和钙溶出率的比较研究[J]. 食品科技, 2016, 41(2): 157-162.DOI:10.13684/j.cnki.spkj.2016.02.030.
[17] 葛静波, 林群英, 吴亮亮, 等. 蛹虫草多糖及可溶性固形物酶法提取试验[J]. 食用菌, 2016, 38(3): 58-60. DOI:10.3969/j.issn.1000-8357.2016.03.028.
[18] 廖兰, 赵谋明, 崔春. 肽与氨基酸对食品滋味贡献的研究进展[J].食品与发酵工业, 2009, 35(12): 107-113. DOI:10.13995/j.cnki.11-1802/ts.2009.12.027.
[19] WANG W K, ZHU Y, TANG Y, et al. Non-volatile taste components of different cultivated mushrooms at mycelia, primordium, and fruit body cultivation stages[J]. International Journal of Food Properties, 2016,19(9): 1938-1948. DOI:10.1080/10942912.2015.1089891.
[20] MARCUS J B. Culinary applications of umami[J]. Food Technology,2005, 59(5): 24-30.
[21] FUKE S, KONOSU S. Taste-active components in some foods: a review of Japanese research[J]. Physiology & Behavior, 1991, 49(5):863-868. DOI:10.1016/0031-9384(91)90195-T.
[22] WU H C, SHIAU C Y. Proximate composition, free amino acids and peptides contents in commercial chicken and other meat essences[J].Journal of Food & Drug Analysis, 2010, 10(3): 170-177.
[23] 陈惜燕, 蒲鹏, 康靖全, 等. 8 种食用菌游离氨基酸的组成及含量比较[J]. 西北农林科技大学学报(自然科学版), 2017, 45(5): 183-190.DOI:10.13207/j.cnki.jnwafu.2017.05.025.
[24] 李丁梅. 食品营养与化学[M]. 昆明: 云南科技出版社, 2015.
[25] 顾复昌, 高大忻. L-苏氨酸的发酵生产[J]. 中国酿造, 1984, 3(6): 20-25.
[26] PHAT C, MOON B, LEE C. Evaluation of umami taste in mushroom extracts by chemical analysis, sensory evaluation, and an electronic tongue system[J]. Food Chemistry, 2016, 192(10): 68-77.DOI:10.1016/j.foodchem.2015.07.113.
[27] 刘瑞新, 李慧玲, 李学林, 等. 基于电子舌的穿心莲水煎液的掩味效果评价研究[J]. 中草药, 2013, 44(16): 2240-2245. DOI:10.7501/j.issn.0253-2670.2013.16.009.
[28] KOBAYASHI Y, HABARA M, IKEZAZKI H, et al. Advanced taste sensors based on artificial lipids with global selectivity to basic taste qualities and high correlation to sensory scores[J]. Sensors, 2010,10(4): 3411-3443. DOI:10.3390/s100403411.
[29] 陈晓婷, 吴靖娜, 路海霞, 等. 基于电子鼻和电子舌优化蓝圆鲹调味基料的制备[J]. 食品科学, 2018, 39(4): 282-289. DOI:10.7506/spkx1002-6630-201804042.
[30] 吴婕, 穆利霞, 林光月, 等. 呈味肽的制备及稳态化研究进展[J].农产品加工, 2016(2): 62-64. DOI:10.16693/j.cnki.1671-9646(X).2016.01.048.
[31] 张铭霞, 陈思羽, 李露, 等. 食品中呈味肽类组分研究进展[J].中国食品学报, 2016, 16(2): 209-217. DOI:10.16429/j.1009-7848.2016.02.029.
[32] 曹承旭, 赵春燕, 马越, 等. 复合风味蛋白酶酶解温度对籽瓜籽蛋白特性的影响[J]. 食品科技, 2017, 42(6): 219-223. DOI:10.13684/j.cnki.spkj.2017.06.020.
Comparison of Efficiencies of Four Proteases in Hydrolyzing Agaricus bisporus and Optimization of Flavorzyme Hydrolysis Process