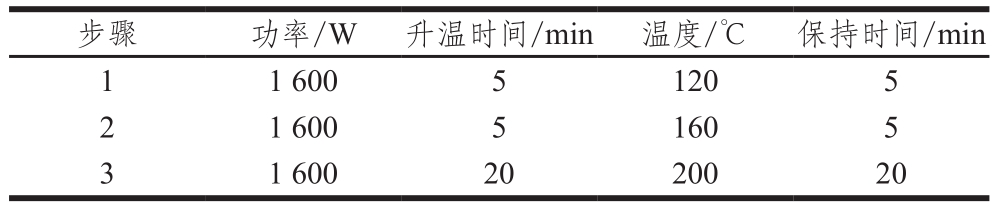
表1 微波消解程序
Table 1 Microwave digestion procedure
步骤 功率/W 升温时间/min 温度/℃ 保持时间/min 1 1 600 5 120 5 2 1 600 5 160 5 3 1 600 20 200 20
镉是一种自然界普遍存在的、具有蓄积性的有毒重金属元素,可通过食物链进入人体损伤肾脏、肝脏、骨骼、免疫系统和心血管系统等[1]。食用植物油在原料种植、生产加工、运输、贮存过程可能会引入镉,因此,建立食用油中镉的简便、快速、准确分析方法,对于保障食用油质量与安全显得至关重要[2]。
食品中重金属的检测仪器主要有原子吸收光谱、电感耦合等离子体质谱(inductively coupled plasma mass spectrometry,ICP-MS)、电感耦合等离子体发射光谱等[3-8]。食用油由于其复杂基质特性、重金属元素低含量特征,导致食用油中的重金属元素的检测较为困难,必须对样品进行前处理[2,9]。前处理过程是食用油中重金属分析准确性、稳定性、便利性等的关键所在,这也一直是检验工作者的难点。
目前,食用油样品前处理方法主要是消解法,包括干法消解、湿法消解以及微波消解。其中微波消解因其密封性好、消解彻底,是目前食品中重金属含量检测应用最为广泛的前处理方法。但是,消解法所需的实验条件较为苛刻,高温、高压也相对危险,容易产生爆炸、环境污染、分析物损失、回收率低等问题[10-11]。针对这些问题,近年来,基于液液萃取、固相萃取、直接进样等温和的食用油样品前处理技术日渐成为研究热点[12-15]。但是重金属元素和食用油基质种类多样,对于特定元素,仍需探索建立适合的前处理方法,才能保证在各类食用油检测中的可靠性。
破乳诱导萃取法是通过乳化作用,分散加速萃取食用油中的金属元素至酸溶液中[16-17]。破乳诱导萃取法需要用乳化剂、酸与食用油样品充分混合形成油包水乳状液,通过加热或离心的方法破乳,破乳后油样品中的重金属转移到酸溶液中,最后移取出酸性水相进行检测。该方法具有简单、耗时短、可减少样品污染和分析物损失的优点[18-19]。ICP-MS具有检出限(limit of detection,LOD)低、灵敏度高、线性范围广等优点,被广泛应用于重金属检测[20-24]。本研究建立操作简单、耗时短的破乳诱导萃取法,并结合ICP-MS测定食用油中镉含量。通过加标回收率测定各实验参数对萃取效率的影响,进而确定较优的实验参数,将优化建立的检测方法应用于各类食用油样品的检测,为实现食用油中重金属检测的快速前处理提供参考。
大豆油、葵花籽油、菜籽油、玉米油、花生油、稻米油和米糠油7 种食用油均购自于南京苏果超市。
硝酸(优级纯) 国药集团化学试剂有限公司;曲拉通X-114(Triton X-114)、曲拉通X-100(Triton X-100) 美国阿拉丁试剂有限公司;S-21重金属标准油溶液(100 mg/L) 美国Conostan公司;国家标准样品GSB 04-1721-2004 Cd单元素标准溶液 国家有色金属及电子材料分析测试中心;Ce、Co、Li、Tl和Y的ICPMS调谐储备液(10 mg/L),Bi、Ge、In、Li、Lu、Rh、Sc和Tb的ICP-MS内标液(100 mg/L) 美国安捷伦公司;超纯水(电阻率≥18.24 MΩ·cm)。
TE214S电子分析天平 赛多利斯科学仪器(北京)有限公司;DMT-2500多管旋涡混合器 常州恩培仪器制造有限公司;B-220恒温水浴锅 上海亚荣生化仪器厂;MARS 6 CLASSIC微波消解仪 美国CEM公司;BHW-09C赶酸仪 上海博通化学科技有限公司;7700X ICP-MS仪(配有同心雾化器和半导体控温石英雾室) 美国安捷伦公司。
1.3.1 破乳诱导萃取法萃取食用油中重金属
称取一定量的食用油至15 mL离心管中,然后向离心管中加入2 mL曲拉通酸性溶液(含一定体积分数的硝酸)。1 500 r/min涡旋10 min后,90 ℃水浴加热,使乳状液破裂而分为三相:上层为富含有机物的油相,中间层为含有从油样品中萃取出来的金属元素的酸溶液,下层为与酸溶液分离的表面活性剂。准确移取出中间层的酸溶液1.0~1.5 mL置于10 mL离心管中,去离子水稀释3 倍,待测。
1.3.2 破乳诱导萃取实验参数的优化
破乳诱导萃取法中影响结果准确性的主要实验参数包括表面活性剂的类型、表面活性剂的质量浓度、酸的体积分数以及取样量[16,25]。本实验采用菜籽油作为方法优化实验的食用油样品。
1.3.2.1 表面活性剂的类型
破乳诱导萃取实验中使用的表面活性剂主要为Triton X-114和Triton X-100,表面活性剂不同,回收率及破乳时间也会有所不同[26]。分别采用Triton X-114和Triton X-100对加标量为10 ng/g的食用油进行破乳诱导萃取,测定加标回收率,选择最佳的表面活性剂。
1.3.2.2 表面活性剂质量浓度
在硝酸体积分数5%不变的条件下,将表面活性剂分为5 个质量浓度梯度0、0.01、0.03、0.09 g/mL和 0.15 g/mL,对加标量为10 ng/g的食用油进行破乳诱导萃取,用ICP-MS检测其中镉的含量,计算加标回收率。
1.3.2.3 硝酸体积分数
金属在食用油中以自由形式存在于有机物中或作为有机配合物的一部分,而酸溶液会取代有机结构的金属,使得金属转移到水溶液中[27]。硝酸体积分数是影响破乳诱导萃取的关键实验参数,在表面活性剂Triton X-114质量浓度为0.09 g/mL的条件下,分别选择硝酸体积分数0%、1%、5%、10%和20% 5 个梯度,对加标量为10 ng/g的食用油进行破乳诱导萃取,并测定其中镉的含量,计算加标回收率。
1.3.2.4 食用油取样量
在保持提取液体积为2 mL的条件下,若取样量减少,部分元素可能由于含量过低而无法检出;若取样量增加,可减小误差并提升灵敏度,但会影响破乳时间及回收率。分别取0.5、1.0、2.0、4.0 g和8.0 g 5 个梯度的加标量10 ng/g的食用油,进行实验,计算加标回收率。
1.3.3 微波消解食用油中重金属
准确称取0.100 0 g食用油样品至微波消解管中,加入10 mL浓硝酸,120 ℃预消解1 h冷却后,进行消解,程序见表1。消解结束之后,在赶酸仪中180 ℃赶酸至溶液剩余约1 mL,冷却至室温,用2%硝酸溶液转移定容至10 mL,待测。
表1 微波消解程序
Table 1 Microwave digestion procedure

步骤 功率/W 升温时间/min 温度/℃ 保持时间/min 1 1 600 5 120 5 2 1 600 5 160 5 3 1 600 20 200 20
1.3.4 ICP-MS测定食用油中重金属的含量
标准溶液:精密量取镉标准溶液适量,用2%硝酸溶液作为溶剂逐级稀释配制含量分别为0、1、10、50、20、100、200 ng/g的标准溶液,用于绘制ICP-MS标准工作曲线。
ICP-MS仪器工作条件:射频功率1 548 W,等离子体气体流量15.00 L/min,辅助气流量1.00 L/min,载气流量1.00 L/min,补偿/稀释气流量1.00 L/min,雾化室温度2 ℃,蠕动泵泵速18 r/min,元素积分时间0.30 s,采集模式:质谱图,峰形3 个点,重复次数3 次,采集质量数111Cd,内标115In。
2.1.1 表面活性剂的类型对回收率的影响
Triton X-114酸溶液的回收率为(107.6±1.9)%(n=3)、Triton X-100酸溶液的回收率为(85.4±1.3)%(n=3),同时Triton X-114酸溶液所需的破乳时间在20~50 min,而Triton X-100需要的时间更长,约为使用Triton X-114的1.2 倍,因此确定Triton X-114作为萃取的表面活性剂。
2.1.2 表面活性剂质量浓度对回收率的影响
由图1可知,表面活性剂Triton X-114质量浓度为0~0.03 g/mL,回收率随着表面活性剂质量浓度的增加而增加;表面活性剂质量浓度大于0.03 g/mL,随着表面活性剂质量浓度增加,萃取效率无显著变化。鉴于适当提高表面活性剂质量浓度可以加速形成均匀的乳液体系,同时可以增强方法对于各类食用油样品的适应性和稳定性[27-28],因此最终选择萃取液中表面活性剂质量浓度为0.09 g/mL用于后续实验。
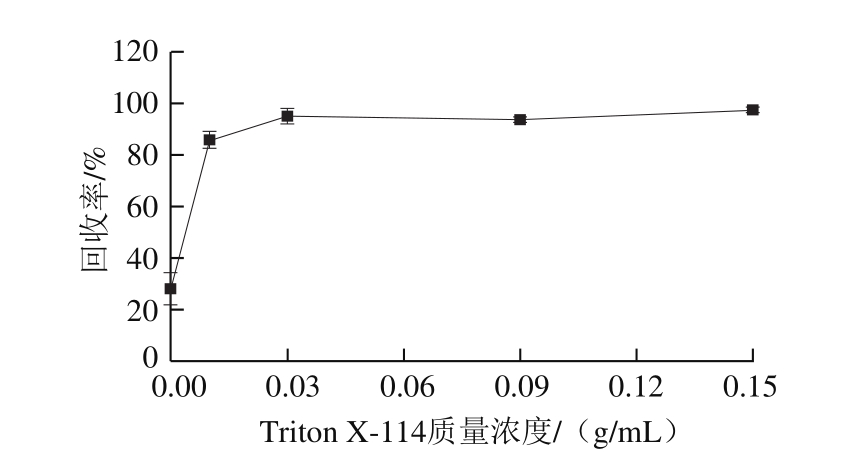
图1 表面活性剂Triton X-114质量浓度对萃取食用油中镉的回收率的影响
Fig. 1 Effect of surfactant concentration on the recovery of Cd in edible oil
2.1.3 硝酸体积分数对回收率的影响
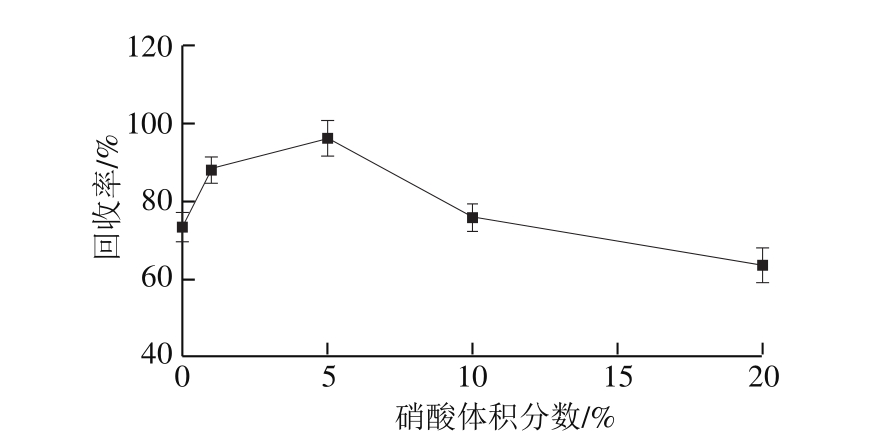
图2 硝酸体积分数对萃取食用油中镉的回收率的影响
Fig. 2 Effect of nitric acid concentration on the recovery of Cd in edible oil
由图2可知,硝酸体积分数为0%~5%,回收率随硝酸体积分数的增加而增加;硝酸体积分数大于5%,回收率则随硝酸体积分数的增加而降低。这可能是由于ICPMS检测对样品基质有一定的要求,高浓度的硝酸有一定的氧化能力,在前处理过程中导致食用油样品和表面活性剂出现一定氧化分解,基质干扰抑制了金属离子的信号,进而出现随着硝酸体积分数增加回收率降低的情况。因此,选择萃取液中硝酸体积分数为5%用于后续实验。
2.1.4 食用油取样量对回收率的影响
由图3可知,取样量为0.5~2.0 g,随着取样量的增加,回收率增加;取样量大于2.0 g,随着取样量的增加,回收率有所降低。可能原因在于食用油量太少难以充分形成稳定的油包水乳液体系,而食用油量太大则导致单位时间内萃取不充分[29]。此外,随着取样量的增加,破乳时间将会延长几倍。因此,综合考虑回收率和破乳时间,取2.0 g作为食用油最佳取样量。

图3 食用油取样量对萃取食用油中镉的回收率的影响
Fig. 3 Effect of edible oil mass on the recovery of Cd
在ICP-MS最佳测定条件下,测定分别为0、0.1、1、10、50、100、200 ng/g的标准溶液,绘制标准曲线,以含量为横坐标x、检测信号强度为纵坐标y,得出线性方程为y=350.52x+81.739、相关系数R大于0.999 9。对空白食用油样品,进行低含量加标并用空白样品进行逐级稀释,再分别按照优化的样品前处理条件和仪器分析条件处理检测,以3 倍信噪比作为标准,得到方法LOD为0.031 ng/g。
2.3.1 不同加标水平的回收率
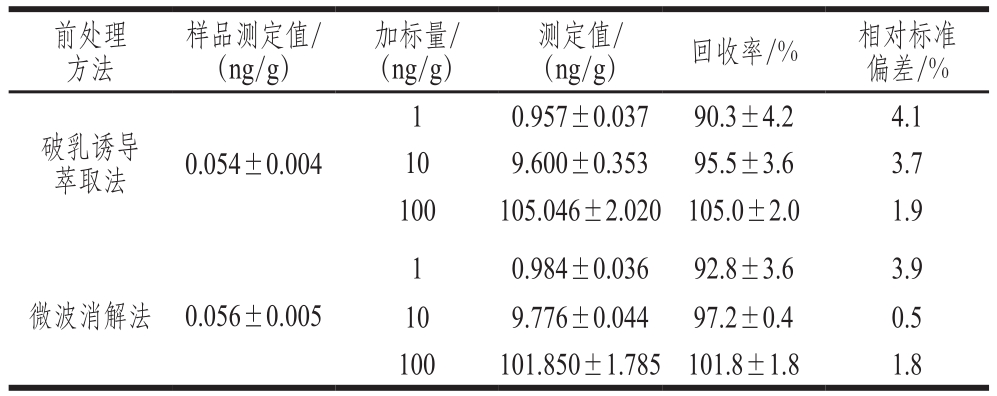
表2 不同加标水平镉的回收率(n=3)
Table 2 Recoveries of Cd at different spiked levels (n= 3)
前处理方法样品测定值/(ng/g)加标量/(ng/g)(ng/g)回收率/%相对标准偏差/%测定值/破乳诱导萃取法 0.054±0.004 1 0.957±0.037 90.3±4.2 4.1 10 9.600±0.353 95.5±3.6 3.7 100 105.046±2.020 105.0±2.0 1.9微波消解法 0.056±0.005 1 0.984±0.036 92.8±3.6 3.9 10 9.776±0.044 97.2±0.4 0.5 100 101.850±1.785 101.8±1.8 1.8
用S-21分析油标准溶液配制3 个不同加标水平的加标油样品,用优化的破乳诱导法和微波消解法提取样品中的重金属,得到加标回收率及相对标准偏差,如表2所示。破乳诱导萃取法的加标回收率为90.3%~105.0%、相对标准偏差为1.9%~4.1%,检测结果与微波消解法所测得的样品中镉元素值和所得的回收率无显著性差异(P>0.05),表明优化建立的破乳诱导法准确性高、稳定性好。
2.3.2 食用油的加标回收率
为验证所建立的方法对不同食用油的适用性,将优化的实验条件应用于玉米油、米糠油及10 ng/g加标样品的萃取和测定,得到玉米油的加标回收率为(95.5±4.7)%(n=3),米糠油的加标回收率为(98.5±2.6)%(n=3),表明破乳诱导萃取法适用于多种食用油样品基质。
在优化的实验条件下对市售的食用油样品进行测定,得到各个食用油中镉的含量,如表3所示。其中,大豆油、葵花籽油、玉米油和稻米油中均未检出镉(<LOD),而花生油中镉含量最高为(0.364±0.070) ng/g。破乳诱导萃取法和微波消解法2 种方法处理所测得的镉含量基本一致,进一步证实了本研究所建立方法的可靠性。
表3 食用油样品的镉含量检测结果
Table 3 Cd contents in various edible oils ng/g

种类 破乳诱导萃取法 微波消解法大豆油 <LOD <LOD葵花籽油 <LOD <LOD菜籽油 0.054±0.004 0.056±0.005玉米油 <LOD <LOD花生油 0.364±0.070 0.383±0.041稻米油 <LOD <LOD米糠油 0.190±0.008 0.176±0.015
本实验以食用油中的镉为研究对象,采用破乳诱导萃取法进行样品前处理,ICP-MS测定食用油中的微量镉,方法简单、快速、准确、稳定,可用于食用油中重金属的快速前处理以及食用油的日常监督检测。调查市售食用油中镉的含量,结果表明市售食用油中镉的含量较低,对健康风险影响较小。该方法与传统检测方法的对比结果令人满意,对食用油中的其他重金属元素测定具有重要的参考价值。
[1] TELLEZPLAZA M, NAVASACIEN A, MENKE A, et al. Cadmium exposure and all-cause and cardiovascular mortality in the U.S. general population[J]. Environmental Health Perspectives, 2012, 120(7): 1017-1022. DOI:10.1289/ehp.1104352.
[2] MA F, WU R, LI P W, et al. Analytical approaches for measuring pesticides, mycotoxins and heavy metals in vegetable oils: a review[J].European Journal of Lipid Science & Technology, 2016, 118(3): 339-352. DOI:10.1002/ejlt.201400535.
[3] 邱会东, 赵波, 张红, 等. 食用植物油中重金属分析方法的研究进展[J]. 中国油脂, 2017, 42(1): 76-79. DOI:10.3969/j.issn.1003-7969.2017.01.019.
[4] 陈尚龙, 刘全德, 李超, 等. 微乳液直接进样-石墨炉原子吸收光谱法测定食用油中的锰[J]. 食品科学, 2011, 32(18): 278-281.DOI:10.7506/spkx1002-6630-201118062.
[5] ALMEIDA J S, SANTOS G L, BRANDÃO G C, et al. Multivariate optimization of ultrasound-assisted extraction using Doehlert matrix for simultaneous determination of Fe and Ni in vegetable oils by high-resolution continuum source graphite furnace atomic absorption spectrometry[J]. Food Chemistry, 2019, 273: 130-135. DOI:10.1016/j.foodchem.2018.01.112.
[6] ACAR O. Evaluation of cadmium, lead, copper, iron and zinc in Turkish dietary vegetable oils and olives using electrothermal and flame atomic absorption spectrometry[J]. Grasas Y Aceites, 2012,63(4): 383-393. DOI:10.3989/gya.047512.
[7] NI Z L, TANG F B, YU Q, et al. Determination of trace elements in camellia oil by vortex-assisted extraction followed by inductively coupled plasma mass spectrometry[J]. Food Analytical Methods, 2016,9(5): 1134-1141. DOI:10.1007/s12161-015-0281-9.
[8] LLORENTMARTÍNEZ E J, ORTEGABARRALES P,FERNÁNDEZDE C M L, et al. Investigation by ICP-MS of trace element levels in vegetable edible oils produced in Spain[J].Food Chemistry, 2011, 127(3): 1257-1262. DOI:10.1016/j.foodchem.2011.01.064.
[9] TOKAY F, BAĞDAT S. Extraction of nickel from edible oils with a complexing agent prior to determination by FAAS[J]. Food Chemistry,2016, 197: 445-449. DOI:10.1016/j.foodchem.2015.11.001.
[10] EULOGIO J L, PILAR O, ANTONIO R, et al. Quantitation of metals during the extraction of virgin olive oil from olives using ICP-MS after microwave-assisted acid digestion[J]. Journal of the American Oil Chemists Society, 2014, 91(10): 1823-1830. DOI:10.1007/s11746-014-2511-5.
[11] BAKIRCIOGLU D, KURTULUS Y B, YURTSEVER S. Comparison of extraction induced by emulsion breaking, ultrasonic extraction and wet digestion procedures for determination of metals in edible oil samples in Turkey using ICP-OES[J]. Food Chemistry, 2013,138(2/3): 770-775. DOI:10.1016/j.foodchem.2012.10.089.
[12] ALMEIDA J S, ANUNCIAÇÃO T A, BRANDÃO G C, et al.Ultrasound-assisted single-drop microextraction for the determination of cadmium in vegetable oils using high-resolution continuum source electrothermal atomic absorption spectrometry[J]. Spectrochimica Acta Part B Atomic Spectroscopy, 2015, 107: 159-163. DOI:10.1016/j.sab.2015.03.002.
[13] YAO L, LIU H T, WANG X, et al. Ultrasound-assisted surfactantenhanced emulsification microextraction using a magnetic ionic liquid coupled with micro-solid phase extraction for the determination of cadmium and lead in edible vegetable oils[J]. Food Chemistry, 2018,256: 212-218. DOI:10.1016/j.foodchem.2018.02.132.
[14] BARRETO I S, ANDRADE S, CUNHA F, et al. A robotic magnetic nanoparticle solid phase extraction system coupled to flow-batch analyzer and GFAAS for determination of trace cadmium in edible oils without external pretreatment[J]. Talanta, 2018, 178: 384-391.DOI:10.1016/j.talanta.2017.09.063.
[15] 熊巍林, 包李林, 周青燕, 等. 溶剂稀释植物油直接进样石墨炉原子吸收测定铅含量[J]. 中国油脂, 2017, 42(12): 142-144. DOI:10.3969/j.issn.1003-7969.2017.12.036.
[16] ROBAINA N F, BRUM D M, CASSELLA R J. Application of the extraction induced by emulsion breaking for the determination of chromium and manganese in edible oils by electrothermal atomic absorption spectrometry[J]. Talanta, 2012, 99: 104-112. DOI:10.1016/j.talanta.2012.05.025.
[17] CORAZZA M Z, TARLEY C R T. Development and feasibility of emulsion breaking method for the extraction of cadmium from omega-3 dietary supplements and determination by flow injection TS-FF-AAS[J]. Microchemical Journal, 2016, 127: 145-151.DOI:10.1016/j.microc.2016.02.021.
[18] BAKIRCIOGLU D, TOPRAKSEVER N, KURTULUS Y B.Determination of zinc in edible oils by flow injection FAAS after extraction induced by emulsion breaking procedure[J]. Food Chemistry,2014, 151(10): 219-224. DOI:10.1016/j.foodchem.2013.11.069.
[19] BAKIRCIOGLU D, TOPRAKSEVER N, KURTULUS Y B. Separation/preconcentration system based on emulsion-induced breaking procedure for determination of cadmium in edible oil samples by flow injectionflame atomic absorption spectrometry[J]. Food Analytical Methods, 2015,8(9): 2178-2184. DOI:10.1007/s12161-015-0112-z.
[20] 贺杨明, 廖上富, 何乔桑, 等. 破乳诱导萃取-电感耦合等离子体质谱法测定柴油中的锰、铁和铅[J]. 理化检验: 化学分册, 2015, 51(3):286-288.
[21] 贺杨明. 破乳诱导萃取-电感耦合等离子体质谱技术在油品分析中的应用研究[D]. 杭州: 浙江工业大学, 2015: 2-13.
[22] 聂西度, 符靓. 食用菌油中多元素的质谱分析[J]. 食品科学, 2016,37(24): 175-179. DOI:10.7506/spkx1002-6630-201624027.
[23] 张萍, 谢华林, 刘宏伟, 等. ORS-ICP-MS测定食用植物油中的多种微量元素[J]. 中国粮油学报, 2014, 29(7): 108-111.
[24] SAVIO M, ORTIZ M S, ALMEIDA C A, et al. Multielemental analysis in vegetable edible oils by inductively coupled plasma mass spectrometry after solubilisation with tetramethylammonium hydroxide[J]. Food Chemistry, 2014, 159: 433-438. DOI:10.1016/j.foodchem.2014.03.041.
[25] HE Y M, CHEN J J, ZHOU Y, et al. Extraction induced by emulsion breaking for trace multi-element determination in edible vegetable oils by ICP-MS[J]. Analytical Methods, 2014, 6(14): 5105-5111.DOI:10.1039/C4AY00218K.
[26] CASSELLA R J, DANIEL M B, NICOLLE F R, et al. Extraction induced by emulsion breaking: a model study on metal extraction from mineral oil[J]. Fuel, 2018, 215: 592-600. DOI:10.1016/j.fuel.2017.11.102.
[27] CASSELLA R J, DANIEL M B, PAULA C E R D, et al. Extraction induced by emulsion breaking: a novel strategy for the trace metals determination in diesel oil samples by electrothermal atomic absorption spectrometry[J]. Journal of Analytical Atomic Spectrometry, 2010,25(11): 1704-1711. DOI:10.1039/C0JA00035C.
[28] WUYKE H, OROPEZA T, FEO L. Extraction induced by emulsion breaking for the determination of As, Co, Cr, Mn, Mo and Pb in heavy and extra-heavy crude oil samples by ICP-MS[J]. Analytical Methods,2017, 9: 1152-1160. DOI:10.1039/C6AY03130G.
[29] AHMAD A L, KUSUMASTUTI A, DEREK C J C, et al. Emulsion liquid membrane for heavy metal removal: an overview on emulsion stabilization and destabilization[J]. Chemical Engineering Journal, 2011,171(3): 870-882. DOI:10.1016/j.cej.2011.05.102.
Determination of Cadmium in Edible Oils by ICP-MS after Extraction Induced by Emulsion Breaking