近年来,我国猪肉产量以平均每年5.8%的速率迅速增长,成为猪肉生产大国[1]。猪肉含有丰富的营养物质,包括蛋白质、脂肪及钙、铁、磷、锌等必需微量元素和维生素,是人类的主要营养来源之一;但因其营养组成丰富极易滋生腐败微生物,因此贮藏期较短。肉制品加工行业常采用传统的冷冻方式保存肉品,以确保肉制品的安全和品质[2-3]。冷冻肉品在进一步加工或销售之前必须进行解冻[4]。冷冻肉制品的品质变化不仅与冻藏速率、冻藏温度有关,还与解冻方法、解冻速率有关[5]。
在解冻过程中,由于环境条件和处理方式的差异,肉制品易出现物理、化学及感官品质的下降,如汁液流失、蛋白变性、脂肪氧化、气味恶化等[6-7]。目前,解冻方式多样化,包括传统的空气、冷/热水、低温(4 ℃冰箱)解冻等[8-9],还包括一些新型解冻方式如微波、超声波、超高压和欧姆解冻[10-12]。传统解冻方式耗时长、效率低下,且易导致产品品质恶化[13];新型技术虽然能提高解冻效率,但仍有一定的局限性[14]。因此选择合适的解冻方式来最大限度地保留“鲜肉”的品质至关重要。
近年来,低温解冻由于其较低的温度处理可有效减少微生物污染、降低品质损失及成本低廉而广泛用于肉制品加工企业。Xia Xiufang等[9]的研究结果也表明与室温、静水、流水和微波解冻相比,低温(冰箱)解冻能最大限度维持冻肉的品质特性,但其解冻时间过长、解冻效率较低,导致蛋白、脂肪氧化严重,肉品发生劣变。张春晖[15]、Li Yin[16]等分别研究了低温高湿变温解冻对羊肉、牛肉品质的影响,结果表明高湿低变温解冻(相对湿度(relative humidity,RH)97%,2 ℃→6 ℃→2 ℃)处理后,羊肉和牛肉品质能够最大限度地得到保持。张昕等[17]筛选得到4 ℃、RH 90%环境下解冻处理后,鸡胸肉品质最佳。以上研究均表明低温高湿解冻有利于维持肉制品的品质。然而目前国内外对于低温高湿解冻对猪肉理化、蛋白变性及流变特性研究较少,尤其是关于在低变温条件(2 ℃→6 ℃→2 ℃)下,对猪肉解冻时最适湿度的筛选研究鲜有提及。因此,本实验以鲜肉和传统低温(4 ℃、RH 65%~73%)解冻作为对照,筛选低变温条件(2 ℃→6 ℃→2 ℃)下,猪肉解冻的最适相对湿度参数,分析其对冷冻猪肉保水性、食用品质、蛋白变性及流变特性的影响,以期改善解冻后猪肉品质,为新型解冻技术的应用提供理论依据,从而为企业提供科学的技术支持。
经常规屠宰和成熟后的猪背最长肌购自河南新乡高金食品有限公司。
牛血清白蛋白 美国Sigma-Aldrich公司;NA培养基 青岛海博生物技术有限公司;2-硫代巴比妥酸、三氯乙酸、氯仿 国药集团化学试剂有限公司。
CTHI-150B恒温恒湿箱 上海施都凯仪器设备有限公司;BCD-368WPC冰箱 合肥美菱(股份)有限公司;YXQ-LS-50S全自动立式压力蒸汽灭菌锅上海博讯医疗设备有限公司;T25高速匀浆器 德国IKA公司;CR-400色差计 日本美能达公司;L93-3温度自动记录仪 杭州路格科技有限公司;testo 106插入式温度计 德国德图公司;低温离心机 中科中佳(安徽)科学仪器有限公司;pH计 上海精密科学仪器有限公司;电导率仪 梅特勒-托利多(上海)仪器有限公司;C-LM4型数显式肌肉嫩度仪 东北农业大学工程学院;差示扫描量热(differential scanning calorimeter,DSC)仪 德国耐驰公司;MCR301流变仪 奥地利Anton Paar公司。
1.3.1 原料处理
在无菌环境中,剔除表面脂肪和结缔组织后,将原料肉分割成规则的肉块(质量为(15.0±0.5)g,尺寸为6 cm×5 cm×3.5 cm),用自封袋(120 mm×170 mm)进行分装后,随机分成6 组,每组3 份。一组作为对照1(鲜肉),直接测定肉样的各项指标。其余5 组于-18 ℃冻藏72 h备用:其中一组作为传统低温组(对照2),放置于4 ℃冰箱(RH 65%~73%)中解冻,另外4 组为低变温解冻组,放置于恒温恒湿箱中采用低变温(2 ℃、3 h→6 ℃、3 h→2 ℃)不同相对湿度(80%、85%、90%、95%)进行解冻(温湿度直接通过仪器按钮控制),直至肉块中心温度达到2 ℃,表明解冻结束。
1.3.2 解冻时间的测定
解冻时间参照Choi等[14]的方法测定,并略作修改。解冻开始之前,用钉子在冷冻肉样品的侧面取一孔道,方便温度计插入样品的中心位置。在解冻过程中,利用数字温度自动记录仪记录解冻过程中样品中心温度的变化情况。
1.3.3 保水性的测定
解冻猪肉的保水性主要是通过汁液损失率、离心损失率、滴水损失率、蒸煮损失率及总损失率来衡量。
1.3.3.1 汁液损失率
参考Utrera等[18]的方法,在解冻前、后分别测定除去表面水分后样品的质量,分别记为m0/g、mt/g,通过公式(1)计算汁液损失率。
1.3.3.2 离心损失率
参考何向丽[19]的方法进行测定,取(10.0±0.5)g的鲜肉或解冻肉样,分别记录离心前、后除去表面水分的肉样质量m0/g、m1/g,并通过公式(2)计算离心损失率。
1.3.3.3 滴水损失率
参照邹华锋等[20]的方法进行测定,取(10.0±0.5)g的鲜肉或解冻肉样,分别记录悬挂前和4 ℃环境下悬挂24 h后除去表面水分的肉样质量m0/g、mt/g,通过公式(3)计算滴水损失率。
1.3.3.4 蒸煮损失率
参照常海军等[21]的方法进行测定,取(10.0±0.5)g的鲜肉或解冻肉样,分别记录蒸煮前、后除去表面水分的肉样质量m0/g、mt/g,通过公式(4)计算蒸煮损失率。
1.3.3.5 总损失率
解冻过程中的总损失率为汁液损失率、离心损失率、滴水损失率和蒸煮损失率之和。
1.3.4 色泽的测定
参考Chang Haijun等[22]的方法测定色泽。使用色差计对每个样品的5 个位点进行检测,并加以标记,尽量使得样品之间测定位点一致,减小误差。取5 个位点的平均值,记录该肉样的亮度值L*、红绿值a*、黄蓝值b*。测定前对色差计进行校准。总色差值(△E)通过公式(5)进行计算。
式中:L0*、a0*、b0*值分别为鲜样的颜色值;L*、a*、b*值为该样品经过冻结解冻后的颜色值。
1.3.5 硫代巴比妥酸反应物值的测定
参考何向丽[19]的方法,利用硫代巴比妥酸法测定硫代巴比妥酸反应物(thiobarbituric acid reactive substances,TBARS)值。
1.3.6 剪切力的测定
将待测肉样(3 cm×3 cm×2 cm)放入小自封袋内置于85 ℃水浴锅中加热,样品中心温度达70 ℃时取出,置于室温自然冷却,用肌肉嫩度仪沿着肌纤维垂直方向剪切肉样,记录剪切力。
1.3.7 新鲜度的测定
新鲜度常用的判定指标包括pH值、挥发性盐基氮(total volatile basic nitrogen,TVB-N)含量和细菌菌落总数。pH值:参考GB 5009.237—2016《食品安全国家标准 食品pH值的测定》[23]利用pH计测定;菌落总数:参考GB 4789.2—2016《食品安全国家标准 食品微生物学检验 菌落总数测定》[24]测定;TVB-N含量:参考GB 5009.228—2016《食品安全国家标准 食品中挥发性盐基氮的测定》[25]测定。
1.3.8 蛋白溶解度的测定
参考Joo等[26]的方法提取总可溶解蛋白和肌浆蛋白。采用双缩脲试剂测定蛋白含量[27],即溶解度。按公式(6)计算肌纤维蛋白溶解度。
1.3.9 DSC分析
DSC分析参考Thorarinsdottir等[28]的方法,并略作修改。准确称取15~20 mg鲜肉样或解冻肉样,放入样品盘中,以5 ℃/min速率升温,分析温度范围25~100 ℃,以空样品盘(即不加肉样)作为对照。通过变性峰的面积计算热焓值ΔH/(J/g),并得到相关蛋白的变性温度Tm/℃。
1.3.10 动态流变特性的测定
参考朱东阳等[29]的方法,并略作修改。将鲜肉或解冻肉样打碎后,均匀涂抹在两个50 mm不锈钢圆形平板探头之间,间隙为0.5 mm。起始温度设置为20 ℃,保温10 min后以2 ℃/min的升温速率上升至80 ℃。同时,在频率固定为0.1 Hz下对样品进行连续剪切,测定储能模量(G’)随温度的变化情况。
每个处理组测定3 次,使用SPSS 18.0软件进行方差分析,方差显著性分析用Duncan multiple-range test进行多重比较(P<0.05),采用Origin 8.0软件作图。

图1 低变温不同相对湿度条件下冷冻肉样中心温度的变化曲线
Fig. 1 Changes in internal temperature of frozen pork samples during thawing at variable low temperatures and different relative humidities
如图1所示,解冻温度在通过最大冰晶形成区域(-5~-1 ℃)所需时间占了所有耗时的较大部分,这与食品冻结过程[19]一致。与传统低温解冻(耗时17 h)相比,低变温解冻组耗时明显缩短,在8.5~10.5 h范围内完成解冻过程,表明低变温解冻明显提高了解冻速率。在低变温条件下,随着解冻环境相对湿度的增加,解冻时间缩短,解冻效率提高,其中RH 90%、RH 95%组解冻效率明显高于RH 80%、RH 85%两组。
表1 不同相对湿度解冻对猪肉保水性的影响
Table 1 Effect of thawing at different relative humidities on water-holding capacity of pork
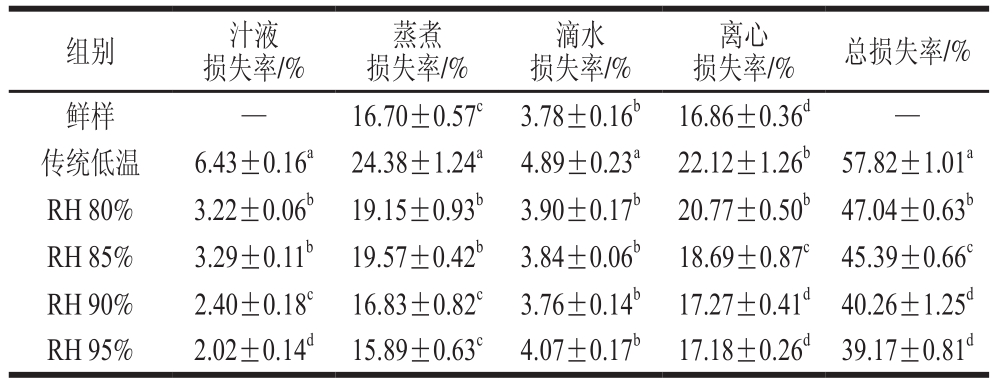
注:—.未检测;同列肩标小写字母不同表示差异显著(P<0.05)。下同。
组别 汁液损失率/%蒸煮损失率/%滴水损失率/%离心损失率/% 总损失率/%鲜样 — 16.70±0.57c 3.78±0.16b 16.86±0.36d —传统低温 6.43±0.16a 24.38±1.24a 4.89±0.23a 22.12±1.26b 57.82±1.01a RH 80% 3.22±0.06b 19.15±0.93b 3.90±0.17b 20.77±0.50b 47.04±0.63b RH 85% 3.29±0.11b 19.57±0.42b 3.84±0.06b 18.69±0.87c 45.39±0.66c RH 90% 2.40±0.18c 16.83±0.82c 3.76±0.14b 17.27±0.41d 40.26±1.25d RH 95% 2.02±0.14d 15.89±0.63c 4.07±0.17b 17.18±0.26d 39.17±0.81d
如表1所示,低变温解冻后样品的汁液损失率显著低于传统低温解冻组(P<0.05),可能是传统低温解冻时间过长导致水分流失严重[21]。而低变温环境下,相对湿度的变化显著影响解冻肉样汁液流失,随着相对湿度的增加,汁液损失率显著降低(P<0.05),可能是高湿度条件可有效保护样品蛋白水合面,降低表面水分蒸发,减少干耗[15]。同样地,与传统低温解冻相比,低变温高湿解冻后的肉样蒸煮损失率、滴水损失率和离心损失率均显著降低(P<0.05)。其中相对湿度达到90%时,蒸煮损失率和离心损失率分别为16.83%和17.27%,显著低于传统低温组和RH 80%、RH 85%处理组(P<0.05),与鲜肉无显著性差异(P>0.05)。相对湿度大于90%后,随着相对湿度的继续升高,蒸煮损失率和离心损失率无显著性变化(P>0.05)。不同相对湿度下解冻后肉样的滴水损失率无显著差异(P>0.05),与鲜肉接近。关于冷冻-解冻后肉样保水性下降的原因主要有以下3 种解释:1)经解冻处理后,蛋白质会发生氧化变性,生成羰基和二硫键,导致肌肉蛋白结构发生改变,降低保水能力[30];2)经解冻处理后,肉样的肌纤维收缩,肌束空隙变大,破坏了肌肉的致密结构,从而导致保水性降低[31];3)肉样在冻结过程中,冰晶的形成易对肉组织造成机械损伤,也会引起保水性变差[15]。总的来说,低变温条件下,RH 90%、RH 95%条件解冻后肉样的总损失率最低,分别为40.26%、39.17%,表明其对猪肉保水性影响最小。
表2 不同相对湿度解冻对猪肉色泽的影响
Table 2 Effect of thawing at different relative humidities on color of pork
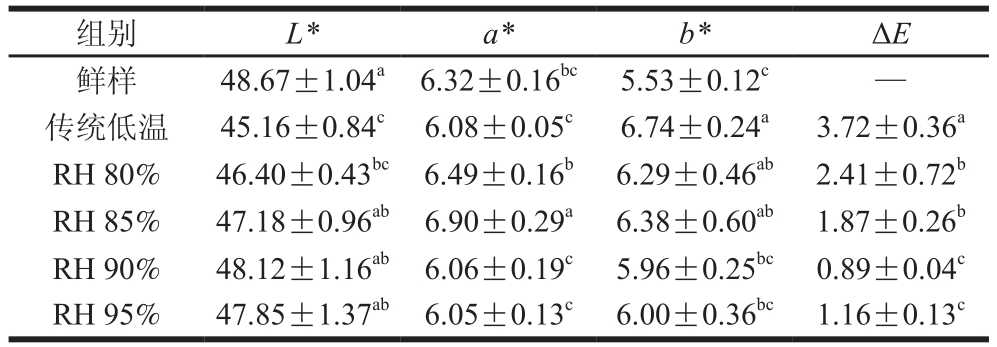
组别 L* a* b* ΔE鲜样 48.67±1.04a 6.32±0.16bc 5.53±0.12c —传统低温 45.16±0.84c 6.08±0.05c 6.74±0.24a 3.72±0.36a RH 80% 46.40±0.43bc 6.49±0.16b 6.29±0.46ab 2.41±0.72b RH 85% 47.18±0.96ab 6.90±0.29a 6.38±0.60ab 1.87±0.26b RH 90% 48.12±1.16ab 6.06±0.19c 5.96±0.25bc 0.89±0.04c RH 95% 47.85±1.37ab 6.05±0.13c 6.00±0.36bc 1.16±0.13c
猪肉色泽的改变直接影响消费者的购买欲望,影响猪肉制品的销量。由表2可知,与鲜肉相比,解冻后猪肉的色泽均发生不同程度的变化。经传统低温解冻后,猪肉的L*值显著下降,b*值显著升高(P<0.05),表明猪肉色泽劣变严重;而经高湿低变温解冻处理,猪肉色泽变化程度虽不同,但△E值相较于传统低温解冻显著降低(P<0.05),表明高湿低变温解冻可有效缓解猪肉色泽的劣变,与张昕等[17]的实验结果相符,原因可能是高湿环境下,解冻时间缩短,猪肉保水性增强,从而维持猪肉光泽[8];同时高湿环境抑制了解冻过程中猪肉蛋白和脂肪的氧化[32]。随着相对湿度增加(RH 80%~90%),L*值逐渐升高,b*、△E值逐渐降低,相对湿度为90%时,猪肉色泽最接近鲜肉,此时L*、b*、△E值分别为48.12、5.96、0.89;随着相对湿度的进一步增加,猪肉色泽无较大变化。因此,低变温环境下,相对湿度达到90%以上可有效保持猪肉色泽。
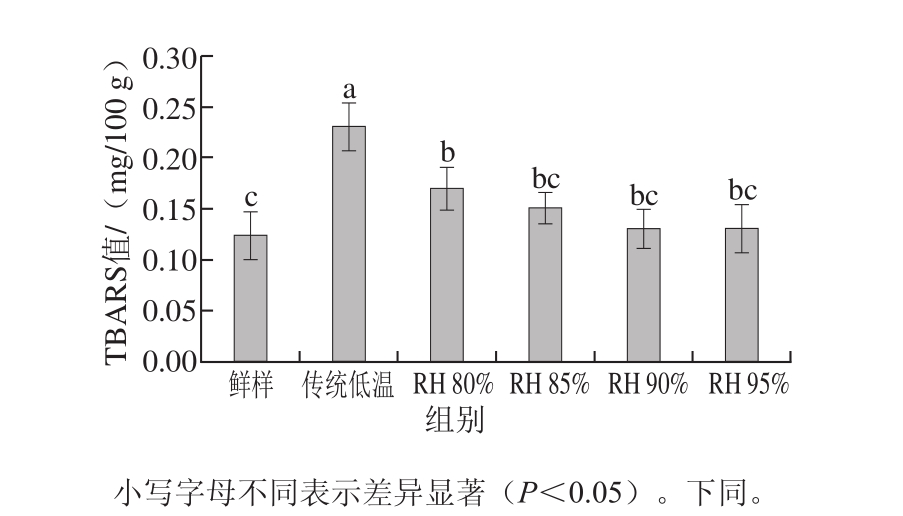
图2 低变温不同相对湿度解冻对猪肉TBARS值的影响
Fig. 2 Effect of thawing at different relative humidities on TBARS value of pork
TBARS值能够反映猪肉的脂肪氧化程度。如图2所示,高湿低变温解冻后猪肉的TBARS值显著低于传统低温解冻组(P<0.05)。在低变温环境中,相对湿度为85%~95%时,猪肉的TBARS值与鲜肉无显著性差异(P>0.05),表明高湿度环境可有效抑制脂肪的氧化变性。
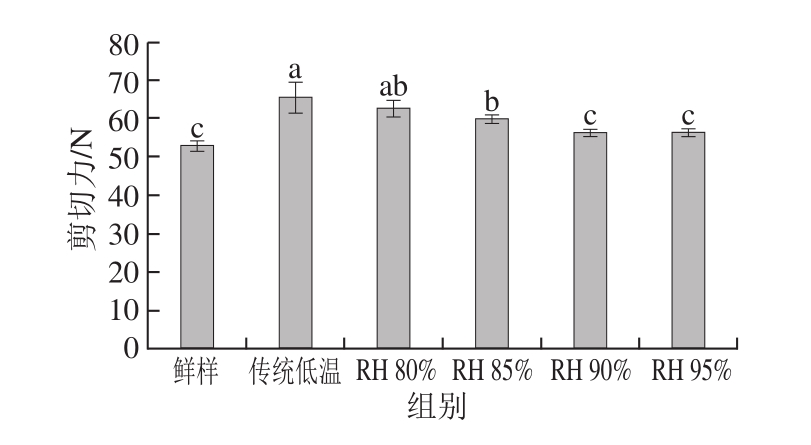
图3 低变温不同相对湿度解冻对猪肉剪切力的影响
Fig. 3 Effect of thawing at different relative humidities on shear force of pork
嫩度是衡量猪肉品质的重要指标之一,剪切力越大表明嫩度越差[15]。如图3所示,与鲜肉相比,经传统低温解冻后肉样的剪切力显著升高(P<0.05),这可能是由于猪肉在冷冻过程中,温度的降低和冻结时间的延长都会增大样品中产生的冰晶,减小了样品的可塑性;同时解冻时间过长,导致汁液损失严重[31]。低变温高湿解冻后猪肉的剪切力显著低于传统低温处理(P<0.05),且随着相对湿度升高,剪切力逐渐降低;达到RH 90%后剪切力变化不大,与鲜肉接近(P>0.05),可能是由于高湿环境有利于减少汁液损失,从而维持猪肉的嫩度。
如图4A所示,与鲜肉及传统低温解冻组相比,低变温高湿度下解冻后肉样的pH值没有显著性变化(P>0.05),均在5.80~6.10之间,此范围内系水力最好,属于一级鲜肉[33]。
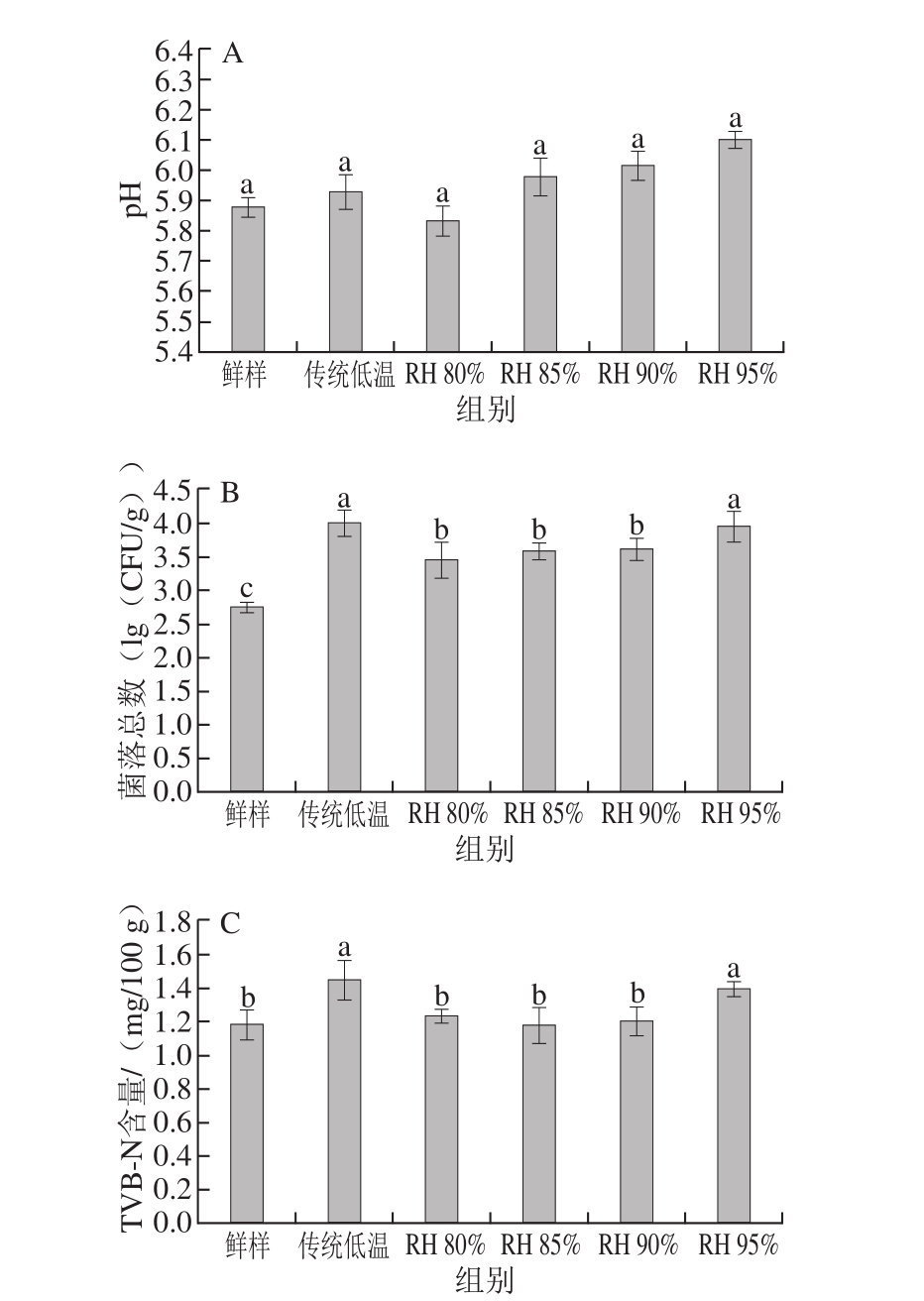
图4 低变温不同相对湿度解冻对猪肉pH值(A)、菌落总数(B)和TVB-N含量(C)的影响
Fig. 4 Effect of thawing at different relative humidities on pH (A),total bacterial count (B) and TVB-N content (C) of pork
在冷冻肉解冻过程中,解冻温度的升高、解冻时间的延长均容易造成微生物污染,促使猪肉成分和感官特性发生变化,产生有毒有害物质。如图4B所示,在低变温条件下,相对湿度达95%时,菌落总数(3.97(lg(CFU/g)))显著高于其他3 组,接近传统低温解冻组;可能是因为随着解冻环境相对湿度增加,微生物活动增强,但RH 95%解冻组菌落总数仍在一级鲜肉范围之内,可安心使用[22]。
由图4C可知,低变温条件下,RH 80%、RH 85%、RH 90%处理组的TVB-N含量与鲜肉相比没有显著差异(P>0.05),但显著低于RH 95%处理组(1.40 mg/100 g)和传统低温对照组(1.45 mg/100 g)(P<0.05)。TVB-N是指动物性食品因酶和细菌的作用使蛋白质分解而产生氨、伯胺、仲胺及叔胺等碱性含氮物质[31]。其中腐败菌的滋生是诱发TVB-N含量增加的主要因素[17]。TVB-N含量增加也预示着腐败程度增加,肌肉组织发黏,严重时会散发不愉悦的异味。
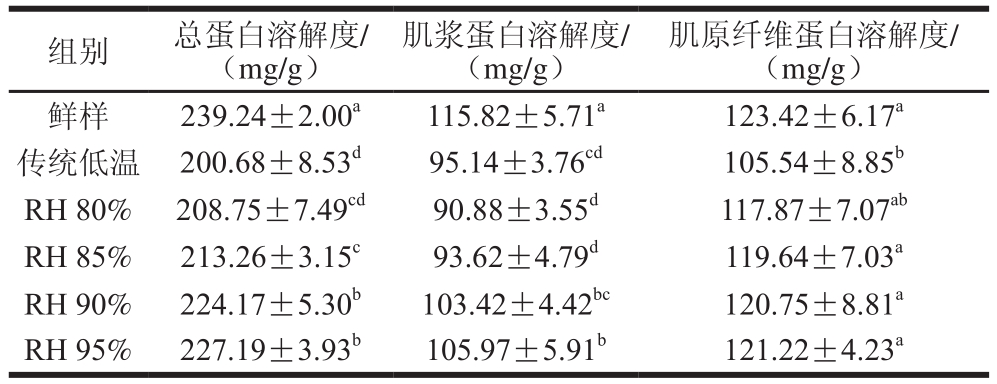
蛋白溶解度是评价蛋白变性程度的常用指标之一,只有蛋白质处于高度溶解状态才可表现出肌肉蛋白的功能特性[15]。如表3所示,与鲜肉相比,经不同解冻处理后,样品的总蛋白溶解度和肌浆蛋白溶解度均显著下降(P<0.05),分析原因是冻结-解冻过程能促进猪肉的肌纤维收缩,提高蛋白质去折叠及变性的程度,因而降低蛋白溶解度,具体表现为蛋白可提取性的降低[34];而经高湿低变温解冻后肌原纤维蛋白溶解度与鲜肉无显著性差异(P>0.05)。在低变温条件下,随着相对湿度的增加,蛋白溶解度逐步增加;相对湿度为90%时,猪肉总蛋白、肌浆蛋白及肌原纤维蛋白溶解度均达到最大;随着相对湿度继续增加,其蛋白溶解度差异不显著(P>0.05)。
表3 低变温不同相对湿度解冻对猪肉蛋白溶解度的影响
Table 3 Effect of thawing at different relative humidities on protein solubility of pork
肌原纤维蛋白溶解度/(mg/g)鲜样 239.24±2.00a 115.82±5.71a 123.42±6.17a传统低温 200.68±8.53d 95.14±3.76cd 105.54±8.85b RH 80% 208.75±7.49cd 90.88±3.55d 117.87±7.07ab RH 85% 213.26±3.15c 93.62±4.79d 119.64±7.03a RH 90% 224.17±5.30b 103.42±4.42bc 120.75±8.81a RH 95% 227.19±3.93b 105.97±5.91b 121.22±4.23a组别 总蛋白溶解度/(mg/g)肌浆蛋白溶解度/(mg/g)
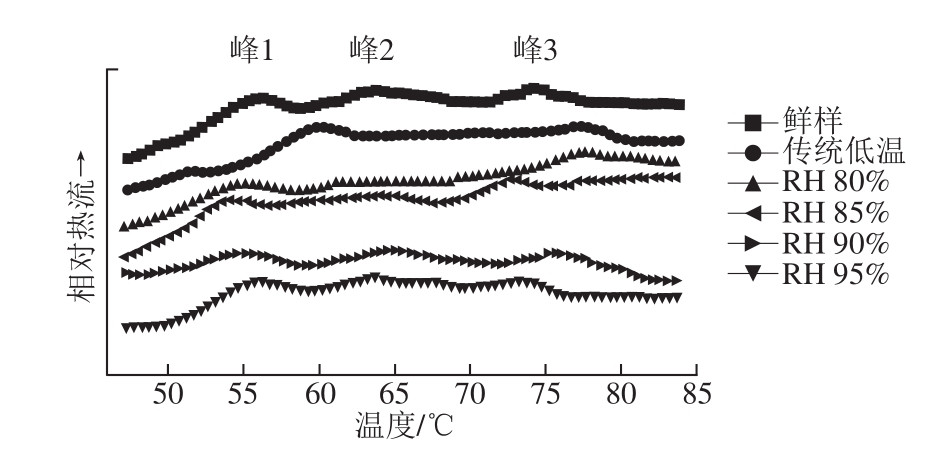
图5 低变温不同相对湿度解冻对猪肉肌肉蛋白热稳定性影响的DSC分析
Fig. 5 DSC thermograms showing the effect of thawing at different relative humidities on thermal stability of pork samples
由图5可知,鲜肉的DSC热分析图谱有3 个峰,代表了蛋白分子的展开和加热期蛋白由原始构象转变到变性构象的过程[22]。其中峰1在55 ℃左右,代表肌球蛋白头部的变性;峰2在65 ℃左右,代表肌球蛋白尾部和肌浆蛋白变性;峰3在75 ℃左右,表示肌动蛋白变性[28]。传统低温解冻和低变温RH 80%解冻后,峰2消失,表明传统低温和低变温RH 80%解冻可导致肌浆蛋白和肌球蛋白尾部严重的变性。
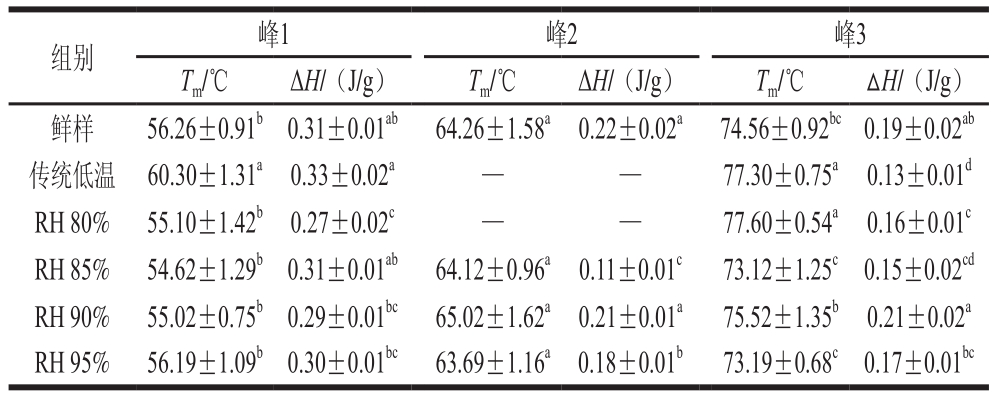
表4为DSC分析法所得到的变性温度Tm和热焓ΔH,与鲜肉相比,经传统低温解冻后样品峰1的变性温度(60.30 ℃)显著升高,传统低温和低变温RH 80%解冻后样品峰3的Tm显著升高,ΔH显著降低(P<0.05),表明传统低温和低变温RH 80%解冻也导致肌动蛋白的变性;与鲜肉相比,经低变温RH 90%解冻后3 个峰的Tm均无显著差异,且ΔH最接近鲜肉水平,表明低变温RH 90%的解冻处理对蛋白变性程度影响最小。
表4 不同解冻处理后猪肉肌肉蛋白的变性温度Tm和变性热焓ΔH
Table 4 Denaturation temperature Tm and enthalpy ΔH of proteins in pork samples treated by different thawing methods
组别 峰1 峰2 峰3 Tm/℃ ΔH/(J/g) Tm/℃ ΔH/(J/g) Tm/℃ △H/(J/g)鲜样 56.26±0.91b 0.31±0.01ab 64.26±1.58a 0.22±0.02a 74.56±0.92bc0.19±0.02ab传统低温 60.30±1.31a 0.33±0.02a — — 77.30±0.75a 0.13±0.01d RH 80% 55.10±1.42b 0.27±0.02c — — 77.60±0.54a 0.16±0.01c RH 85% 54.62±1.29b0.31±0.01ab 64.12±0.96a 0.11±0.01c 73.12±1.25c0.15±0.02cd RH 90% 55.02±0.75b0.29±0.01bc 65.02±1.62a 0.21±0.01a 75.52±1.35b 0.21±0.02a RH 95% 56.19±1.09b0.30±0.01bc 63.69±1.16a 0.18±0.01b 73.19±0.68c0.17±0.01bc

图6 不同相对湿度解冻对肉样品储能模量(G’)的影响
Fig. 6 Effect of thawing at different relative humidities on dynamic storage modulus (G’) of pork
低变温不同相对湿度下解冻后猪肉样品的G’随温度(20~80 ℃)的变化曲线如图6所示。鲜肉打碎后的G’大体呈现4 个阶段:20~44 ℃时,G′缓慢下降;45~51 ℃时,G’因猪肉蛋白相互作用增强而增加[35];随着温度的继续升高,猪肉中肌球蛋白尾部发生变性,结构遭到破坏,导致G’在52~56 ℃间略微下降;随后G’迅速升高,主要是温度升高引发蛋白质聚集、交联,黏性胶体转变为有弹性的凝胶网络结构所致[36]。经不同解冻处理后,G’均有所下降,其中经传统低温和低变温RH 80%解冻处理后,肉样的G’最低,80 ℃时分别为22 452 Pa和23 516 Pa,且在45~56 ℃之间G’变化不明显,峰形较弱;而经低变温RH 90%、RH 95%解冻处理后,样品的G’明显高于其他两组和对照组2,80 ℃时分别为26 143 Pa和26 239 Pa,且G’变化趋势与鲜肉最为接近。Ali等[37]研究指出,解冻过程破坏样品凝胶结构主要是解冻过程中蛋白质发生变性而导致蛋白聚集和结构改变所造成的。另外,样品的G’越高,表明凝胶结构越好[29]。所以,低变温RH 90%、RH 95%解冻对猪肉流变特性影响最小,能较好地保持猪肉糜原有的结构特性。
与传统低温解冻相比,低变温(2 ℃→6 ℃→2 ℃)高湿度(RH 80%~95%)解冻所耗时间短,能有效提高解冻效率,且有利于保持解冻猪肉的品质。RH 90%、RH 95%解冻明显优于RH 80%、RH 85%两组,能够较快地完成解冻,减少汁液损失,降低解冻过程对猪肉保水性的影响,有效改善解冻后猪肉的色泽、嫩度,降低脂肪氧化程度,提高蛋白溶解度;RH 90%解冻后猪肉蛋白变性程度较低,且热焓值与鲜肉水平接近;RH 90%、RH 95%解冻处理能较好地维持G’(80 ℃时分别为26 143 Pa和26 239 Pa);但RH 95%解冻后猪肉的菌落总数((3.97(lg(CFU/g)))和TVB-N含量(1.40 mg/100 g)较RH 90%解冻处理后显著升高,不能有效防止微生物污染。另外,环境所需湿度越大,能耗就越高。综合分析,2 ℃→6 ℃→2 ℃低变温RH 90%解冻是最佳的解冻条件,该条件可有效提高解冻效率,维持猪肉品质。本研究可积极推动解决冷冻肉品解冻后品质不佳、出品率低等问题,提高企业经济效益。
[1] ZHOU G H, ZHANG W G, XU X L. China’s meat industry revolution:challenges and opportunities for the future[J]. Meat Science, 2012,92(3): 188-196. DOI:10.1016/j.meatsci.2012.04.016.
[2] 章杰, 彭新书, 马丹, 等. 不同解冻方式对猪肉营养价值的影响[J].食品与发酵工业, 2017, 43(6): 203-207. DOI:10.13995/j.cnki.11-1802/ts.201706034.
[3] LEYGONIE C, BRRITZ T J, HOFFMAN L C. Impact of freezing and thawing on the quality of meat: review[J]. Meat Science, 2012, 91(2):93-98. DOI:10.1016/j.meatsci.2012.01.013.
[4] TAHER B J, FARID M M. Cyclic microwave thawing of frozen meat:experimental and theoretical investigation[J]. Chemical Engineering and Processing, 2001, 40(4): 379-389. DOI:10.1016/S0255-2701(01)00118-0.
[5] EASTRIDGE J S, BOWKER B C. Effect of rapid thawing on the meat quality attributes of USDA select beef strip loin steaks[J].Journal of Food Science, 2011, 76(2): 156-162. DOI:10.1111/j.1750-3841.2010.02037.x.
[6] UYAR R, BEDANE T F, ERDOGDU F, et al. Radio-frequency thawing of food products: a computational study[J]. Journal of Food Engineering, 2015, 146: 163-171. DOI:10.1016/j.jfoodeng.2014.08.018.
[7] LEYGONIE C, BRITZ T J, HOFFMAN L C. Meat quality comparison between fresh and frozen/thawed ostrich M. iliofibularis[J]. Meat Science, 2012, 91(3): 364-368. DOI:10.1016/j.meatsci.2012.02.020.
[8] CHANDIRASEKARAN V, THULASI G. Effect of different thawing methods on physico-chemical characteristics of frozen buffalo meat[J].Journal of Food Technology, 2010, 8(6): 239-242. DOI:10.3923/jftech.2010.239.242.
[9] XIA Xiufang, KONG Baohua, LIU Jing, et al. Influence of different thawing methods on physicochemical changes and protein oxidation of porcine longissimus muscle[J]. LWT-Food Science and Technology,2012, 46(1): 280-286. DOI:10.1016/j.lwt.2011.09.018.
[10] ZHANG X, GAO T, SONG L, et al. Effects of different thawing methods on the quality of chicken breast[J]. International Journal of Food Science and Technology, 2017, 52(9): 2097-2105. DOI:10.1111/ijfs.13488.
[11] MANIOS S G, SKANDAMIS P N. Effect of frozen storage,different thawing methods and cooking processes on the survival of Salmonella spp. and Escherichia coli O157:H7 in commercially shaped beef patties[J]. Meat Science, 2015, 101: 25-32. DOI:10.1016/j.meatsci.2014.10.031.
[12] ICIER F, IZZETOGLU G T, BOZKURT H, et al. Effects of ohmic thawing on histological and textural properties of beef cuts[J].Journal of Food Engineering, 2010, 99(3): 360-365. DOI:10.1016/j.jfoodeng.2010.03.018.
[13] CHAKANYA C, ARNAUD E, MUCHENJE V, et al. Colour and oxidative stability of mince produced from fresh and frozen/thawed fallow deer (Dama dama) meat[J]. Meat Science, 2017, 126: 63-72.DOI:10.1016/j.meatsci.2016.12.008.
[14] CHOI E J, PARK H W, CHUNG Y B, et al. Effect of tempering methods on quality changes of pork loin frozen by cryogenic immersion[J]. Meat Science, 2017, 124: 69-76. DOI:10.1016/j.meatsci.2016.11.003.
[15] 张春晖, 李侠, 李银, 等. 低温高湿变温解冻提高羊肉的品质[J]. 农业工程学报, 2013, 29(6): 267-273. DOI:10.3969/j.issn.1002-6819.2013.06.033.
[16] LI Yin, JIA Wei, ZHANG Chunhui, et al. Fluctuated low temperature combined with high-humidity thawing to reduce physicochemical quality deterioration of beef[J]. Food and Bioprocess Technology,2014, 7(12): 3370-3380. DOI:10.1007/s11947-014-1337-3.
[17] 张昕, 高天, 宋蕾, 等. 低温解冻相对湿度对鸡胸肉品质的影响[J].食品科学, 2016, 37(20): 241-246. DOI:10.7506/spkx1002-6630-201620041.
[18] UTRERA M, MORCUENDE D, ESTEVEZ M. Temperature of frozen storage affects the nature and consequences of protein oxidation in beef patties[J]. Meat Science, 2014, 96(3): 1250-1257. DOI:10.1016/j.meatsci.2013.10.032.
[19] 何向丽. 猪里脊肉冻结解冻特性及高压静电场(HVEF)解冻机理研究[D]. 北京: 中国农业大学, 2016: 19-27.
[20] 邹华锋, 文美英, 魏星华, 等. 生猪宰前不同静养时间和屠宰方式对背最长肌肌肉pH值和滴水损失的影响[J]. 肉类工业, 2013(5): 19-21.DOI:10.3969/j.issn.1008-5467.2013.05.007.
[21] 常海军, 唐翠, 唐春红. 不同解冻方式对猪肉品质特性的影响[J]. 食品科学, 2014, 35(10): 1-5. DOI:10.7506/spkx1002-6630-201410001.
[22] CHANG Haijun, XU Xinglian, ZHOU Guanghong, et al. Effects of characteristics changes of collagen on meat physicochemical properties of beef semitendinosus muscle during ultrasonic processing[J]. Food and Bioprocess Technology, 2012, 5(1): 285-297. DOI:10.1007/s11947-009-0269-9.
[23] 国家卫生和计划生育委员会. 食品安全国家标准 食品pH值的测定:GB 5009.237—2016[S]. 北京: 中国标准出版社, 2016: 1-4.
[24] 国家食品药品监督管理总局, 国家卫生和计划生育委员会. 食品安全国家标准 食品微生物学检验 菌落总数测定: GB 4789.2—2016[S]. 北京: 中国标准出版社, 2016: 1-4.
[25] 国家卫生和计划生育委员会. 食品安全国家标准 食品中挥发性盐基氮的测定: GB 5009.228—2016[S]. 北京: 中国标准出版社, 2016: 1-3.
[26] JOO S T, KAUFFMAN R G, KIM B C, et al. The relationship of sarcoplasmic and myofibrillar protein solubility to colour and waterholding capacity in porcine longissimus muscle[J]. Meat Science,1999, 52(3): 291-297. DOI:10.1016/S0309-1740(99)00005-4.
[27] 谢笔钧, 何慧. 食品分析[M]. 北京: 科学出版社, 2009: 183.
[28] THORARINSDOTTIR K A, ARASON S, GEIRSDOTTIR M, et al.Changes in myofibrillar proteins during processing of salted cod(Gadus morhua) as determined by electrophoresis and differential scanning calorimetry[J]. Food Chemistry, 2002, 77(3): 377-385.DOI:10.1016/S0308-8146(01)00349-1.
[29] 朱东阳, 康壮丽, 何鸿举, 等. 猪血浆蛋白乳化棕榈油对猪肉糜凝胶特性的影响[J]. 食品科学, 2018, 39(5): 71-75. DOI:10.7506/spkx1002-6630-201805011.
[30] HUFFLONERGAN E, PARRISH F C, ROBAON R M. Effects of postmortern aging time, animal age, and sex on degradation of titin and nebulin in boving longissimus muscle[J]. Journal of Animal Science,1995, 77(4): 1064-1073. DOI:10.2527/1995.7341064x.
[31] 余力, 贺稚非, ENKHMAA B, 等. 不同解冻方式对伊拉兔肉品质特性的影响[J]. 食品科学, 2015, 36(14): 258-264. DOI:10.7506/spkx1002-6630-201514049.
[32] CHANDHYLASEKARAN V, THULAS G. Effect of different thawing methods on physicochemical characteristics of frozen buffalo meat[J].Journal of Food Technology, 2010, 8(6): 239-242. DOI:10.3923/jftech.2010.239.242.
[33] LLAVE Y, TERADA Y, FUKUOKA M, et al. Dielectric properties of frozen tuna and analysis of defrosting using a radio-frequency system at low frequencies[J]. Journal of Food Engineering, 2014, 139: 1-9.DOI:10.1016/j.jfoodeng.2014.04.012.
[34] 周光宏. 畜产品加工学[M]. 北京: 中国农业出版社, 2004: 69.
[35] 施雪, 夏继华, 卢进峰, 等. 冻结、解冻过程对肌肉品质的影响[J].食品工业, 2012, 33(7): 21-24.
[36] ALI S, ZHANG W G, RAJPUT N, et al. Effect of multiple freezethaw cycles on the quality of chicken breast meat[J]. Food Chemistry,2015, 173(8): 808-814. DOI:10.1016/j.foodchem.2014.09.095.
[37] KANG Z L, LI B, MA H J, et al. Effect of different processing methods and salt content on the physicochemical and rheological properties of meat batters[J]. International Journal of Food Properties,2016, 19(7): 1604-1615. DOI:10.1080/10942912.2015.1105819.
Effect of Variable Low Temperature Combined with High-Humidity Thawing on Physicochemical Characteristics,Thermal Denaturation and Rheological Properties of Pork
朱明明, 彭泽宇, 赵贺开, 等. 低变温高湿解冻对猪肉理化特性、蛋白热变性及流变特性的影响[J]. 食品科学, 2019,40(11): 131-138. DOI:10.7506/spkx1002-6630-20180606-056. http://www.spkx.net.cn
ZHU Mingming, PENG Zeyu, ZHAO Hekai, et al. Effect of variable low temperature combined with high-humidity thawing on physicochemical characteristics, thermal denaturation and rheological properties of pork[J]. Food Science, 2019, 40(11):131-138. (in Chinese with English abstract) DOI:10.7506/spkx1002-6630-20180606-056. http://www.spkx.net.cn