植物多糖降血糖作用及机制研究进展
肖瑞希,陈华国,周 欣*
(贵州师范大学 贵州省山地环境信息系统与生态环境保护重点实验室,贵州省药物质量控制及评价技术工程实验室,天然药物质量控制中心,贵州 贵阳 550001)
摘 要:糖尿病是高血糖的临床表现之一,长期罹患糖尿病易引发各种并发症。目前尚未发现彻底根治糖尿病的方法,主要采用西药治疗;但是西药具有较严重的副作用,因此,有效降血糖、低毒、副作用小的天然物质备受关注。研究发现,广泛分布于自然界的植物多糖具有良好的降血糖功效,是一类天然的生物活性物质,具有低毒、副作用小的特点,其已成为医药界及保健食品领域的研究热点。本文主要概括了近几年国内外研究的降血糖植物多糖的种类及其降血糖机制。
关键词:植物多糖;糖尿病;降血糖作用;作用机制
当机体内的胰岛素分泌相对或绝对不足时,会导致血糖超出正常范围,引发高血糖。糖尿病是高血糖临床表现之一,它是以慢性高血糖为主要特征的一组内分泌代谢性疾病[1],长期的糖尿病易导致眼、肾、心血管等各种部位的并发症[2]。糖尿病有I型糖尿病、II型糖尿病、妊娠糖尿病3 种主要类型[1],其中II型糖尿病占糖尿病病例的90%[3],主要以高血糖引起的胰岛素抵抗和相对胰岛素缺乏为特征。目前尚未发现根治糖尿病的方法,患者需要长期采用西药治疗、控制饮食并适当运动,但是传统西药治疗对机体有一定的毒副作用[4]。因此,找出并利用具有降血糖活性的天然物质已成预防和治疗糖尿病的研究热门。
多糖广泛存在于自然界,是由超过10 个糖苷键连接单糖而成的天然高分子多聚物,参与生物体各项生命活动,是保证生物体生命活动正常运转的物质之一。植物多糖来源广泛,具有毒性低、副作用小的特点。我国植物资源丰富,为植物多糖的研究、利用提供了有利的条件,现已有大量的研究表明植物多糖具有抗肿瘤、降血糖、抗氧化、免疫调节等多种重要生物活性[5],其中对植物多糖降血糖作用的研究已取得巨大的进展,本文主要总结近几年国内外40余种降血糖植物多糖的种类及其降血糖机制。
1 植物多糖降血糖的种类
目前,具有降血糖生物活性的植物多糖已被广泛发现,按其所属门类可分为被子植物门、裸子植物门、红藻门、蓝藻门及绿藻门等,其中包括百合科黄精属、菊科苍木属、五加科有参属等不同科属类的植物(表1)。
表1 具有降血糖活性的植物多糖
Table 1 Plant polysaccharides with hypoglycemic activity
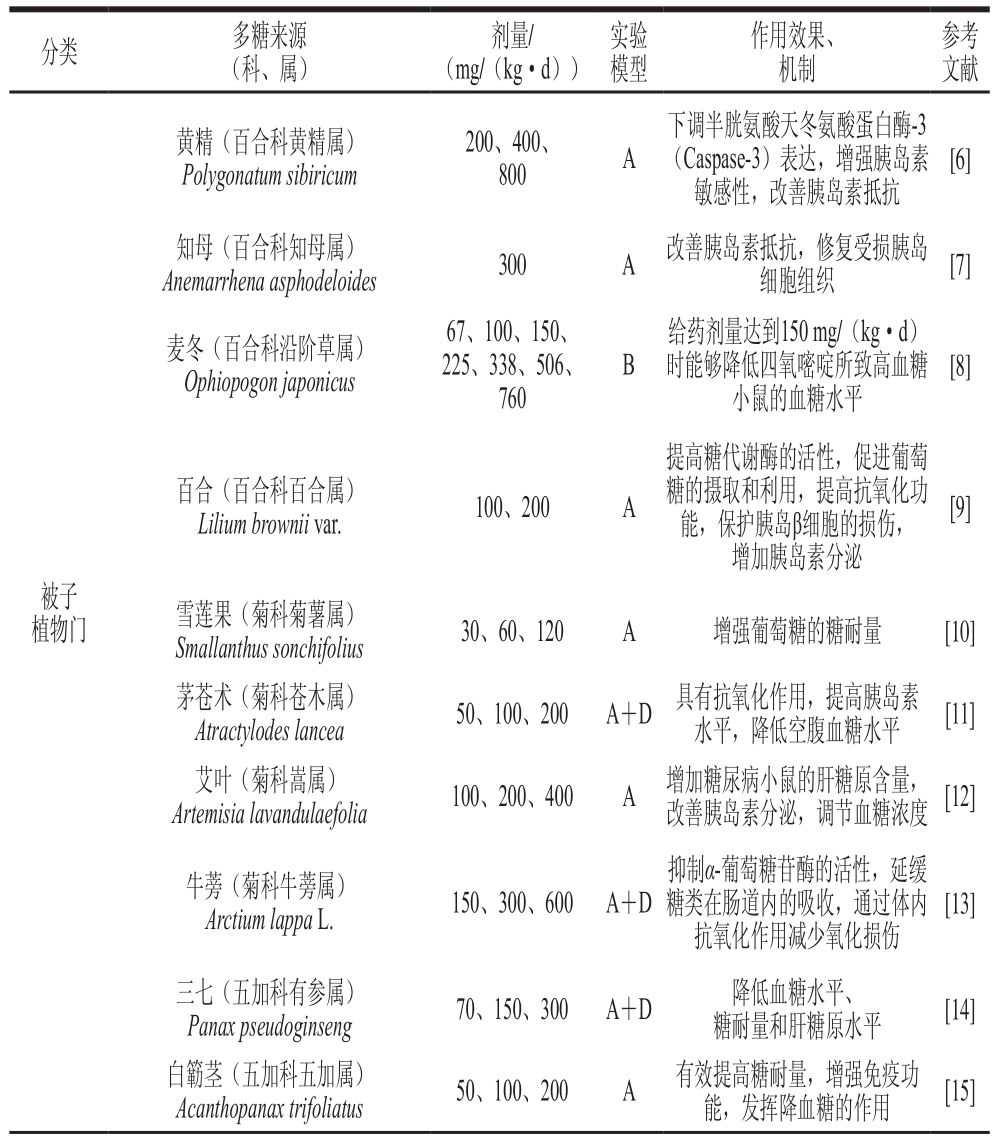
分类 多糖来源(科、属)剂量/(mg/(kg·d))实验模型作用效果、机制参考文献被子植物门黄精(百合科黄精属)Polygonatum sibiricum 200、400、800 A下调半胱氨酸天冬氨酸蛋白酶-3(Caspase-3)表达,增强胰岛素敏感性,改善胰岛素抵抗[6]知母(百合科知母属)Anemarrhena asphodeloides 300 A 改善胰岛素抵抗,修复受损胰岛细胞组织 [7]麦冬(百合科沿阶草属)Ophiopogon japonicus 67、100、150、225、338、506、760 B给药剂量达到150 mg/(kg·d)时能够降低四氧嘧啶所致高血糖小鼠的血糖水平[8]百合(百合科百合属)Lilium brownii var. 100、200 A提高糖代谢酶的活性,促进葡萄糖的摄取和利用,提高抗氧化功能,保护胰岛β细胞的损伤,增加胰岛素分泌[9]雪莲果(菊科菊薯属)Smallanthus sonchifolius 30、60、120 A 增强葡萄糖的糖耐量 [10]茅苍术(菊科苍木属)Atractylodes lancea 50、100、200 A+D 具有抗氧化作用,提高胰岛素水平,降低空腹血糖水平 [11]艾叶(菊科嵩属)Artemisia lavandulaefolia 100、200、400 A 增加糖尿病小鼠的肝糖原含量,改善胰岛素分泌,调节血糖浓度 [12]牛蒡(菊科牛蒡属)Arctium lappa L. 150、300、600 A+D抑制α-葡萄糖苷酶的活性,延缓糖类在肠道内的吸收,通过体内抗氧化作用减少氧化损伤[13]三七(五加科有参属)Panax pseudoginseng 70、150、300 A+D 降低血糖水平、糖耐量和肝糖原水平 [14]白簕茎(五加科五加属)Acanthopanax trifoliatus 50、100、200 A 有效提高糖耐量,增强免疫功能,发挥降血糖的作用 [15]
续表1

楤木(五加科楤木属)Aralia chinensis 100、300、500 A 显著降低糖尿病大鼠血糖水平,有效调节糖尿病大鼠血脂代谢紊乱 [16]黄芪(豆科黄耆属)Astragalus membranaceus 400 A 有效降低血糖水平,改善胰岛素抵抗 [17]刺糖(豆科骆驼刺属)Alhagi-honey 200、400、800 A 改善体内氧化应激作用,降低血糖水平 [18]豆薯(豆科豆薯属)Pachyrhizus erosus 100 A 降低空腹血糖水平,发挥降血糖作用 [19]打瓜干皮(葫芦科西瓜属)Catullus landaus var. 50、100、150 E 抑制α-葡萄糖苷酶活性 [20]南瓜(葫芦科南瓜属)Cucurbita moschata 500 B 提高机体抗氧化能力,改善糖尿病 [21]苦瓜(葫芦科苦瓜属)Momordica charantia L. 100、200、300 A 刺激胰岛素分泌,保护胰岛β细胞 [22]油茶籽(山茶科山茶属)Camellia oleifera Abel. 100 B提高机体抗氧化活性,清除自由基,保护受自由基侵害的胰岛β细胞[23]茶花(山茶科山茶属)Camellia sinensis 75、150、300 B 抑制α-葡萄糖苷酶和α-淀粉酶活性,降低血糖 [24]铁皮石斛(兰科石斛属)Dendrobium officinale 100、200、400 B 上调PI3K/Akt信号,调节糖代谢酶活性,改善糖代谢紊乱 [25]被子植物门金线莲(兰科开唇兰属)Anoectochilus roxburghii/Anoectochilus formosanus 300 A 良好的降血糖活性 [26]山药(薯蓣科薯蓣属)Dioscoreae opposite 50、75、150 B 降低GLU、TC、TG、LDL-C含量,有效改善血糖水平和血脂代谢紊乱 [27]桑叶(桑科桑属)Morus alba L. 150 A+D 下调胰腺组织NF-κB和TNF-α的表达,改善胰腺组织氧化应激损伤 [28]杜仲(杜仲科杜仲属)Eucommia ulmoides 125、250、500 A 提高抗氧化能力,降低炎症因子含量、TLR4及NF-κB蛋白含量 [29]当归(伞形科当归属)Angelica sinensis 100、200、400 D降低炎症因子TNF-α和IL-6水平,缓解胰岛素抵抗,具有降血糖水平和增强胰岛素功能的作用[30]苦丁茶(冬青科冬青属)Iatifolia latifolia Thumb./Iatifolia kudingcha 100、150、300 B 提高糖尿病小鼠的糖耐量,对正常小鼠血糖含量无影响 [31]金耳环(马兜铃科细辛属)Asarum insigne Diels 2 000、4 000、8 000(以生药计) A 具有抗氧化应激和降血糖、降血脂、改善肾功能的作用 [32]苦竹叶(禾木科大明竹属)Pleioblastus amarus 500 B使空腹胰岛素水平显著上升,MDA含量下降,有显著的降血糖效果,可能与调节自由基代谢有关[33]玄参(玄参科玄参属)Radix Scrophulariae 40、80、160 A+D改善糖代谢、脂代谢功能,提高机体的抗氧化能力,促进胰岛素的分泌[34]秋葵(锦葵科秋葵属)Abelmoschus esculentus 50、200 A 降低血糖含量,提高糖耐受能力 [35]太子参(石竹科孩儿参属)Pseudostellaria heterophylla 1 000、2 000、4 000A、B 具有抗炎作用,保护胰岛β细胞,减轻胰岛素抵抗 [36]莪术(姜科姜黄属)Curcuma kzoangsiensis 500、1 000、2 500A+D 保护胰岛β细胞,减少其凋亡 [37]桔梗(桔梗科桔梗属)Platycodon grandiflorus 150、300、600 A 改善空腹胰岛素含量,提高抗氧化能力 [38]马齿苋(马齿苋科马齿苋属)Portulaca oleracea L.5 000、2 000(以生药计) A 保护和修复损伤的胰岛细胞,提高胰岛素分泌 [39]软枣猕猴桃(猕猴桃科猕猴桃属)Actinidia chinensis 100、200、400 B 调节糖代谢及肝糖原合成,减少肝糖原分解 [40]金银花(忍冬科忍冬属)Lonicera japonica 800 A 降低空腹血糖含量,改善胰岛素抵抗 [41]枸杞(茄科枸杞属)Lycium barbarum 200、400、800 μg/mL B+C 提高胰岛β细胞的存活率,改善细胞中SOD活力和NO、MDA含量 [42]裸子植物门红豆杉(红豆杉科红豆杉属)Taxus chinensis var. mairei 0.005、0.01、0.05、0.1、0.5 mg/mL F 改善胰岛素抵抗,抑制α-葡萄糖苷酶活性 [43]
续表1

注:A.链脲佐菌素(streptozocin,STZ)诱导模型;B.四氧嘧啶诱导模型;C.小鼠NIT-L1胰岛β细胞模型;D.高热量喂养模型;E.蔗糖和淀粉负荷模型;F. HepG2细胞和α-葡萄糖苷酶体外受体模型;PI3K/Akt.磷脂酰肌醇3-激酶/蛋白激酶B(phosphatidyl inositol kinase 3/protein kinase B);GLU.葡萄糖(glucose);TC.总胆固醇(total cholesterol);TG.甘油三酯(triglyceride);LDL-C.低密度脂蛋白胆固醇(low density lipoprotein cholesterol);NF-κB.核转录因子-κB(nuclear factor-κB);TNF-α.肿瘤坏死因子-α(tumor necrosis factor-α);TLR4. Toll样受体4(Toll-like receptors 4);IL-6.白介素-6(inter leukin-6);MDA.丙二醛(malondialdehyde);SOD.超氧化物歧化酶(superoxide dismutase)。
分类 多糖来源(科、属)剂量/(mg/(kg·d))实验模型作用效果、机制参考文献红藻门 蜈蚣藻(隐丝藻科蜈蚣藻属)Grateloupia filicina 2、8、16 B 具有较好的抗氧化、降血脂、降血糖作用 [44]蓝藻门 螺旋藻(颤藻科螺旋藻属)Spirulina 100、200 A修复受损的胰岛细胞,增加胰岛素的分泌、血清中胰岛素含量及胰岛β细胞功能指数[45]绿藻门蛎菜(石莼科石莼属)Ulva conglobata Kjellm 25、100、200 B 显著降低血糖水平 [46]孔石莼(石莼科石莼属)Ulva pertusa Kjellm 250、1 000 B增强机体的抗氧化能力,减轻胰岛细胞的氧化损伤;调节糖代谢关键酶的活性,促进机体对葡萄糖的吸收、利用,促进肝糖原的合成,减少糖异生[47]不等鞭毛门 马尾藻(马尾藻科马尾藻属)Sargassum pallidum 0.1、0.5、1.0、2.0 mg/mL F 抑制α-淀粉酶和α-葡萄糖苷酶活性,改善胰岛素抵抗 [48]
2 植物多糖降血糖机制
正常情况下,机体的血糖由胰岛α细胞分泌的胰高血糖素与胰岛β细胞分泌的胰岛素保持平衡。当胰岛素分泌相对或绝对不足时,血糖水平超出正常范围,血糖平衡破坏,就可能引起糖尿病。胰岛素分泌不足和胰岛素抵抗是引起糖尿病的两大主要原因,胰岛素抵抗指胰岛素促进葡萄糖摄取和利用的效率下降。研究表明:各种科属类植物多糖的降血糖机制具有多样性,不同种属之间无显著差别,其机制包含:抑制胰岛β细胞凋亡;通过抗氧化、抗炎、保护胰岛β细胞结构和功能等方式促进胰岛素的分泌;改善胰岛素与靶细胞特异性结合,通过增强胰岛素敏感性改善胰岛素抵抗;通过调节关键酶活性、促进糖吸收利用和代谢以及信号通路等途径调节血糖含量。
2.1 促进胰岛素分泌
胰岛素是体内唯一能降低血糖水平的激素,胰岛β细胞是体内分泌胰岛素的细胞,当胰岛β细胞结构和功能受损时,会导致胰岛素分泌相对不足,引起糖尿病。研究表明植物多糖可通过抑制胰岛β细胞凋亡、保护和修复胰岛β细胞以促进胰岛素分泌[49]。
2.1.1 抑制胰岛β细胞凋亡
细胞凋亡是细胞自主有序的死亡,由基因严格控制,其中B淋巴细胞瘤-2(B-cell lymphoma-2,Bcl-2)、Caspase-3在细胞凋亡中起重要作用[50]。Bcl-2是抑制细胞凋亡蛋白,Caspase-3是促细胞凋亡蛋白。研究表明,植物多糖可通过上调Bcl-2和抑制Caspase-3的表达抑制胰岛β细胞的凋亡,刺激胰岛素分泌,调节血糖水平。
桑叶多糖[51-52]能上调STZ诱导糖尿病大鼠的抗凋亡性蛋白Bcl-2的mRNA表达,抑制促凋亡蛋白Caspase-3活化,刺激胰岛细胞分泌胰岛素,增加胰岛素含量,降低血糖水平。黄精多糖[6]能降低STZ糖尿病大鼠的空腹血糖水平和糖化血清蛋白含量,下调Caspase-3表达,增加血清胰岛素含量,改善胰岛细胞形态,降低血糖水平。
2.1.2 保护并修复胰岛β细胞
除了胰岛β细胞的凋亡外,胰岛β细胞的结构和功能受损同样也会引起胰岛素分泌的不足。研究表明,植物多糖可通过抗氧化、抗炎等途径保护和修复胰岛β细胞。
2.1.2.1 抗氧化
SOD、过氧化氢酶(catalase,CAT)、谷胱甘肽过氧化物酶(glutathione peroxidase,GSH-Px)等自由基抗氧化酶在胰岛β细胞内表达相对较低,造成胰岛素对活性氧(reactive oxygen species,ROS)和活性氮(reactive nitrogen species,RNS)等自由基敏感[53]。一旦ROS、RNS等自由基过量,存在于细胞环境中的多余自由基可破坏细胞大分子(如DNA、蛋白质和脂质等),引起氧化应激,导致胰岛β细胞结构及功能受损,引起胰岛素分泌不足。SOD、CAT和GSH-Px活性等指标可反映氧自由基的清除能力,进而反映胰岛β细胞的受损程度。
苦瓜多糖[54]通过改善STZ诱导大鼠的体质量和高血糖、高脂血症,上调抗氧化酶(GSH-Px、SOD和CAT)活力、下调MDA含量,恢复其总抗氧化能力,减轻氧化应激导致的肾脏损伤,改善血糖水平。仙人掌多糖[55]能增强SOD、GSH-Px和CAT的活性,并降低STZ诱导的糖尿病大鼠血清、肝脏、肾脏和胰腺中的MDA水平,保护并修复胰岛β细胞,具有抗氧化和降血糖的作用。黑果枸杞果实多糖[42]能显著降低糖尿病小鼠的血糖含量,增强糖尿病小鼠血清和肝脏SOD活性,降低其血清和肝脏MDA含量,通过促进机体对SOD等抗氧化酶的生物合成,增强机体抗氧化能力及清除氧化产物的能力,减轻或阻止自由基对胰岛β细胞的损伤,促进胰岛β细胞的修复与再生,并能促进葡萄糖转变为肝糖原,因此具有降血糖的作用,且抗氧化能力优于盐酸二甲双胍。
2.1.2.2 抗炎
炎症细胞因子如IL-1、TNF-α、IL-6和IL-8等的表达会引发炎症,是胰岛β细胞功能受损的原因之一[53]。研究表明植物多糖可降低炎症因子的表达,保护胰岛β细胞,控制血糖含量。
当归多糖[30]可以降低IL-6和TNF-α的表达,表现出抗炎作用,保护胰岛β细胞,降低血糖含量。太子参多糖[56]可通过降低TNF-α、提高IL-10的水平保护胰岛β细胞,减轻胰岛素抵抗,降低血糖含量。
2.2 改善胰岛素与靶细胞特异性结合,增强胰岛素敏感性
脂肪、骨骼肌和肝脏细胞都是胰岛素作用的靶细胞,胰岛素通过与靶细胞表面的胰岛素受体(insulin receptor,InsR)特异性结合而发挥作用。InsR的数量以及与靶细胞特异性结合的亲和力都能呈现一定的降血糖作用。
仙人掌果多糖[57]可通过增加STZ诱导的糖尿病大鼠胰岛β细胞数量刺激胰岛素的分泌,从而降低血糖水平,并降低血清中TC和TG含量,调节血脂代谢。丹皮多糖[58]能提高肝细胞低亲和力和InsR最大结合容量,使胰岛素敏感性指数增加,提高InsR数量、改善受体环节的胰岛素抵抗,显著降低STZ诱导的糖尿病大鼠空腹血糖含量,改善糖耐量异常及血脂异常。
2.3 调节关键酶活性
糖类吸收、利用和代谢以及胰岛素与受体结合都需要一定的关键酶才能发挥作用。机体内有的关键酶可促进糖类的消化吸收、利用及代谢,有的会妨碍胰岛素与受体结合。目前,植物多糖可通过调节葡萄糖吸收、利用、代谢关键酶活性以及蛋白酪氨酸磷酸酶1B(protein tyrosine phosphatase-1B,PTP-1B)的表达调节血糖含量,改善糖代谢紊乱,减轻胰岛素抵抗[49]。
2.3.1 抑制α-淀粉酶和α-葡萄糖苷酶活性
α-淀粉酶和α-葡萄糖苷酶是机体中碳水化合物消化和吸收的两个最关键的酶。α-淀粉酶可分解长链碳水化合物;α-葡萄糖苷酶可水解葡萄糖苷键,释放出葡萄糖,它们是直接参与淀粉及糖原代谢途径必不可少的酶。因此,抑制α-淀粉酶和α-葡萄糖苷酶的活性可以抑制碳水化合物水解释放葡萄糖,减缓小肠对葡萄糖的吸收[53]。
山茶花多糖[24]和马尾藻多糖[48]都可以通过抑制α-淀粉酶和α-葡萄糖苷酶活性缓解胰岛素抵抗,从而降低血糖含量。打瓜干皮多糖[20]对淀粉和蔗糖负荷小鼠均有降血糖作用,且对α-葡萄糖苷酶有明显的抑制作用。Chen Chun等[59]证实辣木叶多糖具有抑制α-淀粉酶和α-葡萄糖苷酶活性的作用,并具有治疗糖尿病的潜力。
2.3.2 提高糖代谢关键酶活性,促进肝糖原合成,抑制糖异生
肝脏是葡萄糖代谢的主要器官之一[60],当血糖不平衡时,可通过肝糖原的合成和分解维持机体血糖平衡。葡萄糖激酶(glucokinase,GK)是糖代谢中的关键酶,催化葡萄糖转化为6-磷酸葡萄糖,促进肝糖原的合成。葡萄糖6-磷酸酶(glucose-6-phosphatase,G6Pase)是肝脏糖异生的关键酶,催化6-磷酸葡萄糖转化为葡萄糖。葡萄糖运转体2(glucose transporter,GLUT2)是肝脏最主要的葡萄糖转运体,运送葡萄糖进出肝脏,与GK协调作用促使胰岛素分泌,参与机体血糖调节[61]。
白簕中性均一多糖[62]通过提高GLUT2和GK表达,降低G6Pase表达,促进葡萄糖在肝脏中的转化,抑制糖异生,降低STZ诱导的I型糖尿病小鼠的血糖水平。薏苡仁多糖[63]能通过增加肝脏GK活力和促进肝糖原合成,调节糖尿病大鼠的糖代谢异常,降低血糖水平。
2.3.3 下调PTP-1B的表达
PTP-1B与蛋白酪氨酸激酶(protein tyrosine kinases,PTK)共同维持着酪氨酸蛋白磷酸化的平衡。InsR或其底物上的酪氨酸残基会被PTP-1B去磷酸化,对胰岛素信号转导进行负调节;组织细胞中PTP-1B过多表达会降低PTK的活性,使InsR无法与胰岛素结合,引起胰岛素抵抗,导致血糖水平升高[64]。
桑叶多糖[65]能改善STZ诱导的糖尿病大鼠的口服葡萄糖耐量,恢复糖原合成酶(glycogen synthase,GS)活性。胰岛素信号通路中InsR底物2、PI3K、蛋白激酶A(protein kinase A,PKA)表达上调,降低PTP-1B表达、激活PI3K-Akt途径可以有效调节糖代谢。
2.4 调节信号通路
2.4.1 PI3K/Akt信号通路
葡萄糖通过协助扩散方式透过细胞膜脂质双层结构进入细胞,但其扩散方式需要细胞膜上的GLUT载体蛋白转运才能完成。当PI3K/Akt信号通路被激活后,GLUT4从细胞内转移到细胞膜,可增加葡萄糖的摄取[66]。
PI3K是由调节亚基p85和催化亚基p110所组成的异二聚体。Akt又称蛋白激酶B,是PI3K信号通路下游的重要靶蛋白。Akt有3 个亚型,其中Akt2主要参与胰岛素效应组织中葡萄糖的稳态调节,在胰岛素敏感的组织如脂肪、骨骼肌和肝脏中都有较高的表达[67]。因此,激活PI3K/Akt信号通路可调节血糖水平。
茶多糖[68]可以降低Ⅱ型糖尿病小鼠的TC和LDL-C含量,使TG和高密度脂蛋白胆固醇含量恢复正常水平;改善肝脏和肾脏组织中SOD、GPX-Px活性,保护细胞;上调PI3K、磷酸化-Akt(p-Akt)、GLUT4表达,激活PI3K/Akt信号通路,发挥降血糖的作用。铁皮石斛多糖[25]通过调节肝脏和肌肉中的糖原合成激酶-3β、GS和GLUT4促进糖原合成;增强肝脏中的葡萄糖代谢酶、丙酮酸激酶、己糖激酶、磷酸烯醇丙酮酸羧激酶活性;改善糖代谢障碍,上调PI3K/Akt信号通路,降低STZ诱导的糖尿病小鼠的血糖水平。2.4.2 MAPK信号通路
丝裂原活化蛋白激酶(mitogen-activated protein kinase,MAPK)是信号从细胞表面传导到细胞核内部的重要传递者,参与细胞增殖、分化、存活和凋亡等活动。它分为4 个亚族:细胞外调节蛋白激酶(extracellular regulated protein kinases,ERK)、p38、Jun氨基末端激酶(Jun N-terminal kinase,JNK)和ERK5。其中JNK和p38 MAPK信号通路在炎症和细胞凋亡的应激反应中起关键作用,植物多糖可调节此信号通路,抑制胰岛细胞凋亡,提高胰岛素水平[69]。
桑葚多糖[70]通过下调p-JNK、p-p38和Caspase-3蛋白的表达,抑制胰岛细胞的凋亡,降低STZ诱导的糖尿病小鼠的空腹血糖和血红蛋白A1c水平,并提高胰岛素水平。
2.4.3 cAMP-PKA信号通路
环磷酸腺苷(cyclic adenosine monophosphate,cAMP)是一种环状核苷酸,具有调节细胞代谢的作用,但是需要依赖PKA下游靶蛋白磷酸化发挥作用。cAMP-PKA信号通路的激活可以刺激胰岛β细胞分泌胰岛素[71]。
研究证实绿茶多糖[72]在体外可上调胰高血糖素样肽-1受体、PKA、胰十二指肠同源框因子(pancreatic and duodenal homeobox 1,PDX-1)、INS-1、INS-2、GLUT2和GK的转录,并通过在胰岛素调节细胞系RIN-5F细胞中加入SQ22536(AC抑制剂)和H-89(PKA抑制剂)检测胰岛素的分泌,证实绿茶多糖通过cAMP-PKA通路刺激胰岛素的分泌,从而降低血糖水平。
2.5 其他降血糖作用机制
2.5.1 拮抗胰高血糖素
胰高血糖素和胰岛素是保持机体内血糖平衡的两大激素,刺激胰岛素的分泌可有效控制血糖水平,拮抗胰高血糖素的产生也是控制机体血糖含量的手段之一。
芦荟多糖[73]可能是通过降低胰高血糖素水平、促进糖原的合成及抑制糖异生降低四氧嘧啶糖尿病大鼠和小鼠的血糖水平,而并非是通过刺激胰岛β细胞分泌胰岛素从而起到降血糖的作用。同时它还可以促进糖尿病小鼠损伤的胰岛组织结构修复,抑制胰岛细胞空泡变性及纤维化。
2.5.2 胰十二指肠同源框因子
PDX-1是同源盒家族中的一员,其主要功能为指导胰腺的发育和分化,促进胰岛β细胞增殖,抑制胰岛β细胞凋亡,调节胰岛素基因及几个重要的胰岛β细胞特异性基因的转录,对于胰岛β细胞功能的稳定性及糖尿病的发生、发展有一定意义[74]。
桑叶多糖[52]可以改善高脂肪饮食和STZ诱导的糖尿病大鼠胰岛素的分泌,增加胰岛素含量,其机制可能是恢复糖尿病大鼠胰岛细胞中PDX-1蛋白的核定位和增加PDX-1的mRNA和蛋白的表达。
3 结 语
糖尿病是威胁全球人类健康的疾病之一,长期罹患糖尿病可导致各种并发症。然而,至今尚未发现能根治糖尿病的方法,目前主要采用西药治疗,但各种合成抗糖尿病西药如噻唑烷二酮类、美格列奈类、双胍类等具有较严重的副作用。因此,毒性低、副作用小的植物多糖被广泛研究。研究发现,具有降血糖作用的植物多糖种类多样,包含不同科、属类植物,其降血糖机制也具有多样性,不同种、属之间无显著差别;其可通过抑制胰岛β细胞凋亡,保护修复胰岛细胞,调节糖代谢关键酶活性,促进葡萄糖的吸收、利用,促进肝糖原的合成,减少糖异生以及调节信号通路等途径达到降血糖目的。
但是,目前植物多糖在糖尿病方面的研究主要集中在降血糖作用及机制,对糖尿病引发的各种并发症研究较缺乏,进一步了解植物多糖对并发症的抑制作用及机制可能会减少糖尿病带来的伤害,这对糖尿病及降血糖药物的研究都具有一定的意义。
参考文献:
[1] 钱虹, 陆锐明. 糖尿病的研究现状及进展[J]. 医学综述, 2015, 21(13):2418-2420. DOI:10.3969/j.issn.1006-2084.2015.13.045.
[2] 中华医学会糖尿病学分会. 中国2型糖尿病防治指南(2017年版)[J]. 中国实用内科杂志, 2018, 38(4): 292-344. DOI:10.19538/j.nk2018040108.
[3] 汪会琴, 胡如英 , 武海滨, 等. 2型糖尿病报告发病率研究进展[J].浙江预防医学, 2016, 28(1): 37-39; 57. DOI:10.19485/j.cnki.issn1007-0931.2016.01.010.
[4] 温玉琴. 光活化药物可降低糖尿病药物的毒副作用[J]. 广东药学院学报, 2014, 30(5): 548. DOI:10.1038/ncomms6116.
[5] 梁轶媛. 植物多糖生物活性研究进展[J]. 产业与科技论坛, 2014,13(9): 68-69. DOI:10.3969/j.issn.1673-5641.2014.09.036.
[6] 王艺, 彭国庆, 江新泉, 等. 黄精多糖对糖尿病大鼠模型的保护机制研究[J]. 中医药导报, 2017, 23(2): 8-16. DOI:10.13862/j.cnki.cn43-1446/r.2017.02.003.
[7] 侯红瑞, 陈玲, 孙国勇, 等. 知母多糖对链脲佐菌素诱导糖尿病大鼠的降血糖作用研究[J]. 食品工业科技, 2018, 39(12): 69-72; 78.DOI:10.13386/j.issn1002-0306.2018.12.013.
[8] 李晶, 苏薇薇, 王永刚, 等. 麦冬多糖提取工艺的优选及降血糖作用研究[J]. 中医药导报, 2017, 23(24): 52-54. DOI:10.13862/j.cnki.cn43-1446/r.2017.24.019.
[9] 肖遐, 吴雄, 何纯莲. 百合多糖对I型糖尿病大鼠的降血糖作用[J].食品科学, 2014, 35(1): 209-213. DOI:10.7506/spkx1002-6630-201401041.
[10] 朱振元, 李楠, 张静怡, 等. 雪莲果多糖降血脂及降血糖活性的研究[J]. 现代食品科技, 2017, 33(5): 39-46; 76. DOI:10.13982/j.mfst.1673-9078.2017.5.007.
[11] 牛月华. 茅苍术多糖对II型糖尿病大鼠的治疗作用及机制研究[J].北华大学学报(自然科学版), 2014, 15(4): 476-479.
[12] 尹美珍, 胡岗, 苏振宏, 等. 艾叶多糖I型糖尿病小鼠的降血糖作用[J]. 时珍国医国药, 2015, 26(9): 2072-2074.
[13] 王佳佳, 刘玮, 朱静, 等. 牛蒡多糖的降血糖活性[J]. 中国药科大学学报, 2013, 44(5): 455-459. DOI:10.11665/j.issn.1000-5048.20130514.
[14] 杨洁, 马英慧, 崔秀成, 等. 三七多糖对糖尿病模型大鼠的降血糖作用和眼视网膜病变的治疗作用及其机制[J]. 吉林大学学报(医学版),2017, 43(4): 734-738; 860. DOI:10.13481/j.1671-587x.20170414.
[15] 杨慧文, 周露, 张旭红, 等. 白簕茎多糖对链脲佐菌素致糖尿病小鼠的降血糖作用研究[J]. 现代食品科技, 2017, 33(5): 52-57.DOI:10.13982/j.mfst.1673-9078.2017.5.009.
[16] 赵博, 王一峰, 侯宏红. 中国楤木粗多糖对糖尿病大鼠的降血糖作用[J]. 食品科学, 2015, 36(13): 211-214. DOI:10.7506/spkx1002-6630-201513039.
[17] 王晓琳. 黄芪多糖降低2型糖尿病大鼠血糖水平及预防糖尿病相关并发症的实验研究[D]. 新乡: 新乡医学院, 2016: 1-58.
[18] 向阳, 贺家勇, 郑杰, 等. 刺糖粗多糖对糖尿病大鼠降糖及抗氧化功能的实验研究[J]. 时珍国医国药, 2017, 28(6): 1281-1284.
[19] MA Q Y, YUAN L, ZHUANG Y L. Preparation, characterization and in vivo antidiabetic effects of polysaccharides from Pachyrrhizus erosus[J]. International Journal of Biological Macromolecules, 2018,114: 97-105. DOI:10.1016/j.ijbiomac.2018.03.099.
[20] 张义晖, 田丽萍, 薛琳, 等. 打瓜干皮中多糖的含量测定及降血糖作用机制[J]. 医药导报, 2017, 36(5): 477-480. DOI:10.3870/j.issn.1004-0781.2017.05.004.
[21] 宋丽君. 南瓜多糖对糖尿病大鼠血糖、血脂及氧化应激能力的影响[J]. 中国应用生理学杂志, 2015, 31(1): 65-66; 71. DOI:10.13459/j.cnki.cjap.2015.01.019.
[22] ZHANG C, CHEN H M, BAI W Q. Characterization of Momordica charantia L. polysaccharide and its protective effect on pancreatic cells injury in STZ-induceddiabetic mice[J]. International Journal of Biological Macromolecules, 2018, 115: 45-52. DOI:10.1016/j.ijbiomac.2018.04.039.
[23] 张宽朝, 马皖燕, 文汉. 油茶籽多糖降血糖作用的初步研究[J].食品工业科技, 2014, 35(2): 337-339; 345. DOI:10.13386/j.issn1002-0306.2014.02.009.
[24] HAN Q, YU Y Q, SHI J, et al. Molecular characterization and hypoglycemic activity of a novel water-solublepolysaccharide from tea (Camellia sinensis) flower[J]. Carbohydrate Polymers, 2011, 86(2):797-805. DOI:10.1016/j.carbpol.2011.05.039.
[25] WANG K P, WANG H X, LIU Y G, et al. Dendrobium officinale polysaccharide attenuates type 2 diabetes mellitus via the regulation of PI3K/Akt-mediated glycogen synthesis and glucose metabolism[J].Journal of Functional Foods, 2018, 40: 261-271. DOI:10.1016/j.jff.2017.11.004.
[26] TANG T T, DUAN X Y, KE Y, et al. Antidiabetic activities of polysaccharides from Anoectochilus roxburghii and Anoectochilus formosanus in STZ-induced diabetic mice[J]. International Journal of Biological Macromolecules, 2018, 112: 882-888. DOI:10.1016/j.ijbiomac.2018.02.042.
[27] 李新萍, 周书琦, 徐丽丽, 等. 山药多糖的提取及其对糖尿病小鼠的影响研究[J]. 黑龙江医药, 2018, 31(1): 20-22. DOI:10.14035/j.cnki.hljyy.2018.01.007.
[28] 任春久, 孙永亮, 李伟庆, 等. 桑叶多糖MLP II对糖尿病大鼠胰腺组织氧化应激的保护作用[J]. 蚕业科学, 2017, 43(4): 671-676.DOI:10.13441/j.cnki.cykx.2017.04.018.
[29] 苏卓, 郭诚, 梁韬. 杜仲多糖对链脲佐菌素致糖尿病小鼠的作用[J].中国实验方剂学杂志, 2016, 22(14): 159-162. DOI:10.13422/j.cnki.syfjx.2016140161.
[30] 杨秋香. 当归多糖对2型糖尿病预防及治疗作用的初步研究[D]. 武汉: 华中科技大学, 2013: 1-99.
[31] 于淑池, 陈文, 杭瑜瑜, 等. 海南苦丁茶多糖的降血糖功效评价[J].食品研究与开发, 2017, 38(4): 161-164. DOI:10.3969/j.issn.1005-6521.2017.04.036.
[32] 周多强, 李溥, 罗良琦, 等. 水药金耳环多糖对实验性2型糖尿病模型大鼠糖脂代谢、肾功能及氧化应激的影响[J]. 中国药房, 2017,28(31): 4415-4419. DOI:10.6039/j.issn.1001-0408.2017.31.25.
[33] 潘静, 杨建琼, 欧阳文, 等. 苦竹叶多糖降血糖作用研究[J]. 亚太传统医药, 2017, 13(22): 10-12. DOI:10.11954/ytctyy.201722004.
[34] 赵洪伟, 张宁, 李自辉, 等. 玄参多糖对2型糖尿病大鼠降糖作用的研究[J]. 中医药信息, 2017, 34(5): 8-12. DOI:10.3969/j.issn.1002-2406.2017.05.004.
[35] LIU J, ZHAO Y P, WU Q X, et al. Structure characterisation of polysaccharides in vegetable “okra” and evaluation of hypoglycemic activity[J]. Food Chemistry, 2018, 242: 211-216. DOI:10.1016/j.foodchem.2017.09.051.
[36] HU J, PANG W S, CHEN J L, et al. Hypoglycemic effect of polysaccharides with different molecular weight of Pseudostellaria heterophylla[J]. BMC Complementary and Alternative Medicine,2013, 13: 267-276. DOI:10.1186/1472-6882-13-267.
[37] 肖旺, 曾建红, 陈旭. 广西莪术多糖对2型糖尿病大鼠的降血糖作用[J]. 中国实验方剂学杂志, 2015, 21(21): 144-147. DOI:10.13422/j.cnki.syfjx.2015210144.
[38] 乔彩虹, 孟祥顺. 桔梗多糖降血糖作用及其机制[J]. 中国老年学杂志,2015, 35(7): 1944-1946. DOI:10.3969/j.issn.1005-9202.2015.07.095.
[39] 郑智音, 贾晓斌, 舒娈, 等. 鲜马齿苋多糖、生物碱和多酚类组分的制备及其降血糖活性研究[J]. 中草药, 2014, 45(18): 2673-2677.DOI:10.7501/j.issn.0253-2670.2014.18.019.
[40] 刘延吉, 刘金凤, 田晓艳, 等. 软枣猕猴桃多糖降血糖降血脂活性研究[J]. 食品与生物技术学报, 2012, 31(1): 86-89. DOI:10.3969/j.issn.1673-1689.2012.01.013.
[41] WANG D Y, ZHAO X M, LIU Y L. Hypoglycemic and hypolipidemic effects of a polysaccharide from flower buds of Lonicera japonica in streptozotocin-induced diabetic rats[J]. International Journal of Biological Macromolecules, 2017, 102: 396-404. DOI:10.1016/j.ijbiomac.2017.04.056.
[42] 汪建红, 陈晓琴, 张蔚佼. 黑果枸杞果实多糖降血糖生物功效及其机制研究[J]. 食品科学, 2009, 30(5): 244-248. DOI:10.3321/j.issn:1002-6630.2009.05.056.
[43] 汤彬, 薛平, 李祥, 等. 南方红豆杉多糖的含量测定及体外降血糖活性研究[J]. 食品工业科技, 2013, 34(9): 128-131; 136. DOI:10.13386/j.issn1002-0306.2013.09.007.
[44] 张婧婧, 刘秋凤, 吴成业. 蜈蚣藻多糖降血糖及降血脂活性的研究[J]. 福建水产, 2014, 36(1): 21-28. DOI:10.14012/j.cnki.fjsc.2014.01.012.
[45] 常雪莹, 王苏仪, 张汝南, 等. 螺旋藻多糖对糖尿病大鼠血糖及胰岛素水平的影响[J]. 职业与健康, 2016, 32(17): 2348-2350; 2355.DOI:10.13329/j.cnki.zyyjk.2016.0738.
[46] 陈小娥, 方旭波, 钟秋琴. 蛎菜酸性多糖的分离纯化和降血糖活性研究[J]. 中国食品学报, 2008(5): 75-79. DOI:10.16429/j.1009-7848.2008.05.002.
[47] 林龙. 孔石莼多糖对四氧嘧啶诱导的糖尿病小鼠的降血糖作用及其机制研究[D]. 厦门: 集美大学, 2013: 1-59.
[48] CAO C L, HUANG Q, ZHANG B, et al. Physicochemical characterization and in vitro hypoglycemic activities of polysaccharides from Sargassum pallidum by microwave-assisted aqueous two-phase extraction[J]. International Journal of Biological Macromolecules,2018, 109: 357-368. DOI:10.1016/j.ijbiomac.2017.12.096.
[49] 廖冬冬, 林文庭. 植物多糖降血糖作用机制的研究进展[J]. 海峡预防医学杂志, 2012, 18(2): 26-28.
[50] 李敏, 林俊. 细胞凋亡途径及其机制[J]. 国际妇产科学杂志, 2014,41(2): 103-107.
[51] ZHANG Y, REN C, LU G, et al. Purification, characterization and antidiabetic activity of a polysaccharide from mulberry leaf[J]. Regulatory Toxicology and Pharmacology, 2014(3): 687-695. DOI:10.1016/j.yrtph.2014.10.006.
[52] ZHANG Y, REN C, LU G, et al. Anti-diabetic effect of mulberry leaf polysaccharide by inhibiting pancreatic islet cell apoptosis and ameliorating insulin secretory capacity in diabetic rats[J].International Immunopharmacology, 2014(1): 248-257. DOI:10.1016/j.intimp.2014.06.039.
[53] WU J J, SHI S S, WANG H J, et al. Mechanisms underlying the effect of polysaccharides in the treatment of type 2 diabetes: a review[J]. Carbohydrate Polymers, 2016, 144: 474-494. DOI:10.1016/j.carbpol.2016.02.040.
[54] RAISH M, AHMAD A, JAN B L, et al. Momordica charantia polysaccharides mitigate the progression of STZ induced diabetic nephropathy in rats[J]. International Journal of Biological Macromolecules, 2016, 91: 394-399. DOI:10.1016/j.ijbiomac.2016.05.090.
[55] GAO J, HAN Y L, JIN Z Y, et al. Protective effect of polysaccharides from Opuntia dillenii Haw. fruits on streptozotocin-induced diabetic rats[J]. Carbohydrate Polymers, 2015, 124: 25-34. DOI:10.1016/j.carbpol.2015.01.068.
[56] KANAGASABAPATHY G, KUPPUSAMY U R, ABD MALEK S N, et al.Glucan-rich polysaccharides from Pleurotussajor-caju (Fr.) Singer prevents glucose intolerance, insulin resistance and inflammation in C57BL/6J mice fed a high-fat diet[J]. BMC Complementary and Alternative Medicine, 2012, 12(1): 2-9. DOI:10.1186/1472-6882-12-261.
[57] 梁秋云, 蒙华琳, 刘华钢, 等. 仙人掌果多糖降血糖作用及其机制[J].中国新药杂志, 2010, 19(14): 1252-1254; 1259.
[58] 王钦茂, 洪浩, 赵帜平, 等. 丹皮多糖-2b对2型糖尿病大鼠模型的作用及其降糖作用机制[J]. 中国药理学通报, 2002, 8(4): 456-459.DOI:10.3321/j.issn:1001-1978.2002.04.026.
[59] CHEN Chun, ZHANG Bin, HUANG Qiang, et al. Microwave-assisted extraction of polysaccharides from Moringaoleifera Lam. leaves:characterization and hypoglycemic activity[J]. Industrial Crops and Products, 2017, 100: 1-11. DOI:10.1016/j.indcrop.2017.01.042.
[60] LIM E L, HOOLLINGSWORTH K G, ARIBISALALA B S, et al.Reversal of type 2 diabetes: normalisation of beta cell function in association with decreased pancreas and liver triacylglycerol[J].Diabetologia, 2011, 54(10): 2506-2514. DOI:10.1007/s00125-011-2204-7.
[61] 汪建辉, 欧瑜. 葡萄糖激酶与糖尿病[J]. 药物生物技术, 2012, 19(6):552-556. DOI:10.19526/j.cnki.1005-8915.2012.06.020.
[62] 周露, 杨慧文, 程轩轩, 等. 白簕中性均一多糖对链脲佐菌素诱导的糖尿病小鼠降糖作用机制研究[J]. 食品工业科技, 2017, 38(17):288-291. DOI:10.13386/j.issn1002-0306.2017.17.056.
[63] 徐梓辉, 周世文, 黄林清, 等. 薏苡仁多糖对实验性2型糖尿病大鼠胰岛素抵抗的影响[J]. 中国糖尿病杂志, 2002(1): 42-46.DOI:10.3321/j.issn:1006-6187.2002.01.012.
[64] 付建平, 熊伟, 吴磊, 等. 蛋白酪氨酸磷酸酶抑制剂的研究进展[J].生物化工, 2017, 3(6): 82-85; 88.
[65] REN C, ZHANG Y, CUI W, et al. A polysaccharide extract of mulberry leaf ameliorates hepatic glucose metabolism and insulin signaling in rats with type 2 diabetes induced by high fat-diet and streptozotocin[J].International Journal of Biological Macromolecules, 2015, 72:951-959. DOI:10.1016/j.ijbiomac.2014.09.060.
[66] 张楠, 赵颖. 葡萄糖转运蛋白GLUT4表达的调节机制[J]. 中国生物化学与分子生物学报, 2016, 32(3): 237-244. DOI:10.13865/j.cnki.cjbmb.2016.03.01.
[67] 杨萍. 白背三七的体内降血糖作用及其对小鼠AKT/PI3K信号通路的影响[D]. 苏州: 苏州大学, 2015: 1-55.
[68] LI S Q, CHEN H X, WANG J, et al. Involvement of the PI3K/Akt signal pathway in the hypoglycemic effects of tea polysaccharides on diabetic mice[J]. International Journal of Biological Macromolecules,2015, 81: 967-974. DOI:10.1016/j.ijbiomac.2015.09.037.
[69] 宁崇. 基于菊苣菊粉调节JNK和p38 MAPK信号通路对II型糖尿病血糖作用机制的研究[D]. 沈阳: 沈阳农业大学, 2017: 1-114.
[70] XU L, YANG F, WANG J, et al. Anti-diabetic effect mediated by Ramulus mori polysaccharides[J]. Carbohydrate Polymers, 2015, 117:63-69. DOI:10.1016/j.carbpol.2014.09.052.
[71] LUO G, KONG X, LU L, et al. Glucagon-like peptide 1 potentiates glucotoxicity-diminished insulin secretion via stimulation of cAMPPKA signaling in INS-1E cells and mouse islets[J]. International Journal of Biochemistry and Cell Biology, 2013(2): 483-490.DOI:10.1016/j.biocel.2012.11.016.
[72] WANG H, SHI S, BAO B, et al. Structure characterization of an arabinogalactan from green tea and its anti-diabetic effect[J].Carbohydrate Polymers, 2015, 124: 98-108. DOI:10.1016/j.carbpol.2015.01.070.
[73] 郭冷秋, 苏慧, 黄莉莉. 芦荟多糖防治糖尿病作用的实验研究(II)[J]. 中医药学报, 2006(3): 21-22. DOI:10.19664/j.cnki.1002-2392.2006.03.010.
[74] 范鑫, 何军华. PDX-1与2型糖尿病[J]. 临床医药实践, 2016, 25(5):367-370. DOI:10.16047/j.cnki.cn14-1300/r.2016.05.020.
Recent Progress in Understanding of Hypoglycemic Effect and Underlying Mechanism of Plant Polysaccharides
XIAO Ruixi, CHEN Huaguo, ZHOU Xin*
(Key Laboratory for Information System of Mountainous Areas and Protection of Ecological Environment, Guizhou Engineering Laboratory for Quality Control & Evaluation Technology of Medicine, Research Center for Quality Control of Natural Medicine,Guizhou Normal University, Guiyang 550001, China)
Abstract: Diabetes is one of the clinical manifestations of hyperglycemia, and various complications may be caused by long-term diabetes. At present, no therapy has been found to cure diabetes and the treatment of this disease using western medicine is prevalent. However, western medicine has serious side effects. For this reason, natural substances with high potential to lower blood glucose, low toxicity and few side effects have gained much attention. Plant polysaccharides, widely distributed in nature, have been reported for their good hypoglycemic effect. As natural bioactive substances, they have the characteristics of low toxicity and small side effects making them a research hotspot in the fields of medicinal and health foods. The types of plant polysaccharides with hypoglycemic effects that have been researched worldwide in recent years and the underlying mechanisms are summarized in this article.
Keywords: plant polysaccharides; diabetes; hypoglycemic effect; mechanism
收稿日期:2018-04-29
基金项目:国家自然科学基金面上项目(31570358);贵州省高层次创新人才培养项目(黔科合人才(2015)4033号);贵州省优秀青年科技人才项目(黔科合人才[2017]5625);贵州省教育厅青年科技人才成长项目(黔教合KY字[2017]123);贵州省科技计划项目(黔科合支撑[2018]2826)
第一作者简介:肖瑞希(1992—)(ORCID: 0000-0003-0788-6636),女,硕士研究生,研究方向为药用植物开发与利用。E-mail: 375973259@qq.com
*通信作者简介:周欣(1962—)(ORCID: 0000-0002-9946-5806),女,教授,博士,研究方向为中药质量控制、药物体内代谢以及药品、保健食品开发。E-mail: alice9800@sina.com
DOI:10.7506/spkx1002-6630-20180429-385
中图分类号:R285.1;TS201.4
文献标志码:A
文章编号:1002-6630(2019)11-0254-07
引文格式:
肖瑞希, 陈华国, 周欣. 植物多糖降血糖作用及机制研究进展[J]. 食品科学, 2019, 40(11): 254-260. DOI:10.7506/spkx1002-6630-20180429-385. http://www.spkx.net.cn
XIAO Ruixi, CHEN Huaguo, ZHOU Xin. Recent progress in understanding of hypoglycemic effect and underlying mechanism of plant polysaccharides[J]. Food Science, 2019, 40(11): 254-260. (in Chinese with English abstract)DOI:10.7506/spkx1002-6630-20180429-385. http://www.spkx.net.cn


