随着社会经济的高速发展及人们生活水平的提高,淡水鱼因具有较好的适应能力、生长快、食性杂、抗病能力强、产量高、易养殖、肉质细嫩等特点[1],日益受到人们在餐桌上的青睐。淡水鱼因营养物质丰富,含有多种人体必需的氨基酸、维生素和大量的不饱和脂肪酸等[2],在贮藏、加工、运输过程中,酶和微生物的作用极易导致淡水鱼品质急剧降低;因此淡水鱼类的保鲜技术始终是食品科研中的热点,在鱼类长期贮藏保鲜中主要依赖于冻藏技术[3]。冻藏技术依据冻结速率可以分为快速冻结和慢速冻结,在冷冻过程中冻结速率决定了冰晶大小与数目,快速冻结能够使物料快速通过最大冰晶生成带,形成大量分布均匀、颗粒细小的冰晶体,使得细胞内外的压力保持均衡,对细胞损伤小,能够最大限度维持物料的品质;而慢速冻结形成冰晶数目少、体积大,易造成细胞产生机械损伤、细胞破裂、汁液外流,使得物料品质急剧降低[4]。不同冷冻方式其不同冻结速率对细胞组织结构产生不同程度的影响,进而影响烹调口感及营养价值。
食品加工中的冷冻方式主要有静止空气冻结、鼓风冻结和液氮冻结等,这些冷冻方式相较于其他冻结方式具有以下优点:速冻快、产量高、产品质量好、干耗小、抗氧化、杂菌少、环境友好。另外,液氮冻结设备占地面积小、结构简单、操作方便、易于维护[5];随着空气分离技术发展,液氮冻结成本逐渐下降,使得液氮冻结技术在食品行业中成为新的研究热点[6],此外,液氮无色、无味、化学性质稳定,不与其他物质发生化学反应,产品质量和营养价值能够更好地维持[7]。目前对液氮速冻的水产品研究主要包括鲍鱼、带鱼、银鲳鱼、蟹、鱼丸等产品,其中常用-20、-40、-60 ℃及喷淋式、沉浸式等液氮冷冻方式维持产品品质,但是关于-80 ℃液氮速冻对淡水水产品的影响还鲜见报道。因此,本研究通过-30 ℃平板冷冻、-80 ℃冰箱冷冻、-80 ℃液氮冷冻方式进行对比,研究不同冷冻方式对鮰鱼、鲈鱼、鳜鱼品质的影响,以期为液氮速冻技术在淡水鱼流通、运输、贮藏方面应用及进一步研究提供理论依据和技术指导。
鲜活的斑点叉尾鮰(约2 kg)、鲈鱼(约1 kg)、鳜鱼(约1 kg)各12 条,购于湖北省武汉市白沙洲水产品批发市场。
酒石酸钾钠 西陇化工股份有限公司;无水硫酸铜 上海麦克林生化科技有限公司;氢氧化钠、氯化钠、二甲苯、盐酸、氨水、中性树胶、无水乙醇、十二烷基硫酸钠 国药集团化学试剂有限公司;苏木精-伊红染液(hematoxylin-eosin,HE) 武汉谷歌生物科技;Tissue-Tek® O.C.T.试剂 日本樱花SAKURA公司。
KLS-YXD-1柜式液氮速冻机 成都科莱斯低温设备有限公司;BD-255LTB低温冷冻柜 青岛海尔特种电冰柜有限公司;DW-HL388超低温冷冻存储箱 中科美菱低温科技有限责任公司;184 T4 USB温度记录仪德国德图公司;RC-4HA/C迷你型温湿度记录仪 江苏省精创电气股份有限公司;CR-400/410色彩色差 美能达(中国)投资有限公司;FG2-B便携式pH计 梅特勒-托利多仪器(上海)有限公司;HH-ZK2恒温水浴锅巩义市予华仪器有限责任公司;YYW-2应变控制式无侧限压力仪 南京土壤仪器有限公司;Eclipse CI光学显微镜、NMI20-025V-I成像系统 日本尼康公司;NMI20-025V-I核磁共振成像分析仪 苏州纽迈分析仪器股份有限公司;TA.XT 2i/50质构仪 英国Stable Micro Systems公司。
1.3.1 样品处理
在4 ℃的冷库中分别将鮰鱼、鲈鱼和鳜鱼敲击致晕,去除内脏,流水清洗干净后,放置备用。将每种待冷冻鱼随机分成3 组,每组4 条,然后进行如下处理。
将温度记录仪探头分别插入每种鱼的背部中,然后将每种鱼分别放置于-30 ℃平板冷冻、-80 ℃冰箱、-80 ℃液氮速冻柜中进行冷冻处理,其中-30 ℃平板冷冻和-80 ℃冰箱冷冻24 h(即1 440 min),-80 ℃液氮则用液氮速冻柜控制冷冻30 min;然后取出鮰鱼、鲈鱼、鳜鱼样品称质量并置于4 ℃进行解冻;待解冻完成后,分别取每种冷冻方式每种鱼背部肉的测定各种指标。
1.3.2 组织切片制作及微观结构分析
参考赵玉华等[8]的方法,取每种样品背部鱼肉(尺寸为3 mm×3 mm×6 mm)制作冷冻组织切片,将新鲜组织固定于4 g/100 mL多聚甲醛24 h以上,然后从固定液取出组织修平整,依次放入10 mL质量分数为15%、30%的蔗糖溶液中,于4 ℃冰箱脱水沉底,取出脱水组织稍吸干表面水,切面朝上置于包埋台上,组织周围滴上O.C.T.包埋剂,将包埋台放在切片机的速冻台上速冻包埋,待O.C.T.变白变硬后,将包埋台固定于切片机上,先粗切织面,待修切平整后即可开始切片,切片厚度8~10 μm,然后将干净的载玻片平放于切片上方,即可将组织贴于载玻片上,-20 ℃保存备用。
切片HE染色:切片用4 g/100 mL多聚甲醛固定15 min,磷酸盐缓冲液漂洗3 次,5 min/次,然后用Harris苏木精染3~8 min,自来水洗,1%盐酸-乙醇分化数秒,自来水冲洗后采用体积分数0.6%氨水返蓝,流水冲洗;再将切片置于伊红染液中染色1~3 min;然后将切片依次放入95%(体积分数,后同)乙醇溶液5 min、95%乙醇溶液5 min、无水乙醇5 min、无水乙醇5 min、二甲苯5 min、二甲苯5 min,脱水呈透明,从二甲苯中取出稍晾干,中性树胶封片;用Eclipse CI光学显微镜镜检,最后用NMI20-025V-I成像系统采集图像进行分析。用ImagePro Plus 6.0软件处理所得图片。
1.3.3 解冻损失率测定
不同冷冻方式处理之后,参考刘欢[9]、Mortensen[10]等的方法,用滤纸吸去解冻后鮰鱼、鲈鱼、鳜鱼鱼体表面的水分并称取质量,按照公式(1)计算解冻损失率。
式中:m0表示冻结鱼肉的质量/g;m1表示解冻后鱼肉的质量/g。
1.3.4 加压失水率测定
不同冷冻方式处理后,参考董开成[11]的方法,分别称取2 g左右的白肉,准备大小为4 cm×4 cm的纱布。先称取纱布质量(m1/g),再称取纱布与样品的总质量(m2/g),纱布对折包裹住样品,向其上下各放8 层滤纸使样品置于滤纸中心位置,并放在YYW-2型应变控制式无侧限压力仪的加压板中心,转动摇把使试样与加压板刚好接触,停止转动摇把,将测力计的百分表读数调至零点,然后进行手动加压,顺时针转动摇把直至测力计的百分表读数为145,开始计时并维持此数值5 min,测试结束后,逆时针转动摇把,取下试样,剥去上下8 层滤纸,称量加压后纱布与样品的总质量(m3/g)。加压失水率的计算见公式(2)。
1.3.5 蒸煮损失率测定
不同冷冻方式处理后,参考王凤玉[12]、Kiliç[13]等的方法,取解冻后的样10 g左右(m1/g)放入保鲜袋中,置于85 ℃水浴锅中进行蒸煮,25 min后取出,冷却至室温,用滤纸拭去鱼肉表面的水分,再称质量(m2/g),按公式(3)计算蒸煮损失率。
1.3.6 pH值的测定
经过不同冷冻方式处理后,用pH值标准校正缓冲液校正便携式pH计,然后用蒸馏水冲洗探头,用滤纸擦拭干净,用便携式pH计探头插入鱼肉中,分别测定解冻后鮰鱼、鲈鱼、鳜鱼的pH值。
1.3.7 色泽测定
不同冷冻方式处理后,参考胡亚芹等[14]的方法,将解冻后鮰鱼、鲈鱼、鳜鱼切成1 cm×1 cm×1 cm大小的块状,去皮,用色度测定仪测定样品的亮度L*、红绿度a*、黄蓝度b*值,白度按公式(4)计算。
1.3.8 质构特性的测定
不同冷冻方式处理后,参考宋敏等[7]的方法,将解冻后鮰鱼、鲈鱼、鳜鱼切成1 cm×1 cm×1 cm大小的块状,并将鱼块置于质构仪A/CKB探头下进行韧性(剪切力)的测定,力臂25 kg、测前速率5.0 mm/s、测中速率1.0 mm/s、测后速率5.0 mm/s、压缩形变50%,每组平行测定6 次。
1.3.9 低场核磁共振测定样品水分分布
使用NMI20-025V-I核磁共振分析及成像系统测定样品,研究经过不同温度冷冻方式处理后,解冻样品水分与组织结合程度和水分分布情况。核磁共振分析参数为:共振频率21.3 MHz、磁体强度0.55 T、线圈直径60 mm、磁体温度32 ℃;将新鲜和-60、-80、-100 ℃鮰鱼样品切成2 cm×2 cm×2 cm鱼肉块,称质量,保鲜膜包裹后,放置于室温下使样品的温度与环境的温度达到平衡,然后放入核磁共振分析仪中进行测定;使用Q-FID及标准品对机器进行校正,然后使用CPMG脉冲序列采集样品T2(自旋-自旋弛豫时间)信号,硬脉冲CPMG序列参数:采样频率SW为100 kHz、模拟增益RG1为20.0 dp、90°射频脉宽(P1)为8.00 μs、数字增益DRG1为3、采样点个数TD为399 998、增益参数PRG为1、重复采样间隔时间TW为40 00 ms、累加次数NS为4、180°射频脉宽P2为16.00 μs、回波时间TE为0.400 ms、回波个数NECH为10 000。每组样品3 个平行,每个平行样测3 次[15]。
CPMG测试后的样品进行MSE序列成像测试,运用核磁共振成像(magnetic resonance imaging,MRI)软件及MSE多层自旋回波序列采集样品冠状面质子密度像,成像系统分析参数为:成像厚度5 mm、MRI视野FOVRead=100 mm、FOVPhase=80 mm、Averages=4、TR=500 ms、TE=20 ms、Slices=1、Slice Width=3.0 mm。
采用SPSS 20.0软件进行数据处理,采用Duncan’s法进行差异显著性分析,P<0.05表示差异显著,采用GraphPad Prism 5.0软件作图。
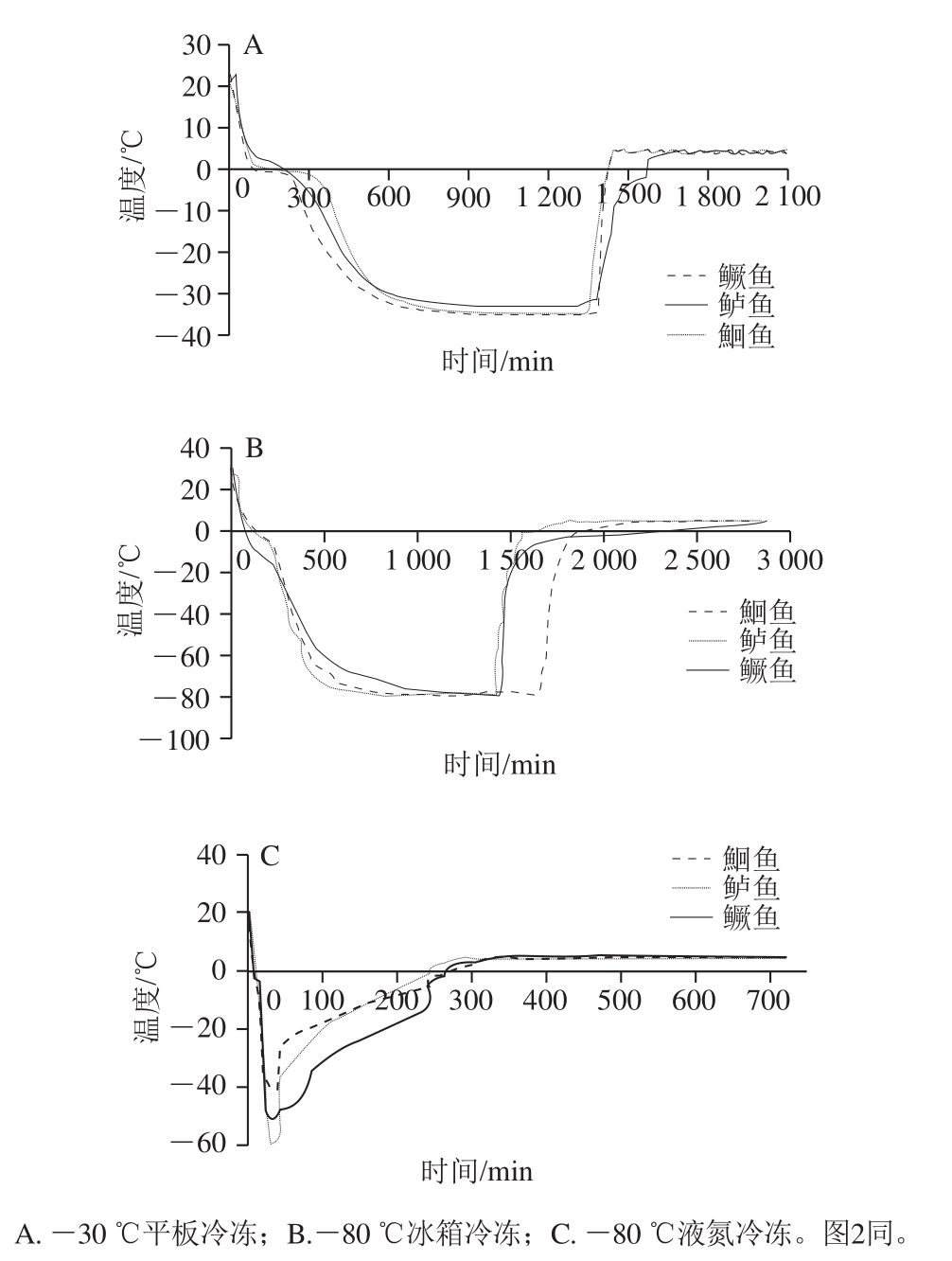
图1 不同冷冻方式淡水鱼的冷冻解冻过程
Fig. 1 Freezing and thawing curves of freshwater fish with different freezing methods
如图1所示,同种淡水鱼经过不同冷冻方式处理其冷冻解冻温度曲线明显不同;其中-80 ℃液氮冷冻处理的降温速率最大,-80 ℃冰箱冷冻降温速率次之,-30 ℃平板冷冻降温速率最小,表明-80 ℃液氮较另两种冷冻方式可以更快地通过最大冰晶生成带(-5~0 ℃),使得肌肉组织中形成小而多且均一的冰晶,减小冰晶对肌肉组织的破坏[16];在降温过程中,-30 ℃平板冷冻和-80 ℃冰箱冷冻处理的样品都能分别降到-30 ℃和-80 ℃,而30 min液氮冷冻样品则不能降到目标温度,其中鲈鱼最低降到了接近-60 ℃。在解冻过程中,-30 ℃平板和-80 ℃液氮冷冻样品在4 ℃解冻约12 h(约720 min),而-80 ℃冰箱冷冻样品解冻约24 h(约1 440 min)。-30 ℃平板冷冻中鳜鱼降温终点略低于另外两种淡水鱼;-80 ℃冰箱冷冻降温过程中,鲈鱼降温速率小于另外两种淡水鱼,鮰鱼解冻升温过程出现迟滞现象,这可能是鱼体较大引起的;-80 ℃液氮冷冻,鮰鱼的降温速率最小;不同淡水鱼经同种冷冻方式处理后其降温速率曲线基本一致,其较小差异性可能是物种间差异导致的。
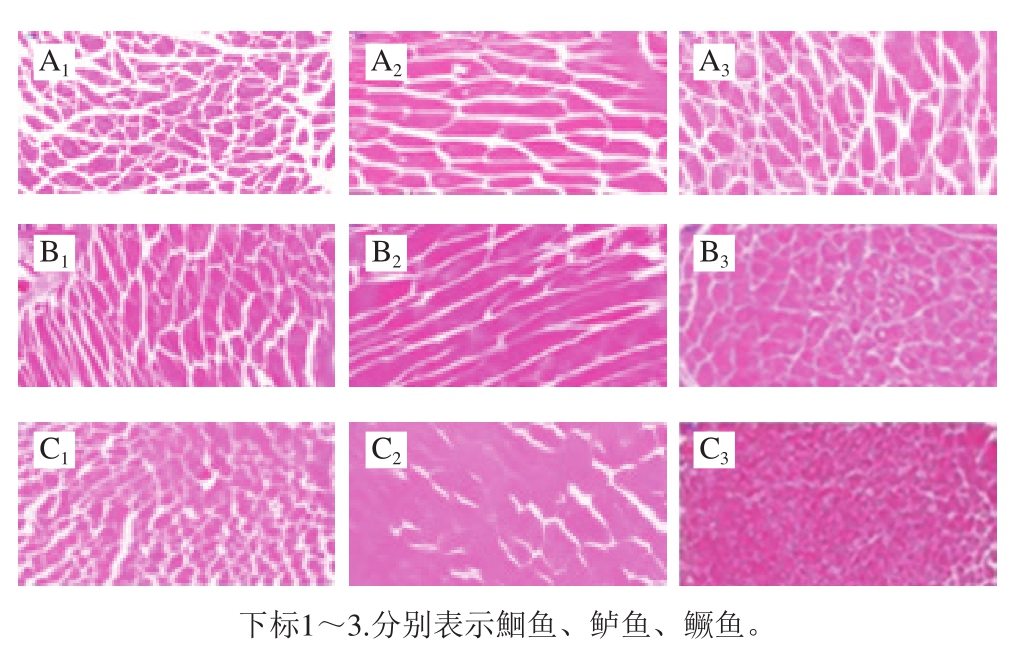
图2 不同冷冻方式对淡水鱼微观组织结构的影响
Fig. 2 Effect of different freezing methods on microstructure of freshwater fish
由图2可知,不同冷冻方式下的同种淡水鱼微观组织结构存在差异;同种淡水鱼经过-30 ℃平板冷冻、-80 ℃冰箱冷冻、-80 ℃液氮冷冻处理后,样品微观组织结构的细胞间隙都呈现依次减小趋势,-30 ℃平板冷冻样品的肌原纤维细胞间隙间冰晶大,对肌原纤维细胞产生严重的损伤,-80 ℃冰箱冷冻样品其细胞间隙和冰晶产生的损伤次之,而-80 ℃液氮处理样品其肌原纤维间较为整齐致密,细胞也较完整,其细胞间隙间冰晶小且均一;这可能是-80 ℃液氮处理较其他两种冷冻降温速率快,形成小而多且均一的冰晶,其对肌肉肌原纤维造成的破坏程度相对较小,这在向迎春[17]和Tinacci[18]等的研究中都得到了证实,同时鲁珺等[6]的研究结果也表明,在冷冻过程中样品组织在低于玻璃化转变温度条件下进行冷冻时,样品呈现部分玻璃化状态对细胞结构具有保护作用,因此-80 ℃液氮处理较其他两种冷对微观组织结构的损伤最小,并且通过冷冻解冻过程的温度速率曲线变化也可以得到证实。综合分析可知,不同冷冻方式处理对样品组织结构产生不同程度损伤,其中-30 ℃平板冷冻最大,-80 ℃冰箱冷冻次之,-80 ℃液氮冷冻最小。
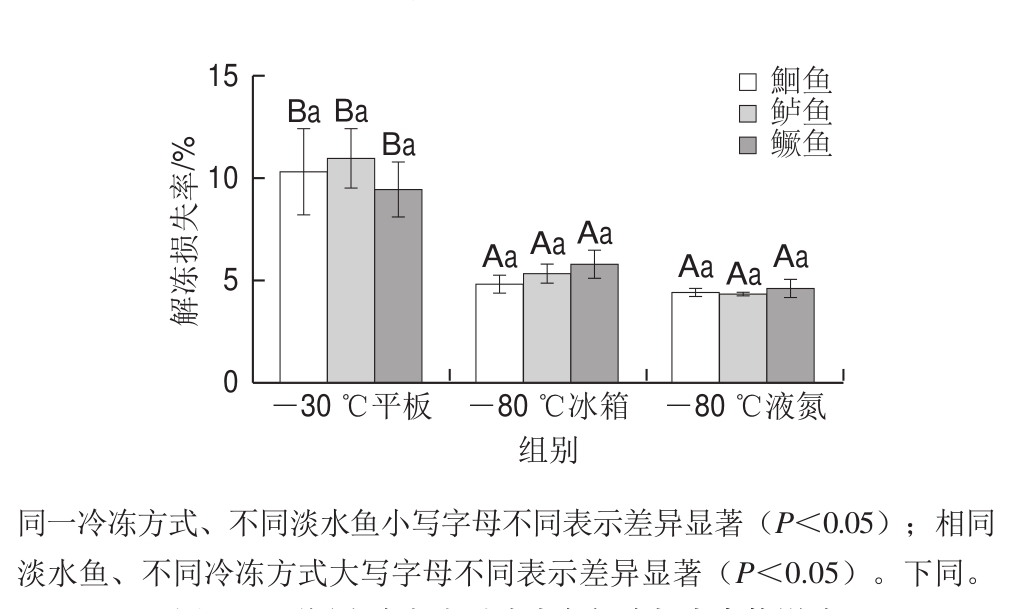
图3 不同冷冻方式对淡水鱼解冻损失率的影响
Fig. 3 Effect of different freezing methods on thawing loss percentage of freshwater fish
如图3所示,对于同种淡水鱼,-30 ℃平板冷冻处理组解冻损失率显著大于-80 ℃冰箱、-80 ℃液氮处理组,但-80 ℃冰箱和-80 ℃液氮处理组之间差异不显著。可能是因为-80 ℃冰箱、-80 ℃液氮较-30 ℃平板冷冻降温速率更快,快速冷冻能够使样品快速通过最大冰晶生成带形成小而多的冰晶,且冰晶分布均匀,对肌肉组织破坏较小[15,19];而-30 ℃平板冷冻相对慢速冷冻形成的较大冰晶破坏了肌肉纤维结构的紧密性,同时使得肌原纤维细胞内部水分流出,导致汁液流失且解冻中肌肉组织对水分的重吸收能力减弱[20],所以-30 ℃平板冷冻样品其解冻损失率显著大于-80 ℃冰箱和-80 ℃液氮。对于不同淡水鱼经过同种冷冻方式处理后其解冻损失率无显著性差异(P>0.05),这可能是因为相对于物种间的差异性,冷冻方式对组织结构的影响更大,所以鱼的品种对解冻损失率不产生显著性影响。
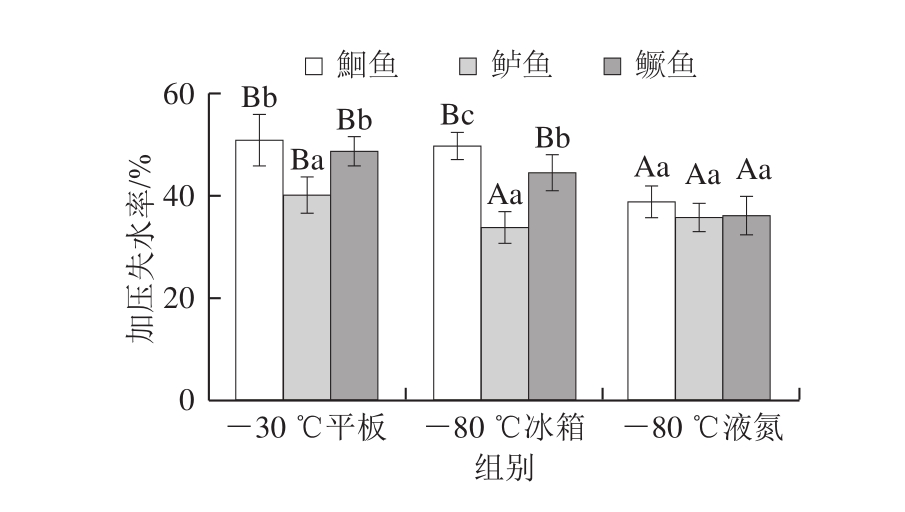
图4 不同冷冻方式对淡水鱼加压失水率的影响
Fig. 4 Effect of different freezing methods on pressure-induced water loss percentage of freshwater fish
如图4所示,不同冷冻方式对同种淡水鱼加压失水率影响差异显著(P<0.05);鮰鱼、鳜鱼加压失水率:-30 ℃平板冷冻、-80 ℃冰箱组>-80 ℃液氮组,而-30 ℃平板冷冻组和-80 ℃冰箱组间不存在显著性差异;鲈鱼加压失水率:-30 ℃平板冷冻组>-80 ℃冰箱组、-80 ℃液氮组,而-80 ℃冰箱组和-80 ℃液氮组之间不存在显著性差异。综合分析可知,-30 ℃平板冷冻较-80 ℃冰箱和-80 ℃液氮处理对样品组织结构影响大,Wang Hang等[21]研究发现慢速冷冻形成的较大冰晶对肌肉组织产生较强的机械破坏作用,使得肌肉组织对水分的束缚能力减弱,这可能是造成-30 ℃平板冷冻处理加压失水率显著大于其他两种冷冻方式的原因。
不同淡水鱼同种冷冻方式处理后,鮰鱼和鳜鱼的加压失水率显著大于鲈鱼(P<0.05);-80 ℃液氮处理组的不同淡水鱼间不存在显著性差异(P>0.05),表明-30 ℃平板冷冻和-80 ℃冰箱对不同淡水鱼的加压失水率影响程度不同,而-80 ℃液氮对不同淡水鱼的加压失水率不产生显著影响。
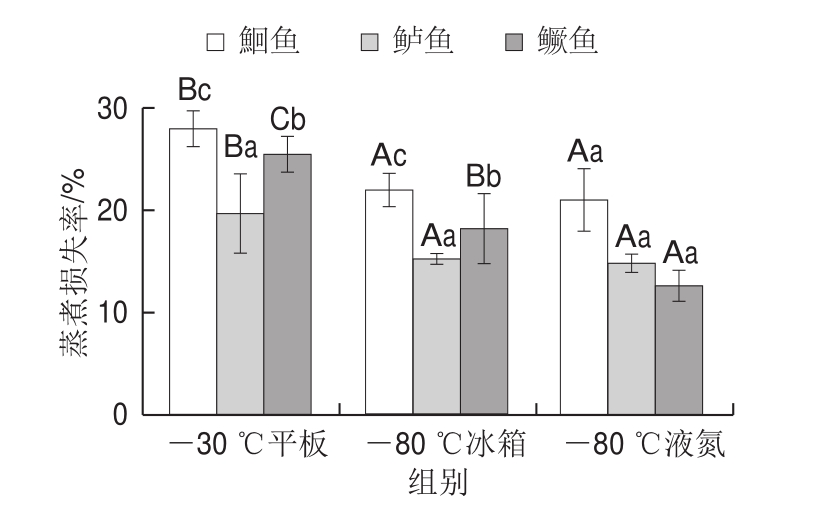
图5 不同冷冻方式对淡水鱼蒸煮损失率的影响
Fig. 5 Effect of different freezing methods on cooking loss rate of freshwater fish
如图5所示,同种淡水鱼不同冷冻方式处理后,不同淡水鱼蒸煮损失率存在显著性差异(P<0.05),鮰鱼和鲈鱼的蒸煮损失率:-30 ℃平板组>-80 ℃冰箱组、-80 ℃液氮组,而-80 ℃冰箱和-80 ℃液氮处理组之间不存在显著性差异性;鳜鱼的蒸煮损失率按-30 ℃平板组、-80 ℃冰箱组、-80 ℃液氮组依次呈现减小趋势。综合分析可知,-30 ℃平板冷冻较另外两种冷冻方式对样品组织结构影响大,使得-30 ℃平板冷冻处理的蒸煮损失率显著大于其他两种冷冻方式;这是由于在解冻过程中,肌肉蛋白的构象发生部分改变,同时-30 ℃平板冷冻形成的较大冰晶破坏了肌肉组织细胞,使其持水力下降[22],且崔珺[23]研究发现,当较大冰晶对鱼肉肌肉产生损伤时,会使得组织暴露在空气中的面积更大,加快了水分向细胞外扩散的速度;宋敏等[7]研究也发现,蒸煮中肌肉组织易发生聚合,降低了肌肉的持水力,所以同种淡水鱼的蒸煮损失率-30 ℃平板冷冻处理大于另外两种冷冻方式,这与前面解冻损失率变化基本一致。不同淡水鱼经同种冷冻方式后其蒸煮损失率存在显著性差异(P<0.05),-30 ℃平板、-80 ℃冰箱组蒸煮损失率均为:鮰鱼>鳜鱼>鲈鱼;而-80 ℃液氮处理其蒸煮损失率为:鮰鱼>鲈鱼、鳜鱼,鲈鱼和鳜鱼的蒸煮损失率不存在显著性差异(P>0.05),这可能是由于物种差异性产生的,具体原因还需要进一步研究。

图6 不同冷冻方式对淡水鱼pH值的影响
Fig. 6 Effect of different freezing methods on pH of freshwater fish
如图6所示,同种淡水鱼经不同冷冻方式后其pH值整体上不存在显著性差异性(P<0.05)。不同淡水鱼经过同种冷冻方式处理后其pH值存在显著性差异(P<0.05),这可能是由物种差异性产生的。-30 ℃平板、-80 ℃液氮冷冻组pH值:鳜鱼>鮰鱼>鲈鱼;-80 ℃冰箱组:鮰鱼、鳜鱼>鲈鱼,而鮰鱼与鳜鱼不存在差异性。

图7 不同冷冻方式对淡水鱼白度的影响
Fig. 7 Effect of different freezing methods on whiteness of freshwater fish
如图7所示,淡水鱼经不同冷冻方式后其白度存在显著性差异(P<0.05),鮰鱼、鲈鱼、鳜鱼白度:-30 ℃平板冷冻显著高于-80 ℃冰箱和-80 ℃液氮,这可能是-30 ℃平板冷冻组冰晶对肌肉组织产生机械破坏作用,使水分渗出鱼肉表面形成水膜,光的反射或折射增强[14],最终使得白度增大;而-80 ℃冰箱和-80 ℃液氮组之间不存在显著性差异,这可能是因为形成小而多的冰晶对肌肉组织的损坏较小,水分向肌肉表面流失的相对较少,因此二者白度小于-30 ℃平板冷冻组且不存在显著性差异。不同淡水鱼经同种冷冻方式后其白度存在显著性差异(P<0.05),各组白度均是:鮰鱼显著大于鲈鱼和鳜鱼,而鲈鱼与鳜鱼白度无显著性差异,这可能是由于物种差异性产生的,具体原因还需要进一步的研究。

图8 不同冷冻方式对淡水鱼韧性的影响
Fig. 8 Effect of different freezing methods on toughness of freshwater fish
如图8所示,同种淡水鱼经不同冷冻方式后其韧性存在显著性差异(P<0.05),整体来说,-30 ℃平板组<-80 ℃冰箱组<-80 ℃液氮组,这可能是因为冷冻速率不同形成的冰晶对细胞产生的破坏程度不同;-30 ℃平板冷冻速率慢,其对细胞膜的破坏较大,使得肌肉组织持水能力降低,这在前面解冻损失率、加压失水率和蒸煮损失率的结果中也得到了证实,水分含量的减少可能会使得作用于肌肉组织上的剪切力不能得到较好缓冲[24],因此其剪切力(韧性)最小。
不同淡水鱼经同种冷冻方式处理后其韧性存在显著性差异(P<0.05),-30 ℃平板冷冻和-80 ℃冰箱处理组中鮰鱼、鲈鱼、鳜鱼依次呈现显著增大趋势;-80 ℃液氮处理组中鳜鱼显著大于鮰鱼和鲈鱼,而鮰鱼和鲈鱼间不存在差异性,这可能是物种差异性产生的。
低场核磁共振技术多以氢核(1H)为研究对象,1H核以非辐射方式从高能态转变为低能态的过程称为弛豫;在肉及肉制品中弛豫时间的测量多用H质子的横向弛豫时间T2来表示。T2的分布可以表示肉中存在多种性质的水分,T2越短表明水分与底物结合的越紧密,反之,水分则越自由;其中T21(1~10 ms)代表与大分子结合的结合水,T22(30~100 ms)代表不可移动的水,T23(>100 ms)代表自由水[25]。
表1 不同淡水鱼解冻后的T2所占面积比(A2)
Table 1 Ratio ofT2peak area in frozen-thawed freshwater fish (A2)

注:小写字母不同表示不同淡水鱼、同种冷冻方式间差异显著(P<0.05);同列大写字母不同表示同种淡水鱼、不同冷冻方式间差异显著(P<0.05)。
A21/% A22/% A23/%鮰鱼 鲈鱼 鳜鱼 鮰鱼 鲈鱼 鳜鱼 鮰鱼 鲈鱼 鳜鱼-30 ℃平板 4.39±0.59Bb4.54±1.23Bb4.13±0.40Ba 93.29±0.48Ab92.91±3.08Aa94.57±0.54Ac 2.42±0.14Bc1.13±0.18Ca1.31±0.54Bb-80 ℃冰箱 2.51±0.29Aa3.54±0.26Ab3.01±0.32Ab 95.79±1.07Bb93.50±1.97Aa96.76±0.51Bc 2.39±0.65Bc1.04±0.59Bb0.17±0.07Aa-80 ℃液氮 2.50±0.25Aa3.22±0.19Ac2.99±0.27Ab 95.73±0.99Ba96.40±0.19Bb96.90±0.30Bc 1.80±0.07Ac0.41±0.05Ab0.18±0.07Aa组别
如表1所示,从T2所占面积可知,鱼肉样品中不可移动水(T22)的含量相对较高,结合水和自由水的含量相对较少,这与Sánchez-Alonso等[26]的研究结果基本一致。与其他两个冷冻组相比,经-30 ℃平板冷冻后样品不可移动水(T22)含量降低,自由水(T23)含量升高,这可能是因为-30 ℃平板冷冻形成的冰晶较-80 ℃冰箱冷冻和-80 ℃液氮冷冻处理对样品肌原纤维结构破坏程度更大,其造成细胞膜表面形成许多通道,使得存在于肌原纤维细胞间和肌原纤维细胞内的不可移动水(T22)部分转变为自由水(T23)[27],类似的结果在王尊[28]、杨宏旭[29]等的研究中也得到证实。不同淡水鱼经同种冷冻方式后其T2含量也存在差异,这可能是因为物种间的差异性所导致的。

图9 不同冷冻方式处理的不同淡水鱼MRI伪彩图
Fig. 9 MRI pseudo-color images of different freshwater fish with different freezing treatments
MRI是利用磁场和射频脉冲使样品中的氢核振动发出射频信号,然后经计算机处理后成像的一种技术,通过该技术可以获得肌肉中水分的高分辨率MRI,该图像能直观反映水分的分布,若信号值强则显红色,无信号值则显蓝色,同时其质子密度越高,MRI图像中亮度越强,样品中水分含量越高[30]。由图9可知,同种淡水鱼经不同冷冻方式后其质子密度加权像亮度存在差异,在实验所用3 种鱼中,-30 ℃平板冷冻处理的样品整体偏向于亮绿色,而-80 ℃冰箱和-80 ℃液氮处理组样品整体偏向于蓝绿色且二者差异不明显。表明-30 ℃平板冷冻处理组样品水分含量高,持水性减弱,汁液流失严重;而-80 ℃冰箱和-80 ℃液氮处理组水分含量低且持水性较好,这在廖媛媛[15]、梁钻好[27]等的研究中也有相关发现。不同淡水鱼经同种冷冻方式后其质子密度加权像亮度差异不明显。
经过-30 ℃平板冷冻、-80 ℃冰箱冷冻和-80 ℃液氮冷冻处理后,同种淡水鱼其解冻损失率、加压失水率、蒸煮损失率均呈现下降趋势,pH值整体上不存在显著性差异性,韧性呈现增大趋势,细胞间隙呈现降低趋势。相比之下,-30 ℃平板组白度最大,不可移动水含量最低,自由水含量最高。同种冷冻方式不同淡水鱼间的指标差异性较小。本研究结果表明:-30 ℃平板冷冻较-80 ℃冰箱冷冻和-80 ℃液氮冷冻处理对淡水鱼的品质影响较大,从冷冻速率和品质角度考虑,选择-80 ℃冰箱冷冻和-80 ℃液氮冷冻处理更有利,这为不同冷冻方式在水产品在流通、运输、贮藏方面进一步研究提供了一定的参考。
[1] 唐春江. 斑点叉尾鮰鱼速冻鱼片生产工艺优化研究[D]. 长沙: 湖南农业大学, 2009: 1.
[2] 宋丽丽, 毛金林, 陈杭君, 等. 冻藏对斑点叉尾鮰鱼片蛋白质冷冻变性和肌原纤维超微结构的影响[J]. 中国食品学报, 2013, 13(1): 61-67.DOI:10.16429/j.1009-7848.2013.01.017.
[3] 王亚会, 王锡昌, 王帅, 等. 水产品新鲜及腐败程度的评价指标[J]. 食品与发酵工业, 2015, 41(10): 240-246. DOI:10.13995/j.cnki.11-1802/ts.201510044.
[4] 叶琼娟, 余铭, 张全凯, 等. 速冻技术在食品工业中的应用研究进展[J]. 农产品加工(学刊), 2012(12): 97-100. DOI:10.3969/j.issn.1671-9646(X).2012.12.026.
[5] 王旋, 张鹏, 杨方, 等. 酶法脱脂对鮰鱼品质及干燥特性的影响[J].食品工业科技, 2015, 36(16): 100-103. DOI:10.13386/j.issn1002-0306.2015.16.012.
[6] 鲁珺, 余海霞, 杨水兵, 等. 液氮速冻对银鲳鱼品质及微观结构的影响[J]. 现代食品科技, 2015, 31(4): 210-216; 94. DOI:10.13982/j.mfst.1673-9078.2015.4.034.
[7] 宋敏, 许艳顺, 夏文水, 等. 冻结方式对鮰鱼片品质的影响[J]. 食品科技, 2017(8): 154-159. DOI:110.13684/j.cnki.spkj.2017.08.029.
[8] 赵玉华, 牛玲玲, 李永红, 等. 板栗果实显微结构冷冻切片制作方法的建立[J]. 保鲜与加工, 2013, 13(5): 43-48. DOI:10.3969/j.issn.1009-6221.2013.05.009.
[9] 刘欢, 陈雪, 宋立玲, 等. 不同解冻方式对鲐鱼鲜度及品质的影响[J]. 食品科学, 2016, 37(10): 259-265. DOI:10.7506/spkx1002-6630-201610044.
[10] MORTENSEN M, ANDERSEN H J, ENGELSEN S B, et al. Effect of freezing temperature, thawing and cooking rate on water distribution in two pork qualities[J]. Meat Science, 2006, 72(1): 34-42. DOI:10.1016/j.meatsci.2005.05.027.
[11] 董开成. 不同低温预处理对小黄鱼贮藏过程中品质的影响[D].杭州: 浙江大学, 2015: 1.
[12] 王凤玉, 曹荣, 赵玲, 等. 解冻方式对冷冻秋刀鱼品质的影响[J].食品安全质量检测学报, 2015, 6(11): 4584-4590.
[13] KILIÇ B, ŞIMŞEK A, CLAUS J R, et al. Encapsulated phosphates reduce lipid oxidation in both ground chicken and ground beef during raw and cooked meat storage with some influence on color, pH, and cooking loss[J]. Meat Science, 2014, 97(1): 93-103. DOI:10.1016/j.meatsci.2014.01.014.
[14] 胡亚芹, 胡庆兰, 杨水兵, 等. 不同冻结方式对带鱼品质影响的研究[J]. 现代食品科技, 2014, 30(2): 23-30. DOI:10.13982/j.mfst.1673-9078.2014.02.020.
[15] 廖媛媛, 欧昌荣, 汤海青, 等. 三种冻结方式对大黄鱼品质的影响[J].现代食品科技, 2014, 30(7): 218-223; 186. DOI:186.10.13982/j.mfst.1673-9078.2014.07.042.
[16] KAALE D L, EIKEVIK T M, RUSTAD T, et al. Ice crystal development in pre-rigor Atlantic salmon fi llets during; superchilling process and following storage[J]. Food Control, 2013, 31(2): 491-498.DOI:10.1016/j.foodcont.2012.11.047.
[17] 向迎春, 黄佳奇, 杨志坚, 等. 冻结方式对凡纳滨对虾贮藏中组织冰晶及品质的影响[J]. 食品工业科技, 2018, 39(5): 280-287.DOI:10.13386/j.issn1002-0306.2018.05.052.
[18] TINACCI L, ARMNI A, GUIDI A, et al. Histological discrimination of fresh and frozen/thawed fish meat: European hake (Merluccius merluccius) as a possible model for white meat fi sh species[J]. Food Control, 2018, 92: 154-161. DOI:10.1016/j.foodcont.2018.04.056.
[19] 杨志坚. 液氮速冻对舌鳎和梭子蟹品质的影响[D]. 杭州: 浙江大学,2017: 15.
[20] 张南海. 不同冻结方式、贮藏温度和解冻方式对彭泽鲫品质的影响[D]. 南昌: 南昌大学, 2018: 29-30.
[21] WANG Hang, LUO Yongkang, SHI Ce, et al. Effect of different thawing methods and multiple freeze-thaw cycles on the quality of common carp (Cyprinus carpio)[J]. Journal of Aquatic Food Product Technology, 2015, 24(2): 153-162. DOI:10.1080/10498850.2013.763884.
[22] LIU D, LIANG L, XIA W, et al. Biochemical and physical changes of grass carp (Ctenopharyngodon idella) fillets stored at -3 and 0 ℃[J]. Food Chemistry, 2013, 140(1): 105-114. DOI:10.1016/j.foodchem.2013.02.034.
[23] 崔珺. 速冻方式和贮藏温度对带鱼品质影响的研究[D]. 舟山: 浙江海洋学院, 2011: 15.
[24] LEE J, FONG Q, PARK J W. Effect of pre-freezing treatments on the quality of Alaska pollock fi llets subjected to freezing/thawing[J]. Food Bioscience, 2016, 16: 50-55. DOI:10.1016/j.fbio.2016.09.003.
[25] 蓝蔚青, 车旭, 许巧玲, 等. 银杏叶提取液与竹醋液流化冰对鲳鱼冰藏期间品质变化的影响[J]. 食品科学, 2017, 38(23): 249-256.DOI:10.7506/spkx1002-6630-201723040.
[26] SÁNCHEZ-ALONSO I, MORENO P, CARECHE M. Low field nuclear magnetic resonance (LF-NMR) relaxometry in hake(Merluccius merluccius L.) muscle after different freezing and storage conditions[J]. Food Chemistry, 2014, 153(12): 250-257. DOI:10.1016/j.foodchem.2013.12.060.
[27] 梁钻好, 陈海强. 梁凤雪, 等. 基于LF-NMR的液浸速冻牡蛎品质研究[J/OL]. 食品科学, (2019-01-04)[2019-06-04]. http://kns.cnki.net/kcms/detail/11.2206.TS.20190102.1529.111.html.
[28] 王尊, 谢晶, 钱韻芳. 带鱼冷藏过程中品质变化与水分迁移的相关性[J]. 食品科学, 2017, 38(13): 257-262. DOI:10.7506/spkx1002-6630-201713042.
[29] 杨宏旭. 不同低温贮藏对青鱼肉品质的影响[D]. 无锡: 江南大学,2016: 26-28.
[30] MARCONE M F, WANG S, ALBABISH W, et al. Diverse food-based applications of nuclear magnetic resonance (NMR) technology[J].Food Research International, 2013, 51(2): 729-747. DOI:10.1016/j.foodres.2012.12.046.
Effect of Different Freezing Methods on the Quality of Freshwater Fish
ZHOU Junpeng, ZHU Meng, ZHANG Wei, et al. Effect of different freezing methods on the quality of freshwater fi sh[J].Food Science, 2019, 40(17): 247-254. (in Chinese with English abstract) DOI:10.7506/spkx1002-6630-20180913-137.http://www.spkx.net.cn