
图1 空白甲醇(A)、乙酰丙酮(B)、乙酰丙酮钛(C)气相色谱图
Fig. 1 Gas chromatograms of methanol (A), AA (B), and TAA (C)
食品包装中的印刷油墨及上光油虽然涂覆在包装外层,不与食品直接接触,但会通过材料印刷过程中的背面蹭脏及食品存储过程中的迁移进入食品[1-6],对人体健康造成潜在威胁[7-10]。
乙酰丙酮钛是一种以乙酰丙酮为媒介的螯合物,它添加在油墨或上光油中能够增强与承印物表面的附着力[11-14]。目前,关于乙酰丙酮金属螯合物的研究主要集中在乙酰丙酮金属螯合物的合成、应用等,而鲜见关于乙酰丙酮金属螯合物的检测、安全性的研究等。乙酰丙酮又名2,4-戊二酮,用途广泛,通过吸入、摄入或经皮肤吸收对身体有害,中毒表现为头痛、恶心和呕吐等[15-22]。2006年,欧洲油墨协会指出[23]:由于乙酰丙酮具有基因毒性,已经从“能够作为食品添加剂的清单”中清除,并且指出乙酰丙酮通常不是油墨中的构成组分,但是在使用含有乙酰丙酮钛的油墨时可能会释放出乙酰丙酮。乙酰丙酮的常用检测方法有气相色谱法[24-25]、高效液相色谱法[26-30]、紫外吸收光度法和化学法[29],而鲜见有关于乙酰丙酮的气相色谱-质谱和液相色谱-质谱检测方法的报道,气相色谱-质谱法和液相色谱-质谱法相较于上述方法有更强的定性、定量的优势。
本实验采用液相色谱-质谱法、气相色谱-质谱法对标准溶液中乙酰丙酮钛的存在形式进行了鉴别,然后对样品中的乙酰丙酮含量和钛含量进行对比分析,通过傅里叶红外光谱法对乙酰丙酮钛的紫外照射稳定性和热稳定性进行研究。本研究对油墨、涂料中乙酰丙酮钛的分析检测提供参考依据,为食品印刷包装材料中乙酰丙酮的迁移和安全研究提供一定的参考依据。
低密度聚乙烯薄膜(薄膜的厚度为(0.050±0.001)mm)珠海市德燊环保包装有限公司;WA2U-593C凹印油墨广州市富林特有限公司;高滑型上光油 中山市安姆科(软包装)有限公司。
乙酰丙酮标准品 北京百灵威科技有限公司;乙酰丙酮钛标准品 广东翁江化学试剂有限公司;钛标液 国家有色金属及电子材料分析测试中心;甲醇(色谱纯) 美国Merck投资(中国)有限公司;乙醇、乙腈、甲醇(均为色谱纯) 瑞典Oceanpak公司;硝酸、高氯酸、氢氟酸(均为分析纯) 广州化学试剂有限公司。
API 3200液相色谱-质谱联用仪(配有电喷雾离子源及MutiquantTM数据处理系统) 美国AB SCIEX公司;Alliance 2695型高效液相色谱仪(配有2996二极管阵列检测器) 美国Waters科技有限公司;EQUINOX 55型傅里叶红外光谱仪 布鲁克(北京)科技有限公司;7890A-5975C气相色谱-质谱联用仪、5100 VDV等离子体发射光谱仪 美国安捷伦有限公司;ZF-90暗箱式紫外投射仪(254 nm时功率为60 W) 上海宝山顾村电光仪器厂;flexiproof 100凹版打样机 英国RK公司;GZX-9420MBE鼓风式烘箱 上海博讯有限公司;高速离心机南京科技发展有限公司。
1.3.1 乙酰丙酮和乙酰丙酮钛的标准溶液配制
称取乙酰丙酮和乙酰丙酮钛标准品50 mg,用甲醇定容至50 mL,配制成1 000 mg/L的标准储备液,密封后将其放置于4 ℃冰箱中冷藏保存,使用时用甲醇稀释成所需质量浓度的标准溶液。
1.3.2 钛标准溶液的配制
取质量浓度为100 mg/L的钛标液10 mL,用超纯水定容至100 mL,配制成质量浓度为10 mg/L的标准储备液,密封放置于4 ℃冰箱中冷藏保存,使用时用超纯水稀释成所需质量浓度的标准溶液。
1.3.3 样品中乙酰丙酮的提取
对于呈液体状的油墨和上光油,取5 g左右样品至洁净的玻璃培养皿中并将其铺匀,然后将其放置于60 ℃鼓风干燥箱中,2 h后烘干固化成膜取出。称取烘干后的样品0.05 g于试管中,加入10 mL乙醇溶剂,在60 ℃条件下超声提取1 h[31-33]。对提取液进行高速离心15 min,温度下限20 ℃、上限25 ℃,离心机转速1 000 r/min。取上层清液过0.22 μm滤膜后上HPLC检测,所有样品均取3 个平行。
对于印刷后的聚乙烯薄膜样品,直接取样品0.05 g进行超声提取,提取方法与烘干后的油墨、上光油样品一致。
1.3.4 样品中钛的提取
对于剪碎的印刷薄膜样品(约5 mm×5 mm)及烘干后的油墨,各取0.5 g于广口瓶中,置于电热板上加热碳化。碳化完成后,冷却至室温,加入20 mL混酸(硝酸-高氯酸(4∶1,V/V)),然后再放置到电热板上消解,直到样品消解完全[34]。对于乙酰丙酮钛标准品及烘干后的上光油,由于采用混酸不能将其消解完全,在消解过程中产生了白色小颗粒状物质,可能是在消解过程中产生了钛的氧化物,所以对消解方案进行了优化。取0.1 g样品于聚四氟乙烯瓶中,置于电热板上加热碳化。碳化完成后,冷却至室温,加入10 mL混酸,并滴入3~4 滴氢氟酸,然后再放置到电热板上消解,直至样品消解完全。
样品冷却至室温后用超纯水定容至50 mL,上等离子体发射光谱检测,所有样品均取3 个平行。
1.3.5 聚乙烯薄膜的印刷
采用凹版打样机对聚乙烯薄膜进行印刷,先在印刷层涂覆一层油墨,待油墨干燥后再涂覆一层上光油,上光油的印刷方法与油墨的印刷方法相同。其中,所选用的网纹辊线数为300 线。
1.3.6 乙酰丙酮钛的紫外光照射处理和加热处理
紫外光照射处理:称取乙酰丙酮钛标准品10 mg左右(精确到0.1 mg),均匀平铺在干净的培养皿中,然后将其放置于暗箱式紫外投射仪中,紫外波长设置为254 nm(254 nm的紫外波长通常用于杀菌消毒,本实验选择254 nm的紫外波长用来模拟食品包装的杀菌消毒),照射1、3 d后取出。
加热处理:称取乙酰丙酮钛标准品10 mg左右(精确到0.1 mg),均匀平铺在干净的培养皿中,然后将其放置于70 ℃的鼓风干燥箱中,加热12 h后取出。
取少量经紫外光照射处理和加热处理的样品与溴化钾混合压片,进行傅里叶红外测试,与未经处理的样品进行对照。
1.3.7 高效液相色谱条件
色谱柱:X B r i d g e T M C1 8色谱柱(4.6 mm×250 mm,5 μm);柱温30 ℃;流动相:甲醇-乙腈(60%∶40%);流速1 mL/min;运行时间8 min;进样量10 μL;检测波长274 nm;乙酰丙酮的保留时间5.00 min。
1.3.8 气相色谱-质谱条件
色谱条件:色谱柱:19091S-433HP-5MS 5% Phenyl Methy Silox(30.0 m×250 μm,0.25 μm);升温程序:初始温度40 ℃,保持8 min;载气(He)流速1.1 mL/min;进样量1 μL;分流比20∶1。
质谱条件:电子电离源;电子能量70 eV;传输线温度275 ℃;离子源温度230 ℃;全扫描模式;质量扫描范围m/z 40~400;在上述条件下测得乙酰丙酮的保留时间为5.20 min。
1.3.9 液相色谱-质谱条件
色谱条件:色谱柱:Z O R B A X S B-C1 8(4.6 mm×150 mm,5 μm);流动相:甲醇;流速1 mL/min;柱温40 ℃;进样量10 μL。
质谱条件:负离子检测;离子源喷射电压-4.5 kV;毛细管温度400 ℃;毛细管电压25 V;鞘气流速50 arb;辅助气流速20 arb;碰撞气:氦气。
1.3.10 等离子体原子发射光谱条件
测量条件:重复次数为2;泵速为12 r/min;快速泵提升延时为25 s;读取时间为5 s;雾化器流量为0.7 L/min;观察方式为轴向;观察高度为8 mm。
采用美国IBM公司的SPSS 21.0软件进行统计分析,在置信水平为95%时,通过单因素方差分析对数据进行统计分析,P<0.05,差异显著。色谱图及红外光谱图的图像处理均采用美国OriginLab公司的Origin 9.0版本。
高效液相色谱法:选取5 个质量浓度点(1、5、10、20、50 mg/L)为横坐标,以乙酰丙酮的色谱峰面积为纵坐标建立标准曲线,得到乙酰丙酮的线性方程为y=55 617x+12 976,r=0.999 6。当乙酰丙酮的色谱峰高是基线噪音高的3 倍和10 倍时,分别得到其检出限和定量限为0.5 mg/L和2 mg/L。
等离子体原子发射光谱法:选取5 个质量浓度点(0.2、0.4、0.6、0.8、1.0 mg/L)为横坐标,以钛的色谱峰面积为纵坐标建立标准曲线,得到钛的线性方程为y=28 715.9x+239.6,r=0.999 8。进空白样品11 次,得到11 个空白样品的标准偏差的3 倍为检出限,11 个空白样品标准偏差的10 倍为定量限。钛的检出限为2.0 μg/L,定量限为8.0 μg/L。
为了验证乙酰丙酮提取方法的准确性,对乙酰丙酮的超声提取法进行加标回收实验,使得乙酰丙酮的加标质量浓度为5、10、20 mg/L,每组实验6 个平行,然后按照1.3.3节的方法进行前处理和仪器检测,计算平均回收率和相对标准偏差。结果表明,方法的回收率为80.6%~106.9%,相对标准偏差为3.4%~8.9%,说明该超声提取方法可靠。
为了验证钛的提取方法的准确性,对钛的湿法消解法进行加标回收实验,使得钛的加标质量浓度为0.4、0.8 mg/L,每组实验2 个平行。然后按照1.3.4节的方法进行样品处理和仪器检测,计算加标回收率和相对标准偏差。结果表明,该方法钛的加标回收率为82.7%~93.4%,相对标准偏差为0.68%~2.0%,说明了该消解方法有效。
2.4.1 气相色谱-质谱法

图1 空白甲醇(A)、乙酰丙酮(B)、乙酰丙酮钛(C)气相色谱图
Fig. 1 Gas chromatograms of methanol (A), AA (B), and TAA (C)
以甲醇为溶剂所配制的乙酰丙酮和乙酰丙酮钛标准溶液的气相色谱图如图1所示,并给出空白甲醇的色谱图排除杂质峰。由质谱定性可知乙酰丙酮和乙酰丙酮钛标液中在5.20 min检测到的物质均为乙酰丙酮,其他峰为色谱柱中遗留的其他物质的杂质峰。由此可以初步判断乙酰丙酮钛在溶剂甲醇中的存在乙酰丙酮。但由于气相色谱-质谱法一般适用于挥发性、半挥发性物质的检测,而不适用于不挥发性的物质的检测,所以实验采用液相色谱-质谱法对两种标液中的物质进行了进一步的鉴别。
2.4.2 液相色谱-质谱法

图2 乙酰丙酮和乙酰丙酮钛的液相色谱母离子图(负离子模式)
Fig. 2 Parent ions of AA and TAA in ESI- mode
如图2所示,在负离子模式下(减氢),以乙酰丙酮(AA)以及乙酰丙酮钛(TAA)的标准溶液(质量浓度均为5 mg/L)分别直接进样,在质量数从50~300的区间搜寻母离子,乙酰丙酮和乙酰丙酮钛的母离子图并不一致,确证了这是两种不同的物质。但乙酰丙酮钛的标准溶液在质荷比为[TAA-H]-1处却没有响应(图2),说明乙酰丙酮钛在以甲醇作为溶剂配制标准溶液时已经发生变化,溶液中不再含有乙酰丙酮钛。而乙酰丙酮和乙酰丙酮钛在质荷比为[AA-H]-1时均有响应,并且以[AA-H]-1为母离子寻找子离子时,两种物质的子离子相一致,以此子离子扫描做出乙酰丙酮和乙酰丙酮钛的液相色谱-质谱图如图3所示,这说明了这两种标准溶液中都存在乙酰丙酮。综合考虑乙酰丙酮钛甲醇溶液的气相色谱图(图1)与液相色谱图(图2、3)可以确认,乙酰丙酮钛标准溶液中存在乙酰丙酮,而不存在乙酰丙酮钛,其定性定量需要通过分别测定乙酰丙酮和钛综合计算。
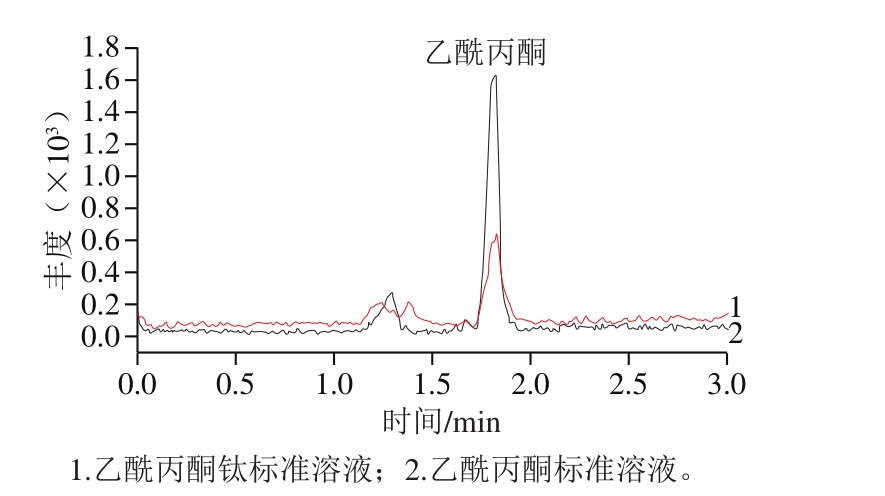
图3 乙酰丙酮和乙酰丙酮钛标准溶液的液相色谱图
Fig. 3 Liquid chromatograms of AA and TAA standard solutions
表1 样品中乙酰丙酮和乙酰丙酮钛的含量(x ±s,n=3)Table 1 Contents of AA and TAA in samples (x s,n= 3)
s,n= 3)

注:—.未检测到目标物质。
样品名称 乙酰丙酮含量/(mg/kg) 钛含量/(mg/kg)聚乙烯薄膜 — —乙酰丙酮钛标准品 790 000.12±1 806.15 188 676.38±295.24高滑型上光油 13 144.19±236.14 111 626.08±156.76油墨 — 19.52±2.61印刷聚乙烯薄膜 — 183.55±19.60
由表1可知,实验所选用聚乙烯薄膜中既不含有乙酰丙酮也不含有钛。实验测得乙酰丙酮钛标准品中钛的含量和乙酰丙酮的含量与其分子式中计算所得含量基本一致,其中乙酰丙酮的含量大约为钛含量的3.7 倍。而上光油中乙酰丙酮含量约为钛含量的1.13 倍,即乙酰丙酮含量偏少,钛的含量偏多,这说明了这种高滑型上光油中除了含有乙酰丙酮钛之外,还含有钛的其他化合物。油墨样品中不含有乙酰丙酮,含有少量的钛。
经油墨和上光油印刷后的聚乙烯薄膜中钛含量为183.55 mg/kg,未检测到乙酰丙酮。而综合以上分析,该印刷样品中钛的来源只有油墨和上光油。油墨中钛含量相较于上光油来说极少,所以可以判定样品中钛的来源主要为上光油。上光油中乙酰丙酮与钛含量之间有一个比例关系,比值约为1.13,按照此比值计算,印刷后的聚乙烯薄膜中乙酰丙酮的含量理论上应为207 mg/kg左右,但实际样品中并未检出乙酰丙酮。分析乙酰丙酮钛的作用机理:在涂料的使用过程中随着溶剂的挥发,乙酰丙酮基团可与底材及油墨连接体中的活泼基团如—OH、—COOH、—NH2、—CONH2、—SH发生交联反应,形成桥架,使分子质量增大从而使得油墨的附着力提高,同时还可以起到增加印刷品光泽度、耐磨性、防水性的作用。所以印刷样品中未检测到乙酰丙酮可能是因为乙酰丙酮基团发生交联反应生成了其他物质。由于油墨及上光油中组成成分复杂多样,乙酰丙酮钛在作用过程中生成的新物质需要更深一步的实验验证。
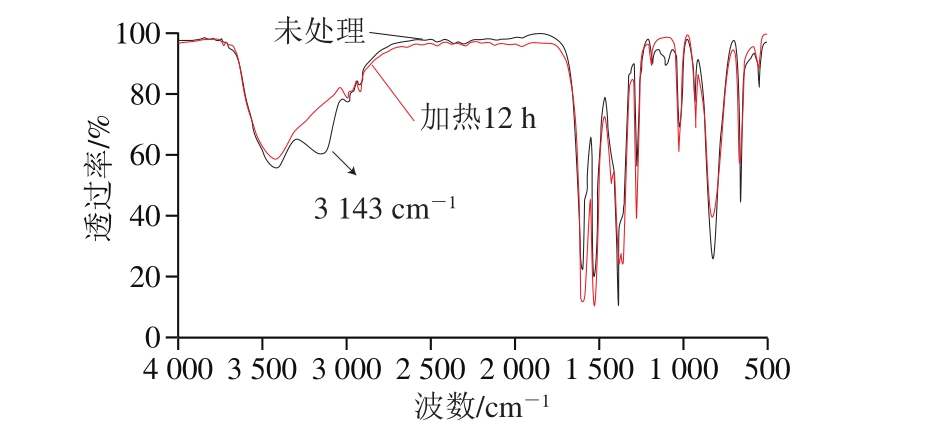
图4 加热处理条件下乙酰丙酮钛的红外光谱图
Fig. 4 Infrared spectra of TAA before and after heat treatment
由图4可以看出,3 500~3 300 cm-1处的吸收峰为O—H的伸缩吸收峰;2 962 cm-1处是—CH3吸收峰,1 364 cm-1和668 cm-1处的吸收峰归属为—CH3的变形吸收峰,2 927 cm-1处为—CH2—的吸收峰;1 606、1 531、1 389 cm-1处的吸收峰为C=O的振动吸收;1 277 cm-1处为含有羰基的碳骨架的吸收峰;1 029 cm-1处的吸收峰归属为C=O的对称伸缩振动;664、556 cm-1处的吸收峰为O—Ti=O的伸缩振动及螯合环的变形振动;3 143 cm-1处的吸收峰归属于与乙酰丙酮钛C=C相连的C—C的伸缩振动[13]。而乙酰丙酮钛在70 ℃条件下加热处理12 h后,其在波数为3 143 cm-1处的谱峰消失,说明加热使得乙酰丙酮钛的C=C消失,乙酰丙酮钛在加热条件下发生了氧化反应。并且乙酰丙酮钛的标准品在未经加热处理时能够溶解于甲醇溶剂中,但经加热12 h处理后的乙酰丙酮钛标准品不能完全溶于甲醇溶剂中,这进一步说明乙酰丙酮钛在经加热处理后,其成分发生了变化。
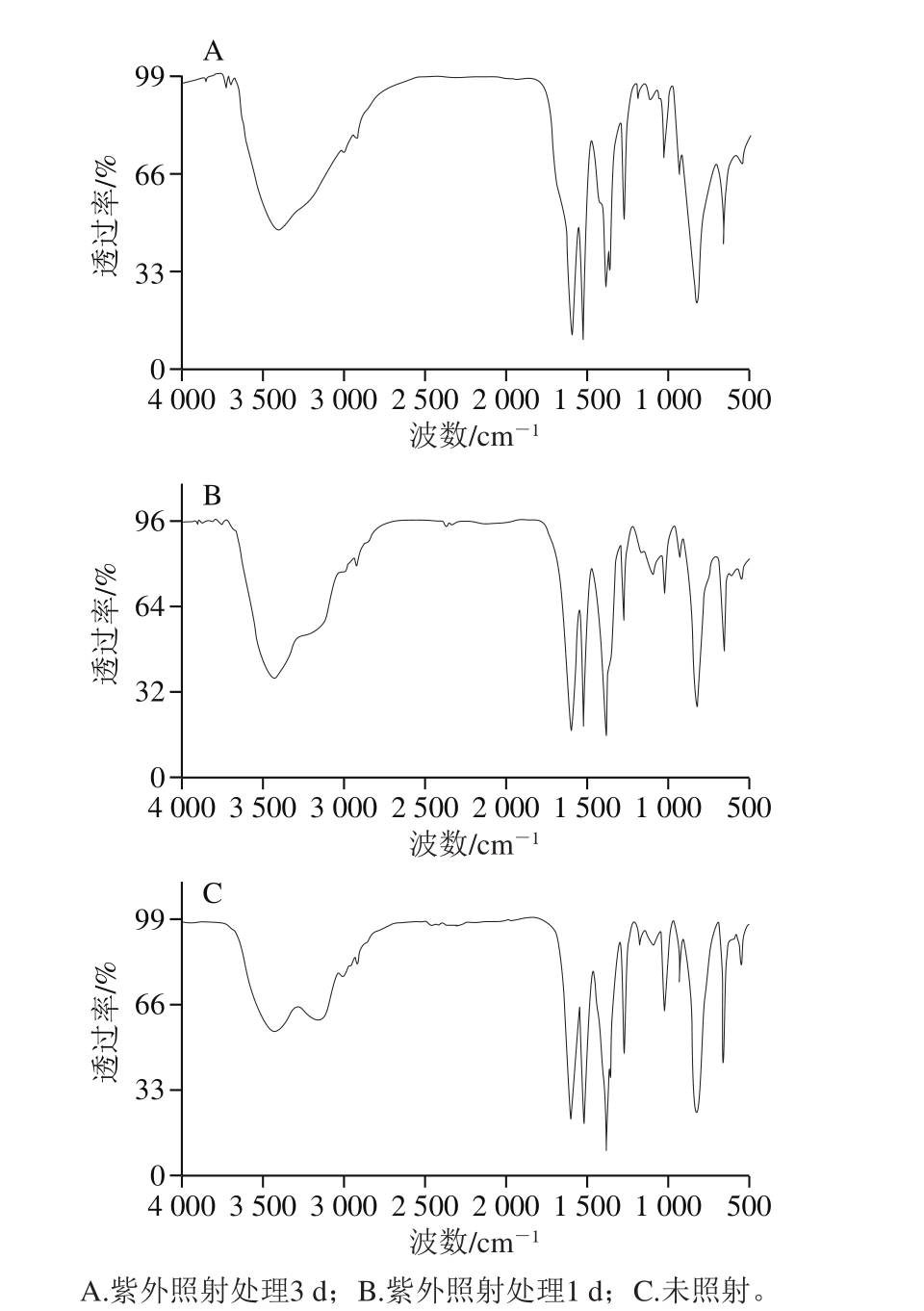
图5 紫外光照射处理后乙酰丙酮钛的红外光谱图
Fig. 5 Infrared spectra of TAA before and after UV irradiation
乙酰丙酮钛标准品(粉末)在254 nm紫外波长下照射1、3 d后,如图5所示,在波数为3 143 cm-1处的谱峰同样消失,这说明乙酰丙酮钛的碳碳双键消失,即其在紫外照射条件下也发生了氧化反应。在波数为2 000~500 cm-1的范围内,乙酰丙酮钛在紫外照射1 d和3 d的条件下其红外光谱图并没有发生明显变化。从外观上看,乙酰丙酮钛的颜色变淡。此时的乙酰丙酮钛不再溶于甲醇溶液,这也从另一方面说明乙酰丙酮钛在紫外照射的条件下成分已经发生了变化。
本实验探究了标准溶液中乙酰丙酮钛的存在形式,对比分析了油墨、上光油及印刷样品中乙酰丙酮和钛含量,研究了乙酰丙酮钛标准品在加热和紫外照射条件下的稳定性。结果表明,乙酰丙酮钛在配制的标准溶液中以乙酰丙酮的形式存在。乙酰丙酮钛标准品及上光油样品中既含有乙酰丙酮也含有钛。油墨样品中不含有乙酰丙酮,含有少量的钛。印刷样品中含有钛而不含有乙酰丙酮,分析原因是乙酰丙酮基团与底材及油墨连接体中的活泼基团发生了交联反应,生成了其他物质。乙酰丙酮钛在70 ℃加热2 h和紫外照射1、3 d后,其碳碳双键消失,说明加热和紫外照射均使其发生氧化反应,导致其发生变质。本研究对食品包装材料中乙酰丙酮钛的检测提供了依据,为印刷样品中乙酰丙酮钛的迁移研究提供了基础,对乙酰丙酮钛的安全性研究具有重要的指导作用。
[1] 朱金红, 张欣涛. 油墨中23 种邻苯二甲酸酯含量的检测[J]. 印染,2017(9): 44-46.
[2] 许亚宁, 杜维维. 食品包装印刷油墨中有害成分分析及检测方法[J].今日印刷, 2015(12): 63-66. DOI:10.16004/j.cnki.pt.2015.12.017.
[3] 高松. 纸包装油墨中增塑剂的迁移研究[D]. 无锡: 江南大学, 2014.
[4] PAPILLOUD S, BAUDRAZ D. Migration tests for substrates printed with UV ink systems in aqueous simulants[J]. Progress in Organic Coatings, 2002, 45: 231-237. DOI:10.1016/S0300-9440(02)00040-1.
[5] OESTERREICHER A, ROTH M, HENNEN D, et al. Low migration type I photoinitiators for biocompatible thiol-ene formulations[J].European Polymer Journal, 2017, 88: 393-402. DOI:10.1016/j.eurpolymj.2016.10.040.
[6] KANNGIESSER B, HAHN O, WILKE M, et al. Investigation of oxidation and migration processes of inorganic compounds in inkcorroded manuscripts[J]. Spectrochimica Acta Part B, 2004, 59(10):1511-1516. DOI:10.1016/j.sab.2004.07.013.
[7] LUIS APARICIO J, ELIZALDE M. Migration of photoinitiators in food packaging: a review[J]. Packaging Technology and Science,2015, 28(3): 181-203. DOI:10.1002/pts.2099.
[8] CLEMENTE I, AZNAR M, NERIN C, et al. Migration from printing inks in multilayer food packaging materials by GC-MS analysis and pattern recognition with chemometrics[J]. Food Additives and Contaminants Part A, 2016, 33(4): 703-714. DOI:10.1080/19440049.2 016.1155757.
[9] AZNAR M, DOMEÑO C, NERÍN C, et al. Set-off of non volatile compounds from printing inks in food packaging materials and the role of lacquers to avoid migration[J]. Dyes and Pigments, 2015, 114: 85-92. DOI:10.1016/j.dyepig.2014.10.019.
[10] AZNAR M, ALFARO P, NERIN C, et al. Progress in mass spectrometry for the analysis of set-off phenomena in plastic food packaging materials[J]. Journal of Chromatography A, 2016, 1453:124-133. DOI:10.1016/j.chroma.2016.05.032.
[11] 王福芝, 孙刚, 谭占鳌. 以醇溶性钛螯合物为阴极修饰层的高效聚合物太阳能电池[J]. 光电子·激光, 2014(4): 658-663. DOI:10.16136/j.joel.2014.04.011.
[12] 王迪, 贺安琪, 康晓燕, 等. 基于钛酸盐的黄色复合氧化物颜料的制备和光谱表征[J]. 光谱学与光谱分析, 2016(增刊1): 295-296.
[13] 刘青宝. 乙酰丙酮金属化合物的合成及其对PVC的热稳定作用研究[D]. 北京: 北京化工大学, 2009.
[14] 程进, 刘长春, 陈群, 等. 乙酰丙酮钛催化本体开环聚合制备聚己内酯[J]. 中国胶粘剂, 2017(5): 18-20. DOI:10.13416/j.ca.2017.05.005.
[15] 翟宇恺, 李轶. 乙酰丙酮金属化反应研究[J]. 应用化工, 2013,42(12): 2249-2251. DOI:10.16581/j.cnki.issn1671-3206.2013.12.011.
[16] 于涛, 朱尽顺. 用乙酰丙酮法检测纺织品中的甲醛含量[J]. 中国纤检, 2017(1): 72-75. DOI:10.3969/j.issn.1671-4466.2017.01.021.
[17] 宣燕飞. 水基胶中甲醛测定乙酰丙酮分光光度法的应用[J]. 科技经济市场, 2018(1): 21-23. DOI:10.3969/j.issn.1009-3788.2018.01.013.
[18] 王璐阳, 赵振, 苑蕊, 等. 乙酰丙酮法检测水性涂料中游离甲醛的方法确认结果[J]. 化学工程师, 2016, 30(9): 22-24. DOI:10.16247/j.cnki.23-1171/tq.20160922.
[19] 李俊, 刘辉, 刘嘉, 等. 乙酰丙酮分光光度法检测果蔬中甲醛含量的改进研究[J]. 食品科技, 2016, 41(9): 289-294. DOI:10.13684/j.cnki.spkj.2016.09.057.
[20] 崔娜, 张曼玲, 田艳玲, 等. 乙酰丙酮法测定啤酒中甲醛含量的研究[J].食品安全质量检测学报, 2016, 7(3): 906-910.
[21] 陈嘉敏, 张志强, 陈建津, 等. 乙酰丙酮分光光度法测定食糖中甲醛含量的研究[J]. 甘蔗糖业, 2017(3): 71-74. DOI:10.3969/j.issn.1005-9695.2017.03.014.
[22] BALLANTYNE B. Systemic toxicity from repeated cutaneous contact with 2,4-pentanedione[J]. Veterinary and Human Toxicology, 2001,43(1): 14-18.
[23] Register of flavouring substances used in or on foodstuffs[EB/OL].http://www.efsa.eu.int/press_room/press_release/817_en.html.
[24] KISSA E. Determination of acetylacetone and alcohols in titanium chelates[J]. Analytica Chimica Acta, 1993, 281(2): 385-389.DOI:10.1016/0003-2670(93)85196-Q.
[25] 徐水平. 乙酰丙酮混合物的气相色谱法测定[J]. 浙江化工, 1997(4):44-45.
[26] 李广梅, 郑典模, 彭海龙, 等. 高效液相色谱法测定乙酰丙酮含量[J]. 化学世界, 2010, 51(7): 398-400. DOI:10.19500/j.cnki.0367-6358.2010.07.005.
[27] 曾红艳, 段正康, 罗爱文, 等. 高效液相色谱法同时测定乙酰丙酮反应液中的乙酰丙酮和丙酮[J]. 色谱, 2010, 28(10): 955-958.DOI:10.3724/SP.J.1123.2010.00955.
[28] 曾红艳, 段正康, 陈韩志, 等. 高效液相色谱法测定2,6-二甲基吡喃酮和乙酰丙酮的含量[J]. 分析化学, 2011, 39(3): 382-386.DOI:10.3724/SP.J.1096.2011.00382.
[29] ZENG H Y, DUAN Z K, CHEN H Z, et al. Determination of 2,6-dimethyl-gamma-pyrone and acetylacetone by high performance liquid chromatography[J]. Chinese Journal of Analytical Chemistry,2011, 39(3): 382-386. DOI:10.3724/SP.J.1096.2011.00382.
[30] LI G, ZHENG D, PENG H, et al. Determination of acetylacetone with HPLC[J]. Chemical World, 2010, 7: 398-400.
[31] 杨丽香, 盛颖晗, 尹德胜. 高光水性上光油的研制及检测[J].福建分析测试, 2 0 1 1, 2 0(4): 4 4-4 7. D O I:1 0.3 9 6 9/j.issn.1009-8143.2011.04.014.
[32] 李霞. 高光泽水性上光油的研究[D]. 西安: 西安理工大学, 2006.
[33] LIN Q B, SONG X C, FANG H, et al. Migration of styrene and ethylbenzene from virgin and recycled expanded polystyrene containers and discrimination of these two kinds of polystyrene by principal component analysis[J]. Food Additives and Contaminants Part A, 2017, 34(1): 126-132. DOI:10.1080/19440049.2016.1253875.
[34] LIN Q B, LI H, ZHONG H N, et al. Migration of Ti from nano-TiO₂-polyethylene composite packaging into food simulants[J]. Food Additives & Contaminants Part A, 2011, 31(7): 1284-1290. DOI:10.10 80/19440049.2014.907505.
Determination and Stability of Titanium Acetylacetone in Printed Layer of Polyethylene Film
WANG Yini, LIN Qinbao, LI Zhong, et al. Determination and stability of titanium acetylacetone in printed layer of polyethylene fi lm[J]. Food Science, 2019, 40(18): 329-334. (in Chinese with English abstract) DOI:10.7506/spkx1002-6630-20180727-320. http://www.spkx.net.cn