脱胶与脱酸对菜籽油挥发性组分的影响
姚英政1,2,董 玲1,梁 强1,黎 剑1,李 浦1,朱 宇3,*,周 琦2
(1.四川省农业科学院农产品加工研究所,四川 成都 610066;2.中国农业科学院油料作物研究所,湖北 武汉 430062;3.四川省农业科学院生物技术核技术研究所,四川 成都 610066)
摘 要: 采用气相色谱-质谱联用法研究传统脱胶和脱酸工艺对冷榨和热榨菜籽油中挥发性组分的影响,发现冷榨油与热榨油中的挥发性组分及风味差异较大,热榨油中的挥发性组分比冷榨油更为复杂,且脱胶和脱酸工艺可以降低菜籽油中挥发性组分的复杂性;主成分分析结果表明脱酸工艺对冷榨油和热榨油的挥发性组分影响较大,而脱胶工艺的影响程度相对较小。通过测定各阶段菜籽油中酸价和过氧化值的变化,发现脱胶工艺对菜籽油的酸价没有显著影响;脱胶和脱酸工艺对冷榨油的过氧化值均有显著影响,但对热榨油的过氧化值没有显著影响。
关键词: 冷榨;热榨;精炼;风味;主成分分析
菜籽油是我国传统食用植物油之一,其消费量仅次于大豆油[1]。菜籽油具有合理的脂肪酸组成,尤其是人体必需脂肪酸α-亚麻酸含量较高,且亚油酸与α-亚麻酸的比例符合营养学推荐比例[2],是一种健康的食用植物油。菜籽油中含有生育酚、甾醇、canolol等有益微量成分。生育酚是一种抗氧化剂,能够淬灭单线态氧,是菜籽油中的重要组成[3];甾醇具有预防心血管疾病等多种重要生理功能[4];canolol是菜籽油中存在的一种脂溶性良好的多酚类物质,在加热过程中会形成二聚体或低聚体[5],具有良好的自由基清除能力[6]。同时,菜籽油中也含有多环芳烃[7]、反式脂肪酸[8]等对人体有害的微量成分。这些有益或有害的成分在菜籽油加工过程中会发生不同程度的变化。不同的制油工艺对菜籽油中的脂肪酸组成没有显著影响,但对菜籽油中的微量成分影响较大[3]。例如脱酸过程中甾醇含量损失近2/3;脱臭过程中生育酚含量降低17%,而反式脂肪酸含量升高约4 倍[4];精炼后90%的canolol都将损失[5];苯并(a)芘(多环芳烃之一)含量在菜籽炒制和压榨过程中一般不会升高,而脱胶和脱酸可以有效降低其含量[9]。
菜籽油特有的浓郁香气是其深受消费者喜爱的原因之一,不同加工工艺条件下的菜籽油具有不同的风味特征。菜籽油中挥发性成分主要包括硫苷降解产物、氧化挥发物和杂环化合物[10-13]。炒制温度对这3 类物质的产生具有显著影响[13]。热榨毛油中杂环类物质种类和相对含量明显高于浸出毛油、脱皮冷榨油和一级菜籽油,而一级菜籽油中的挥发性成分主要是氧化挥发物[10,12]。经过热处理和微波处理后,冷榨菜籽油中的硫苷降解产物含量比未经任何处理时更低,而氧化挥发物和杂环化合物含量则更高[11]。
脱胶与脱酸是油脂精炼的2 个工艺环节。脱胶主要是为了除去油脂中的磷脂。尽管磷脂能提高油脂的抗氧化能力,且对降低人体胆固醇和治疗神经障碍具有积极作用,但其对菜籽油的加工工艺和感官品质会产生负面影响,因此必须在精炼过程中将其除去[14]。脱酸主要是为了除去油脂中的游离脂肪酸,因为油脂中的游离脂肪酸会加速氢过氧化物的分解,加快油脂腐败变质[15],因此必须将其含量降低至符合相关标准。
目前,鲜见精炼过程对菜籽油挥发性成分及风味影响的报道。本实验研究传统脱胶和脱酸工艺分别对冷榨和热榨菜籽油中挥发性成分的影响,并考察酸价和过氧化值的变化,为菜籽油生产工艺优化提供理论依据。
1 材料与方法
1.1 材料与试剂
冷榨菜籽油(C1):菜籽压榨温度约85 ℃,采用YZYX-12X2L冷榨机压榨制得;冷榨脱胶菜籽油(C2):由C1经脱胶制得;冷榨脱酸菜籽油(C3):由C2经脱酸制得;热榨菜籽油(H1):菜籽压榨温度约130 ℃,采用YZYX140-8热榨机压榨制得;热榨脱胶菜籽油(H2):由H1经脱胶制得;热榨脱酸菜籽油(H3):由H2经脱酸制得。
标准品1,5-己二烯-3-醇、己醛、反-2-庚烯醛、异硫氰酸烯丙酯、辛醛、辛醇、壬醛、辛酸、苯甲酸、癸醛、壬酸、吲哚、5-硝基间二甲苯、2-吡咯烷酮、5-羟甲基-2-呋喃甲醛 美国Sigma公司;标准品反,反-2,4-庚二烯醛 日本WAKO公司;标准品己醇、2-呋喃甲酸甲酯 日本TCI公司;标准品5-甲基-2-呋喃甲醛、四氢-4,4,6-三甲基-2H-吡喃-2-酮、4-甲基-2,5-二甲氧基苯甲醛 加拿大TRC公司。
1.2 仪器与设备
YZYX-12X2L冷榨机 武汉新概念农业机械设备制造有限公司;YZYX140-8热榨机 绵阳市广鑫粮油机械制造有限公司;6890-5973S气相色谱-质谱联用仪 安捷伦科技有限公司;二乙基苯/碳分子筛/聚二甲基硅氧烷萃取头 美国Supelco公司。
1.3 方法
1.3.1 油样制取
菜籽经脱皮、皮仁分离后进入调温塔,在85 ℃条件下调温30 min,立即放料至冷榨机进行压榨,沉降后取上清液即得C1;将C1加热至60 ℃,加入油质量5%的热水(80 ℃左右),并加入油质量0.2%的磷酸搅拌30 min,沉淀过滤后得C2;根据C2的酸价计算加碱量,将相应量的食品级烧碱配成16%的水溶液,并加热至80 ℃,加入60 ℃的C2中搅拌30 min,沉降过滤后得C3;菜籽不脱皮经130 ℃高温炒制后,立即放料至热榨机进行压榨,沉降后取上清液即得H1;H2制取过程同C2;H3制取过程同C3。
1.3.2 顶空固相微萃取
参照杨湄等[10]的方法,略有改动。准确量取8 mL油样于20 mL顶空瓶中,用聚四氟乙烯隔垫密封,插入萃取头,在80 ℃条件下平衡10 min,推出纤维头萃取40 min后抽回纤维头,拔出萃取头。将萃取头插入气相色谱-质谱进样口,推出纤维头于250 ℃解吸5 min。
1.3.3 气相色谱-质谱分析条件
色谱条件:HP-5毛细管柱(30 m×0.25 mm,0.25 μm);载气为氦气,流量1.0 mL/min,分流比2∶1;升温程序:色谱柱初始温度50 ℃,保持3 min,以5 ℃/min升至150 ℃,然后以10 ℃/min升至260 ℃,保持2 min;进样口温度260 ℃。
质谱条件:电子电离源;电子能量70 eV;传输线温度280 ℃;离子源温度230 ℃;检测器电压350 V;质量扫描速率5 scans/s;质量扫描范围m/z 20~450。
1.3.4 酸价与过氧化值测定
酸价测定:参照GB 5009.229—2016《食品中酸价的测定》[16]中第1法的步骤进行,以KOH计;过氧化值测定:参照GB 5009.227—2016《食品中过氧化值的测定》[17]中第1法的步骤进行。
1.4 数据处理
挥发性成分鉴定通过2 种方式进行,一是由计算机检索与标准谱库相匹配,得到各挥发性成分的种类,二是通过与标准品进行比对。采用峰面积归一化法计算挥发性成分的相对含量。采用XLSTAT 2010进行主成分分析[18]。采用Excel 2007软件计算相对标准偏差。采用PASW Statistics 18进行Duncan检验。
续表1
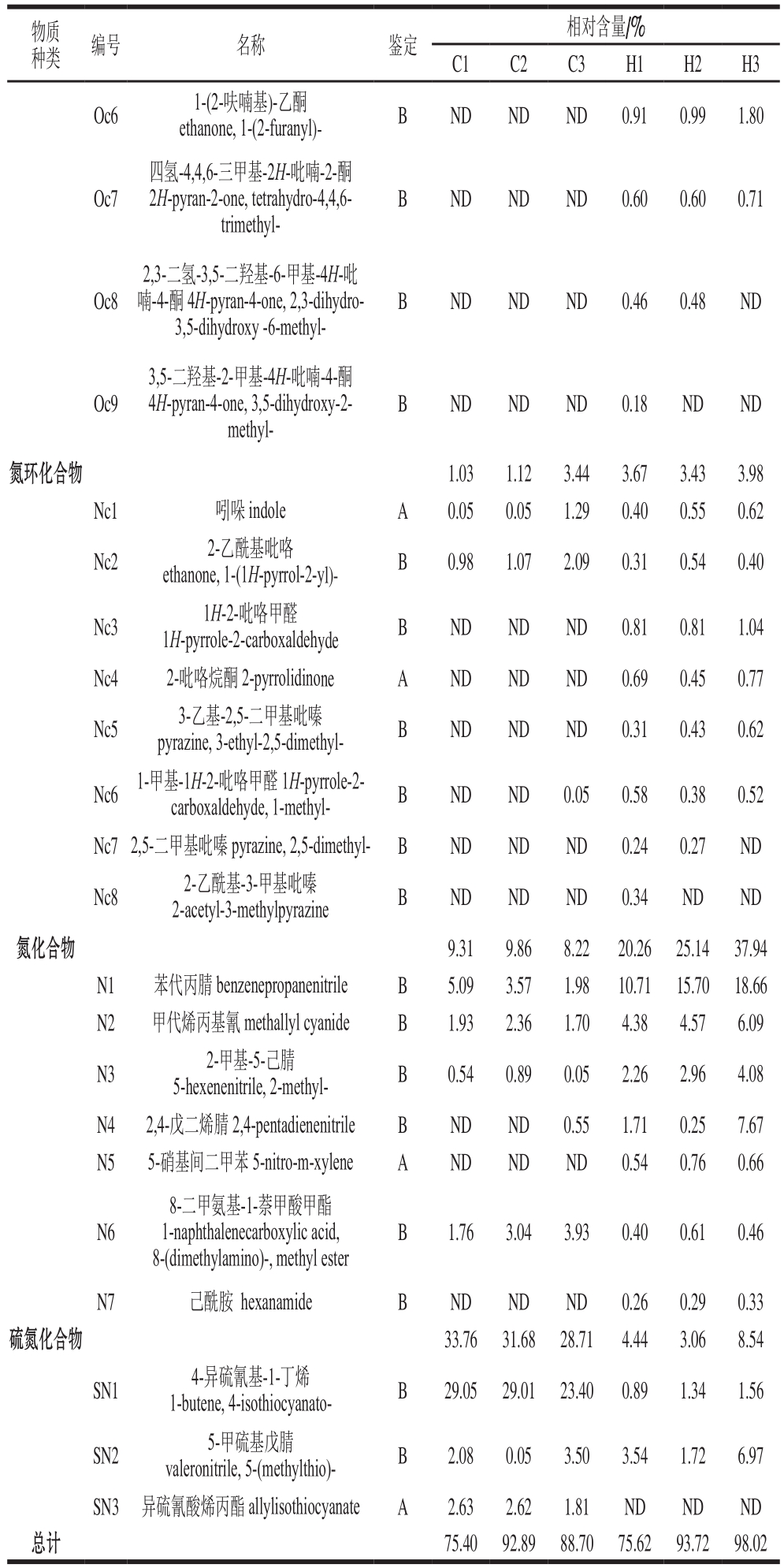
注:A.与标准品进行比对;B.与Wiley7.0和Nist05数据库进行比对;ND.未检出;所有分析的相对标准偏差小于12.2%,通常情况下低于5.3%(n=2)。
物质种类 编号 名称 鉴定 相对含量/%C1 C2 C3 H1 H2 H3 Oc6 1-(2-呋喃基)-乙酮ethanone, 1-(2-furanyl)- B ND ND ND 0.91 0.99 1.80 Oc7四氢-4,4,6-三甲基-2H-吡喃-2-酮2H-pyran-2-one, tetrahydro-4,4,6-trimethyl-B ND ND ND 0.60 0.60 0.71 Oc8 2,3-二氢-3,5-二羟基-6-甲基-4H-吡喃-4-酮 4H-pyran-4-one, 2,3-dihydro-3,5-dihydroxy -6-methyl-B ND ND ND 0.46 0.48 ND Oc9 3,5-二羟基-2-甲基-4H-吡喃-4-酮4H-pyran-4-one, 3,5-dihydroxy-2-methyl-B ND ND ND 0.18 ND ND氮环化合物 1.03 1.12 3.44 3.67 3.43 3.98 Nc1 吲哚 indole A 0.05 0.05 1.29 0.40 0.55 0.62 Nc2 2-乙酰基吡咯ethanone, 1-(1H-pyrrol-2-yl)- B 0.98 1.07 2.09 0.31 0.54 0.40 Nc3 1H-2-吡咯甲醛1H-pyrrole-2-carboxaldehyde B ND ND ND 0.81 0.81 1.04 Nc4 2-吡咯烷酮 2-pyrrolidinone A ND ND ND 0.69 0.45 0.77 Nc5 3-乙基-2,5-二甲基吡嗪pyrazine, 3-ethyl-2,5-dimethyl- B ND ND ND 0.31 0.43 0.62 Nc6 1-甲基-1H-2-吡咯甲醛 1H-pyrrole-2-carboxaldehyde, 1-methyl- B ND ND 0.05 0.58 0.38 0.52 Nc7 2,5-二甲基吡嗪 pyrazine, 2,5-dimethyl- B ND ND ND 0.24 0.27 ND Nc8 2-乙酰基-3-甲基吡嗪2-acetyl-3-methylpyrazine B ND ND ND 0.34 ND ND氮化合物 9.31 9.86 8.22 20.26 25.14 37.94 N1 苯代丙腈 benzenepropanenitrile B 5.09 3.57 1.98 10.71 15.70 18.66 N2 甲代烯丙基氰 methallyl cyanide B 1.93 2.36 1.70 4.38 4.57 6.09 N3 2-甲基-5-己腈5-hexenenitrile, 2-methyl- B 0.54 0.89 0.05 2.26 2.96 4.08 N4 2,4-戊二烯腈 2,4-pentadienenitrile B ND ND 0.55 1.71 0.25 7.67 N5 5-硝基间二甲苯 5-nitro-m-xylene A ND ND ND 0.54 0.76 0.66 N6 8-二甲氨基-1-萘甲酸甲酯1-naphthalenecarboxylic acid,8-(dimethylamino)-, methyl ester B 1.76 3.04 3.93 0.40 0.61 0.46 N7 己酰胺 hexanamide B ND ND ND 0.26 0.29 0.33硫氮化合物 33.76 31.68 28.71 4.44 3.06 8.54 SN1 4-异硫氰基-1-丁烯1-butene, 4-isothiocyanato- B 29.05 29.01 23.40 0.89 1.34 1.56 SN2 5-甲硫基戊腈valeronitrile, 5-(methylthio)- B 2.08 0.05 3.50 3.54 1.72 6.97 SN3 异硫氰酸烯丙酯 allylisothiocyanate A 2.63 2.62 1.81 ND ND ND总计 75.40 92.89 88.70 75.62 93.72 98.02
2 结果与分析
2.1 挥发性组分分析
表1 冷榨与热榨菜籽油中的挥发性组分
Table 1 Volatile compositions of cold- and hot-pressed rapeseed oils
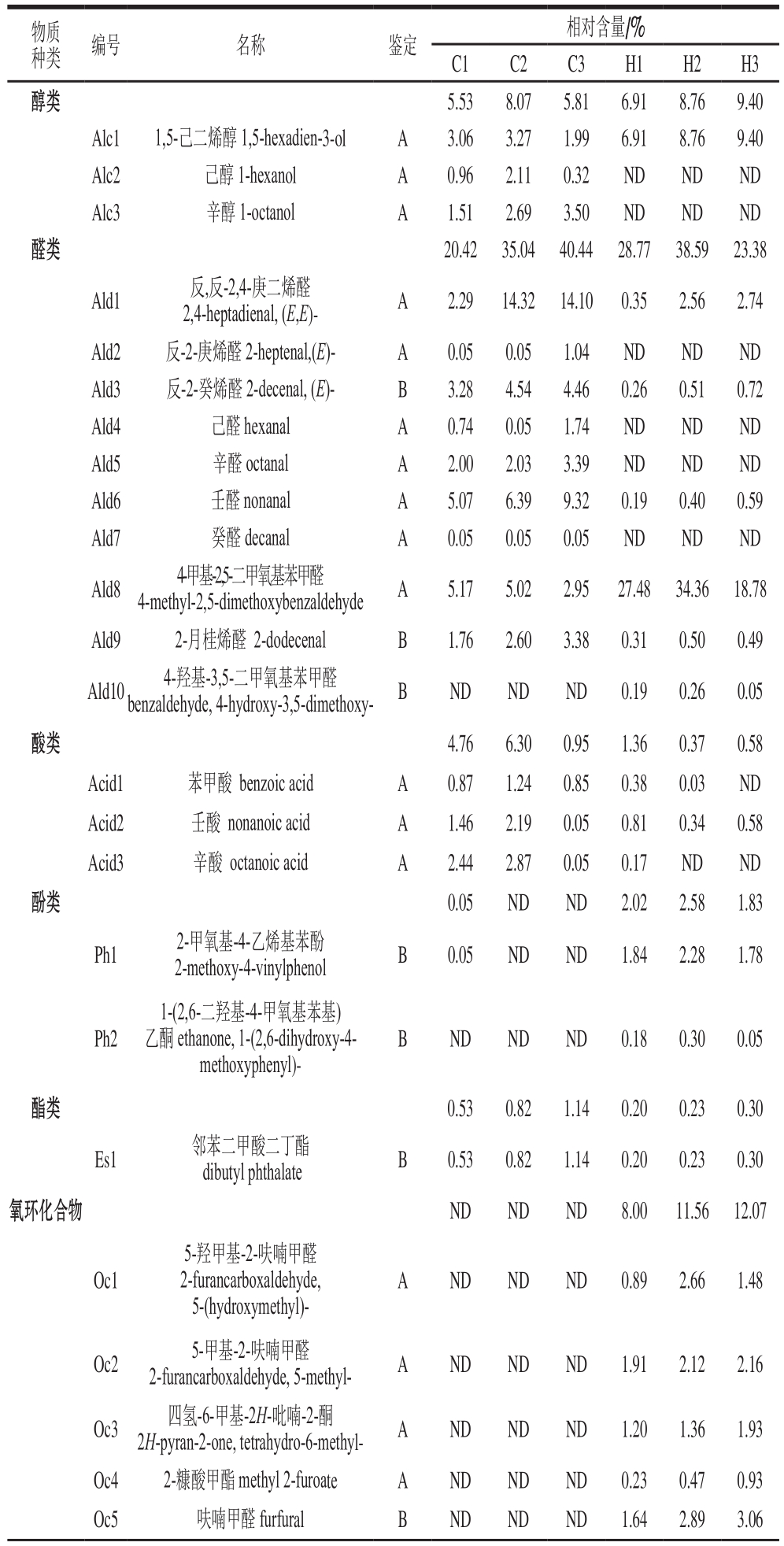
物质种类 编号 名称 鉴定 相对含量/%C1 C2 C3 H1 H2 H3醇类 5.53 8.07 5.81 6.91 8.76 9.40 Alc1 1,5-己二烯醇 1,5-hexadien-3-ol A 3.06 3.27 1.99 6.91 8.76 9.40 Alc2 己醇 1-hexanol A 0.96 2.11 0.32 ND ND ND Alc3 辛醇 1-octanol A 1.51 2.69 3.50 ND ND ND醛类 20.42 35.04 40.44 28.77 38.59 23.38 Ald1 反,反-2,4-庚二烯醛2,4-heptadienal, (E,E)- A 2.29 14.32 14.10 0.35 2.56 2.74 Ald2 反-2-庚烯醛 2-heptenal,(E)- A 0.05 0.05 1.04 ND ND ND Ald3 反-2-癸烯醛 2-decenal, (E)- B 3.28 4.54 4.46 0.26 0.51 0.72 Ald4 己醛 hexanal A 0.74 0.05 1.74 ND ND ND Ald5 辛醛 octanal A 2.00 2.03 3.39 ND ND ND Ald6 壬醛 nonanal A 5.07 6.39 9.32 0.19 0.40 0.59 Ald7 癸醛 decanal A 0.05 0.05 0.05 ND ND ND Ald8 4-甲基-2,5-二甲氧基苯甲醛4-methyl-2,5-dimethoxybenzaldehyde A 5.17 5.02 2.95 27.48 34.36 18.78 Ald9 2-月桂烯醛 2-dodecenal B 1.76 2.60 3.38 0.31 0.50 0.49 Ald10 4-羟基-3,5-二甲氧基苯甲醛benzaldehyde, 4-hydroxy-3,5-dimethoxy- B ND ND ND 0.19 0.26 0.05酸类 4.76 6.30 0.95 1.36 0.37 0.58 Acid1 苯甲酸 benzoic acid A 0.87 1.24 0.85 0.38 0.03 ND Acid2 壬酸 nonanoic acid A 1.46 2.19 0.05 0.81 0.34 0.58 Acid3 辛酸 octanoic acid A 2.44 2.87 0.05 0.17 ND ND酚类 0.05 ND ND 2.02 2.58 1.83 Ph1 2-甲氧基-4-乙烯基苯酚2-methoxy-4-vinylphenol B 0.05 ND ND 1.84 2.28 1.78 Ph2 1-(2,6-二羟基-4-甲氧基苯基)乙酮 ethanone, 1-(2,6-dihydroxy-4-methoxyphenyl)-B ND ND ND 0.18 0.30 0.05酯类 0.53 0.82 1.14 0.20 0.23 0.30 Es1 邻苯二甲酸二丁酯dibutyl phthalate B 0.53 0.82 1.14 0.20 0.23 0.30氧环化合物 ND ND ND 8.00 11.56 12.07 Oc1 5-羟甲基-2-呋喃甲醛2-furancarboxaldehyde,5-(hydroxymethyl)-A ND ND ND 0.89 2.66 1.48 Oc2 5-甲基-2-呋喃甲醛2-furancarboxaldehyde, 5-methyl- A ND ND ND 1.91 2.12 2.16 Oc3 四氢-6-甲基-2H-吡喃-2-酮2H-pyran-2-one, tetrahydro-6-methyl- A ND ND ND 1.20 1.36 1.93 Oc4 2-糠酸甲酯 methyl 2-furoate A ND ND ND 0.23 0.47 0.93 Oc5 呋喃甲醛 furfural B ND ND ND 1.64 2.89 3.06
如表1所示,冷榨油和热榨油的6 个样品中检测到9 类共46 种物质,包括醇、醛、酸、酚、酯、氧环化合物、氮环化合物、氮化合物和硫氮化合物。C1、C2、C3、H1、H2和H3中分别检测到26、25、27、39、36 种和33 种挥发性成分,这些成分分别占各自样品中总挥发性成分的75.40%、92.89%、88.70%、75.62%、93.72%和98.02%。可以看到,热榨油(H1~H3)比冷榨油(C1~C3)中的挥发性成分更复杂。这可能与压榨温度相关,更高的压榨温度引起更复杂的化学反应,从而产生种类更多的挥发性成分。另外,C1和H1中检测到的挥发性成分只占总挥发性成分的75%左右,而C2和C3中达90%左右,H2和H3中更高达93%以上。这表明脱胶和脱酸可以降低菜籽油中挥发性组分的复杂性,换言之,脱胶和脱酸有利于菜籽油的纯化。
表1中,冷榨油中相对含量较高的挥发性组分为硫氮化合物(28%~34%)、醛类(20%~40%)和氮化合物(8%~10%),热榨油中相对含量较高的组分为醛类(23%~39%)、氮化合物(20%~38%)和氧环化合物(8%~12%)。由此可见,醛类和氮化合物在冷榨油和热榨油中都占有较为重要的地位;硫氮化合物主要存在于冷榨油中,其在热榨油中相对含量较低;氧环化合物在冷榨油中未检出,在热榨油中占有较为重要的地位。
2.1.1 醛类
醛类是不饱和脂肪酸氧化后形成的过氧化物的裂解,对油脂的风味具有重要作用[19]。由表1可知,冷榨油中均含有9 种醛,而热榨油中均含有6 种醛。冷榨油中反,反-2,4-庚二烯醛和壬醛相对含量较高,未检测到热榨油中存在的4-羟基-3,5-二甲氧基苯甲醛;热榨油中以4-甲基-2,5-二甲氧基苯甲醛为主,未检测到冷榨油中存在的反-2-庚烯醛、己醛、辛醛和癸醛。反,反-2,4-庚二烯醛和壬醛是油酸氧化的产物[10,20],前者具有青草、水果、脂肪和香辛料的香味[12],后者具有青草味、柑橘味和脂肪味[2];己醛、辛醛和癸醛等直链饱和醛通常呈现出令人不愉快的青草味和辛辣的刺激性气味,且阈值很低[19];4-羟基-3,5-二甲氧基苯甲醛则产生令人愉快的坚果味[10]。热榨油中的4-甲基-2,5-二甲氧基苯甲醛从结构上看与4-羟基-3,5-二甲氧基苯甲醛相近,推测前者可能是后者的前体物质,有可能对热榨油的风味具有重要贡献,但尚需进一步验证。以上可能是冷榨油呈青草味、刺激味,而热榨油呈坚果香味的原因之一。
2.1.2 氮化合物和硫氮化合物
氮化合物和硫氮化合物是硫苷降解产物。硫苷降解产物是菜籽油中重要的风味物质,是菜籽油具有独特辛辣味的主要原因之一[10]。1-丁烯基-4-异硫氰酸酯、苯基丙腈和2-甲代-1-丙烯基氰等是菜籽油中的主要硫苷硫苷降解产物[10,12]。1-丁烯基-4-异硫氰酸酯在冷榨菜籽油中相对含量较高,在热榨菜籽油中相对含量较低,而苯基丙腈在冷榨菜籽油中相对含量较低,在热榨菜籽油中相对含量较高,这与杨湄等[10]的研究结果一致。但是本研究中,2-甲代-1-丙烯基氰在冷榨菜籽油中相对含量较低,在热榨菜籽油中相对含量较高,而杨湄等[10]的研究中,2-甲代-1-丙烯基氰在冷榨油中未检出,在热榨油中占有一定比例。异硫氰酸酯是一类重要的硫苷降解产物[21],其中异硫氰酸烯丙酯是芥菜中的主要风味成分,具有较强的刺激性气味[22-23]。异硫氰酸烯丙酯在冷榨油中占有一定比例,而未在热榨油中检出,这与冷榨油刺激味强、热榨油刺激味弱的情况相吻合。但异硫氰酸烯丙酯是否是冷榨油中刺激性气味的主要来源尚待研究。
2.1.3 杂环化合物
研究表明,杂环化合物可能是油菜籽在高温过程中发生美拉德反应产生的风味物质[24]。杨湄等[10]的研究表明,热榨油中杂环化合物成分种类和相对含量明显高于冷榨油。由表1可知,热榨油中杂环类成分(氧环化合物和氮环化合物)的相对含量为11%~16%,而冷榨油中为1%~3.5%;其中氧环化合物差别最为明显,热榨油中相对含量为8%~13%,而冷榨油中均未检出。因此,杂环化合物中的氧环化合物有可能是热榨菜籽油中风味成分的主要构成之一。氮环化合物是另一类重要的风味成分,如吡嗪类化合物是美拉德反应的中间产物,香气强烈[25],其中烷基吡嗪具有坚果、烘烤和焦糖气(如3-乙基-2,5-二甲基吡嗪和2,5-二甲基吡嗪),而烷基乙酰基吡嗪具有爆玉米的香气(如2-乙酰基-3-甲基吡嗪);3-乙基-2,5-二甲基吡嗪和2,5-二甲基吡嗪在炸土豆、炒坚果、烘烤芝麻、可可粉和木烟等中均有发现,2-乙酰基-3-甲基吡嗪在面包和烟草中存在[26]。这些吡嗪类化合物虽然在热榨油中的相对含量较低,但其所具有的风味特征与热榨油的风味相符,可能是热榨油中的重要香气组成。
2.1.4 主成分分析
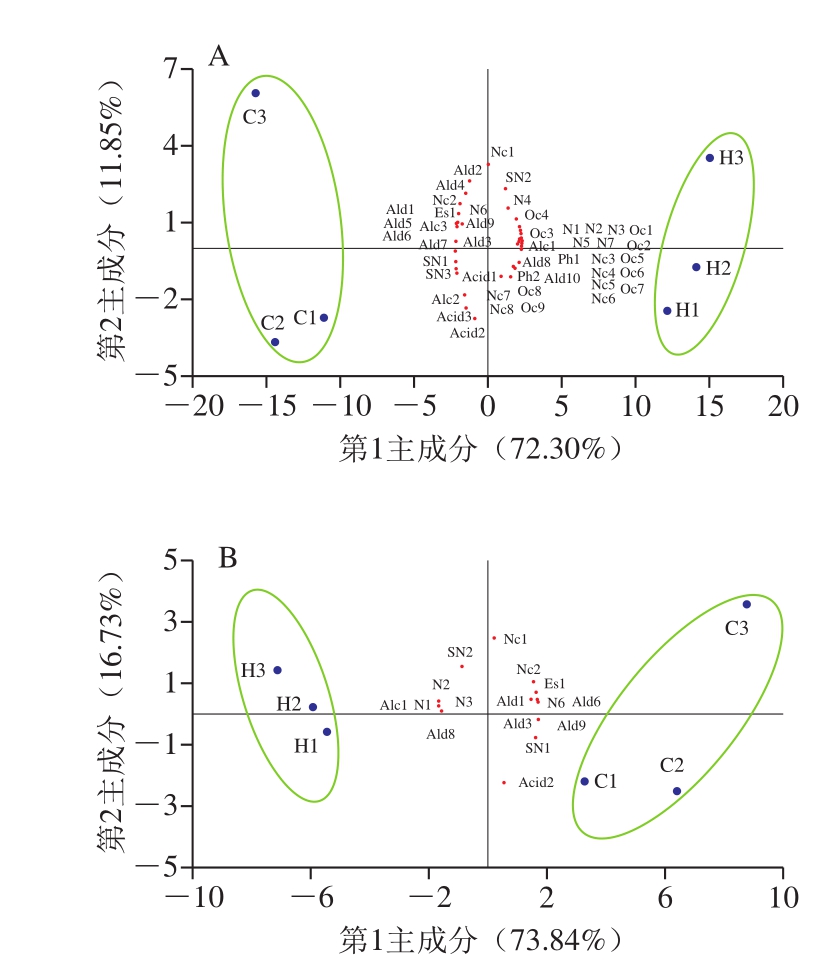
如图1A所示,第1主成分贡献率为72.30%,第2主成分贡献率为11.85%,前2 个主成分累计贡献率为84.15%。第1主成分很好地将冷榨油(C1~C3)和热榨油(H1~H3)样品区分开来,其中冷榨油样品位于第1主成分的负半轴,而热榨油样品位于第1主成分的正半轴。第1主成分负半轴的挥发性成分有18 种,包括8 种醛、3 种酸、2 种醇、2 种氮环化合物和3 种其他成分,它们可能决定了冷榨油的风味特征;第1主成分正半轴的挥发性成分有28 种,包括9 种氧环化合物、7 种氮环化合物、6 种氮化合物和6 种其他成分,它们可能决定了热榨油的风味特征。可以看到,与热榨油相关的挥发性成分多于与冷榨油相关的挥发性成分,说明热榨油的风味组成比冷榨油更为复杂。
如图1B所示,第1主成分贡献率为73.84%,第2主成分贡献率为16.73%,前2 个主成分累计贡献率为90.57%。第1主成分仍然很好地将冷榨油和热榨油样品区分开来,其中冷榨油样品位于第1主成分的正半轴,而热榨油样品位于第1主成分的负半轴。第1主成分正半轴的挥发性成分有10 种,包括4 种醛、2 种氮环化合物和4 种其他成分;第1主成分负半轴的挥发性成分有6 种,包括3 种氮化合物和3 种其他成分。
由图1A可知,第2主成分将脱酸油(C3和H3)与其他样品区分开来,表明脱酸工艺对冷榨油和热榨油的挥发性成分有一定程度的影响,而脱胶工艺的影响程度相对较小。而图1B中,第2主成分仍然可以将C3与C1、C2区分开来,但对热榨油的区分度并不好,这可能是因为脱胶工艺对热榨油中全检出的16 种成分影响较小,而对冷榨油中全检出的16 种成分影响较大。由图1可知,无论对于冷榨油还是热榨油,随着精炼不断进行,样品点距离挥发性成分所在区域的距离呈递增趋势,这说明精炼过程对菜籽油中的挥发性成分具有减弱作用,且随精炼程度加大,这种作用越来越大,进而会减弱菜籽油的风味。
2.2 酸价与过氧化值测定结果
表2 酸价与过氧化值
Table 2 Acid value and peroxide value

注:同列不同大写字母表示差异显著(P<0.05)。
样品 酸价/(mg/g) 过氧化值/(mmol/kg)C1 2.03±0.02B 1.66±0.06C C2 2.02±0.02B 2.56±0.13B C3 1.13±0.02D 3.19±0.10A H1 3.26±0.06A 2.80±0.11AB H2 3.20±0.14A 2.96±0.17AB H3 1.60±0.04C 2.63±0.37B
如表2所示,无论是冷榨油还是热榨油,脱胶工艺都对酸价没有影响(P>0.05),且脱酸前热榨油(H1、H2)的酸价显著高于冷榨油(C1、C2)(P<0.05)。脱酸处理后,冷榨油和热榨油的酸价相对于脱酸前均显著降低(P<0.05)。脱胶和脱酸工艺对冷榨油的过氧化值均有显著影响(P<0.05),但对热榨油的过氧化值没有显著影响(P>0.05)。热榨油过氧化值的变化与文献报道并不一致,如谢丹等[8]研究表明,经脱胶碱炼后,菜籽油过氧化值由3.2~5.8 meq/kg上升至5.9~7.3 meq/kg,变化幅度较大;而王瑛瑶等[27]研究表明,脱酸菜籽油的过氧化值由毛油中的7.9 mmol/kg下降至7.1 mmol/kg,变化幅度并不大。冷榨油中过氧化值的变化可能是由于加工过程中温度较低,没有完全破坏氧化酶的活力,导致后续加工中过氧化值不断升高。另外,美拉德反应产物具有良好的抗氧化性[28],而褐变程度与美拉德反应产物含量呈正相关[29],热榨油褐变程度一般高于冷榨油,因此会产生更多的美拉德反应产物,从而具有更强的抗氧化性。这可能是热榨油过氧化值在脱胶与脱酸过程中没有显著差异的原因之一。但也有研究报道,美拉德反应产物的化学稳定性增加时(例如通过聚合形成稳定的大分子产物),体系整体抗氧化能力下降[30]。因此,导致本实验结果与其他研究不一致的原因还有待进一步研究。
3 结 论
综上所述,冷榨油与热榨油中的挥发性组成及风味差异较大,且热榨油中的挥发性组成比冷榨油更为复杂。冷榨油的风味特征可能由醛、酸、醇、氮环化合物等挥发性成分所决定,其呈现的青草味和刺激味等风味特征可能与己醛、辛醛、癸醛等醛类物质以及异硫氰酸烯丙酯等硫苷降解产物密切相关;热榨油的风味特征可能由醛、氧环化合物、氮环化合物、氮化合物等挥发性成分所决定,其呈现的坚果味和烘烤味等风味特征可能与4-羟基-3,5-二甲氧基苯甲醛等醛类物质以及吡嗪类等氮环化合物密切相关。
检测到的挥发性成分占总挥发性成分的比例由毛油中的75%左右提高到精炼后的88%以上,表明脱胶和脱酸工艺可以降低菜籽油中挥发性组分的复杂性,有利于菜籽油纯化。主成分分析可以将冷榨与热榨工艺条件下的脱酸油与其他样品区分开来,表明脱酸工艺对冷榨油和热榨油的挥发性成分有较大影响,而脱胶工艺的影响程度相对较小。随着精炼步骤不断进行,菜籽油中的挥发性成分和风味会不断减弱。脱胶工艺对菜籽油的酸价没有影响;脱胶和脱酸工艺对冷榨油的过氧化值均有影响,但对热榨油的过氧化值没有影响。
氧环化合物在冷榨油中未检出,而在热榨油中占有一定比例,其可能是热榨油中的重要风味组成,但还需进一步验证。另外,要进一步明确冷榨油与热榨油中的风味成分,还需借助人工嗅辨仪等仪器进行分析。
参考文献:
[1] 吴亮鑫. 精炼对一级菜籽油抗冻性的影响[J]. 中国油脂, 2015,40(1): 19-21.
[2] GRACKA A, JELEŃ H H, MAJCHER M, et al. Flavoromics approach in monitoring changes in volatile compoundsof virgin rapeseed oil caused by seed roasting[J]. Journal of Chromatography A, 2016, 1428:292-304. DOI:10.1016/j.chroma.2015.10.088.
[3] 张亮, 李世刚, 曹培让, 等. 制油工艺对菜籽油微量成分和氧化稳定性的影响[J]. 中国油脂, 2017, 42(2): 1-6. DOI:10.3969/j.issn.1003-7969.2017.02.001.
[4] 方冰, 魏翠平, 王瑛瑶, 等. 精炼对大豆油和菜籽油抗氧化活性的影响[J].中国油脂, 2014, 39(10): 45-48.
[5] KRALJIĆ K, ŠKEVIN D, BARIŠIĆ L, et al. Changes in 4-vinylsyringol and other phenolics during rapeseed oil refining[J]. Food Chemistry, 2015, 187: 236-242. DOI:10.1016/j.foodchem.2015.04.039.
[6] SHRESTHA K, GEMECHU F G, MEULENAER B D. A novel insight on the high oxidative stability of roasted mustard seed oil in relation to phospholipid, Maillard type reaction products, tocopherol and canolol contents[J]. Food Research International, 2013, 54(1):587-594. DOI:10.1016/j.foodres.2013.07.043.
[7] SHI L K, ZHANG D D, LIU Y L. Incidence and survey of polycyclic aromatic hydrocarbons in edible vegetable oils in China[J]. Food Control, 2016, 62: 165-170. DOI:10.1016/j.foodcont.2015.10.037.
[8] 谢丹, 金青哲, 王兴国. 精炼对菜籽油品质的影响[J]. 中国油脂,2012, 32(1): 1-5. DOI:10.3969/j.issn.1003-7969.2012.01.001.
[9] 熊巍林, 邹燕娣, 金瑚, 等. 不同加热温度和时间对菜籽油中苯并(α)芘含量影响的研究[J]. 食品研究与开发, 2015, 36(16): 25-28.DOI:10.3969/j.issn.1005-6521.2015.16.007.
[10] 杨湄, 刘昌盛, 周琦, 等. 加工工艺对菜籽油主要挥发性风味成分的影响[J]. 中国油料作物学报, 2010, 32(4): 551-557.
[11] WEI F, YANG M, ZHOU Q, et al. Varietal and processing effects on the volatile profile of rapeseed oils[J]. LWT-Food Science and Technology, 2012, 48(2): 323-329. DOI:10.1016/j.lwt.2012.04.007.
[12] 谢婧, 徐俐, 吴浪, 等. SPME-GC-MS对菜籽毛油和精炼菜籽油挥发性风味成分的分析[J]. 中国油脂, 2012, 37(8): 84-87. DOI:10.3969/j.issn.1003-7969.2012.08.024.
[13] 吴浪, 徐俐, 谢婧, 等. 不同炒制温度对菜籽毛油挥发性风味物质的影响[J]. 中国油脂, 2012, 37(11): 39-43. DOI:10.3969/j.issn.1003-7969.2012.11.011.
[14] SZYDŁOWSKA-CZERNIAK A, ŁASZEWSKA A. Optimization of a soft degumming process of crude rapeseed oil: changes in its antioxidant capacity[J]. Food and Bioproducts Processing, 2017, 105:26-35. DOI:10.1016/j.fbp.2017.05.012.
[15] CHEW S C, TAN C P, NYAMK L. Optimization of neutralization parameters in chemical refining of kenaf seed oil by response surface methodology[J]. Industrial Crops and Products, 2017, 95: 742-750.DOI:10.1016/j.indcrop.2016.11.043.
[16] 国家卫生和计划生育委员会. 食品中酸价的测定: GB 5009.229—2016[S]. 北京: 中国标准出版社, 2016: 1-4.
[17] 国家卫生和计划生育委员会. 食品中过氧化值的测定: GB 5009.227—2016[S]. 北京: 中国标准出版社, 2016: 1-4.
[18] YAO Y, PAN S, FAN G, et al. Evaluation of volatile profile of Sichuan dongcai, a traditional salted vegetable, by SPME-GC-MS and E-nose[J]. LWT-Food Science and Technology, 2015, 64(2): 528-535.DOI:10.1016/j.lwt.2015.06.063.
[19] 王怡娟, 娄永江, 陈梨柯. 养殖美国红鱼鱼肉中挥发性成分的研究[J]. 水产科学, 2009, 28(6): 303-307. DOI:10.3969/j.issn.1003-1111.2009.06.001.
[20] DRUMM T D, SPANIER A M. Changes in the content of lipid autoxidation and sulfur-containing compounds in cooked beef during storage[J]. Journal of Agriculture and Food Chemistry, 1991, 39(2):336-343. DOI:10.1021/jf00002a023.
[21] SILVERO G, ÁVALOS M, BABIANO R, et al. A bioinspired look at the glucosinolate metabolic pathway. Structural insights into the reaction of benzyl isothiocyanate and D-glucosamine[J]. Tetrahedron,2011, 67(40): 7811-7820. DOI:10.1016/j.tet.2011.07.073.
[22] LI C, XUE F, XU Y, et al. Influence of different gel complexes on flavour and colour change in Chongcai paste during storage[J].Food Chemistry, 2012, 130(3): 632-637. DOI:10.1016/j.foodchem.2011.07.095.
[23] SINDHU S, MAYA P, INDIRA T N. A method for preparation of mustard (Brassica juncea) powder with retained pungency and reduced bitterness[J]. LWT-Food Science and Technology, 2012, 49(1): 42-47.DOI:10.1016/j.lwt.2012.04.016.
[24] 沈晓玲, 李晨. 脂类物质与肉的风味[J]. 肉类研究, 2008, 22(3): 25-28.DOI:10.3969/j.issn.1001-8123.2008.03.009.
[25] 谢婧, 徐俐, 张秋红, 等. 顶空固相微萃取法提取菜籽油挥发性风味成分[J]. 食品科学, 2013, 34(12): 281-285. DOI:10.7506/spkx1002-6630-201312058.
[26] 卫舒平, 张华, 徐晓彬, 等. 吡嗪衍生物的天然存在及其在食用香精中的应用[J]. 香料香精化妆品, 2000(2): 25-31.
[27] 王瑛瑶, 魏翠平, 段章群, 等. 精炼对大豆油和菜籽油中主要微量成分的影响研究[J]. 中国粮油学报, 2014, 29(10): 47-50; 55.
[28] VHANGANI L N, WYK J V. Antioxidant activity of Maillard reaction products (MRPs) in a lipid-rich model system[J]. Food Chemistry,2016, 208: 301-308. DOI:10.1016/j.foodchem.2016.03.100.
[29] ZAMORA R, HIDALGO F J. Phosphatidylethanolamine modification by oxidative stress product 4,5(E)-epoxy-2(E)-heptenal[J]. Chemical Research in Toxicology, 2003, 16: 1632-1641. DOI:10.1021/tx034126w.
[30] MANZOCCO L, CALLIGARIS S, MASTROCOLA D, et al. Review of non-enzymatic browning and antioxidant capacity in processed foods[J]. Trends in Food Science & Technology, 2001, 11(9/10):340-346. DOI:10.1016/S0924-2244(01)00014-0.
Effects of Degumming and Deacidification on Volatile Composition of Rapeseed Oil
YAO Yingzheng1,2, DONG Ling1, LIANG Qiang1, LI Jian1, LI Pu1, ZHU Yu3,*, ZHOU Qi2
(1. Institute of Agro-Products Processing Science and Technology, Sichuan Academy of Agricultural Sciences, Chengdu 610066,China; 2. Oil Crops Research Institute, Chinese Academy of Agricultural Sciences, Wuhan 430062, China;3. Biotechnology and Nuclear Technology Research Institute, Sichuan Academy of Agricultural Sciences, Chengdu 610066, China)
Abstract: In this experiment, gas chromatography-mass spectrometry (GC-MS) was used to study the effects of traditional degumming and deacidification on the volatile compositions of cold- and hot-pressed rapeseed oils. It was found that both volatile compositions and fl avors of cold- and hot-pressed oils varied greatly and the volatile composition of hot-pressed oil was more complicated than that of cold-pressed oil. Degumming and deacidification could reduce the complexity of volatile composition in rapeseed oil. Principal component analysis (PCA) indicated that deacidification had a great influence on the volatile compositions of both oils, while degumming had a lesser inf l uence. The degumming process had no significant effect on the acid value of rapeseed oil. Degumming and deacidification had significant effects on the peroxide value of coldpressed oil but not on hot-pressed oil.
Keywords: cold pressing; hot pressing; refining; fl avor; principal component analysis (PCA)
收稿日期:2018-01-15
基金项目:现代农业产业技术体系四川油菜创新团队项目;四川省科技计划项目(2018NZ0004);四川省财政创新能力提升工程青年基金专项(2017QNJJ-020);国家自然科学基金青年科学基金项目(31501528)
第一作者简介:姚英政(1984—)(ORCID: 0000-0003-2207-3799),男,助理研究员,博士,研究方向为油脂加工技术。E-mail: yaoyingzheng@126.com
*通信作者简介:朱宇(1969—)(ORCID: 0000-0001-9990-3557),男,副研究员,硕士,研究方向为农产品加工。E-mail: zy200458@126.com
DOI:10.7506/spkx1002-6630-20180115-186
中图分类号:TS221
文献标志码:A
文章编号:1002-6630(2019)06-0247-06
引文格式:姚英政, 董玲, 梁强, 等. 脱胶与脱酸对菜籽油挥发性组分的影响[J]. 食品科学, 2019, 40(6): 247-252. DOI:10.7506/spkx1002-6630-20180115-186. http://www.spkx.net.cn
YAO Yingzheng, DONG Ling, LIANG Qiang, et al. Effects of degumming and deacidification on volatile composition of rapeseed oil[J]. Food Science, 2019, 40(6): 247-252. (in Chinese with English abstract) DOI:10.7506/spkx1002-6630-20180115-186. http://www.spkx.net.cn