人参(Panax ginseng C.A. Mey.)是五加科植物人参的干燥根和根茎,具有大补元气,补脾益肺、生津养血、安神益智等功效[1]。人参作为一种传统药物已有数千年的食用和药用历史,现代研究表明,人参具有抗癌[2-3]、抗糖尿病[4]、抗衰老[5-6]、抗抑郁[7]、抗炎[8-9]、增强免疫力[10-11]等多种医疗保健功效,同时也是食品加工、临床及保健的重要原料[12-14]。人参的多个部位可以作为食用[15-16]和药用[17-18],作为典型的多年生草本植物,产品质量起伏较大,一直是人们关注的焦点。
人参的主要活性成分包括皂苷、维生素、多糖、蛋白质、有机酸、氨基酸及多肽等[19-23]。近年来,有关人参的研究主要集中在有效成分的分析及药理作用上[24-25],但综合对比分析人参不同生长年限及不同部位(包括入药部位和生物学部位)的化学成分差异报道较少。本实验对比分析不同年生及不同部位人参单体皂苷、总皂苷、总多糖、氨基酸、蛋白质含量,并进行详细分析,以期为它们的实际应用提供理论参考。
3~6 a生人参,5 a生人参芦头、主根、侧根、须根,茎、叶、花须由吉林中森药业种植基地提供,并经吉林农业大学中药材学院李伟教授鉴定。将样品粗粉过筛(60 目),装袋,标记对应名称3~6 a生人参编号分别为A1、A2、A3、A4;5 a生人参芦头、主根、侧根、须根编号分别为B1、B2、B3、B4;5 a生人参根、茎、叶、花编号分别为C1、C2、C3、C4。
人参单体皂苷标准品Rg1、Re、Rf、Rh1、Rg2、Rb1、Rc、Rb2、Rb3、Rd、香兰素 上海源叶生物科技有限公司;氨基酸混合标准液(H型) 日本Woke公司;甲醇、乙腈(均为色谱纯) 美国Thermo Fisher公司;超纯水(Milli-Q Advantage A10超纯水器制备);EDTA基准物质、硅藻土、锡箔纸 意大利VELP公司;葡萄糖 国药集团化学试剂有限公司;苯酚 天津市光复精细化工研究所;浓硫酸、正丁醇、盐酸(均为分析纯) 北京化工厂。
752N紫外分光光度计 上海仪电分析仪器有限公司;NDA701杜马斯快速定氮仪 意大利VELP公司;L-8900全自动氨基酸分析仪 日本Hitachi公司;ACQUITY UPLC H-Class超高效液相色谱仪美国Waters公司;MS204S电子分析天平 瑞士Mettler Toledo公司;Milli-Q Advantage A10超纯水器 美国Millipore公司;低速台式大容器离心机 上海菲恰尔分析仪器有限公司。
1.3.1 人参单体皂苷的测定
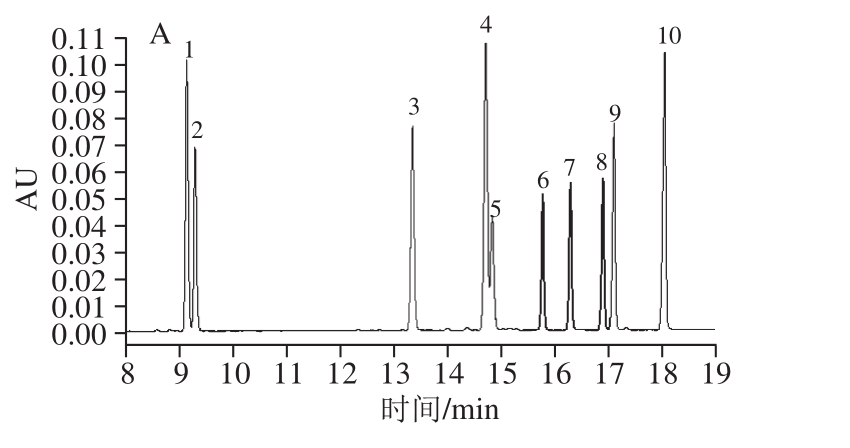
对照品溶液的制备:精密称取适量人参皂苷对照品,用甲醇溶解配制成人参皂苷Rg1、Re、Rf、Rh1、Rg2、Rb1、Rc、Rb2、Rb3、Rd质量浓度分别为0.324、0.288、0.302、0.326、0.224、0.258、0.264、0.270、0.282、0.328 mg/mL的混合对照品溶液,取适量置于进样瓶,进行上机检测,得标准品色谱图(图1A)。
供试品溶液的制备:准确称取人参粉末加入25 mL甲醇混合,超声提取30 min两次,以8 000 r/min离心5 min,合并提取液至旋转蒸发瓶中进行干燥,将干燥物转移到5 mL容量瓶中,并用甲醇定容,用标准人参皂苷或提取样品的混合物溶解于5 mL甲醇中,过滤到(0.22 μm)样品瓶中进行分析。采用Acquity UPLC H-级C18柱(2.1 mm×50 mm,1.7 μm)。乙腈和超纯水为洗脱剂,采用梯度洗脱法分离人参皂苷,流速1.0 mL/min,进样量20 μL,检测波长203 nm。人参典型样品色谱图见图1B。


图 1 人参皂苷混合标准品(A)和人参样品(B)色谱图
Fig. 1 Chromatograms of mixture of gensenoside standards (A) and ginseng sample (B)
1~10.分别为Rg1、Re、Rf、Rh1、Rg2、Rb1、Rc、Rb2、Rb3、Rd。
1.3.2 人参总皂苷的测定
总皂苷标准曲线的绘制:精密称取人参皂苷Re对照品10 mg于5 mL容量瓶中,加甲醇适量溶解并定容至刻度,配制成1 mg/mL的人参皂苷Re的标准溶液。取7 支试管依次加入0、20、40、60、80、100、120 μL人参皂苷Re标准溶液,甲醇补充至200 μL,充分混匀后,在80 ℃干燥,加入8%香兰素和72% H2SO4溶液在60 ℃进行显色反应10 min,放到冷水中10 min,于544 nm波长处测定吸光度,以甲醇为空白对照。以人参皂苷Re标准品溶液质量浓度为横坐标,吸光度为纵坐标,绘制标准曲线。回归方程为Y=1.026X-0006 3,R2=0.998 2。
供试品溶液的制备:准确称取人参粉末0.5 g,加15 mL水饱和正丁醇,在50 ℃超声提取30 min两次,以8 000 r/min离心5 min,提取两次的溶剂合并后与20 mL蒸馏水混合,静止30 min后,8 000 r/min离心5 min,将上清液转移至50 mL容量瓶中,用甲醇定容。取萃取液200 μL至试管中,在80 ℃干燥,加入8%香兰素和72% H2SO4溶液在60 ℃进行显色反应10 min,然后放到冷水中10 min。以人参皂苷Re作为人参总皂苷的标准品,用紫外分光光度计于544 nm波长处测定吸光度。
1.3.3 人参总多糖的测定
总多糖标准曲线得绘制:精密称取葡萄糖标准品10 mg于10 mL容量瓶中,蒸馏水定容至刻度,配制成1 mg/mL的葡萄糖标准溶液。取7 支试管依次加入0、0.2、0.4、0.6、0.8、1.0、1.2 mL葡萄糖标准溶液,蒸馏水补充至2 mL,充分混匀后,依次取出0.5 mL不同质量浓度标准品至试管中加入6%苯酚0.5 mL,加入质量分数为98%浓硫酸2.5 mL,室温放置30 min冷却,于490 nm波长处测定吸光度,空白对照以蒸馏水代替糖溶液。以葡萄糖质量浓度为横坐标,吸光度为纵坐标,绘制标准曲线。回归方程为Y=0.010 6X-0.006 3,R2=0.998 9。
供试品溶液的制备:准确称取人参粉末0.5 g,加入10 mL蒸馏水在50 ℃超声提取30 min两次,将两次滤液合并获得上清液,上清液中加入无水乙醇,在4 ℃过夜沉淀,离心后加入50 mL蒸馏水在50 ℃超声溶解沉淀,取1 mL提取液稀释10 倍,用苯酚-硫酸比色法测定人参总多糖的含量。用紫外分光光度计于490 nm波长处测定吸光度。
1.3.4 人参氨基酸的测定
氨基酸标准图谱的绘制:氨基酸混合标准液组分:天冬氨酸(Asp)、苏氨酸(Thr)、丝氨酸(Ser)、谷氨酸(Glu)、脯氨酸(Pro)、甘氨酸(Gly)、丙氨酸(Ala)、半光氨酸(Cys)、缬氨酸(Val)、甲硫氨酸(Met)、异亮氨酸(Ile)、亮氨酸(Leu)、酪氨酸(Tyr)、苯丙氨酸(Phe)、赖氨酸(Lys)、组氨酸(His)、精氨酸(Arg),各组分浓度均为2.5 mmol/L。用0.1 mol/L HCl溶液将混合标准液稀释1 000 倍,取适量置于进样瓶,参考标准GB/T 5009.124—2003《食品中氨基酸的测定》对标准品进行上机测试,得标准氨基酸色谱图(图2A)。设定通道1(VIS 1)位570 nm波长通道,通道2(VIS 2)位440 nm波长通道,除Pro在VIS 2显示外,其余16 种氨基酸组分均在VIS 1显示,人参样品典型氨基酸色谱图见2B。

图 2 氨基酸混合标准品(A)和人参样品(B)色谱图
Fig. 2 Chromatograms of mixture of amino acid standards (A) and ginseng sample (B)
水解氨基酸试样制备:准确称取人参粉末0.5 g,置于35 mL水解管中;加6 mol/L HCl溶液20 mL,拧紧螺旋塞密封;超声10 min;于恒温干燥箱中110 ℃水解22 h,水解结束冷却至室温,每管取800 μL至小试管,70 ℃真空干燥挥干溶剂;用0.22 μm水系针头过滤器过至样品瓶,上机备用。
1.3.5 人参粗蛋白的测定。
氮量标准曲线的绘制:准确称取乙二胺四乙酸(ethylenediaminetetraacetic,EDTA)(基准物质)0、10、20、30、40、50、60、70、80、90、100 mg,置于锡箔纸中,紧密包裹,用压样器排除内部空气,压实,依次放入仪器自动进样器样品槽中,盖上进样器盖子保持密闭空间,上机检测。以EDTA总氮量为横坐标(X)、峰面积为纵坐标(Y)绘制标准曲线,得回归方程Y=1.761 93×10-3+2.998 786×10-4X-1.497 155×10-9X2+1.614 818×10-14X3,R2=0.999 9。
粗蛋白试样的制备:准确称取人参粉末50 mg,参照1.3.5节方法进行上机测试。取压实的空锡箔纸作为空白试样。
所有数据采用IBM SPSS Statistics 19.0和Origin 8.0软件处理,应用单因素方差分析对数据进行显著性分析。所有数据以 ±s表示。
不同年生人参单体皂苷含量如表1所示,人参总皂苷含量如图3所示,随着生长年限的增长,人参皂苷含量呈逐年增加趋势,人参10 种单体皂苷含量分别为9.26、23.72、25.93、30.94 mg/g,均具有显著性差异(P<0.05),总皂苷含量分别为24.6、43.39、51.39、59.77 mg/g,且3~4 a生人参间皂苷含量增加最快,随着参龄的增加,皂苷含量呈逐年上升的趋势,但增加幅度随参龄的增加而减少。其中Rg1、Re、Rb1含量随参龄变化较大,其总量分别占3、4、5、6 a生的65%、64%、77%、76%。
表 1 不同年生及不同部位人参单体皂苷含量
Table 1 Ginsenoside contents in ginseng samples from different ages and parts mg/g

注:肩标不同字母表示差异显著(P<0.05)。下同。
样品 Rg1 Re Rf Rh1 Rg2 Rb1 Rc Rb2 Rb3 Rd 总和A1 1.55±0.12c2.80±0.10d0.65±0.07c0.02±0.01a0.14±0.01c1.65±0.10d1.00±0.01c0.85±0.03d0.15±0.01c0.45±0.03c9.26±0.49d A2 6.75±0.07b3.95±0.02c1.40±0.04b0.03±0.01b0.17±0.01c4.55±0.07c2.85±0.07a2.35±0.10b0.25±0.02a1.40±0.04a23.72±0.45c A3 9.05±0.11a4.85±0.09b1.35±0.03b0.03±0.01b0.25±0.01b6.15±0.08b1.95±0.04b1.40±0.01c0.20±0.02b0.70±0.02b25.93±0.42b A4 9.95±0.11a6.25±0.18a1.55±0.14a0.05±0.01ab0.29±0.02a7.35±0.18a2.45±0.07ab2.10±0.06a0.25±0.01a0.70±0.02b30.94±0.80a B110.13±0.18c5.36±0.14b2.20±0.10c0.07±0.02a0.31±0.02a7.39±0.13b2.05±0.03b1.75±0.03c0.20±0.01c0.60±0.02b30.06±0.68b B211.65±0.21ab2.05±0.10c1.70±0.05d0.05±0.01a0.23±0.02b4.45±0.11d1.95±0.03b1.55±0.03c0.15±0.01c0.45±0.02c24.23±0.59c B39.75±0.19bc4.95±0.05b1.80±0.07b0.05±0.01a0.27±0.03b5.65±0.06c2.01±0.05b2.10±0.09b0.45±0.03b1.08±0.04b28.11±0.61b B412.60±0.21a11.95±0.16a4.80±0.04a0.06±0.02a0.33±0.03a11.70±0.25a10.50±0.17a8.90±0.07a1.10±0.03a6.00±0.12a67.94±1.10a C1 9.05±0.15c4.85±0.13c1.35±0.05c0.03±0.01a0.25±0.01b6.15±0.08c1.95±0.12b1.40±0.03c0.20±0.01c0.70±0.01c25.93±0.60c C2 1.25±0.07d2.10±0.06d0.35±0.02d0.01±0.00b0.01±0.00c0.45±0.01d0.25±0.01c0.45±0.01d0.15±0.01d0.35±0.01d5.37±0.20d C315.30±0.27b32.55±0.25b2.55±0.08a0.08±0.02ab0.43±0.03a8.50±0.14a1.70±0.01b10.05±0.18a5.70±0.09a12.95±0.13b89.81±1.20b C419.00±0.31a39.70±0.29a1.80±0.04b0.06±0.01ab0.38±0.02a7.35±0.23b8.50±0.25a8.50±0.18b0.90±0.06b19.80±0.34a105.99±1.73a
人参总多糖含量如图4所示,3、4、5、6 a生人参的总多糖含量分别为12.48、18.86、22.80、19.84 mg/g,5 a生>6 a生>4 a生>3 a生,且6 a生与4 a生人参没有显著差异(P>0.05),表明3~5 a生人参总多糖随着参龄的增加呈逐年上升的趋势,但6 a生多糖含量有所降低;人参氨基酸含量如表2所示,3~6 a生人参的氨基酸含量分别为93.34、71.21、65.77、96.53 mg/g,6 a生>3 a生>4 a生>5 a生,且具有显著性差异(P<0.05),表明,3~5 a生人参氨基酸含量随着参龄的增加呈逐年递减趋势,但6 a生含量有所增加,且要高于3 a生人参含量。不同年生人参粗蛋白含量如图5所示,3~6 a生人参的粗蛋白含量为155.06、156.14、163.89、170.11 mg/g,6 a生>5 a生>4 a生>3 a生,且3 a生与4 a生没有显著性差异(P>0.05),5 a生与6 a生没有显著性差异(P>0.05)。
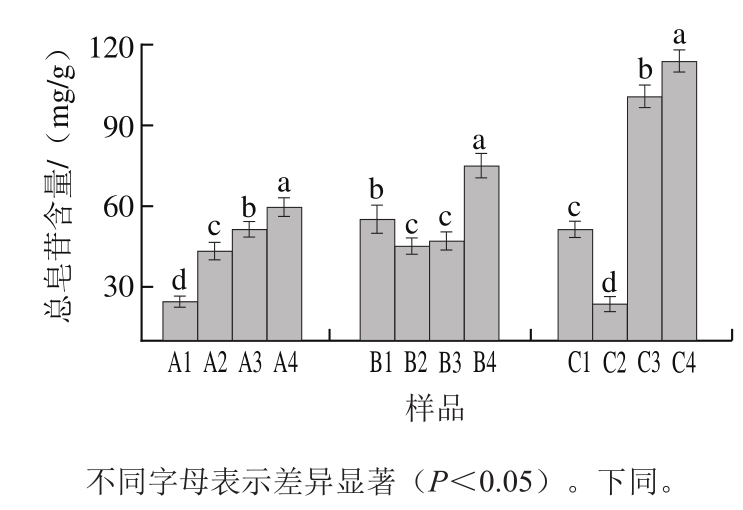
图 3 不同年生及不同部位人参总皂苷含量
Fig. 3 Total saponin contents in ginseng samples from different ages and parts
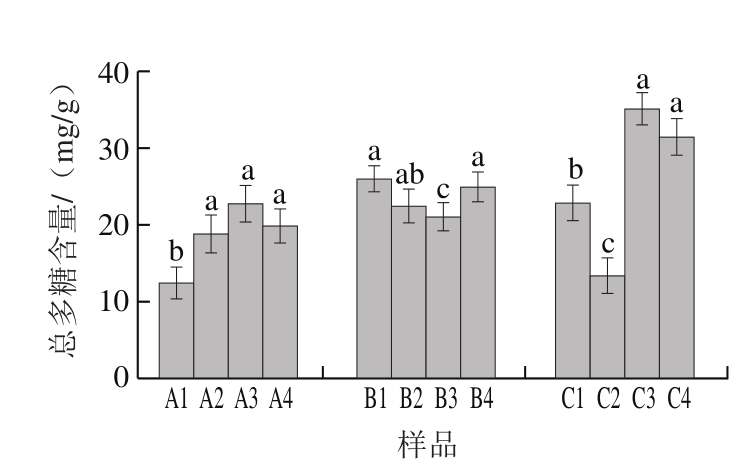
图 4 不同年生及不同部位人参总多糖含量
Fig. 4 Total polysaccharide contents in ginseng samples from different ages and parts
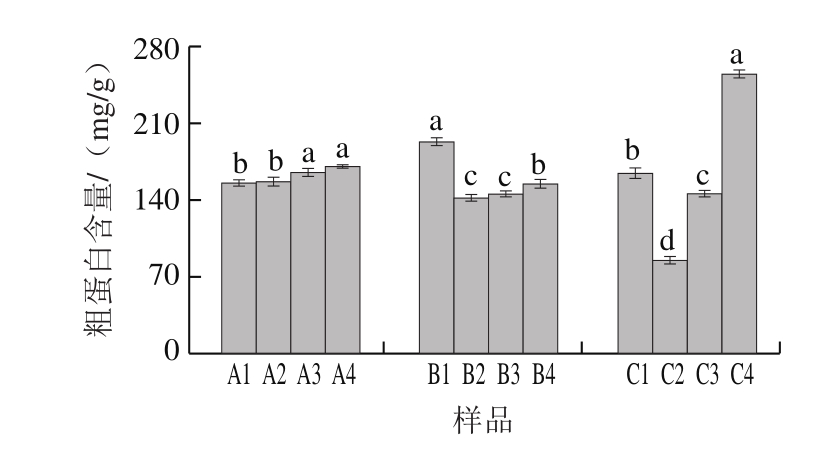
图 5 不同年生及不同部位人参粗蛋白含量
Fig. 5 Total crude protein contents in ginseng samples from different ages and parts
人参单体皂苷含量如表1所示,芦头、主根、侧根、须根中人参10 种单体皂苷含量分别为30.06、24.23、28.11、67.94 mg/g,须根>芦头>侧根>主根,但芦头与侧根间没有显著性差异(P>0.05);人参总皂苷含量如图3所示,芦头、主根、侧根、须根中总皂苷含量分别为55.11、45.23、47.14、75.01 mg/g,须根>芦头>侧根>主根,但主根和侧根间没有显著性差异(P>0.05),芦头和须根间有显著性差异(P<0.05)。人参总多糖含量如图4所示,根的不同入药部位芦头、主根、侧根、须根中总多糖含量分别为25.94、22.39、21.13、24.93 mg/g,芦头>须根>主根>侧根,但芦头、主根、须根间没有显著性差异(P>0.05);人参氨基酸含量如表2所示,芦头、主根、侧根、须根中氨基酸含量分别为121.76、90.33、95.60、100.26 mg/g,芦头>须根>侧根>主根,但主根和侧根间没有显著性差异(P>0.05);人参粗蛋白含量如图5所示,芦头、主根、侧根、须根中粗蛋白含量分别为193.36、142.15、145.47、154.80 mg/g,芦头>须根>侧根>主根,但主根和侧根间没有显著性差异(P>0.05)。
表 2 不同年生及不同部位人参氨基酸含量
Table 2 Amino acid contents in ginseng samples from different ages and parts mg/g

样品 Asp Thr Ser Glu Gly Ala Cys Val Met Ile Leu Tyr Phe Lys His Arg Pro 总和A1 8.50±0.05b 3.13±0.02a 2.71±0.01a14.41±0.12b3.85±0.01a4.74±0.02b 0.40±0.04c 3.84±0.03a0.00±0.00b 6.05±0.05a 2.16±0.01ab 3.35±0.02a 7.62±0.06a 0.56±0.02a 1.96±0.01b 26.53±0.36ab 3.51±0.08c 93.34±0.91b A2 6.40±0.04c2.32±0.01b1.70±0.01b 7.28±0.09c2.06±0.07c4.56±0.02bc0.53±0.01a3.45±0.03b0.10±0.001a 5.08±0.08b 2.06±0.08b 2.81±0.08b 1.55±0.01d 0.29±0.01c 1.53±0.06c 24.86±0.29b 4.64±0.07b 71.21±0.96c A3 6.13±0.08c2.18±0.02b1.58±0.01b 6.62±0.07c1.42±0.02d 4.34±0.06c0.50±0.01ab3.07±0.03c0.11±0.001a 4.37±0.09c 1.84±0.06c 2.43±0.02c 2.78±0.10c 0.25±0.02c 1.39±0.01c 21.59±0.24c 5.16±0.06a 65.77±0.88d A4 9.15±0.11a 3.15±0.02a 2.53±0.01a16.28±0.21a3.65±0.06b 5.15±0.02a 0.47±0.02b 3.79±0.12a0.10±0.00a 6.03±0.13a 2.39±0.07a 3.36±0.04a 5.67±0.07b 0.46±0.04a 2.25±0.01a 28.80±0.24a 3.30±0.05c 96.53±1.22a B1 13.60±0.12a4.72±0.08a 4.04±0.08a24.01±0.24a6.47±0.09a6.97±0.05a 0.56±0.01a5.95± 0.05a0.16±0.01a 9.14±0.14a 3.32±0.06a 4.87±0.06a 5.57±0.08b 0.40±0.01b 6.44±0.13b 23.79±0.18ab 4.83±0.04b 121.76±1.27a B2 8.70±0.04c3.35±0.07c 2.86±0.05c12.19±0.20c4.46±0.03c5.23±0.07c 0.39±0.01b 3.93±0.16c0.16±0.01a 6.53±0.09c 2.64±0.02bc 3.98±0.02b 4.24±0.04d 0.46±0.01a 7.92±0.24a 21.46±0.22b 7.31±0.06a 90.33±1.40c B3 8.78±0.04c3.36±0.01c 2.63±0.02c14.91±0.18b3.60±0.06d 4.40±0.02d 0.37±0.03b 3.84±0.08c0.09±0.001b 6.16±0.23c 2.48±0.06c 3.50±0.06c 6.55±0.28a 0.46±0.03a 4.83±0.25c 29.23±0.22c 2.99±0.10d 95.60±1.77c B4 10.27±0.12b3.98±0.04b3.25±0.08b15.98±0.23b4.84±0.06b 5.52±0.05b 0.41±0.01b4.76±0.07b0.10±0.00b 7.35±0.06b 2.75±0.08b 4.05±0.05b 5.25±0.07c 0.40±0.01b 4.36±0.08d 25.07±0.21a 3.66±0.04c 100.26±1.27b C1 6.13±0.11b2.18±0.06c1.58±0.02d6.62±0.12c1.42±0.04d4.34±0.09c0.50±0.01c3.07±0.04c0.11±0.00c 4.37±0.09c 1.84±0.06c 2.43±0.12c 2.78±0.04c 0.25±0.01c 1.39±0.04c 21.59±0.12a 5.16±0.06b 65.77±1.03c C2 6.07±0.17b 2.43±0.02c 2.41±0.05c8.28±0.12b4.86±0.08c3.52±0.11c 0.36±0.01b 3.35±0.06c0.20±0.01b 4.80±0.14c 1.72±0.08c 2.37±0.06c 2.23±0.08d 0.28±0.03bc 1.35±0.07c 3.41±0.13d 2.60±0.10c 50.23±1.32d C3 11.29±0.14a5.13±0.09b4.79±0.09b15.65±0.26a10.04±0.16a6.85±0.06b 0.49±0.02b6.93±0.13b 0.21±0.2b 10.11±0.18b 3.93±0.07b 5.14±0.20b 2.97±0.04b 0.29±0.02b 2.97±0.10b 5.83±0.07c 5.13±0.07b 97.74±1.90b C4 12.63±0.18a6.37±0.14a 5.76±0.08a14.50±0.16a9.30±0.07b11.13±0.12a1.07±0.03a11.05±0.15a0.33±0.01a 15.73±0.16a 6.10±0.11a 7.56±0.08a 4.58±0.09a 0.49±0.02a 3.45±0.07a 18.57±0.37b 8.91±0.25a 137.53±2.09a
人参单体皂苷含量如表1所示,不同生物学部位根、茎、叶、花中人参单体皂苷含量为25.93、5.37、89.81、105.99 mg/g,花>叶>根>茎,均具有显著性差异(P<0.05),表明同一年生不同生物学部位中单体皂苷含量差异性很大,且花中单体皂苷含量是茎的19.7 倍;人参总皂苷含量如图3所示,根、茎、叶、花中总皂苷含量为51.39、23.69、100.65、113.78 mg/g,花>叶>根>茎,均具有显著性差异(P<0.05),且花中总皂苷含量是茎中的4 倍。
人参总多糖含量如图4所示,不同生物学部位根、茎、叶、花中人参总多糖含量分别为22.80、13.46、35.09、31.44 mg/g,叶>花>根>茎,但叶和花间没有显著性差异,且花中总多糖含量是茎中的2.3 倍。人参氨基酸含量如表2所示,根、茎、叶、花中人参氨基酸含量分别为65.77、50.23、97.74、137.53 mg/g,花>叶>根>茎,且均具有显著性差异(P<0.05),且花中氨基酸含量是茎的2.7 倍。人参粗蛋白含量如图5所示,5 a生不同生物学部位中粗蛋白含量分别为164.60、84.96、145.41、255.05 mg/g,花>根>叶>茎,均具有显著性差异(P<0.05),且花中粗蛋白含量是茎中的3 倍。
人参的生长年限被认为是影响人参品质的重要因素之一。人参的次级代谢产物皂苷是一种固醇类化合物,三萜皂苷,有重要的生物活性,多糖、氨基酸、蛋白质等初级代谢产物在人参的生长发育过程中必不可少,其也在很大程度上体现人参的营养价值。本实验从不同年生人参有效成分测定结果发现,3~6 a生人参10 种单体皂苷含量和总皂苷含量呈逐年上升趋势,3~4 a生人参中人参皂苷含量增长最快,4~6 a间增加缓慢,且人参皂苷Rg1、Re、Rb1的含量随着参龄变化较大,人参皂苷的总量随着参龄的增加而增加,但增加幅度随着参龄的增长呈减少的趋势,与石威等[26]的研究结果一致,说明,人参的生长年限是皂苷含量增加的主要因素之一;人参多糖含量在3~5 a内呈递增趋势,但6 a生人参总糖含量有所降低,与4 a生含量无明显差别,与白雪媛等[27]的研究结果相似,说明人参多糖的积累与参龄非正相关;人参氨基酸含量在3~5 a内成递减趋势,但6 a生含量有所增加,且要高于3 a生含量,这与岳彬[28]研究的不同年生人参根中氨基酸含量有增有减结果一致;人参蛋白含量随着参龄的增长稍有增加,但增加幅度不明显,说明生长年限对粗蛋白含量的影响不大。
根据卫生部[29]规定,强调“5 a及5 a以下人工种植参”可以作为新资源食品。通过对5 a生人参根的不同入药部位和不同生物学部位的营养成分进行分析,结果表明人参各部位的营养成分较为全面。5 a生人参根的不同入药部位中须根的单体皂苷和总皂苷含量最高,分别为67.94、75.01 mg/g,且5 a生人参根的不同入药部位中10 种单体皂苷和总皂苷含量比值分别为芦头∶主根∶侧根∶须根=1.2∶1.0∶1.2∶2.8和1.2∶1.0∶1.0∶1.3,表明同一年生人参的不同入药部位皂苷含量有所差异,且都以主根含量为最低;总多糖、氨基酸、粗蛋白含量均为芦头最高,分别为25.94、121.76、193.36 mg/g,且总多糖、氨基酸、粗蛋白的比值分别为芦头∶主根∶侧根∶须根=1.2∶1.1∶1.0∶1.2、1.3∶1.0∶1.0∶1.1和1.9∶1.0∶1.7∶3.0,总多糖含量为侧根最低,氨基酸、粗蛋白含量为主根最低,其不同部位的有效成分的含量差异显著。
5 a生人参不同生物学部位中花的单体皂苷、总皂苷、氨基酸和粗蛋白含量最高,分别为105.99、113.78、137.53、255.06 mg/g,且单体皂苷、总皂苷、氨基酸和粗蛋白比值分别为根∶茎∶叶∶花=4.8∶1.0∶16.7∶19.7、2.2∶1.0∶3.6∶4.0、1.3∶1.0∶1.9∶2.7和1.9∶1.0∶1.7∶3.0,表明同一年生人参的不同入药部位有效成分含量均有所差异,且都以茎中的含量最低;总多糖含量为叶中最高,为35.09 mg/g,且不同部位的比值为根∶茎∶叶∶花=1.7∶1.0∶2.6∶2.3。
人参皂苷具有重要的生物活性,本研究表明,不同年生及不同部位中皂苷含量为6 a生人参和5 a生人参花中最高,从营养成分更全面的角度分析,亦是6 a生人参和5 a生人参花中营养成分含量更高。人参茎、叶、花等部位研究起步较晚,广度及深度都远不及人参根,其相关质量标准,药理活性评价等内容仍待完善。在科研和临床中人参叶常与人参茎混用,扩大了人参药材的药用部位,实现了对珍贵的人参资源的充分利用[30],且人参须的价格远低于人参主根的价格,从原料成本角度分析,更适合投料[31]。
[1] 国家药典委员会. 中国药典: 一部[M]. 北京: 中国医药出版社, 2015.
[2] WONG A S T, CHE C M, LEUNG K W. Recent advances in ginseng as cancer therapeutics: a functional and mechanistic overview[J].Natural Product Reports, 2015, 32(2): 256-272. DOI:10.1039/C4NP00080C.
[3] LEE M S, KIM M S, YOO J K, et al. Enhanced anticancer effects of a mixture of low-dose mushrooms and Panax ginseng root extracts in human colorectal cancer cells[J]. Oncology Reports, 2017, 38(3):1597-1604. DOI:10.3892/or.2017.5796.
[4] LI W, ZHANG M, GU J, et al. Hypoglycemic effect of protopanaxadiol-type ginsenosides and compound K on Type 2 diabetes mice induced by high-fat diet combining with streptozotocin via suppression of hepatic gluconeogenesis[J]. Fitoterapia, 2012,83(1): 192-198. DOI:10.1016/j.fitote.2011.10.011.
[5] SEO E, KIM S, LEE S J, et al. Ginseng berry extract supplementation improves age-related decline of insulin signaling in mice[J]. Nutrients,2015, 7(4): 3038-3053. DOI:10.3390/nu7043038.
[6] HWANG E, PARK S Y, CHANG S Y, et al. Antiaging effects of the mixture of Panax ginseng and Crataegus pinnatifidain human dermal fibroblasts and healthy human skin[J]. Journal of Ginseng Research,2017, 41(1): 69-77. DOI:10.1016/j.jgr.2016.01.001.
[7] CHEN L, DAI J G, WANG Z L, et al. The antidepressant effects of ginseng total saponins in male C57BL/6 N mice by enhancing hippocampal inhibitory phosphorylation of GSK-3β[J]. Phytotherapy Research, 2014, 28(7): 1102-1106. DOI:10.1002/ptr.5103.
[8] BAEK K S, HONG Y D, KIM Y, et al. Anti-inflammatory activity of AP-SF, a ginsenoside-enriched fraction, from Korean ginseng[J].Journal of Ginseng Research, 2015, 39(2): 155-161. DOI:10.1016/j.jgr.2014.10.004.
[9] HOSSEN M J, HONG Y D, BAEK K S, et al. In vitro antioxidative and anti-inflammatory effects of the compound K-rich fraction BIOGF1K, prepared from Panax ginseng[J]. Journal of Ginseng Research, 2017, 41(1): 43-51. DOI:10.1016/j.jgr.2015.12.009.
[10] HEO S B, LIM S W, JHUN J Y, et al. Immunological benefits by ginseng through reciprocal regulation of Th17 and Treg cells during cyclosporine-induced immunosuppression[J]. Journal of Ginseng Research, 2016, 40(1): 18-27. DOI:10.1016/j.jgr.2015.04.005.
[11] HE L X, REN J W, LIU R, et al. Ginseng (Panax ginseng Meyer)oligopeptides regulate innate and adaptive immune responses in mice via increased macrophage phagocytosis capacity, NK cell activity and Th cells secretion[J]. Food & Function, 2017, 8(10): 3523.DOI:10.1039/c7fo00957g.
[12] 刘焕焕, 何天竺, 王伟楠, 等. 人参健康产品的研究开发进展[J].食品工业, 2017, 38(5): 264-267.
[13] 彭军, 高小蔷, 李琼, 等. 卫生部批准的795 种参类保健食品情况分析[J]. 中国食品卫生杂志, 2006, 18(3): 214-220.
[14] XIANG Y Z, SHANG H C, GAO X M, et al. A comparison of the ancient use of ginseng in traditional Chinese medicine with modern pharmacological experiments and clinical trials[J]. Phytotherapy Research, 2008, 22(7): 851-858. DOI:10.1186/1749-8546-5-20.
[15] 文连奎, 张微, 王立芳, 等. 人参发酵酒加工工艺优化[J]. 食品科学,2010, 31(22): 508-511.
[16] 刘学军, 殷涌光, 于晓霞, 等. 人参果、山楂复合饮料的研制[J].食品科学, 2005, 26(9): 655-659.
[17] GANESAN P, KO H M, KIM I S, et al. Recent trends of nano bioactive compounds from ginseng for its possible preventive role in chronic disease models[J]. RSC Advances, 2015, 5(119): 98634-98642. DOI:10.1039/C5RA20559J.
[18] DAI D, ZHANG C F, WILLIAMS S, et al. Ginseng on cancer:potential role in modulating inflammation-mediated angiogenesis[J].The American journal of Chinese Medicine, 2017, 45(1): 13-22.DOI:10.1142/S0192415X17500021.
[19] 张万博, 代月, 廉美兰, 等. 不同栽培年限人参不同部位中皂苷含量的分析[J]. 延边大学农学学报, 2016, 38(1): 13-17. DOI:10.13478/j.cnki.jasyu.2016.01.003.
[20] RU W W, WANG D L, XU Y P, et al. Chemical constituents and bioactivities of Panax ginseng (C A Mey.)[J]. Drug Discoveries &Therapeutics, 2015, 9(1): 23-32. DOI:10.5582/ddt.2015.01004.
[21] ZHANG K, XIAO W, LAN D, et al. Determination of seven major ginsenosides in different parts of Panax quinquefolius L.(American ginseng) with different ages[J]. Chemical Research in Chinese Universities, 2008, 24(6): 707-711. DOI:10.1016/S1005-9040(09)60011-8.
[22] SHIN B K, KWON S W, PARK J H. Chemical diversity of ginseng saponins from Panax ginseng[J]. Journal of Ginseng Research, 2015,39(4): 287-298. DOI:10.1016/j.jgr.2014.12.005.
[23] SUN H, LIU F, SUN L, et al. Proteomic analysis of amino acid metabolism differences between wild and cultivated Panax ginseng[J].Journal of Ginseng Research, 2016, 40(2): 113-120. DOI:10.1016/j.jgr.2015.06.001.
[24] SUN Y Y, GUO M F, FENG Y J, et al. Effect of ginseng polysaccharides on NK cell cytotoxicity in immunosuppressed mice[J].Experimental and Therapeutic Medicine, 2016, 12(6): 3773-3777.DOI:10.3892/etm.2016.3840.
[25] NG T B, WANG H. Panaxagin, a new protein from Chinese ginseng possesses anti-fungal, anti-viral, translation-inhibiting and ribonuclease activities[J]. Life Sciences, 2001, 68(7): 739-749. DOI:10.1016/S0024-3205(00)00970-X.
[26] 石威, 王玉堂, 陈晓东, 等. 高效液相色谱蒸发光散射检测法测定人参根中人参皂昔的含量[J]. 分析化学, 2006, 34(2): 243-246.
[27] 白雪媛, 赵雨, 刘海龙, 等. 不同品种和年限人参中糖类含量比较研究[J]. 安徽农业科学, 2012, 40(1): 152-153.
[28] 岳彬. 人参与西洋参根中氨基酸积累规律的研究[D]. 长春: 吉林农业大学, 2008.
[29] 卫生部. 第56号新资源食品管理办法: 中华人民共和国卫生部令第56号[S]. 2006-12-26.
[30] 陆维承. 人参叶和参叶考辨[J]. 中药材, 2016, 39(1): 213-215.
[31] 张秀莲, 赵卉, 许世泉, 等. 人参芦、体、须中蛋白质含量对比分析[J].特产研究, 2016, 38(4): 28-30.
A Comparative Study of Effective Components in Ginseng Samples from Different Parts and Ages