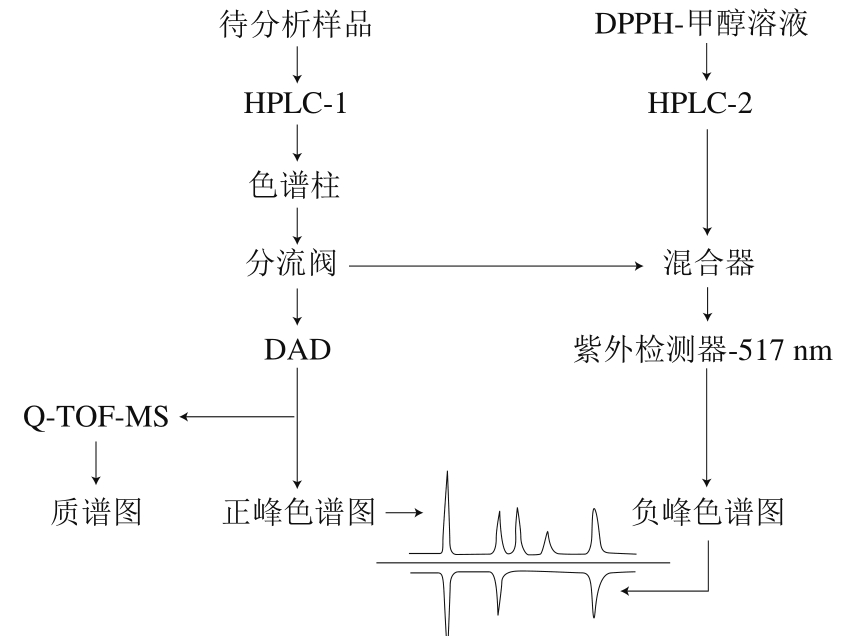
图 1 抗氧化成分在线筛选与鉴别流程图
Fig. 1 Flow chart of on-line screening for and identification of antioxidant compounds
牛蒡(Arctium lappa L.)为菊科两年生草本植物,《本草纲目》记载其“久服轻身耐老”[1],现代研究证明牛蒡具有抗衰老、降血脂、抗肿瘤、降血糖等活性[2-4],对高血压、糖尿病、动脉硬化等疾病具有治疗作用[5-7]。牛蒡提取物具有很好的抗氧化作用,可以有效清除自由基、提高超氧化物歧化酶活性、抑制脂质体和蛋白质的氧化损伤并与VE形成协同作用增强抗氧化性[8-13]。牛蒡中具有抗氧化活性的化合物主要为咖啡酰奎宁酸类和黄酮类化合物,其中咖啡酰奎宁酸类化合物的报道远多于黄酮,是牛蒡中主要的次级代谢产物[14-17]。咖啡酰奎宁酸类化合物属于咖啡酸的衍生物,主要存在牛蒡乙酯相中,该化合物具有明显的抗氧化作用[18-19],对氧化应激引起的缺血性损伤、肝细胞脂质过氧化和胰岛素抵抗等症状具有明显改善作用[20-23],是牛蒡中最重要的一类活性成分。先前的研究通过高效液相色谱-质谱联用对牛蒡中该成分进行分析[24-25],分析过程仅依据分子质量进行推断,并未经对照品进行验证,因此鉴定结果的准确性有待于进一步考证。
基于1,1-二苯基-2-三硝基苯肼(1,1-diphenyl-2-picrylhydrazyl,DPPH)模型建立的高效液相色谱-二极管阵列检测器-质谱法已成为天然产物研究中抗氧化活性成分筛选的重要方法之一[26-29],样品中的抗氧化活性成分与DPPH-甲醇溶液反应后进入紫外检测器,由于自由基的清除导致在517 nm波长处在线检测形成负峰。通过DPPH模型中出现的负吸收峰结合化合物的紫外吸收和精准分子质量,可以快速、定向和准确鉴定样品中的抗氧化成分。
本研究以牛蒡提取物的乙酸乙酯相为研究对象,基于DPPH筛选模型建立高效液相色谱-二极管阵列检测器-串联三重四极杆飞行时间质谱(high performance liquid chromatography-quadrupole time-of-flight mass spectrometry,HPLC-DAD-Q-TOF-MS)在线筛选鉴别自由基清除剂的方法对牛蒡中天然抗氧化活性成分进行快速筛选和鉴定,为食品及中药等复杂体系中抗氧化活性成分的筛选提供技术参考。
牛蒡购于江苏沛县轶伟食品有限公司,经山东省分析测试中心王晓研究员鉴定为菊科植物牛蒡(Arctium lappa L.)的根,品种为柳川理想。
DPPH 美国Sigma公司;乙腈(色谱纯) 瑞士Oceanpak公司;纯净水 娃哈哈集团有限公司。
1260 HPLC仪(配置DAD)、G6520A Q-TOF-MS(配置电子电离源) 美国安捷伦公司。
1.3.1 供试品溶液及DPPH-甲醇溶液制备
牛蒡干燥粉碎后过80 目筛,称取2.0 g牛蒡样品,100 mL 50%乙醇溶液回流提取30 min,抽滤后低压浓缩至无明显醇味后用纯水定容至10 mL,依次用3 倍体积的石油醚、乙酸乙酯和正丁醇萃取,各萃取相蒸干,分别用50%乙腈溶液定容至2 mL,过0.45 μm有机滤膜,备用。
准确称取DPPH标准品,配制成浓度为6×10-5 mol/L甲醇溶液,置于4 ℃冰箱中避光保存,现配现用。1.3.2 抗氧化成分在线筛选与鉴别

图 1 抗氧化成分在线筛选与鉴别流程图
Fig. 1 Flow chart of on-line screening for and identification of antioxidant compounds
实验流程见图1。待测样品经HPLC-1分离通过经分流阀分成2 部分,一部分进入混合器,与HPLC-2泵入的DPPH-甲醇溶液混合反应后进入DAD,在517 nm波长处形成的负峰即为抗氧化成分;另一部分进入DAD和MS仪,实现各成分的紫外吸收检测以及各成分的在线质谱分析。负峰色谱图结合精准的分子质量信息与紫外吸收特征,实现牛蒡中抗氧化成分的在线快速筛选。
1.3.3 仪器工作条件
HPLC-1工作条件:色谱柱:Phenomenex Gemini-NX C18(250 mm×4.6 mm,5 µm);乙腈(A)-0.1%甲酸溶液,梯度洗脱程序:0~7 min(15% A),7~8 min(15%~20% A),8~29 min(20% A),29~30 min(20%~25% A),30~50 min(25%~30% A);流速1 mL/min;检测波长280 nm;进样量10 μL;柱温25 ℃。样品经HPLC-1色谱柱后分流至DAD-Q-TOF-MS流速为0.3 mL/min,另一路液体流速为0.7 mL/min。
HPLC-2工作条件:反应器为PEEK盘管(10 m×0.254 mm);流动相为DPPH-甲醇溶液,流速0.5 mL/min,检测波长517 nm。
HPLC-1的正峰色谱图和HPLC-2的负峰色谱图由Agilent液相色谱化学工作站同时获得。
质谱工作条件:分别采用电喷雾正、负离子模式;全扫描范围m/z 100~1 000;毛细管电压4.5 kV;雾化气压力35 psi;干燥气流速10.0 L/min;干燥气温度325 ℃;裂解电压100 V;锥孔电压60 V。
本实验分别考察50%乙醇溶液超声提取和回流提取2 种方式对牛蒡化学成分的提取效果,结果表明回流提取30 min的效果优于200 W超声提取1.5 h,故采用回流方式进行提取。提取浓缩后用石油醚、乙酸乙酯和正丁醇萃取,通过HPLC对牛蒡的不同萃取部位分析比对,结果见图2。石油醚相(图2A)、乙酸乙酯相(图2B)和正丁醇相(图2C)差异较大,说明采用不同极性的溶剂进行萃取富集的前处理过程初步实现牛蒡化学成分的分段富集与净化。从图2可以看出,乙酸乙酯相的HPLC图与回流提取总样最为接近,所以将乙酸乙酯相作为后续的分析对象。


图 2 牛蒡不同相液相色谱图
Fig. 2 Chromatograms of different solvent extracts of burdock
分别考察乙腈-0.1%甲酸溶液和甲醇-0.1%甲酸溶液2 种流动相对目标物的分离效果,结果表明,在实现较好分离的目标下,乙腈-0.1%甲酸溶液体系洗脱时间为50 min,甲醇-0.1%甲酸溶液体系洗脱时间为70 min,且前者的分离效果优于后者。在同一HPLC条件和色谱柱规格(250 mm×4.6 mm,5 µm)下,分别考察Phenomenex Gemini-NX C18、YMC-Pack ODS-A、Waters Symmetry C18和Spax Amethyst C18-H四种不同色谱柱对于目标物的分离效果。经实验比较,Phenomenex Gemini-NX C18色谱柱的分离效果最佳,因此选取该色谱柱作为分析色谱柱,样品HPLC分析结果见图3。
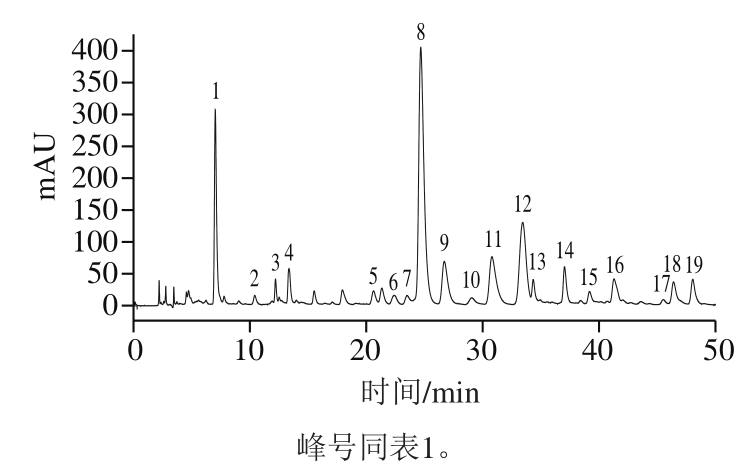
图 3 牛蒡提取物HPLC图
Fig. 3 HPLC of burdock extract
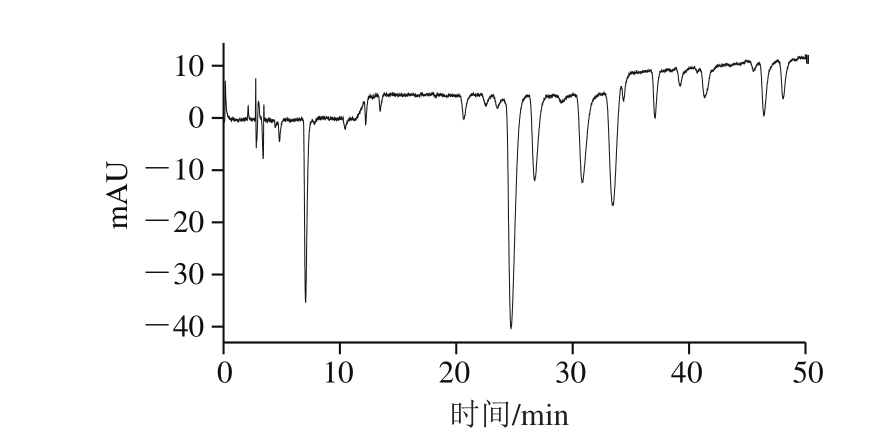
图 4 牛蒡提取物在线清除自由基HPLC图
Fig. 4 HPLC chromatograms of burdock extract and on-line screening for free radical scavengers
DPPH浓度是影响筛选灵敏度的一个重要因素,信噪比随着浓度的增加而相应增加,同时基线噪音和基线波动也随之增大。研究分别考察2×10-4、1×10-5 mol/L和6×10-5 mol/L三个浓度下的筛选效果,结果表明DPPH-甲醇溶液浓度为6×10-5 mol/L时的筛选效果最佳,因此选取该浓度作为筛选浓度,自由基清除剂筛选结果见图4。
利用DAD对样品中峰面积相对含量在0.5%以上且具有抗氧化活性的化合物进行全波长扫描,结果见表1。从全波长扫描结果来看,该样品中具有抗氧化活性化合物的紫外吸收情况具有高度相似性,主要成分的紫外吸收最大波长在216、240 nm和320 nm附近,初步判断为结构类似物,且样品中大多数化合物在300 nm波长处有特征肩峰,判定为咖啡酰奎宁酸类系列化合物。
表 1 牛蒡提取物的HPLC-DAD-Q-TOF-MS测量结果
Table 1 Analytical data from HPLC-DAD-Q-TOF-MS for burdock extract
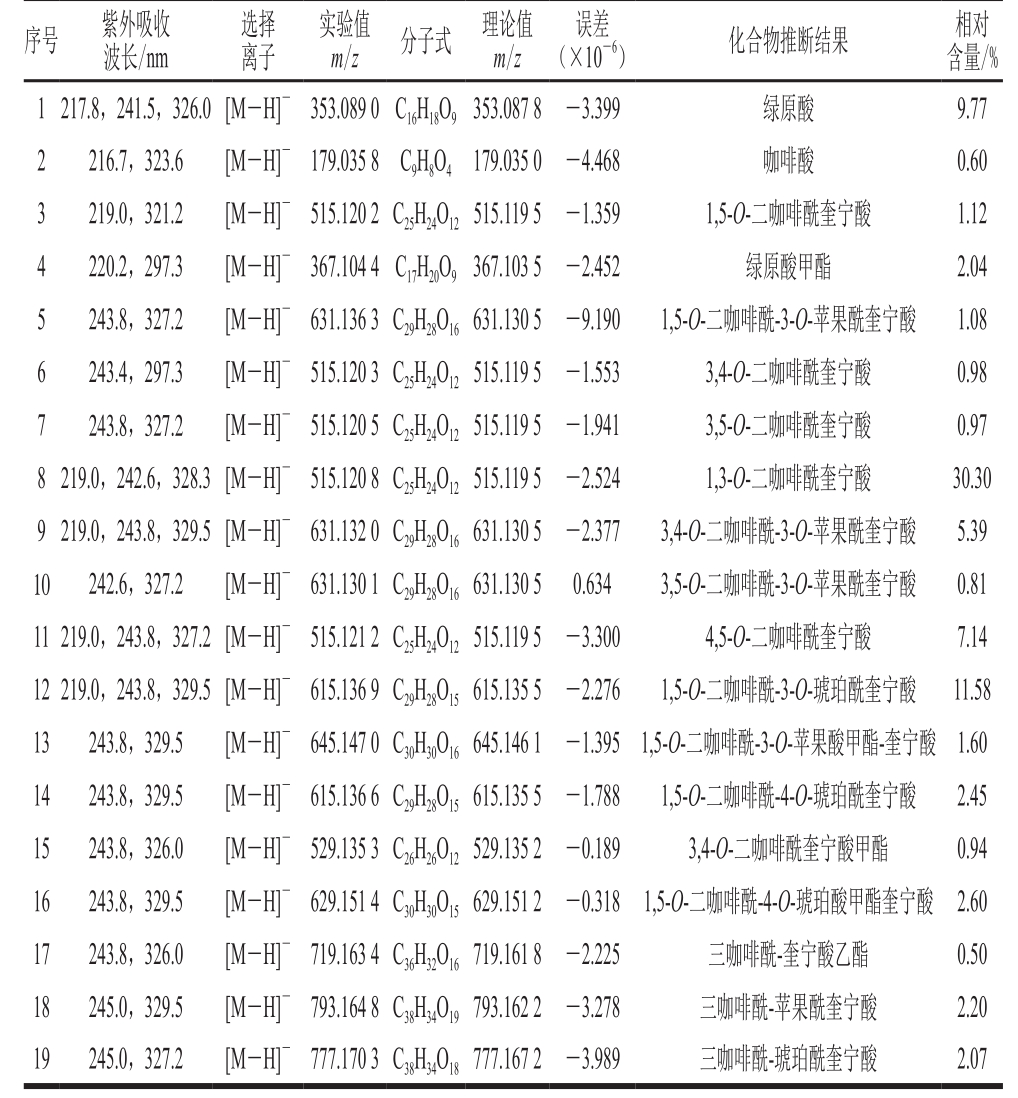
序号 紫外吸收波长/nm选择离子实验值m/z 分子式 理论值m/z误差(×10-6) 化合物推断结果 相对含量/%1217.8,241.5,326.0[M-H]- 353.089 0C16H18O9353.087 8 -3.399 绿原酸 9.77 2 216.7,323.6 [M-H]- 179.035 8 C9H8O4179.035 0 -4.468 咖啡酸 0.60 3 219.0,321.2 [M-H]- 515.120 2C25H24O12515.119 5 -1.359 1,5-O-二咖啡酰奎宁酸 1.12 4 220.2,297.3 [M-H]- 367.104 4C17H20O9367.103 5 -2.452 绿原酸甲酯 2.04 5 243.8,327.2 [M-H]- 631.136 3C29H28O16631.130 5 -9.190 1,5-O-二咖啡酰-3-O-苹果酰奎宁酸 1.08 6 243.4,297.3 [M-H]- 515.120 3C25H24O12515.119 5 -1.553 3,4-O-二咖啡酰奎宁酸 0.98 7 243.8,327.2 [M-H]- 515.120 5C25H24O12515.119 5 -1.941 3,5-O-二咖啡酰奎宁酸 0.97 8219.0,242.6,328.3[M-H]- 515.120 8C25H24O12515.119 5 -2.524 1,3-O-二咖啡酰奎宁酸 30.30 9219.0,243.8,329.5[M-H]- 631.132 0C29H28O16631.130 5 -2.377 3,4-O-二咖啡酰-3-O-苹果酰奎宁酸 5.39 10 242.6,327.2 [M-H]- 631.130 1C29H28O16631.130 5 0.634 3,5-O-二咖啡酰-3-O-苹果酰奎宁酸 0.81 11219.0,243.8,327.2[M-H]- 515.121 2C25H24O12515.119 5 -3.300 4,5-O-二咖啡酰奎宁酸 7.14 12219.0,243.8,329.5[M-H]- 615.136 9C29H28O15615.135 5 -2.276 1,5-O-二咖啡酰-3-O-琥珀酰奎宁酸 11.58 13 243.8,329.5 [M-H]- 645.147 0C30H30O16645.146 1 -1.395 1,5-O-二咖啡酰-3-O-苹果酸甲酯-奎宁酸 1.60 14 243.8,329.5 [M-H]- 615.136 6C29H28O15615.135 5 -1.788 1,5-O-二咖啡酰-4-O-琥珀酰奎宁酸 2.45 15 243.8,326.0 [M-H]- 529.135 3C26H26O12529.135 2 -0.189 3,4-O-二咖啡酰奎宁酸甲酯 0.94 16 243.8,329.5 [M-H]- 629.151 4C30H30O15629.151 2 -0.318 1,5-O-二咖啡酰-4-O-琥珀酸甲酯奎宁酸 2.60 17 243.8,326.0 [M-H]- 719.163 4C36H32O16719.161 8 -2.225 三咖啡酰-奎宁酸乙酯 0.50 18 245.0,329.5 [M-H]- 793.164 8C38H34O19793.162 2 -3.278 三咖啡酰-苹果酰奎宁酸 2.20 19 245.0,327.2 [M-H]- 777.170 3C38H34O18777.167 2 -3.989 三咖啡酰-琥珀酰奎宁酸 2.07
分别考察正离子和负离子模式下待测样品的总离子流图,由图5可以看出,待测组分在负离子模式下响应值优于正离子模式,杂质的干扰程度低于正离子模式,因此选取负离子模式为质谱检测条件。
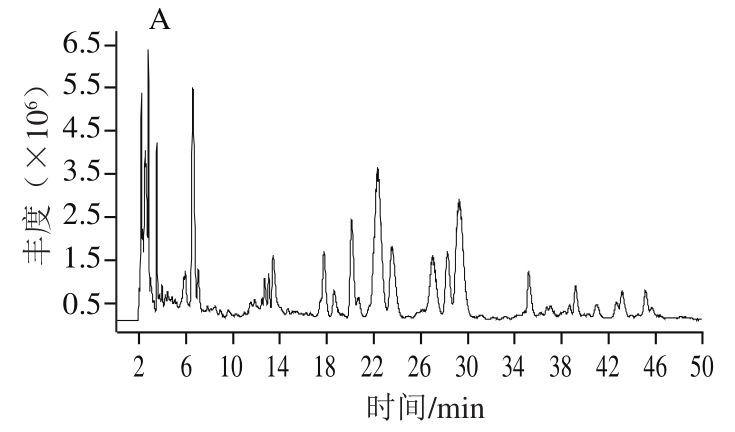
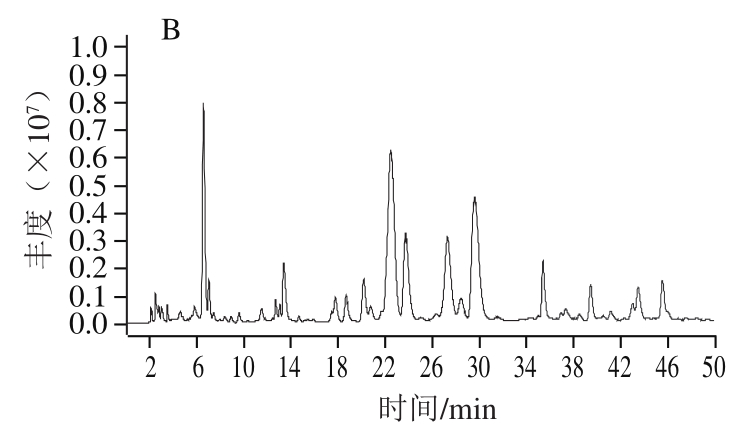
图 5 正(A)、负(B)离子模式下总离子流图
Fig. 5 Total ion current chromatograms of burdock extract in the positive (A) and negative ion (B) modes
在优化HPLC条件下,采用Q-TOF-MS技术对目标化合物进行鉴别。根据获得化合物的精确分子质量信息与DAD获得的紫外吸收信息,对相对含量0.5%以上的咖啡酸及其衍生物进行鉴别,结果见表1。参考文献[30-32]并与山东省分析测试中心国家天然产物参比实验室自有的绿原酸、咖啡酸、1,5-O-二咖啡酰奎宁酸、绿原酸甲酯、3,4-O-二咖啡酰奎宁酸、3,5-O-二咖啡酰奎宁酸、1,3-O-二咖啡酰奎宁酸、4,5-O-二咖啡酰奎宁酸、1,5-O-二咖啡酰-3-O-琥珀酰奎宁酸共9 种对照品进行比对,对照品的色谱峰分别对应图3中的峰1、2、3、4、6、7、8、11和峰12共9 个化合物。峰5、9和峰10分子质量相同,根据极性大小和二咖啡酰奎宁酸的出峰顺序推断峰5为1,5-O-二咖啡酰-3-O-苹果酰奎宁酸,峰9为3,4-O-二咖啡酰-3-O-苹果酰奎宁酸,峰10为3,5-O-二咖啡酰-3-O-苹果酰奎宁酸。峰13分子质量与峰5、峰9和峰10相差14,相差的基团为—CH2—,根据参考文献[33]和已发现化合物的信息推断峰13为1,5-O-二咖啡酰-3-O-苹果酸甲酯奎宁酸。峰15为二咖啡酰奎宁酸甲酯,筛选范围为1,3-O-二咖啡酰奎宁酸甲酯、3,4-O-二咖啡酰奎宁酸甲酯、3,5-O-二咖啡酰奎宁酸甲酯和4,5-O-二咖啡酰奎宁酸甲酯中的一种,考虑到成键的顺序和甲酯基团引起的极性差异,推断该化合物为3,4-O-二咖啡酰奎宁酸甲酯。峰14和峰16相对分子质量相差14,相差的基团为—CH2—,从已发现琥珀酸在类似结构中的取代情况推断峰14为1,5-O-二咖啡酰-4-O-琥珀酰奎宁酸,峰16为1,5-O-二咖啡酰-4-O-琥珀酰甲酯奎宁酸。峰17为三咖啡酰-奎宁酸乙酯,峰18、19分别为三咖啡酰-苹果酰奎宁酸和三咖啡酰-琥珀酰奎宁酸的同分异构体,由于三咖啡酰-奎宁酸化合物目前发现有1,3,5-O-三咖啡酰奎宁酸、1,4,5-O-三咖啡酰奎宁酸和3,4,5-O-三咖啡酰奎宁酸3 种,结构中可结合苹果酸和琥珀酸的羟基较多,难以确定具体结合位点,因此峰17~19只能归属到三咖啡酰奎宁酸类化合物衍生物的范畴。
本研究建立在线筛选鉴定抗氧化活性成分方法,实现牛蒡乙酸乙酯相中抗氧化活性成分的在线筛选与鉴定,结果显示牛蒡中重要的抗氧化成分主要为咖啡酰奎宁酸类化合物。本方法快速、准确,与紫外分光光度计法和传统天然产物中复杂成分的分离与鉴别模式相比,具有更高的筛选效率;与前期的MS鉴定方法比较,新增活性筛查以及采用部分对照品进行确证,从而保证结果更加准确。由于咖啡酰奎宁酸类化合物结构类似且存在多种同分异构体,在无对照品的前提下,即使通过多级质谱也难以实现精准鉴定。对于未明确具体名称的咖啡酰奎宁酸类化合物,需在后期研究中通过多种色谱技术制备获得高纯度单体,结合核磁共振二维谱实现结构确证。
[1] 杨玲, 王小龙. 牛蒡保健食品开发的研究进展[J]. 中国食物与营养,2015, 21(11): 23-26.
[2] 王晓娟, 蒋林. 牛蒡根HPLC指纹图谱和抗氧化活性谱效研究[J]. 中药材, 2014, 37(12): 2195-2197. DOI:10.13863/j.issn1001-4454.2014.12.018.
[3] 刘萍. 牛蒡的开发利用现状及展望[J]. 食品研究与开发, 2013,34(15): 128-130. DOI:10.3969/j.issn.1005-6521.2013.15.034.
[4] 陈世雄, 陈靠山. 牛蒡根化学成分及活性研究进展[J]. 食品与药品,2010, 12(7): 281-285. DOI:10.3969/j.issn.1672-979X.2010.04.018.
[5] 张婷, 杨润强, 陈旭, 等. 护色保脆复配物对鲜切牛蒡品质及酶促褐变的影响[J]. 食品科学, 2014, 35(4): 236-242. DOI:10.7506/spkx1002-6630-201404048.
[6] 何虎翼, 甘秀芹, 陆柳英, 等. 不同牛蒡品种根的营养品质分析[J].中国蔬菜, 2011, 1(6): 73-75.
[7] 王海东, 吴文华, 王印, 等. 牛蒡成分提取、活性研究及加工利用概述[J]. 食品工业, 2014, 35(4): 164-167.
[8] CHEN F A, WU A B, CHEN C Y. The influence of different treatments on the free radical scavenging activity of burdock and variations of its active components[J]. Food Chemistry, 2004, 86(4): 479-484.DOI:10.1016/j.foodchem.2003.09.020.
[9] 李玉洁, 刘树民, 李淑莲, 等. 牛蒡根抗衰老作用的实验研究[J]. 时珍国医国药, 2004, 15(9): 545-546. DOI:10.3321/j.issn:1001-1668.2004.08.033.
[10] WANG B S, YEN G C, CHANG L W, et al. Protective effects of burdock (Arctium lappa Linne) on oxidation of low-density lipoprotein and oxidative stress in RAW 264.7 macrophages[J]. Food Chemistry,2007, 101(2): 729-738. DOI:10.1016/j.foodchem.2006.01.051.
[11] 魏东. 牛蒡抗氧化、降血脂保健功能研究[J]. 食品科学, 2008,29(7): 380-382. DOI:10.3321/j.issn:1002-6630.2008.02.084.
[12] 胡喜兰, 许瑞波, 姜琴, 等. 牛蒡根中抗氧化活性和黄酮含量的测定[J]. 食品科技, 2012, 37(12): 184-188. DOI:10.13684/j.cnki.spkj.2012.12.061.
[13] 马利华, 秦卫东, 陈学红, 等. 牛蒡皮提取物抗氧化活性及组成的研究[J]. 中国食品学报, 2011, 11(9): 23-29. DOI:10.3969/j.issn.1009-7848.2011.08.004.
[14] MARUTA Y, KAWABATA J, NIKI R. Antioxidative caffeoylquinic acid derivatives in the roots of burdock (Arctium lappa L.)[J]. Journal of Agricultural and Food Chemistry, 1995, 43(10): 2592-2595.DOI:10.1021/jf00058a007.
[15] FERRACANE R, GRAZIANI G, GALLO M, et al. Metabolic profile of the bioactive compounds of burdock (Arctium lappa) seeds, roots and leaves[J]. Journal of Pharmaceutical and Biomedical Analysis,2010, 51(2): 399-404. DOI:10.1016/j.jpba.2009.03.018.
[16] 蒋晓文, 白俊鹏, 田星, 等. 牛蒡根中黄酮苷类化学成分及其抗氧化活性构效关系的研究[J]. 中草药, 2016, 47(5): 726-731.DOI:10.7501/j.issn.0253-2670.2016.05.006.
[17] ZHENG Z J, WANG X, LIU P L, et al. Semi-preparative separation of ten caffeoylquinic acid derivatives using high speed countercurrent chromatogaphy combined with semi-preparative HPLC from the roots of burdock (Arctium lappa L.)[J]. Molecules, 2018, 23: 429.DOI:10.3390/molecules23020429.
[18] 杨剀舟, 翟晓娜, 王佳良, 等. 绿原酸协同抗氧化机理的电化学和光谱-色谱学研究[J]. 光谱学与光谱分析, 2016, 36(8): 2405-2413.DOI:10.3964/j.issn.1000-0593(2016)08-2405-09.
[19] JIANG X W, BAI J P, ZHANG Q, et al. Caffeoylquinic acid derivatives from the roots of Arctium lappa L. (burdock) and their structureactivity relationships (SARs) of free radical scavenging activities[J].Phytochemistry Letters, 2016, 15: 159-163. DOI:10.1016/j.phytol.2015.12.008.
[20] 李成檀, 张丽慧, 赵建波, 等. 咖啡酸对氧化应激诱导的PC12细胞5-脂氧酶激活的抑制作用[J]. 中国药理学与毒理学杂志, 2011,25(1): 45-51. DOI:10.3867/j.issn.1000-3002.2011.01.009.
[21] AUBERT J, BEGRICHE K, KNOCKAERT L, et al. Increased expression of cytochrome P450 2E1 in nonalcoholic fatty liver disease: mechanisms and pathophysiological role[J]. Clinics and Research in Hepatology and Gastroenterology, 2011, 35(10): 630-637.DOI:10.1016/j.clinre.2011.04.015.
[22] CHTIOUI H, SEMELA D, LEDERMANN M, et al. Expression and activity of the cytochrome P450 2E1 in patients with nonalcoholic steatosis and steatohepatitis[J]. Liver International, 2007, 27(6): 764-771. DOI:10.1111/j.1478-3231.2007.01524.x.
[23] 黎文卓, 刘亚云, 陈勇. 高浓度绿原酸对L02细胞脂质堆积与氧化应激损伤的影响[J]. 中草药, 2017, 48(21): 4471-4477. DOI:10.7501/j.issn.0253-2670.2017.21.017.
[24] LIN L Z, HARNLY J M. Identification of hydroxycinnamoylquinic acids of arnica flowers and burdock roots using a standardized LC-DAD-ESI/MS profiling method[J]. Journal of Agricultural and Food Chemistry, 2008, 56(21): 10105-10114. DOI:10.1021/jf802412m.
[25] JAISWAL R, KUHNERT N. Identification and characterization of five new classes of chlorogenic acids in burdock (Arctium lappa L.)roots by liquid chromatography/tandem mass spectrometry[J]. Food &Function, 2011, 2(1): 63-71. DOI:10.1039/c0fo00125b.
[26] 王媛媛, 马飞祥, 李凤英, 等. 在线色谱联用技术检测天然产物抗氧化活性的研究进展[J]. 北方药学, 2016, 13(9): 123-125.
[27] 王虹, 陈军辉, 赵恒强, 等. 高效液相色谱-质谱-二苯基三硝基苯肼在线筛选与鉴别茶叶中抗氧化活性成分[J]. 分析化学, 2009, 37(6):795-800. DOI:10.3321/j.issn:0253-3820.2009.06.003.
[28] 张强, 张京芳, 苏印泉. HPLC在线检测果汁抗氧化成分[J]. 食品科学, 2013, 34(12): 165-170. DOI:10.7506/spkx1002-6630-201312035.
[29] 耿丹丹, 董琦, 谭亮, 等. HPLC-DAD-ESI/MSn-DPPH在线筛选与鉴别丹参和康定鼠尾草中抗氧化活性成分[J]. 分析测试学报, 2015,34(3): 314-320. DOI:10.3969/j.issn.1004-4957.2015.03.010.
[30] 赵昱, 赵军, 李湘萍, 等. 咖啡酰奎尼酸类化合物研究进展[J]. 中国中药杂志, 2006, 31(11): 869-874. DOI:10.3321/j.issn:1001-5302.2006.11.001.
[31] 席利莎, 木泰华, 孙红男. 绿原酸类物质的国内外研究进展[J]. 核农学报, 2014, 28(2): 292-301. DOI:10.11869/j.issn.100-8551.2014.02.0292.
[32] LOU Z X, WANG H X, ZHU S, et al. Improved extraction and identification by ultra performance liquid chromatography tandem mass spectrometry of phenolic compounds in burdock leaves[J].Journal of Chromatography A, 2010, 1217(16): 2441-2446.DOI:10.1016/j.chroma.2009.12.022.
[33] 白俊鹏, 胡晓龙, 蒋晓文, 等. 牛蒡根中咖啡酸类化学成分及其神经保护活性研究[J]. 中草药, 2015, 46(2): 163-168. DOI:10.7501/j.issn.0253-2670.2015.02.002.
On-line Screening for and Identification of Antioxidant Compounds from Burdock Roots (Arctium lappa L.) by High Performance Liquid Chromatography-Quadrupole Time-of-Flight Mass Spectrometry