许多食品属于水包油(O/W)型乳液体系,如牛奶、饮料、调味酱和调味品等,是热力学不稳定体系,经常出现聚结、絮凝和脂质氧化等问题[1]。氧化会影响以乳状液形式存在的食品稳定性[2],导致感官品质劣变[3],出现如气味难闻、营养素降解和色泽变化等现象[4]。
高压处理可以改变大豆分离蛋白(soy protein isolate,SPI)的天然构象,影响其诸多功能特性[5]。Wang Xiansheng等[6]研究发现,高压处理会使球蛋白的结构展开,同时伴随着亚基的解离与重聚,显著改善球蛋白的溶解性、乳化性等特性。高压均质技术可以提高食品加工的效率[7],还能显著提高乳液体系的物理和微生物稳定性[8],有利于乳液食品的贮存。
乳液流变学特性与其内部体系紧密相关,乳液的流变行为也能够反映乳液稳定性[9]。目前关于SPI乳液流变学特性的研究和报道越来越多,Rosech等[10]研究通过高压均质处理的大豆浓缩蛋白乳液流变学特性,发现乳液能够形成凝胶网络结构,且稳定性增强。Liu Fu等[11]研究发现,超高压处理SPI乳液可以通过增加乳化能量输入,促进凝胶网络结构的形成。目前提高SPI氧化稳定性主要是通过添加抗氧化剂、表面活性剂等方式,李秋慧等[12]采用酶法改性磷脂,通过添加适量的改性磷脂提高大豆蛋白的氧化稳定性。关于高压均质对SPI氧化稳定性的影响研究较少,Fernández-Ávila等[13]研究发现,经过超高压(100~300 MPa)处理大豆蛋白乳液,300 MPa处理后的乳液氧化稳定性下降,脂质氧化乳剂强烈依赖于油滴中油相的体积分数和蛋白质附着。本实验主要研究了不同均质次数对SPI乳液体系平均粒径、乳析指数、界面蛋白吸附量、流变学特性以及氧化稳定性的影响,并通过光学显微镜对SPI乳液进行观察,以期为高稳定型乳液食品的实际生产提供理论依据。
1 材料与方法
1.1 材料与试剂
大豆由东北农业大学大豆研究所提供;大豆油 九三粮油工业集团有限公司;三氯乙酸 永华精细化学品有限公司;十二烷基硫酸钠、Tris 美国Sigma公司;四乙氧基丙烷 天津市光复精细化工研究所;其他试剂均为国产分析纯。
1.2 仪器与设备
T18 Basic型高速分散机/匀浆机 德国IKA公司;LD4-2A型低速离心机 北京医用离心机厂;AVP-2000型高压均质机 英国Stansted Fluid Power公司;Mastersizer 2000型激光粒度分析仪、Bohlin Gemini 2型旋转流变仪 英国Malvern公司;ALPHA1-4 LSC型冷冻干燥机 德国Christ公司;YS100型生物显微镜 日本Nikon 公司;HYP-314型消化炉、KDN-102C型定氮仪 上海纤检仪器有限公司。
1.3 方法
1.3.1 SPI的制备
根据Sorgentini等[14]方法制备SPI。大豆粉碎并过60 目筛,用索氏提取器经过乙醚提取后获得脱脂豆粕。再将脱脂豆粕与蒸馏水以体积比1∶10混合。用2 mol/L NaOH溶液调至pH 8.5,室温搅拌2 h。4 000h g离心2 min,取上清液,用2 mol/L HCl溶液调至pH 4.5,将样品置于4 ℃条件下静置过夜,4 000h g离心5 min,将获得的沉淀物水洗两次,复溶后调至pH 7.0,倒平板, -18 ℃预冻后进行冷冻干燥。
1.3.2 乳液的制备
将SPI溶于0.2 mol/L磷酸盐缓冲液(pH 7.0),配制质量浓度为5 mg/mL的蛋白溶液,加入叠氮化钠 (0.02 g/mL),室温搅拌2 h,水化过夜。加入体积分数为20%大豆油,使用分散机处理1 min,转速为 10 800 r/min,得到初乳液。然后以120 MPa均质压力处理,均质循环次数分别为0(未处理)、1、2、3、4 次,每次5 s。分别贮藏0、2、4、6、8、12 d。
1.3.3 粒径测定
将处理后的SPI样品分别用去离子水稀释至质量浓度1 mg/mL,在粒度测定仪上进行测定,参数设置为:颗粒折射率(1.460),分散剂折射率(1.330)。
1.3.4 乳析指数的测定
参照Firebaugh等[15]的方法稍作修改,测定乳液的乳析指数。取10 mL乳液置于玻璃管中(高度12 cm、直径1.5 cm),密闭保存。室温贮藏10 d,观察乳液的状态,上层为乳析层,下层为清液层。乳析指数计算公式 如式(1)所示。
式中:Hs为下层清液高度/cm;Ht为整个乳液的 高度/cm。
1.3.5 光学显微镜观察
将不同高压均质次数处理后的乳液振荡混合均匀,取少量新鲜乳液置于载玻片的中心,盖上盖玻片,将其置于光学显微镜的观察区,将放大倍数调整为100 倍,观察乳液的微观结构。
1.3.6 界面蛋白吸附量的测定
根据Desrumaux等[16]的方法略作改动,取50 mL待测乳液于离心管中,室温下离心(15 000h g、45 min),用注射器小心吸取底部清液于另一离心管中,再次离心(15 000h g、45 min),收集下层清液,用凯氏定氮法测定清液中的蛋白含量Ci(CNh 6.25),界面蛋白吸附量(C)的计算公式如式(2)所示。
式中:C0为初始乳液中蛋白的含量/(mg/mL); Ci为乳状液中未吸附蛋白的含量/(mg/mL)。
1.3.7 表观黏度的测定
取样品于旋转流变仪感应板上,平板直径为40 mm,间距为15 mm,剪切速率0.01~100 s-1,选取30 个取样点,温度为25 ℃,平衡时间为1 min。测试前需将待测样品置于室温下放置30 min,取2 mL乳液于平板间隙并在样品四周覆盖硅油。
1.3.8 G’和G”的测定
取样品于旋转流变仪感应板上,平板直径为40 mm,检测间隙为15 mm,在应变力为0.5%的条件下进行频率扫描,频率范围为0.1~10 Hz,测定温度为25 ℃,以角频率为横坐标,弹性模量(G’)和黏性模量(G”)为纵坐标,绘制曲线。
1.3.9 氧化稳定性的测定
1.3.9.1 初级氧化产物
氢过氧化物值的测定参考Shao Yun等[17]的方法并稍加修改,将添加0.02 g/mL叠氮化钠的乳液分装在密封玻璃试管中,于50 ℃烘箱中加速氧化。隔天取出,进行氢过氧化物值的测定。具体方法为:将异辛烷和异丙醇按照体积比3∶1混合,即为溶剂1。将甲醇和丁醇按照体积比2∶1混合,即为溶剂2。取0.2 mL样品,加入1.5 mL溶剂1。充分振摇,3 400h g离心2 min,吸取200 μL上层有机相,加入2.8 mL溶剂2混匀。加入0.3 g/mL硫氰酸铵和亚铁离子溶液(0.264 moL/L氯化钡和0.288 mol/L硫酸亚铁混合后离心)各15 μL,室温静置20 min,于510 nm波长处测吸光度。用过氧化氢作标准曲线并计算样品中的氢过氧化物值。
1.3.9.2 次级氧化产物
硫代巴比妥酸反应产物(thiobarbituric acid reactive substances,TBARS)值的测定参考Sørensen等[18]的方法,取3 mL乳液于试管中,加入6 mL三氯乙酸试剂(7.5 g/mL)混合并漩涡混匀,将得到的混合物用1 μm微孔滤膜过滤,取2 mL滤液置于含有硫代巴比妥酸试剂(0.8 g/mL)的试管中,混合均匀。将混合物95 ℃水浴15 min处理,然后立即在冰水浴中冷却,在532 nm波长处记录最终提取物的吸光度。乳液中TBARS值通过1,1,3,3-四乙氧基丙烷标准曲线进行计算。
1.4 数据统计与分析
所有的实验重复3 次,结果用平均值±标准差表示,采用SPSS 19.0软件对实验数据进行方差分析 (P<0.05);采用Origin 9软件作图。
2 结果与分析
2.1 高压均质对SPI乳液粒径的影响

图 1 均质次数对SPI乳液平均粒径的影响
Fig. 1 Effect of homogenization cycles on average particle size of SPI-stabilized emulsion
高压均质处理对SPI乳液平均粒径的影响如图1所示,不同均质次数处理后样品的平均粒径均低于未处理样品。随着均质次数的增加,体积平均粒径先减小后缓慢增加。在均质3 次时,乳液体系平均粒径达到最小值(0.73 μm),说明高压均质处理会导致SPI乳液粒径降低,随着均质次数的增加效果更好。增加均质次数即增加了输入能量,Lizarraga等[19]发现,增加输入能量,乳状液粒径分布向低粒径趋势转移,即乳滴粒径减小。均质4 次时,乳滴粒径增大,可能是乳液发生“过处理” 现象[20],由于高压处理使乳滴粒径过小,颗粒之间布朗运动速率加快,增加了相互碰撞的次数,从而破坏界面膜,导致蛋白质聚集;同时,高压均质作用也会引起蛋白变性[16],蛋白相互作用导致聚集,从而使溶解度下降,蛋白从界面脱落,阻碍了均质对液滴的破坏,减弱了均质的效果[21]。
2.2 SPI乳液的微观结构
不同均质次数处理的SPI乳液显微结构如图2所示,乳滴以絮凝的形式存在,未经处理的乳液油滴数目多,且大小不均一,说明发生了聚结现象,乳液不稳定。经均质处理1~2 次时,仍可见较小尺寸的油滴,但并未有强烈的聚结现象(大尺寸油滴)。在均质3~4 次时均未出现油滴,乳液的粒径明显减小,说明高压均质作用可以阻止聚结现象的发生。


图 2 不同均质次数处理SPI乳液的光学显微结构图
Fig. 2 Optical microstructure of SPI-stabilized emulsion subjected to different homogenization cycles
2.3 高压均质对SPI乳液乳析指数的影响

图 3 均质次数对SPI乳液的乳析指数的影响
Fig. 3 Effect of homogenization cycles on creaming index of SPI-stabilized emulsion
图3为贮存10 d后不同高压均质次数处理条件下乳液的乳析指数,未经高压均质处理的初乳液乳析指数最高,为67.64%;高压均质处理后的乳液乳析指数较未处理乳液大幅下降,均质3 次和4 次时未发生乳析现象,说明高压均质处理能够提高乳液稳定性。Fernández-Ávila等[13] 也在研究中发现,利用高压均质技术能生产出物理稳定性较高的SPI乳液。其原因可能是随着高压均质次数的增加,蛋白乳液被高压剪切力切割形成小分子,使蛋白颗粒粒径减小,更多的蛋白吸附至油-水界面,为液滴间提供足够的排斥力,从而阻止乳层析的发生,使蛋白乳液的贮存稳定性增强。Li Jinlong等[22]研究指出,乳液粒径减小、比表面积增加,液滴之间的摩擦力增加,乳液的黏度增大,使乳液聚合速率减缓,从而提高乳液稳定性。这也解释了随均质次数的增加乳液表观黏度增加这一变化趋势产生的原因。
2.4 高压均质对SPI乳液界面蛋白吸附量的影响
界面的蛋白含量对乳状液的稳定性有重要影响[23]。界面蛋白吸附量越高,蛋白吸附至水-油界面的能力越强。均质次数对SPI乳液界面蛋白吸附量影响结果如图4所示,高压均质处理1~4 次后,其界面蛋白吸附量分别为93.32%、94.14%、95.63%、94.31%,显著高于未经处理的乳液(86.73%)。高压均质处理能够提高蛋白的柔性结构[24],使蛋白空间结构展开,更多的疏水基团暴露,促使更多的蛋白吸附到油-水界面,并在乳液界面形成蛋白膜,故高压均质处理可以提高界面蛋白吸附量[25]。界面蛋白吸附量随着均质次数的增加而先增加后降低,均质4 次时略有降低,可能是因为界面膜已经达到蛋白的最大吸附量。当界面蛋白吸附量达到一定值时,蛋白之间的相互作用反而抑制连续相中蛋白的进一步吸附[26]。
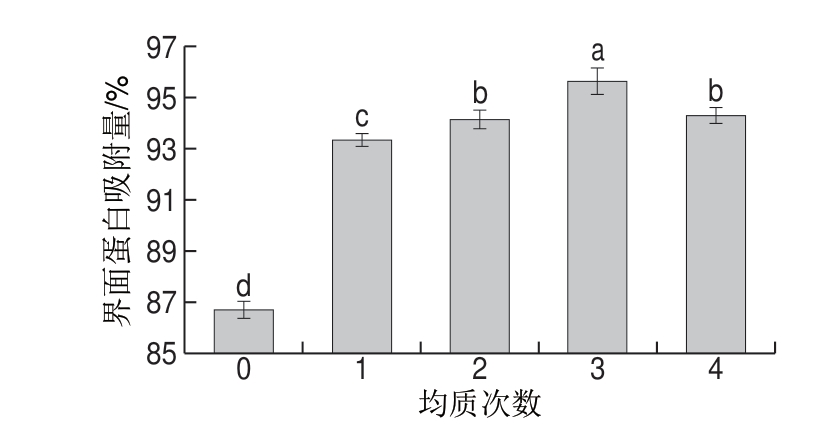
图 4 均质次数对SPI乳液界面蛋白吸附量的影响
Fig. 4 Effect of homogenization cycles on interfacial protein adsorption of SPI-stabilized emulsion
2.5 高压均质对SPI乳液表观黏度的影响

图 5 不同均质次数SPI乳液的表观黏度随剪切速率的变化
Fig. 5 Apparent viscosity versus shear rate curves of emulsion subjected to different homogenization cycles
根据Stoke定律,当乳液体系黏度较大时,液滴的上浮速率减缓,有利于乳液保持更好的稳定性[27]。由图5可以看出,经高压均质处理的乳液表观黏度随剪切速率的增加而下降,发生了非牛顿流体的剪切稀化现象[28]。在未受到剪切力时,流体分子间相互缠结在一起;在剪切力的作用下,流体动力将破坏体系中的絮凝物,聚集的脂肪球破碎,液滴定向排布阻力减小,乳液表观黏度减小。剪切速率增加到一定值后,分子间排列完成,黏度不再变化[29]。
乳液表观黏度随均质次数增加呈先升高后降低的趋势,均质3 次的乳液表观黏度最大,这与乳析指数的结果一致。随着均质次数的增加,乳液粒径减小,分散相中液滴数目增加,两个液滴进入相互吸引区的机会迅速增加,从而使其位移困难,导致乳液表观黏度增大。当均质4 次时,乳液表观黏度反而降低。Perrier-Cornet等[30] 的研究表明,蛋白颗粒粒径较大容易导致蛋白质的聚集,随着蛋白颗粒粒径的增大,其聚集更加明显。这可能是由于随着均质次数的增多,体系出现了“过处理”效应,部分解离的SPI分子重新聚集,通过新的二硫键形成复杂的聚集体[31],从而使乳液表观黏度降低。
2.6 高压均质对SPI乳液剪切流变行为的影响
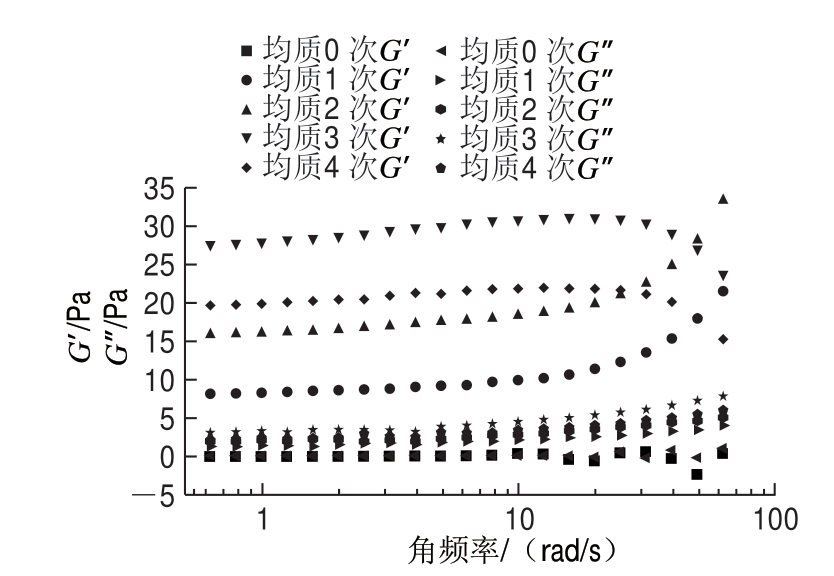
图 6 不同均质次数SPI乳液G’和G”随角频率的变化
Fig. 6 Curves of G’ and G” values versus angle frequency with different homogenization cycles
乳液的流变学性质可以反映乳液分散体系的贮藏稳定性[32]。G’和G”的变化趋势如图6所示,未处理的乳液G’和G”很小,接近0 Pa。但经高压均质处理后,乳液G’和G”明显增加,表明高压均质处理可以提高乳液的G’和G”。处理后乳液的G’都大于相应的G”,表现出明显的弹性行为,表明以弹性为主的凝胶状网络结构形成。随着均质次数的增加,G’和G”呈先增加后降低的趋势,当均质3 次时,G’和G”最大。这与乳析指数的结果一致。当均质4 次时,乳液均质发生“过处理”现象,蛋白质相互作用并发生聚集,由于空间位阻作用抑制了后续吸附蛋白质的去折叠,从而使蛋白质分子间的相互作用位点不易接近,减小了G’和G”[33]。高压均质作用提高了SPI的表面疏水性和柔性[34],蛋白质通过疏水作用结合,增加了G’[35]。同时,高压均质作用使乳液粒径降低,更多的蛋白颗粒吸附到油-水界面上,由于蛋白颗粒对油滴的稳定作用,蛋白形成稳定的网络结构,从而提高乳液黏度,并增加了乳液的G’,进而增强了乳液稳定性。
2.7 高压均质对SPI乳液氧化稳定性的影响
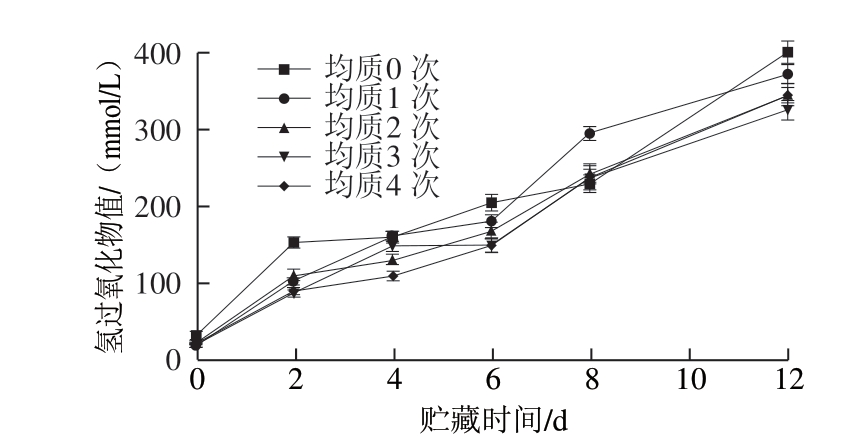
图 7 高压均质对SPI乳液初级氧化产物的影响
Fig. 7 Effect of high pressure homogenization on hydroperoxide value of SPI-stabilized emulsion

图 8 高压均质对SPI乳液TBARS值的影响
Fig. 8 Effect of high pressure homogenization on TBARS value of SPI-stabilized emulsion
如图7、8所示,随着贮存时间的延长,脂肪氧化程度逐渐加深,蛋白乳液的氢过氧化物值增加,体系TBARS值呈现先增加后减少再增加的趋势。氢过氧化物能够被分解转化为次级氧化产物[36],从而导致TBARS值增加。当贮存4 d时,氧化过程中部分次级氧化产物可能转化为其他氧化成分[37],从而使TBARS值下降。在贮存6 d后,TBARS值再次增加,可能是由于氢过氧化物含量增加较快且极易分解,其分解速率大于次级氧化产物的分解速率。
高压均质处理样品的氢过氧化物值和TBARS值均低于未处理样品,在均质3 次时,其氢过氧化物值和TBARS值均最低。这是由于高压均质处理使蛋白颗粒减小,更多的蛋白吸附至油-水界面并维持乳液稳定,在水相和油相之间形成空间位阻。此外,乳液中的蛋白质吸附在油滴表面后形成一层黏弹性蛋白膜,蛋白膜可以有效阻止脂质氧化的引发剂扩散到油滴内部,同时限制水相中的过渡金属与油相相互作用,从而起到抑制油脂氧化的作用[17]。Ries[38]和Mei Longyuan[39]等的研究也表明,粒径较小的乳液在贮藏过程中测得的脂质过氧化物和挥发性脂质氧化产物含量都更少。因此,均质3 次时,乳液体系的氧化稳定性更佳。
3 结 论
随均质次数的增加,乳液粒径先减小后增加,乳析指数呈降低趋势,在均质3 次和4 次时未发生乳析现象,表明乳液体系稳定性更好。根据微观结构观察结果,随着均质次数的增加,油滴尺寸逐渐减小至消失,乳滴粒径逐渐减小,且分布逐渐均匀,说明高压均质作用可以阻止聚结现象发生。
随着均质次数的增加,界面蛋白吸附量、表观黏度、G’和G”均呈先增加后减小的趋势,在均质3 次时达到最大,说明此时乳液体系的稳定性最佳。剪切流变学特性实验结果说明高压均质处理的乳液具有良好的动力学稳定性。
高压均质处理的样品氢过氧化物值和TBARS值均低于未处理样品,说明高压均质作用能够抑制脂肪氧化。随着贮存时间的延长,乳液体系的氢过氧化物值增加,TBARS值呈现先增加后减少再增加的趋势。当均质3 次时,乳液体系的氢过氧化物值和TBARS值最低,即氧化稳定性更佳。
[1] LIANG Y, GILLIES G, PATEL H. Physical stability, microstructure and rheology of sodium-caseinate-stabilized emulsions as influenced by protein concentration and non-adsorbing polysaccharides[J]. Food Hydrocolloids, 2014, 36(2): 245-255. DOI:10.1016/j.foodhyd.2013.10.006.
[2] CALLIGARIS S, MANZOCCO L, NICOLI M C. Modelling the temperature dependence of oxidation rate in water-in-oil emulsions stored at sub-zero temperatures[J]. Food Chemistry, 2007, 101(3): 1019-1024. DOI:10.1016/j.foodchem.2006.02.056.
[3] VERCELLOTTI J R, ANGELO A J, SPANIER A M. Lipid oxidation in foods: an overview[M]. Washington DC: American Chemical Society, 1992: 175-224. DOI:10.1002/chin.199307316.
[4] SHAHIDI F, ZHONG Y. Lipid oxidation and improving the oxidative stability[J]. Chemical Society Reviews, 2010, 39(11): 4067-4079. DOI:10.1039/b922183m.
[5] SUBIRADE M, LOUPIL F, ALLAIN A F, et al. Effect of dynamic high pressure on the secondary structure of β-lactoglobulin and on its conformational properties as determined by Fourier transform infrared spectroscopy[J]. International Dairy Journal, 1998, 8(2): 135-140. DOI:10.1016/s0958-6946(98)00034-x.
[6] WANG Xiansheng, TANG Chuanhe, LI Biansheng, et al. Effects of high-pressure treatment on some physicochemical and functional properties of soy protein isolates[J]. Food Hydrocolloids, 2008, 22(4): 560-567. DOI:10.1016/j.foodhyd.2007.01.027.
[7] SUGIURA S, NAKAJIMA M, YAMAMOTO K, et al. Preparation characteristics of water-in-oil-in-water multiple emulsions using microchannel emulsification[J]. Journal of Colloid & Interface Science, 2004, 270(1): 221-228. DOI:10.1016/j.jcis.2003.08.021.
[8] KAJIYAMA N, ISOBE S, UEMURA K, et al. Changes of soy protein under ultra-high hydraulic pressure[J]. International Journal of Food Science & Technology, 2010, 30(2): 147-158. DOI:10.1111/j.1365-2621.1995.tb01366.x.
[9] CAMILO A R, KOKINI J L. Effect of egg yolk and egg yolk + salt on rheological properties and particle size distribution of model oil-in-water salad dressing emulsions[J]. Journal of Food Science, 1988, 53(5): 1352-1354. DOI:10.1111/j.1365-2621.1988.tb09275.x.
[10] ROESCH R R, CORREDING M. Characterization of oil-in-water emulsions prepared with commercial soy protein concentrate[J]. Journal of Food Science, 2002, 67(8): 2837-2842. DOI:10.1111/j.1365-2621.2002.tb08825.x.
[11] LIU Fu, TANG Chuanhe. Emulsifying properties of soy protein nanoparticles: influence of the protein concentration and/or emulsification process[J]. Journal of Agricultural and Food Chemistry, 2014, 62(12): 2644-2654. DOI:10.1021/jf405348k.
[12] 李秋慧, 隋晓楠, 徐靓, 等. 酶法改性磷脂对大豆蛋白共建体系乳化稳定性及氧化稳定性的影响[J]. 食品科学, 2016, 37(23): 64-69. DOI:10.7506/spkx1002-6630-201623011.
[13] FERNÁNDEZ-ÁVILA C, TRUJILLO A J. Ultra-high pressure homogenization improves oxidative stability and rheological properties of soy protein isolate-stabilized emulsions[J]. Food Chemistry, 2016, 209: 104-113. DOI:10.1016/j.foodchem.2016.04.019.
[14] SORGENTINI D A, WAGNER J R. Comparative study of structural characteristics and thermal behavior of whey and isolate soybean proteins[J]. Journal of Food Biochemistry, 1999, 23(5): 489-507. DOI:10.1111/j.1745-4514.1999.tb00033.x.
[15] FIREBAUGH J D, DAUBERT C R. Emulsifying and foaming properties of a derivatized whey protein ingredient[J]. International Journal of Food Properties, 2005, 8(2): 243-253. DOI:10.1081/JFP-200060245.
[16] DESRUMAUX A, MARCAND J. Formation of sunflower oil emulsions stabilized by whey proteins with high pressure homogenization (up to 350 MPa): effect of pressure on emulsion characteristics[J]. International Journal of Food Science & Technology, 2002, 37(3): 263-269. DOI:10.1046/j.1365-2621.2002.00565.x.
[17] SHAO Yun, TANG Chuanhe. Characteristics and oxidative stability of soy protein-stabilized oil-in-water emulsions: influence of ionic strength and heat pretreatment[J]. Food Hydrocolloids, 2014, 37(2): 149-158. DOI:10.1016/j.foodhyd.2013.10.030.
[18] SØRENSEN G, JØRGENSEN S S. A critical examination of some experimental variables in the 2-thiobarbituric acid (TBA) test for lipid oxidation in meat products[J]. Zeitschrift für Lebensmittel-Untersuchung und Forschung, 1996, 202(3): 205-210. DOI:10.1007/bf01263541.
[19] LIZARRAGA M S, PAN L G, AÑON M C, et al. Stability of concentrated emulsions measured by optical and rheological methods. effect of processing conditions: I. whey protein concentrate[J]. Food Hydrocolloids, 2008, 22(5): 868-878. DOI:10.1016/j.foodhyd.2007.04.012.
[20] JAFARI S M, ASSADPOOR E, HE Y H, et al. Re-coalescence of emulsion droplets during high-energy emulsification[J]. Food Hydrocolloids, 2008, 22(7): 1191-1202. DOI:10.1016/j.foodhyd.2007.09.006.
[21] 毕爽, 李杨, 隋晓楠, 等. 高压均质对大豆蛋白-磷脂复合体系结构及理化/功能性质的影响[J]. 食品科学, 2017, 38(5): 148-153. DOI:10.7506/spkx1002-6630-201705024.
[22] LI Jinlong, QIAO Zhihong, TATSUMI E, et al. A novel approach to improving the quality of bittern-solidified tofu by W/O controlledrelease coagulant. 1: preparation of W/O bittern coagulant and its controlled-release property[J]. Food and Bioprocess Technology, 2013, 6(7): 1790-1800. DOI:10.1007/s11947-012-0896-4.
[23] IZMAILOVA V N, YAMPOLSKAYA G P, TULOVSKAYA Z D. Development of the Rehbinder’s concept on structure-mechanical barrier in stability of dispersions stabilized with proteins[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 1999, 160(2): 89-106. DOI:10.1016/s0927-7757(99)00361-1.
[24] 王喜波, 徐晔晔, 于洁, 等. 高压均质对大豆蛋白柔性和乳化性的影响及相关性分析[J]. 农业机械学报, 2018, 49(6): 362-367. DOI:10.6041/j.issn.1000-1298.2018.06.043.
[25] MANEEPHAN K, MILENA C. Heat-induced changes in oil-in-water emulsions stabilized with soy protein isolate[J]. Food Hydrocolloids, 2009, 23(8): 2141-2148. DOI:10.1016/j.foodhyd.2009.05.010.
[26] 孟凡欢. 燕麦品种及成分对燕麦乳稳定性的影响[D]. 天津: 天津科技大学, 2017: 43.
[27] 严成, 严夏. 枸杞多糖提取工艺比较及体外抗氧化性研究[J]. 食品科学, 2008, 29(17): 183-187. DOI:10.332 1/j.issn:1002-6630.2008.07.037.
[28] BOUTIN C, GIROUX H J, PAQUIN P, et al. Characterization and acid-induced gelation of butter oil emulsions produced from heated whey protein dispersions[J]. International Dairy Journal, 2007, 17(6): 696-703. DOI:10.1016/j.idairyj.2006.08.009.
[29] ZHAO Q, SELOMULYA C, WANG S Q, et al. Enhancing the oxidative stability of food emulsions with rice dreg protein hydrolysate[J]. Food Research International, 2012, 48(2): 876-884. DOI:10.1016/j.foodres.2012.07.004.
[30] PERRIER-CORNET J M, MARIE P, GERVAIS P. Comparison of emulsification efficiency of protein-stabilized oil-in-water emulsions using jet, high pressure and colloid mill homogenization[J]. Journal of Food Engineering, 2005, 66(2): 211-217. DOI:10.1016/j.jfoodeng.2004.03.008.
[31] APICHARTSRANGKOON A. Effects of high pressure on rheological properties of soy protein gels[J]. Food Chemistry, 2003, 80(1): 55-60. DOI:10.1016/s0308-8146(02)00235-2.
[32] ROMERO A, FELIPE C. Influence of pH on linear viscoelasticity and droplet size distribution of highly concentrated O/W crayfish flour-based emulsions[J]. Food Hydrocolloids, 2009, 23(2): 244-252. DOI:10.1016/j.foodhyd.2008.02.001.
[33] 彭伟伟. 热处理对豌豆蛋白乳化性质及界面吸附行为的影响[D]. 无锡: 江南大学, 2016: 31.
[34] XU Yeye, WNAG Guorong, WANG Xibo, et al. Effects of homogenization on the molecular flexibility and emulsifying properties of soy protein isolate[J]. Food Science & Biotechnology, 2018, 27(5): 1293-1299. DOI:10.1007/s10068-018-0361-x.
[35] FREER E M, YIM K S, FULLERULL G G, et al. Interfacial rheology of globular and flexible proteins at the hexadecane/water interface: comparison of shear and dilatation deformation[J]. The Journal of Physical Chemistry B, 2004, 108(12): 3835-3844. DOI:10.1021/jp037236k.
[36] WARNER K, MOUNTS T L. Frying stability of soybean and canola oils with modified fatty acid compositions[J]. Journal of the American Oil Chemists’ Society, 1993, 70(10): 983-988. DOI:10.1007/bf02543024.
[37] 侯留鑫. 三种抗氧化剂在不同体系中抗氧化能力的比较研究[D]. 南京: 南京师范大学, 2014: 50.
[38] RIES D, YE A, HAISMAN D, et al. Antioxidant properties of caseins and whey proteins in model oil-in-water emulsions[J]. International Dairy Journal, 2010, 20(2): 72-78. DOI:10.1016/j.idairyj.2009.09.001.
[39] MEI Longyuan, MCCLEMENTS D J, DECKER E A. Lipid oxidation in emulsions as affected by charge status of antioxidants and emulsion droplets[J]. Journal of Agricultural & Food Chemistry, 1999, 47(6): 2267-2273. DOI:10.1021/jf980955p.