冷鲜肉以其安全性、营养性、后熟速度及价格上的优势,成为了我国生肉消费的主流产品。然而,冷鲜肉在清洁处理和排酸切割过程中易被微生物污染[1],导致肉腐败变质,影响其安全性和营养性[2];所以对微生物含量的控制和微生物群落演替驱动机制的研究在冷鲜肉加工贮藏过程中具有重要意义。杨文婷等[3]对手抓羊肉在加工过程中减菌真空包装材料的选择及杀菌条件工艺参数进行了优化。赵光辉[4]对冷却猪肉在分割过程中微生物污染和增殖情况进行了研究。随着多组学技术的发展,可以从宏基因组学、蛋白组学、代谢组学等方面对微生物的菌种及其代谢途径、代谢调控机制进行阐述[5]。Lu Dongmei等[6]发现参与戊糖磷酸途径的蛋白质过量表达会增加鸟氨酸产量,而影响鸟氨酸合成的鸟氨酸合成酶可能不能限制鸟氨酸产量。Wendler等[7]的研究表明不同条件下的蛋白质对糖转运途径产生影响,导致菌体代谢物的差异。慕春龙[8]发现高蛋白日粮增加了大鼠体内与炎症相关微生物代谢物的产生,且低蛋白氨基酸日粮对大鼠和仔猪的肠道微生物影响大于高蛋白日粮。代谢途径的变化会因代谢环境、代谢所需原料、酶活力等的变化而发生转变[9],Zampieri等[10]也研究发现部分代谢途径中的产物以及细菌所处的生长环境能够影响细菌代谢途径的变化。Muroya等[11]通过电喷雾电离飞行时间质谱联用(capillary electrophoresis with electrospray ionization time-of-flight mass spectrometry,CE-TOF-MS)的代谢组学分析法揭示了猪死后与肉质相关的关键化合物和代谢途径,并得出部分蛋白质会对代谢途径产生影响,从而导致代谢物变化。因此,微生物在代谢过程中蛋白质的变化对其代谢产物产生影响。而在冷鲜肉的贮藏过程中,对导致其变质的微生物在贮藏过程中发生怎样变化的研究相对较少。代谢组学作为一种系统生物学研究中十分有力的分析技术,可从整体角度出发对生命体系微妙的变化进行深入挖掘,为食品微生物的研究分析开拓了新的方向与思路[12-13]。
本课题组胡倩倩等[14]前期采用表面增强激光解吸电离飞行时间质谱(surface enhanced laser desorption ionization-TOF-MS,SELDI-TOF-MS)技术找出了冷鲜滩羊肉贮藏中微生物的菌体差异蛋白质,并通过气相色谱(gas chromatography,GC)-TOF-MS技术检测到了微生物主要差异代谢物[15]。本研究在此基础上通过分析冷鲜滩羊肉贮藏中微生物的菌体差异蛋白质及其差异代谢产物,研究二者的变化规律及代谢产物的代谢途径,采用热力图分析菌体蛋白质与代谢产物的关联性,研究因微生物群落演替形成的差异菌体蛋白质的变化在贮藏过程中与代谢产物的关系,及其对微生物代谢途径的影响。为深入探究微生物群落演替的内在驱动机制,通过抑制微生物新陈代谢和繁衍延长滩羊肉货架期及开发保鲜新技术提供理论参考。
1 材料与方法
1.1 材料
滩羊肉购自宁夏盐池县大夏牧场食品有限公司,当天屠宰切割后立刻密封包装放入冷藏箱,运回实验室后迅速放入-20 ℃冰箱1 h,使其中心温度降至0 ℃,后将其置于0 ℃冰箱中贮藏[16]。
1.2 仪器与设备
7890A气相色谱仪 美国Agilent公司;Chroma TO F P E G A S U S H T 质谱仪 美国L E C O 公司; JXFSTPRP-24研磨仪 上海净信科技有限公司;TGL-16M 高速冷冻台式离心机 湘仪离心机仪器有限公司;AE240分析天平 瑞士梅特勒公司。
1.3 方法
1.3.1 样品处理
无菌条件下,随机选取均等滩羊胴体分割(每块约10 g),保鲜膜密封包装,贮藏于0 ℃冰箱中,采集贮藏期分别为0、4、8、12 d的滩羊肉表面刮擦物150 mg(表面刮擦物含微生物、血液、肉汁液等[17])。每组样品3 个平行。
1.3.2 冷鲜滩羊肉贮藏过程中微生物菌体差异蛋白分析
参考胡倩倩等[14]的方法,采用SELDI-TOF-MS平台对贮藏0、4、8 d的滩羊肉微生物菌体差异蛋白进行检测、分析和筛选,得到微生物菌体蛋白质在贮藏期间的变化规律。
1.3.3 采用GC-TOF-MS技术分析冷鲜滩羊肉微生物差异代谢物
参考胡倩倩等[14]的方法,通过GC-TOF-MS技术对冷鲜滩羊肉微生物的代谢产物进行分析,找出冷鲜滩羊肉表面微生物分别在0、4、8、12 d 4 个贮藏时间点呈现出2 次差异的代谢产物,并以Similarity值大于900且 OPLS-DA模型变异权重系数VIP值大于1.0作为筛选标准,筛选出D-甘油酸、天冬酰胺、1-磷酸葡萄糖、5’-肌苷酸、核糖、乙酰苯胺、苯丙氨酸和天冬氨酸共8 种差异代谢产物,分析其在贮藏过程中的变化规律。
1.4 数据处理与分析
采用SPSS 22.0软件对滩羊肉在贮藏过程中微生物菌体蛋白质及代谢产物的变化规律进行分析。然后使用R软件的“Pearson”算法及SIMCA软件(V 14.1)对菌体蛋白质和代谢产物进行热力图分析,找出菌体蛋白质与代谢产物之间的关联性。并通过京都基因与基因组百科全书(Kyoto Encyclopedia of Genes and Genomes,KEGG)找出差异代谢物的代谢途径,研究冷鲜滩羊肉表面微生物的菌体蛋白质对其差异代谢物的影响。
2 结果与分析
2.1 冷鲜滩羊肉贮藏过程中菌体蛋白质及差异代谢物的变化规律
2.1.1 冷鲜滩羊肉贮藏过程中菌体蛋白质的变化规律
表 1 冷鲜滩羊肉微生物的菌体蛋白质相对含量在贮藏过程中的变化
Table 1 Changes in bacterial proteins on fresh Tan sheep meat during chilled storage

样品编号 蛋白质名称 蛋白质英文名称 ID 蛋白相对含量/%0 d 4 d 8 d M7823-80 生长调节α蛋白质 growth-regulated alpha protein A0A1V4JWG2 5.50f 0.21 4.97f 0.18 4.29f 0.18 M8414-05 坏死诱导疫霉蛋白质 necrosis-inducing phytophthora protein A0A0W8CRK9 6.11f 0.27 7.78f 0.24 9.17f 0.30 M10880-9 NADH-泛醌氧化还原酶链4L NADH-ubiquinone Oxidoreductase 4L P33602 6.01f 0.17 8.91f 0.27 9.75f 0.32 M3130-58 生长抑制素-28 somatostatin-28 O46688 5.06f 0.19 8.67f 0.23 10.23f 0.46 M5109-45 GRF/GHRH生长激素释放素growth hormone releasing factor P07217 10.04f 0.32 6.57f 0.19 4.14f 0.16 M6199-14 60S核糖体蛋白质L40 60S ribosomal protein L40 P14794 5.63f 0.22 5.02f 0.14 4.41f 0.17 M7451-79 抗菌肽 antibacterial peptide P85078 5.20f 0.16 5.98f 0.19 7.52f 0.21 M7668-64 ATP合酶F(0)复合体亚基C1 ATP synthase F(0) complex subunit C1 P68699 5.07f 0.17 6.00f 0.11 7.06f 0.39 M7709-26 ATP合成蛋白质8 ATP synthase subunit P0AB98 8.49f 0.24 6.36f 0.17 4.29f 0.13 M8136-55 载脂蛋白质C-II apolipoprotein C-II A0A3B4WGI6 5.25f 0.15 6.75f 0.15 7.93f 0.06 M9074-86 朊蛋白质类 prion protein P31658 5.22f 0.13 6.73f 0.14 8.52f 0.12 M11722-8 硫氧还蛋白质 thioredoxin P0AA25 6.01f 0.18 5.14f 0.22 4.75f 0.14 M11870-3 β2-微球蛋白质 β2-microglobulin Q6QAT4 5.50f 0.14 4.92f 0.16 4.19f 0.11 M12826-1 40S核糖体蛋白质S26 40S ribosomal protein S26 Q54TL8 5.76f 0.16 5.24f 0.21 4.62f 0.08 M34203-3 载脂蛋白质E apolipoprotein E P23930 8.99f 0.21 6.16f 0.24 4.58f 0.15 M38968-8 磷脂结合蛋白质 annexin V W5PSZ5 6.17f 0.16 4.80f 0.16 4.54f 0.04
采用SELDI-TOF-MS测得冷鲜滩羊肉在贮藏过程中微生物的16 个菌体蛋白质,从表1可看出,在贮藏过程中,菌体蛋白中的坏死诱导疫霉蛋白质、NADH-泛醌氧化还原酶链4L、生长抑制素-28、GRF/GHRH生长激素释放素、抗菌肽、ATP合酶F(0)复合体亚基C1、ATP合成蛋白质8、载脂蛋白质C-II、朊蛋白质类、载脂蛋白质E的相对含量随着贮藏时间延长出现明显的变化。说明冷鲜滩羊肉在贮藏过程中,微生物的菌体蛋白质在贮藏期间发生了明显变化。
2.1.2 冷鲜滩羊肉贮藏过程中差异代谢物的变化规律
采用GC-TOF-MS技术测得冷鲜滩羊肉贮藏过程中的30 种微生物胞内差异代谢物,以Similarity值大于900且OPLS-DA模型变异权重系数VIP值大于1.0作为筛选标准,筛选出8 种差异代谢物:D-甘油酸、1-磷酸葡萄糖、天冬酰胺、核糖、磷酸-5’-肌苷酸、乙酰苯胺3、天冬氨酸1、苯丙氨酸1,这8 种差异代谢物在贮藏期间的变化规律见图1。
图1表明,在冷鲜滩羊肉贮藏过程中,差异代谢物D-甘油酸、天冬酰胺4、核糖、天冬氨酸1、苯丙氨酸1相对含量随着贮藏时间的延长而增长,1-磷酸葡萄糖、磷酸-5’-肌苷酸、乙酰苯胺3相对含量随着贮藏时间延长而下降。其主要原因可能是在不同贮藏时间的优势菌发生演替变化,优势菌经过代谢途径中三羧酸循环、苯丙氨酸代谢、甘油酯代谢等,与其相关的差异代谢物相对含量出现了或增或减的趋势[16]。表1和图1结果表明冷鲜滩羊肉在贮藏中微生物在演替过程中发生了变化,采用热力图研究菌体蛋白质和代谢产物之间的关联性,以验证二者之间的关系。

图 1 冷鲜滩羊肉贮藏过程中微生物差异代谢物变化规律
Fig. 1 Changes of differential metabolites in bacteria of fresh Tan sheep meat during chilled storage
2.2 冷鲜滩羊肉贮藏过程中菌体蛋白质与代谢物的相关性分析
利用R软件的Spearman算法对冷鲜滩羊肉贮藏过程中微生物的菌体蛋白质与差异代谢物进行相关性分析,根据其相关性系数矩阵分析的结果和相关性P值矩阵分析的结果作热力图(图2)。
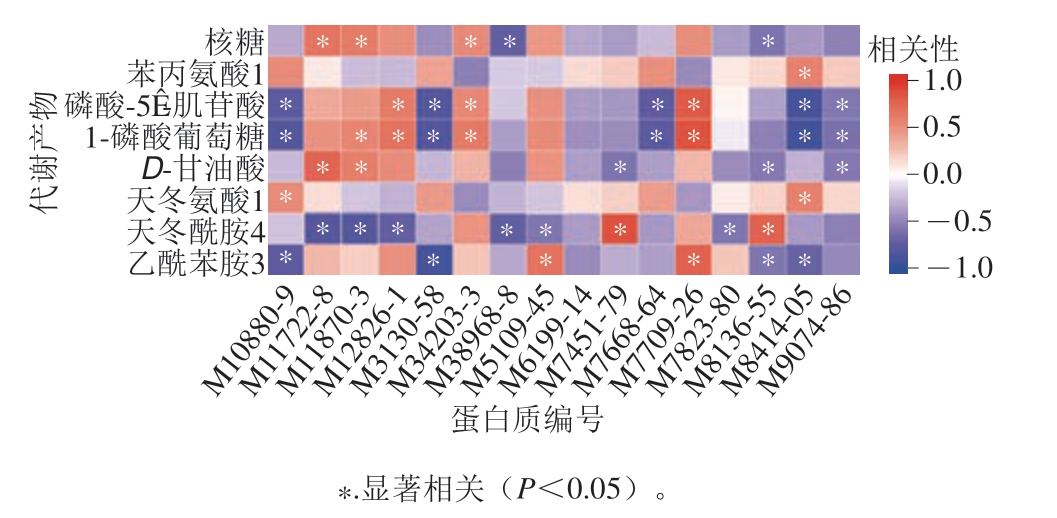
图 2 冷鲜滩羊肉贮藏过程中菌体蛋白质与其代谢物相关性热力图
Fig. 2 Heat map of bacterial proteins and metabolites in fresh Tan sheep meat during chilled storage
由图2可看出冷鲜滩羊肉贮藏过程中16 种菌体蛋白质与8 种代谢物的相关性。通过KEGG数据库查找这8 种代谢物的代谢通路,分析菌体蛋白质对代谢物产生的影响。结合冷鲜滩羊肉贮藏过程中菌体蛋白质和差异代谢物变化规律及二者之间的相关性可看出,微生物在生长代谢过程中,菌体蛋白质对与其相关联的代谢物的代谢过程产生着促进或抑制的作用,导致代谢物的种类及含量也发生变化。
苯丙氨酸代谢(map00360)会产生苯丙氨酸1[17],冷鲜滩羊肉在贮藏过程中苯丙氨酸1相对含量呈增长趋势,该变化可能与坏死诱导疫霉蛋白(M8414-05)相对含量随着贮藏时间延长而增长有关。
代谢途径为嘌呤代谢(map00230)的磷酸-5’-肌苷 酸[18-19],其相对含量随着贮藏时间延长呈下降趋势,其原因可能为,40S核糖体蛋白质S26(M12826-1)、载脂蛋白质E(M34203-3)、ATP合成蛋白质8(M7709-26)有利于代谢过程,NADH-泛醌氧化还原酶链4L(M10880-9)、 生长抑制素-28(M3130-58)、ATP合酶F(0)复合体亚基C1(M7668-64)、坏死诱导疫霉蛋白质(M8414-05)会抑制代谢过程。
1-磷酸葡萄糖的代谢途径为戊糖和葡萄糖醛酸的相互转化[20](map00040),1-磷酸葡萄糖相对含量随着贮藏时间的延长而下降,可能是因为β2-微球蛋白质(M11870-3)、载脂蛋白质E(M34203-3)、ATP合成蛋白质8(M7709-26)促进代谢过程,NADH-泛 醌氧化还原酶链4L(M10880-9)、生长抑制素-28 (M 3 1 3 0-5 8)、AT P 合酶F(0)复合体亚基C 1 (M7668-64)、坏死诱导疫霉蛋白质(M8414-05)、朊蛋白质类(M9074-86)抑制代谢过程。
D - 甘油酸的代谢途径为戊糖磷酸途径[ 2 1 ](map00030),甘氨酸、丝氨酸和苏氨酸代谢[22](map00260),甘油脂代谢[23](map00561),乙醛酸代谢[24](map00630)及甲烷代谢[25](map00680)。随着贮藏时间延长,D-甘油酸相对含量增加,D-甘油酸产生的代谢途径中,硫氧还蛋白质(M11722-8)、β2-微球蛋白质(M11870-3)有利于代谢物产生,抗菌肽(M7451-79)、 载脂蛋白质C-II(M8136-55)、朊蛋白质类(M9074-86)抑制代谢物产生。
天冬氨酸1的代谢途径为丙氨酸、天冬氨酸和谷氨酸代谢[26](map00250)、组氨酸代谢[27](map00340)、氰基氨基酸代谢[28](map00460),随着贮藏时间的延长,天冬氨酸1的相对含量上升,与其呈正相关的菌体蛋白质NADH-泛醌氧化还原酶链4L(M10880-9)、坏死诱导疫霉蛋白质(M8414-05)相对含量呈增长趋势。
核糖相对含量在贮藏期间呈趋势增长,与其相关性较大的菌体蛋白质硫氧还蛋白质(M11722-8)、β2-微球蛋白质(M11870-3)、载脂蛋白质E(M34203-3)及磷脂结合蛋白质(M38968-8)的相对含量随着贮藏时间延长呈递减趋势,可能是这些菌体蛋白质对其代谢途径(戊糖磷酸途径)产生了影响。
可产生天冬酰胺4的代谢途径为丙氨酸、天冬氨酸和谷氨酸代谢[29],氰基氨基酸代谢[30-31],天冬酰胺4相对含量在贮藏过程中逐渐增加,在第0、4、8、12天时分别为2.10%、7.29%、9.80%和10.60%,与其呈负相关的菌体蛋白质硫氧还蛋白质(M11722-8)、β2-微球蛋白质(M11870-3)、40S核糖体蛋白质S26(M12826-1)、GRF/GHRH生长激素释放素(M5109-45)、磷脂结合蛋白(M38968-8)、生长调节α蛋白质(M7823-80)相对含量呈下降趋势,但呈正相关的抗菌肽(M7451-79)、载脂蛋白质C-II(M8136-55)相对含量呈递增趋势。因此可得出这些菌体蛋白质可能对天冬酰胺4的代谢途径产生影响。
乙酰苯胺3的代谢途径尚未被收录到KEGG数据库,GRF/GHRH生长激素释放素(M5109-45)、ATP合成蛋白质(M7709-26)会促进其产生,而NADH-泛 醌氧化还原酶链4L(M10880-9)、生长抑制素-28 (M3130-58)、载脂蛋白质C-II(M8136-55)、坏死诱导疫霉蛋白质(M8414-05)会抑制其生成。
综上所述,冷鲜滩羊肉贮藏过程中,微生物发生变化的菌体蛋白质与一同发生变化的代谢产物的关联性很大,通过查找KEGG数据库,分析其相关代谢途径,具体见图3。

图 3 菌体蛋白质对微生物代谢通路的影响
Fig. 3 Effect of bacterial proteins on microbial metabolic pathways
苯丙氨酸代谢及甘氨酸、丝氨酸和苏氨酸代谢通路对氰基氨基酸代谢通路有间接影响作用,硫氧还蛋白质、β2-微球蛋白质、坏死诱导疫霉蛋白质和NADH-泛醌氧化还原酶链4L促进了这些代谢通路产生相应的代谢物,而抗菌肽、载脂蛋白质C-II、朊蛋白质类、磷脂结合蛋白质和生长调节α蛋白质抑制了这些代谢过程;因氰基氨基酸代谢通路对丙氨酸、天冬氨酸、谷氨酸代谢通路起间接调控作用,所以上述菌体蛋白质对丙氨酸、天冬氨酸、谷氨酸代谢通路仍有影响。
糖醛酸途径与戊糖磷酸途径起相互调控作用,其中β2-微球蛋白质、载脂蛋白质E和ATP合成蛋白质、硫氧还蛋白质促进相互的代谢过程产生代谢产物,而NADH-泛醌氧化还原酶链4L、生长抑制素-28、ATP合酶F(0)复合体亚基C1、坏死诱导疫霉蛋白质、抗菌肽、载脂蛋白质C-II、和朊蛋白质类会抑制相互间的代谢通路。
戊糖磷酸途径、组氨酸代谢途径及丙氨酸、天冬氨酸和谷氨酸代谢途径通过影响嘌呤代谢不同阶段中间产物而影响嘌呤代谢途径,即硫氧还蛋白质、β2-微球蛋白质、NADH-泛醌氧化还原酶链4L、坏死诱导疫霉蛋白质和40S核糖体蛋白质S26促进代谢物的产生,而抗菌肽、载脂蛋白质C-II、朊蛋白质类、磷脂结合蛋白质和生长调节α蛋白质抑制代谢物的产生。
嘌呤代谢通路对甘氨酸的代谢通路起间接调控作用;甲烷代谢途径调控丝氨酸代谢途径,而丝氨酸代谢途径又调控甘油酯代谢途径。综上所述,图3表明菌体蛋白质会对微生物代谢通路产生影响,其原因之一是菌体蛋白质影响了代谢物的产生过程,即影响了产生该代谢产物的代谢途径,推测是因为菌体蛋白含量在代谢期间有差异,导致其对代谢通路影响的程度发生变化。
3 结 论
本实验采用热力图分析了冷鲜滩羊肉贮藏过程中微生物的8 种差异代谢物和16 个菌体差异蛋白的关联性,并通过KEGG查找了代谢产物的代谢通路,并探寻其中关系,研究了菌体蛋白质的变化对代谢产物的影响。结果表明:冷鲜滩羊肉贮藏中菌体蛋白质的变化与代谢产物有相关性,菌体蛋白所占比例上升,影响代谢产物的代谢途径,导致相关代谢产物在贮藏过程中的含量也发生增加或减少。该发现不仅为微生物群落演替的内在驱动机制提供了前期研究基础,也为延长滩羊肉货架期及开发保鲜新技术提供了理论参考。
[1] 金鑫, 周光宏, 徐幸莲. 冷却肉微生物腐败与冷链系统[J]. 食品工业科技, 2012, 33(6): 417-420. DOI:10.13386/j.issn1002-0306.2012.06.102.
[2] 张雷蕾. 冷却肉微生物污染及食用安全的光学无损评定研究[D]. 北京: 中国农业大学, 2015: 1-3.
[3] 杨文婷, 牛佳, 罗瑞明. 手抓羊肉包装材料选择及常压低温杀菌工艺优化[J]. 中国调味品, 2017, 42(7): 46-50. DOI:10.3969/j.issn.1000-9973.2017.07.010.
[4] 赵光辉. 冷却分割猪肉中腐败微生物分离鉴定与生长特性的 研究[D]. 郑州: 河南农业大学, 2011: 1-5.
[5] 王亚军, 王超儿, 朱津, 等. 蛋白质组学技术及其在工业微生物研究中的应用[J]. 发酵科技通讯, 2016, 45(2): 123-128. DOI:10.16774/j.cnki.issn.1674-2214.2016.02.028.
[6] LU Dongmei, LIU Jianzhong, MAO Zongwan. Engineering of Corynebacterium glutamicum to enhance L-ornithine production by gene knockout and comparative proteomic analysis[J]. Chinese Journal of Chemical Engineering, 2012, 20(4): 731-739. DOI:10.1016/S1004-9541(11)60242-5.
[7] WENDLER S, OTTO A, ORTSEIFEN V, et al. Comparative proteome analysis of Actinoplanes sp. SE50/110 grown with maltose or glucose shows minor differences for acarbose biosynthesis proteins but major differences for saccharide transporters[J]. Journal of proteomics, 2016, 131: 140-148. DOI:10.1016/j.jprot.2015.10.023.
[8] 慕春龙. 日粮蛋白质水平对大鼠和仔猪机体代谢和肠道微生物的影响[D]. 南京: 南京农业大学, 2016: 1-9.
[9] 苑昱东, 尤丽琴, 罗瑞明, 等. 基于气相色谱-质谱和液相色谱-质谱技术的冷鲜滩羊肉贮藏中脂肪差异代谢物检测[J]. 食品科学, 2019, 40(18): 195-202. DOI:10.7506/spkx1002-6630-20180724-297.
[10] ZAMPIERI M, ZIMMERMANN M, CLAASSEN M, et al. Nontargeted metabolomics reveals the multilevel response to antibiotic perturbations[J]. Cell Reports, 2017, 19(6): 1214-1228. DOI:10.1016/j.celrep.2017.04.002.
[11] MUROYA S, OE M, NAKAJIMA I, et al. CE-TOF MS-based metabolomic profiling revealed characteristic metabolic pathways in postmortem porcine fast and slow type muscles[J]. Meat Science, 2014, 98(4): 726-735. DOI:10.1016/j.meatsci.2014.07.018.
[12] VAN DER GREEF J, STROOBANT P, VAN DER HEIJDEN R. The role of analytical sciences in medical systems biology[J]. Current Opinion in Chemical Biology, 2004, 8(5): 559-565. DOI:10.1016/j.cbpa.2004.08.013.
[13] COTTINGHAM K. Systems biology: a boon for analytical chemists?[J]. Analytical Chemistry, 2005, 77(9): 197A-200A. DOI:10.1021/ac053371c.
[14] 胡倩倩, 杨波, 罗瑞明, 等. 基于SELDI-TOF-MS的冷却滩羊肉微生物差异蛋白分析[J]. 肉类研究, 2018, 32(2): 47-53. DOI:10.7506/rlyj1001-8123-201802006.
[15] 胡倩倩, 张同刚, 尤丽琴, 等. 冷鲜滩羊肉微生物菌群代谢物与其关联性分析[J]. 食品工业科技, 2017, 38(8): 322-325; 355. DOI:10.13386/j.issn1002-0306.2017.08.054.
[16] 王福红, 刘伯钧. 微生物与肉和肉制品的货架期[J]. 肉类工业, 2006(8): 11-13. DOI:10.3969/j.issn.1008-5467.2006.08.007.
[17] 张同刚, 苏春霞, 李俊丽, 等. 气相色谱-质谱法分析冷鲜滩羊肉微生物差异代谢物[J]. 食品科学, 2017, 38(10): 291-296. DOI:10.7506/spkx1002-6630-201710047.
[18] 汪渤森, 韩笑, 马天天, 等. 单核细胞增多性李斯特菌硫氧还蛋白TrxA调控磷脂酶PlcB研究[J]. 中国兽医学报, 2018, 38(9): 1686-1692; 1724. DOI:10.16303/j.cnki.1005-4545.2018.09.09.
[19] 张赫宇. 冷鲜滩羊肉微生物群落多样性及演替规律研究[D]. 银川: 宁夏大学, 2016: 10-30.
[20] TEUFEL R, MASCARAQUE V, ISMAIL W, et al. Bacterial phenylalanine and phenylacetate catabolic pathway revealed[J]. Proceedings of the National Academy of Sciences of the United States of America, 2010, 107: 14390-14395. DOI:10.1073/pnas.1005399107.
[21] CUSA E, OBRADORS N, BALDOMÀ L, et al. Genetic analysis of a chromosomal region containing genes required for assimilation of allantoin nitrogen and linked glyoxylate metabolism in Escherichia coli[J]. Journal of Bacteriology, 1999, 181(11): 7479-7484. DOI:10.1063/1.1681825.
[22] XI H, SCHNEIDER B L, REITZER L. Purine catabolism in Escherichia coli and function of xanthine dehydrogenase in purine salvage[J]. Journal of Bacteriology, 2000, 182(19): 5332-5341. DOI:10.1128/JB.182.19.5332-5341.2000.
[23] YEW W S, GERLT J A. Utilization of L-ascorbate by Escherichia coli K-12: assignments of functions to products of the yjf-sga and yia-sgb operons[J]. Journal of Bacteriology, 2002, 184(1): 302-306. DOI:10.1128/JB.184.1.302-306.2002.
[24] KOURIL T, WIELOCH P, REIMANN J, et al. Unraveling the function of the two Entner-Doudoroff branches in the thermoacidophilic Crenarchaeon Sulfolobus solfataricus P2[J]. FEBS Journal, 2013, 280(4): 1126-1138. DOI:10.1111/febs.12106.
[25] BURSY J, PIERIK A J, PICA N, et al. Osmotically induced synthesis of the compatible solute hydroxyectoine is mediated by an evolutionarily conserved ectoine hydroxylase[J]. Journal of Biological Chemistry, 2007, 282(43): 31147-31155. DOI:10.1074/jbc.M704023200.
[26] BERG S, EDMAN M, LI L, et al. Sequence properties of the 1,2-diacylglycerol 3-glucosyltransferase from Acholeplasma laidlawii membranes. recognition of a large group of lipid glycosyltransferases in eubacteria and archaea[J]. Journal of Biological Chemistry, 2001, 276(25): 22056-22063. DOI:10.1074/jbc.M102576200.
[27] KHOMYAKOVA M, BUKMEZ O, THOMAS L K, et al. A methylaspartate cycle in haloarchaea[J]. Journal Science, 2011, 331: 334-337. DOI:10.1126/science.1196544.
[28] LIFFOURRENA A S, SALVANO M A, LUCCHESI G I. Pseudomonas putida A ATCC 12633 oxidizes trimethylamine aerobically via two different pathways[J]. Archives of Microbiology, 2010, 192(6): 471-476. DOI:10.1007/s00203-010-0577-5.
[29] ENGSKOG M K R, ERSSON L, HAGLÖF J, et al. β-N-Methylaminol-alanine (BMAA) perturbs alanine, aspartate and glutamate metabolism pathways in human neuroblastoma cells as determined by metabolic profiling[J]. Amino Acids, 2017, 49(5): 905-919. DOI:10.1007/s00726-017-2391-8.
[30] TELOH J K, ANSORGE L, PETERSEN M, et al. Histidine metabolism after bretschneider cardioplegia in cardiac surgical patients[J]. Physiological Research, 2018, 67(2): 209-216. DOI:10.33549/physiolres.933691.
[31] HICKEL A, HASSLACHER M, GRIENGL H. Hydroxynitrile iyases: functions and properties[J]. Journal Physiologia Plantarum, 2006, 98(4): 891-898. DOI:10.1111/j.1399-3054.1996.tb06700.x.