玛咖(Lepidium meyenii)为十字花科独行菜属一年生或两年生草本植物,原产于海拔3 500~4 500 m的南美安第斯山区,为当地常用食物[1]。近年来,玛咖在世界各地广泛种植,在我国主要分布于云南、新疆、西藏、四川及青海等地区[2]。随着人们对健康问题的关注,对于在极端恶劣环境下(如高原地区)具有极强生命力和良好适应性的作物研究逐渐增多[3]。玛咖能很好地适应高原环境(低温度、强紫外线、低氧气含量等),含有丰富的蛋白质、碳水化合物、维生素和矿物质等营养物质,也含有生物碱、芥子油苷、甾醇等次级代谢产物[4]。已有研究表明,玛咖具有抗疲劳、抗氧化、免疫调节、提高生育力、调节内分泌以及抗肿瘤等方面的生物活性[5]。本文旨在对玛咖的不同活性成分、淀粉及玛咖生物活性研究进行综述,以期为玛咖的深入研究和合理开发利用提供参考。
1 玛咖活性成分
1.1 玛咖活性多糖
多糖是自然界含量最为丰富的天然大分子物质之一,是玛咖的主要活性成分之一[6]。近年来国内外对玛咖活性多糖的研究主要集中在提取、分离纯化及结构测定等方面。
1.1.1 玛咖活性多糖的提取方法
玛咖活性多糖常用的提取方法有热水浸提法、超声波辅助提取法、微波辅助提取法、有机溶剂提取法、酸碱提取法、酶辅助提取法等[7-9]。热水浸提法是利用高温加快分子的热运动,加速活性多糖进入水相进而提高提取率,操作简便,但浸提温度过高会使活性多糖生物活性降低、蛋白质溶出增加[10],导致后续处理困难[11]。超声波辅助提取法是利用超声波产生的空化、振动、粉碎和搅拌等效应,通过破坏细胞壁、加强细胞的传质作用,高效快速地提取活性多糖[12-13]。浦跃武等[14]采用超声波提取玛咖活性多糖,确定最佳提取条件:超声时间20 min、温度50 ℃、料液比1∶20(m/V)、功率200 W,活性多糖提取率提高了12.9%。超声波辅助提取法效率高,但活性多糖分子质量普遍会更小,需要考虑超声波对活性多糖高级结构的破坏。
1.1.2 玛咖活性多糖的分离纯化
玛咖活性多糖为非均一性杂多糖,需进一步分离纯化得到均一活性多糖。纯化步骤一般包括去除蛋白、脱色、层析分离等[15]。其中去除蛋白常用方法是Sevag法,即利用蛋白质在三氯乙烷等有机溶剂中变性的特点,经分离去除活性多糖中的蛋白。脱色常用的方法是层析分离法,即根据活性多糖的理化性质,选取相应的固定相和流动相,实现活性多糖的高效分离纯化,其中最常用的固定相为二乙基氨基乙基纤维素(diethylaminoethyl cellulose,DEAE)。脱色后的活性多糖常采用离子交换层析及凝胶过滤层析进一步分级分离。Li Jing等[16]先用Sevag法脱蛋白得到玛咖活性粗多糖(Maca polysaccharide,MPS),再通过DEAE-52纤维素柱及Sephadex G-100柱层析进行分级纯化,分别得到MPS-1和MPS-2两种活性纯多糖。Zhang Lijun等[7]从玛咖根中提取一种水溶性活性多糖,用Sevag法脱蛋白后,再通过DEAE-52纤维素离子交换柱得到玛咖主要多糖(main polysaccharide from Maca,MP)-1,其质量分数为91.63%。由于提取的活性多糖中常含蛋白质、色素和小分子等杂质,仅用一种纯化方法很难得到组分较纯的活性多糖,通常将两种或多种纯化方法相结合,使活性多糖组分高效分离。
1.1.3 玛咖活性多糖的结构测定
为研究玛咖活性多糖的结构,将化学方法(如酸水解、甲基化、高碘酸氧化、Smith降解)与红外光谱(infrared spectroscopy,IR)、核磁共振(nuclear magnetic resonance,NMR)、高效凝胶渗透色谱(high performance gel permeation chromatography,HPGPC)、高效液相色谱(high performance liquid chromatography,HPLC)、气相色谱(gas chromatography,GC)等现代仪器分析手段相结合,确定活性多糖的相对分子质量、单糖组分、糖苷键类型及位置等,从而判断活性多糖的结构。Zha Zhengqi等[17]利用阴离子交换层析法和Sephadex G-100柱层析从各组分中提取水溶性多糖(water-soluble polysaccharide,LMP)-1,经过HPGPC测定LMP-1的分子质量为10.1 kDa,HPLC结果表明该活性多糖由葡萄糖和阿拉伯糖组成,其物质的量比为7.03∶1.08。Tang Weimin等[18]将去除蛋白、透析后的玛咖活性粗多糖经HPGPC进一步纯化后,再由NMR联合甲基化、IR等分析方法确定了玛咖活性多糖的分子结构是β-1,3-Galp(A)、β-1,3-Glcp和α-1,3-Manp按5∶4∶1交替形成多糖支链。此外,陈燕文等[19]将去除蛋白的玛咖活性粗多糖酸水解后,并利用1-苯基-3-甲基-5-吡唑啉酮柱前衍生化对活性多糖进行处理,再利用HPLC分析其单糖组成及物质的量比,确定该活性多糖是由D-甘露糖、葡萄糖、D-半乳糖、阿拉伯糖按物质的量比1∶196∶6∶6组成。活性多糖的结构比较复杂,每种测定方法各有优势,多种方法联合使用可获得较为完整的结构信息。玛咖活性多糖分子质量及结构见表1。
表1 玛咖活性多糖分子质量及结构
Table 1 Molecular masses and structures of bioactive polysaccharides in Maca
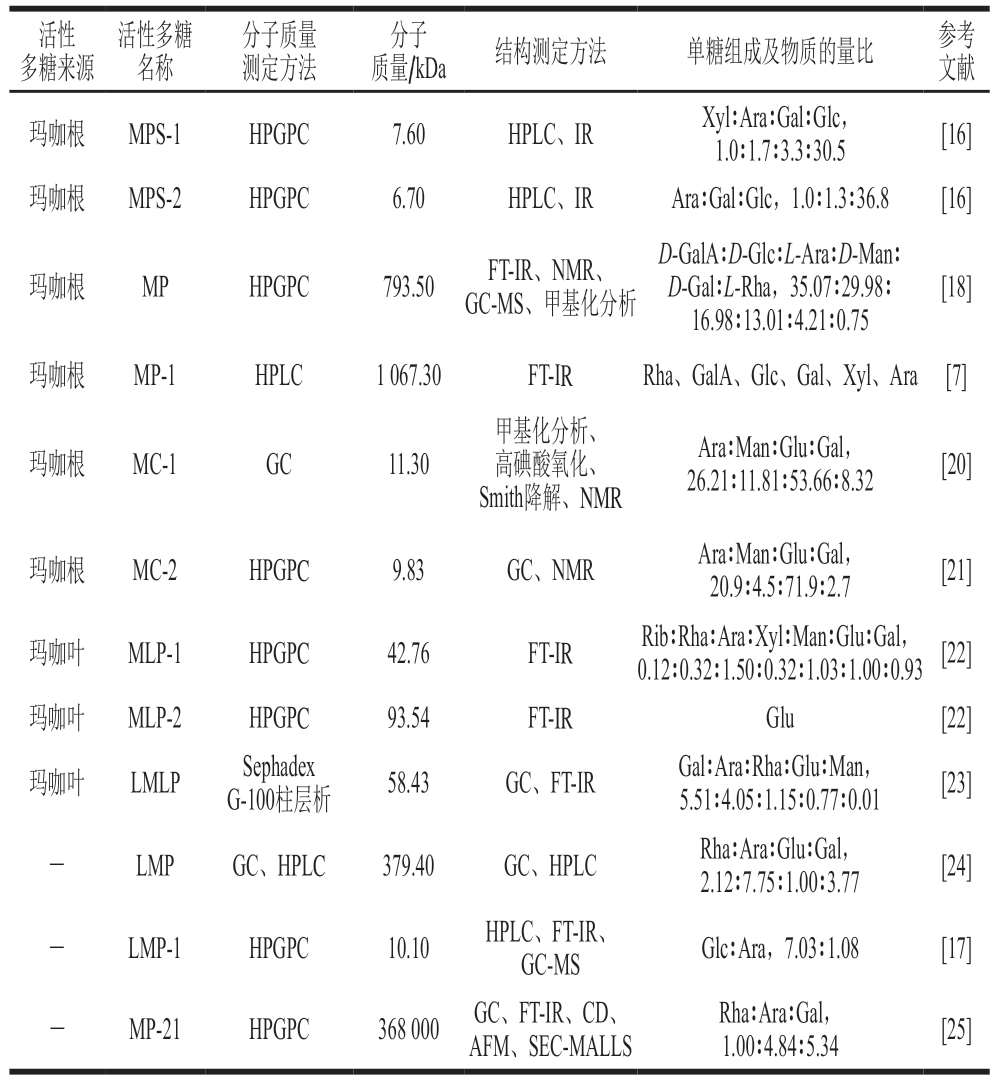
注:-.未知;LMLP.玛咖叶多糖(polysaccharide from Lepidium meyenii leaves);MLP.玛咖叶多糖(polysaccharides from the leaves of Maca);MC.玛咖根多糖(polysaccharide from Lepidium meyenii roots);FT-IR.傅里叶变换红外光谱(Fourier transform infrared spectrometer);CD.圆二色谱(circular dichroism);AFM.原子力显微镜(atomic force microscopy);SEC-MALLS.尺寸排阻色谱法与多角度激光光散射法联用(size exclusion chromatography coupled with multi-angle laser light scattering);MS.质谱(mass spectrum)。
活性多糖来源 质量/kDa 结构测定方法 单糖组成及物质的量比 参考文献玛咖根 MPS-1 HPGPC 7.60 HPLC、IR Xyl∶Ara∶Gal∶Glc,1.0∶1.7∶3.3∶30.5 [16]玛咖根 MPS-2 HPGPC 6.70 HPLC、IR Ara∶Gal∶Glc,1.0∶1.3∶36.8 [16]活性多糖名称分子质量测定方法分子玛咖根 MP HPGPC 793.50 FT-IR、NMR、GC-MS、甲基化分析D-GalA∶D-Glc∶L-Ara∶D-Man∶D-Gal∶L-Rha,35.07∶29.98∶16.98∶13.01∶4.21∶0.75[18]玛咖根 MP-1 HPLC 1 067.30 FT-IR Rha、GalA、Glc、Gal、Xyl、Ara [7]玛咖根 MC-1 GC 11.30甲基化分析、高碘酸氧化、Smith降解、NMR Ara∶Man∶Glu∶Gal,26.21∶11.81∶53.66∶8.32 [20]玛咖根 MC-2 HPGPC 9.83 GC、NMR Ara∶Man∶Glu∶Gal,20.9∶4.5∶71.9∶2.7 [21]玛咖叶 MLP-1 HPGPC 42.76 FT-IR Rib∶Rha∶Ara∶Xyl∶Man∶Glu∶Gal,0.12∶0.32∶1.50∶0.32∶1.03∶1.00∶0.93 [22]玛咖叶 MLP-2 HPGPC 93.54 FT-IR Glu [22]玛咖叶 LMLP Sephadex G-100柱层析 58.43 GC、FT-IR Gal∶Ara∶Rha∶Glu∶Man,5.51∶4.05∶1.15∶0.77∶0.01 [23]- LMP GC、HPLC 379.40 GC、HPLC Rha∶Ara∶Glu∶Gal,2.12∶7.75∶1.00∶3.77 [24]- LMP-1 HPGPC 10.10 HPLC、FT-IR、GC-MS Glc∶Ara,7.03∶1.08 [17]- MP-21 HPGPC 368 000 GC、FT-IR、CD、AFM、SEC-MALLS Rha∶Ara∶Gal,1.00∶4.84∶5.34 [25]
续表2
化合物名称 结构式N-苄基-十八碳酰胺 N HO O N-苄基-十七碳酰胺 N H O O N-苄基-5-羰基-(6E,8E)-十八碳二烯酰胺 NH O H 1,2-二氢-N-羟基吡啶酰胺N OH COOH β-咔啉生物碱NH NHimages/BZ_264_2023_884_2033_897.pngH咪唑类生物碱A N NCl-+H3C CH3咪唑类生物碱B咪唑类生物碱C咪唑类生物碱D CH3 N NCl-+H3C CH3 H H3CO N NCl-+H3C CH3 CH3 H3CO N NCl-+H3C CH3 O H羟基吡啶衍生物类生物碱N OH
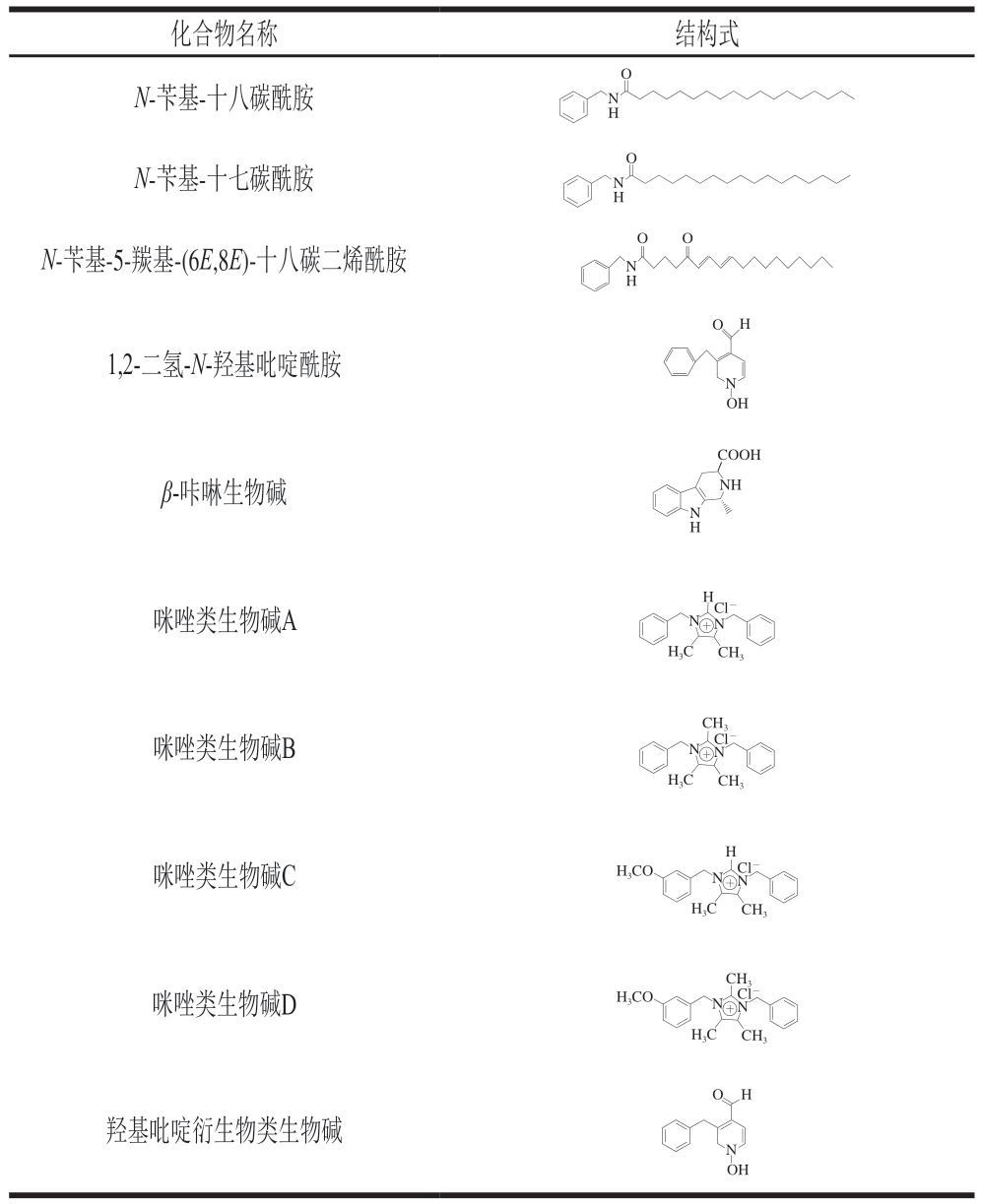
1.2 玛咖生物碱
生物碱是一类含氮有机物,是玛咖中的一种次级代谢产物[26],主要包括玛咖酰胺、β-咔啉生物碱、咪唑生物碱[27]以及羟基吡啶衍生物类生物碱[28]等,其中玛咖酰胺是仅在玛咖中发现的特征物质。玛咖生物碱的化学结构见表2[29-31]。
表2 各种玛咖生物碱的化学结构[29-31]
Table 2 Chemical structures of various Maca alkaloids[29-31]
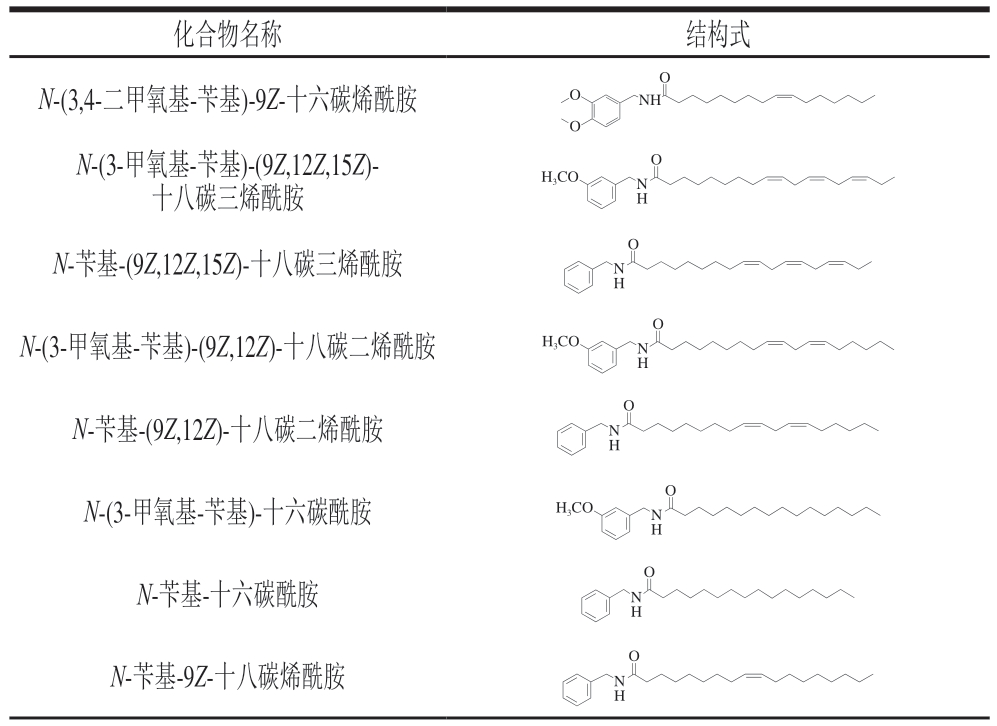
化合物名称 结构式N-(3,4-二甲氧基-苄基)-9Z-十六碳烯酰胺O O O NH N-(3-甲氧基-苄基)-(9Z,12Z,15Z)-十八碳三烯酰胺NH O H3CO O N-苄基-(9Z,12Z,15Z)-十八碳三烯酰胺 N H O H3CO N-(3-甲氧基-苄基)-(9Z,12Z)-十八碳二烯酰胺 N H O N-苄基-(9Z,12Z)-十八碳二烯酰胺 N H O H3CO N-(3-甲氧基-苄基)-十六碳酰胺NH O N-苄基-十六碳酰胺NH O N-苄基-9Z-十八碳烯酰胺 N H
1.2.1 玛咖生物碱的提取方法
玛咖生物碱的常用提取方法包括匀浆法[27]、酸水提取法[32]、循环超声法[33]等。玛咖生物碱中的玛咖酰胺含有疏水性的长碳键,属于弱极性化合物,常用弱极性的有机溶剂进行提取,辅助微波、超声等技术可提高其提取效率[34]。匀浆法[27]是通过加入提取溶剂(乙醇、甲醇等)对玛咖进行充分匀浆,获得玛咖总生物碱的方法。该方法的优点是提取速率快、温度低、消耗低等。酸水提取常用于提取碱性强的生物碱,其提取原理是利用无机酸水对其进行提取,可使生物碱从大分子有机酸盐转变为小分子无机酸盐,从而增大其在水中的溶解度。高斌等[32]利用酸水提取的方法对云南丽江3 种色型(黄色、紫色和黑色)的玛咖生物碱进行提取,以乌头碱为标准品并确定了最佳提取条件。
1.2.2 玛咖生物碱的分离纯化
对于弱极性化合物玛咖酰胺主要的分离纯化方法有:柱色谱分离、薄层色谱(thin-layer chromatography,TLC)法、HPLC及超临界色谱法等,硅胶柱层析色谱是分离纯化玛咖酰胺的常用方法。Zhao Jianping等[35]利用体积分数95%乙醇提取玛咖总碱粗提物,己烷萃取后上硅胶色谱柱,乙酸乙酯-氯仿梯度洗脱,再经TLC纯化得5 个玛咖酰胺类单体化合物。大孔树脂吸附法利用物理吸附从水溶液中选择性地吸附目标化学成分,常用来分离纯化玛咖中极性较大的生物碱。谢逸欣等[36]确定了利用AB-8大孔树脂分离纯化生物碱的最佳条件为:上样液质量浓度1 g/mL、药量与树脂干质量比为2∶1、水洗量3 BV、洗脱溶剂为体积分数40%乙醇、洗脱剂用量6 BV、洗脱速率1.5 BV/h,洗脱率达29.66%。杜广香[37]采用HP-20大孔树脂对生物碱进行了分离纯化,纯化后的生物碱质量分数由24.6%提高到62.4%。大孔树脂吸附法纯化玛咖中生物碱具有操作简便、吸附容量大、重复性好、无有机溶剂残留等特点,在生物碱的纯化中应用广泛。
1.2.3 玛咖生物碱的含量测定
玛咖生物碱含量测定常用的方法有酸性染料比色法、酸碱滴定法、HPLC、GC等。酸性染料比色法的原理是在适当pH值的介质中,生物碱与酸性染料形成离子对,利用有机溶剂萃取生成有色溶液,通过测定其吸光度从而间接计算生物碱含量。卢馨等[38]采用酸性染料比色法对玛咖中的总生物碱含量进行了测定,结果显示云南丽江玛咖总生物碱质量分数为0.7%。查圣华[39]利用酸性染料比色法检测出秘鲁产玛咖生物碱质量分数为0.083%,云南产玛咖生物碱质量分数为0.126%。酸性染料比色法操作简单、重复性好,是玛咖总生物碱含量测定最常用的方法。对于玛咖酰胺常用的检测方法主要有TLC、HPLC、GC-MS或液相色谱-质谱(liquid chromatograph-MS,LC-MS)联用法、超高效液相色谱法、1H-NMR或13C-NMR及超临界色谱法等,其中TLC和HPLC主要用于玛咖酰胺定性或定量检测,其他方法还可以用于玛咖酰胺结构测定[40]。
1.3 玛咖芥子油苷
芥子油苷是十字花科植物中特有的活性成分,其含量丰富,是玛咖含有辛辣气味的主要原因[41]。玛咖芥子油苷结构上包含一个多变的侧链R基团和一个硫原子相连的D-吡喃葡萄糖。根据侧链R基团的不同,可以把芥子油苷分为3 类:脂肪族芥子油苷、芳香族芥子油苷和吲哚族芥子油苷,其基本结构见图1[42]。玛咖中已发现的芥子油苷有9 种[43],其中苄基芥子油苷为其主要活性成分及特征物质。玛咖芥子油苷化学式[42]及结构[43-44]见表3。
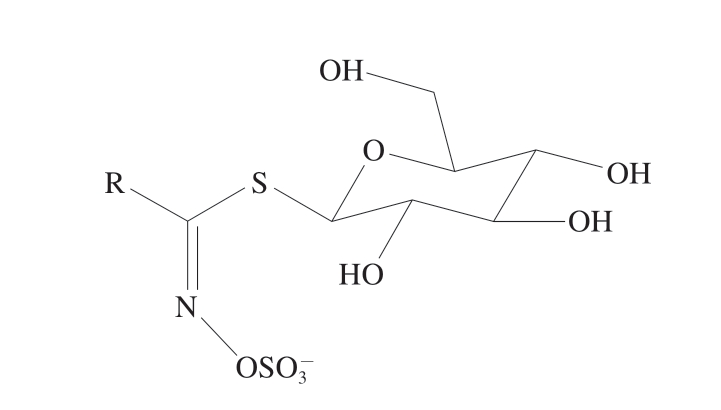
图1 芥子油苷母核结构[42]
Fig. 1 Mother nuclear structure of glucosinolates[42]
表3 玛咖芥子油苷类的化学式及结构[42-44]
Table 3 Chemical structures of glucosinolates in Maca[42-44]
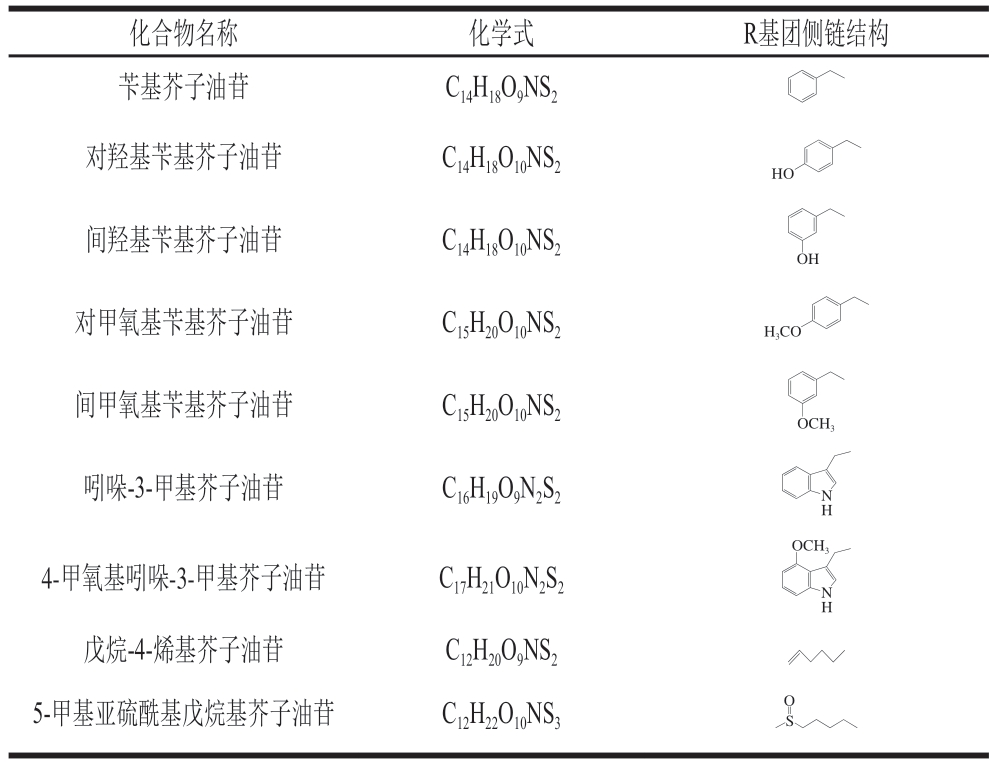
化合物名称 化学式 R基团侧链结构苄基芥子油苷 C14H18O9NS2对羟基苄基芥子油苷 C14H18O10NS2 HO间羟基苄基芥子油苷 C14H18O10NS2 OH对甲氧基苄基芥子油苷 C15H20O10NS2 H3CO间甲氧基苄基芥子油苷 C15H20O10NS2 OCH3吲哚-3-甲基芥子油苷 C16H19O9N2S2 NH OCH3 4-甲氧基吲哚-3-甲基芥子油苷 C17H21O10N2S2N H戊烷-4-烯基芥子油苷 C12H20O9NS2 5-甲基亚硫酰基戊烷基芥子油苷 C12H22O10NS3 S O
1.3.1 玛咖芥子油苷的提取方法
芥子油苷的提取方法主要有水提取法、有机溶剂提取法以及超声波辅助提取法。水提取法为传统方法,是通过沸水对玛咖芥子油苷进行提取。金文闻[45]将秘鲁玛咖干根于4 ℃下保存12 h后采取沸水浴提取芥子油苷,低温处理可使提取率提高到1.89%。有机溶剂提取法是利用溶剂(醇、酯)萃取提取芥子油苷,并去除大部分杂质。何雪梅[46]利用体积分数70%乙醇对玛咖芥子油苷进行提取,确定玛咖中含有脱硫苄基芥子油苷与脱硫间-甲氧基苄基芥子油苷。杨晓飞[44]利用不同的溶剂(水、乙醇、甲醇)对芥子油苷提取进行对比,发现不同提取溶剂所得的芥子油苷在含量和作用方面差异不大。超声波辅助提取法是在水提取法、有机溶剂提取法的基础上,利用超声波加速玛咖芥子油苷溶出。本课题组利用甲醇作为溶剂,超声波辅助提取芥子油苷,提取率提高到1.66%[47]。超声波辅助提取法时间短、效率高,是目前较为常用的玛咖芥子油苷提取方法。
1.3.2 玛咖芥子油苷的分离纯化
玛咖芥子油苷初级分离纯化主要利用吸附分离法(大孔树脂吸附、离子交换树脂吸附)和离子交换柱层析法,进一步纯化常利用酸性氧化铝柱层析和HPLC等。Gasco等[48]利用DEAE-Sephadex A-25阴离子交换柱初级分离,再经HPLC分离,测定了红玛咖中芥子油苷的质量分数为0.639%。张利军[49]采用D101大孔树脂和IRA-67离子交换树脂对芥子油苷进行初级纯化,得到质量分数为78.3%的玛咖芥子油苷。新鲜玛咖经甲醇提取、酸性氧化铝柱层析、半制备液相分离纯化,芥子油苷质量分数可达到98.3%[50]。仅用一种分离纯化方法很难分离出高纯度的芥子油苷,通常先利用大孔树脂初级处理,然后采用正、反相硅胶或氧化铝柱层析分离,或利用HPLC进一步分离纯化。
1.3.3 玛咖芥子油苷的含量测定
玛咖中芥子油苷的定量测定方法有氯化钯比色法、GC、HPLC、LC-MS、葡萄糖释放法和硫酸钡质量法等。氯化钯比色法是利用钯离子与芥子油苷生成一种有色络合物,即可按比色法计算芥子油苷的含量[51]。金文闻[45]采用改良的氯化钯比色法对玛咖中芥子油苷的含量进行快速检测,测得玛咖干根中芥子油苷质量分数为1.92%。GC是对单个芥子油苷进行分析,但亚磺酸芥子油苷和吲哚族芥子油苷的不易挥发性和一些芥子油苷对高温敏感性等限制了其应用,且该方法预处理较为复杂[44]。HPLC以乙腈-水系统作为流动相,采用梯度洗脱以提高分离效果,适用于芥子油苷组分及含量测定,唐霖等[52]利用葡糖硫苷酶酶解苄基芥子油苷,得到异硫氰酸苄酯,以异硫氰酸苄酯为标准品采用HPLC准确测定了不同产地玛咖中苄基芥子油苷的含量。艾中等[53]以丙烯基芥子油苷作为对照品,利用LC-MS对国内不同颜色、不同地区和不同部位的玛咖芥子油苷的主要组分和含量进行鉴定和分析。目前很多检测方法都是采用玛咖中不含的丙烯基芥子油苷作为标准品,为了避免标准品带来的误差,应尽量采用苄基芥子油苷作为玛咖芥子油苷检测的标准品。
1.4 玛咖甾醇
甾醇作为玛咖重要的次生代谢产物,主要存在于它的根、茎、叶中,与玛咖的保健功效紧密相关。玛咖甾醇主要包括β-谷甾醇、菜油甾醇、麦角固醇、菜籽甾醇和麦角二烯[54],其化学结构见表4[42]。
表4 玛咖甾醇的化学结构[42]
Table 4 Chemical structures of sterols in Maca[42]

化合物名称 化学式 结构式β-谷甾醇 C29H50O H H H HO菜油甾醇 C28H48O H HO H H麦角甾醇 C28H44O H H H H H HO菜籽甾醇 C28H46O H HO H H麦角二烷醇 C28H46O HO H H豆甾醇 C29H46O H HO H H OH HO β-蜕皮激素 C27H44O7HO OH HO OH H H O
1.4.1 玛咖甾醇的提取方法
甾醇是玛咖中重要的活性成分之一,占玛咖成分的0.03%左右,不溶于水,易溶于有机溶剂。因此,常利用脂溶性溶剂来提取玛咖中的甾醇。Dini等[55]使用二氯甲烷提取秘鲁玛咖,经过硅胶柱吸附层析后,利用二氯甲烷洗脱后得到玛咖甾醇。杜萍等[56]将玛咖根粉碎,经乙醇提取、石油醚萃取,再经硅胶柱减压柱层析,最终得到β-谷甾醇。何雪梅[46]利用乙醇提取甾醇,测得国产玛咖中甾醇的质量分数为0.037%。有机溶剂提取甾醇操作简单、提取速率快、成本低。
1.4.2 玛咖甾醇的分离纯化
甾醇的纯化采用吸附法、溶剂提取法、皂化法、结晶法等。甘瑾等[57]利用皂化法对3 种色型(红、紫、黄)云南产玛咖的甾醇类化合物进行分离纯化,并通过GC-MS技术对其进行定量分析,结果表明3 种色型玛咖中甾醇类化合物包括β-谷甾醇和菜油甾醇,白色、紫色、黄色原料中甾醇总含量分别为36.60、32.28、27.97 mg/100 g。随着技术的进步,具有高选择性和高效性特点的分子蒸馏法和酶法也被应用于甾醇的分离纯化中。但由于操作简单、提取率高,目前还是以溶剂提取法、吸附法等传统方法为主。
1.5 玛咖黄酮
黄酮是玛咖中重要的生物活性成分之一,是玛咖通过光合作用产生的一类低分子质量物质,具有抗癌、抗炎等活性[58]。
1.5.1 玛咖黄酮的提取方法
玛咖黄酮的提取方法主要有超声波辅助提取法[59]、浸提法[60]、回流提取法[61]等。超声波辅助提取法最为常用,此方法能够有效地提高黄酮的提取率。周晓明等[59]利用响应面分析法对玛咖总黄酮的超声波辅助提取工艺进行了优化,确定了最佳提取条件为:乙醇体积分数70.3%、料液比1∶27(m/V)、超声时间28.4 min,此条件下玛咖总黄酮的提取率为2.113%。浸提法是利用乙醇等有机溶剂对玛咖中的黄酮进行提取。本课题组采用响应面法优化了浸提法提取云南玛咖总黄酮的条件,最佳条件为:乙醇体积分数65%、提取温度65 ℃、料液比1∶29(m/V),此条件下总黄酮提取率为(2.49±0.02)%[62]。回流提取法是利用乙醇等挥发性有机溶剂提取黄酮,将浸出液加热蒸馏,其中挥发性溶剂馏出后又被冷却,重复流回浸出容器中浸提原料。李玉娟等[61]采用响应面法优化回流提取玛咖总黄酮的条件,确定了最佳提取条件为:料液比1∶26(m/V)、乙醇体积分数71%、单次回流提取时间2.2 h、提取2 次,总黄酮提取率为0.843%。
1.5.2 玛咖黄酮的分离纯化
黄酮的分离纯化方法比较单一,常采用大孔树脂吸附法来得到较高纯度的玛咖黄酮。李玉娟等[61]确定了利用AB-8大孔树脂分离纯化玛咖黄酮的最佳条件:上样液质量浓度为0.84 g/mL,pH 3~4,洗脱速率为1 mL/min,先用体积分数20%的乙醇杂质去除,再用体积分数70%的乙醇进行洗脱,得到的总黄酮的质量分数可达15.73%。
1.6 玛咖淀粉
目前,对玛咖的研究主要集中于活性成分含量测定、提取、分离纯化及生物活性的研究,有关玛咖中的淀粉性质研究较少,玛咖的主要食用部位是其膨大的根,类似玛咖具有膨大根的独行菜属植物在我国十分罕见,在世界范围内富含淀粉且具有贮藏根的十字花科作物也很鲜见[63]。
1.6.1 玛咖淀粉的分离纯化
淀粉的传统分离提取技术较为成熟。张玲[63]采用正丁醇-异戊醇混合物沉淀法对玛咖直链淀粉和支链淀粉进行初级分离,利用正丁醇重结晶得到纯的直链淀粉和支链淀粉,最后采用酶法及高效阴离子层析分析推测支链淀粉分子结构。孙晓东等[64]对丽江玛咖的营养成分进行分析,淀粉质量约占玛咖片干质量的31.57%。余龙江等[65]通过酶水解法测定出玛咖中的淀粉质量分数为34.74%,与甘薯淀粉含量相近[66-67]。
1.6.2 玛咖淀粉的结构特征与理化性质
玛咖淀粉是玛咖块根或提取残渣的主要成分,可作为一种淀粉新资源[68]。玛咖淀粉颗粒多呈棒状和圆形、颗粒较为完整、表面光滑、无明显层状结构,其粒径范围为3.57~14.28 μm,平均粒径为8.57 μm,属于小颗粒淀粉[69],其基本成分包括水分(10.14±0.43)%(质量分数,下同)、灰分(0.32±0.03)%、脂肪(0.35±0.03)%、蛋白质(0.47±0.05)%、直链淀粉(20.56±0.90)%[70]。长轴介于7.4~14.9 nm,短轴介于5.8~9.3 nm,其直链淀粉与支链淀粉质量比为20∶80[68]。玛咖淀粉为C型晶体结构,结晶度为49.22%,热焓值为7.366 J/g,且含有伯、仲醇羟基的α-D-吡喃环等特征结构[69],具有黏性和弹性,冷糊稳定性良好,不易老化[66]。玛咖淀粉的吸水性和膨胀性较高,其具有较低的凝胶温度和较好的稳定性[70]。玛咖淀粉作为一种新淀粉资源,具有一定的开发价值和广阔的发展前景。
2 玛咖生物活性
2.1 抗疲劳
疲劳是伴随着极度的压力、剧烈的体力或脑力劳动导致的身体或精神的疲劳感,可分为身体疲劳与心理疲劳[71]。近年来,关于玛咖抗疲劳的研究越来越多[72-74]。Choi等[75]研究发现,玛咖粉脂溶性提取物提高了大鼠游泳耐力,经进一步鉴定表明玛咖脂溶性提取物的主要成分为玛咖酰胺、脂肪酸、甾醇和酚类。Yang Qin等[76]研究发现补充N-苄基烯酰胺(40 mg/kg)可延长负重游泳时间、提高游泳耐力,进而证明苄烯酰胺具有抗运动性疲劳的作用。余龙江等[65]证明了在服用玛咖干粉后,小鼠的游泳时间可延长56.88%,血清中尿素氮水平可降低15.35%。Tang Weimin等[18]发现玛咖活性多糖可以有效延长小鼠游泳力竭时间。查圣华[39]连续30 d分别给3 组小鼠灌胃不同剂量的玛咖生物碱(0.13、0.27、0.8 g/kg),小鼠力竭时间分别延长了39.46%、66.67%和123.44%。玛咖中的活性多糖、芥子油苷、玛咖酰胺等多种活性成分,对玛咖抗疲劳功效发挥了重要作用。
2.2 抗氧化
氧化应激、自由基代谢与人类的多种疾病及衰老有十分紧密的关系。玛咖在体外和体内均表现出较强的抗氧化作用,能清除自由基、抑制过氧化物产生、提高体内抗氧化酶活性[77]。玛咖根和叶中的活性多糖对羟自由基、DPPH自由基和超氧阴离子自由基均具有清除能力[78]。甘瑾[79]对玛咖抗氧化活性与次生代谢物的相关性进行研究,发现玛咖中多酚含量和生物碱含量与总抗氧化能力、羟自由基清除能力及脂质氧化抑制率都具有极显著的线性相关,玛咖对H2O2诱导的SH-SY5Y细胞损伤具有保护作用,使细胞存活率提高17.18%。
2.3 免疫调节
免疫系统是由非特异性免疫、体液免疫和细胞免疫共同构成的防御体系[80]。玛咖对小鼠的体液免疫、巨噬细胞的吞噬功能、自然杀伤细胞活性具有协同作用[81]。张永忠等[82]通过小鼠实验发现玛咖醇提取物对特异性体液和细胞免疫具有一定的增强作用,促使血清溶血素含量提高186.27%,并使抗体生成细胞水平提高23.58%。玛咖活性多糖具有体外免疫调节活性,能够提高巨噬细胞RAW 264.7的吞噬能力及NO分泌能力[23]。
2.4 提高生育力
玛咖增强生育力是其传统功效之一。玛咖水提物能够对抗有机磷酸酯杀虫剂诱导的小鼠精子损伤,增加精子产生数量[83]。周意等[84]研究表明,玛咖活性多糖可使果蝇在60 min内交配率提高38%左右。玛咖生物碱可提高动物成熟卵泡小体的数量、精子的数量及其流动性,从而显著提高哺乳动物和鱼类的生育力[55]。玛咖能够提高生育力与其含有的活性多糖、生物碱及丰富的精氨酸和果糖等关系密切[4]。
2.5 调节内分泌
内分泌系统是指体内所有的内分泌腺、激素(内分泌腺的分泌物)构成的体液调节系统[85]。玛咖醇提物能改善大鼠卵巢切除后的血脂及骨质代谢情况,对内分泌失调具有一定的调节作用[86-87]。玛咖中的生物碱能够作用于视丘下部和脑垂体,具有调节内分泌腺如肾上腺、甲状腺、胰腺、卵巢等功能,从而平衡荷尔蒙[55]。玛咖生物碱、芥子油苷、异硫氰酸苄酯和甾醇等多种活性成分均能调节生物体的内分泌系统[88]。
2.6 抗癌
癌症是指机体在各种致瘤因素作用下,局部组织的细胞异常增生而形成的局部肿块。玛咖具有抗癌活性,如减缓白血病、肺癌、食道癌、胃癌等疾病的症状[89]。Cui Baoliang等[90]对两种咪唑生物碱(lepidiline A和lepidiline B)进行了体外细胞毒性实验,结果证明lepidiline A对人卵癌细胞有抑制作用(半最大效应质量浓度为7.39 µg/mL),lepidiline B对人膀胱癌细胞、人胰腺癌细胞、人胸腺癌细胞和人卵巢癌细胞等多种癌细胞具有抑制作用(半最大效应质量浓度分别为6.47、1.38、1.66 µg/mL和5.26 µg/mL),因此确认生物碱是玛咖抗癌活性的功效物质之一。玛咖生物碱、芥子油苷、甾醇都是抑制癌症的有效成分[91]。
2.7 其他生物活性
玛咖除了上述活性外,还具有缓解肝损伤[7]、缓解更年期综合征及改善骨质疏松症[92]、神经保护功能[93-94]、抗炎[95]等生物活性(表5)。
3 结 语
玛咖作为新资源食品,是重要的功能食品原料,其主要活性成分有活性多糖、生物碱、芥子油苷、甾醇等,具有抗疲劳、提高生殖细胞活力等多种生物活性。但目前关于玛咖活性的研究多是基于粗提物,对单体化合物的活性研究近几年主要集中于玛咖酰胺和芥子油苷,但在活性评价方面缺乏系统性和深入性的研究,活性组分作用靶点和机制尚不清楚。因此,提取、分析玛咖各组分的生物活性,并从分子水平对其作用机制进行研究,将对玛咖产品品质提升和应用拓展发挥积极的推动作用。
此外,当前有关玛咖生物活性成分的研究主要集中于玛咖根、茎部位,对玛咖地上部分的开发利用研究较少。即使是根、茎部位的研究,在分离提取过程中并没有考虑有关玛咖淀粉的利用和开发问题,致使大量的玛咖淀粉被废弃,同时也没有考虑其营养成分的提取。因此,未来应加大对玛咖营养成分的分离纯化研究,实现玛咖资源的综合利用。
表5 玛咖的生物活性
Table 5 Bioactivities of Maca
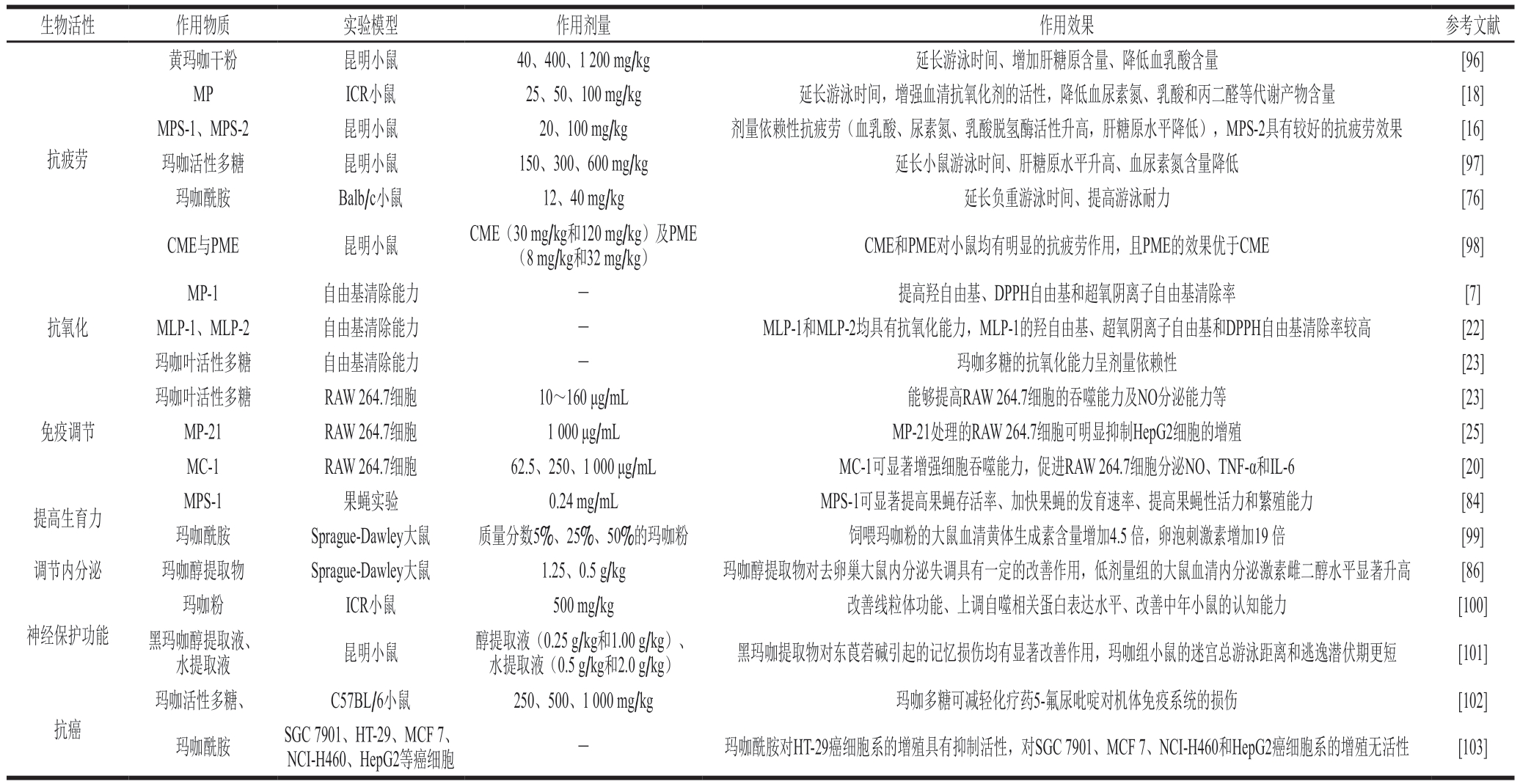
注:CME.玛咖酰胺粗提物(crude macamide extract);PME.玛咖酰胺纯提物(purified macamide extract);TNF-α.肿瘤坏死因子-α(tumor necrosis factor-α);IL-6.白细胞介素-6(interleukin-6)。
生物活性 作用物质 实验模型 作用剂量作用效果 参考文献抗疲劳黄玛咖干粉 昆明小鼠 40、400、1 200 mg/kg 延长游泳时间、增加肝糖原含量、降低血乳酸含量 [96]MP ICR小鼠 25、50、100 mg/kg 延长游泳时间,增强血清抗氧化剂的活性,降低血尿素氮、乳酸和丙二醛等代谢产物含量 [18]MPS-1、MPS-2 昆明小鼠 20、100 mg/kg 剂量依赖性抗疲劳(血乳酸、尿素氮、乳酸脱氢酶活性升高,肝糖原水平降低),MPS-2具有较好的抗疲劳效果 [16]玛咖活性多糖 昆明小鼠 150、300、600 mg/kg 延长小鼠游泳时间、肝糖原水平升高、血尿素氮含量降低 [97]玛咖酰胺 Balb/c小鼠 12、40 mg/kg 延长负重游泳时间、提高游泳耐力 [76]CME与PME 昆明小鼠 CME(30 mg/kg和120 mg/kg)及PME(8 mg/kg和32 mg/kg) CME和PME对小鼠均有明显的抗疲劳作用,且PME的效果优于CME [98]抗氧化免疫调节MP-1 自由基清除能力 - 提高羟自由基、DPPH自由基和超氧阴离子自由基清除率 [7]MLP-1、MLP-2 自由基清除能力 - MLP-1和MLP-2均具有抗氧化能力,MLP-1的羟自由基、超氧阴离子自由基和DPPH自由基清除率较高 [22]玛咖叶活性多糖 自由基清除能力 - 玛咖多糖的抗氧化能力呈剂量依赖性 [23]玛咖叶活性多糖 RAW 264.7细胞 10~160 μg/mL 能够提高RAW 264.7细胞的吞噬能力及NO分泌能力等 [23]MP-21 RAW 264.7细胞 1 000 μg/mL MP-21处理的RAW 264.7细胞可明显抑制HepG2细胞的增殖 [25]MC-1 RAW 264.7细胞 62.5、250、1 000 μg/mL MC-1可显著增强细胞吞噬能力,促进RAW 264.7细胞分泌NO、TNF-α和IL-6 [20]MPS-1 果蝇实验 0.24 mg/mL MPS-1可显著提高果蝇存活率、加快果蝇的发育速率、提高果蝇性活力和繁殖能力 [84]玛咖酰胺 Sprague-Dawley大鼠 质量分数5%、25%、50%的玛咖粉 饲喂玛咖粉的大鼠血清黄体生成素含量增加4.5 倍,卵泡刺激素增加19 倍 [99]调节内分泌 玛咖醇提取物 Sprague-Dawley大鼠 1.25、0.5 g/kg 玛咖醇提取物对去卵巢大鼠内分泌失调具有一定的改善作用,低剂量组的大鼠血清内分泌激素雌二醇水平显著升高 [86]提高生育力神经保护功能玛咖粉 ICR小鼠 500 mg/kg 改善线粒体功能、上调自噬相关蛋白表达水平、改善中年小鼠的认知能力 [100]黑玛咖醇提取液、水提取液 昆明小鼠 醇提取液(0.25 g/kg和1.00 g/kg)、水提取液(0.5 g/kg和2.0 g/kg) 黑玛咖提取物对东莨菪碱引起的记忆损伤均有显著改善作用,玛咖组小鼠的迷宫总游泳距离和逃逸潜伏期更短 [101]抗癌玛咖活性多糖、 C57BL/6小鼠 250、500、1 000 mg/kg 玛咖多糖可减轻化疗药5-氟尿吡啶对机体免疫系统的损伤 [102]玛咖酰胺 SGC 7901、HT-29、MCF 7、NCI-H460、HepG2等癌细胞 - 玛咖酰胺对HT-29癌细胞系的增殖具有抑制活性,对SGC 7901、MCF 7、NCI-H460和HepG2癌细胞系的增殖无活性 [103]
[1] OCHOA C, UGENT D. Maca (Lepidium meyenii Walp.;Brassicaceae): a nutritious root crop of the central Andes[J]. Economic Botany, 2001, 55(3): 344-345. DOI:10.1007/bf02866557.
[2] HE Y Y, SUN Q Q, ZHANG X W, et al. Authentication of the geographical origin of Maca (Lepidium meyenii Walp.) at different regional scales using the stable isotope ratio and mineral elemental fingerprints[J]. Food Chemistry, 2020, 311: 8. DOI:10.1016/j.foodchem.2019.126058.
[3] HUARANCCA R T, ESPARZA E, CRESTANI G, et al. Physiological responses of maca (Lepidium meyenii Walp.) plants to UV radiation in its high-altitude mountain ecosystem[J]. Scientific Reports, 2020,10(1): 2654. DOI:10.1038/s41598-020-59638-4.
[4] 李颖, 李鹏英, 周修腾, 等. 玛咖研究及应用进展[J]. 中国中药杂志,2018, 43(23): 4599-4607. DOI:10.19540/j.cnki.cjcmm.2018.0122.
[5] 许敏, 徐丽, 宋晖, 等. 玛咖的研究进展[J]. 食品安全质量检测学报,2015, 6(7): 2775-2782. DOI:10.19812/j.cnki.jfsq11-5956/ts.2015.07.069.
[6] 汤媛媛. 玛咖多糖的制备及性能研究[D]. 武汉: 湖北工业大学,2017: 32-53.
[7] ZHANG Lijun, ZHAO Qingsheng, WANG Liwei, et al. Protective effect of polysaccharide from maca (Lepidium meyenii) on Hep-G2 cells and alcoholic liver oxidative injury in mice[J]. International Journal of Biological Macromolecules, 2017, 99: 63-70. DOI:10.1016/j.ijbiomac.2017.01.125.
[8] 唐云. 玛咖多糖的提取分离纯化、结构表征及抗疲劳活性研究[D].天津: 天津科技大学, 2018: 5-7.
[9] ZHENG Y, ZHANG W C, WU Z Y, et al. Isolation of an antifatigue preparation from cellulase-treated Maca by hydroalcoholic extraction[J]. Current Topics in Nutraceutical Research, 2019, 17(1):93-98.
[10] 杜晶, 汪珊. 多糖提取技术的研究进展[J]. 中国社区医师, 2018,34(17): 9-11. DOI:10.3969/j.issn.1007-614x.2018.17.003.
[11] 王宏慧, 李翠翠, 罗双群, 等. 玛咖多糖的研究进展[J]. 食品研究与开发, 2018, 39(10): 201-204; 224. DOI:10.3969/j.issn.1005-6521.2018.10.037.
[12] 徐娟, 张水滔, 李云仙, 等. 黑玛咖多糖超声辅助提取研究[J]. 粮食与油脂, 2017, 30(3): 72-74. DOI:10.3969/j.issn.1008-9578.2017.03.019.
[13] 陈杰, 周芳. 百合多糖超声提取工艺条件优化[J]. 现代食品,2019(22): 79-82. DOI:10.16736/j.cnki.cn41-1434/ts.2019.22.023.
[14] 浦跃武, 王金全. 超声波提取玛咖多糖的工艺研究[J]. 食品科技,2010, 35(3): 174-177. DOI:10.13684/j.cnki.spkj.2010.03.001.
[15] 刘玉峰, 马海燕, 李鲁盼, 等. 天然活性多糖提取工艺及结构解析研究进展[J]. 辽宁大学学报(自然科学版), 2018, 45(2): 154-161.DOI:10.16197/j.cnki.lnunse.2018.02.010.
[16] LI Jing, SUN Qingrui, MENG Qingran, et al. Anti-fatigue activity of polysaccharide fractions from Lepidium meyenii Walp. (Maca)[J].International Journal of Biological Macromolecules, 2017, 95: 1305-1311. DOI:10.1016/j.ijbiomac.2016.11.031.
[17] ZHA Zhengqi, WANG Suyan, CHU Weihua, et al. Isolation,purification, structural characterization and immunostimulatory activity of water-soluble polysaccharides from Lepidium meyenii[J]. Phytochemistry, 2018, 147: 184-193. DOI:10.1016/j.phytochem.2018.01.006.
[18] TANG Weimin, JIN Lu, XIE Lianghua, et al. Structural characterization and antifatigue effect in vivo of Maca (Lepidium meyenii Walp.) polysaccharide[J]. Journal of Food Science, 2017,82(3): 757-764. DOI:10.1111/1750-3841.13619.
[19] 陈燕文, 李玉娟, 宋梦璐, 等. PMP柱前衍生化-HPLC法分析玛咖多糖的单糖组成[J]. 当代化工, 2017, 46(8): 1513-1516; 1520.DOI:10.13840/j.cnki.cn21-1457/tq.2017.08.004.
[20] ZHANG M, WANG G, LAI F, et al. Structural characterization and immunomodulatory activity of a novel polysaccharide from Lepidium meyenii[J]. Journal Agricultural Food Chemistry, 2016, 64(9): 1921-1931. DOI:10.1021/acs.jafc.5b05610.
[21] ZHANG M, WU W, REN Y, et al. Structural characterization of a novel polysaccharide from Lepidium meyenii (Maca) and analysis of its regulatory function in macrophage polarization in vitro[J].Journal of Agricultural and Food Chemistry, 2017, 65(6): 1146-1157.DOI:10.1021/acs.jafc.6b05218.
[22] KANG C C, HAO L M, ZHANG L M, et al. Isolation, purification and antioxidant activity of polysaccharides from the leaves of maca (Lepidium Meyenii)[J]. International Journal of Biological Macromolecules, 2018,107: 2611-2619. DOI:10.1016/j.ijbiomac.2017.10.139.
[23] LI S, HAO L, KANG Q, et al. Purification, characterization and biological activities of a polysaccharide from Lepidium meyenii leaves[J]. International Journal of Biological Macromolecules, 2017,103: 1302-1310. DOI:10.1016/j.ijbiomac.2017.05.165.
[24] WANG C, XU L, HUANG L, et al. Optimization of Maca polysaccharide extraction process and its chemo-protective effects on cyclophosphamide-induced mice[J]. Journal of Food Process Engineering, 2018, 41(7): 10-14. DOI:10.1111/jfpe.12856.
[25] WEI W, YE Z, QIAN L, et al. Immunomodulatory effects of a polysaccharide purified from Lepidium meyenii Walp. on macrophages[J]. Process Biochemistry, 2016, 51(4): 542-553.DOI:10.1016/j.procbio.2016.01.003.
[26] 王爱华, 刘英梅, 王丽丽, 等. 玛咖生物碱对人肝癌细胞Bel-7402和H22荷瘤小鼠的抑制作用[J]. 现代食品科技, 2018, 34(11): 52-56.DOI:10.13982/j.mfst.1673-9078.2018.11.009.
[27] 刘建祥, 刘祥义, 李云仙, 等. 匀浆法提取新鲜玛咖中总生物碱的工艺优化研究[J]. 粮食与油脂, 2018, 31(9): 25-28. DOI:10.3969/j.issn.1008-9578.2018.09.008.
[28] 周严严. 玛咖化学成分分析及其神经保护作用机制研究[D]. 北京:中国中医科学院, 2017: 15-19.
[29] 许敏, 王兆杰, 杨少杰, 等. 玛咖的化学成分和生物活性研究进展[J]. 食品研究与开发, 2017, 38(1): 193-199. DOI:10.3969/j.issn.1005-6521.2017.01.045.
[30] 刘淼, 黄莹莹, 林梦雅, 等. 黑玛咖不同提取物的抗疲劳作用与谱效关系研究[J]. 中草药, 2018, 49(9): 2090-2096. DOI:10.7501/j.issn.0253-2670.2018.09.017.
[31] ZHOU M, ZHANG R Q, CHEN Y J, et al. Three new pyrrole alkaloids from the roots of Lepidium meyenii[J]. Phytochemistry Letters, 2018,23: 137-140. DOI:10.1016/j.phytol.2017.12.002.
[32] 高斌, 李双玲, 刘凤静, 等. 不同色型玛咖中总生物碱酸水提取工艺的优化[J]. 食品工业科技, 2018, 39(18): 176-180. DOI:10.13386/j.issn1002-0306.2018.18.031.
[33] 王未, 贾清东, 毛日文, 等. 循环超声提取玛咖生物碱动力学及热力学研究[J]. 食品与生物技术学报, 2017, 36(5): 512-518.DOI:10.3969/j.issn.1673-1689.2017.05.011.
[34] 付玲, 陈芮. 玛咖酰胺及玛咖烯的研究进展[J]. 化工管理, 2019(1):55-56. DOI:10.3969/j.issn.1008-4800.2019.01.034.
[35] ZHAO Jianping, MUHAMMAD I, DUNBAR D C, et al. New alkamides from Maca (Lepidium meyenii)[J]. Journal of Agricultural and Food Chemistry, 2005, 53(3): 690-693. DOI:10.1021/jf048529t.
[36] 谢逸欣, 赖富饶, 曾婷, 等. 大孔吸附树脂分离纯化玛咖生物碱的研究[J]. 食品科技, 2014(10): 241-245. DOI:10.13684/j.cnki.spkj.2014.10.052.
[37] 杜广香. 玛咖生物碱的分离纯化及抗氧化活性研究[D]. 广州: 华南理工大学, 2011: 40-52.
[38] 卢馨, 刘文虎, 曾里, 等. 酸性染料比色法测定玛咖总生物碱含量的方法研究[J]. 食品工业, 2014, 35(1): 241-244.
[39] 查圣华. 玛咖活性成分及抗疲劳功能研究[D]. 北京: 中国科学院大学, 2016: 31-33.
[40] XIA C, DENG J L, CHEN J, et al. Simultaneous determination of macaenes and macamides in maca using an HPLC method and analysis using a chemometric method (HCA) to distinguish maca origin[J]. Revista Brasileira de Farmacognosia, 2019, 29(6): 702-709.DOI:10.1016/j.bjp.2019.05.009.
[41] MEISSNER H O, XU L J, WAN W T, et al. Glucosinolates profiles in Maca phenotypes cultivated in Peru and China (Lepidium peruvianum syn. L. meyenii)[J]. Phytochemistry Letters, 2019, 31: 208-216.DOI:10.1016/j.phytol.2019.04.011.
[42] 朱龙波, 詹志来, 郝庆秀, 等. 玛咖化学成分与生物活性研究进展[J].中国中药杂志, 2019, 44(19): 4142-4151. DOI:10.19540/j.cnki.cjcmm.20190419.202.
[43] 周严严, 赵海誉, 司南, 等. 药用植物玛咖研究新进展[J]. 中国中药杂志, 2015, 40(23): 4521-4530. DOI:10.4268/cjcmm20152301.
[44] 杨晓飞. 玛咖有效成分提取工艺设计[D]. 济南: 山东师范大学,2015: 12-42.
[45] 金文闻. 药食两用植物玛咖(Lepidium meyenii)的功效物质研究[D].武汉: 华中科技大学, 2007: 42-52.
[46] 何雪梅. 缓解良性前列腺增生的功能食品研究与开发[D]. 武汉: 华中科技大学, 2013: 10-17.
[47] 郝利民, 鲁吉珂, 巴建明, 等. 云南栽培玛咖芥子油苷提取工艺的优化[J]. 食品与发酵工业, 2013, 39(3): 202-205. DOI:10.13995/j.cnki.11-1802/ts.2013.03.018.
[48] GASCO M, VILLEGAS L, S, RUBIO J, et al. Dose-response effect of red Maca (Lepidium meyenii) on benign prostatic hyperplasia induced by testosterone enanthate[J]. Phytomedicine, 2007, 14(7): 460-464.DOI:10.1016/j.phymed.2006.12.003.
[49] 张利军. 玛咖对II型糖尿病降糖作用及机理研究[D]. 北京: 中国科学院大学, 2017: 27-38.
[50] 李婧. 玛咖主要水溶性抗疲劳功能成分研究[D]. 无锡: 江南大学,2018: 12-26.
[51] 徐涓, 张弘, 孙彦琳, 等. 鲜玛咖块根中芥子油苷提取工艺研究[J].中国食品学报, 2013, 13(6): 62-68. DOI:10.16429/j.1009-7848.2013.06.021.
[52] 唐霖, 殷红军, 斯聪聪, 等. HPLC测定不同产地玛咖中苄基芥子油苷的含量[J]. 中国中药杂志, 2015, 40(23): 4541-4544. DOI:10.4268/cjcmm20152304.
[53] 艾中, 程爱芳, 孟际勇, 等. 国产玛咖芥子油苷的组分分析和含量测定[J]. 食品科技, 2012, 37(4): 182-186. DOI:10.13684/j.cnki.spkj.2012.04.011.
[54] PARVINA J E, FUENTES K, PEREZ J C, et al. Characterization of sterols in lipidic fraction of maca (Lepidium meyenii Walp.) through chromatographic techniques[J]. Revista de la Sociedad Química del Perú, 2009, 75(2): 254-265.
[55] DINI A, MIGLIUOLO G, RASTRELLI L. Chemical composition of Lepidium meyenii[J]. Food Chemistry, 1994, 49(4): 347-349.DOI:10.1016/0308-8146(94)90003-5.
[56] 杜萍, 杨敏, 朱艳琴, 等. 云南玛咖中功能性成分的分析研究[J].食品工业科技, 2 0 1 6, 3 7(1 6): 7 1-7 5. D O I:1 0.1 3 3 8 6/j.issn1002-0306.2016.16.005.
[57] 甘瑾, 冯颖, 张弘, 等. 3 种色型玛咖甾醇组分及含量分析[J].林业科学研究, 2013, 26(1): 129-132. DOI:10.13275/j.cnki.lykxyj.2013.01.006.
[58] BAI N, HE K, ROLLER M, et al. Flavonolignans and other constituents from Lepidium meyenii with activities in anti-inflammation and human cancer cell lines[J]. Journal of Agricultural and Food Chemistry, 2015, 63(9): 2458-2463.DOI:10.1021/acs.jafc.5b00219.
[59] 周晓明, 闫鹏, 马凯, 等. 响应面法优化超声波辅助提取玛咖总黄酮的工艺研究[J]. 新疆农业科学, 2012, 49(8): 1414-1420.DOI:10.6048/j.issn.1001-4330.2012.08.007.
[60] 李会端. 响应面优化玛咖总黄酮提取对·OH抑制作用探究[J]. 食品科技, 2015, 40(4): 302-308. DOI:10.13684/j.cnki.spkj.2015.04.059.
[61] 李玉娟, 陈燕文, 席晓志, 等. 响应面法优化玛咖总黄酮提取工艺[J]. 食品与药品, 2017, 19(4): 251-256. DOI:10.3969/j.issn.1672-979X.2017.04.006.
[62] 张黎明, 李瑞超, 郝利民, 等. 响应面优化玛咖叶总黄酮提取工艺及其抗氧化活性研究[J]. 现代食品科技, 2014, 30(4): 233-239.DOI:10.13982/j.mfst.1673-9078.2014.04.019.
[63] 张玲. 玛咖淀粉的物理化学性质及分子结构研究[D]. 无锡: 江南大学, 2018: 28-30.
[64] 孙晓东, 唐辉, 杜萍, 等. 丽江玛咖的营养成分分析及多糖体外的抗氧化作用[J]. 光谱实验室, 2013, 30(5): 2365-2371. DOI:10.3969/j.issn.1004-8138.2013.05.071.
[65] 余龙江, 金文闻. 玛咖(Lepidium meyenii.)干粉的营养成分及抗疲劳作用研究[J]. 食品科学, 2004, 25(2): 164-166. DOI:10.3321/j.issn:1002-6630.2004.02.038.
[66] ZHANG L, LI G, WANG S, et al. Physicochemical properties of maca starch[J]. Food Chemistry, 2017, 218: 56-63. DOI:10.1016/j.foodchem.2016.08.123.
[67] WANG S, NIE S, ZHU F. Chemical constituents and health effects of sweet potato[J]. Food Research International, 2016, 89: 90-116.DOI:10.1016/j.foodres.2016.08.032.
[68] 张黎明, 刘娜, 郝利民, 等. 玛咖淀粉与马铃薯、淮山药淀粉的理化性质比较[J]. 现代食品科技, 2016, 32(3): 73-78. DOI:10.13982/j.mfst.1673-9078.2016.3.013.
[69] 刘娜, 郝利民, 刘雪涵, 等. 玛咖淀粉的结构特征与糊化特性[J].天津科技大学学报, 2016, 31(2): 26-30. DOI:10.13364/j.issn.1672-6510.20150066.
[70] 刘娜. 玛咖总黄酮和多酚的提取及植物不同部位营养成分分析[D].天津: 天津科技大学, 2016: 39-46.
[71] HUANG L Z, HUANG B K, YE Q, et al. Bioactivity-guided fractionation for anti-fatigue property of Acanthopanax senticosus[J].Journal of Ethnopharmacology, 2011, 133(1): 213-219. DOI:10.1016/j.jep.2010.09.032.
[72] 李婧, 孙清瑞, 张连富. 玛咖水溶性成分的抗疲劳活性研究[J].食品与生物技术学报, 2019, 38(8): 97-103. DOI:10.3969/j.issn.1673-1689.2019.08.014.
[73] 李世林. 玛咖多糖提取工艺的优化及对大鼠抗疲劳能力的影响[J]. 辽宁体育科技, 2018, 40(3): 42-46. DOI:10.13940/j.cnki.lntykj.2018.03.012.
[74] TANG W M, JIN L, XIE L H, et al. Structural characterization and antifatigue effect in vivo of Maca (Lepidium meyenii Walp.)polysaccharide[J]. Journal of Food Science, 2017, 82(3): 757-764.DOI:10.1111/1750-3841.13619.
[75] CHOI E H, KANG J I, CHO J Y, et al. Supplementation of standardized lipid-soluble extract from Maca (Lepidium meyenii)increases swimming endurance capacity in rats[J]. Journal of Functional Foods, 2012, 4(2): 568-573. DOI:10.1016/j.jff.2012.03.002.
[76] YANG Qin, JIN Wenwen, LU Xueyuan, et al. Effects of macamides on endurance capacity and anti-fatigue property in prolonged swimming mice[J]. Pharmaceutical Biology, 2016, 54(5): 827-834. DOI:10.3109/13880209.2015.1087036.
[77] WANG W, ZHANG F M, LI Q, et al. Structure characterization of one polysaccharide from Lepidium meyenii Walp., and its antioxidant activity and protective effect against H2O2-induced injury RAW264.7 cells[J]. International Journal of Biological Macromolecules, 2018,118: 816-833. DOI:10.1016/j.ijbiomac.2018.06.117.
[78] LEE Y K, CHANG Y H. Physicochemical and antioxidant properties of methanol extract from Maca (Lepidium meyenii Walp.) leaves and roots[J]. Food Science and Technology, 2019, 39: 278-286.DOI:10.1590/fst.03818.
[79] 甘瑾. 玛咖(Lepidium meyenii Walp.)抗氧化活性及活性物质基础的研究[D]. 北京: 中国林业科学研究院, 2013: 51-96.
[80] 李慧敏, 贺凯, 郑慧, 等. 中医药健脾的保健作用机制及药食资源[J]. 中草药, 2020, 51(3): 780-787. DOI:10.7501/j.issn.0253-2670.2020.03.031.
[81] 汪颖姣, 胡琪, 乔旺, 等. 玛咖生物碱通过调节小鼠免疫力抑制结肠癌细胞的成瘤能力[J]. 现代食品科技, 2019, 35(10): 38-43; 65.DOI:10.13982/j.mfst.1673-9078.2019.10.007.
[82] 张永忠, 余龙江, 万军梅, 等. 玛咖醇提物对正常小鼠免疫功能的影响[J].天然产物研究与开发, 2007, 19(2): 274-276. DOI:10.16333/j.1001-6880.2007.02.024.
[83] BUSTOS-OBREGON E, YUCRA S, GONZALES G F. Lepidium meyenii (Maca) reduces spermatogenic damage induced by a single dose of malathion in mice[J]. Asian Journal of Andrology, 2005, 7(1):71-76. DOI:10.1111/j.1745-7262.2005.00006.x.
[84] 周意, 栾洁, 刘玉香, 等. 玛咖多糖对果蝇性活力及繁殖力影响[J]. 中国食品添加剂, 2016(8): 86-90. DOI:10.3969/j.issn.1006-2513.2016.08.007.
[85] 乐娜, 周雪, 费文婷, 等. 玛咖对虚寒及虚热证大鼠环核苷酸水平及神经-内分泌-免疫网络的影响[J]. 中国中药杂志, 2020, 45(5): 1004-1010. DOI:10.19540/j.cnki.cjcmm.20190916.401.
[86] 张永忠, 余龙江, 敖明章. 玛咖醇提取物对去卵巢大鼠内分泌激素及血脂水平的影响[J]. 中国新药杂志, 2008, 17(24): 2112-2114.DOI:10.3321/j.issn.1003-3734.2008.24.009.
[87] 王竹, 杨晶明, 王国栋, 等. 玛咖独行菜对卵巢切除术后大鼠血脂及骨质代谢的影响[J]. 卫生研究, 2009, 38(4): 420-422. DOI:10.19813/j.cnki.weishengyanjiu.2009.04.012.
[88] 王义强, 陈章靖, 王启业, 等. 玛咖药用价值与引种培育研究进展[J]. 经济林研究, 2014, 32(2): 167-172. DOI:10.14067/j.cnki.1003-8981.2014.02.006.
[89] BAI N S, HE K, ROLLER M, et al. Flavonolignans and other constituents from Lepidium meyenii with activities in antiinflammation and human cancer cell lines[J]. Journal of Agricultural and Food Chemistry, 2015, 63(9): 2458-2463. DOI:10.1021/acs.jafc.5b00219.
[90] CUI Baoliang, ZHENG Bolin, HE Kan, et al. Imidazole alkaloids from Lepidium meyenii[J]. Journal of Natural Products, 2003, 66(8): 1101-1103. DOI:10.1021/np030031i.
[91] 姜立科, 董浩, 张仁堂, 等. 玛咖功能作用及开发利用研究进展[J]. 中国食物与营养, 2015, 21(5): 69-71. DOI:10.3969/j.issn.1006-9577.2015.05.017.
[92] LIU H, JIN W, FU C, et al. Discovering anti-osteoporosis constituents of Maca (Lepidium meyenii) by combined virtual screening and activity verification[J]. Food Research International, 2015, 77: 215-220. DOI:10.1016/j.foodres.2015.06.028.
[93] YU Z, JIN W, CUI Y, et al. Protective effects of macamides from Lepidium meyenii Walp. against corticosterone-induced neurotoxicity in PC12 cells[J]. RSC Advances, 2019(40): 23096-23108.DOI:10.1039/c9ra03268a.
[94] YU Z, JIN W, DONG X, et al. Safety evaluation and protective effects of ethanolic extract from Maca (Lepidium meyenii Walp.) against corticosterone and H2O2 induced neurotoxicity[J]. Regulatory Toxicology and Pharmacology, 2020, 111: 13-21. DOI:10.1016/j.yrtph.2019.104570.
[95] LEE Y K, JUNG S K, CHANG Y H. Rheological properties of a neutral polysaccharide extracted from maca (Lepidium meyenii Walp.)roots with prebiotic and anti-inflammatory activities[J]. International Journal of Biological Macromolecules, 2020, 152: 757-765.DOI:10.1016/j.ijbiomac.2020.02.307.
[96] LI J Y, CHEN L F, LI J W, et al. The composition analysis of Maca(Lepidium meyenii Walp.) from xinjiang and its antifatigue activity[J].Journal Food Quality, 2017(2): 1-7. DOI:10.1155/2017/2904951.
[97] LI Y, XU F, ZHENG M, et al. Maca polysaccharides: a review of compositions, isolation, therapeutics and prospects[J]. International Journal of Biological Macromolecules, 2018, 111: 894-902.DOI:10.1016/j.ijbiomac.2018.01.059.
[98] ZHENG Y, ZHANG W C, WU Z Y, et al. Two macamide extracts relieve physical fatigue by attenuating muscle damage in mice[J].Journal of the Science of Food and Agriculture, 2019, 99(3): 1405-1412. DOI:10.1002/jsfa.9318.
[99] FUMIAKI U, TAMAKI J, RYOSUKE T, et al. Lepidium meyenii(Maca) enhances the serum levels of luteinising hormone in female rats[J]. Journal of Ethnopharmacology, 2014, 151(2): 897-902.DOI:10.1016/j.jep.2013.11.058.
[100] GUO S S, GAO X F, GU Y R, et al. Preservation of cognitive function by Lepidium meyenii (Maca) is associated with improvement of mitochondrial activity and upregulation of autophagy-related proteins in middle-aged mouse cortex[J]. Evidence Based Complementary and Alternative Medicine, 2016: 1-9. DOI:10.1155/2016/4394261.
[101] RUBIO J, DANG H, GONG M, et al. Aqueous and hydroalcoholic extracts of black Maca (Lepidium meyenii) improve scopolamineinduced memory impairment in mice[J]. Food and Chemical Toxicology, 2007, 45(10): 1882-1890. DOI:10.1016/j.fct.2007.04.002.
[102] 严颖, 孔娜, 沈花, 等. 玛咖多糖增强机体免疫状态提高5-氟尿嘧啶对荷瘤小鼠的疗效[J]. 江苏大学学报(医学版), 2019, 29(1): 37-41.DOI:10.13312/j.issn.1671-7783.y180114.
[103] XIA C, CHEN J, DENG J L, et al. Novel macamides from maca (Lepidium meyenii Walpers) root and their cytotoxicity[J].Phytochemistry Letters, 2018, 25: 65-69. DOI:10.1016/j.phytol.2018.03.001.