全二维气相色谱-质谱法对鱼露发酵过程中挥发性风味成分分析
陈丽丽,白春清,袁美兰,江 勇,赵 利*
(江西科技师范大学生命科学学院,国家淡水鱼加工技术研发分中心,江西 南昌 330013)
摘 要:采用静态顶空固相微萃取结合全二维气相色谱-质谱法分析发酵过程中鱼露挥发性化合物的变化。取不同发酵时间点的样品进行检测,通过相近发酵时间之间的对比,选择发酵过程中变化较明显的化合物进行研究,共检测化合物116 种,对其进行分类,并结合质谱数据库和保留指数进行鉴定。在此基础上采用主成分分析法和热图分析挥发性化合物的变化规律,结果发现:在发酵至第20天时,鱼露的风味可以被明显地区分开,说明鱼露风味化合物的产生主要是在发酵后期。
关键词:顶空固相微萃取;气相色谱-质谱;鱼露;挥发性物质
收稿日期:2019-10-16
基金项目:江西省现代农业产业技术体系建设专项(赣财文指[2018]13号);江西省高等学校科技落地计划项目(KJLD12009);江西省教育厅科学计划青年项目(GJJ190609)
第一作者简介:陈丽丽(1986—)(ORCID: 0000-0002-8227-7884),女,讲师,硕士,研究方向为水产食品加工贮藏。E-mail: 328181539@qq.com
*通信作者简介:赵利(1967—)(ORCID: 0000-0002-2182-5568),女,教授,博士,研究方向为食品化学。E-mail: 13970892565@126.com
DOI:10.7506/spkx1002-6630-20191016-155
中图分类号:TS254.4
文献标志码:A
文章编号:1002-6630(2020)22-0238-07
引文格式:
陈丽丽, 白春清, 袁美兰, 等. 全二维气相色谱-质谱法对鱼露发酵过程中挥发性风味成分分析[J]. 食品科学, 2020,41(22): 238-244. DOI:10.7506/spkx1002-6630-20191016-155. http://www.spkx.net.cn
CHEN Lili, BAI Chunqing, YUAN Meilan, et al. Analysis of volatile flavor components of fish sauce during fermentation by using comprehensive two-dimensional gas chromatography-mass spectroscopy[J]. Food Science, 2020, 41(22): 238-244.(in Chinese with English abstract) DOI:10.7506/spkx1002-6630-20191016-155. http://www.spkx.net.cn
Analysis of Volatile Flavor Components of Fish Sauce during Fermentation by Using Comprehensive Two-dimensional Gas Chromatography-Mass Spectroscopy
CHEN Lili, BAI Chunqing, YUAN Meilan, JIANG Yong, ZHAO Li*
(National Freshwater Fish Processing Technology Research and Development Branch Center, College of Life Science,Jiangxi Science & Technology Normal University, Nanchang 330013, China)
Abstract: Static headspace solid phase micro-extraction (HS-SPME) combined with comprehensive two-dimensional gas chromatography-mass spectrometry (GC × GC-MS) was used to analyze the changes of volatile compounds during the fermentation process of fish sauce. Samples were taken at different fermentation time points and used for comparison. The compounds whose contents obviously changed during fermentation were selected for comparison. A total of 116 compounds were identified by their mass spectra and retention indexes. Future, principal component analysis (PCA) and heat map were used to analyze the changes of volatile compounds. The results showed that the flavor of fish sauce could be clearly distinguished after 20 days of fermentation, indicating that the flavor compounds of fish sauce were mainly produced in the late stage of fermentation.
Keywords: headspace solid phase micro-extraction; gas chromatography-mass spectrometry; fish sauce; volatile compounds
鱼露是最受欢迎的烹饪酱料之一,具有独特的风味,给人以味觉上的愉悦。鱼露风味形成是蛋白质和脂肪的氧化分解,形成含有氨基酸、肽等复杂的呈香、呈味的化合物体系[1]。目前,国内外鱼露挥发性风味物质的研究很多,但主要是不同发酵工艺、风味和微生物方面[2-5]的研究,对挥发性风味物质和前体物质的来源研究较少[6]。鱼露风味组成相当复杂,Katsuya等[7]通过炙烤香、鱼腥味、氨味、酸败味、奶酪香、肉香描述鱼露的特征性风味;Pham等[8]通过鱼腥味、奶酪味、黄油爆米花味和熟米饭味描述鱼露的特征性风味;Giri等[9]认为鱼露的主要特征气味是坚果味、奶酪味、氨味、鱼腥味,其中氨、胺类等构成氨味。Shimoda等[10]对鱼露进行碱化处理,提高了鱼露中含氮和含硫化合物的释放,采用气相色谱-质谱分析法对鱼露的挥发性物质进行检测,鉴定124 种化合物,碱化后对三甲胺、二甲基二硫等不易被现有方法检测到的高挥发性含氮含硫化合物检测得到了加强。大多数脂类化合物对风味有重要的贡献,脂类化合物在发酵过程中经过水解和氧化后被降解成酮、醛类等小分子化合物[11]。海水鱼中含有多种不饱和脂肪酸如二十二碳六烯酸、二十碳五烯酸[12],不同脂肪酸含量发生改变,都对鱼露风味的形成有重要的作用。
鱼露风味物质的分析,除了需选择萃取方法之外,检测方法的选择也同样重要。全二维气相色谱是在传统二维基础上发展起来的一种新技术,与传统色谱不同,样品的组分都经过了两根独立色谱柱的分离。分离的组分最后进入检测器,检测到的响应信号经过数据采集软件处理后,就会在计算机上得到三维色谱图。色谱图的2 个横坐标代表两根色谱柱的保留时间,纵坐标代表检测器信号的强度,根据色谱图的出峰时间和峰体积,可以对每个组分定性定量分析鉴定[13-15]。全二维气相色谱具有分离度好、峰容量大、杂质干扰较小等特点[16]。主要是由于在色谱柱中样品经2 次独立的分离并在第1次分离运行的同时完成二维分离,能够在短时间内检测到较多成分信息[13]。目前全二维气相色谱已经被应用于环境、植物和食品等领域内,其中一些研究将全二维气相色谱与质谱连接应用于食品加工检测、食品污染评估、食品真实性评估等食品分析领域[17-20]。使得食品风味成分的分析检测有了新的突破。
本研究采用静态顶空固相微萃取(headspace-solid phase micro extraction,HS-SPME)结合全二维气相色谱-质谱(full two-dimensional gas chromatography-mass spectrometry,GC×GC-MS)法分析发酵过程中鱼露挥发性化合物的变化。取不同发酵时间点的样品进行检测,通过相近发酵时间之间进行对比,选择发酵过程中变化较明显的化合物进行研究。并结合质谱数据库和保留指数(retention index,RI)进行鉴定。在此基础上采用主成分分析(principal component analysis,PCA)法和热图分析挥发性化合物的变化规律。为探讨鱼露风味的产生机理以及生产中提高鱼露的风味口感提供理论依据。
1 材料与方法
1.1 材料与试剂
将草鱼和鳗鱼的内脏经分段加盐、低盐速酿的方法发酵制备鱼露[21]。分别取发酵过程中第0、5、10、15、20、25、30天和成品鱼露为样品进行测定,所有样品4 ℃冰箱保存。银鱼鱼露由青岛正道食品有限公司提供。
混合正构烷烃标准溶液 美国Restek公司;2,4,6-三甲基吡啶标准品 美国Alfa Aesar公司;氯化钠(分析纯)上海麦克林生化科技有限公司。
1.2 仪器与设备
AOC-5000 HS-SPME三合一自动进样器 瑞士CTC公司;65 μm PDMS/DVB萃取头 美国Supelco公司;GCMS-TQ8050三重四极杆型GC-MS联用仪 日本岛津公司;20 mm聚四氟乙烯磁性盖头 德国CNW公司;20 mL顶空瓶 美国Altech公司。
1.3 方法
1.3.1 草鱼鱼露样品挥发性风味物质检测
1.3.1.1 样品处理
向20 mL的顶空瓶中加入5 mL鱼露样品和5 g NaCl,振摇1 min,使其达到过饱和,加入10 μL质量浓度为50 mg/L的标准品2,4,6-三甲基吡啶,然后用聚四氟乙烯磁性盖头迅速密封,置于自动进样器中。萃取头(250 ℃活化30 min)按照程序设定的萃取条件在顶空瓶中上部吸附样品中的挥发性物质,然后插入GC进样口解吸5 min,进行GC×GC-MS分析。每组样品分别测5 个不同的批号样品。
1.3.1.2 检测条件
G C 条件:色谱柱一:聚乙二醇毛细色谱柱HP-INNOWax(30 m×0.25 mm,0.25 μm);色谱柱二:ID-BPX1毛细色谱柱(10 m×0.1 mm,0.1 μm)。载气为He(99.999%);柱前压为285.7 kPa;柱箱温度50 ℃;进样口温度250 ℃;不分流进样;流速1 mL/min;进样时间1 min;程序升温:起始温度50 ℃,保持2 min,然后以2 ℃/min升温到250 ℃,保持10 min。
MS条件:电子电离源;离子源温度200 ℃,接口温度250 ℃,电子能量70 eV;不分流进样;溶剂延迟1.5 min后采集信号;检测模式为全扫描,质量扫描范围m/z 45~330。
HS-SPME条件:将顶空瓶(加入处理后的样品)置于自动进样器中,顶空瓶到达SPME加热装置中,在温度57 ℃和振荡频率510 r/min条件下(250 ℃活化30 min)吸附70 min,然后在GC进样口解吸5 min,进行GC×GC-MS分析。
1.3.2 鱼露发酵过程中挥发性化合物的聚类分析
对鱼露样品进行检测分析,找出发酵过程中含量变化较为突出的24 种化合物,再利用HemI 1.0.3.7软件对样品发酵过程中这些化合物含量的变化进行聚类分析,并绘制热图。
1.3.3 鱼露发酵过程中挥发性化合物的PCA
通过对鱼露样品进行GC×GC-MS检测分析,得到数据利用Simca 14.1进行PCA,得出相对应的PCA图。
1.4 数据分析及作图
实验数据采用GC Image、MATLB 7.0和Simca 14.1分析。在1.3.1.2节色谱条件下对正构烷烃标准溶液进行单独进样检测,得到各个烷烃的出峰时间,根据正构烷烃中各个烷烃的出峰时间,计算样品中挥发性化合物的RI,然后在NIST Chemistry WebBook网站中根据化合物的名称在已发表的文献中搜索被测物质的RI,如果2 种化合物的RI误差在±3%以内,则可以对被检测的物质定性分析。采用Excel 2010作图。热图采用HemI 1.0.3.7绘制作图,PCA采用Simca 14.1作图。
2 结果与分析
2.1 鱼露发酵过程中挥发性风味化合物的鉴定
采用静态HS-SPME结合GC×GC-MS对鱼露发酵过程中的挥发性风味化合物进行检测,分别取发酵的第0、5、10、15、20、25、30天以及成品鱼露样品进行检测。通过0 d与5 d、5 d与10 d、10 d与15 d依次类推两两之间进行比较,找出其中含量变化较大的一些挥发性风味化合物进行对比研究,共检测出化合物117 种,不同发酵时间的鱼露样品中检测出来的峰体积结果如表1所示,包括醇类27 种、醛类6 种、酮类11 种、酸类22 种、酯类13 种、烃类14 种、酚类2 种、杂环类8 种、苯环类8 种和其他未分类的化合物6 种。不同的时间点鱼露样品的挥发性风味化合物的差异较大,这种差异可能是因为发酵过程中风味前体物质发生分解代谢反应所产生的[22]。
发酵0 d,样品中共检测到78 种化合物,其中包括醇类19 种(16.21%)、醛类5 种(9.95%)、酮类9 种(0.67%)、酸类15 种(14.53%)、酯类10 种(21.70%)、烃类8 种(25.96%)、杂环类2 种(0.13%)、苯环类5 种(0.19%)和5 种其他类化合物(14.65%)。其中未检测到酚类化合物,酯类化合物的含量最高。其中,2,5,8,11,14-五氧杂-16-十六烷醇(6.59%)、N,N-双(2-羟乙基)-2-氨基乙磺酸(5.26%)、泼尼松龙醋酸酯(15.79%)、洋地黄毒苷(9.65%)、四甲基-硅烷(21.56%)等挥发性物质的含量较高。
随着发酵时间的延长,检测到的化合物种类不断增加,当发酵到第20、25天时,检测到的化合物种类最多为93 种;发酵第25天时,检测到醇类17 种(9.09%)、醛类5 种(6.79%)、酮类7 种(2.37%)、酸类21 种(16.48%)、酯类11 种(36.34%)、烃类11 种(16.29%)、酚类2 种(1.69%)、杂环类6 种(0.56%)、苯环类7 种(0.80%)和6 种其他类化合物(9.61%)。在发酵前期,酮类、酸类和酯类化合物占比不断增加,其中酯类化合物占比增加最快,在酯类化合物中泼尼松龙醋酸酯(25.72%)、赤霉素(5.23%)等挥发性物质的含量较高。
发酵后期,检测到化合物的种类稍有下降,这可能是后期加入酱油酵母进行赋香发酵所致。发酵成品中检测到87 种化合物,包括醇类16 种(9.33%)、醛类5 种(7.6 7%)、酮类6 种(3.5 8%)、酸类21 种(17.11%)、酯类11 种(30.14%)、烃类12 种(16.85%)、酚类2 种(2.09%)、杂环类3 种(0.39%)、苯环类6 种(0.97%)和5 种其他类化合物(11.88%)。其中醛类、酮类、酸类等化合物占比稍有上升,但酯类占比却有一定的下降,可能是发酵后期加入的酱油酵母对酯类的反应产生一定的抑制作用。在发酵完成的鱼露中,检测到洋地黄毒苷(7.27%)、维生素A醛(4.65%)、泼尼松龙醋酸酯(22.57%)、四甲基-硅烷(11.82%)等挥发性物质的含量较高。
表1 鱼露发酵过程中挥发性风味物质的组成
Table 1Composition of volatile flavor substances in fish sauce during fermentation

RI 出峰体积(×107)文献 计算 0 d 5 d 10 d 15 d 20 d 25 d 30 d 成品单甲酸酯-1,2-乙二醇 32.2 — 1 447.62 ND 45.23 75.68 75.87 92.94 75.81 ND ND 1,3,5-苯三醇 62.2 — 1 816.36 ND ND 4.58 3.69 6.22 7.10 4.62 4.32 3,7-二甲基-1,6-辛二烯-3-醇 46.6 1 498 1 481.67 6.00 0.77 ND ND ND ND ND ND 1-己醇 25.8 1 329 1 346.88 7.01 1.69 1.15 ND 1.62 1.82 ND ND 2-乙基-1-己醇 34.6 1 484 1 485.71 0.74 ND ND ND ND ND ND ND 1-戊醇 17.0 1 256 1 254.92 1.59 2.30 ND ND ND ND ND ND 1-十四烷醇 47.9 2 175 2 173.08 4.74 6.96 4.12 6.16 1.41 2.20 10.49 8.71 2,3-丁二醇 37.9 — 1 538.71 ND 43.20 22.42 46.96 114.47 127.10 10.77 95.70 2,5,8,11,14-五氧杂-16-十六烷醇 109.0 — 2 956.10 181.26 167.53 166.89 223.32 233.32 172.58 155.84 135.64 2-呋喃甲醇 45.4 1 666 1 661.67 65.89 82.92 72.35 74.84 94.79 109.64 75.86 64.21 3-甲基-2-庚醇 21.8 — 1 283.61 2.60 5.47 7.04 6.09 4.29 2.44 4.56 13.09 1-(1-甲基乙氧基)-2-丙醇 106.6 — 2 856.76 8.34 8.77 8.50 31.09 178.14 10.72 71.90 61.74醇类 1,3-二氯-2-丙醇 16.4 1 765 1 794.55 ND ND ND ND 3.27 6.14 6.35 6.12 3,4-双(4-羟基苯基)-3,4-己二醇 90.2 — 2 570.73 9.64 10.60 15.79 33.27 38.13 79.35 80.74 95.16 3,6,9,12-四氧杂十六烷-1-醇 108.6 — 2 948.78 111.32 104.99 93.74 108.23 4.78 18.20 25.94 15.47 3-呋喃甲醇 37.8 1 684 1 687.10 0.37 ND ND ND ND ND ND ND 4-戊二醇 5.5 1 154 1 147.71 ND 2.45 5.53 ND ND ND ND ND(Z)-9-十六烯-1-醇 58.6 2 413 2 412.73 15.11 10.06 6.75 4.94 26.07 23.06 89.31 32.82环己醇 32.1 1 376 1 363.03 9.09 ND ND ND ND ND ND ND环十五醇 40.1 — 1 686.67 3.86 2.74 0.93 10.11 ND ND ND ND 2-[2-(2-丁氧基乙氧基)乙氧基]乙醇 21.4 — 1 277.05 3.06 3.00 10.02 7.99 ND ND ND ND类别 风味物质 保留时间/min
续表1
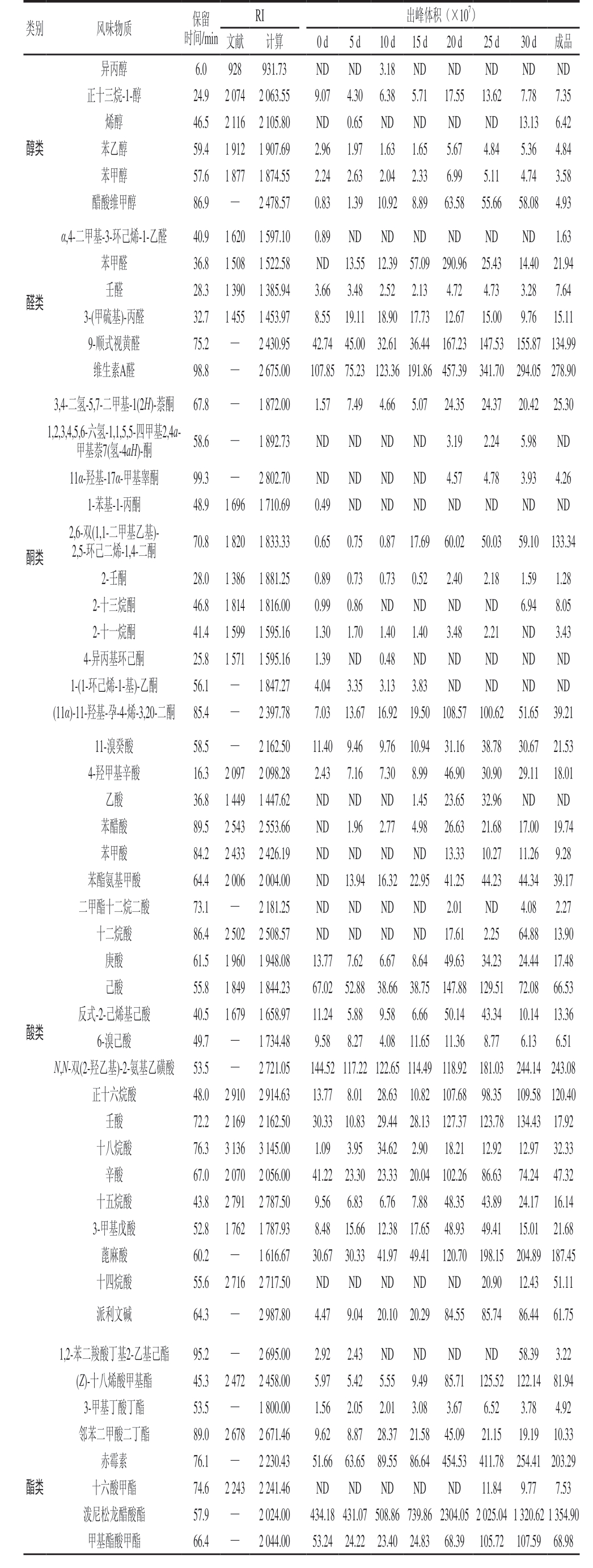
RI 出峰体积(×107)文献 计算 0 d 5 d 10 d 15 d 20 d 25 d 30 d 成品异丙醇 6.0 928 931.73 ND ND 3.18 ND ND ND ND ND正十三烷-1-醇 24.9 2 074 2 063.55 9.07 4.30 6.38 5.71 17.55 13.62 7.78 7.35烯醇 46.5 2 116 2 105.80 ND 0.65 ND ND ND ND 13.13 6.42醇类 苯乙醇 59.4 1 912 1 907.69 2.96 1.97 1.63 1.65 5.67 4.84 5.36 4.84苯甲醇 57.6 1 877 1 874.55 2.24 2.63 2.04 2.33 6.99 5.11 4.74 3.58醋酸维甲醇 86.9 — 2 478.57 0.83 1.39 10.92 8.89 63.58 55.66 58.08 4.93类别 风味物质 保留时间/min醛类α,4-二甲基-3-环己烯-1-乙醛 40.9 1 620 1 597.10 0.89 ND ND ND ND ND ND 1.63苯甲醛 36.8 1 508 1 522.58 ND 13.55 12.39 57.09 290.96 25.43 14.40 21.94壬醛 28.3 1 390 1 385.94 3.66 3.48 2.52 2.13 4.72 4.73 3.28 7.64 3-(甲硫基)-丙醛 32.7 1 455 1 453.97 8.55 19.11 18.90 17.73 12.67 15.00 9.76 15.11 9-顺式视黄醛 75.2 — 2 430.95 42.74 45.00 32.61 36.44 167.23 147.53 155.87 134.99维生素A醛 98.8 — 2 675.00 107.85 75.23 123.36 191.86 457.39 341.70 294.05 278.90 3,4-二氢-5,7-二甲基-1(2H)-萘酮 67.8 — 1 872.00 1.57 7.49 4.66 5.07 24.35 24.37 20.42 25.30 1,2,3,4,5,6-六氢-1,1,5,5-四甲基2,4a-甲基萘7(氢-4aH)-酮 58.6 — 1 892.73 ND ND ND ND 3.19 2.24 5.98 ND酮类11α-羟基-17α-甲基睾酮 99.3 — 2 802.70 ND ND ND ND 4.57 4.78 3.93 4.26 1-苯基-1-丙酮 48.9 1 696 1 710.69 0.49 ND ND ND ND ND ND ND 2,6-双(1,1-二甲基乙基)-2,5-环己二烯-1,4-二酮 70.8 1 820 1 833.33 0.65 0.75 0.87 17.69 60.02 50.03 59.10 133.34 2-壬酮 28.0 1 386 1 881.25 0.89 0.73 0.73 0.52 2.40 2.18 1.59 1.28 2-十三烷酮 46.8 1 814 1 816.00 0.99 0.86 ND ND ND ND 6.94 8.05 2-十一烷酮 41.4 1 599 1 595.16 1.30 1.70 1.40 1.40 3.48 2.21 ND 3.43 4-异丙基环己酮 25.8 1 571 1 595.16 1.39 ND 0.48 ND ND ND ND ND 1-(1-环己烯-1-基)-乙酮 56.1 — 1 847.27 4.04 3.35 3.13 3.83 ND ND ND ND(11α)-11-羟基-孕-4-烯-3,20-二酮 85.4 — 2 397.78 7.03 13.67 16.92 19.50 108.57 100.62 51.65 39.21 11-溴癸酸 58.5 — 2 162.50 11.40 9.46 9.76 10.94 31.16 38.78 30.67 21.53 4-羟甲基辛酸 16.3 2 097 2 098.28 2.43 7.16 7.30 8.99 46.90 30.90 29.11 18.01乙酸 36.8 1 449 1 447.62 ND ND ND 1.45 23.65 32.96 ND ND苯醋酸 89.5 2 543 2 553.66 ND 1.96 2.77 4.98 26.63 21.68 17.00 19.74苯甲酸 84.2 2 433 2 426.19 ND ND ND ND 13.33 10.27 11.26 9.28苯酯氨基甲酸 64.4 2 006 2 004.00 ND 13.94 16.32 22.95 41.25 44.23 44.34 39.17二甲酯十二烷二酸 73.1 — 2 181.25 ND ND ND ND 2.01 ND 4.08 2.27十二烷酸 86.4 2 502 2 508.57 ND ND ND ND 17.61 2.25 64.88 13.90庚酸 61.5 1 960 1 948.08 13.77 7.62 6.67 8.64 49.63 34.23 24.44 17.48己酸 55.8 1 849 1 844.23 67.02 52.88 38.66 38.75 147.88 129.51 72.08 66.53反式-2-己烯基己酸 40.5 1 679 1 658.97 11.24 5.88 9.58 6.66 50.14 43.34 10.14 13.36 6-溴己酸 49.7 — 1 734.48 9.58 8.27 4.08 11.65 11.36 8.77 6.13 6.51 N,N-双(2-羟乙基)-2-氨基乙磺酸 53.5 — 2 721.05 144.52 117.22 122.65 114.49 118.92 181.03 244.14 243.08正十六烷酸 48.0 2 910 2 914.63 13.77 8.01 28.63 10.82 107.68 98.35 109.58 120.40壬酸 72.2 2 169 2 162.50 30.33 10.83 29.44 28.13 127.37 123.78 134.43 17.92十八烷酸 76.3 3 136 3 145.00 1.09 3.95 34.62 2.90 18.21 12.92 12.97 32.33辛酸 67.0 2 070 2 056.00 41.22 23.30 23.33 20.04 102.26 86.63 74.24 47.32十五烷酸 43.8 2 791 2 787.50 9.56 6.83 6.76 7.88 48.35 43.89 24.17 16.14 3-甲基戊酸 52.8 1 762 1 787.93 8.48 15.66 12.38 17.65 48.93 49.41 15.01 21.68蓖麻酸 60.2 — 1 616.67 30.67 30.33 41.97 49.41 120.70 198.15 204.89 187.45十四烷酸 55.6 2 716 2 717.50 ND ND ND ND ND 20.90 12.43 51.11派利文碱 64.3 — 2 987.80 4.47 9.04 20.10 20.29 84.55 85.74 86.44 61.75酸类1,2-苯二羧酸丁基2-乙基己酯 95.2 — 2 695.00 2.92 2.43 ND ND ND ND 58.39 3.22(Z)-十八烯酸甲基酯 45.3 2 472 2 458.00 5.97 5.42 5.55 9.49 85.71 125.52 122.14 81.94 3-甲基丁酸丁酯 53.5 — 1 800.00 1.56 2.05 2.01 3.08 3.67 6.52 3.78 4.92邻苯二甲酸二丁酯 89.0 2 678 2 671.46 9.62 8.87 28.37 21.58 45.09 21.15 19.19 10.33赤霉素 76.1 — 2 230.43 51.66 63.65 89.55 86.64 454.53 411.78 254.41 203.29酯类 十六酸甲酯 74.6 2 243 2 241.46 ND ND ND ND ND 11.84 9.77 7.53泼尼松龙醋酸酯 57.9 — 2 024.00 434.18 431.07 508.86 739.86 2304.05 2 025.04 1 320.62 1 354.90甲基酯酸甲酯 66.4 — 2 044.00 53.24 24.22 23.40 24.83 68.39 105.72 107.59 68.98
续表1
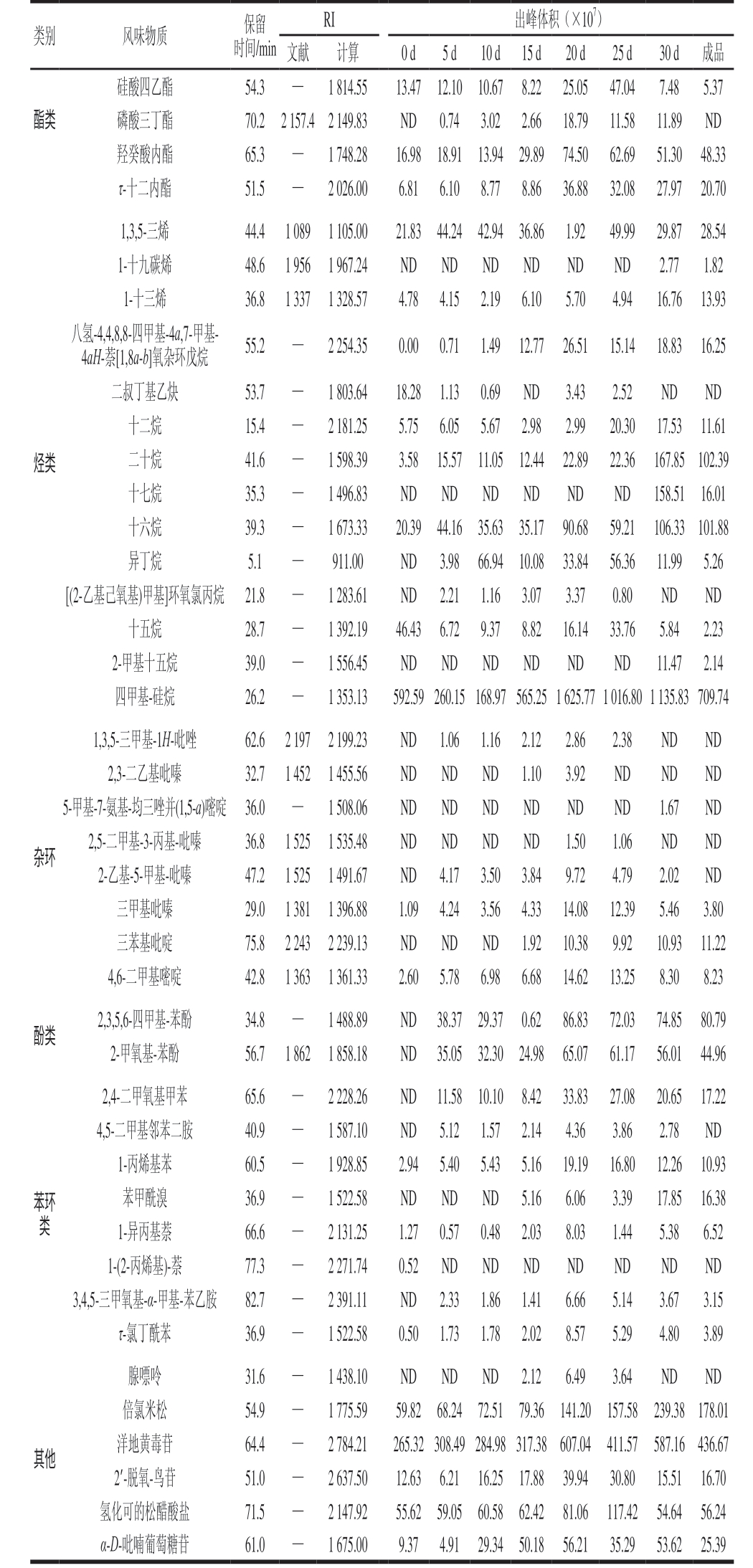
注:—.未检索到相关报道;ND.未检出。
RI 出峰体积(×107)文献 计算 0 d 5 d 10 d 15 d 20 d 25 d 30 d 成品硅酸四乙酯 54.3 — 1 814.55 13.47 12.10 10.67 8.22 25.05 47.04 7.48 5.37酯类 磷酸三丁酯 70.2 2 157.4 2 149.83 ND 0.74 3.02 2.66 18.79 11.58 11.89 ND羟癸酸内酯 65.3 — 1 748.28 16.98 18.91 13.94 29.89 74.50 62.69 51.30 48.33 τ-十二内酯 51.5 — 2 026.00 6.81 6.10 8.77 8.86 36.88 32.08 27.97 20.70类别 风味物质 保留时间/min 1,3,5-三烯 44.4 1 089 1 105.00 21.83 44.24 42.94 36.86 1.92 49.99 29.87 28.54 1-十九碳烯 48.6 1 956 1 967.24 ND ND ND ND ND ND 2.77 1.82 1-十三烯 36.8 1 337 1 328.57 4.78 4.15 2.19 6.10 5.70 4.94 16.76 13.93八氢-4,4,8,8-四甲基-4a,7-甲基-4aH-萘[1,8a-b]氧杂环戊烷 55.2 — 2 254.35 0.00 0.71 1.49 12.77 26.51 15.14 18.83 16.25烃类二叔丁基乙炔 53.7 — 1 803.64 18.28 1.13 0.69 ND 3.43 2.52 ND ND十二烷 15.4 — 2 181.25 5.75 6.05 5.67 2.98 2.99 20.30 17.53 11.61二十烷 41.6 — 1 598.39 3.58 15.57 11.05 12.44 22.89 22.36 167.85 102.39十七烷 35.3 — 1 496.83 ND ND ND ND ND ND 158.51 16.01十六烷 39.3 — 1 673.33 20.39 44.16 35.63 35.17 90.68 59.21 106.33 101.88异丁烷 5.1 — 911.00 ND 3.98 66.94 10.08 33.84 56.36 11.99 5.26[(2-乙基己氧基)甲基]环氧氯丙烷 21.8 — 1 283.61 ND 2.21 1.16 3.07 3.37 0.80 ND ND十五烷 28.7 — 1 392.19 46.43 6.72 9.37 8.82 16.14 33.76 5.84 2.23 2-甲基十五烷 39.0 — 1 556.45 ND ND ND ND ND ND 11.47 2.14四甲基-硅烷 26.2 — 1 353.13 592.59 260.15 168.97 565.25 1 625.77 1 016.80 1 135.83 709.74杂环1,3,5-三甲基-1H-吡唑 62.6 2 197 2 199.23 ND 1.06 1.16 2.12 2.86 2.38 ND ND 2,3-二乙基吡嗪 32.7 1 452 1 455.56 ND ND ND 1.10 3.92 ND ND ND 5-甲基-7-氨基-均三唑并(1,5-a)嘧啶 36.0 — 1 508.06 ND ND ND ND ND ND 1.67 ND 2,5-二甲基-3-丙基-吡嗪 36.8 1 525 1 535.48 ND ND ND ND 1.50 1.06 ND ND 2-乙基-5-甲基-吡嗪 47.2 1 525 1 491.67 ND 4.17 3.50 3.84 9.72 4.79 2.02 ND三甲基吡嗪 29.0 1 381 1 396.88 1.09 4.24 3.56 4.33 14.08 12.39 5.46 3.80三苯基吡啶 75.8 2 243 2 239.13 ND ND ND 1.92 10.38 9.92 10.93 11.22 4,6-二甲基嘧啶 42.8 1 363 1 361.33 2.60 5.78 6.98 6.68 14.62 13.25 8.30 8.23酚类2,3,5,6-四甲基-苯酚 34.8 — 1 488.89 ND 38.37 29.37 0.62 86.83 72.03 74.85 80.79 2-甲氧基-苯酚 56.7 1 862 1 858.18 ND 35.05 32.30 24.98 65.07 61.17 56.01 44.96苯环类2,4-二甲氧基甲苯 65.6 — 2 228.26 ND 11.58 10.10 8.42 33.83 27.08 20.65 17.22 4,5-二甲基邻苯二胺 40.9 — 1 587.10 ND 5.12 1.57 2.14 4.36 3.86 2.78 ND 1-丙烯基苯 60.5 — 1 928.85 2.94 5.40 5.43 5.16 19.19 16.80 12.26 10.93苯甲酰溴 36.9 — 1 522.58 ND ND ND 5.16 6.06 3.39 17.85 16.38 1-异丙基萘 66.6 — 2 131.25 1.27 0.57 0.48 2.03 8.03 1.44 5.38 6.52 1-(2-丙烯基)-萘 77.3 — 2 271.74 0.52 ND ND ND ND ND ND ND 3,4,5-三甲氧基-α-甲基-苯乙胺 82.7 — 2 391.11 ND 2.33 1.86 1.41 6.66 5.14 3.67 3.15 τ-氯丁酰苯 36.9 — 1 522.58 0.50 1.73 1.78 2.02 8.57 5.29 4.80 3.89其他腺嘌呤 31.6 — 1 438.10 ND ND ND 2.12 6.49 3.64 ND ND倍氯米松 54.9 — 1 775.59 59.82 68.24 72.51 79.36 141.20 157.58 239.38 178.01洋地黄毒苷 64.4 — 2 784.21 265.32 308.49 284.98 317.38 607.04 411.57 587.16 436.67 2’-脱氧-鸟苷 51.0 — 2 637.50 12.63 6.21 16.25 17.88 39.94 30.80 15.51 16.70氢化可的松醋酸盐 71.5 — 2 147.92 55.62 59.05 60.58 62.42 81.06 117.42 54.64 56.24 α-D-吡喃葡萄糖苷 61.0 — 1 675.00 9.37 4.91 29.34 50.18 56.21 35.29 53.62 25.39
2.2 鱼露发酵过程中挥发性风味物质组成
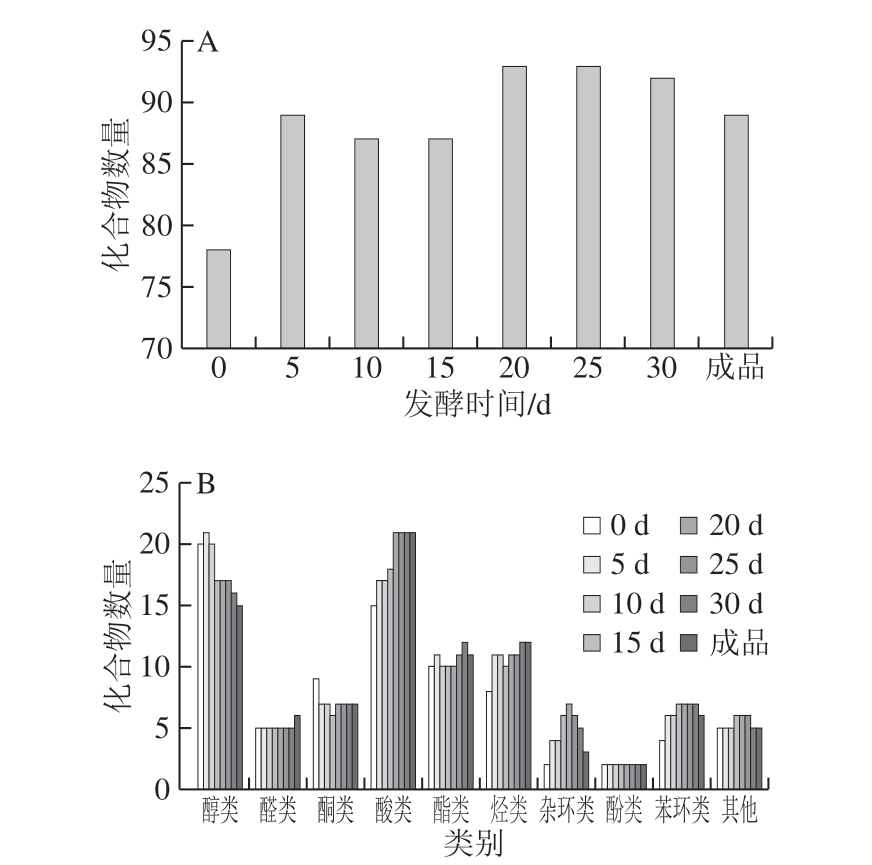
由图1A可知,鱼露发酵过程中风味化合物种类大体呈现上升趋势,后期明显高于前期,说明在鱼露发酵期间,其主要风味物质的形成是在发酵后期产生的。在发酵初期,检测出的风味化合物的种类最少有78 种;从第5~15天时,风味化合物的种类变化有所上升,约有87 种;第20~30天时,化合物的种类变化达到最高有93 种;发酵成品时,其风味化合物的种类又稍有下降,为89 种。在发酵后期,化合物的种类有所下降,可能是因为这个阶段在发酵液中加入酱油酵母进行赋香发酵,在增加风味成分的同时可能抑制某些化合物的反应。
如图1 B 所示,样品中种类最多的分别是醇类(16.30%~24.36%)和酸类(19.1%~23.6%)化合物,其次是酯类(11.83%~14.10%)和烃类(10.26%~13.48%),而酚类(2.15%~2.30%)最少。在发酵前期,酸类化合物种类增加,到后期保持不变;醇类化合物第5天时种类最多,随着发酵时间的延长,种类不断降低;杂环化合物的种类呈现先增加后下降的趋势;在发酵初期,鱼露中没有检测到酚类化合物,第5天时检测到2 种化合物,之后不再发生变化;其余种类化合物在发酵过程中基本保持不变。
2.3 鱼露发酵过程中挥发性化合物的聚类分析热图
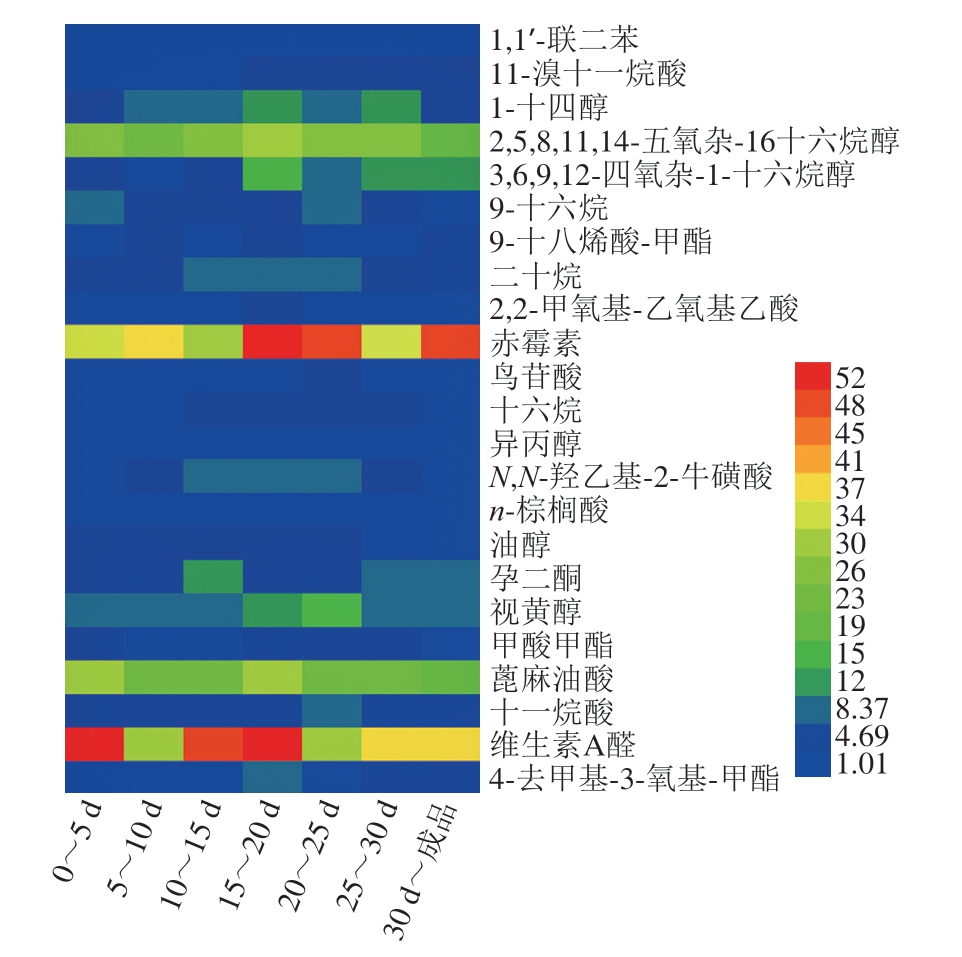
发酵过程为挥发性风味物质的形成提供了丰富的酶和各种前体物质,如碳水化合物、游离氨基酸和脂肪酸等[23]。为了进一步研究在发酵过程中挥发性风味化合物的变化,本研究选取在发酵过程中检测到的含量变化较为突出的23 种化合物,对含量的变化进行聚类分析,结果如图2所示,维生素A醛、赤霉素、蓖麻油酸、2,5,8,11,14-五氧杂-16-十六烷醇这4 种化合物在发酵过程中含量的变化始终比较明显,可能是这4 种化合物对鱼露的风味有着重要的影响。维生素A醛在发酵前期变化最大,到发酵后期变化稍有减慢,但总体增加还是比较大的。赤霉素在发酵的后期含量变化最大,在发酵前期含量不断增加,但增加的速度可能稍慢于后期。蓖麻油酸和2,5,8,11,14-五氧杂-16-十六烷醇在整个发酵过程中的含量不断增加,通过对比发现,在发酵过程中增加的速度变化较小。其他化合物在发酵过程中的含量也在不断增加,但可能增加的速度与这4 种化合物相比较为缓慢。
2.4 不同种类鱼露挥发性化合物的PCA
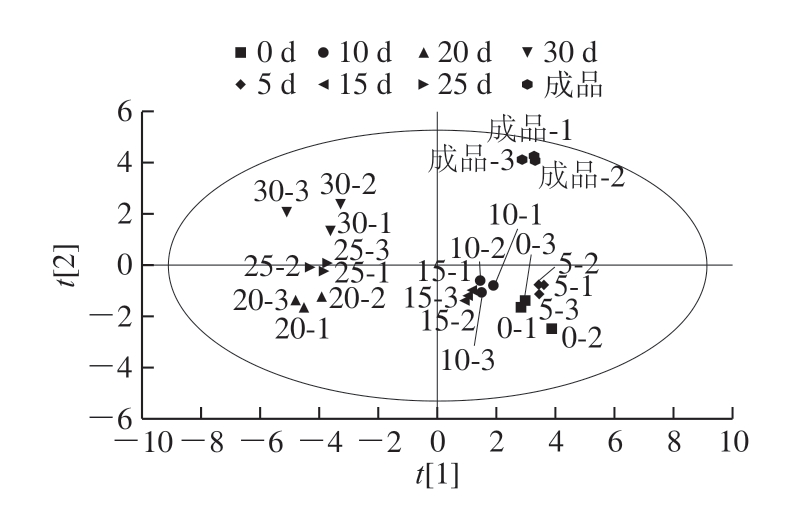
PCA将原始变量重新组合成一组新的独立综合变量,同时根据实际需要提取较少的变量,尽可能地反映原始变量[24]。鱼露挥发性化合物通过HS-SPME-GC×GCMS检测得到的数据,通过SIMCA软件进行PCA,结果如图3所示。在发酵的0~15 d,PCA中样品聚集在一起,说明在发酵的前15 d,样品中的挥发性风味物质成分比较接近。到第20天时,样品与第15天时可以明显地区分开,说明发酵到第20天时鱼露的风味已经发生改变,到后期鱼露样品的挥发性风味化合物都能够区分开,说明鱼露风味化合物在后期发酵过程中不断地发生改变,通过后期不断地发酵才形成了鱼露独特的风味口感。
2.5 鱼露挥发性风味化合物组成分析
通过对鱼露挥发性风味化合物组成的分析发现,鱼露的风味主要是醇类、酸类、酯类和烃类这几种化合物共同作用的结果,其中酯类化合物所占比例最高。
醛可以通过多不饱和脂肪酸在微生物和酶的作用下氧化降解形成[25]。这些挥发性物质中的大多数具有高阈值和令人愉快的气味,例如草味、麦芽味、水果味和奶酪味[26-27],它们可以增强食物的整体风味。在醛类化合物中,维生素A醛的含量最高,在整个反应的过程中,含量呈先增加后下降的趋势,但总体含量增加。苯甲醛是由氨基酸的Strecker反应产生[22],具有令人愉悦的坚果香味、水果香味和杏仁香味,是烤花生中的主要羰基化合物[28],也是水产品中的一种特征风味化合物。壬醛被证实是鱼腥味的主体[29],普遍存在于淡水鱼中。发酵过后,其含量有所降低,说明发酵时间的延长可以降低鱼露的鱼腥味。
醇类化合物主要是由脂肪氧化、氨基酸和碳水化合物的代谢产生[30]。醇类化合物的阈值高,对鱼露整体风味贡献小,但一些不饱和醇的阈值低,对鱼露的整体特征风味有一定贡献。在发酵的前期,醇类化合物种类较多。随着发酵过程的进行,可能一些化合物因为发生反应而被分解,所以发酵后期,醇类化合物的种类和含量都有所下降。
酸类化合物的产生主要是脂肪酸甘油三酯发生氧化或者水解所产生[31]。酸类挥发性物质大多阈值高,因此对主体风味的贡献值不大,在发酵过程中,酸类化合物的总量稍有上升,但变化不显著。
酯类主要来自鱼露发酵过程中酸与醇的酯化反应,乙酯主要与鱼露发酵产生的高浓度乙醇有关,其中乙酸乙酯的含量最高[32-33]。含氮化合物主要来源于美拉德反应,或氨基酸的分解作用。吡嗪和呋喃类化合物虽然含量较少,但因为阈值低,能够产生一定的青草味或豆香味[22]。烷烃类化合物被认为是不具有气味活性的,主要来自于烷氧自由基的裂解,但某些烯烃在一定条件下产生醛和酮类物质,对鱼露的整体风味产生一定的影响[11]。
3 结 论
采用HS-SPME-GC×GC-MS技术,对鱼露发酵过程中挥发性风味物质进行检测,对其发酵过程中变化较明显的化合物进行对比分析,共检测出化合物116 种,分别为醇类、醛类、酮类、酸类、酯类、烃类、杂环、酚类、苯环类。不同时间段检测鱼露挥发性风味化合物差异较明显。在发酵过程中检测到的化合物种类不断增加,到后期稍有下降。鱼露风味化合物含量最多的是酯类化合物。
对检测得到的数据进行PCA,结果发现,在鱼露发酵的前期其气味成分相差不大,当发酵进行到第20天时,挥发性风味化合物成分可以被显著地区分开,说明鱼露的主要风味成分在发酵后期形成。
参考文献:
[1] 吴帅, 杨锡洪, 解万翠, 等. 鱼露的发酵新技术及风味改良研究进展[J].食品与发酵工业, 2014, 40(10): 184-188. DOI:10.13995/j.cnki.11-1802/ts.2014.10.070.
[2] KIM B M, PARK J H, KIM D S, et al. Effects of rice koji inoculated with Aspergillus luchuensis on the biochemical and sensory properties of a sailfin sandfish (Arctoscopus japonicus) fish sauce[J].International Journal of Food Science & Technology, 2016, 51(8):1888-1899. DOI:10.1111/ijfs.13162.
[3] LEE H W, CHOI Y J, HWANG I M, et al. Relationship between chemical characteristics and bacterial community of a Korean saltedfermented anchovy sauce, Myeolchi-Aekjeot[J]. LWT-Food Science and Technology, 2016, 73: 251-258. DOI:10.1016/j.lwt.2016.06.007.
[4] UDOMSIL N, CHEN S, RODTONG S, et al. Quantification of viable bacterial starter cultures of Virgibacillus sp. and Tetragenococcus halophilus in fish sauce fermentation by real-time quantitative PCR[J]. Food Microbiology, 2016, 57(8): 54-62. DOI:10.1016/j.fm.2016.01.004.
[5] YIMDEE T, WANG X C. Comparison of odor and taste of commercial brand fish sauces from east and south east Asian countries[J].International Journal of Food Properties, 2016, 19(4): 873-896.DOI:10.1080/10942912.2015.1045517.
[6] GIRI A, OSAKO K, OHSHIMA T. Identification and characterisation of headspace volatiles of fish miso, a Japanese fish meat based fermented paste, with special emphasis on effect of fish species and meat washing[J]. Food Chemistry, 2010, 120(2): 621-631.DOI:10.1016/j.foodchem.2009.10.036.
[7] KATSUYA F, SACHIYO I, HITOSHI Y, et al. Identification of distinctive volatile compounds in fish sauce[J]. Journal of Agricultural &Food Chemistry, 2002, 50(19): 5412-5416. DOI:10.1021/jf020405y.
[8] PHAM A J, SCHILLING M W, YOON Y, et al. Characterization of fish sauce aroma-impact compounds using GC-MS, SPME-Osme-GCO, and Stevens’ power law exponents[J]. Journal of Food Science,2010, 73(4): C268-C274. DOI:10.1111/j.1750-3841.2008.00709.x.
[9] GIRI A, OSAKO K, OKAMOTO A, et al. Olfactometric characterization of aroma active compounds in fermented fish paste in comparison with fish sauce, fermented soy paste and sauce products[J].Food Research International, 2010, 43(4): 1027-1040. DOI:10.1016/j.foodres.2010.01.012.
[10] SHIMODA M, PERALTA R R, OSAJIMA Y. Headspace gas analysis of fish sauce[J]. Journal of Agricultural and Food Chemistry, 1996,44(11): 3601-3605.
[11] 高先楚, 王锡昌, 顾赛麒, 等. 中华绒螯蟹性腺加热熟制前后挥发性成分和脂肪酸组成分析[J]. 现代食品科技, 2014, 30(9): 265-274.DOI:10.13982/j.mfst.1673-9078.2014.09.044.
[12] OLIVARES-RUBIO H F, VEGA-LÓPEZ A. Fatty acid metabolism in fish species as a biomarker for environmental monitoring[J].Environmental Pollution, 2016, 218: 297-312. DOI:10.1016/j.envpol.2016.07.005.
[13] CORDERO C, BICCHI C, RUBIOLO P. Group-type and fingerprint analysis of roasted food matrices (coffee and hazelnut samples) by comprehensive two-dimensional gas chromatography[J]. Journal of Agricultural & Food Chemistry, 2008, 56(17): 7655-7666.DOI:10.1021/jf801001z.
[14] ROCHAT S, LAUMER J Y, CHAINTREAU A. Analysis of sulfur compounds from the in-oven roast beef aroma by comprehensive twodimensional gas chromatography[J]. Journal of Chromatography A,2007, 1147(1): 85-94. DOI:10.1016/j.chroma.2007.02.039.
[15] ZENG Z D, LI J, HUGEL H M, et al. Interpretation of comprehensive two-dimensional gas chromatography data using advanced chemometrics[J]. Trends in Analytical Chemistry, 2014, 53: 150-166.DOI:10.1016/j.trac.2013.08.009.
[16] 李守权, 况云所, 李俊, 等. HS-SPME-GC×GC-TOFMS分析贵州茶叶的挥发性香气成分[J]. 贵州农业科学, 2017(5): 131-135.DOI:10.3969/j.issn.1001-3601.2017.05.030.
[17] PURCARO G, TRANCHIDA P Q, BARP L, et al. Detailed elucidation of hydrocarbon contamination in food products by using solid-phase extraction and comprehensive gas chromatography with dual detection[J]. Analytica Chimica Acta, 2013, 773: 97-104.DOI:10.1016/j.aca.2013.03.002.
[18] SOARES R D, WELKE J E, NICOLLI K P, et al. Monitoring the evolution of volatile compounds using gas chromatography during the stages of production of Moscatel sparkling wine[J]. Food Chemistry,2015, 183: 291-304. DOI:10.1016/j.foodchem.2015.03.013.
[19] WELKE J E, MANFROI V, ZANUS M, et al. Characterization of the volatile profile of Brazilian Merlot wines through comprehensive two dimensional gas chromatography time-of-flight mass spectrometric detection[J]. Journal of Chromatography A, 2012, 1226(4): 124-139.DOI:10.1016/j.chroma.2012.01.002.
[20] WELKE J E, MANFROI V, ZANUS M, et al. Differentiation of wines according to grape variety using multivariate analysis of comprehensive two-dimensional gas chromatography with time-offlight mass spectrometric detection data[J]. Food Chemistry, 2013,141(4): 3897-3905. DOI:10.1016/j.foodchem.2013.06.100.
[21] 周敏, 吴朝朝, 杜雨芊, 等. 淡水鱼加工副产物低盐风味鱼露速酿工艺的优化[J]. 中国调味品, 2017, 42(10): 11-14; 19. DOI:10.3969/j.issn.1000-9973.2017.10.003.
[22] 王悦齐, 李春生, 李来好, 等. 基于GC-MS联用技术分析传统鱼露发酵过程中挥发性风味成分和脂肪酸组分变化[J]. 水产学报, 2018,42(6): 984-995. DOI:10.11964/jfc.20170710908.
[23] WEI Q, WANG H, ZHIJIA L V, et al. Search for potential molecular indices for the fermentation progress of soy sauce through dynamic changes of volatile compounds[J]. Food Research International, 2013,53(1): 189-194. DOI:10.1016/j.foodres.2013.04.001
[24] 谷风林, 房一明, 胡荣锁, 等. 电子感官在玉兰花茶品质分析中的应用[J]. 中国食品学报, 2012, 12(3): 167-175. DOI:10.3969/j.issn.1009-7848.2012.03.024.
[25] 傅润泽, 沈建, 王锡昌. 底播虾夷扇贝活品流通前后挥发性成分的对比分析[J]. 食品科学, 2015, 36(2): 110-113. DOI:10.7506/spkx1002-6630-201502021.
[26] THIN W, SUPAWAN W, APINYA A, et al. Co-culturing of Pichia guilliermondii enhanced volatile flavor compound formation by Zygosaccharomyces rouxii in the model system of Thai soy sauce fermentation[J]. International Journal of Food Microbiology, 2013,160(3): 282-290. DOI:10.1016/j.ijfoodmicro.2012.10.022.
[27] YING W, JIANG Y T, CAO J X, et al. Study on lipolysis-oxidation and volatile flavour compounds of dry-cured goose with different curing salt content during production[J]. Food Chemistry, 2016, 190:33-40. DOI:10.1016/j.foodchem.2015.05.048.
[28] 李淑荣, 王丽, 张春红, 等. 烘烤花生中关键香味化合物的研究[J].中国农业科学, 2010, 43(15): 3199-3203. DOI:10.3864/j.issn.0578-1752.2010.15.018.
[29] 冯倩倩, 胡飞, 李平凡. SPME-GC-MS分析罗非鱼体中挥发性风味成分[J]. 食品工业科技, 2012, 33(6): 67-70. DOI:10.13386/j.issn1002-0306.2012.06.023.
[30] SIDIRA M, KANDYLIS P, KANELLAKI M, et al. Effect of immobilized Lactobacillus casei on the evolution of flavor compounds in probiotic dry-fermented sausages during ripening[J]. Meat Science,2015, 100: 41-51. DOI:10.1016/j.meatsci.2014.09.011.
[31] FENG Y, CUI C, ZHAO H, et al. Effect of koji fermentation on generation of volatile compounds in soy sauce production[J].International Journal of Food Science & Technology, 2013, 48(3):609-619. DOI:10.1111/ijfs.12006.
[32] SUN S Y, JIANG W G, ZHAO Y P. Profile of volatile compounds in 12 Chinese soy sauces produced by a high-salt-diluted state fermentation[J]. Journal of the Institute of Brewing, 2012, 116(3): 316-328. DOI:10.1002/j.2050-0416.2010.tb00437.x.
[33] 冯云子. 高盐稀态酱油关键香气物质的变化规律及形成机理的研究[D]. 广州: 华南理工大学, 2015: 87-96.