啤酒花(Humulus lupulus.L)又名蛇麻花,是桑科大麻亚科葎草属植物,其球果是重要的啤酒原料,可赋予啤酒抑菌、防腐和增强泡持性等功效,同时为啤酒提供令人愉悦的苦味和香气特征[1]。此外,啤酒花还具有较强的生理活性,国内外对于啤酒花药用价值的研究历史悠久[2],临床证实其具有良好的镇静和促进睡眠的特性[3];德国草药委员会于1984年将啤酒花列为治疗焦虑和睡眠障碍等的有效植物[4]。我国明代《本草纲目》中就记载了啤酒花具有良好的食疗作用,认为其具有防治痨病、化痰止咳等功效。
啤酒花的主要成分包括软/硬树脂、精油、蛋白质、多酚、蜡质、纤维素和氨基酸等;其中软树脂是啤酒花中最主要的苦味组分[5],主要由α-酸和β-酸组成[6]。α-酸是啤酒花中最主要的成分,也是衡量啤酒花品种和品质的重要依据。α-酸根据酰基侧链的不同,主要存在3 种同系物,分别为合葎草酮、正葎草酮和加葎草酮。在麦汁煮沸过程中,α-酸会异构化为水溶性更强的异α-酸,其对啤酒的苦味贡献率约占80%左右。
与α-酸相同,β-酸同样存在3 种主要同系物:合蛇麻酮、正蛇麻酮和加蛇麻酮,结构如图1所示。
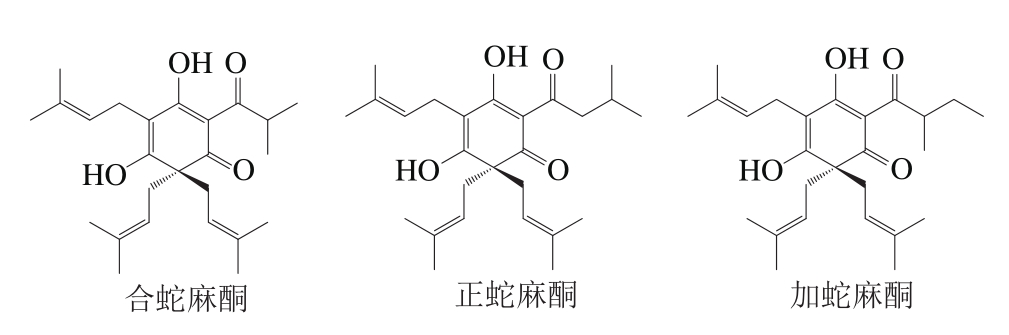
图1 β-酸3 种主要同系物的结构
Fig.1 Chemical structures of β-acid homologues
与α-酸相比,β-酸在分子结构上增加了一个异戊烯基,水溶性较差;同时由于β-酸结构中的芳香环上不存在叔醇基团,不能发生类似α-酸的异构化反应,被认为对啤酒的苦味没有贡献[7-8],因此β-酸往往作为副产物从啤酒花中分离出来。但大量研究结果表明,β-酸具有抑菌、防腐、抗抑郁等生物活性,其中抑菌防腐性能主要是由于β-酸中存在的β-三酮基团具有抑菌作用,可以影响菌类细胞壁的离子通透性[9]。Larson等[10]的研究结果表明,与α-酸及其衍生物相比,β-酸及其衍生物的抑菌活性更强;Simpson等[11]的研究进一步表明β-酸对金黄色葡萄球菌的抑制作用是α-酸的两倍。已有研究结果表明,β-酸具有广谱抑菌性能,其在抑制大肠杆菌、金黄色葡萄球菌、牛链球菌等革兰氏阴/阳性菌方面均体现出良好的性能[12-13]。而抗氧化活性方面的研究也发现,β-酸对过氧化自由基和羟自由基均具有较强的清除能力[14-15];Sbardella等[16]的研究还证实,β-酸对肉类具有较好的保鲜功效,可显著降低肉制品的脂质过氧化。本课题组前期对啤酒花中活性成分的抗氧化活性进行研究也发现,不同品种啤酒花的β-酸提取物在抗氧化活性上存在差异性[17],这可能正是不同品种啤酒花中β-酸3 种同系物的比例存在较大差异导致的。
尽管β-酸的3 种同系物结构类似,但在活性上存在一定的差异[18]。例如,Schulz等[19]的研究结果表明,对标准体质量(60 kg)的人而言,合蛇麻酮、正蛇麻酮和加蛇麻酮作为膳食补充剂的推荐最大日服用剂量分别为9.3、7.3 mg和2.3 mg。相较于α-酸,人们对β-酸的研究较少[20];同时由于大量获取β-酸同系物单体的难度较大,因此无论是从啤酒酿造还是从生理活性利用方面,人们往往将其作为一个整体进行评价,而对于β-酸同系物之间活性差异的相关研究鲜见报道。对于β-酸的制备,目前较为成熟的方法是利用α-酸与β-酸的酸性差异,通过对啤酒花浸膏进行分离来实现,然而该方法只能获得β-酸3 种同系物的混合体;而进一步分离β-酸同系物,现行方法是利用制备型液相色谱来完成[21-22],然而该方法仪器昂贵,且利用该方法无法获取大量的β-酸同系物单体,因此在很大程度上限制了后续研究和实际应用。
本课题组以β-酸为研究对象已进行了一定的研究报道[17,23]。由于不同品种啤酒花所含β-酸同系物的组成差异较大,因此本研究在前期工作的基础上,对β-酸同系物进行了初步分离,得到不同比例β-酸同系物样品,进而采用不同的抗氧化评价方法和抑菌实验,对β-酸同系物的活性进行比较研究,以期为啤酒花品种选育和β-酸的开发应用提供理论参考。
1 材料与方法
1.1 菌株、材料与试剂
金黄色葡萄球菌(26001)和大肠杆菌(44825)由乌鲁木齐市疾病预防控制中心提供。
啤酒花浸膏标准品(ICE-3) 美国酿造化学家协会;啤酒花浸膏 新疆三宝乐农业科技有限公司;1,1-二苯基-2-三硝基苯肼(1,1-diphenyl-2-picrylhydrazyl,DPPH) 美国Sigma-Aldrich公司;芦丁、β-胡萝卜素中国药品生物制品检定所;黄嘌呤氧化酶 上海源叶生物科技有限公司;别嘌呤醇 北京恒业中远化工有限公司;抗坏血酸 天津市博迪化工有限公司;甲醇为国产色谱纯,其他试剂均为国产分析纯。
LB固体培养基自行配制(10 g/L蛋白胨、10 g/L琼脂粉、5 g/L酵母浸粉、10 g/L的NaCl),于120 ℃高压灭菌20 min,供抑菌实验使用。
1.2 仪器与设备
高效液相色谱仪、色谱柱为Hypersil ODS2(150 mm×4.6 mm,4.5 μm) 大连依利特分析仪器有限公司;UV-5300PC紫外-可见分光光度计 上海元析仪器有限公司;WGZ-XT浊度仪 杭州奇威仪器有限公司。
1.3 方法
1.3.1 高效液相色谱分析条件
流动相为V(甲醇)∶V(水)∶V(体积分数85%磷酸)=85∶15∶0.25;流速0.8 mL/min;柱温室温;紫外检测器波长314 nm;进样量10 μL,采用啤酒花浸膏国际标准对照物,通过峰面积外标法定量分析。
1.3.2 β-酸样品分离提取及初步纯化
β-酸的分离提取方法参考本课题组前期研究[24]。称取20 g啤酒花浸膏,加入10 mL无水乙醇,在50 ℃水浴中搅拌至溶液澄清透明;边搅拌边向其中滴加质量分数10%的KOH溶液,调节pH值至13~14;再加约200 mL蒸馏水,充分搅拌后再次以10% KOH溶液调节体系的pH值至13~14。将溶液静置30 min,真空抽滤除去油状物,得到澄清液体。上述过滤液在N2保护下搅拌,缓慢通入CO2,当pH值达到8.2~8.5时停止通气,继续搅拌约1 h,静置30 min,真空抽滤得白色粉末状固体即为β-酸粗提物,质量分数高于80%,于-18 ℃下保存备用。
1.3.3 不同比例β-酸同系物样品的分离
称取约5 g的β-酸粗提物,预实验在考察溶剂、结晶温度、pH值对β-酸重结晶产物中3 种同系物比例影响的基础上,对β-酸粗提物进行了进一步的分离。获得不同比例β-酸同系物样品条件简述如下:1)合蛇麻酮与正蛇麻酮+加蛇麻酮的质量比为1∶1。向β-酸粗提物样品中逐滴滴加体积分数90%甲醇溶液,体系保持在50 ℃至完全溶解,在室温下(25 ℃)重结晶,重复上述过程3 次得产物1,记为S1∶1。2)合蛇麻酮与正蛇麻酮+加蛇麻酮质量比为10∶1。向产物1中逐滴滴加体积分数90%甲醇溶液,体系保持在50 ℃至完全溶解,在4 ℃下重结晶,重复上述过程3 次得产物2,记为S10∶1。3)合蛇麻酮与正蛇麻酮+加蛇麻酮质量比为5∶1。由产物1与产物2按质量比5∶22混合得产物3,记为S5∶1。4)合蛇麻酮与正蛇麻酮+加蛇麻酮质量比为1∶4。在室温下逐滴向产物1中滴加体积分数90%甲醇溶液,至样品完全溶解,向该溶液中缓慢通入CO2(1 mL/min),至溶液pH值约为6~7左右,停止通气,过滤得产物4,记为S1∶4。5)合蛇麻酮与正蛇麻酮+加蛇麻酮质量比为20∶1。逐滴向β-酸粗提物中滴加正己烷,体系保持在50 ℃至β-酸完全溶解,在4 ℃下重结晶,重复上述过程3 次得产物5,记为S20∶1。
1.3.4 抗氧化活性评价
1.3.4.1 抑制黄嘌呤氧化酶活性的测定
参考文献[25]的方法。精确移取3.75 mL磷酸盐缓冲溶液(50 mmol/L的KH2PO4/K2HPO4,pH 7.5),一式四份。一份加入2 mL蒸馏水记作0组;一份加入1 mL的18 mU/mL黄嘌呤氧化酶和1 mL蒸馏水,记作E组;一份加入1 mL的β-酸系列样品溶液和1 mL蒸馏水,记作S组;最后一份加入1 mL的β-酸系列样品溶液和1 mL的18 mU/mL黄嘌呤氧化酶,记作E+S组。将4 组体系均置于37 ℃水浴中恒温保持15 min,水浴结束加入3 mL黄嘌呤启动反应,混匀后立即在290 nm波长处测定其吸光度,记作0时刻,4 组体系的吸光度分别记为A0、AE0、AS0、A(E+S)0。然后将4 组体系放入25 ℃水浴,以100 r/min振荡反应30 min,反应结束后加入1 mL 1 mol/L盐酸终止反应,再次测定吸光度,记作30时刻,4 组体系的吸光度分别记为A30、AE30、AS30、A(E+S)30。根据公式(1)计算不同质量浓度的β-酸系列样品对黄嘌呤氧化酶活性的抑制率。
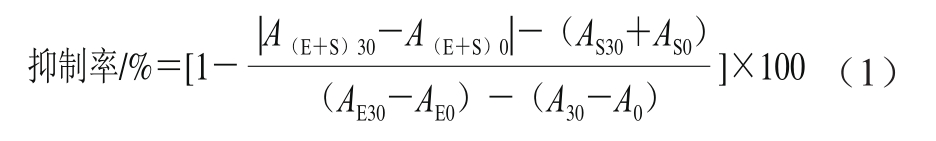
1.3.4.2 DPPH自由基清除能力测定
参考文献[26]的方法,以芦丁作为对照,分别考察不同质量浓度β-酸系列样品的DPPH自由基清除率,按公式(2)进行计算。
式中:As为加入样品时的吸光度;Ab为未加样品时的吸光度。
1.3.4.3 ·OH清除能力测定
β-酸系列样品的·OH清除能力采用邻二氮菲/Fe2+氧化法进行评价[27],以芦丁作为对照,以1 mL 体积分数0.01%的H2O2和1 mL蒸馏水代替2 mL β-酸样品测得未损伤管吸光度,以2 mL蒸馏水代替2 mL β-酸样品测得损伤管的吸光度。根据公式(3)计算不同质量浓度β-酸系列样品·OH清除率。
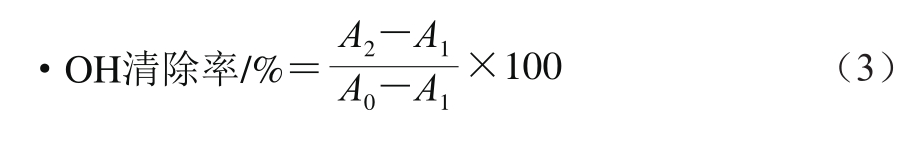
式中:A2是加入样品时溶液的吸光度;A1是以蒸馏水代替β-酸样品时溶液的吸光度;A0是以蒸馏水代替β-酸样品和体积分数0.01% H2O2时溶液的吸光度。
1.3.4.4 总抗氧化能力评价
β-酸系列样品的总抗氧化能力采用β-胡萝卜素-亚油酸乳化液法进行评价[17],以芦丁作为对照,根据公式(4)计算不同样品的抗氧化指数(antioxidant activity index,AAI),评价样品的总抗氧化能力。
式中:ASt和ACt分别表示120 min时样品和蒸馏水(空白)的吸光度;AS0和AC0分别表示起始时样品与空白的吸光度。
1.3.5 抑菌活性评价
1.3.5.1 菌悬液的配制
金黄色葡萄球菌和大肠杆菌悬浊液的配制参考前期工作[28],配制浓度为108~109 CFU/mL的菌悬液,备用。
1.3.5.2 最小抑菌浓度的测定
采用滤纸片法[29]和二倍稀释法[30],确定β-酸系列样品的最小抑菌浓度。利用二倍稀释法分别配制质量浓度为2.00、5.00、10.00、20.00、40.00、80.00 mg/L和160.00 mg/L不同比例β-酸同系物样品的甲醇溶液。将5.00 μL的样品溶液滴于直径为6 mm的圆形滤纸片上,待溶剂挥发后间隔一定距离贴在LB培养基上。阳性对照为160.00 mg/L(与样品最大质量浓度相同)的阿莫西林水溶液,以及75%乙醇溶液;阴性对照为甲醇和无菌水。将上述LB培养基置于培养箱中,在37 ℃下培养24 h后,以十字交叉法测量各样品对两个菌种的抑菌圈直径,抑菌圈直径大于6.5 mm时认为样品对菌种有抑制作用。
1.4 数据处理与统计
所有实验数据均采用Origin 8.5或Excel软件处理,通过方差分析和邓肯氏多重差异分析法分析显著性,实验数据均以平均值±标准偏差表示。抗氧化活性的研究中,比较相邻样品之间的半数清除率(half maximal inhibitory concentration,IC50),当P<0.01时,即存在极显著性差异,记为“<<或>>”;0.05<P<0.01时,即存在显著性差异,记为“<或>”;P>0.05时,即不存在显著性差异,记为“≈”。
2 结果与分析
2.1 不同比例β-酸同系物样品的分离
由于啤酒花中加蛇麻酮在β-酸中的相对含量较为恒定,同时正蛇麻酮与加蛇麻酮的分离难度较大,因此通常将正蛇麻酮和加蛇麻酮看作一个整体进行研究[31-32]。图2为啤酒花浸膏标准品、实验用啤酒花浸膏、β-酸粗提物,以及样品S1∶4、S1∶1、S5∶1、S10∶1和S20∶1的液相色谱图;其中,啤酒花浸膏标准品、实验用啤酒花浸膏以及β-酸粗提物各组分的相对含量见表1。研究结果表明,在β-酸同系物样品分离过程中,以体积分数90%甲醇溶液作为溶剂进行提取分离时,当结晶温度由25 ℃降至4 ℃,β-酸粗提物重结晶后S1∶1比S10∶1中合蛇麻酮的相对含量明显升高,证实合蛇麻酮的溶解度小于正蛇麻酮+加蛇麻酮;当以正己烷作为溶剂进行提取分离时,β-酸粗提物重结晶后合蛇麻酮(S20∶1)的相对含量较体积分数90%甲醇提取分离样品(S10∶1)相对含量明显升高,由于正己烷对含有β-酸的软树脂具有更好的溶解度,因此该结果进一步证实合蛇麻酮的溶解度小于正蛇麻酮+加蛇麻酮;而当在合蛇麻酮与正蛇麻酮+加蛇麻酮质量比为1∶1的体积分数90%甲醇溶液中通入CO2至pH值约为6~7左右时,沉淀物中正蛇麻酮+加蛇麻酮的相对含量明显提高,结果表明该组分的酸性强于合蛇麻酮。
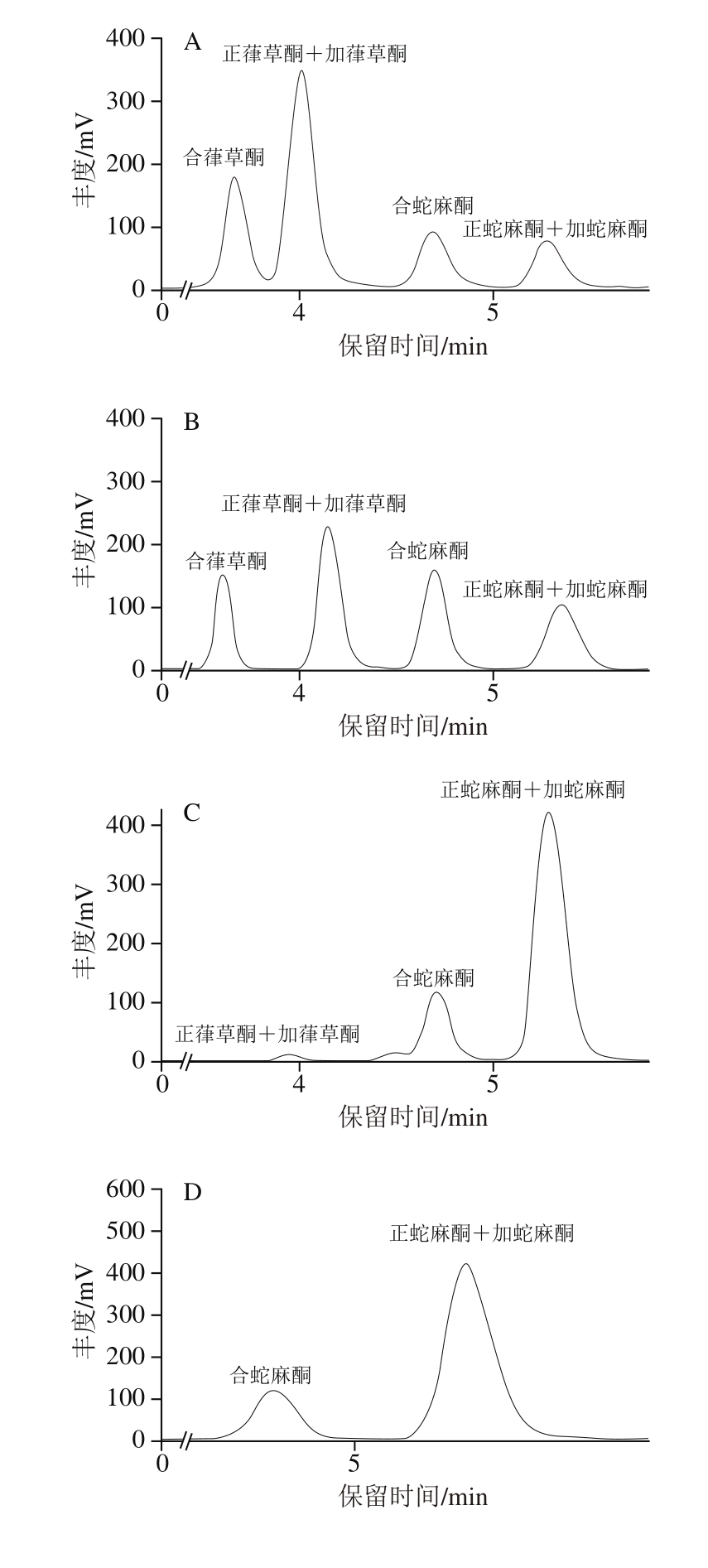
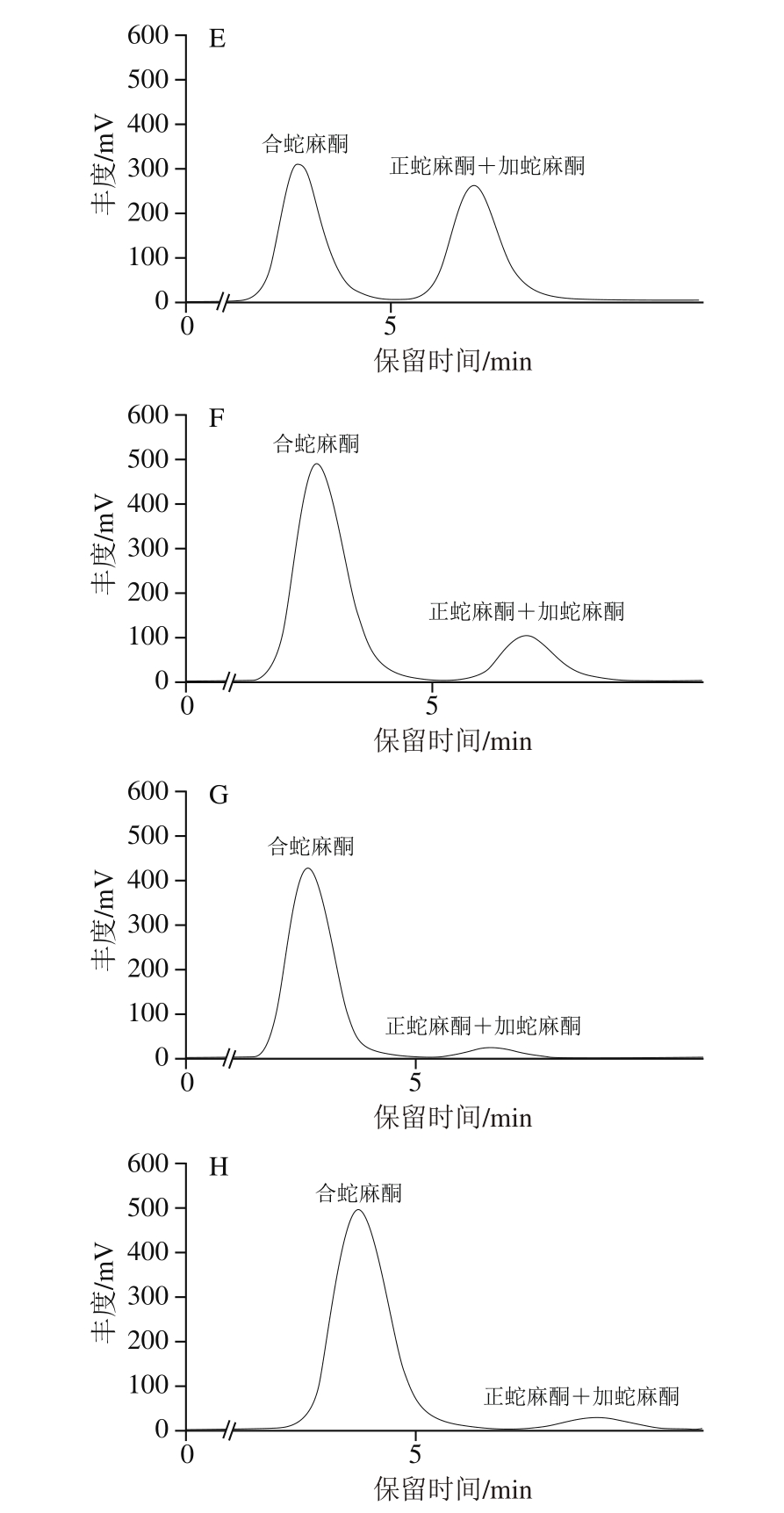
图2 样品的高效液相色谱图
Fig.2 High performance liquid chromatograms of β-acid samples
A.啤酒花浸膏标准品;B.实验用啤酒花浸膏;C.β-酸粗提物;D.S1∶4;E.S1∶1;F.S5∶1;G.S10∶1;H.S20∶1。
表1 酒花浸膏标准品、实验用啤酒花浸膏和β-酸粗提物中各组分的相对含量
Table 1 β-Acid composition of hops extract standard, hops extract used for this experiment and crude β-acid extract%
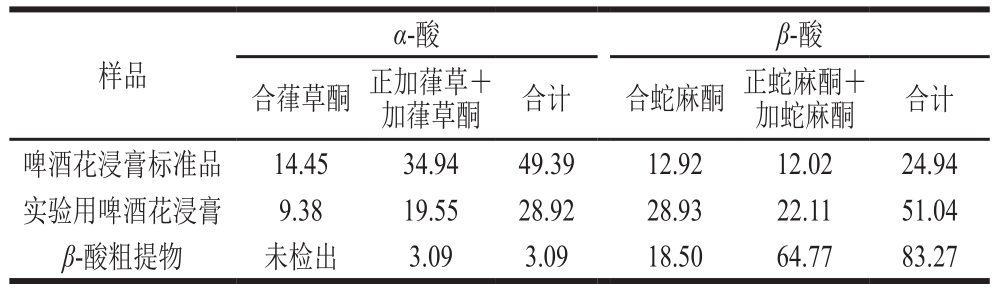
样品α-酸 β-酸合葎草酮 正加葎草+加葎草酮合计合蛇麻酮正蛇麻酮+加蛇麻酮合计啤酒花浸膏标准品 14.45 34.94 49.39 12.92 12.02 24.94实验用啤酒花浸膏 9.38 19.55 28.92 28.93 22.11 51.04 β-酸粗提物 未检出 3.09 3.09 18.50 64.77 83.27
2.2 抗氧化活性评价
2.2.1 不同比例β-酸同系物对黄嘌呤氧化酶活性的抑制作用
黄嘌呤氧化酶是人体内核酸分解代谢中的重要组分,能催化(次)黄嘌呤产生尿酸[33],同时代谢产物会引起氧化应激[34],两者都是导致痛风的重要因素[35]。目前临床治疗痛风的药物主要有别嘌呤醇[36]、秋水仙素[37]、半胱氨酸[38]等。但这些药物具有较强的毒副作用,因此寻找高效低毒的新型抑制剂备受关注[39]。由图3可知,β-酸对黄嘌呤氧化酶的活性具有一定的抑制作用,随着质量浓度的增加,所有样品对黄嘌呤氧化酶活性抑制率呈明显上升趋势,且β-酸同系物的比例显著明显影响样品对黄嘌呤氧化酶活性的抑制能力。由图3可知,几种β-酸同系物样品抑制黄嘌呤氧化酶的IC50依次为S1∶4(0.50 mg/mL)<S1∶1(0.53 mg/mL)<S5∶1(0.65 mg/mL)≈S20∶1(0.63 mg/mL)<S10∶1(0.94 mg/mL),即随着正蛇麻酮+加蛇麻酮比例的下降抑制能力总体逐渐减小,表明正蛇麻酮+加蛇麻酮对黄嘌呤氧化酶活性的抑制能力高于合蛇麻酮。尽管S1∶4样品对黄嘌呤氧化酶活性抑制能力明显高于其他样品,但与阳性对照品别嘌呤醇相比活性明显较差。Mir等[40]以十六烷基三甲基溴化铵为例,研究同系物对黄嘌呤氧化酶活性的抑制作用,结果表明,同系物的分子链长短、分子质量会显著影响其与黄嘌呤氧化酶的结合,进而影响其抑制活性;柳高[41]对B族维生素对小鼠尿酸水平影响的研究结果也证明B族维生素同系物之间在抑制黄嘌呤氧化酶上存在显著性差异,上述研究均与本研究结果相似。
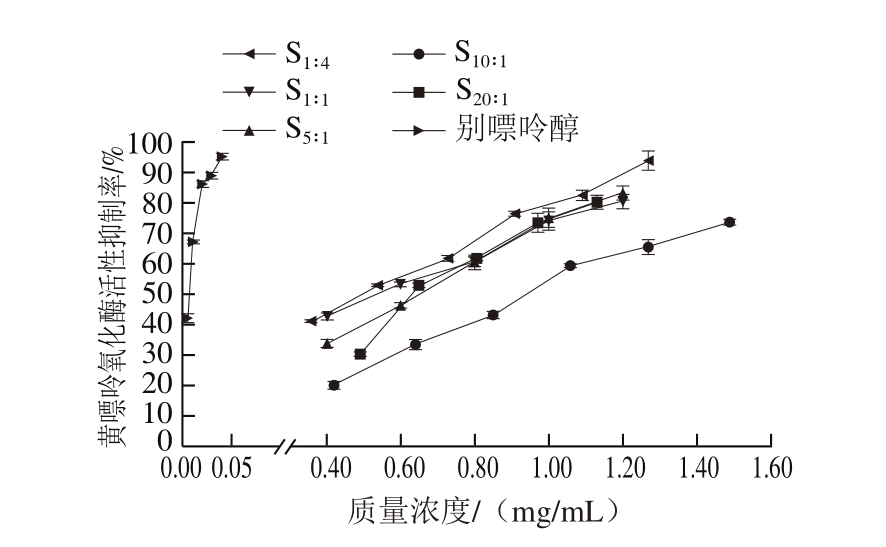
图3 不同比例β-酸同系物样品对黄嘌呤氧化酶活性的抑制率
Fig.3 Inhibitory effect of β-acid homologue mixtures with different ratios on xanthine oxidase activity
2.2.2 不同比例β-酸同系物对DPPH自由基清除能力的影响
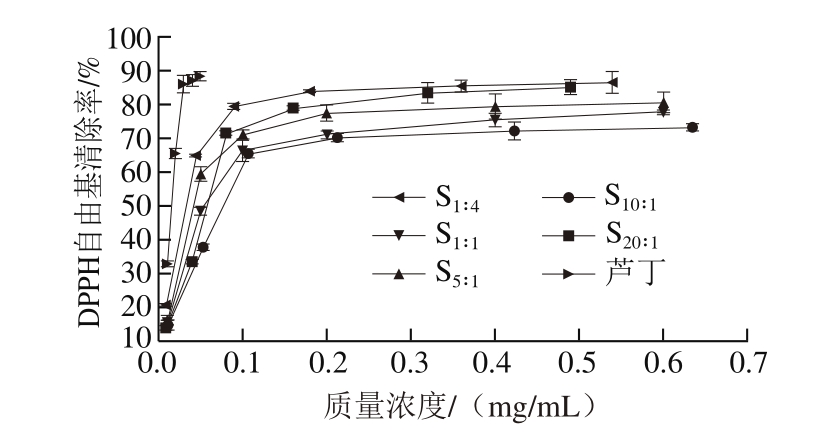
图4 不同比例β-酸同系物样品对DPPH自由基的清除率
Fig.4 DPPH radical scavenging rates of β-acid samples with different ratios of homologues
由图4可知,β-酸对DPPH自由基具有一定的清除能力,随着质量浓度的增加,所有样品对DPPH自由基的清除率均呈上升趋势,且β-酸同系物的比例明显影响样品对DPPH自由基的清除能力。β-酸同系物样品清除DPPH自由基的IC50依次为S1∶4(0.033 mg/mL)<S5∶1(0.042 mg/mL)<S1∶1(0.054 mg/mL)≈S20∶1(0.057 mg/mL)<S10∶1(0.077 mg/mL),清除能力均低于阳性对照品芦丁(0.015 mg/mL)。与抑制黄嘌呤氧化酶活性类似,正蛇麻酮+加蛇麻酮比例较高的样品S1∶4清除DPPH自由基的能力较强。Ma Yongkai等[42]在研究抗氧化肽同系物的抗氧化活性过程中发现,抗氧化肽清除DPPH自由基的能力不仅与氨基酸的组成和关键氨基酸位点有关,而且还与抗氧化肽的空间构型以及同系物分子质量有关,表明同系物之间在清除DPPH自由基能力上存在差异,这与本研究结果类似。
2.2.3 不同比例β-酸同系物对·OH清除能力的影响
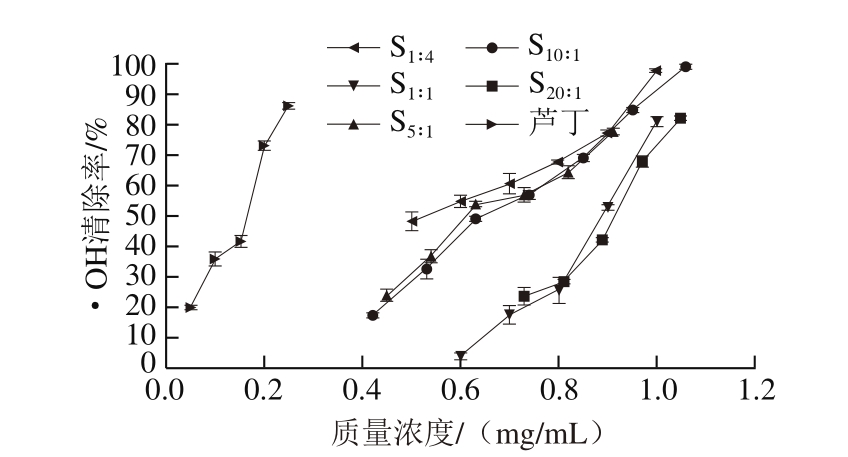
图5 不同比例β-酸同系物样品对·OH的清除率
Fig.5 OH radical scavenging rates of β-acid samples with different ratios of homologues
由图5可知,β-酸也具有较好的·OH清除能力。随着质量浓度的增加,所有样品对·OH的清除率均呈上升趋势,且β-酸同系物的比例与·OH的清除能力也呈现一定相关性。5 种不同比例β-酸同系物样品清除·OH的IC50依次为S1∶4(0.52 mg/mL)<S5∶1(0.61 mg/mL)≈S10∶1(0.64 mg/mL)<S1∶1(0.89 mg/mL)≈S20∶1(0.91 mg/mL),但清除能力均明显小于阳性对照样品芦丁。与前述结果类似,正蛇麻酮+加蛇麻酮比例较高的样品S1∶4样品清除活性也是最强的,表明正蛇麻酮+加蛇麻酮对·OH的清除能力强于合蛇麻酮。Yeung等[43]在对甲酚类化合物抗氧化性能的研究过程中发现,甲酚类同系物之间在清除·OH和超氧化物等的能力上也存在明显差别,与本研究结果类似。
2.2.4 不同比例β-酸同系物的总抗氧化活性
由图6可知,β-酸在胡萝卜素-亚油酸乳化体系中具有较好的总抗氧化能力,随着质量浓度的增加,所有样品的AAI均呈上升趋势,且β-酸同系物的比例对样品的总抗氧化能力具有明显影响。5 种样品的总抗氧化活性达到50%时对应的样品质量浓度依次为S1∶4(0.43 mg/mL)<S20∶1(1.24 mg/mL)≈S5∶1(1.32 mg/mL)<S1∶1(1.74 mg/mL)<S10∶1(1.90 mg/mL),与阳性对照芦丁(0.623 mg/mL)相比,S1∶4样品的总抗氧化能力更高,且S1∶4样品抗氧化活性要明显好于其他比例的样品。该结果与前述各抗氧化评价体系中得出的正蛇麻酮+加蛇麻酮的抗氧化能力强于合蛇麻酮的结果一致。
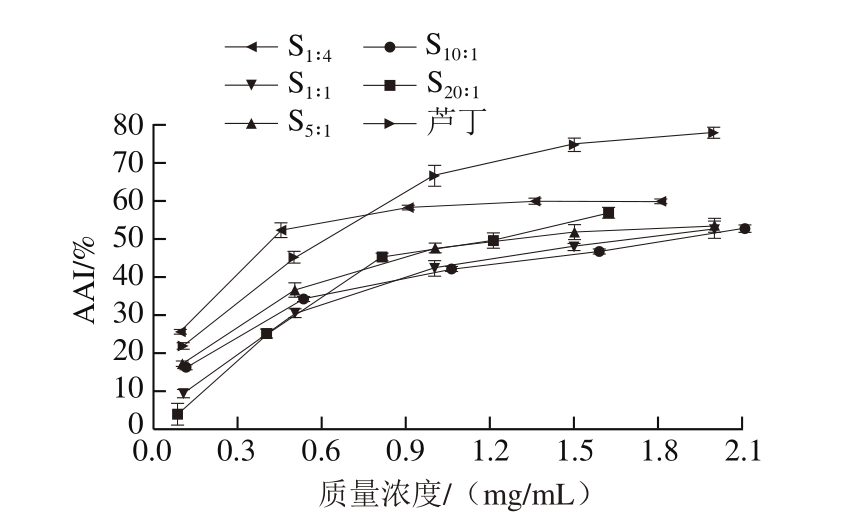
图6 不同比例β-酸同系物样品的总抗氧化活性
Fig.6 Total antioxidant activity of β-acid samples with different ratios of homologues
2.3 不同比例β-酸同系物的抑菌活性
由表2可以看出,不同比例β-酸同系物样品对所测试的2 种菌株均具有良好的抑菌活性,而空白溶液(甲醇、无菌水)对两种菌株均无抑菌作用,阳性对照160.00 mg/L的阿莫西林溶液对金黄色葡萄球菌和大肠杆菌的抑菌圈直径分别为(16.9±0.4)mm和(15.7±0.3)mm。
表2 不同比例β-酸同系物样品的抑菌圈直径
Table 2 Diameter of bacteriostatic zone of β-acid samples with different ratios of homologues
mm
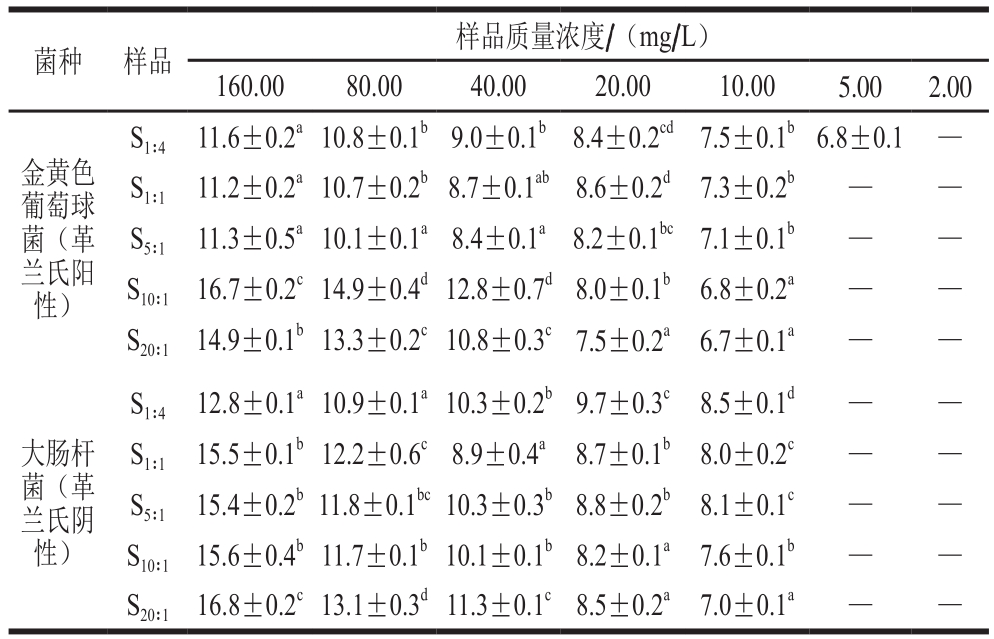
注:同种菌同列肩标小写字母不同表示样品间差异显著(P<0.05)。
菌种 样品 样品质量浓度/(mg/L)160.00 80.00 40.00 20.00 10.00 5.00 2.00金黄色葡萄球菌(革兰氏阳性)S1∶4 11.6±0.2a10.8±0.1b9.0±0.1b 8.4±0.2cd 7.5±0.1b6.8±0.1 —S1∶1 11.2±0.2a10.7±0.2b8.7±0.1ab 8.6±0.2d 7.3±0.2b — —S5∶1 11.3±0.5a10.1±0.1a8.4±0.1a 8.2±0.1bc 7.1±0.1b — —S10∶1 16.7±0.2c14.9±0.4d12.8±0.7d8.0±0.1b 6.8±0.2a — —S20∶1 14.9±0.1b13.3±0.2c10.8±0.3c7.5±0.2a 6.7±0.1a — —大肠杆菌(革兰氏阴性)S1∶4 12.8±0.1a10.9±0.1a10.3±0.2b9.7±0.3c 8.5±0.1d — —S1∶1 15.5±0.1b12.2±0.6c8.9±0.4a 8.7±0.1b 8.0±0.2c — —S5∶1 15.4±0.2b11.8±0.1bc10.3±0.3b8.8±0.2b 8.1±0.1c — —S10∶1 15.6±0.4b11.7±0.1b10.1±0.1b8.2±0.1a 7.6±0.1b — —S20∶1 16.8±0.2c13.1±0.3d11.3±0.1c8.5±0.2a 7.0±0.1a — —
由表2可知,S1∶4对金黄色葡萄球菌的最小抑菌浓度为5.00 mg/L,其余样品的最小抑菌浓度均为10.00 mg/L。但随着样品的质量浓度增大,合蛇麻酮比例较高的样品S10∶1和S20∶1的抑菌活性增加明显,且在160.00 mg/L下,S10∶1的抑菌圈直径与同质量浓度的阳性对照阿莫西林对金黄色葡萄球菌的抑制能力无显著差异(P>0.05)。对于大肠杆菌而言,所有样品的最小抑菌浓度均为10.00 mg/L;当样品质量浓度为160.00 mg/L时,除S1∶4样品外,其他几种样品对大肠杆菌的抑菌圈直径均与同质量浓度的阳性对照阿莫西林相当,甚至更好,同样说明合蛇麻酮比例的提高对抑制大肠杆菌生长更为有利。Bocquet等[32]研究了合葎草酮与正葎草酮+加葎草酮和合蛇麻酮与正蛇麻酮+加蛇麻酮对小麦叶枯病菌(Zymoseptoria tritic)的抑制效果,结果表明合葎草酮和合蛇麻酮的IC50均小于对应的正葎草酮+加葎草酮/蛇麻酮组分,因此推测合葎草酮/蛇麻酮的抗真菌活性较强;但该实验中合蛇麻酮的半数抑菌浓度为660 mg/L,质量浓度远高于本研究,证明β-酸系列组分对细菌的抑制活性远高于真菌。此外,也有研究发现,青霉素在质量浓度为10 g/L时,对金黄色葡萄球菌和大肠杆菌的抑菌圈直径分别为24.0 mm和34.7 mm[44],但其质量浓度约高于本实验100 倍。因此,作为一种有效的抑菌剂,β-酸具有很好的应用前景。
3 结 论
本研究对啤酒花软树脂中不同比例β-酸同系物样品的体外抗氧化活性和抑菌活性进行了初步评价。结果表明,β-酸具有良好的体外抗氧化活性,且其同系物比例的差异在抗氧化活性上存在较大差异;IC50结果表明,高比例正蛇麻酮+加蛇麻酮样品S1∶4在4 种体外抗氧化评价体系中均显示出最高的活性,证实正蛇麻酮+加蛇麻酮的抗氧化活性强于合蛇麻酮。同样,不同比例β-酸同系物样品的抑菌活性也存在差异。与抗氧化活性不同,在较高质量浓度下(≥40.00 mg/L),高比例合蛇麻酮的β-酸样品对金黄色葡萄球菌和大肠杆菌的抑菌活性均较强,与同质量浓度下的阳性对照阿莫西林的抑菌效果相当甚至更高。但高比例正蛇麻酮+加蛇麻酮的β-酸样品S1∶4对金黄色葡萄球菌的最小抑菌浓度最低(5.00 mg/L);尽管S1∶4对大肠杆菌的最小抑菌浓度与其余样品均为10.00 mg/L,但其抑菌圈直径更大。本研究结果可为啤酒花的品种选育和β-酸的开发应用提供理论参考。但为深入阐明β-酸同系物之间活性差异的本质,仍需对上述同系物在分离纯化、结构表征以及构效关系研究等方面开展更加深入细致的工作。
[1]TANIGUCHI Y, MATSUKURA Y, OZAKI H, et al.Identification and quantification of the oxidation products derived from α-acids and β-acids during storage of hops (Humulus lupulus L.)[J].Journal of Agricultural and Food Chemistry, 2013, 61(12): 3121-3130.DOI:10.1021/jf3047187.
[2]欧阳军.啤酒花的化学药理研究与临床应用[J].中国民族医药杂志,1999(增刊1): 92.DOI:10.16041/j.cnki.cn15-1175.1999.s1.092.
[3]KOETTER U, SCHRADER E, KÄUFELER R, et al.A randomized,double blind, placebo-controlled, prospective clinical study to demonstrate clinical efficacy of a fixed valerian hops extract combination (Ze 91019) in patients suffering from non-organic sleep disorder[J].Phytotherapy Research, 2007, 21(9): 847-851.DOI:10.1002/ptr.2167.
[4]NATHAN M, SCHOLTEN R.The complete German Commission Emonographs: therapeutic guide to herbal medicines[J].Annals of Internal Medicine, 1999, 130(5): 459-460.DOI:10.7326/0003-4819-130-5-199903020-00024.
[5]STEENACKERS B, DE COOMAN L, DE VOS D.Chemical transformations of characteristic hop secondary metabolites in relation to beer properties and the brewing process: a review[J].Food Chemistry, 2015, 172: 742-756.DOI:10.1016/j.foodchem.2014.09.139.
[6]刘泽畅, 刘玉梅.啤酒苦味与啤酒花苦味物质[J].中国酿造, 2019,38(1): 13-19.DOI:10.11882/j.issn.0254-5071.2019.01.004.
[7]HASELEU G, INTELMANN D, HOFMANN T.Structure determination and sensory evaluation of novel bitter compounds formed from β-acids of hop (Humulus lupulus L.) upon wort boiling[J].Food Chemistry, 2009, 116(1): 71-81.DOI:10.1016/j.foodchem.2009.02.008.
[8]HASELEU G, INTELMANN D, HOFMANN T.Identification and RPHPLC-ESI-MS/MS quantitation of bitter-tasting β-acid transformation products in beer[J].Journal of Agricultural and Food Chemistry, 2009,57(16): 7480-7489.DOI:10.1021/jf901759y.
[9]SHIMWELL J L.On the relation between the staining properties of bacteria and their reaction towards hop antiseptic[J].Journal of the Institute of Brewing, 1937, 43(2): 111-118.DOI:10.1002/j.2050-0416.1937.tb05727.x.
[10]LARSON A E, ROSA R Y, LEE O A, et al.Antimicrobial activity of hop extracts against Listeria monocytogenes in media and in food[J].International Journal of Food Microbiology, 1996, 33(2/3): 195-207.DOI:10.1016/0168-1605(96)01155-5.
[11]SIMPSON W J, SMITH A R W.Factors affecting antibacterial activity of hop compounds and their derivatives[J].Journal of Applied Bacteriology, 1992, 72(4): 327-334.DOI:10.1111/j.1365-2672.1992.tb01843.x.
[12]VAN CLEEMPUT M, CATTOOR K, DE BOSSCHER K, et al.Hop (Humulus lupulus)-derived bitter acids as multipotent bioactive compounds[J].Journal of Natural Products, 2009, 72(6): 1220-1230.
[13]HARLOW B E, LAWRENCE L M, KAGAN I A, et al.Inhibition of fructan-fermenting equine faecal bacteria and Streptococcus bovis by hops (Humulus lupulus L.) β-acid[J].Journal of Applied Microbiology,2014, 117(2): 329-339.DOI:10.1111/jam.12532.
[14]VAN HOYWEGHEN L, BIENDL M, HEYERICK A.Radical scavenging capacity of hop-derived products[J].Brewing Science,2010, 63(1/2): 1-5.
[15]YAMAGUCHI N, SATOH-YAMAGUCHI K, ONO M.In vitro evaluation of antibacterial, anticollagenase, and antioxidant activities of hop components (Humulus lupulus) addressing acne vulgaris[J].Phytomedicine, 2009, 16(4): 369-376.DOI:10.1016/j.phymed.2008.12.021.
[16]SBARDELLA M, RACANICCI A M C, GOIS F D, et al.Effects of dietary hop (Humulus lupulus L.) β-acids on quality attributes,composition and oxidative stability of pork meat[J].Journal of the Science of Food and Agriculture, 2018, 98(6): 2385-2392.DOI:10.1002/jsfa.8730.
[17]李玉晶, 刘玉梅.啤酒花活性成分与抗氧化活性的相关性[J].食品科学, 2019, 40(5): 24-30.DOI:10.7506/spkx1002-6630-20171118-232.
[18]SOHRABVANDI S, MOUSAVI S M, RAZAVI S H, et al.Application of advanced instrumental techniques for analysis of physical and physicochemical properties of beer: a review[J].International Journal of Food Properties, 2010, 13(4): 744-759.DOI:10.1080/10942910902818145.
[19]SCHULZ C, CHIHEB C, PISCHETSRIEDER M.Quantification of co-, n-, and ad-lupulone in hop-based dietary supplements and phytopharmaceuticals and modulation of their contents by the extraction method[J].Journal of Pharmaceutical and Biomedical Analysis, 2019, 168: 124-132.DOI:10.1016/j.jpba.2019.02.022.
[20]ALMAGUER C, SCHÖNBERGER C, GASTL M, et al.Humulus lupulus: a story that begs to be told.A review[J].Journal of the Institute of Brewing, 2014, 120(4): 289-314.DOI:10.1002/jib.160.
[21]SELIGER J, CICEK S, WITT L, et al.Selective inhibition of human AKR1B10 by n-humulone, adhumulone and cohumulone isolated from Humulus lupulus extract[J].Molecules, 2018, 23(11): 3041.DOI:10.3390/molecules23113041.
[22]HASELEU G, LAGEMANN A, STEPHAN A, et al.Quantitative sensomics profiling of hop-derived bitter compounds throughout a fullscale beer manufacturing process[J].Journal of Agricultural and Food Chemistry, 2010, 58(13): 7930-7939.DOI:10.1021/jf101326v.
[23]陈婷, 赵九阳, 刘玉梅.明胶-壳聚糖抗菌膜中啤酒花提取物的释放研究[J].食品科学, 2020, 41(3): 151-158.DOI:10.7506/spkx1002-6630-20190213-057.
[24]刘玉梅.啤酒花的分析评价及六氢蛇麻酮类的合成与应用[D].无锡: 江南大学, 2007: 87-88.
[25]刘芬, 詹文红.白芍总苷体外抗氧化活性研究[J].现代药物与临床,2015, 30(2): 132-135.DOI:10.7501/j.issn.1674-5515.2015.02.004.
[26]陈林林, 李伟, 韩可, 等.柠檬叶精油的抗氧化活性及其相关性分析[J].中国调味品, 2019, 44(3): 46-50.DOI:10.3969/j.issn.1000-9973.2019.03.010.
[27]凌关庭.抗氧化食品与健康[M].北京: 化学工业出版社, 2004: 333-334.
[28]赵九阳, 赵冠宇, 刘玉梅.六氢β-酸/甲基-β-环糊精包合物的抑菌活性[J].精细化工, 2019, 36(4): 696-702.DOI:10.13550/j.jxhg.20180495.
[29]张佳, 王莹, 张峰, 等.滤纸片法测定黄花蒿提取物对霉菌的抑制活性[J].湖北农业科学, 2009, 48(5): 1153-1154.DOI:10.14088/j.cnki.issn0439-8114.2009.05.017.
[30]段伟丽, 刘艳秋, 包怡红.艾蒿精油的抑菌活性和稳定性[J].食品与生物技术学报, 2015, 34(12): 1332-1337.DOI:10.3969/j.issn.1673-1689.2015.12.016.
[31]MAYE J P, LEKER J.Preparation of dicyclohexylamine alpha acids and dicyclohexylamine beta acids[J].Journal of the American Society of Brewing Chemists, 2014, 72(4): 227-230.DOI:10.1094/ASBCJ-2014-1001-01.
[32]BOCQUET L, RIVIÈRE C, DERMONT C, et al.Antifungal activity of hop extracts and compounds against the wheat pathogen Zymoseptoria tritici[J].Industrial Crops and Products, 2018, 122: 290-297.DOI:10.1016/j.indcrop.2018.05.061.
[33]LI Y, FRENZ C M, LI Z, et al.Virtual and in vitro bioassay screening of phytochemical inhibitors from flavonoids and isoflavones against xanthine oxidase and cyclooxygenase-2 for gout treatment[J].Chemical Biology and Drug Design, 2011, 81(4): 537-544.DOI:10.1111/j.1747-0285.2011.01248.x.
[34]HILLE R.Molybdenum-containing hydroxylases[J].Archives of Biochemistry and Bbiophysics, 2005, 433(1): 107-116.DOI:10.1016/j.abb.2004.08.012.
[35]GAFFO A L, EDWARDS N L, SAAG K G.Hyperuricemia and cardiovascular disease: how strong is the evidence for a causal link?[J].Arthritis Research and Therapy, 2009, 11(4): 240.DOI:10.1186/ar2761.
[36]SORBERA L, RABASSEDA X, CASTANER J.TMX-67: Treatment of gout and hyperuricemia xanthine oxidase inhibitor[J].Drugs of the Future, 2011, 26: 32-38.DOI:10.1358/dof.2001.026.01.607802.
[37]辛雅雯, 曾正英, 陈国良.痛风治疗药物及其研究进展[J].中国药物化学杂志, 2012(5): 416-423.DOI:10.14142/j.cnki.cn21-1313/r.2012.05.015.
[38]JOHNSON P, LOGANATHAN C, IRUTHAYARAJ A, et al.S-allyl cysteine as potent anti-gout drug: Insight into the xanthine oxidase inhibition and anti-inflammatory activity[J].Biochimie, 2018, 154: 1-9.DOI:10.1016/j.biochi.2018.07.015.
[39]王亚杰, 张国文.桑色素对黄嘌呤氧化酶活性的抑制作用[J].食品科学, 2014, 35(13): 143-146.DOI:10.7506/spkx1002-6630-201413027.
[40]MIR M A, KHAN J M, KHAN R H, et al.Interaction of cetyltrimethylammonium bromide and its gemini homologue bis(cetyldimethylammonium)butane dibromide with xanthine oxidase[J].The Journal of Physical Chemistry B, 2012, 116(19): 5711-5718.DOI:10.1021/jp207803c.
[41]柳高.不同种类B族维生素和复方丹参滴丸对高尿酸血症小鼠血尿酸水平的影响[D].北京: 中国人民解放军医学院, 2012: 37-42.
[42]MA Yongkai, WU Yanyan, LI Laihao.Relationship between primary structure or spatial conformation and functional activity of antioxidant peptides from Pinctada fucata[J].Food Chemistry, 2018, 264: 108-117.DOI:10.1016/j.foodchem.2018.05.006.
[43]YEUNG S Y, LAN W H, HUANG C S, et al.Scavenging property of three cresol isomers against H2O2, hypochlorite, superoxide and hydroxyl radicals[J].Food and Chemical Toxicology, 2002, 40(10):1403-1413.DOI:10.1016/S0278-6915(02)00102-3.
[44]徐梦宇, 咸淑慧, 王荣镇, 等.杂交枸树根黄酮类物质的提取及其抑菌活性研究[J].食品科技, 2011, 36(4): 194-196.DOI:10.13684/j.cnki.spkj.2011.04.011.