苦茶(Camellia kucha (Chang et Wang) Chang)是我国特有的一种茶树资源,主要生长于云南[1]及广东、广西、湖南、江西毗邻地区[2],其大多呈野生状态分布,具有芽叶滋味极苦的特征,且含有特殊的嘌呤生物碱——苦茶碱。在我国民间,苦茶很早就作为药物来饮用,但因苦茶生化成分和药理学研究起步较晚,目前对苦茶的系统研究鲜少。近年来,随着对苦茶碱功效研究的深入,苦茶资源逐渐受到重视,市场需求也发生一定的变化,对其生化成分分析、生理活性鉴定及产品开发等相关研究也得到了发展。本文综述了苦茶的分类地位及资源分布、主要生化成分、苦茶碱生物合成途径、制备方法及药理活性等方面的研究,并对今后扩展苦茶研究方向提出了相关建议,以期为苦茶资源的创新利用提供理论参考。
1 苦茶资源分布及植物学分类
1.1 苦茶资源分布
我国苦茶资源蕴藏丰富,主要分布在云南、湖南、广东、四川、福建等地,具体资源分布如表1所示。
表1 我国苦茶资源分布
Table 1 Distribution of Camellia kucha (Chang et Wang) Chang resources in China

产地 资源名称 参考文献云南 曼木苦茶、曼儒苦茶、老曼娥苦茶、曼捌苦茶、吉良苦茶、曼迈苦茶、勐昂苦茶、新南东苦茶、曼囡老寨苦茶、曼新竜苦茶 [1]湖南江华苦茶(白叶苦茶、金叶苦茶、青叶苦茶、牛皮苦茶、竹叶苦茶、紫芽苦茶、白毛苦茶、龙须苦茶、柳叶苦茶)、酃县苦茶、茶陵苦茶、蓝山苦茶、桂东大叶苦茶[3-4]广东 乐昌苦茶、龙山苦茶、乳源苦茶、丹霞苦茶 [5]四川 黄山苦茶 [6]福建 安溪苦茶、尤溪苦茶 [7-8]江西 聂都苦茶、婺源古旦苦茶、安远苦茶、双凤苦茶 [9]浙江 江中红 [9]
1.2 苦茶植物学分类
苦茶作为我国特有的一种茶树资源,其植物学分类存在争议。庄晚芳等[10]根据茶树的生物学性状特征,将其归为云南亚种下的皋芦变种(也称为苦茶变种)(Camellia sinensis L. var. macrophylla or var. kulusio)。而在张宏达[11]的分类中,将其定义为新变种(Camellia sinensis var. kucha Chang et Wang)。杜琪珍等[12]根据生化组分含量、形态学及地理学等特征,将苦茶归为茶组三室茶中的苦茶变种(Camellia sinensis var. kuiea Du et Li)。李光涛等[13]研究了苦茶的染色体数目及核型,认为其基本染色体核型与普洱茶相同,将其归为普洱茶类(Camellia assamica var kucha)。束际林等[14]对茶组植物的花粉形态及花粉外壁超微结构进行观察,发现苦茶的花粉形态及超薄结构属于过渡型,即表明苦茶属于茶树由原始的乔木型过渡到灌木型的中间类型。陈亮等[15]根据对茶树种质资源进行系统研究,以花器官形态上的主要差异为依据,此外再兼顾树型、树姿等形态特征,将苦茶归于茶种下的阿萨姆茶(Camellia sinensis var.assamica)。王新超等[16]根据苦茶资源的主要生化成分析结果,认为其在儿茶素组成和含量接近于阿萨姆变种,聚类分析也可将苦茶与阿萨姆茶聚为一类,此外,其主要的生物学特征也与阿萨姆茶类似。石祥刚等[17]发现苦茶虽然与普洱茶(Camellia assamica (mast) Chang)近似,但其小苞片有3~4 个,萼片宽约4~6 mm,且外面没有毛,内面的白色短柔毛与普洱茶不相同,更为重要的是,其芽叶因含有特殊的苦茶碱而不同于普洱茶,因此提出将其从变种(Camellia assamica (mast) Chang var.kucha Chang et Wang)提升为种(Camellia kucha (Chang et Wang) Chang)。
2 苦茶主要生化成分特征
2.1 高含量的苦茶碱
叶创兴等[18]首次在苦茶中分离出含量较高的苦茶碱,占茶叶干物质含量的1.29%,是苦茶的主要嘌呤生物碱,其他生物碱含量(以茶叶干物质含量计)分别为咖啡碱1.93%、可可碱0.585%、茶碱0.012 8%;而在常规茶树品种中,嘌呤生物碱以咖啡碱为主,其相对含量为2%~4%,可可碱相对含量占第二位,为0.05%,茶碱相对含量占第三位,为0.002%。虽然早在1937年微量的苦茶碱就首次从提取咖啡碱剩余的茶渣中分离出来[19],但之后的研究揭示了苦茶中存在与传统茶叶不同的嘌呤生物碱模式,且苦茶碱的含量在嫩叶、成熟叶、老叶中依次显著降低[20]。续洁琨等[21]采用聚酰胺、凝胶柱、反相液相色谱柱和高效液相色谱(high performance liquid chromatography,HPLC)等分离方法纯化苦茶水提物,通过谱学数据鉴定了10 种化合物,包括3 种嘌呤生物碱(苦茶碱、咖啡碱、可可碱)、7 种茶多酚类化合物(儿茶素、表没食子儿茶素(epigallocatechin,EGC)、没食子儿茶素、表没食子儿茶素没食子酸酯(epigallocatechin gallate,EGCG)、没食子儿茶素酸酯、儿茶素没食子酸酯、1,2,6-三-O-没食子酰-β-D-吡喃葡萄糖),并对苦茶碱的核磁数据进行了全归属分析。
2.2 高含量的茶多酚
王冬梅等[22]采用HPLC-质谱(HPLC-mass spectrometry,HPLC-MS)联用方法,对苦茶及传统绿茶水提物中的儿茶素及嘌呤生物碱进行定性定量分析,发现苦茶中苦茶碱的含量远高于传统绿茶,且儿茶素总相对含量(13.82%)显著高于传统绿茶(7.37%),但两种茶的儿茶素组分均以酯型儿茶素为主。相关研究还发现,江华苦茶鲜叶中茶多酚及其儿茶素物质含量丰富,多酚类总相对含量可达39%以上,此外儿茶素组分EGCG、ECG含量较高[23]。杨春等[24]系统地对江华苦茶群体中100 个单株秋季鲜叶进行生化分析,发现高含量的茶多酚导致苦茶的酚氨比较大,平均为29.12,江华苦茶群体整体表现为制作红茶较优。
2.3 丰富的苦味物质
黄华林等[25]通过分析不同品系的苦茶,发现其产生苦味的黄烷酮类物质含量显著高于福鼎大白。杨超等[26]利用常规生化分析、HPLC、HPLC-MS/MS方法对西双版纳州勐宋乡帕热村苦茶进行分析,发现与其他晒青毛茶相比,苦茶碱是勐宋乡帕热村苦茶的特征性成分,也是苦茶味道较苦的主要原因之一。唐琴等[8]对福建尤溪苦茶的苦涩物质进行研究,认为高含量的花青素、酯型儿茶素、咖啡碱以及它们之间的相互作用是引起苦茶苦涩味的主要原因。
3 苦茶碱生物合成途径及制备方法
苦茶碱结构与咖啡碱相似,其N9位比咖啡碱多一个甲基、C8位比咖啡碱多一个酮基基团(图1)。自1999年叶创兴等[18]首次在苦茶中发现高含量的苦茶碱并揭示其与传统茶叶不同的嘌呤生物碱模式后,引起科研工作者对苦茶碱合成途径的广泛关注。
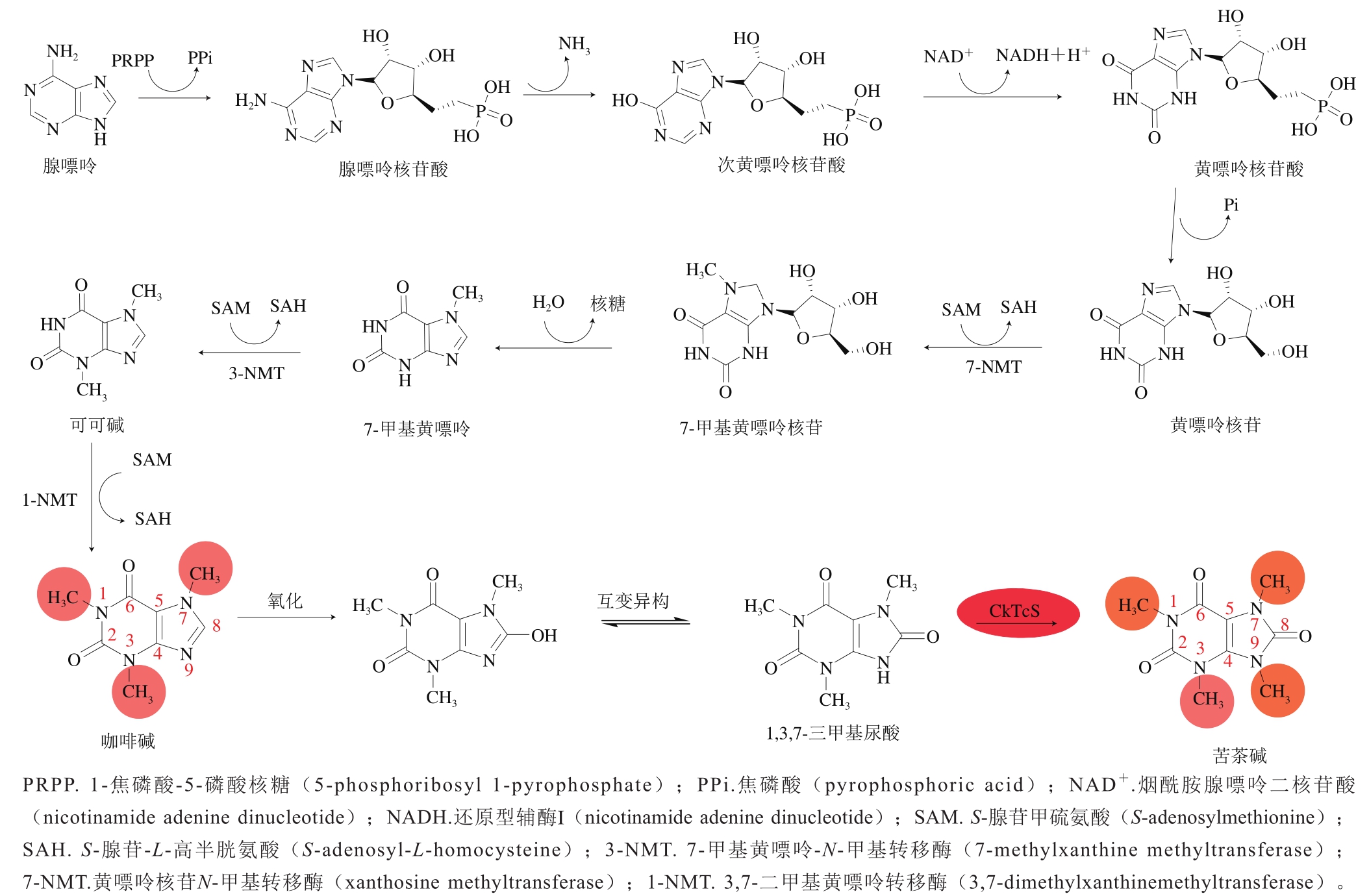
图1 苦茶碱的生物合成路径[28-29]
Fig. 1 Biosynthetic pathways of theacrine[28-29]
3.1 苦茶碱的生物合成途径
Zheng Xinqiang等[27]通过研究同位素14C标记SAM的动态变化,证明苦茶碱是先经咖啡碱的主要合成途径“黄嘌呤核苷→7-甲基黄嘌呤核苷→7-甲基黄嘌呤→可可碱→咖啡碱”(图1),之后咖啡碱在C8氧化酶作用下形成1,3,7-三甲基尿酸中间体,再经N9甲基转移酶作用进一步转化为苦茶碱(图1)。Wang Songlin等[28]通过转录组分析具有高、中、低含量苦茶碱的茶树品种,发现由基因TEA024443编码的N-甲基转移酶可能是最终合成苦茶碱的关键酶。值得注意的是,Zhang Yuehong等[29]通过对普洱茶和苦茶的N-甲基转移酶进行转录组测序,发现并首次鉴定了合成苦茶碱所涉及的N9甲基转移酶CkTcS(图1),并进一步通过体外酶动力学实验证明其活性,且发现CkTcS的高表达是苦茶中大量积累苦茶碱的原因,通过分析CkTcS的晶体结构以及中间体1,3,7-三甲基尿酸与CkTcS的结合位点,揭示出CkTcS的N9甲基化活性的作用机制,但是合成过程中关键的咖啡碱C8氧化酶并未见报道。
3.2 苦茶碱的制备方法
苦茶碱作为茶叶中一种新型的嘌呤生物碱,具有较好的应用前景,目前其制备方法包括天然提取和化学合成两种方法。
3.2.1 天然提取法
从苦茶芽叶中分离提取是目前获取苦茶碱最常用的方法。1937年,Johnson[19]首次在提取咖啡碱剩余茶渣中分离出微量的苦茶碱,但因其在茶叶中含量极低,而在此后茶叶的常规检测中未被发现。直到1999年,叶创兴等[18]采用硅胶柱层析法从苦茶嫩梢中首次分离得到高含量(0.84%)的苦茶碱,并对其结构进行了鉴定。此后的大部分研究主要以苦茶芽叶为原料,用水作为溶剂经回流提取水溶性化合物,再采用硅胶柱层析和制备型HPLC法,获得高纯度苦茶碱[30]。此外,也有文献采用十八烷基硅烷键合硅胶填充色谱柱[31]、高逆流色谱[32]、反相制备色谱[33]等方法来获得高纯度的苦茶碱,但以上提取方法需使用大量溶剂、过程繁琐、成本较高、产率较低。
谢果[34]发现常规的回流法、微波法、超声波法都能高效提取苦茶嘌呤生物碱混合物,提取率为1.225%~1.968%,再通过真空升华法,可获得纯度95.38%的苦茶碱,其纯度略低于采用硅胶柱层析法(99%)[30]、制备型HPLC法(98%)[35]和高速逆流色谱法(99%)[32]提取所得苦茶碱,但该方法简便、成本相对较低、有机溶剂消耗少。
值得注意的是,苦茶芽叶中含有与苦茶碱结构相似的咖啡碱,两者性质相似,在以上的提取过程中都容易混杂咖啡碱,使苦茶碱的提取过程繁琐,但苦茶果皮中不含咖啡碱,以其为原料可以有效提高效率。针对这一现象,卢嘉丽等[36]以苦茶果皮为原料进行水提,其水提物经氯仿萃取后浓缩干燥,再经体积分数70%乙醇溶液重结晶纯化,可获得纯度大于99%的苦茶碱,提取率为1.35%,此提取方法具有步骤简单、提取率高等优点,但因苦茶果皮资源稀缺,限制了该方法的广泛应用。
3.2.2 化学合成法
通过化学合成的方法可获得大量的高纯度苦茶碱,但是目前有关苦茶碱化学合成的研究相对较少。于少静[37]以1,3-二甲基脲(I)和丙二酸二甲酯(II)为原料,以甲醇钠作为催化剂,合成1,3-二甲基巴比妥酸(III);1,3-二甲基巴比妥酸与卤代试剂三氯氧磷反应,生成6-氯-1,3-二甲基嘧啶-2,4-二酮(IV);6-氯-1,3-二甲基嘧啶-2,4-二酮在室温下与甲胺反应合成1,3-二甲基-6-甲氨基嘧啶-2,4-二酮(V);1,3-二甲基-6-甲氨基嘧啶-2,4-二酮与卤代试剂N-溴代丁二酰亚胺反应生成5-溴-1,3-二甲基-6-甲氨基嘧啶-2,4-二酮(VI);5-溴-1,3-二甲基-6-甲氨基嘧啶-2,4-二酮与甲胺反应生成1,3-二甲基-5,6-二甲基嘧啶-2,4-二酮(VII);1,3-二甲基-5,6-二甲基嘧啶-2,4-二酮与三光气和三乙胺反应合成目标产物苦茶碱(VIII)(图2A)。该合成方法经过6 步反应,可获得总产率为38.33%的目标产物。
朱义平等[38]以7 g 1,3-二甲基巴比妥酸为原料,依次经过卤代、取代、卤代、取代、环化5 步反应,可得到2.5 g苦茶碱,产率为25.0%(图2B)。
另有报道以6-氨基-1,3-二甲基-5-亚硝基尿嘧啶为原料,依次经过硝基化、还原、环化、甲基化反应可得到苦茶碱[39],该专利还公布了不同的亚硝化试剂(亚硝酸钠、亚硝酸钾、亚硝酸异戊酯、亚硝酸丁酯)、还原剂(连二亚硫酸钠、铁粉、锌粉、氢气)、环合试剂(N,N-羰基二咪唑、光气、三光气、三乙胺、碳酸二甲酯及碳酸二苯酯)以及甲基化试剂(硫酸二甲酯、碳酸二甲酯、碘甲烷以及溴甲烷)(图2C)。
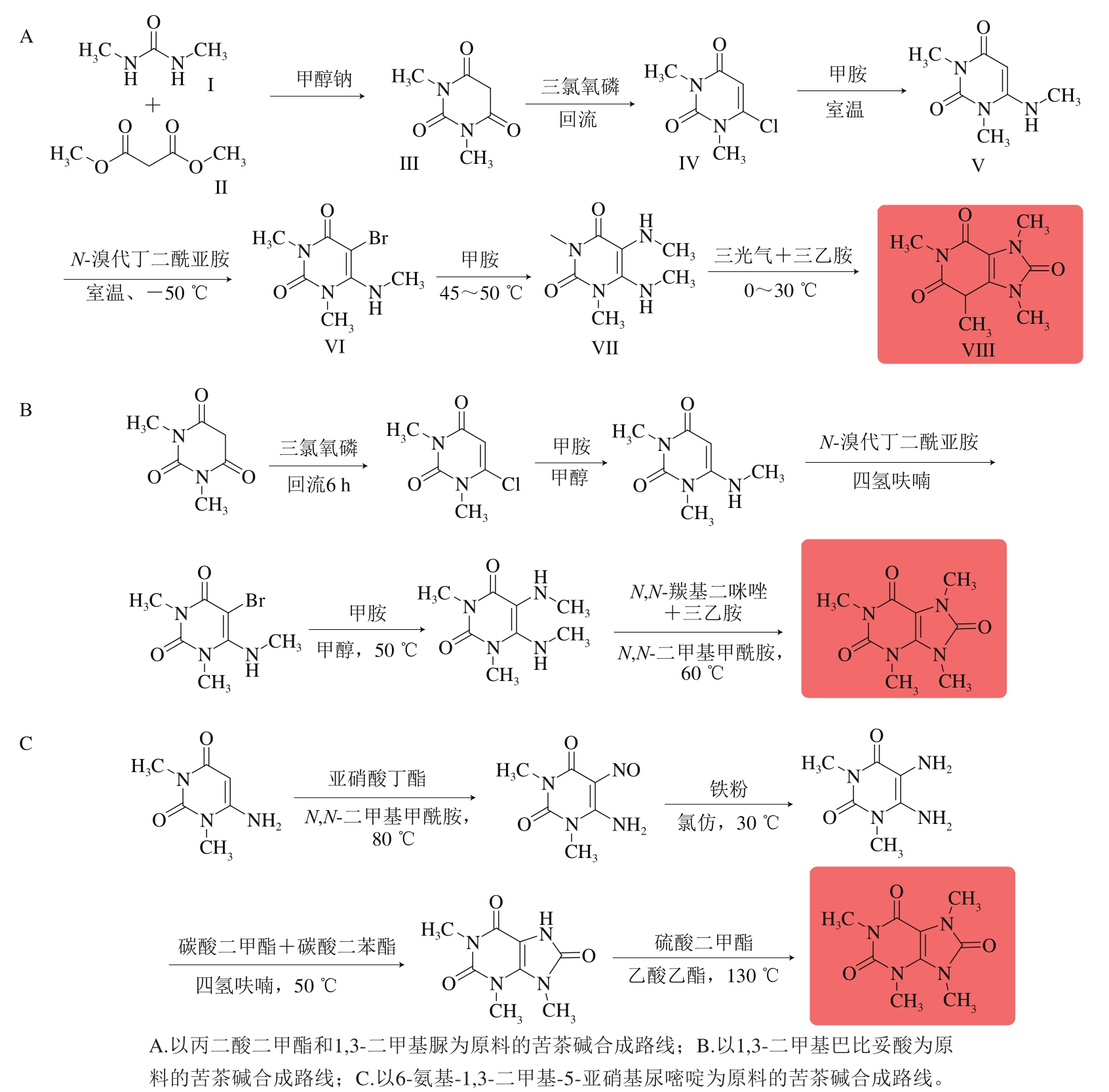
图2 苦茶碱化学合成路线[37-39]
Fig. 2 Chemical synthesis route of theacrine[37-39]
以上3 种全合成的方法反应步骤多、目标产物产率低、工业化生产难度大。针对这一问题,陈福欣等[40]进行了实验方案优化,将尿酸和甲基化试剂(一卤代甲烷、硫酸二甲酯、N,N-二甲基甲酰胺、N,N-二甲基甲酰胺二甲缩醛等其中一种)置于高压反应釜内,充保护气至高压反应釜内使压力为10 MPa,升温至220 ℃,反应结束后,将高压反应釜降温、泄压,物料倒入冰水中搅拌析晶,对抽滤得到的粗品进行重结晶,可获得产率为69.2%~85.0%的目标产物,此合成方法相对简单,但需要高温高压反应。
此外,范文超[41]以咖啡为原料用两步酶法制备苦茶碱,首先用咖啡因脱氢酶催化原料生成1,3,7-三甲基尿酸,之后用氨基酸序列为SEQ ID NO:9的双甲基黄嘌呤-N-甲基转移酶催化生成苦茶碱。该方法具有反应条件温和、安全、环保等优点,但是要实现工业化生产,必须要大幅度提高作为催化剂的相关酶活性,且要保障相关酶的稳定性。
4 苦茶中苦茶碱的药理活性及毒理学研究
尽管苦茶碱与咖啡碱在结构上相似,但其不具有咖啡碱的刺激性,因此引起广大学者对其药理活性及毒理学的关注。从苦茶中提取苦茶碱,并开展其药理功效及毒理学的研究成为热点。
4.1 药理活性
4.1.1 镇静安眠
苦茶碱与咖啡碱虽然结构相似,但咖啡碱具有中枢兴奋作用[42-43],而苦茶碱却表现为镇静安眠的作用[31]。Xu Jiekun等[31]通过对苦茶碱、咖啡碱和可可碱比较,证明30 mg/kg mb的苦茶碱可以明显延长戊巴比妥所引起大鼠睡眠的时间;并通过对大鼠强迫游泳实验的不动时间进行测定,证明苦茶碱具有镇静催眠的活性;进一步对其催眠活性进行药理研究[44-45],发现苦茶碱可明显缩短大鼠睡眠潜伏期并延长大鼠睡眠总时间,其发挥催眠作用可能与调节大鼠脑内腺苷及腺苷脱氨酶的含量有关。此外,当苦茶中苦茶碱的含量大于3 倍咖啡碱含量时,可抑制咖啡碱引起的中枢兴奋作用,苦茶可表现出镇静催眠的作用[46]。
4.1.2 改善肝脏脂肪化及保护肝脏
苦茶碱可以改善小鼠肝脏脂肪化的状态[47-50],通过激活与其相关酶通路,减少游离脂肪酸的合成,抑制肝脏甘油三酯的积累,从而改善高脂饮食引起小鼠的肝损伤;此外还可以通过提高抗氧化酶的活性和基因表达水平,间接清除自由基,进而改善小鼠束缚应激诱导的肝损伤[51]。
苦茶碱对镉损伤的小鼠肝脏具有保护作用[52-54],主要是通过清除过量自由基来降低其对肝脏氧化损伤的程度;此外还可通过提高抗氧化酶(超氧化物歧化酶和过氧化氢酶)活性,增强系统的抗氧化能力以及抗炎作用来协同保护肝脏。
4.1.3 抗炎止痛
口服苦茶碱对于二甲苯造成的耳部水肿、醋酸引起血管通透性增加和卡拉胶造成的足肿胀具有较好的消炎效果,并对热板实验和醋酸造成的扭体反应具有较好的抗炎止痛效果[30]。此外,苦茶碱可以通过降低血清中白细胞介素-6水平,提高血清中转化生长因子-β的水平,从而有效抑制弗氏不完全佐剂诱导的SD大鼠关节炎症反应[55]。
4.1.4 抗抑郁
苦茶碱在悬尾实验、强迫游泳、自主活动等6 种小鼠抗抑郁模型[56]中表现出一定的药理活性,这些作用可能与其影响单胺类神经递质有关。此外,相关研究还发现,其抗抑郁机制可能是通过激活环磷酸腺苷(cyclic adenosine monophosphate,cAMP)/cAMP反应元件结合蛋白(cAMP response element binding protein,CREB)/脑源性神经生长因子(brain derived neurotrophic factor,BDNF)/酪氨酸受体激酶B(tyrosine receptor kinase B,TrkB)信号通路,降低应激小鼠血浆皮质酮水平,促进海马神经元增殖水平,从而改善小鼠抑郁症状[57]。
4.1.5 其他药理活性
口服苦茶碱可调节拘束应激小鼠海马体中的5-羟色胺、多巴胺和其代谢产物水平,减轻小鼠中枢疲劳引起的学习和记忆障碍[58];可增加多巴胺含量,通过促进γ-氨基丁酸的释放来抑制谷氨酸的毒性,从而增强小鼠的运动能力,进而保护多巴胺能神经元的异常,改善小鼠帕金森症[35];也可通过逆转上皮细胞-间充质转化过程来抑制乳腺癌细胞转移[59]。
4.2 毒理学研究
王园园等[60]对苦茶碱毒性进行研究,在连续4 周对大鼠进行不同剂量(150、75、37.5 mg/kg mb)的苦茶碱灌胃后,发现与空白组相比,实验组大鼠体质量增长、血液生化指标、重要脏器系数与组织学检查均无显著性差异,停药后也未见延迟毒性反应;说明长期灌胃高剂量苦茶碱(为临床人用剂量的170 倍)对大鼠没有明显毒性,按临床拟合剂量服用是安全的。此外,王冬梅等[46]对苦茶作为食品饮用的安全性进行研究,通过对小鼠进行连续14 d不同剂量苦茶提取物的灌胃实验,发现小鼠在观察期内未出现任何中毒症状及死亡现象,小鼠苦茶急性毒性经口半数致死量大于21.5 g/kg mb,可将苦茶的毒性分级判定为无毒级。
5 结 语
苦茶作为一类比较特殊的种质资源,因其苦茶碱含量高而受到人们越来越多的关注,但苦茶资源在产业化和现阶段研究中仍面临许多问题。1)苦茶新品种的选育有待加强。目前对苦茶的利用研究较多的是江华苦茶,主要分布在湖南省南岭山脉,适合制作红茶[3]。但对其他区域苦茶的研究较少,主要是因为苦茶种质资源相对稀缺;此外,很多区域苦茶资源未被挖掘,今后需加强对苦茶种质资源的收集、鉴评和评价工作,选育一批综合性状优良、苦茶碱含量高、保健作用良好的苦茶新品种,为其药理活性及深加工产品提供原料支撑;同时可利用苦茶作为亲本,采用传统杂交育种的方法开发一批生化成分特异的茶树新品种,应用于推广和生产。2)苦茶及苦茶碱产品有待改善和创新。苦茶加工的产品因滋味较苦而大众认可度不高,应改进其产品的加工技术,解决苦茶口感欠佳的问题,开发出口感好又不失保健功能的苦茶加工产品,同时还可通过萃取高含量苦茶碱来开发高苦茶碱茶叶深加工产品,提高其应用价值,为苦茶的创新利用提供更为广阔的市场,更好地满足现有茶叶产业的需求。3)苦茶碱合成方法有待改进。苦茶碱具有良好的生理活性,但是当前获取苦茶碱的方法较为有限,主要是依靠从苦茶芽叶中提取分离,但苦茶资源有限,提取步骤多、产率低、成本高;此外,对其化学合成方法的报道也相对较少,且存在反应步骤多、条件苛刻、难以实现工业化生产等问题。因此开发一种操作简单、成本低廉的苦茶碱合成方法,对于其生理活性及作用机制的深入研究及其重要。4)苦茶碱生物合成途径及保健功效有待深入研究。目前苦茶碱在茶树体内合成途径已基本明确,但对参与咖啡碱合成1,3,7-三甲基尿酸中间体的C8氧化酶尚不清楚,有待进一步深入研究。相比常规茶资源,有关苦茶保健功效研究相对较少,且多为针对苦茶碱在实验室或动物身上得出的结论,缺乏临床应用,且保健机理尚不完全明确,应进一步探明其保健机理及特异性功效,这将对苦茶作为功能食品或药物开发利用提供强有力的依据。
[1]漠丽萍. 勐海县苦茶资源现状及开发利用探析[J]. 现代农业科技,2017(13): 27-28. DOI:10.3969/j.issn.1007-5739.2017.13.020.
[2]虞富莲. 茶树种质资源的研究现状及展望[J]. 中国茶叶, 1990(2):29-31.
[3]董利娟, 张曙光, 杨阳. 茶树珍稀资源: 江华苦茶的研究[J]. 茶叶通讯, 2003(3): 3-8.
[4]刘振, 赵洋, 杨培迪, 等. 湖南省茶树种质资源现状及研究进展[J].茶叶通讯, 2011, 38(3): 7-10; 18. DOI:10.3969/j.issn.1009-525X.2011.03.003.
[5]吴华玲, 陈栋, 李家贤. 广东特异茶树种质资源选育研究进展[J].广东农业科学, 2012, 39(20): 15-17; 24. DOI:10.3969/j.issn.1004-874X.2012.20.006.
[6]唐洪, 李承江, 黄新明. 四川宜宾黄山再现古茶树[J]. 中国茶叶,2011, 33(11): 33. DOI:10.3969/j.issn.1000-3150.2011.11.039.
[7]俞永明, 胡海波, 孙松祥. 福建安溪的“苦茶”[J]. 茶叶, 1958(1): 19-21.
[8]唐琴, 孙威江, 陈志丹, 等. 尤溪苦茶资源苦涩味物质测定与分析[J].食品科学, 2019, 40(18): 242-247. DOI:10.7506/spkx1002-6630-20181030-362.
[9]周琼琼, 孙威江. 我国苦茶资源的研究进展[J]. 茶叶科学技术,2011(1): 4-7. DOI:10.3969/j.issn.1007-4872.2011.01.002.
[10]庄晚芳, 刘祖生, 陈文怀. 论茶树变种分类[J]. 浙江农业大学学报,1981(1): 43-50.
[11]张宏达. 茶叶植物资源的订正[J]. 中山大学学报(自然科学版),1984(1): 3-14.
[12]杜琪珍, 李名君, 刘维华, 等. 茶组植物的化学分类及数值分类[J].茶叶科学, 1990(2): 1-12.
[13]李光涛, 梁涛. 中国山茶属4 种2变种核型研究[J]. 广西植物,1990(3): 189-197.
[14]束际林, 陈亮, 王海思, 等. 茶树及其他山茶属植物花粉形态、超微结构及演化[J]. 茶叶科学, 1998(1): 6-15.
[15]陈亮, 虞富莲, 童启庆. 关于茶组植物分类与演化的讨论[J]. 茶叶科学, 2000(2): 89-94. DOI:10.3969/j.issn.1000-369X.2000.02.002.
[16]王新超, 姚明哲, 马春雷, 等. 我国苦茶资源主要生化成分的鉴定评价[J]. 中国农学通报, 2008(6): 65-69.
[17]石祥刚, 郑新强, 宋晓虹, 等. 关于苦茶的新组合[J]. 中山大学学报(自然科学版), 2008(6): 129-130. DOI:10.3321/j.issn:0529-6579.2008.06.027.
[18]叶创兴, 林永成, 苏建业, 等. 苦茶Camellia assamica var. kucha Chang et Wang的嘌呤生物碱[J]. 中山大学学报(自然科学版),1999(5): 82-86. DOI:10.3321/j.issn:0529-6579.1999.05.019.
[19]JOHNSON T B. The discovery and identification of a new purine alkaloid in tea[J]. Science, 1937, 85: 431-431. DOI:10.1126/science.85.2209.431.
[20]LU Jiali, WANG Dongmei, SHI Xianggang, et al. Determination of purine alkaloids and catechins in different parts of Camellia assamica var. kucha by HPLC-DAD/ESI-MS/MS[J]. Journal of the Science of Food and Agriculture, 2009, 89(12): 2024-2029. DOI:10.1002/jsfa.3683.
[21]续洁琨, 张维库, 栗原博, 等. 苦茶的化学成分(英文)[J]. 中国天然药物, 2009, 7(2): 111-114.
[22]王冬梅, 杜丽丽, 卢嘉丽, 等. 苦茶Camellia assamica var. kucha茶多酚的HPLC-DAD/MS分析[J]. 天然产物研究与开发, 2006(6): 978-981. DOI:10.3969/j.issn.1001-6880.2006.06.023.
[23]刘湘鸣. 江华苦茶性状研究[J]. 茶叶通讯, 2006(3): 4-7.DOI:10.3969/j.issn.1009-525X.2006.03.007.
[24]杨春, 王庆, 李丹, 等. 江华苦茶秋季茶叶生化成分分析[J]. 湖南农业科学, 2012(11): 37-39. DOI:10.3969/j.issn.1006-060X.2012.11.013.
[25]黄华林, 乔小燕, 何玉媚, 等. 苦茶品系中苦涩味物质分析[J].浙江农业科学, 2017, 58(7): 1244-1248. DOI:10.16178/j.issn.0528-9017.20170748.
[26]杨超, 马存强, 周斌星, 等. 苦茶特征性成分研究[J]. 昆明学院学报,2014, 36(3): 75-78. DOI:10.14091/j.cnki.kmxyxb.2014.03.027.
[27]ZHENG Xinqiang, YE Chuangxing, KATO M, et al. Theacrine(1,3,7,9-tetramethyluric acid) synthesis in leaves of a Chinese tea,kucha (Camellia assamica var. kucha)[J]. Phytochemistry, 2002, 60(2):129-134. DOI:10.1016/S0031-9422(02)00086-9.
[28]WANG Songlin, CHEN Jiedan, MA Jianqiang, et al. Novel insight into theacrine metabolism revealed by transcriptome analysis in bitter tea(Kucha, Camellia sinensis)[J]. Scientific Reports, 2020, 10(1): 6286.DOI:10.1038/s41598-020-62859-2.
[29]ZHANG Yuehong, LI Yifang, WANG Yongjin, et al. Identification and characterization of N9-methyltransferase involved in converting caffeine into non-stimulatory theacrine in tea[J]. Nature Communications,2020, 11(1): 1473. DOI:10.1038/s41467-020-15324-7.
[30]WANG Yuanyuan, YANG Xiaorong, ZHENG Xinqiang, et al.Theacrine, a purine alkaloid with anti-inflammatory and analgesic activities[J]. Fitoterapia, 2010, 81(6): 627-631. DOI:10.1016/j.fitote.2010.03.008.
[31]XU Jiekun, KURIHARA H, ZHAO Liang, et al. Theacrine, a special purine alkaloid with sedative and hypnotic properties from Cammelia assamica var. kucha in mice[J]. Journal of Asian Natural Products Research, 2007, 9(6/8): 665-672. DOI:10.1080/10286020601103155.
[32]程悦, 严志勇, 卢嘉丽, 等. 高速逆流色谱分离制备苦茶中的苦茶碱[J]. 中山大学学报(自然科学版), 2010, 49(3): 65-69.
[33]尚卫琼, 李友勇, 刘悦, 等. 基于EST-SSR标记的西双版纳苦茶资源遗传多样性分析[J]. 山西农业科学, 2020, 48(2): 167-171.DOI:10.3969/j.issn.1002-2481.2020.02.09.
[34]谢果. 茶叶嘌呤生物碱抗抑郁作用及其机制的研究[D]. 广州: 暨南大学, 2010: 40-44.
[35]李善兵. 甲基黄嘌呤类生物碱theacrine对帕金森病模型小鼠多巴胺能神经元的保护作用研究[D]. 广州: 暨南大学, 2011: 9-10.
[36]卢嘉丽, 王冬梅, 杜丽丽, 等. 从苦茶Camellia assamica var. kucha果皮提取纯化1,3,7,9-四甲基尿酸的研究[J]. 天然产物研究与开发,2009(10): 486-489.
[37]于少静. 1,3,7,9-四甲基尿酸的合成工艺研究[D]. 烟台: 鲁东大学,2017: 13-31.
[38]朱义平, 孙莲花. 一种天然产物四甲基尿酸的全合成方法:CN103755705A[P]. 2014-04-30[2020-11-10]. https://kns.cnki.net/kcms/detail/detail.aspx?dbcode=SCPD&dbname=SCPD2014&filenam e=CN103755705A&v=%25mmd2BjS6pgBzFbHLcpxFaPCT0aaet9k9 5w0K0afea3Ojw41kSkV5s9mWDxrU8sKu15QT.
[39]朱义平, 孙晋. 一种1,3,7,9-四甲基尿酸的全合成方法:CN106046004A[P]. 2016-10-26[2020-11-10]. https://kns.cnki.net/kcms/detail/detail.aspx?dbcode=SCPD&dbname=SCPD2016&filenam e=CN106046004A&v=HVnef3mk3OLGYIm9p7GOeC4Vc5Kx%25m md2BoQAtOL3teJPr2oZpZfZyVzGhPIUHYjnEVSF.
[40]陈福欣, 龚频, 周安宁, 等. 一种四甲基尿酸的合成方法:CN104086550A[P]. 2014-10-08[2020-11-10]. https://kns.cnki.net/kcms/detail/detail.aspx?dbcode=SCPD&dbname=SCPD2014&filenam e=CN104086550A&v=MJRWbtQQJwWBKGkOlHVmzAFSeFDz3b HpjzIizWiEdk96hUC751sjc4zceTutqYYk.
[41]范文超. 两步酶法制备1,3,7,9-四甲基尿酸: CN107326053A[P].2017-11-07[2020-11-10]. https://kns.cnki.net/kcms/detail/detail.aspx?dbcode=SCPD&dbname=SCPD2017&filename=CN107326053A&v=%25mmd2F4IAcxqzxQRguOsW4seFsJzai5cLVUSf2lRjZoTTzK6qqn UY0Y%25mmd2BjKCNLq46J%25mmd2BnxK.
[42]WALDHAUSER S S M, BAUMANN T W. Compartmentation of caffeine and related purine alkaloids depends exclusively on the physical chemistry of their vacuolar complex formation with chlorogenic acids[J]. Phytochemistry, 1996, 42(4): 985-996.DOI:10.1016/0031-9422(96)00072-6.
[43]牟群芳, 李念, 梁瑜, 等. 咖啡因中枢活性双盲实验研究[J]. 泰山医学院学报, 2012, 33(6): 404-406. DOI:10.3969/j.issn.1004-7115.2012.06.002.
[44]QIAO Haoyi, YE Xiansheng, BAI Xiaoyu, et al. Theacrine: a purine alkaloid from Camellia assamica var. kucha with a hypnotic property via the adenosine system[J]. Neuroscience Letters, 2017, 659: 48-53.DOI:10.1016/j.neulet.2017.08.063.
[45]乔灏祎. Theacrine促睡眠作用机制的研究及马钱苷对中枢神经系统作用的初探[D]. 北京: 北京中医药大学, 2017: 36-31.
[46]王冬梅, 卢嘉丽, 程悦, 等. 苦茶的急性毒性与神经药理活性初步研究[J]. 中山大学学报(自然科学版), 2010, 49(1): 76-79.
[47]徐军. 通过SirT3/AMPK信号通路介导的Theacrine对脂质代谢的影响及其机制研究[D]. 沈阳: 辽宁中医药大学, 2014: 49-51.
[48]徐军, 王国恩, 章时杰, 等. 1,3,7,9-四甲基尿酸激活SirT3/AMPK/ACC信号通路减少高脂饮食小鼠肝脏脂肪化[J]. 中国药理学通报,2014, 30(6): 791-795. DOI:10.3969/j.issn.1001-1978.2014.06.012.
[49]徐军, 翟羽佳, 王国恩, 等. 嘌呤类生物碱Theacrine对SIRT3调节的脂肪酸代谢相关基因影响[J]. 中药新药与临床药理, 2014, 25(4):409-414. DOI:10.3969/j.issn.1003-9783.2014.04.006.
[50]WANG Guoen, LI Yifang, ZHAI Yujia, et al. Theacrine protects against nonalcoholic fatty liver disease by regulating acylcarnitine metabolism[J]. Metabolism, 2018, 85: 227-239. DOI:10.1016/j.metabol.2018.04.011.
[51]LI Weixi, LI Yifang, ZHAI Yujia, et al. Theacrine, a purine alkaloid obtained from Camellia assamica var. kucha, attenuates restraint stress-provoked liver damage in mice[J]. Journal of Agricultural and Food Chemistry, 2013, 61(26): 6328-6335. DOI:10.1021/jf400982c.
[52]龚频, 马逢乐, 何蓉蓉, 等. 云南苦茶提取物对镉致小鼠肝脏损伤的保护作用[J]. 陕西科技大学学报(自然科学版), 2017, 35(1): 134-138.DOI:10.3969/j.issn.1000-5811.2017.01.025.
[53]龚频, 皮思慧, 杨文娟, 等. 四甲基脲酸对镉损伤小鼠肝脏的保护作用[J]. 陕西科技大学学报(自然科学版), 2017, 35(2): 131-134.DOI:10.3969/j.issn.1000-5811.2017.02.025.
[54]龚频, 杨倩, 何蓉蓉, 等. 四甲基尿酸对镉致小鼠肾脏损伤的保护作用[J]. 现代食品科技, 2019, 35(11): 1-6; 24. DOI:10.13982/j.mfst.1673-9078.2019.11.001.
[55]GAO Ming, ZHENG Jun, ZHENG Chao, et al. Theacrine alleviates chronic inflammation by enhancing TGF-β-mediated shifts via TGF-β/SMAD pathway in Freund’s incomplete adjuvant-induced rats[J].Biochemical and Biophysical Research Communications, 2020,522(3): 743-748. DOI:10.1016/j.bbrc.2019.11.126.
[56]谢果, 吴敏芝, 黄映如, 等. 1,3,7,9-四甲基尿酸抗抑郁作用的实验研究[J]. 中国药理学通报, 2009, 25(9): 1160-1163. DOI:10.3321/j.issn:1001-1978.2009.09.011.
[57]胡惠华. Theacrine对水浸拘束应激负荷小鼠海马神经元增殖的影响及机制研究[D]. 广州: 暨南大学, 2014: 28-38.
[58]LI Yifang, CHEN Min, WANG Chen, et al. Theacrine, a purine alkaloid derived from Camellia assamica var. kucha, ameliorates impairments in learning and memory caused by restraint-induced central fatigue[J]. Journal of Functional Foods, 2015, 16: 472-483.DOI:10.1016/j.jff.2015.05.003.
[59]KO J H, YANG M H, BAEK S H, et al. Theacrine attenuates epithelial mesenchymal transition in human breast cancer MDAMB-231 cells[J]. Phytotherapy Research, 2019, 33(7): 1934-1942.DOI:10.1002/ptr.6389.
[60]王园园, 杨晓绒, 莫昉, 等. 苦茶碱对大鼠的长期毒性实验研究[J]. 时珍国医国药, 2010, 21(10): 2439-2441. DOI:10.3969/j.issn.1008-0805.2010.10.009.